Изобретение относится к химии фосфорорганических соединений с Р-С связью, а именно к усовершенствованному способу получения дихлоран-гидридов 1-алкил-2-алкоксиэтенилфосфоновых кислот формулы:
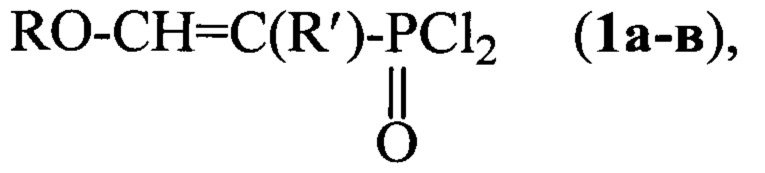
где R=C2H5 R'=H (a), R=C3H7 R'=CH3 (б), R=C4H9, R'=C2H5 (в),
которые являются ценными полупродуктами фосфорорганического синтеза.
Известен способ получения дихлорангидридов 2-алкоксиалкенил-фосфоновых кислот, который заключается в том, что диалкиловые эфиры подвергают взаимодействию с пятихлористым фосфором в среде избытка исходного эфира или смеси хлорокиси фосфора и петролейного эфира (1:1) при температуре 18°С в течение 10 ч и 36°С в течение 6 ч и образующийся промежуточный комплекс обрабатывают сернистым газом при 3-5°С. Выход целевых продуктов составляет 60-78% (А.с. СССР №174627 СССР, Бюл. изобр. 1965, №18).
К недостаткам этого способа следует отнести проведение процесса при нагревании и применение высокотоксичного газообразного сернистого газа.
Наиболее близким к описываемому изобретению по технической сущности и достигаемому результату является способ получения дихлорангидридов 2-алкоксиалкенилфосфоновых кислот, который заключается в том, что что диалкиловые эфиры подвергают взаимодействию с пятихлористым фосфором в среде избытка исходного эфира при комнатной температуре в течение 18-20 ч и образующийся промежуточный продукт обрабатывают оксидом кальция при температуре 30-40°С в течение 7-8 ч. Выход целевых продуктов составляет 67-71% (Авт. свид. СССР №579279, МПК C07F 9/42, Бюл. изобр. 1977, №41).
К недостаткам этого способа следует отнести высокую длительность процесса и применение нагревания при обработке промежуточного продукта оксидом кальция, что требует дополнительного расхода электроэнергии, что в совокупности приводит к повышению себестоимости целевых продуктов 1а-в.
Целью изобретения является упрощение процесса и расширение ассортимента агентов разложения аддуктов пятихлористого фосфора и простых эфиров.
При создании изобретения ставилась задача получить дихлорангидриды 1-алкил-2-алкоксиэтенилфосфоновых кислот формулы 1а-в, которые являются ценными полупродуктами фосфорорганического синтеза.
Техническим результатом является получение дихлорангидридов 1-алкил-2-алкоксиэтенилфосфоновых кислот формулы 1а-в, которые расширяют арсенал соединений, используемых в качестве полупродукта фосфорорганического синтеза.
Поставленная цель достигается описываемым способом получения дихлорангидридов 1-алкил-2-алкоксиэтенилфосфоновых кислот формулы 1а-в, который заключается в том, что диалкиловые эфиры подвергают взаимодействию с пятихлористым фосфором в среде инертного органического растворителя при комнатной температуре и затем обрабатывают образующиеся промежуточные комплексы при комнатной температуре перкарбонатом натрия.
Сущность изобретения заключается в следующем. К суспензии пятихлористого фосфора в инертном органическом растворителе, например, в абсолютном бензоле прибавляют диалкиловые эфиры, выдерживают реакционную смесь при комнатной температуре в течение 20 ч и образующиеся промежуточные комплексы подвергают взаимодействию с перкарбонатом натрия при комнатной температуре.
Пример 1. Дихлорангидрид 2-этоксиэтенилфосфоновой кислоты (1а).
К суспензии 62,5 г (0,3 моль) тонкоизмельченного пятихлористого фосфора и 100 мл абсолютного бензола прибавляют при перемешивании и комнатной температуре 7,4 г (0,1 моль) абсолютного диэтилового эфира. Реакционную смесь перемешивают при комнатной температуре в течение 20 ч. При этом образуется обильный кристаллический аддукт, который обрабатывают 19,2 (0.122 моль) перкарбоната натрия при комнатной температуре. При этом наблюдается выделение углекислого газа и образование осадка хлорида натрия. Осадок отфильтровывают, промывают 15 мл чистого растворителя и последующей перегонкой получают 16,5 г (87%) целевого дихлорангидрида, т. кип. 125-127°С (12 мм рт.ст.), nD20 1,4961. Спектр ЯМР 1Н (δ, м. д.): 7.44 т (1Н, ОСН=, 3JHH=3JHp 13.7 Гц), 5.33 дд (1Н, РСН=, 3JHH 13.7 Гц, 3JHP 20 Гц), 4.02 к (2Н, ОСН2, 3JHH 7.1 Гц), 1.39 т (3Н, СН3, 3JHH 7.1 Гц). Спектр ЯМР 31Р: δΡ 33 м. д. ИК спектр (см-1): 3070, 1619, 992 (Н-С=С-Н), 1275 (Р=О), 1023, 1232 (С-О), 560, 582 (Р-Cl). Найдено %: Cl 37.68, P 16.45. C4H7Cl2O2P. Вычислено %: Cl 37.52, P 16.39. Литературные данные: т. кип. 85°С (1 мм рт.ст.), nD20 1,4948, d420 1.3349.
Пример 2. Дихлорангидрид 1-метил-2-пропоксиэтенилфосфоновой кислоты (1б).
Аналогично примеру 1, из 10.2 г (0.1 моль) дипропилового эфира, 62.5 г (0.3 моль) пятихлористого фосфора и 18.9 г (0,12 моль) перкарбоната натрия в 100 мл абсолютного бензола получают 15.9 г (73%) целевого продукта, т. кип. 117-119 (6 мм рт.ст.), nD20 1,4928, d420 1.2349. ИК спектр (см-1): 3040, 1610 (С=СН), 1270 (Р=О), 565 (Р-Cl). Найдено %: Cl 32.68, P 14.45. C6H11Cl2O2P. Вычислено %: Cl 32.72, P 14.27. Литературные данные: т. кип. 86.5-87.5°С (1.5 мм рт.ст.), nD20 1,4922, d420 1.2355.
Пример 3. Дихлорангидрид 2-бутокси-1-этилэтенилфосфоновой кислоты (1в).
Аналогично примеру 1, из 13 г (0.1 моль) дибутилового эфира, 62.5 г (0.3 моль) пятихлористого фосфора и 18.8 г (0,12 моль) перкарбоната натрия в 100 мл абсолютного бензола получают 19.2 г (78%) целевого продукта, т. кип. 137-139 (10 мм рт.ст.), nD20 1,4858, d420 1.1789. ИК спектр (см-1): 3038, 1610 (С=СН), 1272 (Р=O), 563 (Р-Cl). Найдено %: Cl 28.88, P 12.45. C8H15Cl2O2P. Вычислено %: Cl 28.98, P 12.64. Литературные данные: т. кип. 130-132°С (8 мм рт.ст.), nD20 1,4868, d420 1.1845.
Описываемый способ получения дихлорангидридов 1-алкил-2-алкоксиэтенилфосфоновых кислот обеспечивает проведения процесса при комнатной температуре, сокращает длительность процесса, уменьшает расход электроэнергии и количество кислых отходов за счет их связывания карбонатом натрия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИХЛОРАНГИДРИДОВ 2-АЛКОКСИ-1-ХЛОРЭТЕНИЛФОСФОНОВЫХ КИСЛОТ | 2018 |
|
RU2687562C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИХЛОРАНГИДРИДА 2,3-ДИГИДРОФУРИЛ-4-ФОСФОНОВОЙ КИСЛОТЫ | 2022 |
|
RU2802467C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРАНГИДРИДА 2,4-ДИХЛОР-2-ДИХЛОРФОСФОРИЛБУТАНОВОЙ КИСЛОТЫ | 2024 |
|
RU2838764C1 |
| Способ получения дихлорангидридов алкенилтиофосфоновых кислот | 1987 |
|
SU1502574A1 |
| Способ получения дихлорангидридов алкенилфосфоновых кислот | 1988 |
|
SU1558919A1 |
| Способ получения дихлорангидрида стирилфосфоновой кислоты | 2023 |
|
RU2807368C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИХЛОРАНГИДРИДА 2,3-ДИХЛОРТЕТРАГИДРОФУРИЛ-3-ФОСФОНОВОЙ КИСЛОТЫ | 2022 |
|
RU2797128C1 |
| Способ получения дихлорангидридов замещенных циклопропилалкенил(алкил)фосфоновых или -тиофосфоновых кислот | 1989 |
|
SU1659419A1 |
| Способ получения дихлорангидридов 2-алкоксиалкенилфосфоновых кислот | 1980 |
|
SU883047A1 |
| Способ получения дихлорангидрида стирилфосфоновой кислоты | 1981 |
|
SU1027170A1 |
Изобретение относится к способу получения дихлорангидридов 1-алкил-2-алкоксиэтенилфосфоновых кислот формулы (1а-в), которые могут найти применение в качестве полупродуктов фосфорорганического синтеза. В указанной формуле R=C2H5, R'=H (соединение 1a); R=C3H7, R'=CH3 (соединение 1б); R=C4H9, R'=C2H5 (соединение 1в). Способ заключается во взаимодействии диалкиловых эфиров с пятихлористым фосфором в среде инертного органического растворителя при комнатной температуре и последующей обработке промежуточных аддуктов кислородсодержащим соединением. В качестве кислородсодержащего соединения используют перкарбонат натрия. Процесс ведут при комнатной температуре. Предлагаемый способ позволяет получать дихлорангидриды 1-алкил-2-алкоксиэтенилфосфоновых кислот формулы (1а-в) без повышения температуры и с уменьшением длительности процесса. 3 пр.
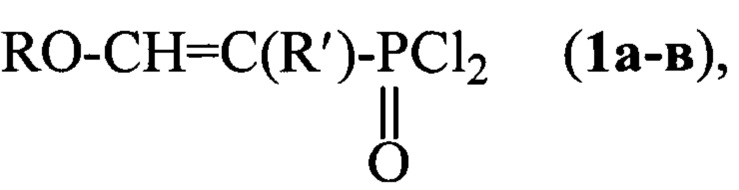
Способ получения дихлорангидридов 1-алкил-2-алкоксиэтенилфосфоновых кислот формулы
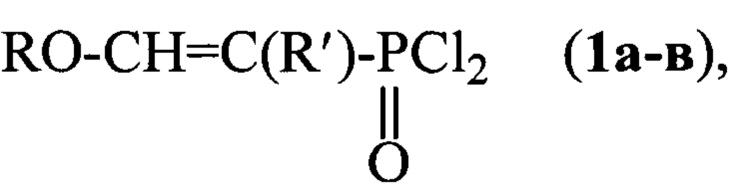
где R=C2H5, R'=H (a), R=C3H7, R'=CH3 (б), R=C4H9, R'=C2H5 (в), взаимодействием диалкиловых эфиров с пятихлористым фосфором в среде инертного органического растворителя при комнатной температуре и последующей обработкой промежуточных аддуктов кислородсодержащим соединением, отличающийся тем, что с целью упрощения процесса в качестве кислородсодержащего соединения используют перкарбонат натрия и процесс ведут при комнатной температуре.
| Способ получения дихлорангидридов алкоксиалкенилфосфоновых кислот | 1973 |
|
SU579279A1 |
| MITRASOV Y | |||
| N | |||
| ET AL, Reaction of allylalkanoates with phosphorus pentachloride, RUSSIAN JOURNAL OF GENERAL CHEMISTRY, 2008, 78(11), рр | |||
| Способ получения вытравок по индиго | 1924 |
|
SU2154A1 |
| US 4526728 A, 02.07.1985 | |||
| Движитель для судов | 1926 |
|
SU4074A1 |
Авторы
Даты
2023-08-01—Публикация
2022-10-04—Подача