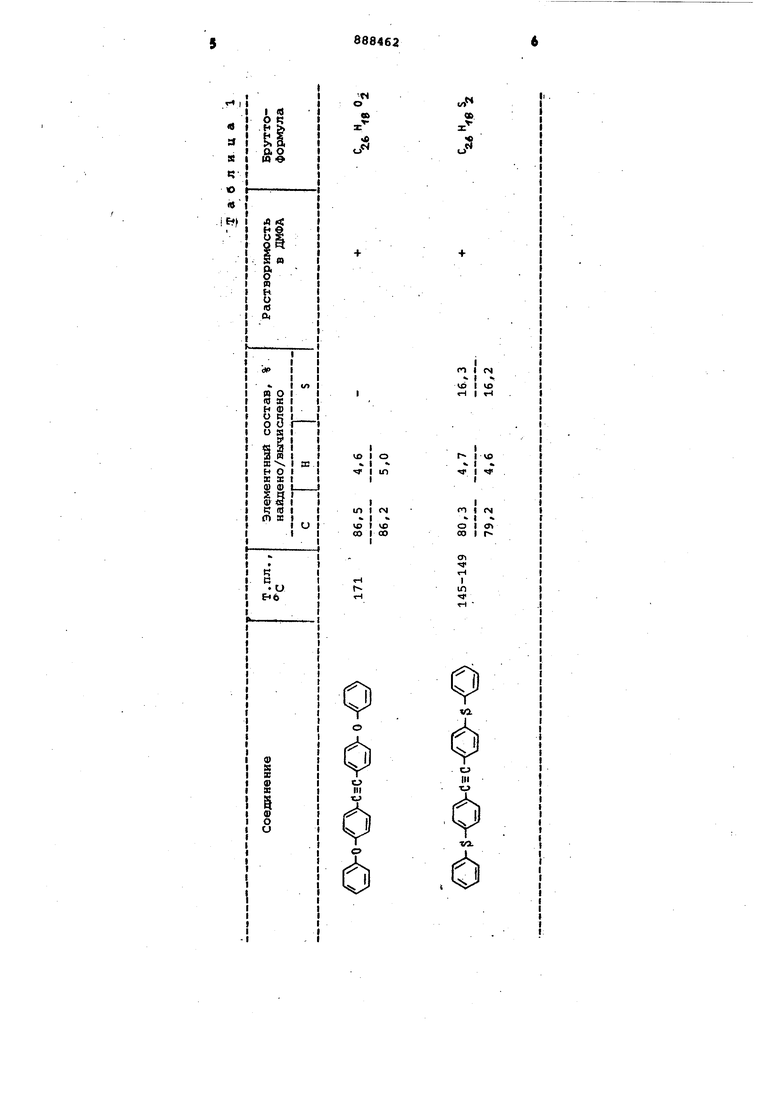
дигидрохлорированием промежуточного соединения формулы Q-K-)-CHСНСЦв присутствии амида натрия в жидком аммиаке. . Первую стгшию процесса осуществл ют при комнатной температуре, прили вая серную кислоту к смеси ароматического соединения и дихлорацёталя, Образупсцуюся вязкую массу раство ряют в четыреххлористом углероде. Промывают водой до нейтральной реакции, отгоняют растворитель и перекристаллиэовывают из спирта. Дигидрохлсчрирование проводят в жидком аммиаке в присутствии трехкратного иэбытка амида натрия при температуре от -55 до -45с. . Полученные ацетали очищают на колонке с AljO-j. . П j и м е р 1. Синтез дифенокситолана. В трехгорлую колбу, снабженную мешалкой, обратным холодильником и капельной воронкой, загружают 5 г (2,9-10 моль) дифенИлоксида, 2,4 мл (1,) дихлорацёталя и при комнатной температуре при интенсивном перемешивании прикапывают 40 мл серной кислоты. Смесь выливают в воду, растворяют в СС./ промывают водой, сушат над отгоняют растворитель, перекристалли зовывают из спирта. По данным ТСХ (хлороформ-гептан 1:1 по объему) исходного в полученном продукте нет Полученный продукт (3,81 г), растворенный в эфире, прикапывают к амиду натрия (1,5 г) в 150 мл жидкого аммиака при (-)55-(-) . После прове дения реакции амид разлагают водой, ацетилен экстрагируют эфиром (или хлороформом) , промывают водой, cjTiiaT отгоняют растворитель, очищают на колонке с А120%|ЭЛюент-:бензол. По ТСХ Rr О,9. Получают белые кристаллы с т.йл. . Вычислено %: С 86,16; Н 5,00, Найдено, %: С 86,51; Н 4,64. Выход по 2 стадиям 50%, Пример 2. Синтез бис-дифенилсульфидацетилеиа. К 5 г (2,) дифенилсульфида и 2,35 МП (1, 4510 моль) дихлорацёталя при комнатной температуре при перемешивании прикапывают 40 мл серной кислоты. Обработка синтеза как в примере 1. Полученный продукт дигидрохлорируют амидом нитрила как в примере 1.1дчистка на колонке с АVLОз.элюент-гексан-бензол 3:1 (по объему). Белые кристаллы с т.пл. 150-157 С, Бычеслено, % С 79,18; Н 4,56 S 16,24. - Найдено, %: С 80,34, Н 4,70, S 16,29. Выход по 2 стадиям 50%, Свойства полученных соединений приведены в табл. 1. Полимеры полифениленового типа по основе предлагаемого диарилзамещенного ацетилена подвергают испытанию на растворимость. Для этого 0,02 г полимера заливают 1-2 мл растворителяхлороформа, бензола, диоксана, диметилформамида, или для определения количественной растворимости навеску полимера 0,02 г растворяют в 2 мл диоксана и раствор титруют до начала помутнений. Результаты испытаний приведены в табл. 2. Как видно из табл. 2 количественная растворимость предлагаемых соединений выше, чем у ранее полученных, лучшая растворимость полимеров расширяет возможности переработки их в изделия.
о fo
9 ,
Формула изобретения
Диарилэамещенный ацетилен общей формулы
где R - -0-, -S-,
р качестве полупродуктов для синтеза
10
888462
карборансодержащих полимеров полифениленового ряда.
Источники информации, .принятые во внимание при экспертизе
l.ft.O. Maxwell The Reaction of Potassium Amide in Liguld Ammonia wi th Chloroethenes, JACS, 56, 132
(тэзм:
2. Авторское свидетельство СССР 717086, кл. С 08 G 61/12,28.09.77.



| название | год | авторы | номер документа |
|---|---|---|---|
| БЕСЦВЕТНЫЕ ЛЮМИНОФОРЫ РЯДА ФЕНИЛБЕНЗАЗОЛОВ | 2018 |
|
RU2683327C1 |
| Бесцветные органические люминофоры | 2016 |
|
RU2650518C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТОКСИИЗОБУТИЛИЗОЦИАНИДА | 1990 |
|
RU2026857C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАЦЕТАТА ТРИПЕПТИДА | 2014 |
|
RU2551276C1 |
| Рентгеноконтрастное средство | 1980 |
|
SU1087052A3 |
| Бис-арил-о-карборан в качестве промежуточного продукта в синтезе полимеров полифениленового типа | 1980 |
|
SU869290A1 |
| Амиды дибензо-18-краун-6, как промежуточные продукты для синтеза их комплексов с солями металлов | 1977 |
|
SU726096A1 |
| Способ получения производных пролина | 1977 |
|
SU747422A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННОГО ДИФЕНИЛАМИНА | 1999 |
|
RU2178784C2 |
| Способ отщепления сульфенильных групп от -сульфениламинокислот и сульфенилпептидов | 1978 |
|
SU767090A1 |


Авторы
Даты
1982-07-15—Публикация
1980-05-08—Подача