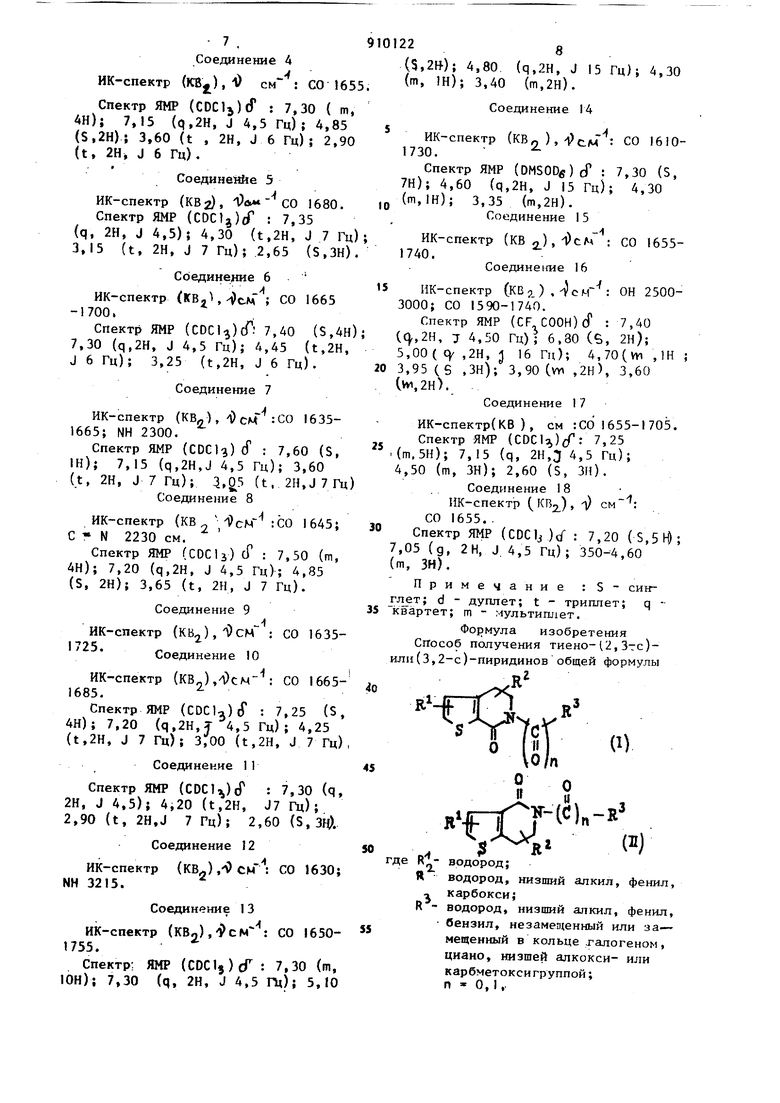
..T-A-icl% ггде R - водород; R водород, низший алкил, фенил, карбокси; водород, низший алкил, фен бензил, незамещенный или замещенный в кольце галоге ном, циано, низшей алкокси или карбметоксигруппой; п 0,1, отличительная особенность которого состоит в том, что соединения общей формулы (а где R, R , R , п имеют вышеуказанные значения, окисляют перманганатом калия при 40-56 с в ацетоне, це левой продукт выделяют или подвергают гидролизу для получения соединений формулы 1 и 11, когда п 1 и f 2. R и R имеют вьшеуказанные значения, R - водород. Исходные реагенты получают извес ными способами. Пример I. 5-0-Хлорбензил-4 оксо-4,5,6,7-тетрагидротиено-{3,2-с пиридин. К перемешиваемому и нагретому до раствору 6,5 г (24,6 ммоль) 5хлорбензш1-4,5,6,7-тетрагидротиеноС 3,)-пиридина в 250 см ацетона, порциями добавляют 15,59 г (98,6 ммо тонко размолотого перманганата ка ЛИЯ. Реакция протекает при темпер туре кипения растворителя с обрат ным холодильником. По окончании добавления при в течение 30 ми охлаждают и фильтруют через слой двуокиси кремния. Выпаривание досуха фильтрата даёт твердое вещество, которое кристаллизуют из диизопропи лового эфира.Кристаллы белого цвета: t пл 60 С, выход 55%. Пример 2. 5-Бензил-4-оксо-4,5,6,7-тетрагидротиено-(3,2-е)-пиридин. Следуют-методике примера I, но исходят из 5-бензил-4,5,6,7-тетрагидротиано-(3,2-с) -пиридина. Кристаллы белого цвета: tп 54C, (0,05 мм рт.ст.) , выход 64%. Пример 3. 5-П-Хлорбензил-4оксо-4,5,6,7-тетрагидротиено- СЗ,2-е)пиридин. Следуют методике примера 1, но исходят из 5-И-хлорбензил-4,5,6,7-тетрагидротиеноЧ 3,2-с)-пиридина. Кристаллы белого цвета: t 120°С (этанол-диизопропиловый эфир),- выход 66%. Пример 4. 6-0-Хлорбензил-7оксо-4,5,6,7-тетрагидротиено-(2,З-с пиридин. Следуют методике примера 1,но исходят из 6-0-хлорбензил-4,5.6.7-тетрагидротиено-f2.3-с}-пиридина. Кристаллы бледножелтого цвета: (диизопропиловый эфир), выход 45%. Пример 5. 5-Ацетил-4-оксо4,5,6,7-тетрагидротиено-(3,2-с )- пиридин. Следуют методике примера 1, но исходят из 5-ацетил-4,5,6,7-тетрагидротиено- (З,2-е)-пиридина. Кристаллы цвета слоновой кости: t-f (диизопропиловый зфир, выход 46%. Пример 6. 4-Оксо-5-0-хлорбензоил-4,5,6,7-тетрагидротиено-(З, 2-е)-пиридин. Следуют методике примера I, но . исходят из 5-0-хлорбензоил-4,5,6,7,тетрагидротиено-(3,2,с)-пиридина. Кристаллы белого цвета: (этанол-диизопропиловый эфир),выход 57%. Пример 7. 4-Оксо-4,5,6,7тетрагидротиено-(3,2,-с/-пиридин. Смесь перемешивают при комнатной температуре 4 ч, первоначально гетерогенную 13,6 г (0,069 моль) 5-аце - ТИЛ-4-ОКСО-4,5,6,7-тетрагидротиено(3,2-с)-пиридина (. пример 5) , 50 см зтанола и 50 см 6 н.соляной кислоты. Концентрируют под вакуумом, слегка подщелачивают остаток добавлением гидроокиси натрия и экстрагируют хлористым, метиленом. Органические экстракты промывают водой, сушат над сульфатом натрия и выпаривают досуха. Остаток кристаллизуют из смеси изопропанола с диизопропиловым эфиром. 5 Кристаллы белого цвета: t-,. 94, выход 70%. Пример 8. З-О-цианобензил-4-ОКСО-4, 5,6 , 7-тетрагияротиено- (-3, 2-с)-пиридин. Следуют методике примера 1, но исходят из 5-0-цианобензил-4,5,6,7тетрагидротиено-(3,2-е)-пиридина. Кристаллы белого цвета: .C (диизопропиловый эфир-изопропанол, выход 69%. . Пример 9. 5-0-Карбометоксибензил-4-оксо-4,5,6,7-тетрагидротиено-( 3,2-с)-пиридин. Получают, следуя методике примера 1, но исходя .из 5-0-карбометокси-4,5,6,7-тетрагидротиено-(3,2-с) пиридина. Кристаллы белого цвета: ПЛ (диизопропиловый эфир - изо пропанол), выход 61%. Пример 10. 6-0-Хлорбензоил-7-ОКСО-4,5,6,7-тетрагидротиено-(2, 3-е)-пиридин. Получают, следуя методике примера I, но исходя из 6-0-хлорбензоил-4,5- 6,7-тетрагидротиено-(2,3-с)-пчридина Кристаллы белого цвета: -ЬрА (этанол-диизопропиловый эфир) , выход 39%. i П р и м е р 11.6-Ацетил-7-оксо-4,5,- 6,7-тетрагидротиено-1,2, 3-е J-пиридин. Получают,следуя методике примера 1, но исхояд из 6-ацетил-4,5,6,7-тет рагидротиено- 2,3-е)-пиридина.Кристаллы белого цвета: 1.., , выход 43%. Пример 12. 7-Окео-4,5,6,7тетрагидротиено-(2,3-е)-пиридина. Получагот, следуя методике примера 7,но иеходя из 6-ацетил-7-оксо-4,5, 6, 7-тетрагидротиено-{;2, 3-е) -пиридина (пример и). Криеталлы белого цвета: t рл 120°С (диизопропиловый эфиризопропанол), выход 66%. Пример 13. 6-Бензилоксикарбонил-5-бензил-4-окео-4,5,6,7-тетрагидротиено- ( 3, 2-е)-пиридин. Получают, еледуя методике- примера 1, но исходя из 6-бензилокеикарбонил -5-бензил-4,5,6,7-тетрагидротиено(3,2-е)-пиридина. Криеталлы белого цвета: t 72° С ( циклогекеан , выход Пример 14. 6-Карбокси-5-бен ЗИЛ-4-ОКСО-4,5,6,7-тетрагидротиено(3,2-е )-пиридин.. Получают омылением 6-бензилокси- карбонил-5-бензил-4-окео-4,5,6,7тетрагидротиено-(3,2-е)-пиридина. . 26 |Криетаплы розового цвета: t 258С (изопропанол-этанол, выход 70%. Пример 15. 6-(3,4,5,-Триметокеибензилокеикарбонил)-5-(3,4,5триметокеибензил)-4-оксо-4,5,6,7тетрагидротиено-(3,2-е)-пиридин. . Получают, следуя методике примера 1, из 6-(3,4,5-т{)иметоксибензилокеикарбонил)-5-(3,4,5-триметокеибензил )-4,5,6,7-тетрагидротиено-(3,2-е пиридина. Кристаплы беловатого цвета: tp 55°С, выход 48%. Пример 16. 6-КарГюкеи-5-{3, 4,5-триметоксибензил)-4-окео-4,5,6,7-тетрагидротиено- (3,2-е) -пиридин. Получают омылением 6-(3,4,5-триметокеибензилоксикарбонил)-5-(3,4,5 триметоксибензил)-4-окео-4,5,6,7тетрагидротиено (З,2-е)-пиридина (пример 15). Кристаллы бежевого цвета: tf / 208C( изопропанол) , выход 65%. Пример 17. 4-фенил-6-ацетил7-ОКСО-4,5,6,7-тетрагидротиено(2,3-с)-пиридина. Получают, следуя методике примера 1, из 4-фенил-6-ацетил-4,5,6,7-т$трагидротиено-(2,3-с -пиридина.Кристаллы белого цвета: t 13. ( циклогексан-этилацетат), вымод 20%. Пример 18. 4-фенил-7-оксо4,5,6, 7-тетрагидро-гиено-(2,3-е)-пиридин. Получают, еледуя методике примера 7, исходя из 4-фенил-6-ацетил-7-окео4,5,6,7-тетрагидротиено-(2,3-е)- пи-. ридина (пример 17). Кристаллы белого цвета: t пд 16СРС (диизопропиловый эфир-изопропанол), выход 68%, Доказательство структуры соединеСоединение 1 ИК-спектр (КВ„) ,1) см : СО . Спектр ЯМР (CDClj) : 7,30 (m, 4Н); 7,20 (q , 2Н, J 4,5 Гц) ; 4,80 (S,2H); 3,55 (t,2H, J6 Гц); 3,00 (t ,2Н, ибГц) . Соединение 2 епектр (КВ) ,-V ем : С О 1645. Соединение 3 ИК-спектр (КВ -г) 1640. Спектр ЯМР (CDC1 ),30 (q , 2Н, J 4,5 Гц);7,25 (S,4ii); 4,70 (5,2Н); 3,55 (t,2H, J 6 ,05 (t,2H, J 6 Гц) . Соединение 4 1 ИК-спектр (KKf), CO 165 Спектр ЯМР (CDCljjtf : 7,30 ( ш, 4Н); 7,15 (q,2H, J 4,5 Гц); 4,85 (S,2H); 3,60 (t , 2H, J 6 Гц); 2,90 (t, 2H, J 6 Гц). . . Соединение 5 ИК-спектр (КВг), 1 л сО 1680. Спектр ЯМР ()«Г : 7,35 (q, 2Н, J 4,5); 4,30 (t,2H, J 7 Гц 3,15 (t, 2Н, J 7 Гц); 2,65 (S,3H) - Соединение 6 ИК-спектр (1ГВ,1,-ilcM ; СО 1665 -1700, Спектр ЯМР (СОСЦ)сГ: 7,40 (5,4н 7,30 (q,2H, J 4,5 Гц); 4,45 (t,2H, J 6 Гц); 3,25 (t,2H, J 6 Гц). Соединение 7 ИК-спектр (КВд), iDcM :СО 16351665; NH 2300. Спектр ЯМР (СОС1з) (f : 7,60 (S, 1Н); 7,15 (q,2H,J 4,5 Гц); 3,60 (t, 2Н, J 7 Гц); ,05 (t, 2H,J7nx Соединение 8 ИК-спектр (КВ , :СО 1645; С « N 2230 см. Спектр ЯМР (CDClj) cf : 7,50 (m, 4Н); 7,20 (q,2H, J 4,5 Гц); 4,85 (S, 2Н); 3,65 (t, 2Н, J 7 Гц). Соединение 9 ИК-спектр (КВ-,), л) см СО 1635 Соединение 10 ИК-спектр (КВ„),Л)см-: СО 16651685. Спектр ЯМР (CDCla) : 7,25 (S, 4Н); 7,20 (q,2H,J 4,5 Гц); 4,25 (t,2H, J 7 Гц); 3,00 (t,2H, J 7 Гц) Соединение 11 Спектр ЯМР (СОС1)сГ : 7,30 (q, 2Н, J 4,5); 4,20 (t,2H, J7 Гц); 2,90 (t, 2H,J 7 Гц); 2,60 (S, ЗЦ). Соединение 12 ИК-спектр , СО 1630; NH 3215. Соединение 13 ИК-спектр (КВ2), СМ-: СО 16501755. Спектр; ЯМР (CDCl5)cf : 7,30 (m, ЮН); 7,30 (q, 2Н, J 4,5 ГЦ); 5,10 2 (S,2№); 4,80 (q,2H, J 15 Гц); 4, 3,40 (т,2Н). Соединение 14 ИК-спектр (KB „ ),-l) см : CO 16101730. Спектр ЯМР (OMSODeJcT : 7,30 (S, 7H); 4,60 (q,2H, J 15 Гц); 4,30 (m,lH); 3,35 (т,2н). Соединение I 5 ИК-спектр (KB 2.) , : CO 16551740. Соединение 16 „К-спектр (КВ,),оМ- ОН 2500ЗООО; СО 1590-1740. Спектр ЯМР (CF СООН) (f : 7,40 q,,2H, 7 4,50 Гц); 6.80 (S, 2Н); ,00 ( су ,2Н, 3 16 Гц); 4,70(yvi ,1Н ; 3,95(6 .ЗН); 3,90CvY ,2н), 3,60 VM,2H). Соединение 17 ИК-спектр(КВ ) , см :СО 1 655-1705. Спектр ЯМР (СОС1а,)сГ: 7,25 (т,5Н); 7,15 (q, 2Н,3 4,5 Гц); ,50 (т, ЗН); 2,60 (5, ЗМ). Соединение 18 НК-спектр (KBj,) l) CO 1655.. Спектр ЯМР (CDClj )Г : 7,20 (S.SH); ,05 (g, 2Н, J 4,5 Гц); 350-4,60 m, ЗН). Примечание :S- синлет; d - дуплет; t - триплет; q вартет; m - мультиплет. Формула изобретения Способ получения тиено-(2,Зтс)ли(3,2-е)-пиридинов общей формулы fjQ г-(С)„-в к (Щ де R,- водород; водород, низший алкил, фенил, , карбокси; R - водород, низший алкил, фенил, бензил, незамеа1енный или за- мещенный в кольце .галогеном, циано, низшей алкокси- или карбметокси гр уппой; п 0,1,
9
отличающийся тем, соедиясп ня общей формулы
R2
-R
II 1
VOJn
или
|0
iiAcln-;
Е
91012210
1° где R, R, R 3, n имеют вышеуказанные значения, окисляют перманганЗтом ка-лия при ДО-Зб С в ацетоне, целевой продукт выделяют или подвергают гидролизу для получения соединений формулы 1 или П, когда n 1 и R и Я имеют вышеуказанные значения, R - водород.
Источники информации,
10 принятые во внимание при экспертизе 1. Michel Farnicr. Recherches en seril heterocycligue,- J. Canadien de Chimi, 1976, V.54, f 7, p.l0661068.





Авторы
Даты
1982-02-28—Публикация
1978-03-24—Подача