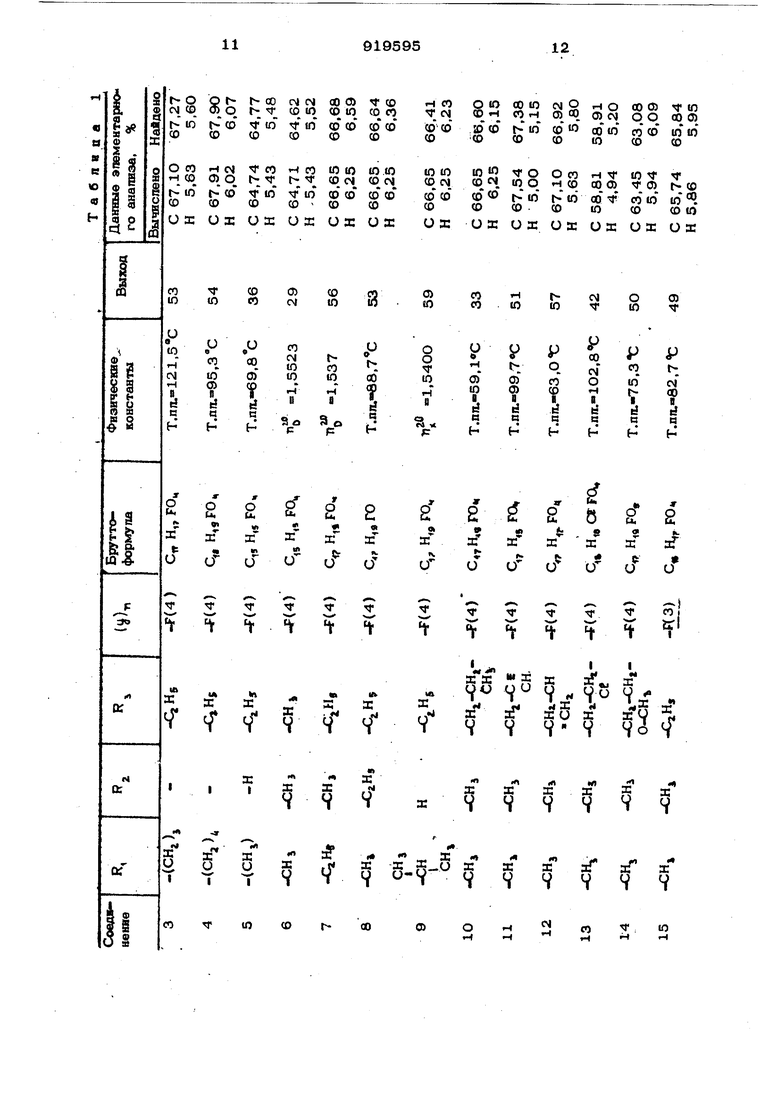
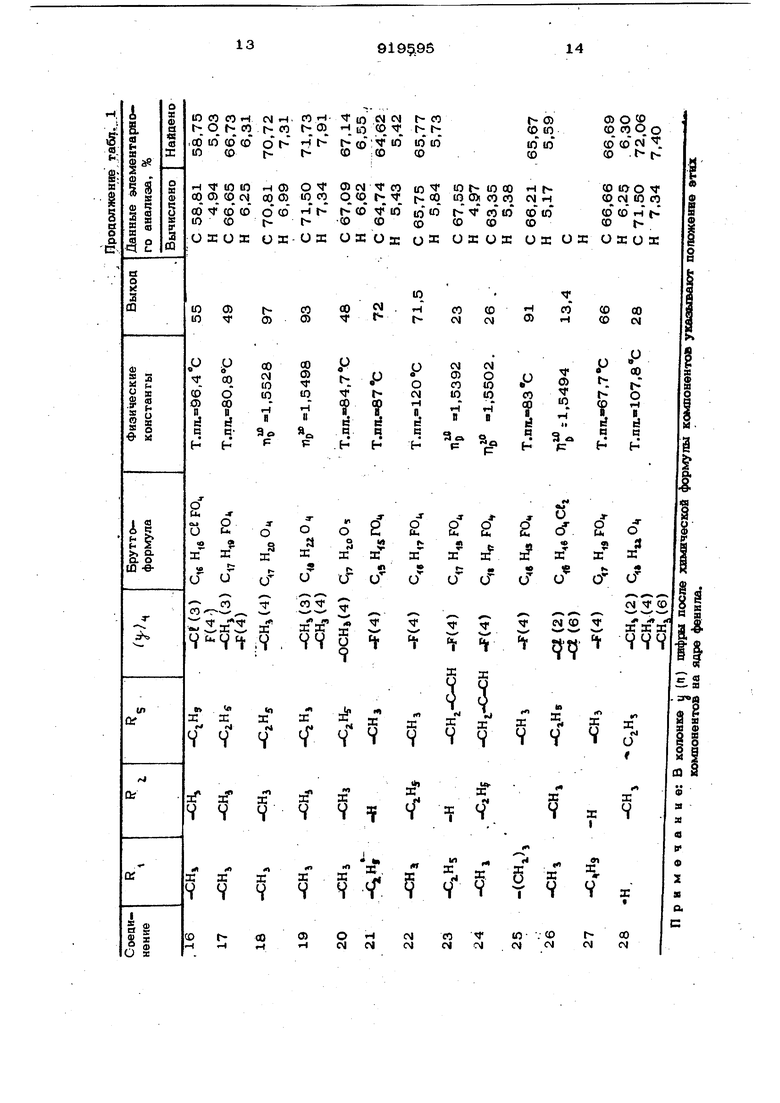
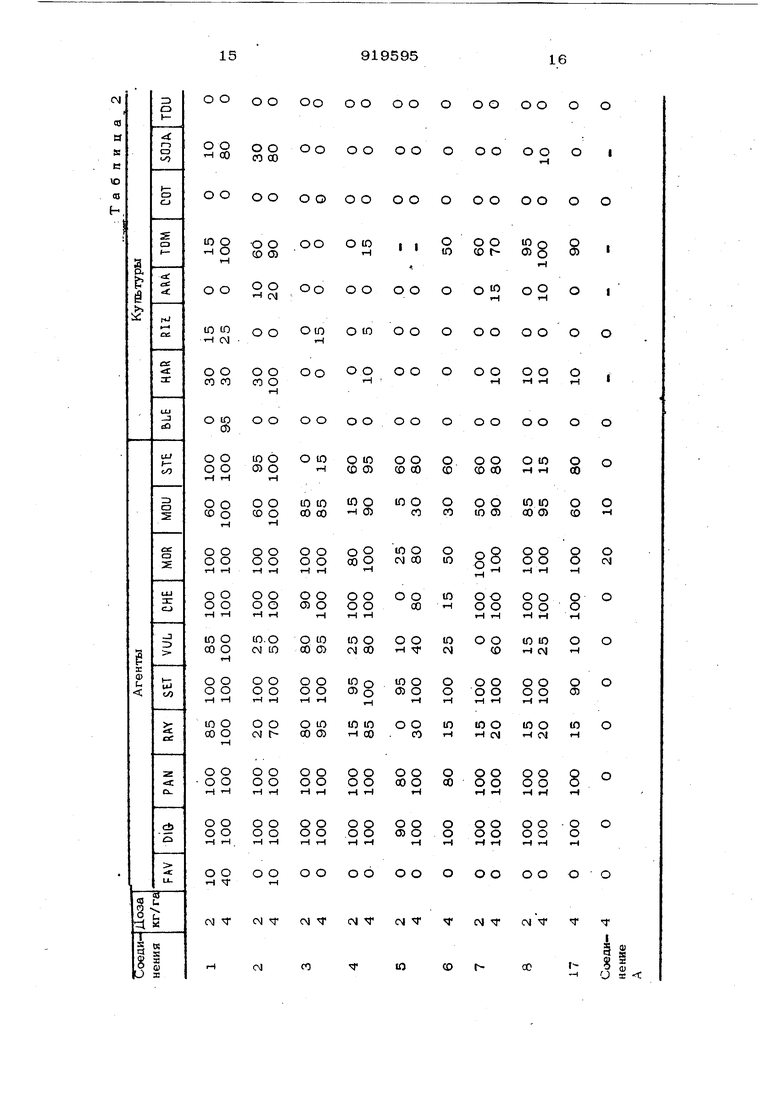
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-ФЕНИЛ-5.6ДИГИДРО-4-ПИРОНАИзобретение относится к способу попу чения новых соединений: производных 2-фенип-5,6-дигидро-4-пирона обшей формупыгде RI - апкил С -Q,; i - водород ипи апкип , ипи R и R вместе цепь - (СНг)), , где -п - 3 или 4; R - апкип , апкенип Cj. апкинип Сг, хпорэтип ипи метоксиэтип; Ц- гапог ген, метип ипи метоксигруппа; « - i, 2 ипи 3, при УСПОВИИ, что, когда Q-IW пичается от 1, заместитепи у могут быть одинаковыми ипи различными. Эти соединения могут быть использованы в качестве гербицидов. Способ основан .на реакции циклизации & -кетоспиртов в присутствии кислоты с получением гидропроизводных -пирона 1. Цепью изобретения является получение новых )f -пиронов формулы (1), обладающих гербицидной активностью. Зта цепь достигается согласно способу, заключающемуся в том, что производное уксусной Кислоты формупы f 3 -CHj- COOR 3 где R имеет указанные значения, t, ;(у)п означает радикал п.худили радикап (Jгде F, , RI , у и -п имеют указанные зн чения, подвергают взаимодействию с а, коголятом магния общей формулы (R40)2Mg где - апкип С -Сц, в среде инертного органического растворителя при тем- пературе кипения реакционной среды, и затем реакционную смось подвергают 39 взаимодействию с хлорангидридом кислоты общрй формулы Zn COCl где отличается от Л и озцдчаёт ра(Y)nx/дйкап «2- 5Н Сили радикап где R , R,, у, и п имеют указанные значения, в среде безводного инертного органического растворителя при О-20 С с последующей обработкой разбавпенный водным раствором сильной кислоты при 020 С, выделением продукта реакции обработкой его безводным разбавленным спиртовым раствором сильной кислоты при 60-10О С и выделением целевого продукта. Взаимодействие соединения (2) с алкогопятом натрия осуществляется в органической инертной безводной срзеде, на пример в бензоле, толуоле, ксилоле или этиловом эфире при температуре кипения реакционной среды до окончания реакции В качестве агаколята магния предпочт тельно используют этилат магния, который можно получить ин ситу путем реак ции между магнием и этанолом в органи ческой инертной безводной среде в присутствии тетрахлорида углерода. Действие хлоридом кислоты на полученную реакцию смесь осуществляется в органической инертной безводной среде, например в эфире, толуоле или бензоле, при О-20°С. Проводят сначала обработку реакционной смеси, при помощи водного разбавленного раствора сильной кислоты, например серной, при 0-2Ос, что ведет к частичной циклизации и разложению гидролизом соединения формулы ЯцО затем обрабатывают выделенный продукт реакции спиртовым безводным разбавлен ным раствором сильной кислоты, например соляной, при 60-100 G. При последней обработке предпочтительно используют этанольный разбавлен ный безводный раствор соляной кислоты, полученной ин ситу в результате деист. ВИЯ незначительного количества ацети)ьхпорида на этанол. Соединения идентифицированы спектро метрией ЯМР. Спектры получены в COPj или с использованием reKcaMeTHj дисипоксана как внутреннего стандарта. 5 Пример 1. Получение 2-(4фторфени л )-3-этоксикарбонип-5-эти л5,6-дигидро-4-пирона (соединение 1). 9,1 г (0,08 моля) этилата магния, 5О мл сухого толуола и 16,8 г{0,О8 мо ля) 4-фторбензоилацетата этила смешивают при комнатной температуре, затем нагревают с обратным холодильником в течение 1 ч и охлаждают в бане с ледяной водой до , добавляют 0,1 г гидрохинона, затем приливают 9,5 г (0,08моля) 2-этилакрилоилхлорида при темпера- , туре в интервале 0-10°С. Во время прилива ния добавляют 30 мл сухого ацетонитрила для разжижения среды. Затем в течение 1 ч проводят пере- мещивание при комнатной температуре и реакционную смесь выливают на смесь 50 г льда и 5 мл концентрированной серной кислоты. После 30 мин перемещивания происходит декантация толуоловой фазы, а водную фазу дважды экстрагируют по 5О мл толуола. Собранные толуоловые фазы промьтвают 50 мл 1О%-ной серной кислоты, затем 5О мл раствора бикарбоната концентрацией 5%, затем 50 мл воды. После сущки над безводным Мог 50ци выпаривания растворителя полученнзю жидкость соединяют с 200 мл этанопа при 95с и 0,5 мл ацетилхлорида, затем нагревают с обратным холодильником в течение 30 мин. После выпаривания спирта маслянистый остаток очищают молекулярной дистилляцией. Получают 13,5 г 2-(4-фторфенил)-3-этоксикарбонип-5-этил-5,6-дигидро-4-пирона в виде вязкой желтой жидкости. Выход 61%; По° 1,5412. Элементный состав. Вычислено, %: С 65,74; Н 5,86. Найдено, %: С 65,57; Н 5,97. 2-( 4-фторфени п)-3-этоксикарбонил-5-этил-5,6-дигидро-4-пирон (соединение 1) получают также следукшим способом: выливают при комнатной температуре 10 г {о,Об моля) 2-этил-акрилацетатаэтила на 6,85 (0,06 моля) этилата магния во взвеси в 6О мл безводного толуола, и смесь нагревают с обрат1 ч, затем ным холодильником в течение охлаждают до ОС. В эту смесь выливают 9,5 г (О,06 моля) парафторбензонпхлорида (9,5 г) при 0-5°С. После доведения до комнатной температуры реакиионную смесь псремещивают 2 ч и доб1авляют ЗО г льда и 3 мл концентрированной серной кислоты при перемешивании в течение 1 ч. Происходит декантация органической фазы, а водную фазу экстрагируют топуолом. Собранные органические фазы промывают 1О%-«ой , затем 5%-ной KaHCOj, затем водой и, сушат и концент рируют. Остаток разбавляют 10О мл абсолюткого этанола и 2 мп ацетилхлорнда, нагревают с обратным холодильником в течение 1 ч, снова концентрируют, сначала осуха .при 1О мм рт.ст, и затем при 1О мм рт.ст. Попучают 14,0 г маслянистой жидкое ти с 9О% 2-(4-фторфенил)-3-этоксикарбони11-5-эти 71-5,6-дигидро-4-пирона. Пример 2. Получение 2-(4-фто фенип)-3-этоксикарбонип-5,6-димети -5,6-дигидро-4-пирона (соединение 2). 1,9 г тонких стружек магния, 12 мл абсогоотного этанола. 5О мл сухого бензола и 0,4 мл сухого тетрахпорметана доводят до 5О-6О С при слабом перемешивании. Когда приостанавливается выцеление водорода, смесь нагревают с обрат ным холодильником в течение 1 ч и охлаждают до комнатной температуры. Приливают 16,8 г (0,О8 моля) 4фторбензоилацетатэтила, смесь затем нагревают с обратным хоподигаьником в течение 1 ч, затем охлаждают до 5 С, добавляют 5О мл ацетонитрила для разжижения среды и по капле добавляют 9,5 г (О,О8 мопя) 2-метил- -бутеноилтрансхлорида. Перемешивание продолжают в течение 1 ч при комнатной температуре. Оставляют на ночь и затем реакционную смесь выливают на 5О г льда и 5м концентрированной серной кислоты. Через 30 мин перемешивания происходит декантация толуоловой фазы, а водную фазу дважды экстрагируют толуолом по 5О мл. Собранные толуоловые фазы промывают 50 мл 1О%-ной серной кислоты, за тем 5О мл 5%-ного раствора бикарбоната, затем 5О мл воды. После сушки безводным Mc(;.SO и 6ы паривания растворителя полученную жид кость сливают с 20О мл 95 -ного этанола и 0,5 мл ацетилхлорида и нагревают с обратным холодильником в ечение ЗО мин. Жидкостной хроматографией определиют, что соединение состоит из смеси изомеров, состоящей по весу на 95% транс-изомера и 5% цис-изомера. Трано-изомер с т. плавп. 7 5 С можно выделить рекристаллизацией в оиктюгек- сане ранее полученнгЧ смеси изомеров. Шс-изомер с т. плавл. 85, можно выделить из маточных вод рекристаяпизаоии ранее полученной смеси изомеров подготовительной жидкостной хроматографией с применением следующей смеси элюирования: 2,2,4-триметиппентан (95%) и 2-изопропаноп (5%). Пример З.С использованием технологии по примеру 1 получают соединеиия № 3-28 производные формупы (1), физико-химические свойства которых приводятся в .табл. 1. П р и м е р 4. Гербицидная активностъ в оранжерее культурных и дикорастущих растений. В горшки размером 9«9«9 см, напоганенные сельскохозяйственной землей, высевали семена, количество которых зависело от типа и величины семени. Семена покрывали слоем земли толщиной около 3 мм. После увлажнения земли горшки обрабатывали распылением определенного количества жидкости на горшок при объеме 5ОО п/га и с содержанием значительной дозы активного вещества. Жидкость готовили разбавлением водой эмульгируемого концентрата со следующим сотношением компонентов, вес.%: Агент эмульгатор-нонилфенолоксиэтилен с 17 окисями этиленаЮ Активное вещество20 Растворитель (ксипол)7О При раэбавпении активное вещество содержится в значительной степени. Исследования проводили при дозах активного вещества 0,25-8 кг/га. Обработанные горщки затем помеща-ли в баки, снабженные системой ния, субирригации и выдерживали 35 дн. при комнатной температуре и относительной влажности 70%. По истечении 35 дн. выявляли коэффициент уничтожения по отношению к контрольным растениям, обработанным в тех же условиях, но без содержания активно го вещества в циснерсии пульверизации. . Кроме того, на протяжении теста наблюдали за возможными морфологическими изменениями растений. Бы пи подвергнуты тесту следукяиие культурные и дикорастущие растения: ДикорастущиеСимвол Дикорастущий овесFA V Напё хгтянкаD 1 ( Бур развесистый Райграсе Лисохвост Лебеда Паслен Горчица Звездный Культурные Фасоль Арахис Хлопок Подсолнух в качестве продукта для сравнения брали известное соединение 2-фенип-З-отоксикарбони л-5, б-димети л-5,6-дигидро-4-пирон (соединение А) Полученные результаты (в процентах разложения обработанных растений по от ношению к необработанным; 100% означает полное уничтожение данного растения) предложены в табл. 2. Указ;анные результаты свидетельствуют о высокой активности в качестве гер бицидов соединения по предмету изобретения, а также их селективность по от ношению к рассмотренным культурам. Следует, что эти соединения обладаю высокой гербицидной активностью по от ношению к большому числу дикорастущих растений, как злаковых, так и двусемянодояьных. Гербицидная активность проявляется особым способом, вызывая у растений я ление альбинизма и затормаживая и/или иссушая их или уничтожая. Особенно интересные результаты наблюдали с использованием следующих со динений: . -2-(4-фторфенил)-3-этоксикарбонил -5-9Тил-5,6« нгидро-4-Ч1Ирон (соединение 1); -2-(4 торфенил)-3-9токсикарбонип -5,6-диметип-5,6-дигидро-4-пирон (сое динение 2); -2-(4-фторфенил)-3-этоксикарбонип -4а,5,6,7,7а-пентагииро (в) циклопента -4-пирон (соединение 3); 2-( 4-фгорфенил)-3-вгоксикарбонил-4а,5,6,7,8,8а-гексагнярофлавон (соеди нение 4); - 2-(4Ц торфенил)-3-этоксикарбонип -5- ти1 -6-метип-5,6-дигидро-4-пирон (ооедине1гае 7); 9 58 - 2-()торфенил)-3-«токсикарбонип-5-метип-6-этил-5,6-дигидро-4-пирон (соединение 8). При использовании перед сбором культурных растений и сорняков от дозы 1 кг/га соединения 1, 2, 3, 4, 7, 8 на 100% разрушают наперстянку. При той же дозе бур разрушается на 100% соединениями 1, 3, 4, 7 и 8, а сетер - соединениями 1, 2, 3, 7 и 8, паслен - со единениякга 3 и 8. При дозе 4 кг/га соединения 1, 2, 3 и 4 проявляют высокую активность по отношению ко всем видам сорняков как злакош 1х, так и д хсемядольных за искшочением дикого овса, а в случае соединения 3 - звездного. Соединения 1, 2, 3, 4, 7 и 8 хорошо переносятся подсолнухом и хлопком, а также другими растениями, например зерновыми (соединения 2, 3, 4, 7 и 8), рисом (соединения 2, 4, 7 и 8), соей (соединения 3, 4, 7 и 8), арахисом (соединения 1, 3 и 4), фасолью (соединение 3) и томатом (соединение 3). При гербицидной обработке, проводимой при помоши соединений: формулы (1) доза активного вешества может составлять 0,25-8 кг/га в зависимости от вида соединения, типа культуры и природы почвы. Предпочтительно эта доза составляет 0,5-5 кг/га. Для применения на практике соедине- . кия формулы (1) редко используют по одному. Чаше всего они являются компонентами составов, KOTOfbie включают помимо активного вешества по предмету изобретени я еще носитель и/или поверхностно-активное вешество, а содержание активного вешества остается в интервале О,О1-95%. Термин носитель означает вешество, органическое или минеральное, приводное или синтетическое, с которым сочетается активное вешество для облегчения иане- сения его на растения, семена и почву, а также транспортировки и манипулирования. Носитель может быть твердым (глины, естественные или синтетические силикаты, смолы, воск, твердые удобрения) или жидким (вода, спирты, кетоны, нефтяные фракции, хлоруглеводороды и разжиженные газы). Поверхностно-активное вешество может быть эмульгатором, диспергатором и пи смачивавшим веществом, ионным или неионным. Можно назвать, например, соли полиакриловых кислот, пигниносульфр99HoBbix кислот, конденсаты окиси этилене ив жирных спиртах, жирных кислотах ипн аминах. Композиции можно получить в виде смачиваемых порошков, .порошков для ра пыпения. гранул, растворов, эмупьгируеколх концентратов, эмульсией, коицентра тов в суспензии и аэрозолей. Смачиваемые порошки обычно получа ют с содержанием 20-95 вес.% активного вешества, .и помимо твердого носителя они содержат О-5- вес.% смачиваемого агента, 3-10 вес,% стабилизатора и/или другие добавки, например агенты пенетрации, адгезии, агенты против образования комков, красители и т.д. Пример смачиваемого порошка, вес.%: Активное вещество (соединение 2)50 Лигносульфонат кальция (дефлоккулянт)5 Изопропилнафталенсульфонат (анионный смачивающий агент)1 Двуокись кремния против образования комков5 Каолин (добавки). 39 Гранулы для нанесения в почву готовят размерами 0, мм, их готовят а гломерацией или импергнированием. Как правило, гранушл содержат 0,5-25% активного вешества и О-10 вес.% добавок например стабилизаторов, и растворителей. Эмульгируемые концентраты для пуль веризации ссшержат обычно кроме раств рителя, естга это необходимо, со-растворитель 10-50 вес.% объема активного вешества, вес.% объема добавок. 5 как стабилизаторов, пенотраторов, ингибиторов коррозии, адгезионных красителей. Пример композиции эмульгируемого концентрата, г/т Активное вещество (соединение 3 )4ОО Додецилбензолсульфонат (шелочной)24 Нонилфенолоксиэтилен с Ю молекулами эти леноксида16 ШЛлогексанон20О Ароматический растворительДо 1 л Концентраты в суспензии для пульверизации получают таким образом, чтобы жидкий стабильный продукт не разлагался, и содержат обычно 1О-75 вес.% активного, вешества. 0,5-15 вес.% поверхностно-активного вешества, О,1 10 вес.% тиксотропных агентов. О- 1О вес.% добавок, например агентов против образования пены, ингибиторов коррозии, стабилизаторов, пенетрантов и адгезийных агентов; в качестве носителей - воду или органическую жидкость, в которой активное вешество почти нерастворяется: некоторые твердые органические вешества или минеральные соли могут быть растворены в носителе, чтобы помочь избежать седиментации, или как антигели для воды. Композиции могут содержать другие ингредиенты, например зашитные коллоиды, агенты или загустители, тиксотропные агенты, стабилизаторы или ее агенты для образования внутрикомплекснрго элементоорганического соединения, а также другие активные вешества с известными пестицидными свойствами, например инсекциды или фунгициды.
л л«л
Ж X Z -С ас
1 С С С С
зГ лГ i
V
V
(N
ю
ф
о
/м тк г n I и и о о оо оо оо оо о оо 2§ пда°° °° - оо оо оо оо оо о оо О 00 ,00 ою , , о 00 оо 2S оо оо оо о о CNI ;«Н ют оооюotoоо о оо тН (N «-Н оо оооо ооо о оо СОСОСОО .Ч ОЮ оооооооо о оо б) оо ю6оюоюоо о оо ОООО--1СОО)СООО COCDOO «-Н 1-ЧтН Оо ооюююоюо о оо соо CDO0000НО)со со ЮО) гЧН оо ооооооюо о .-.о оо оооо«о0)00 ю хо гНтЧтНгЧгЧтнiH i4 оо оооооооо ю оо оо оооооо00 тч оо гНгНтН,- r-tr-t г tHr4 юо ю.ооююооо ю оо соо с 1ЮООО OJOOНгт см(О 1-1 оо ооооЮоюо о оо оо ооооОо 3)О о оо
юо оо ою юю оо ю юо юо ю о
S
ооо МГ- 000) тНОО- со - --(см i-tCM И
се
оо оо оо оо оо о оо оо оо оо оо о о ооо оооо оо
гНгЧ 1-)
о оо оо о оо оо-о о
о о о о о о о о)оооо оо о о о о о
оо оо оо оо оо о оо оо о о
тН ЧгСМ 01 СМ СМТ CVl СМя ts
I § S ё
01со
юсо г-00f- , S
- U а: оо о о оо о о gg g , оо о I Н оо о о оо о , гНгЧгН оо о о ою о о H-H 00 юю о о 000) со - оо о о оо о oj r4.-i-4 оо о о ооо t-tHi-( юю о о rHCvj tH оо о о оо О) t Ф о р м упа изобретен Способ получения производных 2-4 нил-5,6-дигидро-4-пирона общей форму Rt.x 4 300R5 Д, 2 / где R - апкип С -Сц; Rj - водород или апкип С -Сц итш Rj и R вместе образуют це -(СН,)„ где Т1ч - 3 или 4; R,,- алкип , апкеиил С, апк НИЛ Сд, хлорэтип или метокси этил; U, - галоген, метип иш метоксигруппа;Т1 - 1, 2 или 3, при условии, что когда л отличается от 1, за местители у. могут быть один ковыми или различными, отличающийся тем, что про изводное уксусной кислоты общей ф) Z,-С-СИ,-COOS I ,1 2л где RJ, имеет указанные значения, Itj означает радикал K2-CH Jили («адикал 95 где R,i Rj, и n имеют указанные значения, подвергают взаимодействию с алкоголятом магния общей формулы )2Kg, где R - алкил , в среде инертного органического растворителя при температуре кипения реакционной среды, и затем реакционную смесь подвергают взаимодействию с хлорангидридом кислоты обшей формулы Z2COC1 гда Zj отличается от г, и означает ра 1 г-СН-р-1 или радикал где R, , Rj, ц, и я имеют указанные значения в среде безводного инертного органического растворителя при с последующей обработкой реакционной смеси разбавленным раствором сильной кислоты при О-20 С, выделением продукта реакции обработкой его безводным разбавленным спиртовым раствором сильней кислоты при 6О-1ОО°С и выделение целевого продукта. Источники информации, принятые во внимание при экспертизе 1. Эльдерфильд Р. Гетероциклические оединения. М., изд. И-Л, 1953, т. 1, . 303.





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 2-фенил-4-пирона | 1980 |
|
SU938742A3 |
| Способ получения производных 3-цефем4-карбоновой кислоты или их солей | 1976 |
|
SU589921A3 |
| Способ получения производных дибензооксепина | 1974 |
|
SU622403A3 |
| 4-ГИДРОКСИПИРАН-2-ОНЫ, ЦИКЛООКТИЛ-ИЛИ БЕНЗОПИРАН-2-ОНЫ, 4-ГИДРОКСИ-2Н-ПИРАН-2-ОНЫ И 4-ГИДРОКСИ-ЦИКЛООКТАПИРАН-2-ОНЫ | 1995 |
|
RU2139284C1 |
| Способ получения 5-замещенных 10,11,-дигидро-5н-дибензо( @ , @ ) циклогептен-5,10-иминов | 1978 |
|
SU895288A3 |
| Способ получения 8-бензофурилметил1,3,8-триазаспиро-/4,5/-деканов | 1972 |
|
SU442597A1 |
| Гербицидное средство | 1974 |
|
SU530628A3 |
| ТРИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ПИРАЗОЛА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2191176C2 |
| Способ получения -декаметилен -валеролактона | 1976 |
|
SU682519A1 |
| Способ получения эфиров циклопропанкарбоновых кислот | 1973 |
|
SU584759A3 |


Авторы
Даты
1982-04-07—Публикация
1979-03-14—Подача