1
Изобретение относится к новым химическим соединениям, в частности к 4-алкилсульфамоилфталонитрилам, которые могут быть искоцным соединением для синтеза 4-алкилсульфамоипфталоцнанинов, используемых в качестве красителейи пигментов в производстве паст шариковых ручек, резины, лаков, полимерных составов.
Известна 4-сульфамоилфгалевая кислота, которая является структурным предложенного соединения Ц. .
На ее основе можно получить толысо тетра 4-сул ьфамоипфтал оциа ннны.
Известна также 4-сульфофталевая киолота и ее ангидрид 23. На- основе этого ангидрида получают металлические ксадплексы тетра 4-алкипсульфамоилфталО1ша1 нов, в частности тетра-4-октадецилсульгфамоилфталоцианинов 31,
Реакция протекает по следующей cTi& ме: ангидрид 4-сульфофтапевой кислоты -(МаЮ5)ц -4-.ФпМ-()н -.4-ФцМ- -(SOa МНСйН57)ц 4-ФцМ, где М - Ctt,,
In, VO jcpv М - металлический комйЛ51ГС фталошшнина 4 .
Однако сульфохлорзамещенные фталопианины при выделении, а также при sMVдировании гидролизуются и приводят к об разованию смесей сульфид /сульфофталоцианинов. Кроме того, приведенный способ ограничен в выборе металлов, он исключает возможность получения комплексов тетра-4-алкипсульф9моил4ггалоштнннов с переходными металлами, а также безм&тального фталоиианина.
Целью изобретения {шляется расигареяне ассортимента производных фталевой кислоты для синтеза гетра-4-алкилсульфамоилфталоцианинов с улучшенными свойствамв.
Поставленная цель достигается предло,г женныкш 4-алкилсульфамоклфгалонитриламв рбшей формылы
,
Б ККОгЗ
где когаа R - водород, то - метил, этил,
когда N - водород, то f - никлогексил,или -метил, этил, н -бутил.
Соединения обшей формулы получают по известной реакции взаимодействия хлорангиарида 1,2-дибромбензол-4-сульфокислоты с первичными или вторичными, либо алициклическими аминами ИЗ с посследующим цианированием образующихся 4-моно, ди- и циклоалкилсульфамоил- -1,2-дибромбензолов цианистой медью в апротонном полярном органическом растворителе {диметилформамид, М-метилпирролидон) с добавкой разбавителя для подавления гидролитического расщепления нитД-- тв-к « Д °
Вг
рильных групп. В качестве последнего применяют, нейтральный ароматический растворитель, например, нитробензол. Цианирование ведут при температуре кипения реакционной смеси (18О°С) и объ емном соотношении растворителя и разбавителя 1:2 или в случае 4-диметилсульфамоил-1,2-дибромбензола при 190°С и соотношении растворителя и разбавителя 1:5. Продукты реакции выделяют обработкой реакционной массы концентрированным водным раствором аммиака на холоду с последующим хроматографированием на силикагёле. Выход 4-алкилсульфе моил- фталонитрилов составляет 4О-50%.
Процесс протекает по следующей схеме:
,2-r,li
.-цр ДМФА,НБ
г2т,1
Полученные соединения представляют собой кристаллические вещества белого цвета. Пример. 4- Диэтилсульфамоил7 фталонитрил.. .Смесь 0,37 г (0,001 мол 4-диэтилсульфамоил-1,2-дибромбензола, 0,36 г {0,004 моль) СмСМ., Ю мл д метилформамида и 20 мл нитробензола п ремешивают 4 ч при кипении (), охлаждают до 0°С, прибавляют Ю мл 25%-ного водного аммиака и перемешивают ЗО мин при 0-2 °С. Из смеси полностью удаляют аммиак, воду и частично избыток органических растворителей упариванием под вытяжкой при комнатной температуре . Остаток хроматографируют на силикагёле, элюируя петролейным эфиром нитробензол и смесью хлороформ ацетон (1:1) - продукты реакции. Получают 0,19 г твердого вещества. Повторным хроматографированием на силикаге ле выделяют 0,05 г смеси исходного дибромпроизводного и монобромзамешенного нитрила (элюент: петролейный эфир хлороформ 4:1), 0,02 г тетра-4-диэтилсульфамоилфталоиианина меди (элюентхлороформ) и 0,12 г (46%) 4-диэтилсульфамоилфталонитрила. (элюент; петролейный эфир - хлороформ, 2:1), белог цвета кристаллы (из смеси петролейный эфир - хлороформ, 1:1). Т. пл. 112ИЗ С . Найдено, %: С 54,46, 54,54, Н 5,42, 5,40; N15,21, 15,17: ,,r4iOjS . Вычислено, %: С 54,73; Н 4,99, Ml 5,96. 4-.Диэтилсульфамоил-172-дибромбензол получают с выходом 94% кипячением в течение / 2 ч смеси 3 г хлора гидрида 1,2-дибромбензол-4-сульфокис. лоты и 34 мл диэтиламина, бесцветные иглообразные призмы (из петро- лейного эфира). Т. пл. 6О-61,5°С. П р и м е р 2. 4-Метилсульфамош фгал о нитрил. Синтезируют из 4-метил сульфамоил-1,2-дибромбензола при молярном соотношении дибромбензола и Си С К 1:4, как описано в примере. Хроматографированием на силикагёле смесью хлороформ - ацетон {2О:1) выделяют до 10% смеси исходного дибромпроизводного и монобромзамешенного нитрила, хлороформом - тетра-4-метилсульфамоилфталоцианин меди в следах и 4-метилсульфамоилфталонитрил с к 1ходом 45%, белого цвета кристалла, т. пл. 152-153° С. Найдено, %: С 48.43, 48,52 Н 3,25 3,45, N 18,21, 18,30. CflH NbOiS Вычислено, %: С 48,87; Н 3,19) N19,00. 4-Метилсульфамоил-1,2-дибромбеизол получают с выходом 40% кипячением в течение 1 ч раствора 7,65 г сульфохл рида и 25 г метиламина в 1ОО мл абсолютного этанола. Бесцветные иглообраз ные призмы (из петролейного эфира), т. Ш1. 101-102 С. Найдено, %: С 25,38, 25,61 Н 2,08 2,11.; t 4,12, 4,19; Вг 48,93, 48,66. CiHrBrjHOaS Вычислено, %: С 25,56, Н 2,14; N4,26; В .48,66. П р и м е р 3 . 4-Двбутилсульфамонп фталонитрвл. Получают вэ 4-Дибутилсупьфамоил- ,2-дибромбевзола при мол1фном соотношении дибромбензола и СиСМ1:4, как описано в примере 1. Выход 4-дибутилсульфамоилфталонитрила 40%, бесцветные призмы (из петролейного эфщ)а), т. пл. 89-90 С. Найдено, %: Н 12,92; 13,08, 10,О5 10,24. Вычислено, %: N13,15, ЫО,ОЗ. ИК-спектр (табл. КВч, см): 2238 (C2N), наряду с 20% смеси исход ного дибрсмпроизводного и монобромэам& шенного нитрила (элюент - бензол) и 5% тетра-4-дибутилсульфамоипфталоциани на меди (элюент - хлороформ). 4-Дибутилсульфамоип-1,2-дибромбен« зол получают с выходом 92% взаимоде ствием 4,2 г сульфохлсчэида с 8,3 г 1О мл Н -дибутиламина в условиях анало гичных описанным в примере 1 для 4-диэтилсульфамоил-1,2-дибрс бензола. Бесцветные иглообразные призмы (из neiv ролейНого эфира), т. пл. 81-82 С. Найдено, %: МЗ,О7, 3,О6,- S 8,14, 7,88,- Вт 37,65, 37,93. Вычислено, %: N3,28; S7,51, Вт 37,42, П р и м е р 4. 4-Диметилсупьфам0Ю1фталонитрил. Смесь 0,68 (О,002 моль) 4-диметилсульфамоил-1,2-дибромбензола, О,72 т (0,О08 моль) , 20 мл диметилформамида и 10О мл нитробензола перемешивают 4 ч при кипении (19ОС) затем реакционную массу обрабатывают, как описано в примере 1. Хроматографированиал на силикагеле выделяют 0,15 г (26%) 5-диметилсупьфамоил-2-дианобромбензала (элюент: пет ролейный эфир - хлороформ, 4:1), белого цвета кристаллы (из смеси петролейный эфир - бензол, 1:1), т. пл. 1в5-166 С. Найдено, %: N 9,28, 9,43fS. 11,7О, 11,96. C HsBrNzPz Вычислено, %: N 9,69, § 11,08. ИК-спектр (табл. KB, см ): 2245 (CS N ), О,23 г (50%) 4-диметилсульфамоилфгалонитрила (элюент: хлороформ петролейный эфщ), 2:1), белого пвета кристаллы (из смеси петролейный эфир - хлороформ, 2:1), т. пя. 131-132 С. Найцено,%: С 5О,82; 50,е4{Н 4,14; 4,04. N 17,95, 17,93 S 13,66, 13,69, Вычислено, %: С 51,02 Н 3,86 N 17,85; § 13,64 в 0,02 г тетра-4диметилсульфамовлфгалооианвва меди (элюент: CHCli- МеОН, 15il ). 4-Диметвлсульфамовп-1,2-двбрс 4бе зол получают с выходом 95% квпячеввем 1,4 г сульфохлорвда с 4О мл 25%-вого водного раствора двметвламвва. Бесаве ные иглообразные призмы, т. im. 120122 С (вз петролейвого эф|фа). Пример5. 4 вклогексвлсульф мсяшфгалонвтрвл. Получают:из 4-цвкло гексилсульфамовл-1,2.-двбромбевзола прв молярном соотношении двбромбевзола в СцС 1:4, как опвсано в 1фвмере 1. Хрс «атографврованвем ва свлвкагеле бензолом выделяют до 20% смесв всхоД, вого дибромпровзводного в мовобромзамещенного ввтрвла, 4-цвклргексвпсульфа4 мовлфгалонитрвла с выходом 2О%, бесцветные , т. Ш1. 1О4-1О5 С. Найдено, %: N14,15,14,09, . 510,89, 1О,75. C H«Ni0 5 Вычвслено, %: ,J 14,53; 511,07, варяду с 25% тетра-4-т1Клогексвлсульфамовлфгалошшнввом медв (алюевт - хлороформ) . 4-Циклогексвлсульфамовп-1,2-двбромбензол получают с выходом 98% квпяченвем бевзольвого раствора 5,6 г cynt фохлорвда с 5 мл шослогексвламввй. Беоцветвые вглоофазвые првзмы (пз смесв петролейный эф|ф - бевзол, 1:1), т. пп. 140-141 0. Найдено, %: N3,08, 3,13; Ь7,66, 7,69: Qj. Ог9 Вычислено, %: N 3,53, S 8,О6. П р и м е р 6. 4-Этвлсульфамовпфталоввтрвл свитезвруют вз 4-этвпсульфа мовл-1,12-двбромбевзола прв мопярвом соотвошеввв дв омбевзола в , как опвсаво в йрвмере 1. Хроматографврованва ва свлвхагеле хлороформом выделяют до 15% смесв всходвого двбромпрспзводного в монобромзвмешвнкого ннтрвла, смесью хлороформсм - ацетон (4:1) 4-«тилстльфамонлфггалонвтрш с выходом 50%, бесцветные првамы, т. пп. 12О-121 С.
Найдено, %: N17,50, 17,
S 13,15, 13.21.
ОбНэНрг
Вычислено, %: Н 17,86; J 13,61. 4-Этипсупьфамош - 2-двбромбензоп ,, получают с выходом 90% вааимодействием Й78 г сульфохлорнда с 24,4 г солянокислого атиламина, тфедварительно обработанного водЕоым раствором едкого натра до рН 9. Бесцветные иглообразные призмы, т. Ш1. (нз петролейного э(|яфа).
Найдено, %: С 28,32, 28,13, И 2,86 ,79; Вг 46,О4, 46,33; S9,54. 9,52,
CeHgBi NOeS
Вычислено, %: С 27,99; И 2,62,
Вг 46,65; 59,33.
Тетра-4-алк1тсупьфамого1фтало1шанины получают ваанмодействием 4-алкилсульфамоипфталонитрипов с солями соответствук щюс металлов (с ааегилацетонатами или хлоридами меди, либо ванадкла) в нейтральнсял высококипяшвм органическом растворителе (например в трихлорбевзоле) в 1фисутствии катализаторов (для медных комплексов - молибдат аммоння ; для ванадильных метавандат аммония). Синте зированы медные и ванадильные комплексы тетра-4-аля;ил- :ульфамонл-фгалоциа-Г: нов.
Нагреванием соединений с изоамклатс натрия в изоамиповрм спирте в присутствии катализатора - мопибдата аммония, пой учены тетра-4-алкилсульфамоилфгалоцианины натрия, которые обработкой метанолом переводят в безметальные тетра-4 алкилсульфамоилфталоиианнны.
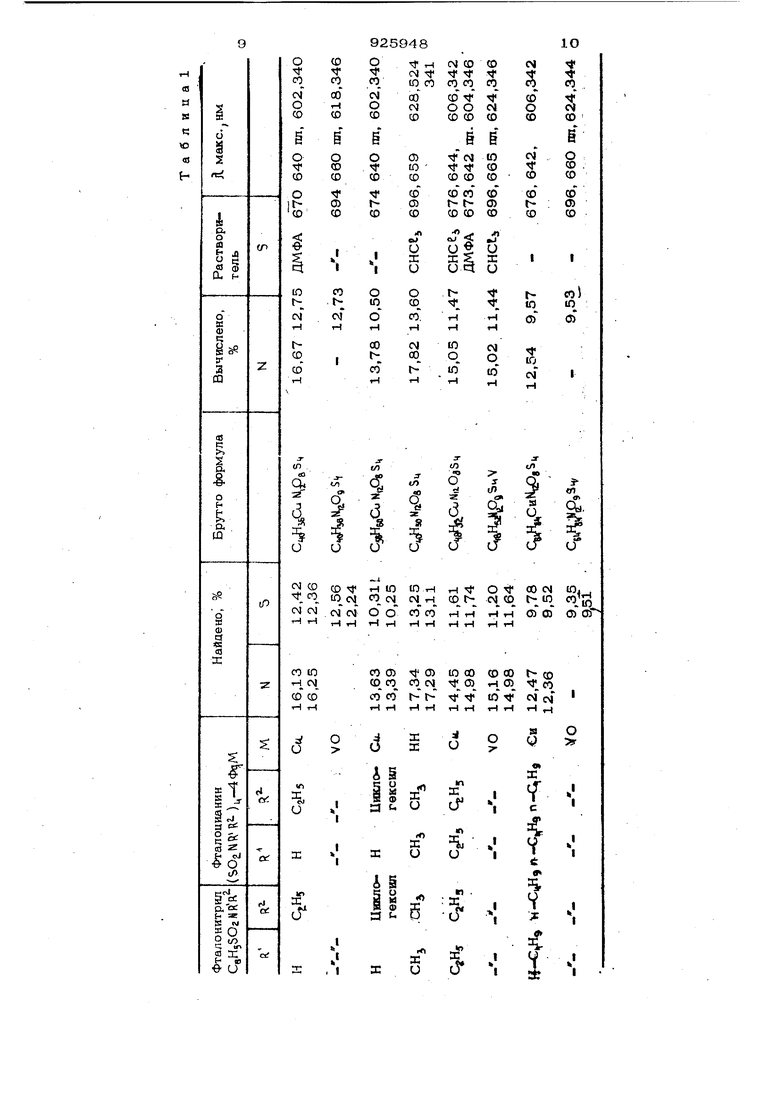
Характеристики полученных тетра-4алкилсульфамоилфгалогшанинов представлены в табл. 1 и 2.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных тетразола | 1982 |
|
SU1400507A3 |
| Способ получения производных пиридина или их солей | 1974 |
|
SU633475A3 |
| Способ получения производных пиридина | 1976 |
|
SU621317A3 |
| Способ получения производных тетразола или их фармакологически приемлемых кислотно-аддитивных солей | 1981 |
|
SU1212324A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЗАМЕЩЕННОЙ ФУЗАРИНОВОЙ КИСЛОТЫ | 1972 |
|
SU427512A3 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ ПЕРФТОРАЛ КИЛ СУЛЬФАМИДОВВСьООЮЗНАЯ|| | 1972 |
|
SU331545A1 |
| Способ получения карбостирильных производных | 1981 |
|
SU1169535A3 |
| Способ получения четвертичных аммониевых солей | 1972 |
|
SU467594A1 |
| 4-[4'-(4''-МЕТИЛФЕНИЛАЗО)ФЕНОКСИ]ФТАЛОНИТРИЛ | 2011 |
|
RU2459846C1 |
| Способ получения карбостирильных производных | 1982 |
|
SU1395140A3 |


Авторы
Даты
1982-05-07—Публикация
1980-03-10—Подача