то в 5- или 6-положении - Н, и соответствующего амида с вьщелением целе- вого продукта в свободном виде. Испытания показывают, что соединения I имеют низкую токсичность (LDjo
1000 мг), оказывают влияние на сердечный ритм при меньших побочных осложнениях, чем у известного (N- -метил-К-(2 -метш1циклогексил)-амино-- карбонилпропоксиЗ-карбостирила, 1 ил, 17 табл.
















| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения карбостирильных производных | 1981 |
|
SU1169535A3 |
| Способ получения карбостириловых производных (его вариант) | 1982 |
|
SU1779249A3 |
| Способ получения карбостирильных производных | 1981 |
|
SU1367857A3 |
| Способ получения производных карбостирила | 1982 |
|
SU1331426A3 |
| Способ получения карбостирильных производных | 1981 |
|
SU1232144A3 |
| Способ получения производных карбостирила или их фармакологически приемлемых кислотно-аддитивных или четвертичных солей | 1980 |
|
SU1091857A3 |
| Способ получения тетразолилалкоксикарбостирилов | 1979 |
|
SU1064868A3 |
| Способ получения карбостирильных производных или их фармацевтически приемлемых солей с кислотами | 1979 |
|
SU1140687A3 |
| Способ получения производных карбостирила | 1982 |
|
SU1356962A3 |
| Способ получения карбостирильных соединений или их фармацевтически приемлемых солей | 1984 |
|
SU1331430A3 |
Изобретение касается карбости- рильньос производных, в частности соединений общей формулы I СН(К)СН - С - CH--iiCR, II I - с - ш,-с(о) где К - -OA-C(0)-N R, - Н; R - низший алкил, или К; R j- низший алкил, НО - низший алкил, низшая алкокси - низшая алкильная, низшая алканоилокси-низшая алкильная или бензилокси-низшая алкильная группа; К - Cj-C,-циклоалкил, который может иметь одну, две или три ОН-группы в качестве заместителей; С,-С,о-цйкло- алкил-низший алкил, фенил, фенил-низший алкил, имеющий одну, две или три низшие алкоксигруппы в фенильном кольце; низший алкил, замещенньй 1, 2 или 3-мя ОН-группами, пирвдил или низший алкил, замещенный пиридином. фурилтетрагидрофурилом, 2Н-пиранилом, 4Н-пираншгом, 3,4-дигидро-2Н-пирани- лом, тетрагидропиранилом или тиени- лом; RJ, R и N, присоединенный к ним как С другим атомом j N, так и без него,могут образовать группу формулы -N-CH2-CH -BR,. при R. - фенил, С,-С,(, -циклоалкил или фенил-низший алкил; В-метин или N; А - насьш1енная С -С -алкиленовая группа или ненасьш5енная С -С -алки- леновая группа; (...) - углерод-углеродная связь между положениями 3 и 4-карбостирильной структуры и представляет собой (-) или () связь; группа ОА-СО находится в 5 или б-по ложении карбостирила при условии, когда RJ - низший алкил, то Н не должен быть С,С,,-циклоалкилом, замещенным 1, 2 или 3-мя ОН-группа- ми/С5-С,о -циклоалкил-низшим алкилом , фенилом, фенил-низшим алKI-UIOM, замещенным 1,2 или 3-мя алкоксигруппами в фениле, которые могут быть использованы Б медицине для предотвращения тромбоза и эмболии. Цель - получение более активных соединений указанного класса. Синтез соединений I ведут из соответствующего оксикарбостирильно- го производного общей формулы II СЕ (он)сн - С - сн CR СН / СН-- С - N-R,- С(0) СО со О1 о где R, указано вьше; R - 1 низший алкил или ОН, причем, когда ОН в 5- или 6-положении карбостирила, то Rj - Н или низший алкил, а когда R -.011,

Изобретение относится к способу получения новых карбостирильных производных, используемых для предотвращения тромбоза и эмболии.
Цель изобретения - синтез новых карбостирильных производных, обладающих ценными фармакологическими свойствами с менее выраженным побочным действием по сравнению со структурным аналогом.
Пример 1. В 50 мл диметил- формамида добавляют 1,73 г 6-оксикар- бостирола, 1,8 г и 0,5 г KI. Полученную смесь нагревают при 60 - при перемешивании, затем к этой смеси постепенно по каплям добавляют 3,2 г Ы-(2-оксиэтил) -К-(4-хлоробути- рил)циклогексиламина. После окончания добавления реакционную смесь перемешивают далее при той же самой температуре в течение 4 ч. Затем растворитель удаляют перегонкой, и полученный при этом остаток растворяют в 200 мл хлороформа, а слой хлороформа промывают разбавленной хлористоводородной кислотой, 1%-нь М водным раствором NaOH и водой в указанной последовательности, а затем сушат над безвЬдным сульфатом натрия. Осушающий агент удаляют фильтрованием, а маточньй раствор концентрируют, затем полученный остаток кристаллизуют из петролейного эфира. Полученньй таким образом остаток перекристалли- зовьшают из смеси хлороформ-петролей- ньй эфир до 0,5 г 6-{3- N- -(2-oкcиэтил)-N-циклoгeкcилaминoкap- бoнилЗпpoпoкcи кapбocтиpилa. Т. пл. 165-166°С.
По способу, аналогичному описанному в примере 1, получают соединения примеров 2-39.
Пример 2. (2-Окси- этил )-К-циклогексила минокарбонил про- покси -3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 139-141,.
Пример 3. 6-tЗ-LN-Meтил-N- -(3-пиpидилмeтил)aминoкapбoнилJпpo пoкcиjкapбocтиpил.
Бесцветные иглообразные кристаллы. 0 Т. пл. 69,5-171°С.
Пример 4. 6-{з- К-Этил-Н- - (3-пиридил) аминокарбонил |пропокси - карбостирил.
Бесцветные иглообразные кристаллы. 5 Т. пл. 148-149°С.
Пример 5. 6- 3- Н-Метш1-Н- -(2-тетрагидропиранилметил)аминокар- бонил пропокси -3,4-дигидрокарбости- рил.
0Бесцветные призмообразные кристаллы. Т. пл. 121,5-123,5°С.
Пример 6. 6-{3- К-Этил-И- c -(2-пиридил)аминокарбонил пропоксиТ - карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 123-125 С.
Пример 7. 6-р- И-Метил-Ы- -(2-тиeнилмeтил)aминoкapбoнил пpoпoк- cи карбостирил .
Бесцветные иглообразные кристаллы. Т. пл. 133,5-135 с.
Пример 8. 6-{3- N-MeTmi-N- 5 (2-3,4-дигидpo-2H-пиpaнилмeтил)aминo- , карбоншт пропокси карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 133,5-135°С.
Пример 9. | Н-Метил-К- 0 -(2-тетрагидропиранилметил)аминокар- бонил пропокси карбостирил.
Бесцветные гранулообразные кристаллы. Т. пл. 150-151,.
Пример 10, 6- 3- К-Этил-К- -(3-пиридилметил)аминокарбонил| про- покси карбостирил.
Бесцветные иглообразные кристаллы Т. пл. 145-147°С.
Пример 11.6- {З- Н-Метил-Н -(2-фурилметил)аминокарбонил пропок- си карбостирил.
Бесцветные иглообразные кристаллы Т. пл. 125,5-127 с.
Пример 12. 6- 3- К-метил- -М-(2-тетрагидрофурилметил)аминокар- бонил } пропокси} карбостирил.
Бесцветные иглообразные кристаллы Т. пл. 123-125°С.
Пример 13. (2-Окси- этил) -N-циклогексипаминокарбонил про покси}-3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы Т. пл. 130-131,З С.
Пример 14. 6- N-Этил-N-(3- пиридш1метил)аминокарбонш1метоксн2- -3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы Т. пл, 82-84°С.
Пример 15. б-{5- н-Метил-Ы -(2-тетрагидропиранилметил)аминокар- боннл пентилокси карбостирш1.
Бесцветные иглообразные кристаллы Т. пл. 81-83 с.
П JJ и м е р 16. 8- з- К-Мётил-Н- -(2-тетрагидропиранилметил)аминокар- бонил пропокси карбостирил.
Бесцветные иглообразные кристаллы Т. пл. П5,5-117 С.
Пример 17. (2-Окси- бутил)-К-циклогексиламинокарбонил} пропокси}-3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы Т. пл. 132-133°С.
Пример 18. 6-{з- N-(2-Qкcи- этил)-Ш-циклооктш1аминокарбонил |про- поксйЯ-3,4-дигидрокарбостирил.
Бесцветный кристаллический поро- шок. Т. пл. 104-107 С,
Пример 19. (2-;Окси пропил)-И-циклогексиламинокарбонил2- пропокси карбостирил.
Бесцветные иглообразные кристаллы Т. пл. 201-203 С.
Пример 20. 6- з-СН-(4-Окси- бутил)-N-циклог ексиламинокарбонил - пропокси карбостирил.
Бесцветный кристаллический- поро
шок. Т. пл. 153-155-С.
Пример 21. (2-Ок- сипропил)-Ы-циклогексиламинокарбонил бутокси}-3,4-дигидрокарбостирил.
Q
J5
20
25
зо
.
.
.
5°
5
Бесцветные иглообразные кристаллы. Т. пл. 120,5-122,5°С.
Пример 22. 6-{4- N-(2-6кси- этил)-К-циклогексиламинокарбонш1 бу- токси}-3,4-дигидрокарбостирил.
Бесцветный кристаллический порошок. Т. пл. 122-123,5°С.
Пример 23. 6-{4- N-(2-OKси- бутил ) -N-циклогексиламинокарбонил - бутоксиJ-3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 91-93°G.
Пример 24. 6-{4- N-(2,3- -Диоксипропил)-N-циклогексиламино карбонш | бутокси -3,4-дигидрокарбо- ртирил.
Бесцветные призмообразные кристаллы. Т. пл. 112,5-113,5 С.
Пример 25. 6-{4- К-(2-Окси- бутил )-К-циклопентиламинокарбоншГ)- бутокси}-3,4-дигидрокарбостирШ1.
Бесцветные иглообразные кристаллы. Т. пл. 102-103 С.
Пример 26. 6-{4- N-(2-OKCH- бутил)-К-циклогексиламинокарбонил - бутокси карбостирил.
Бесцветный кристаллический порошок. Т.Ш1. 127-128,.
Пример 27. 6-((2,3-Ди- оксипропил)-М-циклогексиламинокарбо- нил бутокси карбостирил.
Бесцветные иглообразные кристаллы Т. пл. 138-J40 C.
И р и м е р 28. 6-((2-Окси- бутил )-К-циклооктш1аминокарбонш1 бу- токси}карбостирил.
Бесцветный кристаллический поре-, шок. Т. пл. 86-89 С.
Пример 29. 6-f5- N-(2-OKCH- бутил)-К-циклргексиламинокарбонш1 пен- тилокси -3,4-дигидрокарбостирШ1.
Бесцветный кристаллический-порошок. Т. пл. 98-100 С. .
Пример 30. 7-{ 3- N-(3-OKCH- пропил)-К-циклогексиламинокарбоннл пропокси -3,4-дигидрокарбостирил.
Бесцветньй кристаллический порошок. Т. пл. 140-142 С.
Пример 31. 6-((2-Окси- этил)-1Т-циклогексиламинокарбон ил |бу- токси)карбостирил.
Бесцветные гранулообразные кристаллы, Т. пл. 134-135°С.
П р и м е р 32. 6- 4-СН-Этшг-Н- -(2- тетрагидропиранилметил)аминокар- бонил бутокси -З., 4-дигидрокарбостирил,
Бесцветные иглообразные кристаллы. Т.пл. 87-88,5°С.
Пример 33, 6- 4- К-Пропил- -N-(2-тетрагидропиранилметил)амино- карбонил бутокси -3,4-дигцдрокарбо- стирил.
Бесцветные иглообразные кристаллы. Т. пл. 77-79,5°С.
Пример 34, 6-{4- К-Бутш1- -N-(2-тетрагидропиранштметил)амино- карбонигГ бутокси -3,4-дигидрокарбости рил.
Бесцветные иглообразные кристаллы, Т. пл. 93,5-95,54.
П р .и м е р 35. 6-{з- Н-(2-Окси- этил)-N-(2-тетрагидропиранйлметил)- аминокарбонилЗпропокси карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 175,5-177°С.
Пример 36. 6-((2-Окси- этил )-N-(3-пирчцилметиламинокарбонш1 бутокси|-3,4-дйгидрокарбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 80-82,. Пример 37. (2-Оксиэтил)-N-(2-тетрагидропиранилметил)- аминокарбоншт бутокси -3,4-дигидро- карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 1 17-г,118,5 с.
Пример 38. 6-{4- N-(3-OKCH- пропил)-И-(2-тетрагидропиранилметил) аминокарбонил бутоксиТ-3,4-дигидро- карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 98,5-100°С.
:П р и м е р 39. 6-{4- к-(4-Ок- сибутил)-N(2-тетрагидропирашшме- i; тил}аминокарбонил бутокси 3,4-ди- гидрокарбостирил.
Бесцветные иглообразные кристал- лы. Т. пл. 114-116°С,
П р и м е р 40. К 50 мл диметил- формамида добавляют 1,9 г 1-бензил- -6- окси-3,4-дигидрокарбостирила, 1,8 г , и 0,5 г KI. Смесь нагре- вают при 60-70 с при перемешивании, затем к ней постепенно по каплям добавляют 3,4 г амида Ы-этил-Ы-(2- -тетрагидропиранилметил)-5-хлорпен- тановой кислоты. После окончания добавления реакционную смесь продолжают перемешивать при той же температуре еще в течение 4 ч. Растворитель удаляют перегонкой а полученный при этом остаток растворяют в 200 мл хлороформа, слой хлороформа промывают разбавленной хлористоводородной кислотой, 1%-ным водным раствором NaOH и водой в указанной последовательности, затем сушат над безводным сульфатом натрия. Осушающий агент удаляют фильтрованием и маточный раствор концентрируют, затем полученный при этом остаток обрабатывают на хроматографической колонке с си- ликагелем (в качестве растворителя используют смесь хлороформ:метанол 20:1 (объем/объем). В результате получают 0,6 г 1-бензил-6- 4- К-(2- -тетрагидропиранилметил)-М-этиламино- карбонил2бутокси -3,4-дигидрокарбо стирила в виде бесцветного сиропообразного вещества.
ИК-спектр поглощения 9 , 1620, 1690.
Вычислено, %: С 75,29; Н 8,23; N 6,06..
Найдено, %: С 75,41; Н 8,33; N 6,21.,
Пример 41. В 50 мл диметил- формамида добавляют 1,6 г 6-окси-3,4- -дигидрокарбостирила, 1 ,4 г .j и 0,5 г KI. Полученную смесь нагревают при 60-70 С при перемешивании, затем к ней постепенно по каплям добавляют 3,6 г N-(3-oкcипpoпил)-N-(5-xлopoвa- лерил)-К-циклогексилметиламина, После окончания добавления реакционную смесь продолжают перемешивать при той же самой температуре в течение 5 ч. Растворитель удаляют перегонкой, а полученный таким образом остаток экстрагируют 100 мл хлороформа и слой хлороформа промывают 1%-ным вод- нь1м раствором NaOH, разбавленной хлористоводородной кислотой и водой в указанной последовательности, затем сушат над безводным сульфатом натрия Осушающий агент удаляют фильтрованием, а маточный раствор концентрируют, затем полученный остаток обрабатьша- ют на хроматографической колонке с силикагелем (в качестве растворителя используют смесь хлороформ:метанол 40:1 (объем/объем). Полученный элю- ат концентрируют и.полученньй остаток перекристаллизовывают из смеси этилацетат - петролейный эфир до получения 1,1 г 6-{4- К-(циклогексил- метил-N-(3-оксипропил)аминокарбонилТ бутокси -3,4-дигидрокарбостир1ша в виде бесцветных иглообразных кристаллов. Т. пл. 95-97 С.
По способу, аналогичному описанному в примере 41, получают соединения примеров 42-62.
Пример А2. (2-оксн- этил)-Н-фенш1аминоклрбоннлметокси - карбостирил.
Бесцветный кристаллический порошок, Т. пл. 162-165°С.
Пример 43. 6-{з- И-(2-Ме- токсиэтил)-К-циклогексиламинокарбо- нил пррпокси карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 142,5-143,.
Пример 44, 6-{з- и-(2-Ок- си 1-метилпропил)-Ы-циклогексилме- тиламинокарбонил пропокси карбостирил.
Бесцветные иглообразные кристаллы, Т. пл. 179,5-181,5-0.
Пример 45, 6-{3- Н-(2-Ок си- этил)-й-бутиламинокарбонил пропокси - карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 153-1544.
Пример 46. 6-{3- Ы-ди-(2- -Оксиэтил)аминокарбонш1 пропокси)- карбостирил.
Бесцветные иглообразные кристаллы. Т, пл. 122-123,5 С.
Пример 47. (2-Окси- этил)-Ы-фенш1амииокарбонил бутокси - -3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т, пл. ПЗ-Пб с.
Пример 48о 6-{4- К-(2-Окси- этил).-И-бензиламинокарбонилЗбутокси - -3,4-дигидрокарбостирил.
Бесцветный кристаллический поро- . шок. Т. пл, 91,.
Пример 49. 6-{4- N-(2-OK- сиэтил)-N-циклогексилметилaминoкapбo- ншlЗбyтoкcи}-3,4-дигидpoкapбocтиpил.
Бесцветные пластинчатые кристаллы. Т, пл, 123-125 С.
Пример 50. 6-{4- К-(4-Окси- бутил)-К-циклогексилметиламинокарбо- нил бутокси)-3,4-дигидрокарбостирШ1.
Бесцветные иглообразные кристаллы. Т. пл. 119-120,.
Пример 51, 6-{4- Н-(2-Окси- б утил)-N-цикло г екс иламинок а рб токси -3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 123-125°С.
Пример 52. (5-Оксн- пентил)-Н-циклогексилметиламинокарбо- иил бутокси -3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т, пло 113,5-1154.
Пример 53. 6-{3- н-(4-Окси- бутил)-К-циклогексилметиламинокарбоыилJпpoпoкcи -3,4-ДI г щpoкapбocти - рил.
Бесцветные иглообразные кристаллы. Т. пл. 109-1 ГГС.
Пример 54. (5-npo- пионилоксипентил)-К-циклогексилметил- аминокарбонил бутокси -3,4-дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 60-62°С.
Пример 55. 6-{4- М-(2-Окси- этил)-и-(Я-3,4-диметоксифенэтил)ами- нокарбонил бутоксиЯкарбостирил. Бесцветные иглообразные кристаллы. Т. пл. 78-81°С.
Пример 56. (3-Аце- тш10ксипропил)-К-(2-тетрагидропиранилметил)-аминокарбонил бутокси -3,4- -дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 64,5-66,5°С.
Пример 57, (2,3-Ди- оксипрЬпил)-М-циклогексилметиламино- карбонш1 бутокси|-3,4-дигидрокарбостирил.
Бесцветный кристаллический порошок. Т. пл. 112-1 144.
Пример 58. 6-f4- N-(2,3-Диоксипропш1)-Н-циклогексилметиламинокарбонил бутокси карбостирил.
Бесцветньй кристаллический порошок, Т, пл. 125-128°С.
Пример 59. (2-Ок- сиэтил)-11-(3-оксициклогексш1)амино- карбонил пропокси карбостирил.
Бесцветньй кристаллический порошок. Т. пл. 220-224°С.
Пример 60. 4-{з- и-(2-Окси- этил)-Н-циклогексиламинокарбонил1- пропокси карбостиркп.
Бесцветные иглообразные кристал лы. Т. пл. 176-178°С.
Пример 61. 4-Метил-6- 3- - N-(2-оксиэтил)-N-циклoгeкcилaминo- кapбoнилЗлpoпoкcи кapбocтиpшI.
Бесцветные иглообразные кристаллы. Т. пл, 171-173°С.
Пример 62. 1-Этил-6- 4- Н- -(4-oкcибyтил)-N-циклoгeкcилмeтилaми- нокарбонил бутокси|-3,4-дигидрокарбостирил.
Бесцветное сиропообразное вещество, ИК-спектр поглощения , см : 1620, 1670.
Вычислено, %: С 73,26; И 9,56; N 6,33,
Найдено, %: С 73,42; Н 9,41; N 6,21.
ПримербЗ. КЮОмл изопро- панола добавляют 2,0 г 1-аллил-6-ок- си-3,4-дигидрокарбостирила и 1,8 мл ДБУ. Полученную смесь кипятят с обратным холодильником при перемешивании, а затем к ней добавляют 4,2. г 4-циклогвксил-1-Г-бромбутилпиперази- на. После окончания добавления реакционную смесь снова кипятят с обратным холодильником при перемешивании в течение 8 ч, затем концентрируют. Полученный при этом остаток экстра- гируют хлороформом и полученный слой хлороформа промывают 1 н.водным раствором NaOH и водой, затем сушат над безводным сульфатом натрия. Осушающий агент удаляют фильтрованием и маточный раствор, концентрируют. Полученный остаток обрабатывают на хро- матографической колонке с силикаге- лем (в качестве растворителя используют смесь хлороформ:метанол 20:1 (объем/объем). Получили 3,5 г 1-ал- лил-6- 3-(4-циклогексил-1-пиперази- нилкарбонил)пропокси |-3,4-дигидрокар- бостирила в виде бесцветного сиропообразного ведцества.
ИК-спектр поглощения ) , 1645, 1680.
Вычислено, %: С 71,04; Н 8,84; N9,56.
Найдено, %: С 70,95; Н 8,61; И 9,72.
Пример 64. ВЮОмл изопро- панола добавляют 1,6 г 6-окси-3,4-ди- гидрокарбостирила и 1,8 мл ДБУ. Полученную смесь кипятят с обратным хо- лодильником при перемешивании, а затем к ней добавляют 4,2 г 4-циклогек сил-1-J-бромбутилпиперазина После окончания добавления реакционную смесь продолжают кипятить с обратным холодильником при перемешивании в течение 8 ч, а затем концентрируют. Полученный остаток экстрагируют хлороформом и слой хлороформа промывают 1 н.водным раствором NaOH и водой, затем сушат над безводным сульфатом натрия. Осушающий агент удаляют фильтрованием и маточный раствор концентрируют. Полученный таким образом остаток обрабатывают на хроматографи ческон колонке (в качестве растворителя используют смесь хлороформ:метанол 20:1 (объем/объем). Получают 2,8 г 6-{3-(4-циклогексил-1-пиперази
5 0 5 0
Q 5 Q
5
5
нилкарбонил)-пропокси -3,4-дигидро- карбостирила в виде бесцветных иглообразных кристаллов. Т. пл. 133 - 1344.
По- способу, аналогичному описанному в примере 64, получают соединения примеров 65-70.
Пример 65. 6-{З- 4-Фенил- -1-пиперазинилкарбонил пропокси}- - -карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 202,5-203,5°С.
Пример 66. (4-Фенил-1- -пиперазинилкарбонил)пропокси -3,4- -дигидрокарбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 182,5-183,5 С.
Пример 67. (4-Фeнил-l- -пипepидш кapбoнил)пpoпoкcиJкapбocти- pил.
Бесцветные иглообразные кристаллы. Т.пл. I90-191 C.
Пример 68. (4-Бeнзил- -l-пипepaзинилкapбoнил)пpoпoкcиЗкap- бocтиpил.
Бесцветные призмообразные кристаллы. Т. пл. 174,5-175,5°С.
Пример 69. (4-Цикло гексил-1-пипepaзинилкapбoнил)пpoпoк- cи кapбocтиpил.
Бесцветные иглообразные кристаллы. Т. пл. 184,5-186,.
Пример 70. (4-Бензил- -1-пиперидилкарбонил)пропокси}карбостирил.
Бесцветные иглообразные кристаллы. Т. пл. 145-146°С.
Используя методику примера 1, получают соединения примеров 71-73.
Пример 71. 6-{4- N-(l-Me- тил-2-oкcипpoпил)-N-циклoгeкcилмeтил- аминокарбонил бутокси}-3,4-дигидро- карбостирил.
Т, пл. 95-98°G.
Пример 72. (4-Фенил- -1-пипера 3 инилк арбонил)-бутокси карбостирил.
Т. пл. 196,5-198°С.
Пример 73. (4-Фенш1-1- -пиперазинилкарбонил)-бутокси -3,4- -дигидрокарбостирил.
Т. пл. 188,5-190,5°С.
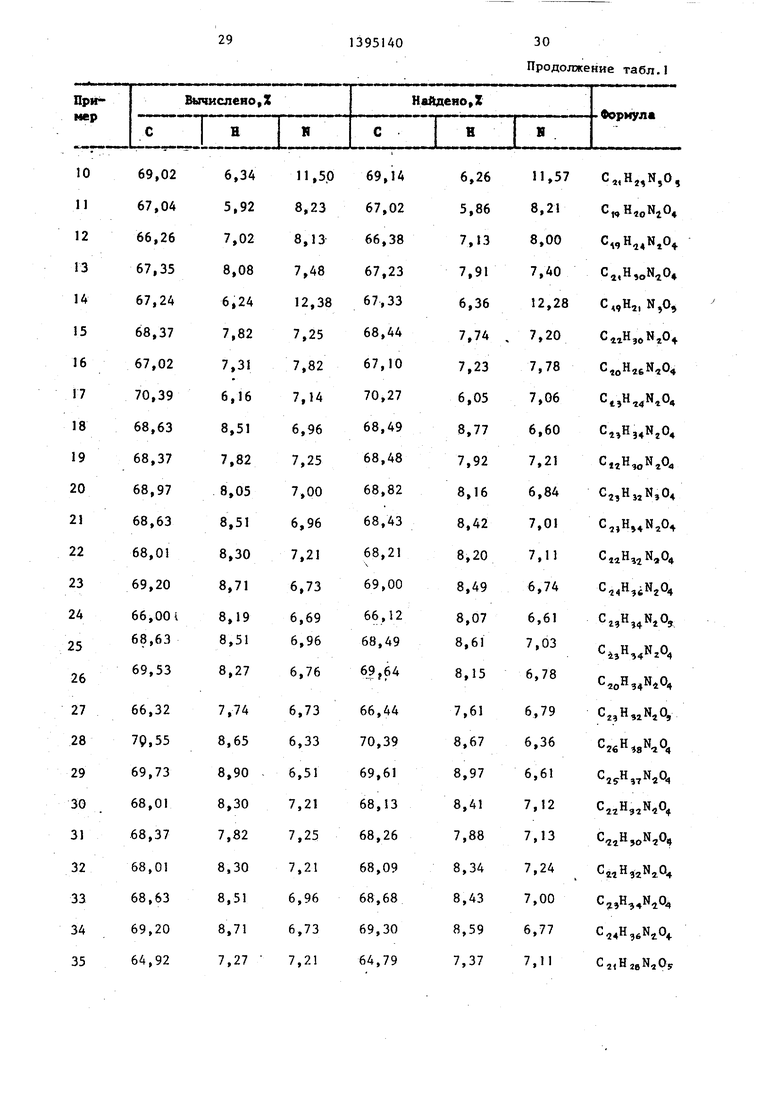
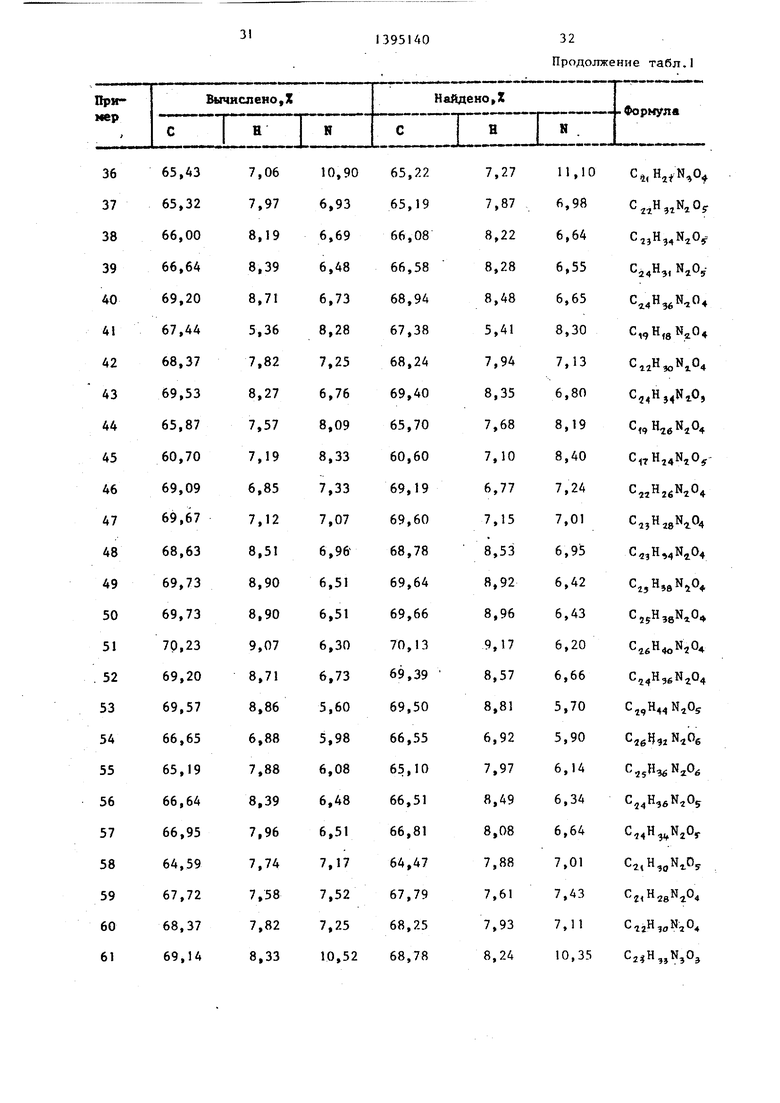
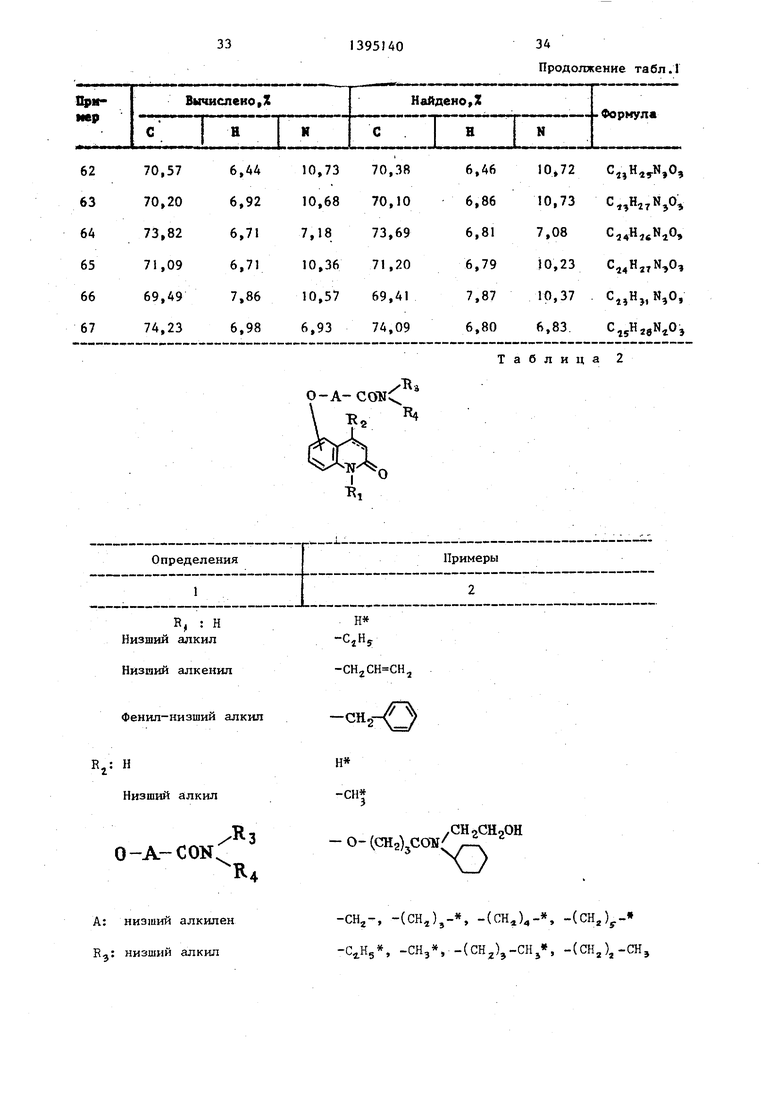
Данные элементного анализа приведены в табл. 1.
Далее приводятся результаты фармакологических тестов, проведенных для соединений предлагаемого изобретения .
i 1
Пример 74. В 50 мл диметил формамида вводят 1,73 г 6-оксикарбо- стирила, 1,8 г ,, затем смесь на гревают при 60-70 с с одновременным перемешиванием и постепенно по каплям вводят 3,8 г И-(2-оксиэтил)-Ы-(4 -метансульфонилбутирил)-циклогексил амина После завершения этого ввода реакционная смесь дополнительно перемешивалась при той же температуре в течение 4 ч. Затем растворитель удаляют путем выпаривания и полученный после выпаривания осадок растворяют в 200 мл хлороформа, хлороформ- ньй слой промывают разбавленной соляной кислотой, 1%-ным водным раствором NaOH и водой в указанном порядке Хлороформный слой сушат безводньм сульфатом натрия и высушивающее вещество удаляют путем фильтрации, маточный раствор концентрируют, образующийся остаточный продукт кристаллизуют из петролейного эфира. Полученные кристаллы перекристаллизовы- вают из смеси хлороформ - петролей- ный эфир и в результате получают 0,48 г 6-{3- Н-(2-оксиэтил)-К-цикло- гексиламинокарбонил пропокси карбо- стирила. Т, пл. 165-166 с.
Пример 75. В 50 мл диметил формамида вводят 1,9 г I-бензил-6- -окси-3,4-дигидрокарбостирш1а, 1,8 г KjCOg, затем смесь нагревают при 60-70°С,при одновременном перемешивании и после этого в нее по каплям вводят 4,95 г амида N-этил-N-(2-тeт- p,aгидpoпиpaнилмeтил)-5-пapa-тoлyoл- cyльфoнилпeнтaнoвoй кислоты. После прекращения операции этого ввода реакционную смесь дополнительно перемешивают при той же температуре в течение 4 ч. Затем растворитель удаляют путем отгонки и полученньй таким образом осадок растворяют в 200 мл хлороформа и хлороформный слой промьшают разбавленной соляной кислотой, 1%-ным раствором NaOH и водой в указанном порядке и затем сушат безводным сульфатом натрия. Высушивающее вещество удаляют путем фильтрации и маточный раствор концентрируют, полученный остаточный продукт концентрирования обрабатывают в хроматографической колонке с силикагелем (с использованием в качестве растворителя смеси хлороформ- метанол в объемном отношении (V/V) 20:1. Получают 51 г 1-бензил-6-{49514012
М-(2-тетрагидропиранилметил)-М-этил- аминокарбонил бутокси}-3,4-дигидро- карбостирила в форме бесцветного сн- ропообразного продукта.
ИК-спектр поглощения (бея примесей) 1620, 1690.
Вычислено, %: С 75,29; Н 8,23; N 6,06.
to Найдено, %: С 75,39; Н 3,35; N 6,19.
Пример 76. В 50 мл диметил- формамида вводят 1,6 г 6-гидрокси- -3,4-дигидрокарбостирила, 1,4 г ,.
tS Смесь нагревают при 60-70°С при одновременном перемешивании, затем в. нее медленно по каплям вводят 5,46 г И-(3-оксипропил)-К- 5-(4-метоксибен- зилсульфонил)валерил -К-циклогексил20 метиламина. После прекращения этого ввода реакционную смесь дополнительно перемешивают при той же температуре в течение 5 ч. Растворитель удаляют путем выпаривания и полученный та-
25 КИМ образом осадок экстрагируют
100 мл хлороформа, хлороформньй слой промывают 1%-ным водным раствором NaOH, разбавленной соляной кислотой и водой в указанном порядке, затем
30 сушат сульфатом натрия. Высушивающее вещество удаляют путем фильтрации и маточный раствор концентрируют, затем полученный в результате остаточный продукт обрабатывают в.хроматографи- 35 ческой колонке, наполненной силикагелем (с использованием в качестве растворителя смеси хлороформ:метанол, 40:1 (V/V). Элюент концентрируют и полученный остаточный продукт пере40 кристаллизовьшают из смеси этилаце- тат - петролейньй эфир, в результате получают 1,0 г 6-| 4- К-циклогексилме- тил-К-(3-оксипропил)аминокарбонил - бутокснЗ-3,4-дигидрокарбостирш1а в
45 форме бесцветных иглообразных кристаллов. Т. пл. 93-97°С.
Используя методику примера 1 получены соединения примеров 77-83. Пример 77. 6-{ 3- и-Цикло5Q гексил-N- (2-ацетилоксиэтил) аминокарбо- нил пропокси карбостирил, т. пл, 137- 139°С.
Пример 78. 6- 3- Н-Цикло- гексил-К-(2-бутирилоксиэтил)аминосг карбонил пропокси карбостирил, т. пл.
95,5-97 с.
Пример 79. 6- 3- Ш-Цикло- гексил-М-(2-изобутирилоксизтнл)амино131395140
карбонил пропокси карбостирил, т. пл. 107,5-109,.
Пример 80. 6-{A- N-(2,3- -Дигид роксипропил)-Н-циклооктиламино- карбонил бутокси}карбостирил, т. пл. 133-135°С, бесцветные гранулированные кристаллы (из этанол-диэтилового эфи- ра)..
П р и м е р ,81. (2,3-flH-jo гидроксипропил)-N-циклог ептиламино- ; карбонилТбутокси карбрстирил, т. пл. 129-131 С, порошкообразное вещество (из этанол-диэтилового эфира).
Пример 82. (2,3- .15 -Дигидроксипропил)-Ы-циклогептилме- тиламинокарбонилЗ бутокси}карбостирШ1, бесцветное аморфное твердое вещество,
114
Количество тромбоцитов в РРР определяют по известному методу и PRP разбавляют РРР для получения PRP-об- разца с концентрацией тромбоцитов 300000/мм для теста агрегации, вызванной аденозиндифосфатом (ADP). Приготавливают также образец РРР с концентрацией тромбоцитов 450000/мм для теста агрегации, вызванной коллагеном.
0,6 мл указанного образца PR добавляют в 0,01 мл раствора тестового соединения заранее определенной концентрации и полученную смесь помещают в термостат с температурой на 1 мин. Затем 0,07 мп ADP или коллагенового раствора добавляют к смеси. Определяют пропускание смеси
ЯМР-спектр (CDClj + D,,0); 1,
(17Н, m), 2,49 (2Н, широк,), 3,00 - 20 и изменение пропускания записывают,
4,10 (9Н, ju ), 6,72 (1Н, g, J
9,5 HZ), 6,98 (IH, g, J 2,5 HZ) ,
7,13 (IH, gg, J 9,0 HZ, 2,5 HZ),
7,39 (IH, g, J 9,0 HZ), 7,76 (IH,
используя агрегометр со скоростью перемешивания 1100 об/мин. В этом тесте используют буфер Auren Beronal (рН 7,35) для приготовления раствора g J HZ).25 fjyp или коллагена. Раствор ADP довоПример 83. 6-{3- К-(2-Гидр- дят до концентрации 7,5x10 М, а ра- оксиэтил)-и-циклогексиламинокарбонш1 - твор коллагена приготавливают, ра- -2-пропенилокси карбостирил, т. пл. стирая 100 мг коллагена с 5 мп ука- 204-207 С, бесцветные иглообразные . занного буфера. Надосадочную жидкость
30 используют в качестве индуктора. Ацетилсалициловую кислоту используют в качестве контроля для теста агрегации, вызванной ADP, и тесТа агрегации, вызванной коллагеном соответст- 35 венно. Ингибирующее агрегацию тромбоцитов действие определяют в единицах; процент ингибирования определяют по отношению к скорости агрегации контроля. Скорость агрегации рассчитывают
кристаллы.
В табл. 1 приведены данные элементного анализа соединений примеров , 1-68.
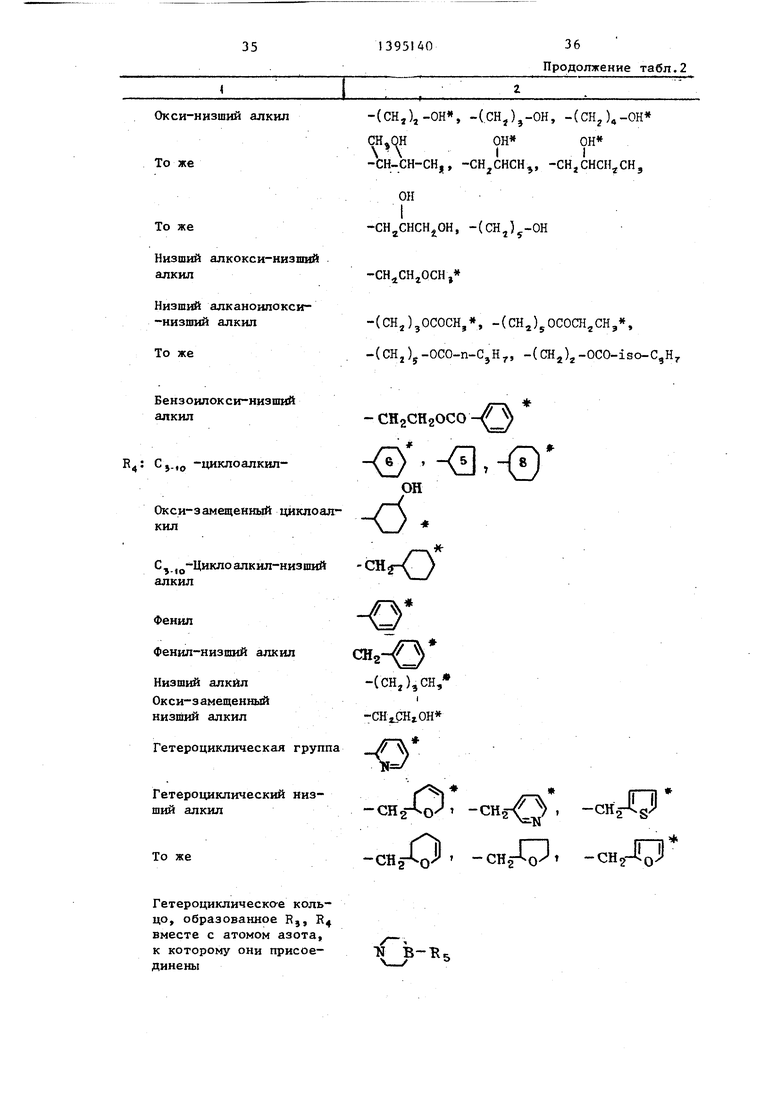
Зависимость между определениями заместителей и примерами, представленными в изобретении, показаны в табл. 2.
Соединения, содержащие заместители, обозначенные в табл. 2 звездочкой (), обладают фармакологическим дей- по формуле ствием.
Фармакологический тест 1.
Способность ингибировать агрегацию тромбоцитов определяют с помощью AG-11 агрегометра. Образец крови, 45 который используют для тестов, представляет собой смесь 1/9 (по объёму) цитрата натрия и полного образца .крови, собранной у кролика. Указанный
Скорость агрегации
с - а
Ъ - а
X 100,
где а - пропускание PRP;
Ъ - пропускание PRP, содержащего тестовое соединение или индуктор агрегации; с - пропускание РРР.
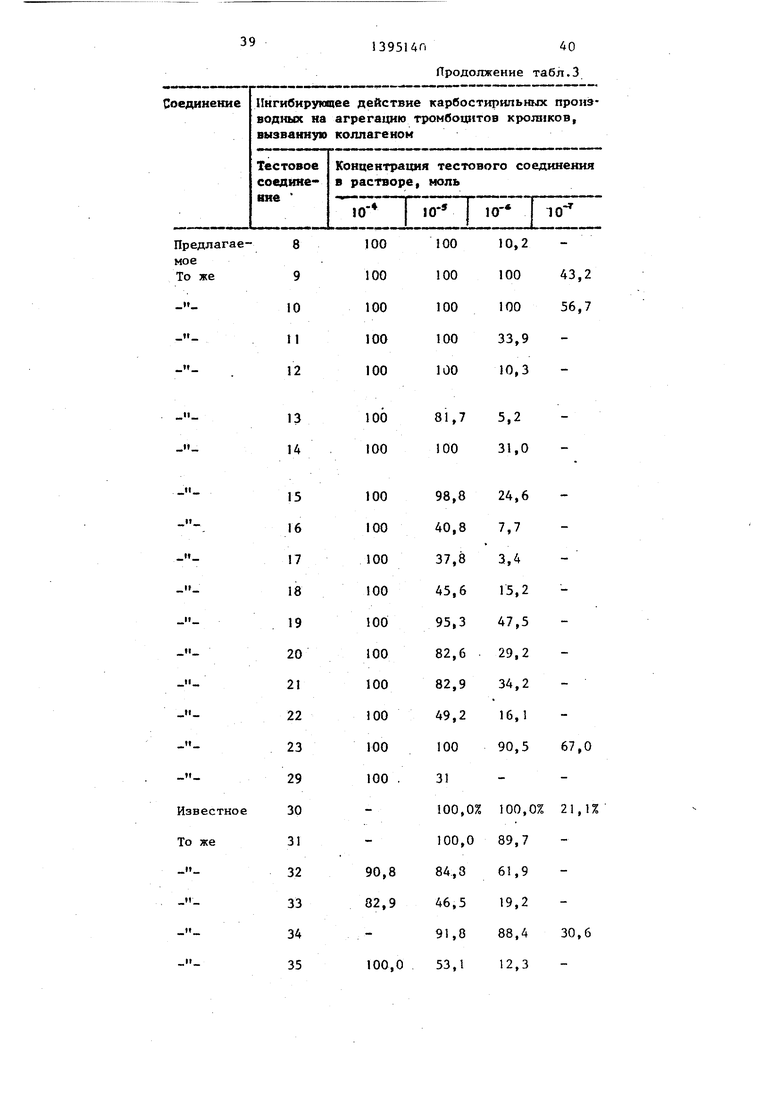
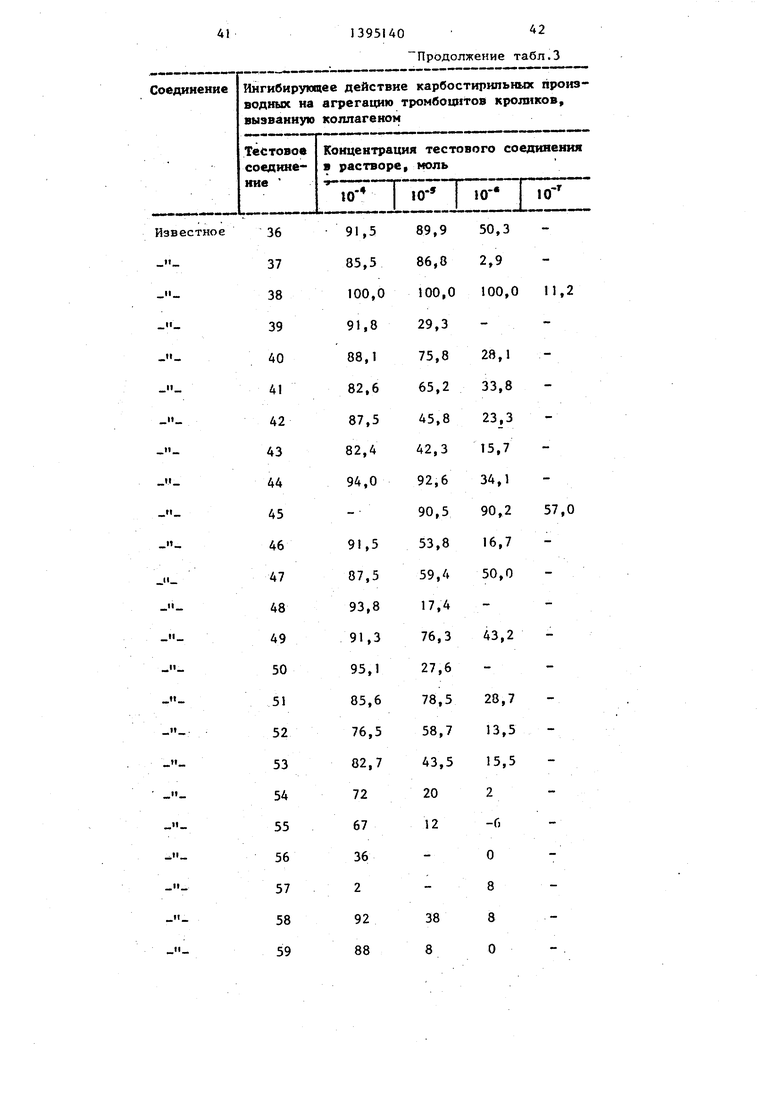
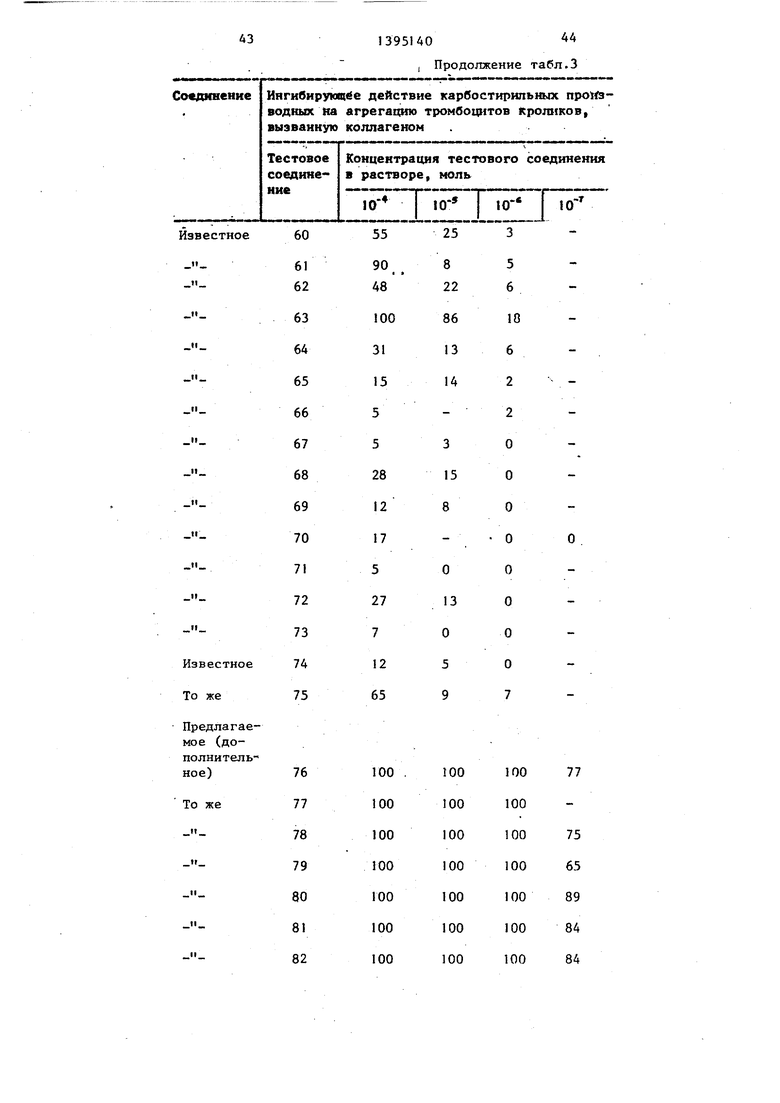
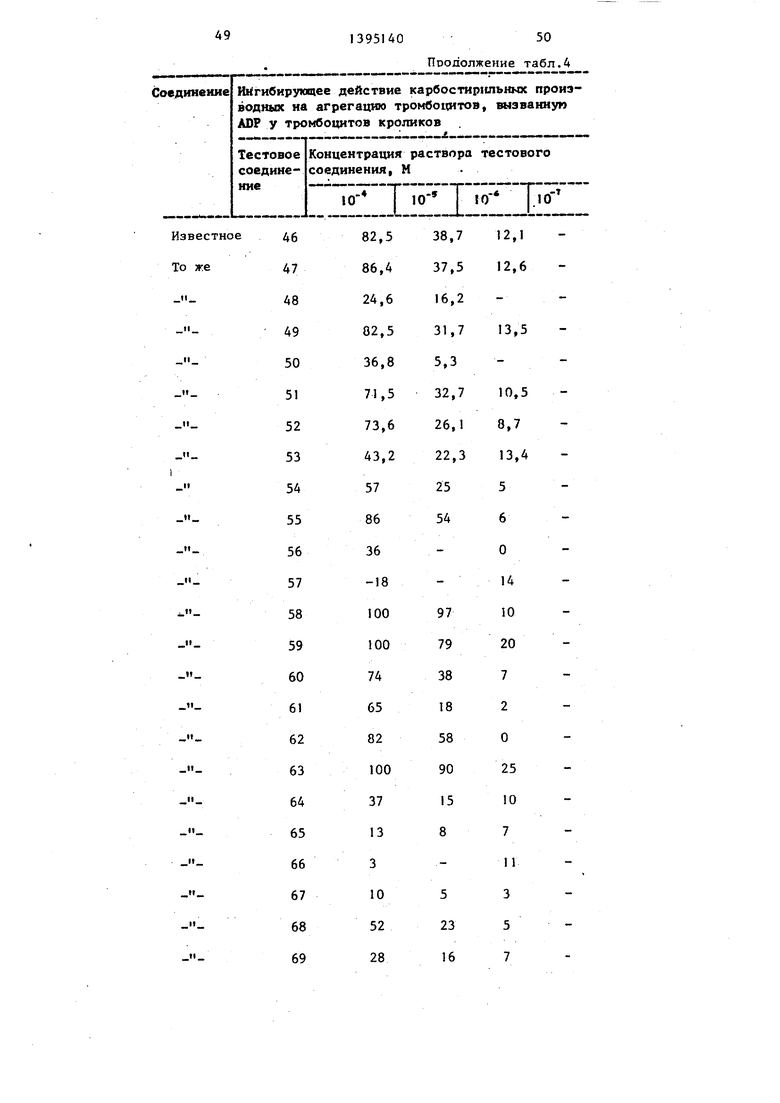
образец в течение 10 «ин центрифуги- Ингибирующее действие тестовых со- руют со.скоростью 1000 об/мин до по- 5° единении на агрегацию тромбоцитов лучения обогащенной тромбоцитами кролика, вызванную.коллагеном, пред плазмы (PRP). Полученньй таким образом PRP выделяют, а оставшийся образец крови подвергают дальнейшей об55
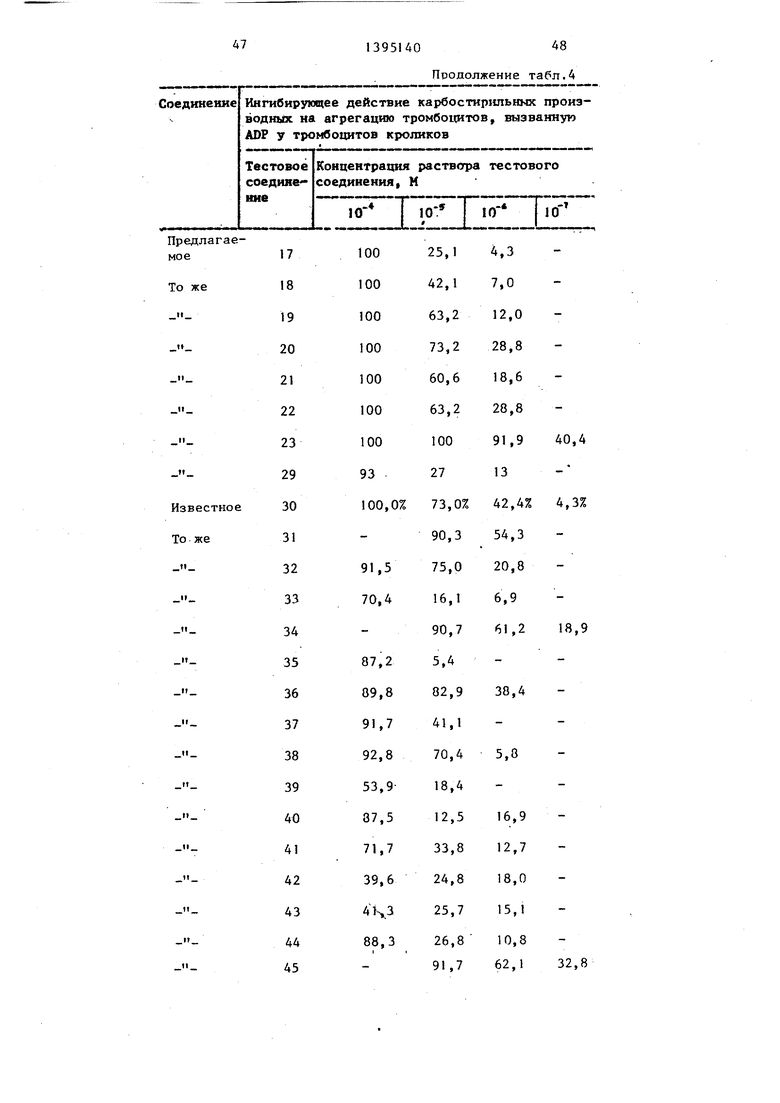
ставлено в табЛо 3, а аналогичное действие на агрегацию, вызванную ADP, представлено в табл. 4.
Тестовым испытаниям подвергались следующие тестовые соединения.
работке на центрифуге в течение 15 мин со скоростью 3000 об/мин для получения объединенной тромбоцитами плазмы (РРР).
114
Количество тромбоцитов в РРР определяют по известному методу и PRP разбавляют РРР для получения PRP-об- разца с концентрацией тромбоцитов 300000/мм для теста агрегации, вызванной аденозиндифосфатом (ADP). Приготавливают также образец РРР с концентрацией тромбоцитов 450000/мм для теста агрегации, вызванной коллагеном.
0,6 мл указанного образца PR добавляют в 0,01 мл раствора тестового соединения заранее определенной концентрации и полученную смесь помещают в термостат с температурой на 1 мин. Затем 0,07 мп ADP или коллагенового раствора добавляют к смеси. Определяют пропускание смеси
и изменение пропускания записывают,
Скорость агрегации
с - а
Ъ - а
X 100,
Ингибирующее действие тестовых со- единении на агрегацию тромбоцитов кролика, вызванную.коллагеном, пред
ставлено в табЛо 3, а аналогичное действие на агрегацию, вызванную ADP, представлено в табл. 4.
Тестовым испытаниям подвергались следующие тестовые соединения.
Соединения предлагаемого изобретения (1-29).
Т Т- -ч -
аминокарбонил пропокси карбостирил.токси|-3,4-дигидрокарбостирил.
бутокси карбостирил.
карбонилЗбутокси -3,4-дигидрокарбости- метоксифенилэтил) аминокарбонил пррпо- рил..,4-дигидрокарбостирил.
-К-циклогексиламинокарбонип пропокси - карбостирил.
Известные соединения-(сравнительные, 30-75).
., . . ,
метоксифенилэтил) аминокарбонил пррпо- ,4-дигидрокарбостирил.
-К-циклогексиламинокарбонип пропокси карбостирил.
Известные соединения-(сравнительные, 30-75).
42; (11-Циклогексиламинокарбо нил)пропокси карбостирил,
A3. (N-AшIил-N циклoгeкcил- aминoкapбoнип)пpoпoкcиJ-3,4-дигидpo- кapбocтиpил.
44; (Н-Метил-И-цИклогексил- аминокарбонил)пропокси -3,4-дигидро- карбостирил.
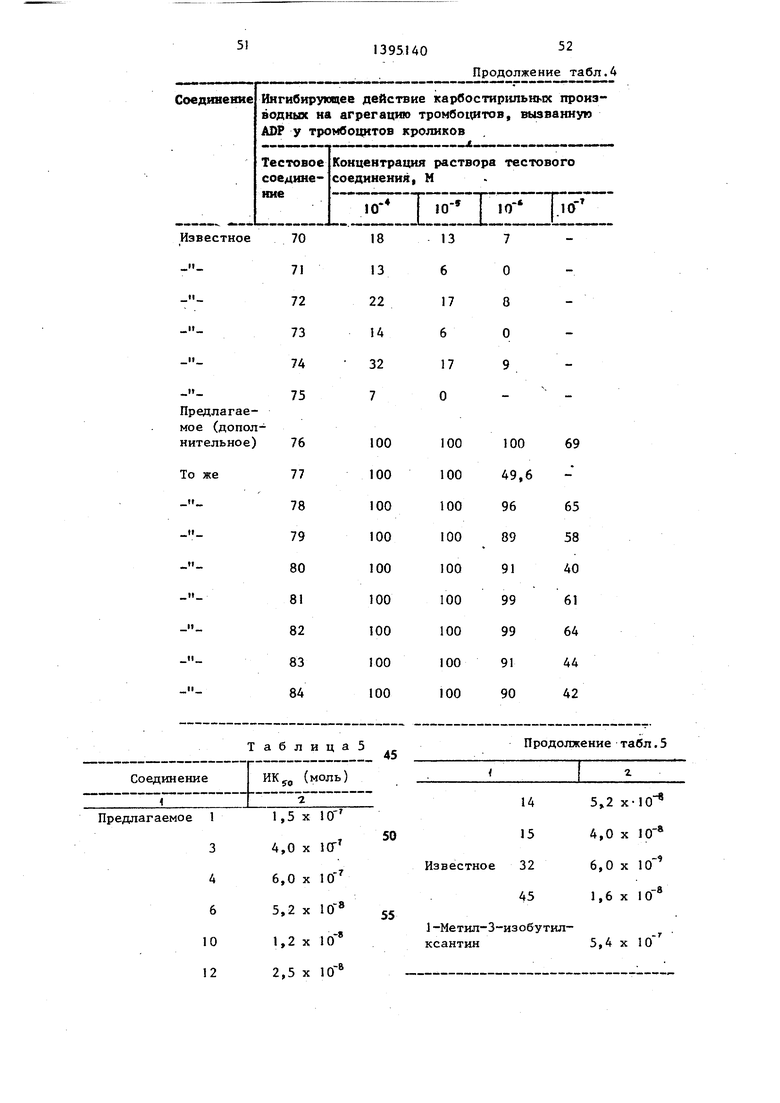
Деполнительные предлагаемые сееди- нения (76-84).
Фармакологический тест 2.
Противодействие против циклической AMP фосфодиэстеразы определяют по методу определения активности, т.е. для определения претиводействия против циклической AMP фосфодиэстеразы 10 мл раствора, полученного добавлением 1 мМ MgCl к 50 мМ буфера (трисхлористоводородная кислота, рН 7,4), добавляют к тромбоцитам, полученным при дальнейшем центрифугировании РРР кролика при 3000 об/мин в течение . 10 мин, и суспендированные тромбоциты измельчают в тефлоновом гомогенизаторе. После этого дважды замораживают препарат и дважды его оттаивают а затем измельчают 300 с ультразву- ком мощностью 200 Вт. После дополнительных 60 мин центрифугирования при 100000 G надосадочную жидкость собирают для использования в качестве неочищенного раствора фермента .
10 мл неочищенного буферного раствора вводят в колонку размером . 1,5x20 см, заполненную ДЕАЕ-целлюло- зой, которую предварительно буфери- руют 50 мМ трис-ацетатного буфера (рН 6,0), с последующей промьшкой и элюированием 30 мл 50 мМ трис-ацетат ным буфером, а затем этот буферный раствор обрабатывают линейным градиентом элюированием от О до 0,5 М бу фера ацетат-трис-ацетат (полное количество элюированное составило 30 мл). Скорость потока составляет 0,5 мл/мин, причем собирают фракции по 5 мл каждая. В результате этой , операции получают фракции с низкой активностью менее 2 н.моль/мл/мин с высокой (100 мкМ) концентрацией циклического AMP субстрата и все еще высокой активностью свьппе 100 р.моль /мл/мин при низкой (0,4 мкМ) концентрации циклического субстрата. Эту фракцию и используют как циклическую AMP фосфодиэстеразу.
0,1 мл водного раствора каждого тестового соединения определенной концентрации смешивают с 40 мМ буфера - трис-хлористоводородная кислота (рН 8,0), содержащего 50 мкг коровьего сывороточного альбумина и 4 мМ MgClj), содержащего заранее определенные 1,0 мкМ циклического AMP (три тиевый циклический АМР), и 0,2 мл этого смешанного раствора используют в качестве раствора субстрата.
0,2 мл ранее приготовленной циклической АМР фосфодиэстеразы заранее определенной концентрации добавляют к указанному раствору субстрата и полученную смесь подвергают реакции при 30 С в течение 20 мин, давая тритиевый 5 -АМР из тритий-циклического АМР.
5
0 5 О
Q д .
0
5
Затем реакционную систему погружают в кипящую воду на 2 мин для остановки реакции, а затем этот реакционный раствор охлаждают в ледяной воде и для превращения полученного тритий 5 -АМР в тритий-аденозин к раствору добавляют 0,05 мл (1 мг) змеиного яда в виде 5 -нуклеотидазы и реакцию ведут при 10 мин. Все количество реакционного раствора вводят в колонку с катионообменной смолой (AG 500 W X 4,200-400 мешей, изготовлена BiO-RaCl Со, размеры колонки: 0,5 X 1,5 см) и полученный тритий-аденозин один оставляют собираться, промывают 6 мл дистиллированной воды и злюируют 1,5 мл 3 н.аммиачной водой, К полному количеству элюата добавляют 10 мл тритон-толу- ольного типа сцинтиллятор и полученный тритий-аденозин определяют с помощью жидкого сцинтилляционного счетчика для определения активности фосфодиэстеразы.
Таким образом, определяют актива- ционное значение (Vg) фосфодиэстеразы тестового соединения соответству- кнцей концентрации и из этого актива- ционного значения (V) и контрольного значения (V), полученного для воды, в которой не содержалось никакого тестового соединения, определяют степень противодействия (%) из следу- клдей формулы:
Vf -Vs
Степень противодействия х
фосфодиэстеразе
ic 100.
Для контроля используют известный 1-метил-3-изобутилксантин.
Полученные результаты приведены в табл. 5.
Фармакологический тест 3.
Положительные инотропные эффекты новых карбостирильных производных настоящего изобретения определяют по известному способу.
Взрослых гибридных собак обоих . полов весом 8-12 кг анестезировали пентобарбиталом-Na в дозе ЗОчМГ/кг внутривенно. После следующего внутривенного введения гепарина натрия, 1000 мгк/кг, тестовых собак згмерщвля- ли, выпуская им кровь. Вырезали сердце собаки и немедленно помещали его в раствор Лока, затем вырезали
артериальную папиллярную мышцу вместе с интервентикулярной перегородкой. Септальную артерию тщательно из- извлекали, проходили полиэтиленовой канюлей и зашивали ниткой. Септаль- ные артерии (остальные, которые не были присоединены к артериальной папиллярной мышце) сшивали t нитками. Затем донорных гибридных собак весом 18-27 кг анестезировали пента- барбиталом-Na в дозе 30 мг/кг внутривенным введением и затем вводили внутривенно гепарин натрия (1000 мкг/кг). Перфузировали артери- альную папиллярную мышцу, канюлиро- ванную через септальную артерию полиэтиленовой канюлей с кровью, поступающей из каротидной артерии донорной собаки с помощью Peristarie насоса. Давление перфузии поддерживали постоянным 100 мм рт.ст-. Мышцу стимули- рорали электричеством с помощью электронного стимулятора через биполярные электроды в контакте с интер- вентикулярной перегородкой. Сила стимулирования была 2 X (минимальное значение, при котором проявлялось действие), с частотой 2 Гц, длительность пульсации 2 мс.
Количество протекающей крови в коронарной артерии определяли, изме- ряя кровяной поток, поступающий в септальную артерию с помощью электро- магнитного измерителя потока. Все данные записывали на самописце.
Раствор, содержащий тестовое соединение, вводили в септальную артерию через .резиновую трубку, соединен- кую с полиэтиленовой канюлей в количестве 10-30 мкл.
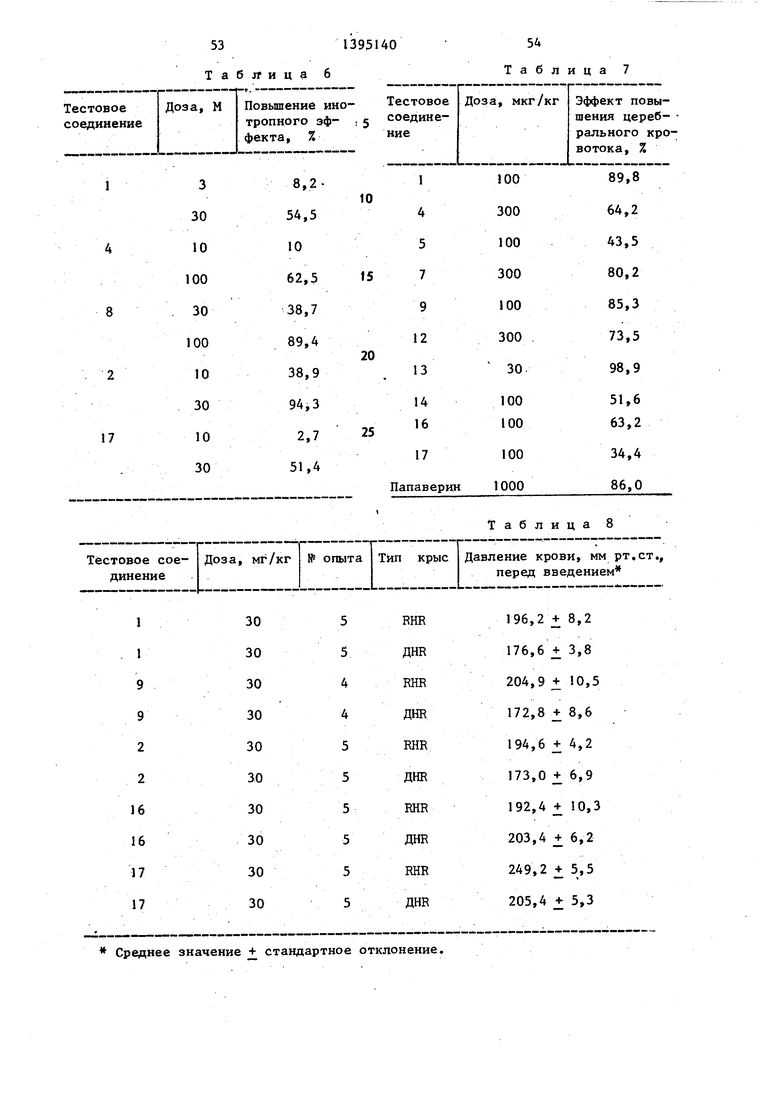
Полученные результаты приведены в табл. 6, где повышение (%) сокращений выражено как отношение количе- ства сокращений до и после введения (инъекции) раствора, содержащего тестовое соединение.
Фармакологический тест 4. Эффект повышения церебрального потока крови определяли по известному методу. Так, гибридную собаку (самца весом 12-20 кг) фиксировали в prone (положении) и анестезировали 20 мг/к пентобарбитала натрия и делали искусственное дыхание с частотой 20 раз/мин. Затем обнажали скулу и удаляли поверхностную кровь для того чтобы открыть венозньв с инус, исполь
д
с
0
зуя гриндер, и венозную кровь отбирали из канюлированной вены. Определяли скорость кроветока из вены, используя электромагнитный измеритель потока, и затем измеряли количество капель крови за 10 с, используя счетчик капель.
Эффект повьппения церебрального кровяного потока определяли, сравнивая число капель крови за 30 с в максимуме повышения, который наблюдался перед и после введения тестового соединения . Каждое соединение растворяли в диметилформамиде, разбавляли физиологическим раствором и вводили через канюлю, вставленную в profimola бедренную вену. В качестве сравнительного соединения использовали папаверин. Полученные результаты приведены в табл. 7.
Фармакологический тест 5.
Гипотензивное действие соединений измеряли, определяя максимальное кровяное давление тестовых животных по известному методу.
Использовали два типа тестовых животных.
1)Гипертензивные крысы (ШК). Взрослых крыс штамма Вистар весом
160-180 г анастезировали эфиром и левостороннюю ренальную артерию пережимали серебряным зажимом с внутренним диаметром 0,2 мм, тогда как правостороннюю ренальную артерию оставляли неоперированной. Спустя 4 недели после операции отбирали крыс с мак- симальньм кровяным давлением вьш1е 150 мм рт.ст. и тестовым животньи не давали пищи в течение ночи.
2)Деоксикортикостеронадетат (ДОКА). Физиологический раствор,Гипертензивные крысы (ДНЕ).
Самцов крыс штамма Вистар весом 150-170 г анестезировали эфиром и вылущивали левую почку. Спустя неделю после операции раз в неделю вводили подкожно 10 мг/кг ДОСА и в качестве питьевой воды давали 1%-ный водный раствор соли. Спустя 5 недель после операции крыс с максимальным кровяным давлением вьш1е 150 мм рт.ст. отбирали и использовали в качестве тестовых животных, которым ке давали пищи в течение ночи.
Каждое из тестируемых соединений вводили орально и кровяное давление измеряли перед введениями и 1, 2, 4,
6 и 8 ч спустя после введения. Полученные результаты приведены в табл. 8 Кровяное давление измеряли с помощью самописца.
Данные по кровяному давлению после введения приведены в табл. 9.
Фармакологический тест 6 (на острую токсичность).
Тестовые соединения вводили орально мышам и определяли Щ (мг/кг) для соединений. Полученные результаты приведены в табл. 10.
Фармакологический тест 7.
Методом, аналогичным фармакологи- ческому тесту 1 по оценке ингибирую- щего действия процесса агрегирования тромбоцитов крови кроликов, определи ли значения HKjj, (концентрация, обеспечивающая 50%-ное ингибирование процесса агрегирования) испытьшаемых соединений с использованием крови человека вместо крови кроликов.
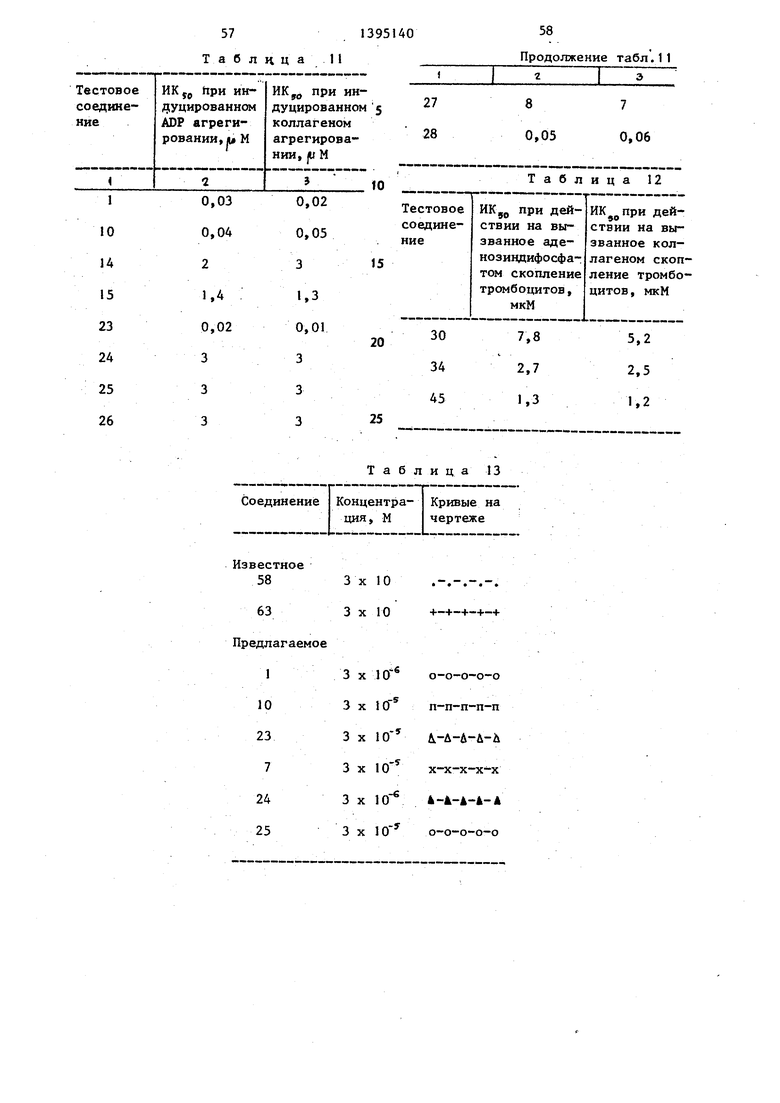
Полученные результаты представлены в табл. 11.
Данные по испытыванию некоторых известных соединений приведены в табл. 12.
Как видно из приведенных в табл. И и 12 данных, предлагаемые соеди- нения обладают более сильным ингиби- рующим действием на скопление тромбоцитов в крови человека, чем известные, оказывая при этом меньщее побочное действие на сердце.
Кроме того, предлагаемые соединения оказывают более длительное инги- бйрующее действие на скопление тромбоцитов по сравнению с соединения 58 и 63 (табл. 16).
Фармакологический тест 8.
Используя шприц, заполненньй вод- ньи раствором тринатрийцитрата (3,8%) отбирали образец крови из передней лапы гончей собаки (самец весом при- мерно 10 кг) в виде смеси 3,8%-водный раствор тринатрийцитрата - кровь в объемном отношении 1:9. Полученный таким путем образец в виде смеси крови с раствором тринатрийцитрата подвергался центрифугированию (200 г в течение 15 мин) и в результате получилась поверхностная жидкость, пред- ставлякщая собой обогащенную тромбоцитами плазму (PRP). Полученную PRP отделяли и оставшийся кровяной обра- зец подвергали дополнительному центрифугированию (100 г в течение Юмин) в результате чего получалась поверх-
с
Q
5 0
5
О
с
5
0
ностная жидкость, представляющая собой обедненную тр омбоцитами плазму (РРР). Подсчитывалось число тромбоцитов в PRP и РР{Р разбавлялся РРР таким образом, чтобы получался образец PRP, имеющий концентрацию тромбоцитов 500000/мкл.
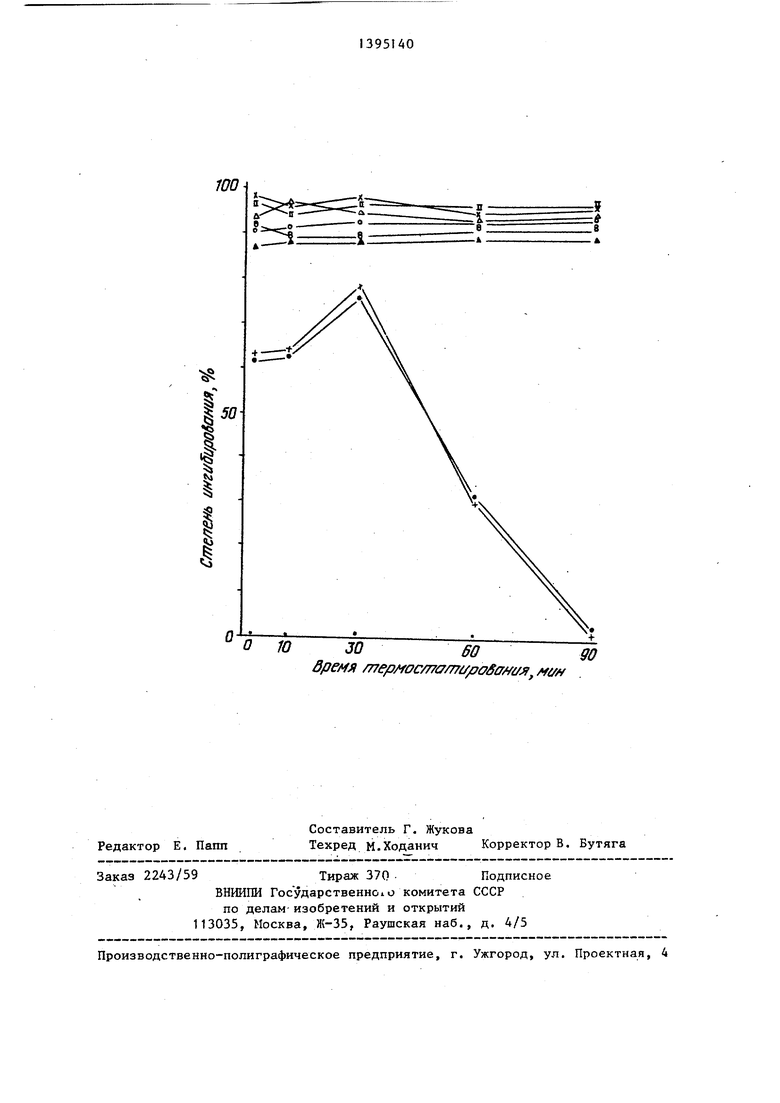
В образец PRP в количестве 3,6 мл вводили соответственно 0,4 мл водного раствора испытываемого соединения, имеющего предварительно заданную концентрацию, или 0,4 мл растворителя с тем, чтобы получить ряд испытываемых смесей. Соответствующие образцы испытываемой смеси термостатировали при комнатной температуре. После начала термостатирования из ряда испытательных смесей отбирали по 0,5мл каждой смеси с интервалами О, 5, 10, 30, 60 и 90 мин.
Затем определилось скопление тромбоцитов соответствукидих образцов смеси путем добавления аденозиндифосфа- та (АДФ) (конечная концентрация 7,5 М) как побудителя скопления тромбоцитов .
Определяли последовательные изменения ингибирующего действия соответствующих испытываемых соединений на скопление тромбоцитов путем сопоставления соответствующего по времени последовательного изменения скопления тромбоцитов с использованием контрольного образца.
Результаты показаны на чертеже и в табл. 13.
Как видно из чертежа,предлагаемые соединения обладают ингибирующим действием в течение более длительного периода времени по сравнению с известными.
Фармакологический тест 9.
Взрослых собак любого пола нечистой породы (помесей) весом 10-18 кг анестезировали пентобарбиталом натрия дозой 30 мг/кг путем внутривенной инъекции, и зти собаки неподвижно закреплялись в положении на спине. Дыхание собак осуществлялось в условиях дыхательного объема 20 мл/кг при скорости 18 пульсаций/мин с использованием респиратора. Кровяное давление собак замеряли от канюли, вставленной в левую сонную артерию, используя для этого измерения датчик давления. Частоту биения сердца измеряли посредством кардиотахометра.
реагирующего на пульсовые колебания кровяного давления.
Раствор испытываемого соединения вводился через канюлю, вставленную в правую бедренную вену. В ходе испытания для безопасности.собак, подвергнутых анестезированию, пентобарбитал натрия вводили дозой 4 мг/кг/час, и кроме того для предотвращения свер- тьшання крови вводился гепарин натрия дозой 100 ед/кг/ч,причем оба эти ввода осуществлялись внутривенно-путем вливания через подкожную вену.
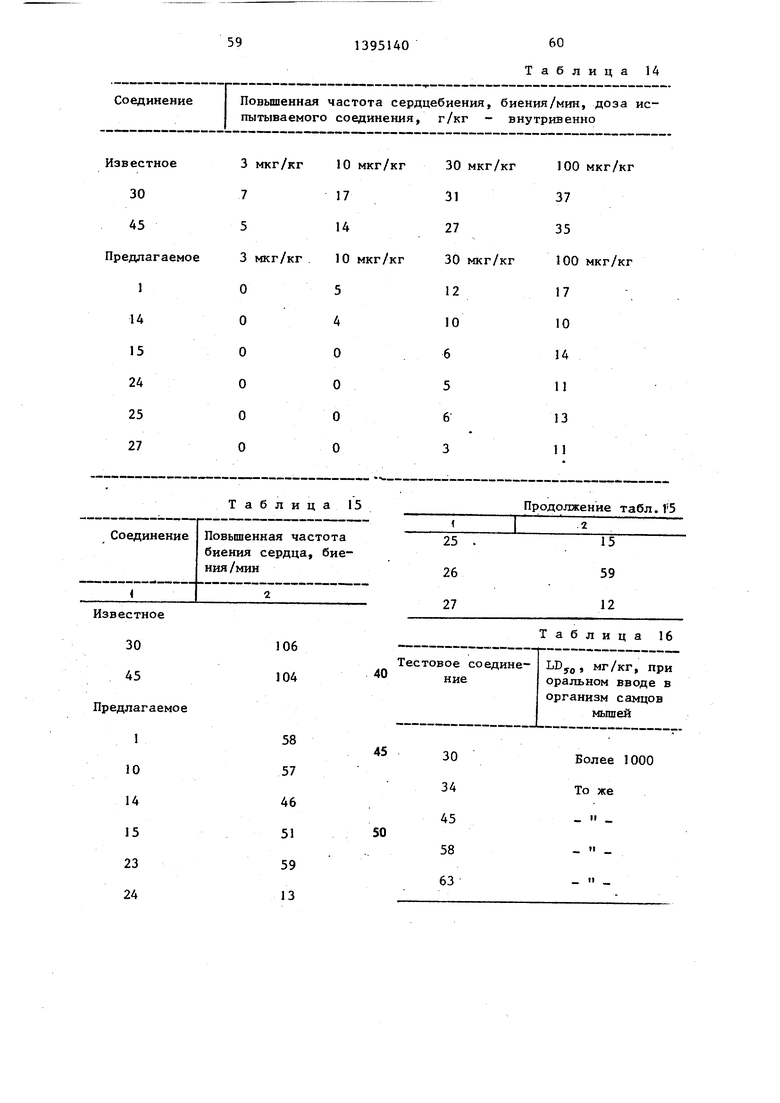
Испытываемое соединение вводилось в форме раствора диметилформамида. Концентрация этого раствора регулировалась таким образом, чтобы доза вводимого растворителя поддерживалась .менее 0,5 мл. Использовался хлоргид- рат.папаверина, разбавленный 0,9% физиологическим солевой раствором. До полнительно вводилось 3 мл 0,9%-ного .физиологического солевого раствора. Результаты представлены в табл. 14.
Фармакологический тест 10.
Крыс самцов вида Вистер весом 200- 280 г лишали пищи на 18-24 ч. Частоту биения сердца крысы рассчитывали с помощью электрокардиограммы, регистрируемой с помощью чернильного само писца, осуществляя наблюдения с 10-се кундными интервалами 3-6 раз.
После того, как частота биения сердца показывала постоянную величину, не превышающую 20 ударов/мин, испытываемое соединение вводили орально в форме суспензии, образуемой из раствора аравийской камеди. Через 30 мин после ввода замеряли частоту биения сердца и рассчитывали влияние вводимого соединения на повышенную частоту биения сердца. Доза введенных испытываемых соединений - 30 мг/кг, орально. Полученные результаты приведены в табл.15.
Как видно из табл. 14 и.. 15, предлагаемые соединения (1, 10, 14 15, 23, 24, 25, 26 и 27), оказывают меньшие побочные эффекты на частоту биения сердца по сравнению с известными соединениями.
Испытание на острую токсичность.
Проводили испытание на острую токсичность способом, аналогичным изве- стному и результаты представлены в табл. 16.
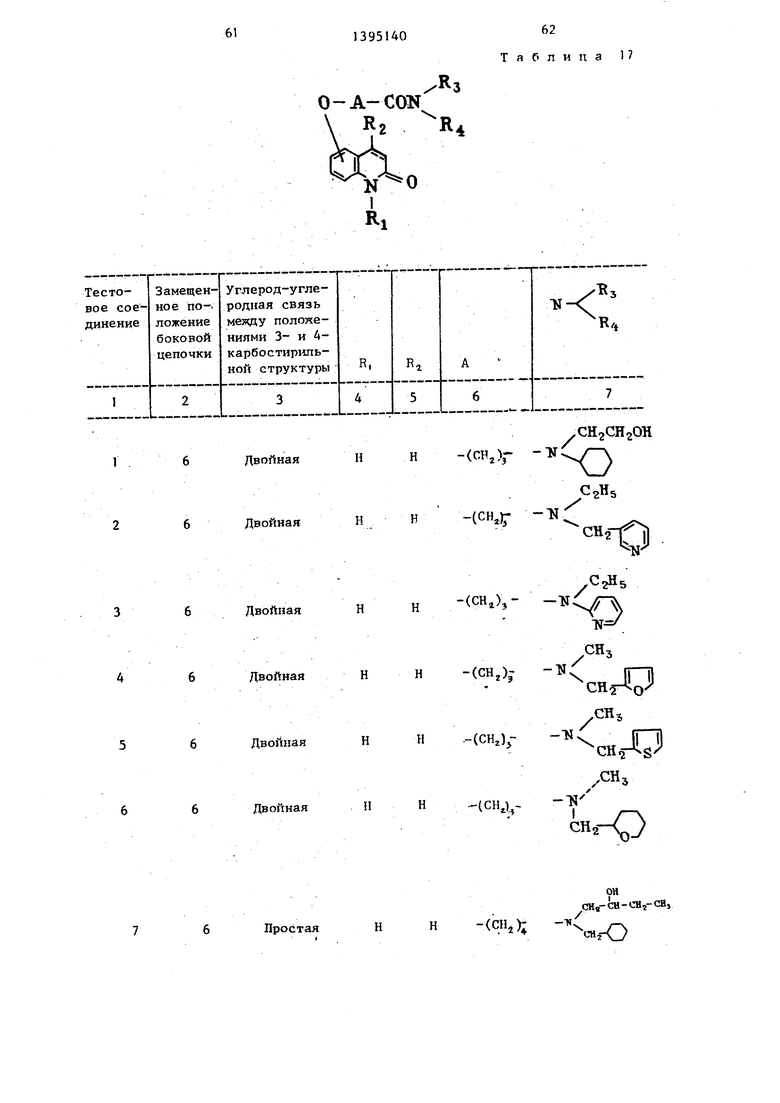
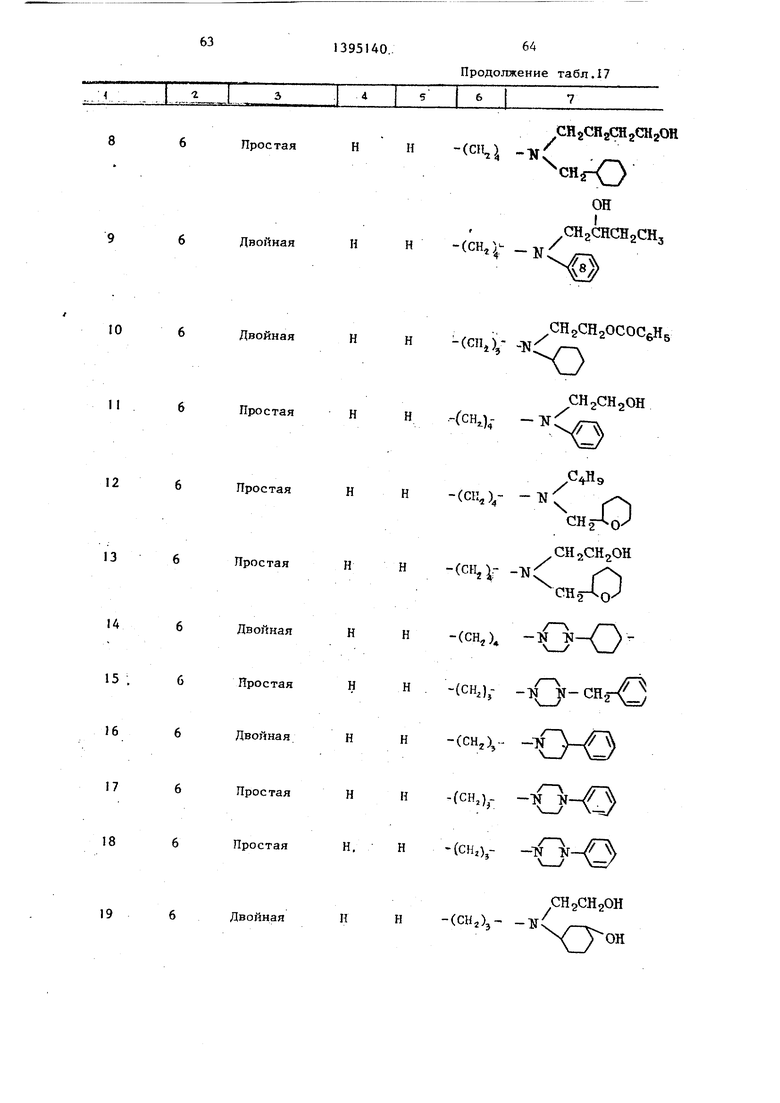
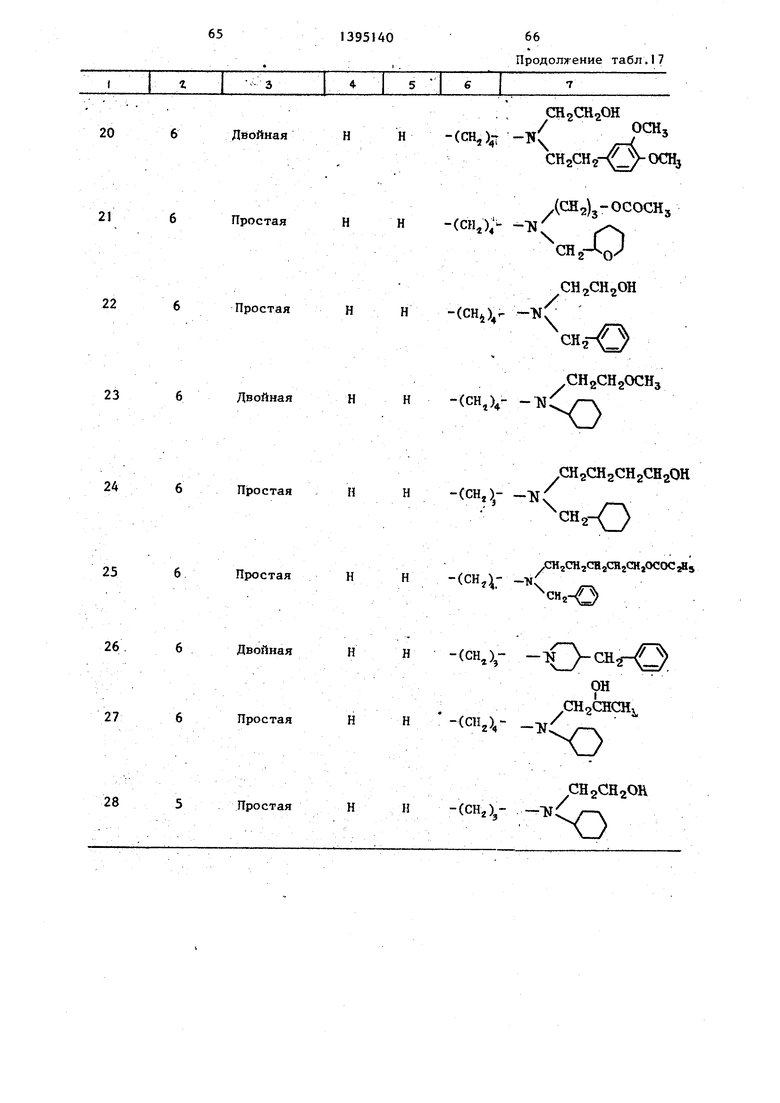
Характеристики испытываемых соё- Динени11 приведены в табл. 17.
Формула изобретения
Способ получения карбостирильных производных общей формулы
О-А- CON
-
15
20
25
где R, - водород;
водород, низшая алкильная
.В
R R. R.. группа или - О-А-CONС ;
R.4
низшая алкильная группа, гидрокси-низшая-алкильная группа, низшая алкокси - низшая-алкильная группа, низшая апканоилокси - 1тз- шая-алкильная группа или бензилокси - низшая-алкильная группа; С -С,о -циклоалкильная груп30 па, которая может-иметь одну, две
или три гидроксильные группы в качестве заместителей в циклоалкильном кольце, C.j-C,(,- циклоалкил-низшая- алкильная группа, фенильная группа,
35 фенил-низшая-алкильная группа, которая может иметь одну, две или три низшие алкоксигруппы в качестве заместителей в фенкльном кольце, низшая алкильная группа, которая может иметь,
40 одну, две или три гидроксильные группы.в качестве заместителей, пи- ридильная группа или низшая алкиль- Ная группа, имеющая один остаток ге- . тероциклического кольца в качестве
R
5
4азот, присоединенньй к ним либо с другим атомом азота, либо без него могут образовать группу формулы
где R 5-- фенильная группа, ,- циклоалкильная группа или фенил-низшая-алкильная группа;
В - метиновая группа или азот; А - насыщенная С,-Cg-алкиленовая группа или ненасыщенная С -С -алкиленовая группа, углерод - углеродная связь между положениями 3- и 4-кар- боксильной структуры и представляет собой одинарную или двойную связь; Q
замещенное положение боковой цепочки формулы -0-А-СО представляет собой любое из положений 5- или 6-кар бостирильной структуры при условии, когда R - низшая алкильная группа, J5 то R4 не может быть ни -хдакло- алкильной группой, содержащей в качестве заместителей одну, две или три гидроксильные группы в циклоалкильном кольце, ни ,о -циклоапкил-низшей- 20 -алкильной группой, феннльной группой, фенил-низшей-алкильной группой, содержащей в качестве заместителей одну, две или три алкоксигруппы в фе- нильном кольце, ни низшей алкильной группой, отличающийся тем, что оксикарбостирильное производное общей формулы
25
где RI и тип углерод-угдородной
связи между положениями 3- и 4-карбостирильной структуры указаны выше; R - водород, низшая алкильная группа или гидроксильная группа;
и замещенным положением гидроксиль- ной группы является любое положение 5- или 6-карбостирильной структуры при условии, когда гидроксильная группа замещена в положении 5- или 6-карбостирильной стрз ктуры, то R водород или низшая алкильная группа; и, наоборот, когда R - гидроксильная группа, то положения 5- и 6- в карбостирильной структуре замещены только водородом, но.не замещены гид- рокснльными группами, подвергают взаимодействию с алкан- амидным производным общей формулы
«3 Ял
где R , R и А указаны выше;
X - галоген, алкансульфонилок- сигруппа, арилсульфонилок- .сигруппа или аралкилсульфо29
1395140
30 Продолжение табл.1
33
О-А-СОКС
Н
-с,н,
-CHjCH CH.,
-сн
Н
Н
Низший алкил
-СИ
А-CON
X
R3
Кл
CHgCHoOH -0-((Ш2)
А: низший алкилен
низший алкил
, -(CHj,-, -(сн)-, -(сн,)- , -сНз, -(cH2),-CHj, -(сн,),-сн.
1395140
34
Продолжение табл.1
35
Окси-низший алкил
То же
То же
Низший алкокси-низший алкил
Низший алканоилокси- -низший алкил
То же
Бензоилокси-низший алкил
- CH2CH20CO-f3
уГ-Л /-
C,., -цикпоалкил- / M 4 J
OH
Окси-замещенный циклоал- /
-/
КИЛ
C, ,,-Циклоалкил-низший алкил
Фенил Фенил-низший алкил
Низший алкил Окси-замещенный низший алкил
Гетероциклическая групп
Гетероциклический низший алкил
То же
Гетероциклическо-е кольцо, образованное R,, R вместе с атомом азота, к которому они присоединены
1395140
36 Продолжение табл.2
-(СН,),-ОН, -(CHj),-OH, -(СЕ)-ОЕ
СН.ОНОН ОН
II
-CH-CH-CHj, -CH.jCHCH, -CHjCHCH CH,
он
t
, -(СН,)у-ОН -CH jCHjOCH,
-(CHj OCOCH,, -{CH4)50COCH,jCH,,,
-(CHj )5 -OCO-n-CjH, -(CHjj) -OCO-iso 2-O
-(CHj),CH, I
-CHjCHiOH «
Г
СйДо -СНо- 0
-СИ,-О
TJ B-RS
Продолжение табл.2
39
Соединение
Ингибирукжее действие карбостиркпьных производных на агрегацию тромбоцитов кроликов, вызванную коллагеном
Концентрация тестового соединения в растворе, ноль
,-
гае
ное
8
9
10
П
12
13 14
15 16 17 18 19 20 21 22 23 29 30 31 32 33 34 35
139514П40
Продолжение табл.3
10
г5
10
L-«
10
100 100 100 100 100
10,2
100
100
33,9
10,3
43,2 56,7
81,7 5,2 100 31,0
.
90,8 82,9
100,0
41
1395140 2
Продолжение табл.3
43
1395140
, Продолжение табл.3
45
1395140
Продолжение табл.3
Таблица 4
47
1395140А8
Продолжение табл.4
49
139514050
Поодолжение табл.4
51
1395140
52 Продолжение табл.4
531395140
Таблица 6
1
1
9
9
2
2
16 16 17 17
Среднее значение + стандартное отклонение.
Таблица 7
1аблица 8
55
139514056
Таблица 9
Максимальное кровяное давление, мм рт.ст., после введения, ч 1чI2ч4ч|6чj8ч
Разница (среднее значение стандартное отклонение) значения, измеренного перед введением за вычетом значения, измеренного после введения в указанные часы.
Таблица 10
Продолжение табл.Ю
Таблица
n
1395140
58 Продолжение табл.11
Таблица 13
59
Таблица 15
1395140
60 Таблица 14
Продолжение табл. 15
Двойная
Двойная
ДвойнаяНН-(CH.i),Двойная
Двойная
Двойная 1Н
Простая
Таблица 17
Н
Н
-(ср,)г -(
-и
-и
/
СНзСНгОН
хз
/
СоН
CHqQ
CgHs
-К
Н -(CHjb
сн.
СН
.СНв
Н-(CHJ cHjgi
.сн
(CH I --N СНг
/
он
,C3Ie-CH-CH,-CHj
);
СН
гО
63
Простая
Двойная
10
Двойная
II
Простая
12
Простая
НН
13
Простая
НН
14
Двойная
15
Простая
16
Двойная
17
Простая
18
Простая
Н,Н
19
Двойная
НН
Продолжение табл.I7
Н
Н
-(СИ,), --М
/
CH CHgCHgCHgOH
-(сн,), -К
сн
он
CHgCHCHgCH,
и чс,„,- .,„.
X
-Ген,),- -TfCT
CHgCHaOH
С4Н9
,,f
(cn,v - у
Н
Н
.X
СНзСНгОН
(%ir -TJ::
-CCH,X
НН
-(CHj- ,H H -(CH),-
к
Н
Н
-(CH,)- J--(
-(CH,),- -1П;г У
CH2CH20H
-(CH.),- -:tr(/xir «
65
1395140
20
ДвойнаяНН
21
ПростаяНН
22
ПростаяНН
23
ДвойнаяНН-(СН)-
24
П|ростаяНН
25
ПростаяНН
26
ДвойнаяНН- (СН
27
ПростаяНН
28
ПростаяНН-(CHj)- -U
66 Продолжение табл.I 7
-(СН,)7 -Tf
еНоСНоОн /оси,
СНаСН -СУоСНз
(СИ);- -7J
,(сн2),-оеосн.
сн
,-Q
-(CH,j)- -N
СНгСНгОН
гО
/
СНгСНгОСНз
43
сен,),- -
CHaCHgCHgCHaOH
СН
Ю
.CHaCHjCHjCHjCMjOCOCaHs
.
СИ,
-V- -Осн, он
CHgCHCHj
.- -т,/
/
СНгСНгОН
43
SO 90
время Л7ер ОС/77 7/771/ а( 
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Методы эксперимента в | |||
| органической химии | |||
| - М., 1968, с | |||
| Телефонная трансляция с катодными лампами | 1922 |
|
SU333A1 |
Авторы
Даты
1988-05-07—Публикация
1982-06-18—Подача