Изобретение относится к способу получения новых производных тетразо- ла общей формулы I
N-1 Т/ А-В-СОК2
К
RI - С ,-С -алкил, циклогексил, замещенный метоксигруппой, фенил, незамещенный или за- мещенный -алкилом; А - сера или С j -алкилентио- группа;
В - С .-алкилен;
2 С 4 -алкоксигруппа или группа общей формулы .
-N
хНз
R.
где R а и R 4 одинаковые или различ- :нь1е,водород, С . -алкил, С , -цикло- |алкнл, незамещенный, или замещенный гидроксилом, ацетилоксигруппой, меток |сигруппой, метилом или N,N-димeтил- аминогруппой, фенил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы: ами :носульфонил-М,Н-диметиламино, метил, галоген, метокси или нитро, циклогек- силметнл, фенил-С -С4.-алкил, в кото- jpoM фенил может быть замещен С -j- -ал ОКСНГруППОЙ, ОКСИЭТИЛ, ПИРИДШ1-2-ф урилметил, 2-тиенипметшт, или Rj и R вместе могут образовьшать с ато- Мом азота, с которым они связаны, гетероциклическую группу, такую как морфолнновая, пиперидиновая или пипе- разиновая, которая может быть замещена метилом или ацетилом, обладающих противоязвенной активностью в отношении дуоденальных и пептических язв.
Целью изобретения является разработка способа получения производных тетразола, обладающих улучшенными Противоязвенньши свойствами по сравнению со структурными аналогами - 1-фенш1-5-аминотетразолом, 2-(3-бром- фенил)-5-(2-карбамош1-этил)тетразо- лом, 2-(3-бромфенш1)- 5-(2-пиперидино- карбонш1этил)тетразолом.
Пример 1. Этил-Н-диклогек- сил-хлорацетамид (3 г) (0,016 моль)
0
5
0
5
5
0 5
о 5
и i-метил-5-меркапто-1,2,3,4-тетра- зол (1,8 г) (0,016 моль) растворяют в ацетоне (50 мл) и добавляют карбонат калия. Смесь нагревают с обратным холодильником в течение 3 ч и при пониженном давлении отгоняют ацетон. После добавления воды, остаток экстрагируют эфиром. Эфирный раствор промывают насыщенным водным раствором хлористого натрия и сушат над сульфатом магния. После отгона эфира, полученный в результате остаток перекристаллизовывают из смеси эфир-пет- ролейный эфир. Получают N-этил-N-цик- ;Логексил-2-(1-метил-1,2,3,4-тетра- зол-5-ил)тио-а цетамида (1,5 г), белые призмы, т. пл. 69-71 С,
Вычислено, %: С 50,85; Н 7,47; N 24,71;
C.jH.NjOS
Найдено, %: С 50,78; Н 7,57; N 24,75.
Пример 2, К раствору N-ме- тил-N-циклoгeкcил-4-xлopбyтиpaмид (6,6 г) (0,03 моль) в сухом бензоле (50 мл) добавляют 1-метил-5-меркаптЬ- -1,2,45-тетразол (3,6 г) (0,03 моль) карбонат калия (4,5 г) (0,033 моль) и йодистый натрий (0,2 г) (0,001 моль). Смесь нагревают с обратным холодильником в течение 5 ч и разбавляют бензолом. Реакционную смесь промьюа- ют водой, водным насыщенным раствором бикарбоната натрия, водным насыщенным раствором хлористого натрия и сушат над сульфатом натрия. После отгона бензола, полученный в результате остаток подвергают хроматографичес- кой очистке (Бакогель С-200), используя в качестве элюента смесь бензол- -хлороформ (4:1, об/об). Получают Н-метил-К-циклогексил-4-(1-метил- -1,2,3,4-тетразол-5-ш1)тио-бутирами- да (5 г), светло-желтая жидкость.
ЯМБ (с/ СС) млн.дол.: 1,00-2,00 (lOfl,, шир.); 1,8-2,70 (4Н, м); 2,73 (ЗН, с, J 6 Гц)| 3,28 (2Н, t, I 6 Гц); 3,85 (ЗН, с); 3,20-4,50 (1Н,м).
вычислено, %: С 62,50; Н 7,79; N 23,55.
Найдено, %: С 52,72; Н 7,85; N 23,61.
Пример 3. 1-Метил-5-меркапто- -t, 2,3,4-тетразол (1,6г) (0,014моль) гидроокись калия (0,9 г ) (0,016 моль) йодистый натрий (3,2 г) (0,021 моль) и З-морфолинокарбонилпропил хлорид (5,1 г) (0,027 моль) добавляют к этанолу (30 мл) и смесь перемешивают при 70-80 с в течение 4,5 ч. После з вершения реакции реакционную смесь переливают в водный насыщенный раствор хлористого натрия и осадившиеся кристаллы отделяют фильтрацией и промывают водой. Сырые кристаллы полученные таким образом перекристалли- зовывают из смеси эфир-петролейный эфир с образованием 5-(3-морфолино- -карбонилпропилтио)-1-метил-1,2,3,4- -тетразола (2,2) белые иглы, т. пл, TI-TB C.
Вьтислено,
С 44,27; Н 6,37;
N 25,81.
C,oHnO,N.
-1,2,3,4-тетразол-5-ил)тио-бутирамид бесцветные иглы (гексан-зтил,ацетат) т.пл. 119-120 С;
N-бyтил-4-(1-метил-1,2,3,4-тетра- зол-5-ил)тио-бутира дад, бесцветная
Найдено, %: С 44,10; Н 6,30; N 25,59.
Пример 4. 1-Метш1-5-меркап- 20 то-1,2, 3,4-тетразол (1,6 г) (0,014 моль) жидкость, Пд 16,5 1,5198; этилат натрия (1,4 г) (0,02 моль), N-(2-гидpoкcиэтшl)-4-(1-мeтил-1,2,3,4-тетразол-5-ил)тиЬбутирамид, бесцветная жидкость, пд 1,5350; 25
йодистый натрий (1,6 г) и N-цикло- гексил-3-хлорбутирамид (4,8 г) (0,024 моль) добавляют к этанолу (30 мл) и смесь нагревают с обратным холодильником в течение 6 ч. После завершения реакции реакционную смесь переливают в водный насыщенный раствор хлористого натрия. Осйдившиеся кристаллы отделяют фильтрацией и про- мьшают водой. Полученные таким образом сырые кристаллы перекристаллизо- вьшают из смеси гексан - -этилацетат с образованием Н-циклогексил-4-(1- -метил-1,2,3,4-тетразол-5-ил)тиобу- тирамида (2,1 г) бесцветные иглы, т.пл. 116,5-117,5°С.
Вычислено, %: С 50,86; Н-7,47; N 24,71 -,
.NjOS
Найдено, %: С 50,87; Н 7,36;
К-этил-К-бензил-4-(1-метил-1,2,3, 4-тетразол-5-ил)тио-бутирамид, бесцветная жидкость, п 1,5596;
М-бутил-Н-циклогексил-4-(1-метил- -1,2, 3, 4 -тетразол-5-ил)тио-бутирамид 30 бесцветная жидкость, п 1,5522; N,N-дибуТШ1-4-(1-метил-1,2,3,4- -тетразол-5-ил)тио-бутирамид бесцвет ная жидкость, Пц 1,5049;
К,М-дибензил-4-(1-метил-1,2,3,4- 22 -тетразол-5-ил)тио-бутирамид, бесцветная жидкость, пд 1,5773;
N,N-диизoпpoпшI-4-(1-ceтил-1,2,3, . -тетразол-5-Ш1)тио-бутирамид, бесцве ная жидкость, Птз 19,5 1,5111; 40N,N-дициклoгeкcип-4-(1-метил-1,2,
3,4-тетразол-5-ил)т.ио-бутирамид, бес цветные иглы (гексан) т.пл. 91-92°С; Н-бензил-Ы-третбутш1-4-(1-метил- -1,2,3,4 тетразол-5-ил)тио-бутирамид
3,4-тетразол-5-ил)т.ио-бутирамид, бесцветные иглы (гексан) т.пл. 91-92°С; Н-бензил-Ы-третбутш1-4-(1-метил- -1,2,3,4 тетразол-5-ил)тио-бутирамид,
. N 24,63.
Примеры 5-59, Согласно ме- . тодике описанной в примерах 1-4, по- 45 бесцветные иглы (гексан), т. пл. отучают следующие соединения:86,5-87,5 С;
Ы5К-диэтил-4-(1-метил-1,2,3,4-тет- N-циклoгeкcил-N-2-(3,4-диметоксифенил)-эти-(4-)1-метил-1,2,3,4-тетра- зол-5-ш1(тио)бутирамид, бесцветная
разол-5-ил)тиобутирамид, бесцветная жидкость Пр 1,5227; .
жидкость Пр 1,5470;
50
N-мeтил-N-(2-тиeнилмeтил)-4-(1- -метил-1,2,3,4-тетрааол-5-ил)тио-бу- тирамид, бесцветная жидкость, п
К-этил-Ы-циклогексил-4-(1-метил- -1,2,3, 4-тетразол-5- ил)тио-бутирамид, бесцветная жидкость, 1,5327;
N-этил-N-фeнил-4-(1-метил-1,2,3,4- -тетразол-5-ил)тио-бутирамид, свет- gg 1,5706; ло-желтая жидкость, п 1,5534; К-бензил-М- 2-(3,4-диметоксифенш1)(4-ацетил-1-пиперазинокар- -этил -4-(1-метш1-1., 2, 3,4-тeтpaзoл- бoнил)пpoпилтиo 3-1-метил-1,2, 3,4-тет- -5-ил)тио-бутирамид, бесцветная жид- разол,, белый кристаллический порошок, кость, п j, 1,5659;
(перекристаллизованный из смеси лиг- ронн - ацетон), т.пл. 90-9155 С;
N- 2-(3,4-диметоксифенил)-этил -4- -Г1-метил-1,2,3,4-тетразол-5-ш1 тио- -бутирамид, бесцветные хлопья (гек- сан-этилацетат), т.пл. 70,5-71,5 С;
Н-гексил-4-(1-метил-1,2,3,4-тетра- зол-5-илтио)бутирамид, бесцветные хлопья (перекристаллизация из смеси гексан-эфир), т.пл. 41-42 С;
N-циклooктил-4-(1-метил-1,2,3,4- -тетразол-3-ил)тиобутирамид, бесцветная жидкость, Пц 1,5323; N циклoдoдoцкaнил-4-(1-метип-1,2,3,4-тетразол-5-ил)тио-бутирамид, бесцветные иглы (гексан-зтил,ацетат), т.пл. 119-120 С;
N-бyтил-4-(1-метил-1,2,3,4-тетра- зол-5-ил)тио-бутира дад, бесцветная
жидкость, Пд 16,5 1,5198; N-(2-гидpoкcиэтшl)-4-(1-мeтил-1,2,3,4-тетразол-5-ил)тиЬбутирамид, бесцветная жидкость, пд 1,5350;
К-этил-К-бензил-4-(1-метил-1,2,3, 4-тетразол-5-ил)тио-бутирамид, бесцветная жидкость, п 1,5596;
М-бутил-Н-циклогексил-4-(1-метил- -1,2, 3, 4 -тетразол-5-ил)тио-бутирамид, бесцветная жидкость, п 1,5522; N,N-дибуТШ1-4-(1-метил-1,2,3,4- -тетразол-5-ил)тио-бутирамид бесцветная жидкость, Пц 1,5049;
К,М-дибензил-4-(1-метил-1,2,3,4- -тетразол-5-ил)тио-бутирамид, бесцветная жидкость, пд 1,5773;
N,N-диизoпpoпшI-4-(1-ceтил-1,2,3,4- -тетразол-5-Ш1)тио-бутирамид, бесцветная жидкость, Птз 19,5 1,5111; N,N-дициклoгeкcип-4-(1-метил-1,2,
3,4-тетразол-5-ил)т.ио-бутирамид, бесцветные иглы (гексан) т.пл. 91-92°С; Н-бензил-Ы-третбутш1-4-(1-метил- -1,2,3,4 тетразол-5-ил)тио-бутирамид,
бесцветные иглы (гексан), т. пл. 86,5-87,5 С;
50
жидкость Пр 1,5470;
N-мeтил-N-(2-тиeнилмeтил)-4-(1- -метил-1,2,3,4-тетрааол-5-ил)тио-бу- тирамид, бесцветная жидкость, п
1,5706; К-бензил-М- 2-(3,4-диметоксифенш1)Н,Н-дигексил-4-( 1-мет1-ш-1,2,3,4- -тетразол-5-ил)тио-бутирамид5 бесцветная жидкость, nlf 1,5011;
N-3THn-N-(2-)3,4-диметоксифенил- (-этил)-4-(1-метил-1,2, 3,,4-тетразол- 5-ил)тио-бутирамид, бесцветная жидкость, п р 1,5451;
Г1-третбутил-4-( 1-метш1-1,2,3,4- -тетразал-5 ил)тио-бутирамид, бесцветные хлопья (гексан-этил ацетат), т. пл.. 71-73°С;
N-э тнл-4- ( 1 -метил-1,2,3,4-тетра-, зол-5-ил)тио-бутиранид, бесцветная жэдкость, Пд 1,5319;
Ы-бензил-4-(1-метил-1,2,3,4-тет- разол-5-ил)тио бутирамвд, бесцветные иглы (гексан-этил ацетат), т, пл. 65-66°;
Ы-(2-метоксифенил)- 4-(1-метил-1, 2,- 3,4-тетразол-5-ил)тио-бутирамид, бесцветные иглы (гексан-этил ацетат), т, гш. 79,5-82 С;
N-3 тил-Ы-(2-пиридил)-4-(1-метил- -1,2,3,4-тетразол-5-ил)тио-бутирамид, бесцветная жидкость, nj, 1,5623;
N-зтил-N-(3-пиридил)-4-(1-метил- -1,2,3,4-тетразол-5-Ш1)тио-бутирамид, бесцветная жидкость, Пд 1,5618;
М-этил-К-циклопентил-4-(1-метил- -1,2, 3,4-тетразол-5-ил)тио-бутирамид, бесцветная жидкость, пП 1,5384;
М-зтил-Н-цнклогексилметил-4-(1- -метил-1,2,3,4-тетразол-5-ил)тио-бутирамид, бесцветная жидкость, п
11 С
1,5293;
М-изопропил-Н-циклогексил-4-(1-ме







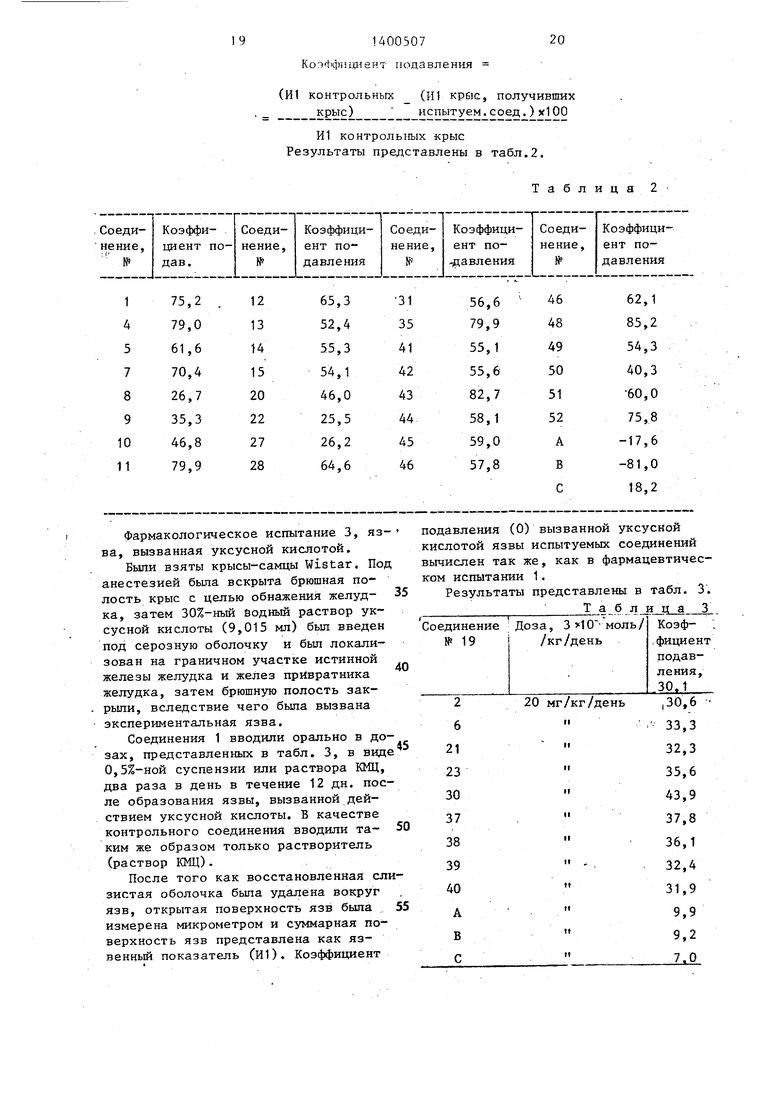

Изобретение касается производных тетра зол а, в частности соединений общей формулы I R-j-N-N N-N(;-A-B-COR j, где R - С -С -алкил, циклогексил, метоксициклогексил, феннл, С- -С -ал- килфенил; А - сера или С -Сз-алкилен- тиогруппа; В - С 1-С4-алкилен; R - С -С алкоксигруппа; Гк з,4 одинаковые или разньш, Н, кил; Cj-C -циклоалкил (он может быть замещен ОН, ацетилокси, метоксигруп- пой, СН ,,; Н,К-диметиламиногруппой}, фенил или его моно- или дизамещенкые Саминосульфонил; Ы,Ы-диметиламино, CHj;, галоген , CHjO, , циклогек--; силметил; фенил-С,-С -алкил фенил может быть замещен С ,-С -алкоксигруп пой, оксиэтил, пир5адил, 2-ф филме- тил; 2-тиенилметил, или вместе KRjR образуют гетероцикл-морфолин1-ш, пипе- ридинил, пиперазишш (он может быть замеп1;ен мет11лом или ацетилом) , которые обладают противоязвенной активностью. Цель изобретения - создание новых более активных веществ указанного класса. Их синтез ведут из соответствующего тетразола вместо группы A-B-COR-i имеется R,,-AH или ДХ, где А указано; Д - С ,-Сз-алкилен; X - галоген и алканкарбоновой кислоты ф-лы II Xg-B-COR где Х - галоген юти меркаптогруппа; В и R указаны, причем если R 3 АН, то X галоген, а если R3 то Хд меркаптогруппа. Процесс ведут в присутствии гидрогалогенирующего агента при (-30)-200 С в течение 1-30 ч, причем соединение ф-лы II ибпользуют либо в эквимольном, либо в 2-5-кратном избытке, если проводят синтез в среде растворителя либо в 5-10-кратном из- . бытке, если проводят реакцию без растворителя (этанол). Новые вещества проявляют активность против пептичес- кой и/или дуоденальной язвы без побочных влияний на центральную нервную cHCTehty, -а также обладают противовоспалительной активностью. 5 табл. § тЙИИВКЯ VssK 
М-гексил-М циклогексил--4-( 1-метил- 20 тил-1, 2,3, 4-тетразол-5-шт)тио-бутир-1,2,3,4-тетразол-5-ил)тио-бутирамид, бесцветная жидкость, п 1,5182|
N циклoгeкcшI-N-(2-гидpoкcиэтил)- -4-(1-метил-1,2,3,4-тетразол-5-1ш)- тио-бут1-фамвд5 бесцветная жидкость, 25 п д 1,5372|
Н-фенил-4(1-метил-1;, 2,, 3,4-тетра- ЗОЛ-5-Ш1)тио-бутирамид, бесцветные иглы (гексан-этил ацетата), т, пл. 106-107 С; 30
й-(2-пиридил)-4-(1-метил-1,2,3,4-- - -тетразол-5-ш1)тио-бутирамид, бесцветные иглы (гексан-этил ацетат)i т,пл 95-96°С;
амид, бесцветная жидкость, п1 1,5238;
М-этил-К-(4-гидроксициклогексил)- -4-(t-метил-1,2,3,4-тетразол-5-Ш1)- тйо-бутщзамид, бесцветная жидкость, 11 1,5363;
К-этил-Ы-(2-гидроксициклогексил)-. -4-(1-метил-1,2,3,4-тетразол-5-ил)- тио-бутирамид, бесцветные иглы (гек- сан)этил-ацетат, т. пл, 132-133°С;
К-этш1-Ы-(2-ацетш1оксициклогек- сил)-4-(1-метил-1,2,3,4-тетразол-5- -ил)тио-бутирамид, бесцветная жид-Ц
t,5218;
кость, Lig
Н-(3 пиридил)-4-(.1-метил-1,2,3,4- -тетразол-3-ил)тио-бутирамид, бесцветные пластины (этил ацетат), т.пл. 110,5-113°С;
л фурфур1ал-4- (1 -метил-1,2,3,4- -тетразол-5-ш1)тио-бутирамид, бесцветные хлопья (гексан-этил ацетат), т.пл. 71-73°С;
N-(4-аминосульфонилфенил)-4-(1-ме
35
40
N, Ы-дипр опш1-4-(1-метил- 1,2,3, 4- -тетразол-5-ил,) тио-бутирамид , бас- цветная жидкость, п д 1,5151;
N-бутил-N -фенил-4- (1 -метил-1,2, 3, 4-тетразол-5-Ш1)тио-бутирамид, бесцветная жидкость, п р 1,5509;
Ы,М-диметил-4-(1-метил-1,2,3,4- -тетразол-5-Ш1)тио-бутирамид, бесцветная жидкость-,. п« 1,5327; ; К-этш1-К-циклооктил-4- (1 -метилтил-.1,2,3,4-тетразОл-5-ил)тио-бутир- ,г -1, 2, 3,4-тетразол-5-ил)тио-бутирамид,
амид, бесцветные иглы (метанол), т.пл. 169,5-170,5°С|
N-(4-)-N,N-димeтшIaминo(фенил)-4- (1-метил-1,2,3,4-тетразол-5-ил)тйо- -бутирамид, бесцветные призмы (гек- сан-этил-ацетат) т,Ш1, 144-147 С;
N- (2-мет -ш-3-хлорфенил) -4- (1 -ме- ТШ1-1,2,3, 4- тетразол-5-ил) тио-бутир- амид, бесцветные иглы (гексан-этил ацетат);
Ы-(4-нитрофенил)-4-(1-метш1-1,2, 3,4-тетразод-5-ил)тио-бутирамид, бесцветные иглы (этил ацетат), т. пл. 194-195°С;
50
55
бесцветная жидкость, Пл 1,5309;
(4-метш1пиперазинокарбонил)- пропш1-тио-1-метил-1,2,3,4-тетразол, бесцветные гранулы (гексан-этил ацетат), т. пл. 65-68°С;
5-(З-пиперидинокарбонилпропилтио)- -1-метил-1,2.3,4-тетразол, бесцветная жидкость, Пд 1,5310;
Н-этип-К-циклогексил-З-(1-метил- .-1,2,3, 4-тетразол-5-ил)тио-пропион- амид,, светло-желтая жидкость, ni 1,5273;
М-этиЛ-К-циклогексил-5-(1-метил- -15 2,, 3, 4-тетразол-5-ил)тио-валерамид,
0 тил-1, 2,3, 4-тетразол-5-шт)тио-бутир5
0
-
амид, бесцветная жидкость, п1 1,5238;
М-этил-К-(4-гидроксициклогексил)- -4-(t-метил-1,2,3,4-тетразол-5-Ш1)- тйо-бутщзамид, бесцветная жидкость, 11 1,5363;
К-этил-Ы-(2-гидроксициклогексил)-. -4-(1-метил-1,2,3,4-тетразол-5-ил)- тио-бутирамид, бесцветные иглы (гек- сан)этил-ацетат, т. пл, 132-133°С;
К-этш1-Ы-(2-ацетш1оксициклогек- сил)-4-(1-метил-1,2,3,4-тетразол-5- -ил)тио-бутирамид, бесцветная жид-Ц
t,5218;
5
0
кость, Lig
N, Ы-дипр опш1-4-(1-метил- 1,2,3, 4- -тетразол-5-ил,) тио-бутирамид , бас- цветная жидкость, п д 1,5151;
N-бутил-N -фенил-4- (1 -метил-1,2, 3, 4-тетразол-5-Ш1)тио-бутирамид, бесцветная жидкость, п р 1,5509;
Ы,М-диметил-4-(1-метил-1,2,3,4- -тетразол-5-Ш1)тио-бутирамид, бесцветная жидкость-,. п« 1,5327; ; К-этш1-К-циклооктил-4- (1 -метил -1, 2, 3,4-тетразол-5-ил)тио-бутирамид,
бесцветная жидкость, Пл 1,5309;
(4-метш1пиперазинокарбонил)- пропш1-тио-1-метил-1,2,3,4-тетразол, бесцветные гранулы (гексан-этил ацетат), т. пл. 65-68°С;
5-(З-пиперидинокарбонилпропилтио)- -1-метил-1,2.3,4-тетразол, бесцветная жидкость, Пд 1,5310;
Н-этип-К-циклогексил-З-(1-метил- .-1,2,3, 4-тетразол-5-ил)тио-пропион- амид,, светло-желтая жидкость, ni 1,5273;
М-этиЛ-К-циклогексил-5-(1-метил- -15 2,, 3, 4-тетразол-5-ил)тио-валерамид,
светло-желтая жидкость, 1,5227;
N-эtил-N-циклoгeкcил-4-(1-фенил-1, 2, 3, 4-тетразол-5-ил)тио-бутирамид, - Злгаат перегоняют при пониженном дав1Р . 3. ,,
бесцветная жидкость, Пр 1,5590,
Пример 58.К раствору 1-ме- тил-5-меркаптометил-1,2,3,4-тетразо- ла (0,1 моль) в ацетоне (100 мл) добавляют К,Ы-диметш1-3-бромиропион- Ю амид (0,12 моль) и карбонат калия (0,12 моль). Смесь нагревают с обратным холодильником в течение 4 ч. После отгона ацетона при пониженном давлении к остатку добавляют воду и j смесь экстрагируют хлороформом. Хлороформный слой промъгоают насыщенным водным раствором хлористого натрия и сушат над сульфатом магния. После отгона растворителя полученный в ре- 20 зультате остаток подвергают хромато- графической очистке (Кизельгель 60, Merch, элюируя колонку смесью хлороформ-метанол (50:1, об/об) с образолении с образованием метил-4-(1-метил -1,2,3,4-тетразол-5-ил)тио-бутирата (20 г), бесцветная жидкость, т.кип. 175-177 С, 0,8 мм Hg 1,5083.
Вычислено, %: С 38,88; Н 5,59; N 25,91
Найдено, %: С 38,98; Н 5,67; N 25,83.
Примеры 62 и 63. Заменяя 1-фенил-или 1-циклогексил-5-меркапто- -1,2,3,4-тетразол - на 1-метил-5-мер- капто-1,2,3,4-тетразол в методике, описанной в примере 61 получают следующие соединения:
метил-4-(1-фенил-1,2,3,4-тетразол- -5-ш1)тио-бутират, бесцветная жидкость, Пр 1,5654;
метил-4-(1-циклогексил-1,2,3,4ванием М,Н-дизтил-3-(1-метил-1,2,3,4-25 -тетразол-5-ил)тио-бутират светло35
40
-тетразол-5-ил)метилтиопропионамида (выход 48%) бесцветная жидкость, 1,5200.
Вычислено, %: С 46,67; Н 7,44; N 27,21.
C,oH«NjOS
Найдено, %: С 46,72; Н 7,53; N 27,29.
Пример ы 59 и 60. Согласно методике, описанной в примере 58, получают следующие соединения:
Ы,К-диэтил-3-1-(4-этилфенил-1,2, 3,4-тетразол-5-ил)метилтио-пропион- амид, бесцветная жидкость, п1 1,5499;°
Ы-зтил-Н-циклогексил-З-(1-этил- -1,2,3,4-тетразол-5-ил)метиптио-про- пионамид, светло-желтая жидкость, % 1,5277.
Пример 61.К раствору 1-ме- тил-5-меркапто-1,2,3,4-тетразола 11,6 г (0,1 моль) в ацетоне (100 мп) добавляют метил-4-бромбутират (21,7 г) (0,12 моль) и карбонат калия (15 г) (0,11 моль). Смесь нагревают с обратным холодильником в течение 4 ч. После отгона ацетонй при пониженном давлении к полученному в результате остатку добавляют воду и водную смесь экстрагируют хлороформом. Хлороформный раствор промывают насыщенньм вод ным раствором хлористого натрия и сушат над сульфатом магния. После отгона хлороформа, остаток подвергают
30
45
50
5
желтая жидкость, Пд 1,5162.
Пример 64, Тем же способом, что описан в примерах 1-4 получали метш1-4-(1-этилфенил-1,2,3,4-тетра- зол-5-ил)тио-бутират, светло-желтая жидкость, п 1,5581.
Примеры 65-76. Аналогично примерам 1-4 получают следующие соединения:
3-(1-фенил-1,2,3,4-тетразол-5-ил)- метилтиопропионамид, в виде бесцветных призм (перекристаллизован из зтилацетата) ,т. пл. 91-92 0;
3-(1-циклогексил-1,2,3,4-тетра- зол-5-ил)метиптиопропионамид, в виде бесцветных игл (йерекристаллизо- ван из этанола) ,т. пл. 137-140 С;
4-(1-метил-1,2,3,4-тетразол-5-ил)- тио-бутирамид, в виде бесцветных призм (перекристаллизован из этанола т.пл. 90-92 С;
3-(1-бутил-1,2,3,4-тетразол-5-ил)-метилтио-пропионамид, в виде бесцветных чешуек (перекристаллизован из этилацетата) ,т.пл. 79-8l C;
3-(1-метш1-1,2,3,4-тeтpaзoл-5-ил)- мeтилтиo-пpoпиoнaмид в виде белых гранул (перекристаллизован из зтано- ла), т. пл. 105,5-108 С;
4-(1-этил-1,2,3,4-тетразол-5-ил)- метилтио-бутирамид,. в виде бесцветных призм (яерекристаллизован из этилацетата - гексана), т.пл. 72-73 С;
хроматографированию на колонке (Ва- коголь-С-200), используя в качестве элюента смесь бензол-эфир (5:1 об/об).
. ,,
лении с образованием метил-4-(1-метил -1,2,3,4-тетразол-5-ил)тио-бутирата (20 г), бесцветная жидкость, т.кип. 175-177 С, 0,8 мм Hg 1,5083.
Вычислено, %: С 38,88; Н 5,59; N 25,91
Найдено, %: С 38,98; Н 5,67; N 25,83.
Примеры 62 и 63. Заменяя 1-фенил-или 1-циклогексил-5-меркапто- -1,2,3,4-тетразол - на 1-метил-5-мер- капто-1,2,3,4-тетразол в методике, описанной в примере 61 получают следующие соединения:
метил-4-(1-фенил-1,2,3,4-тетразол- -5-ш1)тио-бутират, бесцветная жидкость, Пр 1,5654;
метил-4-(1-циклогексил-1,2,3,425 -тетразол-5-ил)тио-бутират светло35
40
30
45
50
5
желтая жидкость, Пд 1,5162.
Пример 64, Тем же способом, что описан в примерах 1-4 получали метш1-4-(1-этилфенил-1,2,3,4-тетра- зол-5-ил)тио-бутират, светло-желтая жидкость, п 1,5581.
Примеры 65-76. Аналогично примерам 1-4 получают следующие соединения:
3-(1-фенил-1,2,3,4-тетразол-5-ил)- метилтиопропионамид, в виде бесцветных призм (перекристаллизован из зтилацетата) ,т. пл. 91-92 0;
3-(1-циклогексил-1,2,3,4-тетра- зол-5-ил)метиптиопропионамид, в виде бесцветных игл (йерекристаллизо- ван из этанола) ,т. пл. 137-140 С;
4-(1-метил-1,2,3,4-тетразол-5-ил)- тио-бутирамид, в виде бесцветных призм (перекристаллизован из этанола) т.пл. 90-92 С;
3-(1-бутил-1,2,3,4-тетразол-5-ил) -метилтио-пропионамид, в виде бесцветных чешуек (перекристаллизован из этилацетата) ,т.пл. 79-8l C;
3-(1-метш1-1,2,3,4-тeтpaзoл-5-ил)- мeтилтиo-пpoпиoнaмид в виде белых гранул (перекристаллизован из зтано- ла), т. пл. 105,5-108 С;
4-(1-этил-1,2,3,4-тетразол-5-ил)- метилтио-бутирамид,. в виде бесцветных призм (яерекристаллизован из этилацетата - гексана), т.пл. 72-73 С;
4-(1-фенил-1,2,3,4-тетразол-5-ил)- тио-бутирамид, в виде бесцветных,игл (перекристаллизован из этилацетата- гексана), т.пл. 115-116,5 С;
N-(2-фeнилэтил)-4-(1-мeтшI-1,2, 3,4-тетразол-5-ш1)тио-бутирамид, в виде бесцветных игл (перелсристаллизо- ван из этилацетата-гексана), т, пл, 58,.
этил-4-(1-метил-1,2,3,4-тетразол- - 5-ил)тио-бутират, в виде бесцветной жидкости, п 1,5053;
метил-К-(1-этил-1,2, 3,4--тетразол- -5-ш1)метилтио-пропионат, в виде бест ветной жвдкости, п 1,5093;
н-бутил-4-(1-метил-1,2,3,4-тетра- 3:ОЛ-5-ш1)тио-бутират, в виде бесцветной жидкости, Пр 1,4969
-(4-фени.пбутил)-4-( 1-метил-1, 2, 3,4-тетразол-5-ил)тио-бутирамид, в в|аде бесцветных чешуек (церекристал- лизован из гексана - простого эфира этилацетата), т.пл. 47-48 С;
Пример 77. К-этш1-М-цикло- гексил хлорацетамид (15 г, 0,08 моль) и 1-метил-5-меркапто-1j 2,3,4-тетразол
(1,8 г, 0,016 моль) смешивают, и к смеси добавляют карбонат кальция. Смесь нагревают до в течение 1 ч, Досле добавления воды остаток экстрагируют эфиром. Эфирный раствор гфомывагот водным насыщенным раствором хлорида натрия и высушивают над сульфатом магния. После отгонки Фира получающийся остаток перекрис- таллизоззывают из смеси зфиргпетролей- ньш эфир. ПoJгyчaют Ы-зтил-Н-циклогек- (1-метил-1,2,3,4-тетразол-5- )тиоацетамида (О,,9 г), в виде бе- Jit TK призматических кристаллов, т.пл. 6 -71°С.
Вычислено, %: С 50,86; Н 7,47; 24,71
Ci HjrNsOS , %: С 50,77; Н 7,58;
N
24,77..
Пример 78. К раствору N-ме- тил-Ы-циклогексил-4-хлорбутирамида (13,2 г, 0,06 моль в сухом бензоле (50 мл) добавляют 1-метил-5-меркапто- -1,2,3,4-тетразол (3,6 г, 0,03 моль) карбонат калия (4,5 г, 0,033 моль) и йодид натрия (0,2 г, 0,001 моль). Смесь перемешивают при температуре - в течение 30 ч и разводят беизо лом. Реакционную смесь промывают во- дОй, водным насыщенным раствором бикарбоната натрия и водным насьяценным
растзороы хлорида натрия, и высушивают Нс1д сульфатом натрия. После отгонки бензола получившийся остаток вводят в хроматографическую колонку (Ва- когель С-200), элюируют смесью бензола и хлороформа в соотношении
Oj, 80Tl6
4:1 по объему. В результате получают Н-метш1-Н-циклогексип-4-(1-метил- 1,2,3, 4-тетразол-5-ил)тио-бутирамид: (3,5 г), в виде бледно-желтой жидкости.
ЯМР (с/ СС) млн.дол.: 1,0-2,00 (10 Н„ широкая); 1,80-2,70 (чнм 4Н, м); 2,73 (ЗН, д, I Гц), 3,28 (2Н, т, I 6 Гц); 3,85 (ЗН, с); 3,20-4,50 (1Н, м).
Вычислено, N 23,55)
%: С 52,50; Н 7,79;
5
5
0
5
0
CnH,,NyOS
N
Найдено, %: С 52,73; Н 7,89; 23,59. .
Пример 79. 1-Метил-57мерка п- то-1,2,3,4-тетразол (1,6 г, 0,014 моль), гидроокись калия (0,9 г, 0,016 моль), иодид натрия (3,2 г, 0,021 моль) и 0 3-морфолинокарбонилпролилхлорид (5,1 г, 0,027 моль) добавляют к этанолу (30 мл), и смесь перемешивают при О в течение 15 ч. По окончании реакции реакционную смесь вьшивают в водньй насыщенный fiacTBOp хлорида натрия и вьтадающие кристаллы отделяют фильтрованием и промывают водой. Полученные таким образом неочищенные крис, таллы перекристаллизовывают из смеси эфир:петролейньй эфир с получением 5-(3-морфолинокарбонилпропил- тио)-1-метил-1,2,3,4-тетразбла (1,4 г) , в виде белых игл, т. пл. 71-73°С.
Вычислено, %: С 44,27; Н 6,37;. N 25,81 ,
C,oH,70aN,;S .
Найдено, Z: С 44,08; Н 6,31; N 25,62.
Пример 80. 1-Метил-5-меркап- то-15 2,3, 4-тетразол (1,6 г, 0,014 моль) этилат натрия (1,4 г, 0,02 моль), иодид натрия (1,6, 0,01 моль) и N- -циклогексил-4-хлорбутирамид (5,7 г, 0,028 моль) добавляют к диметилсуль- фоксиду (30 мл), смесь нагревают до при .перемешивании в течение 3 ч. По окончании реакции реакционную смесь . вьшивают в водный насыщен- ньй раствор хлорида натрия. Вьтадаю111400507
щие кристаллы отделяют фильтрованием и промывают водой. Полученные таким образом неочищенные кристаллы пере- кристаллизовьшают из смеси гексана и этилацетата с получением циклогексил- -4-(1-метиЛ-1,2,3,4-тетразол-5-ил)- тио-бутирамида (1,8 г), в виде бест.пл. 116,5-117,5°С. %: С 50,86; Н 7,47;
цветных игл. Вычислено, :N 24,71; CiiHaiNjOS Найдено, % IN 24,64..
Пример силхлорацетамид
10
С 50,88; Н 7,37;
Рассчитано, %: С 50,86; Н 7,47; N 24,71i
C,,H,NsOS35
Найдено, %: С 50,76; Н 7,59; N 24,76.
Пример 82. Смешивают N-этил- -N-циклогексилхлорацетамид (30 г, 0,16 моль) и 1-метил-5-меркапто-1,2, 40 3 4-тетразол (1,8 г, 0,016 моль) и к смеси добавляют карбонат калия. Смесь нагревают при 200°С в течение 1 ч. После добавления воды остаток экстра12
Пример 83. М,Ы-Диэт1-т-3- -меркаптопропионамид (2,43 г) .растворяют в 1 Н. водном растворе гид- роксида натрия (45 мл) и к нему добавляют по каплям раствор 1-метил-5- -хлорметил-1,2,3,4-тетразола (15,2 г) в ацетоне (20 мл) при перемешивании и охлаждении льдом. Перемешивание продолжают в течение 3 ч при охлаждении льдом. Ацетон отгоняют и остаток подкисляют концентрированной соляной кислотой, насыщенной хлоридом натрия, затем экстрагируют хлороформом. Хлоро- формнЬш раствор сушат над сульфатом
магния После отгонки хлороформа остаток подвергают хроматографии на колонке (кизельгель 60, изготовитель Merck) с применением в качестве элю- ента смеси хлороформ-метанол (50:1, объём/объем) и получают Н,Н-диэтил- -3-(1-метил-1,2,3,4-тетразол-5-ил)ме- тилтиопропионамид (2,6 г) в виде бесцветной жидкости, n 1,5200.
Рассчитано, %: с 46,67; Н 7,44; N 27,21
CtoHt N OS
. Найдено, %: С 46,86; Н 7,60; N 27,38.
Примеры 84-86. Аналогично примеру 83 с применением соответствующих исходных соединений получены следующие соединения:
N,N-диэтил-3-(1-этил-1,2,3,4-тет- разол-5-ил)метилтиопропионамид, бес цветные иглы (перекристаллизации из эфира), т. пл. 58-59 С;
Н,К-диэтил-3-(1-(4-этилфенш1)- -1,2,3,4-тетразол-5-ил)-метш1тиопро- пионамид, бесцветная жидкость, пjj 1,5499;
Ы-этил-К-циклогексил-З -(1-этил- -1,2,3,4-тетразол-5-ил)-метилтиопро- пионамид, бледно-желтая жидкость.
тируют эфиром, эфирный раствор промы-45 S К5277.
Примеры 87-100. Согласно примерам 1-4 с применением соответствующих исходных соединений получены следующие соединения:
Н-этил-Н-циклогексил-4- 1-(2-ме- токсициклогексил)-1,2,3,4-тетразолвают водным насыщенным раствором хлористого натрия и высушивают над сульфатом магния. После отгонки эфира полученный остаток перекристаллизовы- вают из смеси эфира-петролейного ра, получают N-этшl-N-циклoreкcшl-2-{1-метил-1,2,3,4-тетразол-5-Ш1) THOI- -ацетамид (1,0 г), белые призмы, т.пл. 69-71 С.
Рассчитано, %: С 50,86; Н 7,47; N 24,71 л
55
-5-ил тио-бутирамид;
Рассчитано, %: С 58,65; Н.8,61; N 17,10;
Найдено, %: С 58,25; Н 8,34; N 17,20.
C,H,,N50S
Найдено, N 24,69.
%: С 50i87; Н 7,46;
0
5 0
5
0
12
Пример 83. М,Ы-Диэт1-т-3- -меркаптопропионамид (2,43 г) .растворяют в 1 Н. водном растворе гид- роксида натрия (45 мл) и к нему добавляют по каплям раствор 1-метил-5- -хлорметил-1,2,3,4-тетразола (15,2 г) в ацетоне (20 мл) при перемешивании и охлаждении льдом. Перемешивание продолжают в течение 3 ч при охлаждении льдом. Ацетон отгоняют и остаток подкисляют концентрированной соляной кислотой, насыщенной хлоридом натрия, затем экстрагируют хлороформом. Хлоро- формнЬш раствор сушат над сульфатом
магния После отгонки хлороформа остаток подвергают хроматографии на колонке (кизельгель 60, изготовитель Merck) с применением в качестве элю- ента смеси хлороформ-метанол (50:1, объём/объем) и получают Н,Н-диэтил- -3-(1-метил-1,2,3,4-тетразол-5-ил)ме- тилтиопропионамид (2,6 г) в виде бесцветной жидкости, n 1,5200.
Рассчитано, %: с 46,67; Н 7,44; N 27,21
CtoHt N OS
. Найдено, %: С 46,86; Н 7,60; N 27,38.
Примеры 84-86. Аналогично примеру 83 с применением соответствующих исходных соединений получены следующие соединения:
N,N-диэтил-3-(1-этил-1,2,3,4-тет- разол-5-ил)метилтиопропионамид, бес цветные иглы (перекристаллизации из эфира), т. пл. 58-59 С;
Н,К-диэтил-3-(1-(4-этилфенш1)- -1,2,3,4-тетразол-5-ил)-метш1тиопро- пионамид, бесцветная жидкость, пjj 1,5499;
Ы-этил-К-циклогексил-З -(1-этил- -1,2,3,4-тетразол-5-ил)-метилтиопро- пионамид, бледно-желтая жидкость.
-5-ил тио-бутирамид;
Рассчитано, %: С 58,65; Н.8,61; N 17,10;
Найдено, %: С 58,25; Н 8,34; N 17,20.
N-(4-метоксициклогексил)-4-(1-метил- t,2,3,4-тетразол-5-ил)тио-бутир1314
амид, бесцветная жидкость, f,5263;
N- (4-меташциклЬгексил)-4- (1 -мети 152,3,4-тетразол 5-ил)тио-бутирамид
Рассчитано, %г С 52,50; Н 7,79; М 23,55;
H jNgOS
Найдено, %: С 52,31; Н 7,65| N 23,
N-этил-3-(1-бутил-1,2,3,4 тетра- зол-5-и.п)мет:ш1:тиопропионамид, бледно-желтая жидкость, Пр 1,5149;
Н-этйл-3-(1-фенил-1,2,3,тетра- зпл-5 нл)мет1-штиопропионамид, бес- цветные иглы (перекристаллизация из гексан-этилацетат), т.гш, 88- 86,5°С;
N-3TRn-4-(1-этил-1,2,3,4-тетразол )мети.г1тио-бутирамид5 бледно-жел тая жидкость, п 1,5224;
Г,Н-диэтил 4-(1-этил-1,2,3, 4-тет- разол-5-ил)метилтио-бутирамид5 бледНС-желтая жидкость, п., 1,51281
М-этил-Ы-циклогептил -4-(1-метил- -1,2,3s 4-тетразол-5 ил)тио-бутирамид бесцветная жидкость, п 1,5290;
Н-диизопропш1-4-(1-метил-1,2.3,4- -тетразол 5-яп)тио-бутирамид, бесцвеная жидкость, 1,5111;
К-изопропк:г -г1-циклогексил-4- (1 - метил-1J 2,3 J 4-тетразол-5-ил) тио-бут ти)рамид, бесцветная жидкость, 1,5238; ,
N-этил-2(1-этил-1 2,3,4-тетразол- 5 -ш1)цропилтноацетамид, бледно-жел- тля жидкость, п1 1,5210;
М н-гексил-4-(1-метил-1,2,3,4- -тeтpaзoл-5-ил)тнo-бyт фaмид, бесцве ггые. хлопья (перекристаллизация из смфси гексан-эфир), т. пл, 41-42°С;
N-f4-(NS Н-диметиламино)циклогек- (1-метил-1,2,3, 4-тет.разол-5- -ил)тио-бутирамид.
Рассчитано, %: С-51,51; Н 8,03; N 25,74;
Найдено, % С 51,60; Н 8,22; N 26,05,
; 3-(1-этил-1,2,3,4-тeтpaзoл-5-ил)- мeтйлтиoпpoпиoнa mд, бесцветные хлопья т. пл. 74-76 С.
Фармакологи ческие данные. Фармакологические испытания. Фармакологическая активность соединений общей форм мулы I испытана обычными методами, как указано низке по отношению к следующим соединениям (пример №);
0
5
п
0
5
5
, 10. (пример 35) N-фypфypил-4-(1- метил-1J 2,3,4 тетразол-5-Рш)тио-бутирамид;
17,(пример 94) N-этил-N-диклoгeп- (1-мет1-ш-1,2,3, 4-тетразол-5- -1-ш) тио-бутирамид;
18,(пример 95) К,М-диизопрапил- 4-(1-метил-15 2,3,4-тетразол-5-ил)тио- бутирамид;
19,; (пример 96) К-изопропил-Н-цик- логексил- Л(-1 метил-1,2,3, 4-тетразол- 5-ил)тио-бутирамид;
51Л00507
(пример 54) 5-(3-пяперикилкар
бонилпропилтир)-1-метш1-1,2,3,А-тет- разол;
сил-3-(1-этил-1,2,3,4-тетразол-5-ил)- JQ разинокарбонил)пропилтио -1-метил-1,2,3,4-тетразол;
35
метилтиопропионамид;
Р 33. (пример 38) Ы-(2-метил-3-хлор-д0 фенил)-4-(1-метил-1,2,3,4-тетразол- -5-шг)тио-бутирамид;
50
0
5
0
5
-1,2,3,4-тетразол;
Структурные аналоги; А. 1-фенШ1- -5-амино-1,2,3,4-тетразол; В. 2-(3- -бромфенил-5-(2-карбамоилэтш1)-1,2, 3,4-тетразол; С. 2-(3-бромфенш1)-5- -(2-пиперидинокарбонилэтил)-1,2,3,4- -тетразол. Фармакологическое испытание № 1. Фармакологическая активность соединений (I) испытана по методу Shay - наложение лигатуры на привратник желудка крысы, который является наибо лее распространенным методом испыта-
1400507 Коэ фшхиент подавления
(И1 контрольных (рп KP6IC, получивших
Sgbisl. 00
И1 контролыых крыс Результаты представлены в табл.2.
Фармакологическое испытание 3, язва, вызванная уксусной кислотой.
Были взяты крысы-самцы Wistar. Под анестезией бьша вскрыта брюшная полость крыс с целью обнажения желудка, затем 30%-ный йодный раствор уксусной кислоты (9,015 мл) был введен под серозную оболочку и был локализован на граничном участке истинной железы желудка и желез привратника желудка, затем брюшную полость зак- рьши, вследствие чего была вызвана экспериментальная язва.
Соединения 1 вводили орально в дозах, представленных в табл. 3, в виде 0,5%-ной суспензии или раствора КМЦ, два раза в день в течение 12 дн. после образования язвы, вызванной действием уксусной кислоты. В качестве контрольного соединения вводили та- КИМ же образом только растворитель (раствор КМЦ).
После того как восстановленная слизистая оболочка была удалена вокруг язв, открытая поверхность язв бьта измерена микрометром и суммарная поверхность язв представлена как язвенный показатель (И1). Коэффициент
20
Таблица2
5
0
подавления (0) вызванной уксусной кислотой язвы испытуемых соединений вычислен так же, как в фармацевтическом испытании 1.
Результаты представлены в табл. 3.
Т...§ -б ли
Соединение ; Доза, 3 10 -моль/
№ 19
/кг/день
Коэф- . фициент подавления, ЗОИ
2
6
21
23
30
37
38
39
40
А
В
С
20 мг/кг/день
It II
,30,6
33,3
32,3
35,6
43,9
37,8
36,1
32,4
31,9
9,9
9,2
Острая токсичность. Соединения 1 1аодили орально крысам-самцам Wistar и определяли дозу, при которой гибнут 50% животных (LDjp), : Результаты представлены в табл. 5,
Таблица 5
II
500
II
профилактической .или терапевтической актив.ностью против пептической. и/или дуоденальной язвы, особенно против язв, вызванных стрессом и язв, вьи- ванных ивдометацином, без таких побочных эффектов, как влияние на центральную нервную систему, антихолинер- гическая активность, влияние на ско- рость освобождения желудка, и пригодны в качестве медицинских препаратов для лечения таких язв. Эти соединения обладают также противовоспалительной активностью и пригодны в качестве про- противовоспалительных лекарств.
Формула изобретения
Способ получения производных тет- разола общей формулы I
:к-1т
LA
V A-B-CORz
.
RI
231400507
де R:| - С ,-C f-anKHn,iJ,HKnoreKCH.n, замещенный метоксигруппой, фенил, незамещенный или замещенный С -С-г-алкилом; А - сера или C -Cj-алкилентиогруппа ;
В - С -С -алкилен; Rj - С -С -алкоксигруппа или группа общей формулы1Q
-л
-N
/R3
Кд
20
25
де RJ и R - одинаковые или раалич- ные, водород С,-С -алкил, . Су-С циклоалкил,незамещенный или замещенный гидроксилом, ацетилок- сигруппой, метоксигруппой, метилом или N,N- -диметиламиногруппой, фенил,незамещенный или замещенный одним или двумя заместителями, выбранными из группы: аминосульфонил-Ы,N-ди- метиламино,метил, галоген, метокси или нитро, циклогексилметил, фе- нил-С -С4-алкил, в котором фенил может быть замещен С -С -алкоксиГРУППОЙ, ОКСИЭТИЛ, ПИ
ридил-2-фурилметил, 2- 35 -тиенилметил, или R} и R 4- вместе могут обра- зовьшать с атомом азота, с которым они свя-
30
где R имеет
R групп ет ук подвергают вз водным алканк формулы III
где X(j - гало В и R имею
при то Х R груп
в присутствии агента при те в течение 1-3 общей формулы формулы II ис отношении/ 1-5 дят в среде р если процесс
заны, гетероциклическую40 растворителя.
24
группу, такую как мор- фолиновая, пиперидино- вая или пиперазиновая, которая может быть замещена метилом или ацетилом,
чающийся что, ное тетразола общей форму-
-К
11
Ki
И:
где R имеет указанные значения;
R группа АН или ДХ, где А име- ет указанные значения, Д С -С -алкилен, а X - галоген, подвергают взаимодействию .с производным алканкарбоновой кислоты общей формулы III
Хо -6 -COR,, ,
где X(j - галоген или меркаптогруппа В и R имеют указанные значения,
при условии, если Rj - -А-Н, то Хо - галоген, а если R ДХ, то Хр - меркапто- группа,
в присутствии дегидрогалогенирующего агента при температуре (-30) в течение 1-30 ч, причем соединение общей формулы III и соединение общей формулы II используют в молярном соотношении/ 1-5: 1 , если процесс проводят в среде растворителя, или 5-10:1, если процесс проводят в отсутствии

| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| Способ приготовления хлебного вина | 1925 |
|
SU424A1 |
| Устройство станционной централизации и блокировочной сигнализации | 1915 |
|
SU1971A1 |
| .Патент США № 3743646, кл | |||
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
Авторы
Даты
1988-05-30—Публикация
1982-05-04—Подача