Изобретение относится к новым .биологически активным химическим соединениям, конкретно к N-замещенным лактамам, обладающим фармако.гюгической активностью.
В частности, они обнаруживают активность в мнезических процессах и защитную активность против агрессий типа ГИПОКСИИ; Они мэгут найти п|рименение для лечения расстройства памяти, связанных с изменениями клеток, вызываемых как возрастом, так и уменьшением поступления кислорода в мозг вследствие первичных или вторичных травм сосудов. Они могут найти применение во многих других областях, например, для профилактики и лечения травм сосудов головного мозга или сердечно-гсосудистых травм, пост-травматических или токсических коматозных состояний, расстройств памяти, трудностей, вызванных умственным напряжением и т.д.
Известны N-замещенные лактамы (например, пирацетам-2-оксо-1-пирролидинацетамид) , обладакщие анало- . гичной терапевтической активностью 11
Однако известное соединение имеет тот недостаток, что оно бывает эффективньш только повьвиенных дозах..
Цель изобретения - расимрение ассортимента соединений, проявлякад1к активность в мнезических процессах и активность против агрессий типа гипоксии и сердечную активность.
Поставленная цель достигается свойствами N-зёимещенных лактамов общей форму1Ш
(CttaU
Кб
Rj- C-CO- -CH-CO-N:
к
где R,Ri,R3fR4 5 6 т независимо друг от друга водород, алкильньй радикал , или фенил; Rg - водород, или Rg и Rj образуют вместе радикал этилена или триметилена; п - целое число (от 3 до 5). Соединения формулы (Г) пол чают известным способом 2.Обычно конденсируют в инертной среде (хлороформ или хлористый метилен), лактам - N-уксусной кислоты общей форму лы (II) со сложным эфиром аминокис СН2)а R4 c o- -HH-cit-coo тг дик Hj-C-COOH 8 лоты общей формулы (У) в присутствии конденсирующего агента, например дициклогексилкарбодиимида (ДЦК), а полученный таким образом сложньлй эфир общей формулы (ГЦ) затем вводят в реакцию с амином общей формулы , в некоторых случаях в присутствии метилата натрия в качестве катализатора. Реакционная схема может быть представлена следующим образом НККбКу II Кз - С - со.-Т Г-ч;н- ;оо z R. По такой же методике получают следующие соединения формулы (111) Б) Бенэиловый эфир N-(2-oкco-l-пиppoлидииaцeтил)-глицинa. Т.пл. 92°С. Выход 58%. (Формула (111): , Z-бензил). в) Этиловый эфир N-(d-этил-5,5-диметил-2-оксо-1-пирролидинацетил-глицина. Т.пл. 61°С. Выход 68% (формула (111): , Н4-К5-5-мэтил ЕЗ-ЭТИЛ г-этил. пт-3,н -R -5-метил, R -этил, Z-этил 1) Этиловый эфир N-(dL, 5, 5-триметил-2-оксо-1-пирролидинацетил)-г цина. Т.пл. . Выход 55% (форму ла (111): , ,j-5-метил, тил, Z-этил). d ) Этиловый эфир N- (о1-этил-2-рк со-1-пирролидинацетил)-глицина.Т.п 70°С. Выход 63% (Формула (111):п-3 Rэ-этил, Z-этил). е ) Этиловый эфир W- (cL-метил-2-о со-1-пирролидинацетил)-глицина. Т. 4В°С. Выход 66% (формула (111): п , Z-этял) . ж) Этиловый эфир 2- 1-(2-оксо-пирролидино)-циклопропанкарОоксам до -уксусной кислоты. Т. пл. . Выход 51% (формула (111): , Rj и Rg- этилeн, Z-этил). Э) Этиловый эфир N-(2-ОКСО-1-ПИ ролидинацетил)-саркозина. Т.пл.160 (0,01 мм рт.ст.). Выход 67% (форму ла (111): , R -метил,Z-этил). м ) Бензиловый эфир N-(2-оксо-1-пирролидинацетил)-саркозина. Сиро Выход 87% (формула (111), R4-м тил, Z-бензил). к ) Метиловый эфир.1а- (2-оксо-1- пиррол иди нацет ил)-а лани на. Сироп. Выход 79% (формула (111): , Rj-Z-метил) . л) Этиловый эфир N-(2-OKCo-l-пирролидинацетил)-2-фенилглицина. Т.пл. 89°С. Выход 80% (формула (111 , R5-фeнил, Z-этил). . м) Этиловый эфир N-(2-оксо-4-фенил-1-пирролидинацетил)-глицина, Т.пл. . Выход 77% (формула (111 Rxi-4-фенил, , 2-этил) . н) Этиловый эфир Ы- (2-оксо-с1-феНИЛ-1-пирролидинацетил)-глицина. Т.пл. 115С. Выход 66% ( (111): , Rз-Фeнил, Z-этил). о) Этиловый эфир N-(5-метил-2-оксо-1-пирролидинацетил)-глицина. Сироп. Выход 100% (формула (Ml) : , Ri-5-метил, Z-этил). П) Этиловый -эфир N-(гeкcaгидpo-2-oкco-lH-aзeпйн- -aцeтил) -глицина Т.пл. 104С. Выход 61% (формула (111): , Z-этил). р) Этиловый эфир N-(eL-H-бутил-2-оксо-1-пирролидинацетил)-глицина Т.пл. 79°С. Выход 75% (формула (111): , Rз-w-бyтил, Z-этил). с) Этиловый эфир N-(3-н-бутил-2-оксо-1-пирролидинацетил)-глицина. Сироп. Выход 100% (формула (111): Пя, R -3-н-бутил, Z-этил). Пример 2. Синтез кГислот формулы (1У) . «) N-(2-оксо-1-пирролидинацетил)-глицин. Растворяют 2,.9 г (0,01 моль) бензилового эфира N-(2-бксо-1-пирролидинацетил)-глицина (продукт 1Б) в 50 мл уксусной кислоты и гидрируют продукт в присутствии палладированного угля (Pd/C) при комнатной температуре под давлением 4 кг/см . Отфильтровывают катализатор, фильтрат выпаривают досуха и растирают в пороиюк полученный таким образом сироп с безводн1Л4 эфиром, получая jB результате белый пороиюк. Таким образом выделяют 2 г N-(2-оксо-1-пирролидинацетил)-глицина. Т.пл. 149-150°С, йлход 100%. Молекулярная масса 200. Элементный анализ. йлчислено,%: С 48,0; Н 6,0; N 14,0. С Q Найдено,%: С 47,6; Н 6,21; N 13,88. Получают N-(2-oкco-l-ш ppoлидинaцeтил) -саркозин. Т.пл. . Выход 67% (формула (1У): ,R4-мeтил). &) (2-Оксо-пирролидино)-циклопропанкарбоксамидо -уксусная кислота (формула (1У) : , Rj и Ra-этилен) . К ластвору 20,4 г (0,08 моль) этилового эфира (2-оксо-пирролидино) циклопропанкарбоксамидо -уксусной кислоты в 80 МП метанола приливаютраствор 3,5 г NaOH в 80 мл воды. Нагревают полученный таким образом раствор при 40с в течение 5 ч. Выпаривают спирт, остаток обрабатывают водой и подкисляют концентрированной соляной кислотой до рН 1. Выпаривают досуха и перекристаллизовывают остаток из воды. Получают 13 г (выход 69%) 2-Cl-(2-оксо-пирролидино)-циклoпpoпaнкapбoкcaмидoJ-уксусной кислоты.Т.пл. . Элементный анализ. Вычислено,%: С 53,14; Н 6,24: N 12,39. С 0 N,04 Найдено,%: С 53,20; Н, 6,30; N 12,36. Пример 3. Синтез лактамов формулы (1). ч) 2-(2-Оксо-1-пирролидинацетамидо)-ацетамид (формула (1): ,R - водород). Растворяют 17,1 г (0,075 моль) этилового эфира Ы-(2-оксо-1-пирроидинацетил)-глицина в 350 мл метанола. В насыщенный раствор пропускают NHj (примерно 2 ч) и продолжа перемешивание в течение 3 ч при ко натной температуре. После выпарива ния досуха реакционной смеси в вак уме остаток быстрр кристаллизуется Таким образом получают 14,9 г (выход 100%) 2-(2-оксо-1-пирролидинац тамидо)-ацетамид. Т.пл. 147-148°С. Молекулярная масса 199. Элементный анализ. Вычислено %: С 48,24; Н 6,53; N 21,10. Найдено,%: С 48,11; Н 6,49; N 21,24. Б) N-н-Бyтил-2-(2-ОКСО-1-ПИРРОл идинацетамидо)-ацетамид. (Формула (1): , R(,-н-бутил) . Кипятят с обратным холодильнико втечение 12 ч 9,12 г (0,04 моль) сложного этилового эфира N-(2-oкco -l-пиppoлидинaцeтил)-глицинa с 7,7 (0,1 моль) Н-бутиламина. Потом вып ривают в вакууме досуха и закриста лизовавшийся остаток промывают эфи ром. Фильтруют , прокывают эфиром и сушат оставшийся продукт. Таким образом получают 9,9 г (выход 97%) М-н-бутил-2-(2-ОКСО-1- пирролидинацетамидо) -ацета.мида. Т.пл. 105-106 С, молекулярная масса 255. Элементный анализ, вычислено,%: С 56,51; Н 8,23; N 16,47. Найдено,: С 56,66; Н N 16,36. В) N-Метил-2-(2-оксо-1-пирролидинацетамидо) -ацетамид. (формула (1): , Е(5-метил) . Прибавляют 31 г (1 мэль) метиламина к 18,24 г (0,08 моль) этилов го эфира N-(2-oкco-l-пиppoлидинaцe тил) -глицина. Реакционную смесь вы держивают при в течение 8 ч при перемешивании. Потом выпариваю и кристаллизуют остаток из абсолют .ного этанола. При этом получают 15,7 г (выход 92%) N -метил-2-(2-о со-1-пирролидинацетамид6)-аце1амид Т.пл. 139-140°С, молекулярная масс 213. Элементный анализ. Вычислено,%: С 50,74; Н 7,04; N 19,72. Найдено,%: С 50,80; Н 7,10; N 19,60. г) 2-(2-ОКСО-1-пирролидинацетам до) -N-фенилацетамид. (Формула (1): ПвЗ, )енил) ., В колбе смешивают 23,2 г „. (0,102 моль) .этилового эфира N-(2-оксо-1-пирролидинацетил)-глицина с 51 мл анилина (0,51 моль) и 10,5 метанола. К этому раствору прибавляют частями 0,39 г (0,017 моль) натрия. Доводят температуру реакционной среды до . для полного растворения натрия, потом 17ч кипятят с обратным холодильником. Затем спирт и прибавляют 150 Mff безводного толуола. Отфильтровывают образовавшийся осадок, промывают его эфиром и перекристаллизовывают из абсолютного этанола. Потом выделяют 7.4г (выход 26,5%) 2-(2-оксо-1-пирролидинацетамидо)-N-фенилацетамид. Т.пл. 200-201°С. Элементный анализ. Вычислено,%: С 61,14; Н 6,18; N 15,28. CмH 7NзOз Найдено,%: С 61,12; Н 6,22; N 15,30. а) 2-(Ы-Метил-2-оксо-пирролидинацетамидо)-N-фенилацетамид. (Формула (1): , R.-метил, К(,-фенил). Прибавляют раствор 3,8 г ( (0,04 моль) анилина в 40 мл хлористого метилена к суспензии 8,6 г (0,04 моль) N-f2-оксо-1-пирролидинацетилЗ-сакрозина в 60 мл хлористого метилена. Смесь охлаждают До и прибавляют туда по каплям 9,2 г (0,044 моль) ДЦК, растворенного в 20 мл хлористого метилена. Продолжают перемешивание в течение 2 ч при температуре между и 5°С, потом в течение 18 ч при комнатной температуре. Затем отфильтровывают дициклогексилмочевину и прибавляют к фильтрату 6 мл уксусной кислоты, потом выпаривают досуха в вакууме. Остаток обрабатывают этилацетатом, отделяют нерастворимые продукты фильтрованием (дициклогексилмочевина) и выпаривают фильтрат досуха. Получают сироп, который перемешивают в толуоле, чтобы сделать его кристаллизующимся. Можно также провести хроматографию на колонке с окисью кремния (элюент метанол-хлороформ 1/9).. Фильтруют, промывают эфиром и сушат. Таким образом собирают 9.5г (выход 82%) 2- Ы-метил-2-оксо-1-пирролидинацетамидо -N-фенилацетамида. Т.пл. 145-14бс, молекулярная масса 289. Элементный анализ. Вычислено,%: С 62,33; Н 6,57; N 14,54. c gH gNaOj Найдено,%: С 62,50; Н 6,50; N 14,48. е)ы-Изопропил-2-(2-оксо-1-пирролидинацетамкдо)5-ацетамид. Т.пл. , молекулярный вес 241. Элементный анализ. алчислено,%: С 54,81; Н 7,88; N 17,43. C H gNjOj Найдено,%: С 54,80; Н 7,80; N 17,36. 9 ) 2-(е1-Этил-5,5-диметилг-2-оксо-1-пйрролидинацетамидо)-ацетамид. Т.пл. .151°С, молекулярный вес 255. Элементный анализ. Вычислено,%: С 56,51; Н 8,23; N 16,47. C fj Hii NjOj Найдено,%: С 56,56; Н 8,29; N16/48. а ) 2-(1-5,5-Триметил-2-оксо-1-пирролидинацетамидо)-ацетамид.Т.пл 202°С, молекулярный вес 241. Элементный анализ. Вычислено,%: С 54,82; Н 7,88; N 17,42. C H gNiOj Найдено,%: С 54,9,0; Н 7,72; N 17,45. и) 2-(с1-Этил-5,5-диметил-2-оксо-1-пирролидинацетамидо)-Ы-н-пропилацетамид. Т.пл. 177°С, молекулярный вес 297 Элементный анализ. Вычислено,%: С 60,65; Н 9,09; N14,14. Hij-jN Oj Найдено,%: С 60,59; Н 9,10; N14,18. к) 2-(А-Метил-2-оксо-1-пирролидин ацетамидо)-ацетамид. Т.пл. 119°С, молекулярный вес 213. Элементный анализ. Вычислено,%: С 50,76; Н 7,04; N 19,71. CgH jNjOj Найдено,%: С 50,80; Н 7,12; N19,76. л) 2-(1-Этил-2-оксо-1-пирролидинацетамидо)-ацетамид. Т.пл. 122с, молекулярный вес 227. Элементный анализ. Вычислено,%: С 52,90; Н 7,49; ( jg 51 С Н N О Найдено,I: c53,i; Н 7,60; N 18,58. (Л) 2-Г1-(2-ОКСО-ПИррОЛИДИНО)-ЦИКлопропанкарбоксамидо -ацетамид. Т.пл 180°С, молекулярный вес 225. Элементный анализ. Bычиcлeнo,%: С 53,33; Н 6,66; jg gQ С НлЫ О НайДено,%° С Н 6,74; N 18,60, Н) N,N-Димeтил-2-(2-oкco-l-пйppoлидинацетамидо)-ацетамид. Т.пи. Молекулярный вес 227. Вычислено,%: С 52,8б; Н 7,49; N 18,51. Cjo Н-п Найдено,: С 52,80; Н 7,42; N 18,70. . О) 2-(Ы-Метил-2-оксо-1-пирролиIдинацетамидо)-ацетамид.Т.пл. , молекулярный вес 213, 010 Элементный анализ. Вычислено,%: С 50,74; Н 7,04; N 19,72. И« НайденоД: С 50,85; Н б;99; N 19,80. п) Ы-Метил-2-(Ы-метил-2-оксо-1-пирролидинацетамидо)-ацетамид.Т.пл. 111°С, молекулярный вес 227. Элементный анализ , Вычислено,%: С 52,90; Н 7,49; N 18,51. Найдено,%: С 52,84;.Н 7,45; N 18j30. Р) Ы,Ы-Диметил-2-(Н-метил-2-оксо-1-пирролидинацетамидо)-ацетамид. Т.пл. , молекулярный вес 241. Элементный анализ. Вычислено,%: С 54,81; Н 7,88; 17,43. , Найдено,%: С 54,84; Н 7,79; N 17,36. с) 2-Метил-2-(2-оксо-1-пирролидинацетамидо)-ацетамид. Т.пл. 173с, молекулярный вес 213. Элементный анализ. Вычислено,%: С 50,74; Н 7,04; N 19,71. CgH 5NjOi Найдено,%: С 50,64; Н 7,0; N 19,70. т) 2-(2-Оксо-1-пирролидинацетамид)-2-фенилацетамид. Т.пл. 195С, молекулярный вес 275. Элементный анализ. . Вычислено, %: С 61,14; Н 6,18; N 15,28. Найдено,%: С 60,47; Н 6,11; N 15,07. s) 2-{2-Оксо-4-феиил-1-пирролидинацетамидо)-ацетамид. Т.пл.1600С, молекулярный вес 275. Элементный анализ. Вычислеио,%: С 61,14; Н 6,18; N 15,28. „ а , , л2 U с 00 Найдено,: с б1,0в; Н 6,-d-J; лС ,с .. -о , 2-{5-Meтил-2-oкco-l-пиppoлидинацетамидо)-ацетамид. Т.пл. 131«С, молекулярный вес 213. Элементиый анализ. „ , 19,72, „ , в,, .-,,« . ,6Й; Н 7,10; , , « j , X) 2-(2-Оксо-о1-фенил-1-пирролидинацетамидо)-ацетамид. Т.пл. 174с, молекулярный вес 275. Элементный анализ. Вычислено,%: С 61,14; Н 6,18; N 15,29. .tTNjO3 Найдено,%: С 61,10; Н 6,20; N 15,22.
ц) 2-{Гексагидро-1-оксо-1Н-азепин-1-ацетамидо)-ацетамид. Т.пл. , молекулярный вес 227.
Элементный анализ.
Вычислено,%: С, 52,f6; Н 7,50; N 18,51.
.Oj
Найдено,%: С 53,04; Н 7,77; N18,45.
ч) 2-(-н-Бутил-2-оксо-1-пирролидинацетамидо)-ацетамид. Т.пл. молекулярный йес 255.
Элементный анализ.
Вычислено,%: С 56,51; Н 8,23; N 16,47.
C-ioHij NjOj
Найдено,: С 56,23; Н 8,18; N 16,99.
, U1) 2-(3-н-Бyтил-2-oкco- -пиppoлидинaцeтaмидo)-aцeтaмид. Т.пл. 152°С молекулярный вес 255.
Элементный анализ.
Вычислено,%: С 56,51; Н 8,23; N 16,47.
,N,,Oj
Найдено,%: С 56,61; Н 8,25; N 16,42.
щ) N-трет-бутил-2-(2-оксо-1-пирролидинацетамидо)-ацетамид. Т.пл. 14 -150с, молекулярный вес 255.
Элементный анализ.
Вычислено, %: N 16,47, Ci,(i-,N,,O,
Найдено,%: 16,02. . Фармакологические результаты.
Продукты подвергнуты фармакологическим испытаниям, результаты которых воспроизводятся ниже.
1. Действие на мнезические процесы.
Действие на мнезические процессы доказывается, в первую очередь, способностью соединений улучшать тип запоминания у крысы. Наблюдают реакцию сжатия лапы у крысы, которая испытывала возрастающее и количественное давление. Давление, на которое возникает реакция, называется порогом реакции. Этот последний выражаеся числом делений на градусы цкалы используемого аппарата (анальдезиметр UGO BASILE-Милан), и соответствует, тйким образом, минимальному давлению, которое накладывается на лапу животных, вызывающему сжатие. Оно непосредственно считывается на шкале используемого аппарата.
Опыты, проведенные через 24 ч на контрольных животных, не показали никакой видимой задержки предшествующего испытания: устранение наблюдается для интенсивности стимулирования, сравниваемой с интенсивность бодрствования. Напротив, животные, которым было введено вещество,оказывающее положительное действие на мнезические процессы (как, например пирацетам), показывают значительную
степень задержки: раздражитель, с которым крысы реагируют на рефлекс устранения,статистически ниже раздражителя контрольных животных. Используют минимально 20 крыс на один сЛыт (10 обработанных крыс и 10 контрольных крыс) и определяют в качестве активной дозы минимальную дозу, понижающую раздражитель ниже 11 делений шкалы.
Подкожное введение некоторых соединений формулы (Т), а именно соединений а) , ) , 3 ) , м ) , к ), л ), м ), )/п),р),с),т),ц) ич) давало в этих условиях действия, показанные
в та бл. 1.
Из табл. 1 следует, -что все соединения обнаруживают в этом опыте активность, превышающую активность пирацетама, действие которого на
мнезические процессы хорошо известно.
Таблица 1
Действие на мнезические процессы доказываются также сокращением времени спинальной фиксации. У крысы, после одностороннего повреждения мозжечка, имеется асимметрия положения задних лац. Эта асимметрия может продолжаться даже после спинального разреза, если животное находилось достаточно продолжительное время в этой ситуации. Это время, называемое спинальной фиксацией, в экспериментальных условиях, применяемых 5 здесь, составляет 45 мин.
Напротив, если спинальный разрез производился до истечения этого времени, .например, через 35 мин после установления асимметрии, эта последг няя исчезала.
Ни одно животное, обработанное плацебо, не сохраняло асикметрии в этих условиях.
Напротив, любое вещество, позволяющее крысам сохранить асимметрию (следовательно, осуществляющее спинальную фиксацию), когда спинальный разрез осуществляется через 35 мин, считается активным.
Введение интраперитонеальным путем вещества а) давало эффекты,описанные в табл. 2 . Под числсж животных подразумевают число животных, реагирующее положительно на опыт, по отношению к числу животных, испытываемых при указанной дозе.
Т а б л и ц а 2
II. Защита от агрессий типа гипоксии.
Защита от агрессий типа : гипоксии доказывается уменьшением леталь.-. ности, вызываемой кураре с кopoтkим временем действия, хлористым оксидипентонием. При применяемых дозах этот кураре влечет за собой дыхательную депрессию, которая, в свою оче0редь, вызывает синдром гипоксий-гйперкапнии. BeiqecTBO, способное защитить большой мозг во бремя этого короткого периода гипоксии, обеспечивает выживание. Вещества
5 давались rpynifaiM из 10 млией за один .час до инъекций кураре, параллельно контрольная группа из 10 мышей получала перед введением кураре физиологический раствор хлористого Натрия.
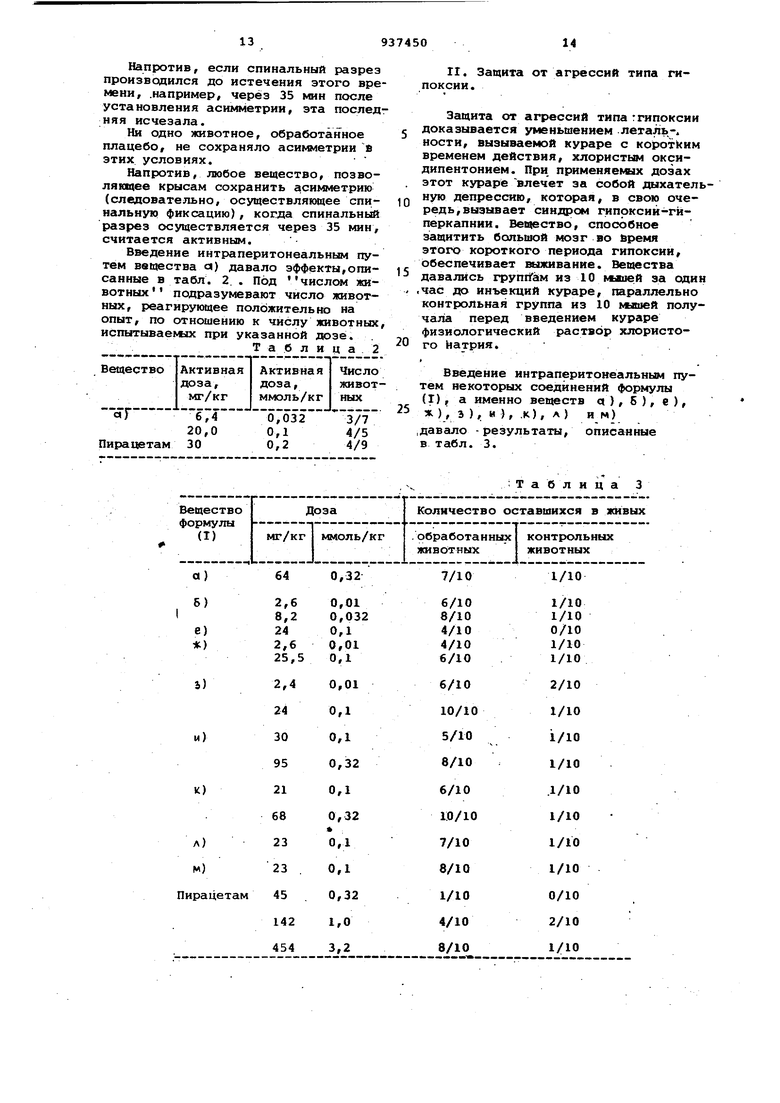
Введение интраперитонеальным путем некоторых соединений формулы (I), а именно веществ а), 5), е),
5 ж ), 3 ), и ), .к), А ) им) .давало -результаты, описанные в табл. 3.
Таблица 3







Авторы
Даты
1982-06-23—Публикация
1978-06-13—Подача