действующих на центральную нервную систему.. UbipOKO известно восстановление кето-групп до спиртовых по реакции Берга-Хюккеля действием щелочных металлов в жидком аммиаке в среде тетр гидрофурана П. Известен также способ восстановле ния двойных связей каталитическим гидрированием в присутствии катализатора - благородного металла, напри мер, палладия на угле при повышенном давлении С2, Цель изобретения - синтез новых соединений обладающих ценными свойствами, позволяющими использовать их в медицине. Поставленная цель достигается пре лагаемым способом получения соединений формулы (I), заключащимся в том что соединение общей формулы 7.-W где Rjf, 2 и W имеют указанны значения, восстанавливают, когда Q - О СС в результате реакции с щелочным металлом а жидком аммиаке или когда х« - HN./W Q представляет собой талитическим гидрированием в присутствии катализатора - благородного металла, с выделением целевого продукта в свободном виде или в виде соли. При испытании анальгезирующего действия на мш1ей с помощью горячей пластины к лапкам мышей прикладывают алюминиевую пластину толщиной 1/8 ( мм), являющуюся регулируемым ис точником тепла. Инфракрасный рефлектор 250 Вт помещают под алюминиевой пластиной. Терморегулятор в виде тер мистера, расположенного на поверхности пластины, регулирует нагрев лампы таким образом, чтобы поддерживать постоянную температуру пластины . Каждую мышь помещают в стеклян ный цилиндр 6l (155 мм) в диаметре, основанией которого служит алюминиевая пластина, и отсчет времени начинают с того момента, когда лапки мышей прикасаются к пластине. Спустя 0,5 и 2 ч после обработки тестовым соединением, наблюдают за первыми конвульсивными движениями одной или обеих задних лапок, или до установления интервала 10 с между этими движениями. Доза морфина составляет MPEj() ,5 мг/кг, МРЕ-МВЭ - максимально возможный эффект. При испытании анальгезирующего действия на мышей по взмахам их хвостов, используют регулируемую подачу интенсивного тепла на мышиный хвост. Каждую мышь помещают в удобно по; огнанный металлический так, чтобы ее хвост высовывался из одного конца цилиндра. Цилиндр устанавливают таким образом, чтобы хвост плоско лежал над экранированной лампой, являющейся источником тепла, В начале испытания удаляют алюминиевый.-экран над лампой, позволяя пучку света проходить через щель и фокусируя его на кончике хвоста. Одновременно включают таймер. Определяют время возникновения конвульсивного движения хвоста. Мыши, не подвергнувшиеся предварительной обработке, обычно реагируют спустя с после экспозиции света лампы. Максимальный срок для защиты составляет ТО с. Каждую мышь подвергают испытанию спустя 0,5 и 2ч после обработки морфином и тестовым соединением. Доза MOpdHiHa составляет MBSjo 3,2-5,6 мг/кг, При подавлении болевого синдрома, вызванного фенилбензохиноном, группы из 5 мышей предварительно обрабатывают путем подкожного или орального рведения с физиологическим pacтвopoм морфина, кодеина или тестового соединения. Спустя 20 мин (при подкожном введении) или 50 мин (при оральном введении), каждую группу подвергают внутрибркйиинной инъекции фенилбензохинона, который вызывает абдоминальные сокращения. Спустя 5 мин после инъекции возбудителя мышей наблюдают в течение 5 мин на предмет наличия или отсутствия конвульсивных сокращений. Определяют действие предварительно введенного препарата в дозе на подавление конвульсивных сокращений. Реузльтаты вышеописанных тестов выражают в процентах максимально возможного эффекта ( МВЭ). МВЭ для 5 каждой группы статистически ляют с % МВЭ контрольного и
5; URO Тестовое время - контрольное время Время отсечки - контрольное время
В приведенных ниже таблицах аналь Незирующая активность выражена в еди нТ1цах МВЭ т.е. доза, при которой в данном испытании достигают полови ны возможного максимального эффекта.
Предлагаемые соединения явлются активными анальгезирующими средствами как при оральном, так и при парентеральном введении, и их вводят обычно в составе композиций. Такие композиции включают фармацевтические носители, выбранные исходя из способа приема и на основании Общепринятой фармацевтической практики. Например, их можно вводить в виде таблеток, пилюль порошков или .гранул, содержащих такие добавки, как крахмал, молочный сахар, некоторые сорта глины и т.д.; в виде капсул в смеси с такими же или эквивалентными добавками, а также в виде суспензий, растворов, эмульсий, сиропов для орального введения и элекси ров, которые могут содержать отдушки и окрашивающие агенты. Для орального введения предлагаемых терапевтических агентов пригодны таблетки и капсулы, содержащие 0,01-100 мк. Доктор должен назначить наиболее подходящую для конкретного пациента дозу в зависимости от возраста, веса и восприимчивости больного и от способа приема. Обычно начальная анальгезирующая доза для взрослых находится в интервале 0,01-500 мг в день для разового приема (или разделенная на части). Во многих случаях нет необходимости превышать дозу 100 мг в день Наиболее подходящей является доза в пределах 0,01-300 мг/день, предпочтительно 0,10-50 мг/день. Наиболее подходящая доза при парентеральном вве.дений 0,01-100 мг/день, предпочтител IHO 0,01-20 мг/день. , С помощью описанных методой определены анальгезирующие-активности некоторых предлагаемых и известных ранее соединений. Возможность использования этих соединений в качестве препаратов, снижающих давление, определяют по их способности понижать, кровяное давление у крыс и собак, у которых оно было повышено искусственным способом, до остаточной величины при оральном
X 100,
введении препарата в указанных выше дозах.
Их активность в качестве транкфилизаторов демонстрируется при оральном введении крысам в дозах -0,0150 мг/кг по соответствующему снижению спонтанной моторной активности. Дневная доза для млекопитающих составляет 0,0t-100 мг.
Использование этих соединений при борьбе с глаукомой связано с их способностью снижать внутриглазное давление. Их действие на внутриглазное давление определяется по тестам на cor сопостав- тельно обработанного животного. % МВЭ предвари- вычисляете сяе ующим образом. баках Испытуемый препарат вводят в глаз собаки в виде раствора или вводят систематически в различные промежутки времени, после чего глаз анастезируют введением хлоргидрата тетрацина (t/2%, 2 капли). Спустя несколько |«1нут после местной анестезии, измеряют внутриглазное давление механическим тонометром Shlotz, а после введения флуореацинового красителя ручным тонометром-. Активность соединений в качестве диуретиков определяют на крысах. Применяют такие же дозы, как и для использования соединений в качестве анэльгезирующих средств. Пример 1. d,1-5,6,6а,7,10,10а-Гексагидро-1;-гидрокси-6и-метил-3-(2-гeптилoкcи)бeнзo-tcЗ-xинoлин-9(8И)-oн. Суспензии d,1-5,6,6 а,7-тетрагидро-1-гидрокси-6В-метил-3- (.2-гептилокси)бензо- с -хинолин-9(8Н)-она (1,0 г, 2,91 ммоль) в тетрагидрофуране (20 кш) по каплям добавляют через дополнительную воронку в интенсивно перемешиваемый раствор лития (0,1 г) в жидком аммиаке (75 мл, перегнанный через таблетки гидроокисей калия). Дополнительную воронку промывают тетрагидрофураном (10 мл). Смесь перемешивают в течение 10 мин, и затем твердый хлористый аммоний добавляют для уничтожения синего цвета. Избыточному количеству аммония дают возможность испариться, и остаток выгружают в -воду (100 мл и этилацетат i50 мл). Слой этилацетата выделяют, и водную фазу экстрагируют этилацетатом (2 X 50 мл). Соединенные экст- акты промывают соляным раствором, сушат (MgS04) и концентрируютпри пониженном давлении до получения коричневого полужидкого продукта (1,35 г). Тщательное растирание полу твердого продукта в смеси пентан/эфи (1:1) приводит к получению светлокоричневого твердого вещества (0,88 Т.ПЛ. 130-138 0. Указанную процедуру f гчрч lOA. .j f m ГЧ f4 ft tr f повторяют, используя 1,8 г (5,3б ммоль) бензо- с -хинолин-9 он реагента, 0,184 г лития, мл жидкого аммония и 5 мл тетрагидрофурана. Остаток (2,1 г), оставшийся после выпаривания аммония, растворяют в бензоле и вводят в хроматографическую колонку (3,8 X 61 см) с силикагелем (250 г). Колонку промывают объемом дегазированного бензола,равным объему колонки, и затем 1700 мл дегазированной смеси бензол/эфир (9:1). Продолжение элюирования (1100 мл) приводит к получению яркокрасного элюента, который концентрируют до светло-пурпурного твердого соединения (580 мг) при пониженном давлении и растирании в смеси бензол/эфир (1:1), и получают 370 мг твердого соединения; т.пл. 15 -15б°С Его хранят в атмосфере азота,в темноте. Выделенное вещество представля ет собой смесь цис- и транс-изомеров указанного соединения, т/е - (т) 1 И ЯМР (100 MHZ) {fTMC / н: 6,85 и 7.9 (1Н, перем. он;; 5,67, 5,71, 5,85,sTSTlfl, I 2HZ 2Н полн., аромаТичн. водороды в смеси цис/транс), 0,90 (т. ЗН, концевые СН); 1,12-i,43 (м. остальные Н). Пример 2. d,l-5,6,6a,7.10, 10а-Гексагидро-1-ацетокси-3-(2-гептилокси)бензоГс З-хинолин-9(8И)-он. Раствор d,1-5,6,6а,7-тетрагидро-1-окси-З-(2-гептилокси)бензо- нолин-9-(8И)-она (9,0 г) в тетрагидр фуране (100 мл) прикапывают к быстро перемешиваемому раствору лития (0,1 в жидком аммиаке (750 мл). Во время прикапывания добавляют дополнительно 0,1 г лития по частям для сохранения синего цвета. Смесь перемешивают в течение 10 мин и затем синий обесцве чивают, добавляя избыток хлористого аммония. Избыточному аммонию дают во можность испариться, а остаток помещают в смесь воды и этилацетата. Орг нический слой отделяют, и водную фаэу дважды экстрагируют этилацетатом, .Соединенные экстракты промывают водой, солевым раствором сушат (MgSO) и выпаривают до получения 8,5 г сырого продукта в виде коричневого твердого соединения. Неочищенный продукт (8,0 г) сусендируют а хлористом метилене (k8 MJ -.../%Ол « ч при и обрабатывают N N-диметил-ft-аминопиридиноМ {3,2k г) и триэтиламином (3,72 мл). Затем добавляют уксусный ангидрид (2,52 мл), и полученную смесь перемешивают в течение 30 мин при . Ее разбавляют хлористым метиленом (ЗОО мл) и выделяют слой хлористого метилена, промывают водой (3 X 150 мл), насыщенным бикарбонатом натрия (l X 100 мл), солевым раствором (1 X 100 мл) и сушат (МдЗОд). После выпаривания хлористого метилена получают 13,7 г темного масла, которое очищают на хроматографииеской колонке с силикагелем (50 г). Колонку промывают последовательно смесью эфир/гексан (1:1), эфир/гексан (2:1) и эфиром. Собирают фракции по 18 мл. Фракции 176-224 соединяют и концентрируют до масла, которое перекристаллизовывают из гексана и получают 3,24 г (32), выход указанного транс-изомера в виде кристаллов светло-желтого цвета; т.пл. 63,, т/е - 373/т . ИК-спектр (КВг): 5,82 (кето ); 5,75 (сложн. эфир ); 2,95 (НН)М, фракции 246-290 соединяют и концентрируют до получения 0,55 г (5%) сырого цис-изомера указанного соединения в виде масла. В дальнейшем его очищают на хроматографической колонке, как описано вьлие, и получают чистый цис-изомер в виде масла, т/е - 373 (т). ИК-спектр (СНС1з) : 5,82 (кето, ); 5,67 (сложн. эфир ); 2,92 (NH)M. Рассчитано, %: С 70,75; Н 8,37; N 3,75. Wi04N. Найдено, %: С 70,90; Н 8,54; N 3,69. d,lrфpaкции 225-245 соединяют и выпаривают до получения 2,69 г (26) смеси цис-транс-изомеров, которые выделяют по описанной методике. Из d, ,6,6а,7 тетрагидро-1-окси-З-(5-фенил-2-пентилокси)бензоtcjхинолин 8(8Н)-она таким же способом получают следующие соединения: 9Э d,l-TpaHC-5,6,6a,7,rO,10a l-reKcaгидро-1-ацетокси-З-(5 Фенил-2-пентилокси)бензо с -хинолин-9(8Н)-он в виде масла m/e - 421 (m). Рассчитано, %: С yt.OS; Н 7,«I; N 3,32. %НзР4. Найдено, %: С .Тб; Н 7,59; N 3,20... а,1-цис-5,6,6а.7,10,10а 5-гексагидро-1-ацетокси-3(5 Феиил-2-пентилокси)бензо- с -хинолин-9(8Н)-он в виде масла m/e - 21 (m).. Рассчитано, %: С 7,08; Н 7, ,N 3,32. - Ь З-Р4 Найдено, %: С 7,.Н 7, , N3,5. ё,-5,6,6а7-Тетрагидро-1-окси-6-о1-метил-3-( 5-фенил-2-пентил-окси 6енэо- с -хинояин-9(8Н)-он превращают в d,6-TpaHG-5,6,6afi,7,10,10ad.-reK сагидро-1-ацетокси-6с1-метио-3 С5-фенил-2-пентил-окси)6ензо- с -хинолин-9(8Н)-ониа ,б-цис-5,6,.6а/5,7,10,10аа -гексагк1Дро-1-ацетокси-6о1-метил-3-(5-фенил-2-пентилоксиj-бенэо-ГсЗ-хинолин-9 (8Н )-он. Изомерные продукты переводят в их соли хлористоводородной кислоты по способу, описанному в общей методике получения солей. Характеристики получения солеи приведены в табл. 1. П р и р 3. d,1-транс-5,6, fea|57,8,9,10,10а«С-Октагидро -1,9-диокси-6 метил-3(2-гептилокси)бензо- с -хинолин. Раствор 130 мг d,1-транс-5,6,6аji 7 8,9,10,10а о1-октагидро-1-ацетокси 9-гидрокси-бргметил-3-(2-гектилокси)бензо- с }-хинолина и k6 мг карбоната калия в 35 мл метанола перемешивают при комнатной температуре. Спустя 30 мин, реакционную смесь нейтрализуют уксусной кислотой и концентрируют при пониженном давлении. Остаток растворяют в эфире (100 мл), промывают последовательно водой (2x35 wn насыщенным раствором бикарбоната (1x3 мл), солевым раствором ( нп сушат (MgSO.) и концентрируют при пониженном давлении до получения Эб мг d,l-TpaHc-5,6,6a (Ь 7,8,9,10,10ас1-окта гидро-1,9-дегидрокси-6ргметил-3-(2-гептилокси)бензоСс}-хинолина в виде аморфного твердого состояния; т.пл. 80-100°С (с разложением). б10 m/e - (m) . В спектре ЯМР (СОСЦ, 60 МГц) отсутствует поглощение метила ацетатной группы и в ИК-спектре отсутствует поглощение карбонила сложного эфира. Аналогичным образом из соответствующих 1-ацетокси производных получают следующие соединения: djl-TpaHC -5,6,6а|5 7,8,9,1Р,10ас1-октагидро 1,9-дигидрокси-бЭ-метил-3-(5-фенил-2-пентилокси)бензо-Гс -хинолин. m/e - 395 (). После превращения в хлоргидрат получают порошок; т.пл. 15Ы56°С. ИК-спектр (КВг): 3,00; it,00;-(); 6,10 и 6,25 М. Аналогично d,С-транс-5,6,6ар,7, 10,10acff гeкcaгидpo-1-aцetoкcи-5 мeтил-6j -мeтил-3-(2-гeптилoкcи)бeнзo- c -xинoлин-9(8H)-oн гидролизуют до .0°властвующего 1-гидрокси-соединения; г.пл. 157-1бО°С. m/e - 359 (m). Рассчитано, %: С 73,50; Н 9,25; N 3,90. ОдН,3 Найдено, I: С 73,16; Н 9, . |N 3,85. Пример k. d,1-транс-5,6, 6а ( 7,10,10ас1.-Гексагидро-1-ацетокси-З(2-гептилокси)-5-бензоил-6 -метилбeнзo-tc -xинoлин-9(8H)-oн К перемешиваемому продукту d,-транс-5,6,6ар) , lOaol -гексагидро-1-ацетокси-6|Ь-метил-3-( 2-гептилокси) бензо-Сс -хинолин-Э(8Н)-ону (812 мг) в 2,5 мл пиридина добавляют мл хлористого бензоила в 5 мл хлороформа. Спустя 2 ч, реакционную смесь выливают на лед и дважды экстрагируют эфиром. Соединенные эфирные экстракты промывают водой, оикарбонатом натрия, сушат (MgSO) и фильтруют до получения после концентрирования И кристаллизации из смеси эфир/ /петролейный эфир d, -транс-5,6,6а(Ь 7 Ю, ЮзА-гексагидро-Т-ацетокси-.З-(2-гептилокси)5-бензоил-6б-метилбензо- с -хинолин-9(8Н)-он; т.пл. 108ПО С. m/e - 491 (m-). В результате повторения этой процедуры при использовании эквивалентных количеств хлористого ацетила вместо хлористого бензоила и соответствующего бензо- с -хинолина получают следующее соеди нени е: d,1-т ран с-5,6,6а р 7,10,10а(1-гексагидро-1-ацетокси-3-(2-гептилокси)-5-ацетил-6Эметилбвнзо-Сс1-хинолин-9(8Н)-он. m/e - 433 (m+). Пример 5. d,1 TpaHc-5,6,6a,ci. 7,10,10act-Гёкcaгидpo-laцeтoкcи-5-мeтил-6(i-мeтил-3(2-гeптилoкcи )бензо- с -хинолин-9(8Н)-он. К перемешиваемому раствору 38 м d, 1-транс-5,6,6a(i 7,10 IOadL-гексагид ро-1-ацетокси-6(5-метил (2-гептилокси)6ензо с -хинолин-9(8Н)-она в 3 мл ацетонитрила, охлажденному до , добавляют 0,5 мл формальде гида, а затем 100 мг цианоборгидрида Уксусную кислоту добавляют для поддержания рН до завершения реакции, НТО контролируют по исчезновению исходногО материала на тонкослойной x матограмме. Продукт выделяют следующим образом. К реакционной смеси добавляют вод и простой эфир, эфирный слой выделяют, а водный еще раз экстрагируют эфиром. Эфирные экстракты соединяют сушат и выпаривают до получения нужного, d ,В-транс-5 ,6,6afb 7,10, lOadL-гексагидро-1-ацетокси-5 метил-6)Ь-метил-3(2-гептилокси)-бензо- с -хи нолин-9(8Н)-она в виде масла. Н ЯМР (60 МГц, CDClij) демонстрирует характеристическое поглощение на 2,85 (ч/млн) для . Аналогичным образом получают из соответствующих реагентов следукяцие соединения: d, 1-транс-5 ,6,6а(Ь 7,10, ЮасАггекс гидро-1-ацетокси-5 метил-3 (гептилокси)бензо- с}-хинолин-9(8Н)-он в ви .де масла; d,TpaHc-5,6,6a(i 7,8,9,10,10adr -октагидро-1,9-Диацетокси-5 метил-6 5-метил-3- (2-гептилокси)бензо-Гс -хинолин в виде масла, т/е - i5 (TI Кроме того, аналогичным образом получают следуЮ1чие соединения (см. табл. 2) o-&-dH Н Б.,-W Рассчитано, %: С 69,19; Н 7,7; N 2,88. Найдено, %: С 68,72; Н 7,18; N 2,7. Рассчитано, I: С 7,80; Н 7,85; N 3,12. С,,. ts12 Найдено : С 7,66; Н 8,05; N 2,66. б9-75 С. Рассчитано, %: С 7, Н 7,64; N 3,22. 4l 3°4 Найдено, %: С 73,89; Н 7,51; N 3,. П р и м е р. 6. d ,l-TpaHC-5,6,.6a(i 7,8,9,10,10ао1-Октагидро-1,9-дигидроокси-5 этил-6|Ь-метил-3(2-гептилокси)бензо- с}-хинолин К раствору 100 мл литийалюминий- гидрида в 5 мл сухого тетрагидрофурана (охлажденного на бане лед/вода) по каплям добавляют раствор 90 мг d, 1-транс-5 ,6,6а1Ъ 7,3,9, Ю, Oad OKTaгидро-1,9-дигидрокси-5-ацетил-6ргметил- 3- (2-гептилокси)бензо-Сс -хинолина в 3 мл тетрагидрофурана. После этого реакционную смесь нагревают и кипятят с обратным холодильником в течение 1 ч и затем да.ют остыть до комнатной температуры. Добавляют эквивалентные количества воды с последуюЩим добавлением 3 н.-гидроокиси калия, получившийся осадок отфильтровывают, и фильтрат концентрируют в вакууме до получения нужного М-этилпроизводного в виде масла, т/е - 375 (п-). Прим ер 7. с ,Е-транс-5,6,6а В 7,10,10а 1 Гексагидро-1-ацетокси-6-изобутирил-3-(5 Фенил-2-пентилокси)бензо- с -хинолин-9(8Н)-он Раствор хлористого изобутирила (IT мг; 1,07 ммоль ) в хлороформе (20 мл ) постепенно добавляют при перемешивании к раствору сЗ ,2-транс-5,6,6afi 7,10,1 Оа{)1 гексагидро-1-пцетокси-3 -()енил-2-пентилокси) бензо- с -хинолин-9(ВН)-она (50 мг; 1,07 ммоль)j te сухом пиридине (1,5 мл) при и в атмосфере азота. Реакционную смесь перемешивают в течение 5 ч и затем выливают в смесь лед/вода (50 мл). Слой хлороформа выделяют в водную фазу, экстрагируют хлороформом (2.x 20 мл). Экстракты хлороформа соединяют и промывают 10%-ной соляной кислотой (2 X 10 мл), затем солевым раствором (1 X 10 мл) и затем сушат (MgSO). После концентрирования хлороформового раствора в вакууме получают желтое масло, которое при стоянии отверждается. Растирание твердого продукта с гексаном дает белое кристаллическое вещество, которое выделяют фильтрованием и сушат С+ОО мг); т.пл. 128-129С. Концентрирование фильтрата гексана дает 121 мг масла. Пример 8. d, 1-транс-5,6,6a|i 7,8,9,10,1 ОаА-Октагидро-1,9|5-ДИацетокси-5 изобутирил-3(5 фенил-пен тилокси)бензо- сЗ-хинолин В атмосфере азота раствор d,l-транс-5,6,6а(Ь 7,8,9, Ю, 10ad-oктaгид po 1-aцeтoкcи-9|i-гидpoкcи-5-изoбyтиpил-3 (5 фенил-2-пентилокси)бензо-1с}-хинолина (213 мг; 0,32 ммоль) и тетрагидрофуране (5 мл) добавляют к взвеси литийалюминийгидрида (100 м 2,6 ммоль) в тетрагидрофуране (5 мл) при комнатной температуре. Смесь перемешивают в течение ночи и затем добавляют воду (0,1 мл), 15%-ный рас вор гидроокиси натрия (0,1 мл) и воДУ (0,3 мл). Затем его отфильтровыва ют в атмосфере азота, и оставшийся фильтрат промывают тетрагидрофураиом (2x5 мл). Соединенный фильтрат и промывочный раствор концентрируют до красноватого масла (0,17 г). Масло растворяют в атмосфере азота в пиридине (1 мл), и полученный раствор ох лаждают до 0°С. Добавляют уксусный ангидрид (1 мл) при перемешивании к пиридиновому раствору, и реакционную смесь перемешивают в течение 30 мин при 0°С. Затем ее выливают в воду (25 мл) и экстрагируют этилацет том (3 X 25 мл), Экстракты соединяшат (MgSO) и концентрируют до корич невого масла (18 мг). Масло быстро промывают аЗотом и хроматографируют на силикагеле (40 г), используя в ка честве элюирующего растворителя смес бензол/зфир (6:1). Собирают фракции по 10 мл каждая. Фракции 2-10 соединяют и концентрируют до масла (109 мг). т/е .- 521 (гп). Рассчитано, :ё: С 73,67; Н 8,31; N2,68. %: С 7+,33; Н 8,89; Найдено, N2,23. лТМС ян ЯРМ (60 МГц)с1зсе,,Ч/млн: 7,22 с. 5Н, аромэтика); 6,05 (д.1И, аро.матика); 5,90 (д, 1Н, ароматика); ,90 (бс. 1Н); i,30 (бс., 1Н); 3,10 (д, 2Н, N-CH/i), 2,90(д, 2Н, N-CH,j); 2,7fl (бс, 2Н); гМ и 2,15 (с. 6Н. 2-СНо -СОО); 1,85 (бс, 211. Н и Hg); ); 1,05 (д, бН,- ); 1,0-3.0 (lepeM. , остальные протоны;. , . Пример 9. d, 1-транс-5 6,6а| 7,10,10а1-Гексагидро-1-окси-5-аце961 тил-6|Ь-метил-9-метилен-3 (2-гептилокси)бензо-Гс -хинолин Триметилфенилфосфонийбромид ( мг; 2,12 ммоль) добавляют к раствору гидрида натрия (0,95 г; 2,0 ммоль) в диметилсульфоксиде (50 мл) при . Затем реакционную смесь нагревают при 70 С в течение 3 ч, после чего добавляют d,l-TpaHC-5,6,6а|Ь 7,10, ЮаоС-гексагидро-Т-ацетокси-5-ацетил-6(5-метил-3(2-гептилокси)бензо-Сс -хинолин-9(8И)-он (0,858 г; 2,0 ммоль) в диметилсульфоксиде (,50 мл). Реакционную смесь нагревают при в течение ночи, затем охлаждают и выливают в смесь льда и воды, содержащей бикарбонат натрия (12,5 г). Водную смесь экстрагируют бензолом, сушат () и выпаривают при пониженном давлении до полученно- , го сырого продукта. Его очищают на хроматографической колонке с силикагелем, используя смесь гексан/бензол (1:1). Пример 10. d, -TpaHc-5,6,6afi 7,8,9,10,1 Oacl-Октагидро- 1-oкcи-5-этил-9 гидpoкcимeтил-6|i-мeтил-3 (2-гептилокси)бензо- с -хинолин К раствору d, 1-транс-5,6,6а 5 7,10,10асА-гексагидро-1-окси-5-ацетил-6(У-метил-9-метилен-3- (2-гептилокси )бензо-Гс -хинолина (0,855 г; 2 ммоль) в тетрагидрофуране (30 мл) при 0°С добавляют по каплям 1М раствор диборана в тетрагидрофуране (комплекс боран-тетрагидрофуран) (6 мл). После добавления реакционную смесь выдерживают при комнатной температуре в течение 30 мин, а затем обрабатывают водой для разложения избытка гидрида. Затем реакционную смесь нагревают до на водяной бане и добавляют 3-гидроокись натрия (3 мл), а затем по каплям добавляют перекись водорода (З мл). После добавления смесь выдерживают при комнатной температуре в течение 1 ч, добавляют карбонат калия (1,5 г) и выделяют тетрегидрофурановый слой. Водную фазу экстрагируют тетрагидрофураном (Зх 10 мл), экстракты соединяют, сушат (MgSO) и концентрируют до получения продукта. Продукт очищают с помощью хроматографической колонки с 1силикагелем, используя в качестве элюента смесь эфир/гексан. Пример 11. d, 1-5,6,6a,7-Teтpaги дро- 1 - (|-морфолинобути рил15окси)-60-метил-3(2-гептилокси)6ен f / Л I зо-Сс}-хинолин-9(8Н)-он К раствору d,1-5,6,6а,7-тетрагидро-1-окси-6&-метил 3-(2-гептилркси) бензо-Сс -хинолин-9(8Н)-она (0,51 г; 1,5 ммоль) в сухом метиленхлориде (25 мл) добавляют хлоргидрат -морфо лин-масляной кислоты (0,315 г; 1,5 ммоль), и полученную смесь перемешивают при комнатной температуре в атмосфере азота. 0,1 М раствор дециклогексилкарбодиимида в хлористом метилене (12,5 мл; 1,5 ммоль) добавляют по каплям, и смесь перемешиваЮТ в дечение ч. Затем ее фильтруют и выпаривают до получения указанного продукта, который очищают далее хроматографией на колонке с силикагелем. П р и м е р 12. d,l-TpaHc-5,6,6a 7,8,9,10,10а(1 Октагидро-1-( -пиперидилбутирилокси)-9 окси-6р|-метил 3(5 фенил-2-пентилокси)бензо- сЗ-х нолина хлоргидрат К раствору при 25°С d,-TpaHc-5,6,6ар1-7,8,9,10,10ас1гоктагидро 1,9 диокси-6рг-метил-3- (З-фенил-2-пентилокси)бензо- с -хинолина (1,0 2,53 ммоль) в хлористом метилене (20 мл) добавляют хлоргидрат 4-Н-пиперидилмасляной кислоты (0,52 г, 2,53 ммоль) и дициклогексилкарбодиимид (0,373 г, 2,78 ммоль). Реакционную смесь перемешивают при 25°С в течение 6 ч затем охлаждают в течение 12 ч и фильтруют. Выпаривание фильтрата и растирание остатка с про тым эфиром дает 1,3 г твердой соли монохлоргидрата. ИК-спектр (КВг): 2,95; 3,60; 5,б5 сложный эфир, ); 6,13 и 6,27 М. Препаративная тонкослойная хроматография части твердого соединения на си лика геле 0,5 мм и метанол/метилендихлориде в качестве элюента дает свободное осно вание -транс-5,6,,9,10,1Oad-O тагидро-1-(4-Н-пипериди/йутирилокси)-Э-окси-б1 -метил-3(5 фенил-2-пен тияокси)бензо- с -хинолин. 1Н ЯМР (60 МГц) ч/млн: 1,12 (д.2 7HZ, С-3 метил боковой цепи); 1,25 (д, 1 6,HZ 0-6 метил); 5,84 (с, два АгН) и 7,16 (с, 5Н). После обработки свободного основа ния избытком хлористого водорода в простом эфире получают дихлоргидрат в виде гигроскопического порошка. i6 Пример 13-d ,е-5,6,6а,7-Тетрагидро-1-(-пиперидилбутирилокси)6 -метил-3( 5 фенил-2-пеитилокси бен|0- с -хинолин-9(8Н)-он При 25С к раствору d, f-5,6,6a,7-тeтpaгидpo-1-гидpoкcи-6-мeтил-3- (5-фенил-2-пентилокси)бензо-СсЗ-хинолин-9(8н)-она (550 мл; T+l ммоль) в хлористом метилене (2б мл) добавляют хлоргидрат -N-пиперидил-масляную кислоту (291 мг; 1,1 ммоль) и дициклогексилкарбодиимид (3,19 мг; 1,55 мкюль). Реакционную смесь перемешивают в течение 18ч, затем охлаждают до 0°С и отфильтровывают. После выпаривания фильтрата и тщательного растирания остатка с получают 800 мг d, 1-5 ,6,6a,7-тeтpaгидpo-1-(t-N-пиперидилбутирилокси)-6(i-мeтил-3-(5-фенил-2-пентилокси)бензо- с -хинолин-9(8Н)-она хлоргидрат в виде гигроскопического желтого продукта. ИК-спектр (СНС1з): 2,92; k,k IHN); 5,69 (ел. эфир), 6,00, 6,20 и 6,(О М. Аналогичным образом хлоргидрат d,1-т ранс-5,6,6а,7,8,9,10,1Oad-октагидро-1-r 14-М-морфолинобутирилокси)-9-окси-6 -метил-3(5 Фенил-2-пентилокси)бензо- с -хинолина получают из 4-Н-морфолиномас}1яной кислоты и d,l-TpaHC-5,6,6a(b7,8,9,10,10aoloKTaгидро-1,9 дигидрокси-6р)-метил-3 (5 -фенил-2-пентилокси)бензо- с J-хинолина. ИК-спектр (КВг): 3,00; 3,75; 5,б7 (ел, эфир, ); 6,15 и 6,30 М. Пример U.d ,Р-7,10-Дигидро-1-окси-3-(2-гептилокси)-6-метилбензо- с -хинолин-9(ВН )-она этиленкеталь Раствор d,,10-дигидро-1-окси-3(2-гептилокси)бензо- с -хинолин-9(.8Н)-он-этилен-кеталь (371 мг; 1,0 ммоль) в эфире (50 мл) медленно добавляют к ледяному (охлажденному до температуры льда ) раствору метиллития (kk мг; 2,0 ммоль) в эфире (25 мл). Полученное таким образом 5-литий-6-метил-производное растворяют в простом эфире и обрабатывают сухим кислородом до получения после фильтрования и выпаривания растворителя указанного соединения. Пример 15. Общий способ получения солей хлористоводородной кислоты.Избыток хлористого водорода пропускают через раствор соответствующего бензо-Сс -хинолина формул (Т) или (II), а полученный осадок выделяют и перекристаллизовывают из соответствующего растворителя, например смеси метанол/простой эфир ). Таким образом получают следующую сол d ,е-транс-5,6,6а|Ь7,8,9,10,10а -октагидро-1-ацетокси-9|1-гидрокси-6Э-метил-3(5 Фенил-2-пентилокси)бензо- с -хинолин; т.пл. 191-193°С,
We - 37 (m).
Рассчитано, %: С 68,8; Н 7,70; N 2,89.
Найдено, %: G 68,it2; Н 7,66;
N 2,96.
Получение исходных соединений.
2-Бром-5 фенилпентан.
К пятибромистому фосфору, .полученному добавлением бромида (9,0 г) в хлористом метилене (10 мл) к трехбромистому фосфору (15,0 г) в хлористом метилене (15 мл) при 0°С, добавляют 5-фенил-2-пентанол (812 г) в хлристом метилене при . Полученную смесь перемешивают в течение 2,5 ч при 0°С, и затем дают ей возможность нагреться до комнатной температуры. Добавляют 50 мл воды, смесь перемеимвают в течение 1 ч и выделяют слой хлористого метилена. Экстрагирование повторяют, и соединенные экстракты промывают водой, насьчденным раствором бикарбоната натрия, рассолом и сушат над сульфатом магния. Сконцент рированные и высушенные экстракты дают 12, г указанного продукта в виде светло-желтого масла.
flHP:(.(j ,1 ,6 (д, 3, метил,
7HZ); 1,6-2,0 (М, 4, э-тилен ; СОСЦ 2,3-3,0 (д. Т, 2 бензильный метилен); 3,,2 (М, 1, метил); 6,, (М, 5, ароматика).
2-(3,5 Диметоксифенил)-5-фенилпентан..
Раствор 1-бромпропилбёнзола (51,7 г) в эфире ( мл) добавляют по каплям в течение 2 ч к смеси, кипящей с обратным холодильником, магния (7,32 г) в эфире (78 мл). Реакционную смесь кипятят с обратным холодильником еще 30 мин, а зётем прикапывают раствор 3,5-Диметокси-ацетофенона (50 г) в простом эфире (78 мл и кипятят с обратным холодильником в течение 1,5 ч. Реакцию останавливают, добавляя насыщенный хлористый аммоний (23 мл) , выделяют эфирный
слой, и водную фазу экстрагируют простым эфиром (3 X 200 мл). Соединенные эфирные экстракты сушат над сульфатом магния и концентрируют в вакууме до получения 81 Г. масла, 0 г масла гидрируют в смеси, содержащей этанол (300 мл), концентрированную соляную кислоту (2 мл ) и 5%-ный палладий на угле (,5 г). Катализатор отфильтровывают и этанол удаляют под вакуум. Остаток перегоняют в вакууме, в результате чего получают 28 г 2-(3,5-Диметоксифенил)-5-фенилпентан; т.кип. при 0,125 мм рт.ст. 15 -159°С.
ЯМР:(,25 (д, 3, СНз); 1,3-2,1
(М, ,этилен); 2,2-2,9 (М, 3 бензильный метилен); 3,+5 (5S, метокси) ; 6,2-6,7 (М, S3, ароматика); 7,2 (55, ароматика).
2-(3,5-Диоксифенил)-5-фенилпентон.
Смесь 2-(3,5-Диметоксипентил)-5 фенилпентан (22 г) и хлоргидрида пиридина (9 г) в атмосфере азота наг гревают до в течение 2 ч при интенсивном перемешивании. Реакционную смесь охлаждают, растворяют а 6 и соляной кислоте (200 мл) и разбавляют водой до 600 мл. Водный раствор экстрагируют этилацетатом CtxIOO мл), экстракты этилацетата сушат над сульфатом натрия и концентрируют в вакууме до получения 24 г неочищенного продукта. Полученный продукт очищают хроматографически на силикагеле до получения 19,2 г 2-(3,5-Дигидpoкcифeнил)-5-фeнилпeнтaнa в виде масла.
,1 (д, 3,о1- метил);
1,35-1,65 (М, V, этилен); 2,2-2,8 (М, 3, бензильный метилен, метинил); 6,1-6,5 (М, 3, ароматика); 6,65 (бд, 52, гидроксид); 7-7,+ (М, 5, ароматика) .
В соответствии с известными методиками получают перечисленные ниже соединения путем замещения соответствующего 1-бромпропилбензола на 1-бромалкилбеизол.
2-(3,5-Диоксифенил)-6-фенилгексан:
,1 .(д, 3, метил,Э 7 CPS)-,
1,0-1,9 (М, 6 (CH,i)CH)s-CHCCHj)-Ar), 2,2-2,8 (М, 3, бензильный метилен, метинил); 6,0 (б.д. 2,-фенольный ОН); 19 .9 6,2-6,4 (М, 3, ароматика); 7,1-7, (М, 5, ароматика). , гидроксифени л)-2-фенилэтан-; т.пл. 7б-77С. 27(З,5-Дигидроксифенил- -фенилбутан)-масло. flHP:Cr™Jgl-1,25 (д, метил); 1,5 2,0 (М, 2, метилен); 2,15-2,7 (М, 3, бензильный метилен, метинил); 6,3 (с, 3, ароматика); 6,85 (С, 2, гидрокси-Д О перекрыв); 7,1 (С, 5, ароматика) . 1 (3,5-Диоксифенил)-2-метил- -фенилбутанРаствор п бутиллития (29 мл; 2, 2М) добавляют по каплям к 3,5-ДиметоксибензилтрифосЛонийбромиду (31,5 г в тетрагидрофуране (200 мл) при пере мешивании, и полученный темно-крас ный раствор перемешивают в течение получаса. Бензилацетон (9, г) добав ляют по каплям, и реакционную смесь перемешивают в течение 12 ч. Затем е доводят до рН 7, добавляя уксусную кислоту и концентрируя ее при пониже ном давлении. Остаток экстрагируют хлористым метиленом, и экстракт выпаривают до получения сырого 1-(3,5-диметоксифенил )-2-мeтил-4-фeнил-1бyтeн в виде масла. Его очищают хроматогра(|ически на сияикагеле (00 г) и элюируют бензолом. Выход: 10 г в виде масла. ,flMP:crJ Jf;(,95 (С, 3), 2,3-3,1 (М, k}; 3,8 (С, 6); 6,15, 6,6 (М, 3); 7,1-7,5 (М, 6). 1(3,5-Диметоксифенил)-2-метил- -фанил-1-бутен (Э, г), полученный таким образом, растворяют в этаноле (250 мл) и подвергают каталитическом гидрированию при {5 пси (3,16 атм) в присутствии палладия на угле (1 г, 10%) и концентрированной соляной кис лоты (1 мл). Выход 9, г 1-(3,5-диметоксифенил)-2-метил- -фенилбутана в виде масла. ЯМР: 0,9 (д); 3,1-35-1,95 (М, З); 2,2-2,9 (М, М; 3,75 (С, 6); 6,35 (с, З); 7,25 (с, 5). Его демитилирую в соответствии с известной методикой до получения 1-(3,5-ДИoкcифeнил) -2-мeтил- -фeнилбyтaнa. 3,5-Диметоксибензилтрифенилфосфонийбромид получают при кипячении с о ратным холодильником смеси 3,5-димет оксибензилбромида (12 г) и трифенил6фосфина (1,2 г), в ацетонитриле (200 мл) в течение 1 ч. Затем реакционную смесь охлаждают, кристаллический продукт выделяют фильтрованием, промывают простым эфиром и сушат (20 г); т.пл. 2б9-270°С. 2-Метил-2-(3.5-Диоксифенил)-5-фенилпентан. К раствору Гриньяровского реагента, полученному из 2-фенилбромэтана (5,5 г), магния (0,8 г) и сухого простого эфира (60 мл), добавляют раствор 2-метил-2-(3,5 диметоксифенил)пропионитрила (2,75 г) в сухом эфире (20 мл). Эфир отгоняют и заменяют сухим бензолом (50 мл), и полученную смесь кипятят с обратным холодильником в течение 48 ч. Затем ее разлагают , осторожно обрабатывая разбавленной серной кислотой, и нагревают на паровой бане в течение 1 ч. Затем смесь экстрагируют простым эфиром, экстракт сушат (N9804) и концентрируют до масла. После дистилляции в вакууме получают 2-метил-2-(3,5-ДИмeтoкcи(})eнил)-5-фeнил-3-пeнтaнoн; т.кип. 168°С (0,2 мм рт.ст.). Выход 2,32 г, 60. Полученный таким образом пентанон (58 г) растворяют в этаноле (k(lQ мл) и обрабатывают боргидридом натрия (10 г) при комнатной температуре. Реакционную смесь перемешивают в течение 12 ч, затем охлаждают и нейтрализуют 6 н. соляной кислотой. Этанол удаляют при пониженном давлении и остаток экстрагируют простым эфиром. Затем экстракт сушат (N9804) и концентрируют до получения 2-метил-2-С395 Диметоксифенил)-5-фенил-3 пен- танола в виде масла. Выход 52 г, 16 г пентанола помещают в эфир (100 мл) и подвергают взаимодействию с порошком калия (2,5 г) в эфире (200 мл). Добавляют сероуглерод (эквимолярное по отношению к калию количество) , и полученную смесь перемешивают в течение получаса. Затем добавляют метилиодид (9,0 г), и реакционную смесь перемешивают в течение 6 ч. Полученную суспензию фильтруют, фильтрат концентрируют при пониженном давлении. Остаток помещают в этанол (150 мл), добавляют никель Ренея (25 г), и смесь кипятят в течение 18 ч. После выпаривания спирта и перегонки остатка получают 2-метил-2 (3,5-диметоксифенил)-3-фенил-3-пентен. Производное пентена подвергают каталитическому гидрированию в соответствии с известной методикой, и полученный 2-нетил-2-(3,5-Диметоксифенил) -5 фенип-3 пентан диметилируют до получения нужного продукта. 3,5-Дибензилоксиаиетофенон. За промежуток времени 1,5 ч метиллитий (531 мл; 2М раствора 1,0б моль) добавляют в атмосфере азота к быстро перемешиваемому раствору 3,5-Дибензилоксибензойной кислоты (175 г; 0,532 М) в простом эфире 250 мл тетраги дрофу ране (1400 мл) при 15-20 После дополнительного перемешивания в течение 0,75 ч при 10-15°С медленно добавляют воду, поддерживая реак.ционную температуру ниже 2°С. Водньй слой выделяют и экстрагируют простым эфиром (3 X 250 мл). Органические-фазы соединяют, промывают насыщенным раствором хлористого натрия («хЗОО мл сушат над сульфатом натрия и концентрируют в вакууме до получения масла, которое медленно кристализуют из изопропилового эфира. Сырой продукт пере кристаллизовывают из смеси эфир/гексан до получения 10,7 г (59) нужног продукта, т,пл, 59-б1°С. Этил-3(3,5-дибензилоксифенил)-про тонет (реакция Виттига). Смесь 3,5-дибензилоксиацетофенона (3,2 г; 0,13 моль) и карбэтоксиметилентрифенилфосфорана (90,5 г; 0,2б моль) нагревают в атмосфере азота при 170°С в течение И ч. Прозрачный расплав охлаждают до комнатной температуры, тщательно растирают с простым эфиром,и осадок трифенилфосфиноксида удаляют фильтрованием. Фильтрат концентрируют под вакуумом до маслянистого остатка, который хроматографируют на силикагеле U500 г) и элюируют смесью бензол/гексан, раст ворами с увеличивающейся концентрацией бензола, начиная с +0:60, и кончая то бензолом. Концентрирование со ртветствую1Дих фракций дает маслянис|гый остаток, который кристаллизуют из гексана. Выход 40,2 г (77%); т.пл. 73-75°С... %: С 77,58; Н 6,61; Рассчитано, С 77,72; Н 6,60. Найдено, : Аналогичным образом получают этил З(3,5-диметоксифенил)кротонат из 3,5-диметоксиацетофенона (51,7 г) и карбэтоксиметилентрифенилфосфорана (200 г). Выход 61,8 г (86), т.кип. 1 6-1б2°С при 0,3 мм рт.ст. 3(3,5-Дибензилоксифенил)-1-бутанол. Раствор этил-3-(3 5-дибензилоксифенил)кротонат (2,1 г; 60 мл) в простом эфире (250 мл) добавляют к смеси литийалюминийгидрида (3, г; 90 мл) и эфира (250 мл). Добавляют (0,18 г; 1,35 нл) хлористого алюминия, и смесь кипятят с обратным холодильником в течение 12 ч, а затем охлаждают. Затем последовательно добавляют к реакционной смеси воду (3, мл), гидроокись натрия (3, мл, 6 н.) и воду (10 мл). Выпадакндие в осадок неорганические соли отфильтроа фильтрат затем концентривываютруют в вакууме до получения нужного в виде масла 2,Ц г (98%). R спирта 0,25 (силикагель, бензол (18): этилацетат (1)). frt/e - Зб2 (т) . Рассчитано, %: С 79,53; Н 7,23 WWi Найдено, %: С 79,37; Н 7,11. Аналогичным образом этил-3-(3,5-диметоксифенил)кротонат (60, г) восстанавливают до 3-(3,5 диметоксифенил) бутанола (,0.г, 90%). 3-(3,5-Дибензилоксифенил)бутил-тозилат. Хлористый тозил (11,1 г; 58,1 мл) добавляют к раствору 3-(3,5-дибензилоксифенил)-1-бутанола (20,7 г; 57 мл) в пиридине (90 мл) при . Реакционную смесь выдерживают при в течение 18ч, затем разбавляют холодной 2 н. соляной кислотой (1500 мл) и экстрагируют эфиром (5x250 мл). Соединенные экстракты промывают насыщенным раствором хлористого натрия (4x250 мл) и затем сушат (Na(),после концентрирования высушенного экстракта получают продукт в виде масла. Его кристаллизуют, обрабатывая смесью эфир/гексан. Выход: 24,63 г (84%). Рассчитано, %: С 72,06; Н 6,24. W5 айдено, %: С 72,05; Н 6,29. Наиде 3 (. 3,5-Дибензилоксифенил) -1-феноксибутан.. Раствор фенола (4,5б г; 48,6 мл) в диметилформамиде (40 мл) добавляют в атмосфере азота к суспензии гидри|Да натрия (2,32 г; 48,6 мл, 5Р%-ного предварительно промытого пентаном) в диметилформамиде (70 мл)при 60°С,. Ре.акционную смесь перемешивают в течение часа при бО-уО С, после чего добавляют раствор ,5 ДИбензилоксифенил)-бутилтоэилата (23,93 г; 46,3 мл) 8 диметилформамиде (ОО мл). Реакционную смесь перемешивают при в течение получаса затем охлаждают до комнатной температуры, разбавляют холодной водой (2500 мл) и экстрагируют эфиром (4х400 мл). Соединенные экстракты Про мывают последовательно холодной 2 н. соляной кислотой (2x30 мл) и насыщенным раствором хлористого натрия (3x300 мл), затем сушат () .После удаления растворителя при пониженном давлении получают продукт в виде масла. Масляный остаток растворяют в бензоле и фильтруют через силика гель. (100 г). После концентрирования фильтрата при пониженном давлении получают продукт в виде масла. Выход: И,86 г (73), R 0,7 (силикагель, бензол), т/е - 438 () Рассчитано, %: С 82,16;,Н 6,Найдено, %: С 82,07; Н 6,. 3(3,5-Диоксифенил)-Т-феноксибутан. Раствор 3(3,5 дибензилоксифенил)-1-феноксибутана (,7 г; 133,5 мл) в смеси этилацетат (110 мл), этанол (100 мл) и концентрированную соляную кислоту (0,7 мл) гидрируют в течение 2 ч .при давлении водорода 60 пси (,2 атм) в присутствии 10 -ного палладия на угле (1,5 г). После удаления катализатора фильтрованием и концентрирования фильтрата получают масло. Масло подвергают хроматографической очистке на силикагеле (100 г) и элюируют смесью бензол/этилацетат, содержащей 0-10 этилацетата. Промежуточные фракции соединяют и концентрируют до получения указанного продукта. Выход: 7,8 г (80) в виде масла R 0,25 (силикагель, бензол (4): метанол (1)), т/е - 258 (П1+). Рассчитано, %: С 7,39; Н 7,02. д , Найдено, t: С 7, 13; Н 7,00. 1- Бром-3-(3,5-диметоксифенил)бутан. Раствор трехбромистого фосфора (5,7 мл; 0,06 моль) в эфире (30 мл) добавляют к раствору 3-( 3,5-диметокси фенил)-1-бутанола (30,0 г; 0, моль в эфире (20 мл) при температуре 5 С до , и реакционную смесь пе96 ремешиаают в течение 2,5 ч. Затем ее нагревают до комнатной температуры и перемешивают дополнительно 30 миИ. Смесь выливают на лед (200 г), и полученную смесь экстрагируют эфиром 3x50 мл). Соединенные экстракты промывают 5%-ным раствором гидроокиси натрия (3x50 мл), насыщенным раствором хлористого натрия (1x50 мл) и сушат (NanSO). После удаления эфира и вакуумной перегонки остатка получают указанный продукт. Выход: 25 г (55); т.кип. 125-132С (О , 4 мм рт. ст.). -(3,5-Диоксифенил)-1-(4-пиридилпентан). Смесь 3-(З ,5-Диметоксифенил)бутилтрифенилфосфонийбромида (19.0 г; 35, ммоль) в диметилсульфоксиде (50 мл) добавляют к А-пиридинкарбоксальдегиду (3,79 г; 35,4 ммоль) в тет рагидрофуране (40 мл) . Полученную смесь добавляют затем по каплям к взвеси 50%-ного гидрида натрия (1,87 г; 39 ммоль) в тетрагидрофуране (20 мл) в атмосфере азота при , а затем концентрируют при пониженном давлении. Концентрат разбавляют водой (200 мл), а затем подкисляют 6 и. НС1, Водный раствор кислоты экстрагируют бензолом (4x50 мл). Затем его превращают в основной и экстрагируют этилацетатом (3x50 мл). После выпаривания соединенных экстрактов получают после сушки (МдЗОф) -(3 5 Димeтoкcифeнил)-1-(-пиpидил)-1-пeнтaн (7,1 г; 70) в виде масла. После каталитического гидрирования полученного таким образом производного пентана по известному способу получают 4-(3,5-Диметоксифенил)-1-(4-пиридил/пентан с количественным выходом; т.пл. . Полученное таким образом производное пентана деметилируют, нагревая смесь соединения (7,15 г; 25 ммоль) и хлоргидрат пиридина (35 г) в атмосфере азота при в течение 8 ч. Горячую смесь выливают в воду (АО мл) и полученный раствор делают основным за счет добавления 6 н. гидроокиси натрия. Воду и пиридин удаляют перегонкой в вакууме. К остатку добавляют этанол (50 мл) и отфильтровывают неорганическую соль, выпавшую в осадок. Фильтрат концентрируют в вакууме, и полученный остаток хроматографируют на силикагеле (150 г), используя в качестве элюирующего агента этанол (бензол) I л), этанол (бензол) (1 л). Продукт выделя ют в виде стеклообразного твердого вещества при концентрировании соответствующиX фракций элюата. Выход 5,0 г (78%). 3-(3,5-Диметоксифенил)бутилтрифенилфосфонийбромид получают при кипячении с обратным холодильником смеси 1-бром-3-(3,5-ДИметоксифенил)б тана (21,5 г; 78,5 ммоль) и трифенил х1)осфина (20,5 г; 78,5 ммоль) в (60 мл) в течение 18 ч. Затем реакционную смесь охлаждают до .комнатной температуры и фильтруют. Оставшийся фильтрат промывают эфиром и сушат в вакуумном эксикаторе, после чего получают Зб,4 г (86%) продукта; т.пл. 190-200 С. 3,5 Диметокси-с1-метилстиролоксид. К раствору диметилсульфоксонийметилиду (69,4 мл) в диметиле сульфоксиде (65 мл) при комнатной температуре добавляют твердый 3,5-Диметоксиацетофенон (10 г; 55,5 мл). Реакционную смесь перемешивают в течение одного часа при 25°С, в течение получаса при и затем охлаждают. Смесь разбавляют водой (50 мл) и добавляют к смеси: ледяная вода (200 мл) - эфир (250 мл) - низкокипящий петролейный эфир (25 мл). Органический экстракт дважды промывают водой (250 мл), сушат (.) и выпаривают до масла. 1осле фракционной перегонки масла получают 8,0 г (75%) 3,5-диметокси -d-метилстнрол-оксида; т.кип. (0,2 мм. рт.ст.). ИК-спекто (СС14): 2780; 1595; 1196; 1151; 1058. УФ-спектр ( этанол): -гпах 279 нм , ( 2068). т/е - 19 (т).. ЯМР (CDC1) (60 МГц); сЛ 1,70 (С, NN3-); 2,76 (д, I 6 Гц, а Н); 2,95 (д, I 6 Гц, & Н); 3,81 (с, СН зО-); 6,41 (т, Гц, АгН) и 6,58 (д, I 2 Гц, АгН). Рассчитано, %: С 68,П2; Н 7,27. 4 3Найдено, %: С 67,96; Н 7,28. 2-(3,5-Диметоксифенил)-2-гидроксипропил-2-фенилэтиловый простой эфир. Смесь сухого 2-фенилэтанола (30 мл 251 мг) и металлический натрий (690 мг, 30 мл) нагревают при в течение 30 мин. Полученный 1М рйствор натрий-2-фенилэтоксида охлаждают до , добавляют 3,5-Диметокси-с1-метилстиролоксид (2 г; 10,3 мл 9 6 и температуру реакционной смеси поддерживают в течение 15 ч около . Реакционную смесь охлаждают и добавляют к смеси простого эфира и воды. Экстракт простого эфира сушат под сульфатом магния и выпаривают. Избыток 2-фенил-этанола удаляют вакуумной перегородкой; т.кип,.б5°С (0,1 мм рт.ст.), после чего остается 3,5 г остатка. Остаток очищают на хроматографической колонке на силикагеле Мер ка-60 (30 г) и элюируют 60%-ной эфирпентановой смесью на фракции по 15 мл. Фракции 52-88 дают 2,9 г (89%) 2-(3,5-Диметоксифенил)-2-гидроксипропил-2-феиилэтилового простого эфира. ИК-спектр (СС14), 353+; 1595, 1202; 1153. УФ-спектр ( этанол) 278 (г 1830); 273 (г 1860).., т/е - 316 (т+) . ЯМР (СОГЛз) 60 МГц;сЛ1,4б (С, СНз-); 2,86 (С, ОН); 2,86 (т, I 7 Гц, -СНо -фенил); 3,53 (с, ); 3,71 (т. Гц, ), 3,80 (С, ОСНз); 6,38 (т, I 2 Гц, АгН); 6,61 (д, Гц, АгН) и 7,23 (с, фенил Н). Рассчитано, %: С 72,12; Н 7,б5. Найдено, %: С 71 ,92; Н 7,63. 2-(3 5-Диметоксифенил)-пропил-2-Фенилэтиловый простой эфир. К раствору 2-(3,5-Димeтoкcифeнил 2- гидроксипропил-2-фенилэтил простого эфира (550 мг; 1,7 мл) в пиридине (2 мл) при добавляют по каплям хлорокись фосфора (77 мг; 5,22 мл). Реакционной смеси дают возможность нагреться до 20°С за период 1,5 ч. Затем ее перемешивают в течение 1,5 ч при , а затем добавляют простой эфир (150 мл) и 15%-ный карбонат натрия (100 мл). Органическую фазу выделяют и промывают 15%-ным карбонатом натрия (3x50 мл), сушат над сульфатом магния и выпаривают до масла. Масло растворяют в абсолютированном этаноле (15 мл), добавляют 10%-ный палладий на угле (100 мг) , и полученную смесь перемешивают в атмосфере водорода. Когда поглощение водорода прекращается (26,5 мл; 20 мин), реакционную смесь фильтруют через диатомитовую землю, и полученный фильтрат выпаривают до масла, и масло очищают с помощью препаративной тонкослойной хроматографии на пластинках силикагеля, лважды элюируя смесью пентан/эфир 6:1/, до получения 211 мг (G%) 2-(3,5-Диметоксифенил)пропил-2 -фенилэтилового простого эфира. ИК-спектр (СС)), 1600; 1205 1155; 1109. т/е - 300 (т-). ЯМР {СОС 60 МГц): ( 1.22 (д, I 7 Гц, ); 2,82 {т, I 7 Гц, CHa,Ph); 2,8 (Н-С-М 3,6 (-CHQ O-CHij); 3.75 (SOCH); 6,35 (М, ЛгН) и 7,18 (S, PhH). 2-(3,5 Лиоксифенил)пропил-2-фенилэтиловый простой эфир. Смесь 2(3,5 диметоксифенил)пропил- 2 фенилэтилово го простого эфира (195 мг; 0,65 мл), пиридина (0, мл; ,96 мл) и сухого хлоргидрата пириди на (k г; З,6 мл) нагревают до в течение 6 ч. Реакционную смесь охлаждают и добавляют к смеси воду (100 мл) и простой эсЬир (150 мл). Эфирный экстракт промывают водой (50 мл) и вместе со вторым эфирным экстрактом (50 лл) эодной Фазы- суша над сульфатом магния и выпаривают до масла. Масло очищают препаративной тонкослойной хроматографией на пластинках силикагеля, шесть .раз элюирую 30%-ным эфир/пентаном до получения 65,В мг (37) 2-(3,5-дигидроксифенил)пропил-2-фенилэтилового простого эфира.. ИК-спектр (СНСЦ), см : 3559; 1б05 1105. т/е - 272 (т+) . ЯМР (CDClj, 60 МГц): сЛ1,18 (д, I --- 7 Гц, CHj-) 2,80 (т. 1 7 Гц, -CHP1i); 2,80 (Н-С-Не); 3,,В (-СН , ОСН,-) ; 6,Об (т, 1 2 Гц, АгН) 6,21 (д, I 2 Гц, АгН) и 7,16 (С, PhH). (3 5-Диоксифенил)1-феноксипентен. В атмосфере азота смесь 3,5-ДИбензилоксиацетобенона (50,0 г; i 0,15 мл) в тетрагидрофуране (175 мл) и 3 феноксипропилтрифенилШосфонийбромид (7,13; 0,16 М) в диметилсульфоксиде (+50 мл) по каплям добавляют за 1,75 ч к суспензии 50 -иого гидрида натрия (7,89; 0,165 М) (предварительно промытого пентаном) в тетрагидрофуране (75 мл), температуру которого поддерживают-около 0-5°С. После перемешивания в течение k м при 0-5 С реакционной смеси дают возможность нагреться до комнатной температуры и затем осторожно перемешивают с ледяной водой (2000 мл), подкисляют концентрированной соляной киС лотой и экстрагируют этилацетатом (5 X lOO мл) . Соединенные органические фазы промывают насыщенным раствором.хлористого натрия (З х 300 мл), сушат над сульфатом магния и концентрируют в вакууме до получения масла, которое тщательно, перетирают с простым эфиром для осаждения трифенилфосфиноксида. Фильтрация с последующим концентрированием фильтрата дает маслянистый остаток, который хроматографируют на силикагеле (1300 г), элюируя смесью бензол/гексан, содержащей 30-100 бензола. Из средних функций 51 г (75) -(3,5-Дибензилоксифенил)-1-феноксипент-З-она выделяют в виде масла Rr 0 (силикагель, 2-бенэол; 1-гексан) т/е - 450 (). Рассчитано, %: С 82,63; Н 6,71. 1айдено, %: С 82,90; Н 6,б9. Раствор 4- (3,5-дибен.зилоксифенил)-1-феноксипент-3 она (51 г; 0,113 М) в смеси абсолютного этанола (1бО мл), этилацетата (l60 мл) и концентрированной соляной кислоты(0,2 мл) гидрируют в течение 12 ч под давлением 55 фунт (2 атм) в присутствии Pd/C, После удаления катализатора фильтрацией и концентрирования фильтрата в вакууме получают 30,8 г (100%) продукта в виде вязкого масла. . Рассчитано,: С 7,97; Н 7,0. Найдено, %: С 7, Н 7,5. 3-Окси-5 Фенилаланин. Оливетол (1,8 г; 0,01 М), хлорисЬ-ый аммоний (2,б5 г; 0,05 М), бисуль-f фит натрия (5,2 г; 0,05 М) и гидроокись аммония (12,5 мл) соединяют и нагревают в стальной бомбе при в течение получаса. Затем бомбу охлаждают, содержимое растворяют в этилацетате (350 мл). Соляную кислоту (300 мл, 101) добавляют, смесь перемешивают и затем выделяют органический слой. Экстракцию повторяют еще два раза. Водный кислый раствор нейтрализуют 6 н. гидроокисью натрия и затем экстрагируют хлороформом (3 X 300 мл). Соединенные экстракты в хлороформе сушат и концентрируют. Остаток помещают в этилацетат, обеспечивают активированным углем и концентрируют. Добавление гексана к остатку вызывает кристаллизацию: 270 мг; т.пл. 88-91 С. После перекристаллизации из горячей смеси этилацетат/гексан (1:1) он плавится при 95-9б С. Рассчитано, %: С 73,70;.Н 9,5б; N 7,81. C,,. Найдено, %: С 73, Н 9,б2; N 7,91. d,l ,М-Ацетил-3-окси-5-(5-фенил-2-пентил)анилин, Раствор 2,4 г (9,5 ммрль) d,l-3 -окси-5- 5 фенил-2-пентил анилина и 24 мл пиридина в 24 мл уксусного ан гидрида перемешивают при комнатной температуре в течение 45 мин. Реакционную смесь выливают в смесь 200 воды и 200 мл этилацетата. После перемешивания в течение 10 мин органический слой выделяют и промывают последовательно водой (4 X 100 мл),, ра солом (1 X 100 мл), сушат (MgSO.) , фильтруют и концентрируют до получения 3,5 г сырого (3 ,б-М-ацетил-З-ацет окси-5(5 фенил-2-пентил)анилина. Раствор d,1-N-ацетил-З-ацетокси-5-(5 фенил-2-пентил)анилина и 1 г кар боната калия в 100 мл метанола перемешивают при комнатной температуре в течение 1ч, фильтруют, концентрируют и растворяют в этилацетате. Органический раствор промывают водой, сушат (МдВОд) И концентрируют до мае па, которое после кристаллизации из гексана дает 1,5 г d , 1-N-ацетил-З-гидрокси-5-(5 фенил-2-пентил)анилина; т.пл. 128-130°С. т/е - 297 (т ). 1Н ЯМР 60 , ч/млн: 8,64 (уш, с, 1Н--Н); 7,12, 6,8 и 6,45 (ушс, 1Н, перем, АгОН); 2,19-2,78 (м, ЗН, Аг-СН и Аг-СН); 2,-05 (с,- ЗН СНз-С-0-); 1,3-1,78 (м, 4Н ( 1,12 (д, ЗН-С-СНз). d,1-3-Бензилокси-5-(фенил-2-пентил)анилин. К перемешиваемому раствору 1,2 г d,P-N aцeтил-3-гидpoкcи 5(5 Фенил-2-пентил)анилин (4,03 ммоль) в 50 м гетрагидрофурана добавляют 193 мг 50 -ного гидрида натрия.(,03 ммоль) Спустя 30 мин перемешивания, добавляют 1,38 г (8,06 ммоль)oL -бромтолу ола, и перемешивание продолжают в те чение 16 ч. Затем реакционную смесь фильтруют, добавляют 1 мл уксусной кислоты к фильтрату, который затем концентрируют и хроматографируют (си ликагель, бензол/эфир (2:1) в качест ве элюента); после чего получают 1,43 г d, l-N-aцeтил-3-бeнзилoкcи-5 (5-фенил-2-пентил)анилина в виде масла, т/е - 387 (т-) . 1Н ЯМР 60 МГц cT-J , ч/млн: 7,88 (ушс, 1Н, 11-Н); 7,38, 7,20, 6,84, 6,59 (ушс, 5Н, 6Н, 1Н, 1Н, аромати30ка); 5,0 (с, 2Н, -0-СН Аг); 2,21-2,8 (м, ЗН, Аг-СН, и Аг-СН(2.); 2,07 (с, ЗН, СНэ-С/ 0/-11); 1,30-1,69 (м, 4Н-(СН,)(); 1,15 (д, ЗН, СНз-С-А). Раствор 1,А г d,l-N-ацетил-З-бензилокси-5-(5 Фенил-2-пентил)-анилина, k мл гидроокиси калия, 14 мл метанола и 10 мл 2-пропанола нагревают при кипячении с обратным холодильником на паровой бане в течение А дней. После охлаждения добавляют воду и этилацетат, и смесь перемешивают в течение 10 мин. Органическую фазу , выделяют в водую и снова экстрагируют этилацетатом. Органические растворы соединяют, сушат (MgSO), концентрируют в вакууме и хроматографируют (35 г силикагеля, бензол/эфир (ЗгО в качестве элюента) и получают d,l-З-бензилокси-5(5-фенил-2-пентил)анилин в виде масла, т/е - (т) . 1Н ЯМР (60 МГц) ч/млн: 7,32 (ушс, .3 5Н, ароматика); 7,13 (ушс; 5Н, ароматика); 6,01-6,33 (м, ЗН, ароматика); 4,9 (с, 2Н, ); 3,48 (ушс, 2Н, перем., Н,); 2, (м, ЗН, Аг-СН и Аг-СН.); 1,32-1,76 (м, 4Н(СН„М, 1,1 (д, ЗН, -C-CHj). d, 1-5-Фенил-2-пентанол-мезитилат К перемешиваемому раствору 5-фенил-2-пентанола (482 г; 2,9 М) в тет рагидрофуране (2250 мл) при 0°С добавляют метансульфонилхлорид (300 мл) с такой скоростью, чтобы температура смеси не поднималась выше 10°С { полное время добавления 4,5 ч). После того, как добавление заканчивают, реакционной смеси дают согреться до комнатной температуры, и перемешивание продолжают в течение дополнительного часа. Реакционную смесь фильтруют и отстоявшийся слой концентрируют до светло-желтого масла (2800 г), которое растворяет в хлороформе (2 л) и промывают водой (4 х 1 л), рассолом (1 X 1л), обрабатывают активирован ным углем (50 г), сушат (MgSO), Аильтруют через диатомитовую землю It концентрируют до светло-оранжевого масла (687 г, 95 выход). Этот ма териал подлежит дальнейшему использованию без дополнительной очистки. 1Н ЯМР (60 МГц) ч/млн: 7.23 (с, 5Н, ароматика); 4,53-5,13 (м, 1Н-СН-0-); 2,93 (с, 2,422,93 (м, 2Н, ); 1,50-1,92 (м, 4Н, -(); 1,23 (с, ЗН,0-СН-СНз). 31З ОбЦ Аналогичным образом из соответствующих спиртов получают следующие мезилаты: -фенилбутанмезилат, желтое масло, т/е - 228 (пТ) . 1Н ЯМР UO МГц) J ч/млн.: 7,22 (ушс, 5Н, ароматика) 4,08-4,3 (м, 2Н, -СНп-0-); 3,93 {с. ЗН 2,iiO-2,82 U, 2Н, -CHijL jHj); Ь511 33 (м, 4H(CHij)f ). е-2-октанолмезилат в виде бесцвет ного масла CclA5 9,695 (с, 2, 6, , чD 1Н ЛМР (60 MfuJcTj.Qg м/млн: +,79 ,. (ушс, 1Н, -СН-0-); 2,97 (с, ЗН,5-Сгу 1,0 (д, ЗН, СНз-СН); 0,87 (у ЗН, lj TU М|- 3 -J - (Ч-- г ); 1,0-2,0 (м, ЮН. -(). d-2-октанолмезилат oLJjj +9,238 (,8, СНС1з) 1Н ЯМР идентичен 1-форме. Пример 16. d,1-5,6 ,6а,7,10, 1Оа-Гексагидро-1-ацетокси-6 -метил 3- (4 фенилбутилокси)бензо- fcJ-хинолин-9(8н)он, цис- и транс-изомеры, d, 1-5,6,6а,7-Тетрагидро 1 окси -6fi мeтил-(4-фенилбутокси)бензо- с }хинолин-9(8Н)-он вначале восстанавли вают литием и аммонием, а затем ацетилируют до получения нужного гексагидро-изомера. Выделение на хроматографической колонке с силикагелем (с использованием простого эфира в качестве элюента) приводит к получению вначале d,1-транс-5(6,6ар7,Ю, 1 Oadr гекса ги д ро 1 -ацетокси- 6|5- метил-3(-фенилбутилокси)бензо- с -кинолин-9(8Н)-она; т.пл. 155-15б°С, после перекристаллизации из смеси этилацетат/пентан (1:5). Рассчитано, %: С 7,08; Н 7,1; N 3,32. Найдено, %: С 7,00; Н 7,7; N 3,22. т/е - 421 (). Дальнейшая очистка последних фрак ций на хроматографической колонке с силикагелем с использованием в качестве элюирующего растворителя смеси циклогексан/эфир (1:1) приводит к получению изомерного d,6-цис-5,6,6 fb7,10,10а|5ггексагидро-1-ацетокси 6 -метил-3 (4-фенилбутилокси)бензо-fcj -хи ноли н-9 (8Н)-она; т.пл. 95-9б С после перекристаллизации из смеси 32 этилацетат/гексан 0:5). гп/е - 421 Рассчитано, : С 7,08; Н 7,1;, N 3,32. Ч НЗ-Р4«Найдено, I: С 73,95; Н 7,б1; N 3,31. Пример 17. d,1-TpaHc-5,6,6а(3,7,8,9,10,10аА-Окт&гидрр-1ацетокси-9Э-окси-6(гметил-3-(5-фенил 2-пентилокси)бензо- ;с -хинолин. Гетерогенную смесь d 1-5,6.6а,7- -тетрагидроН-ацетокси-б -метил-З15-фенил-2-пентилокси}бензо-Сс -хинолин-9(8Н)-он (3,0 г| 7 моль) и пал ладий - на угле (5%; 3,0 г) в метаноле (30 мл) гидрируют при комнатной температуре в аппарате Парра при давлении водорода 50 пси (3,5 атм) в течение 3 м. Затем катализатор отфильтровывают, и метаНольный фильтрат вы паривают при пониженном давлении до полумения указанного продукта. Продукт помещают в этилацетат ( 300 мл), и полученный раствор охлаждают до 0°С. Избыток насыщенного раствора хлористого водорода в этилацетате добавляют затем к смеси для высаживания соли хлористоводородной кислоты указанного продукта в виде твердого белого соединения. Его фильтруют, промывают этилацетатом и сушат. d,-5,6,6а-7-Тетрагидро-1-ацетокси-6|1-метил-3-( 5-фенил-2-пентилокси)бензо- с -хинолин-9(8Н)-он получают следующим образом, К перемешиваемому раствору d,l- 5,6,6а,7-тетрагидро- 1-гидрокси-6| г-метил-3(5-фенил 2-пеитилокси)бензо- с хинолин-9(8Н)-ону (4,5 г; 0,0115 моль) в пиридине (45 мл) при комнатной температуре добавляют уксусный ангидрид (45 мл), Полученный раствор перемешивают в течение 3,5 ч и затем выливают в ледяную воду (250 мл), и смесь экстрагируют диизопропиловым эфиром (2x250 мл). Соединенные экстракты промывают водой.(3x200 мл), сушат (MgSO) и выпаривают при пониженном давлении до желто-коричневого масла, которое отверждается при соскабливании со стенок колбы, содержащей его. Растирание твердого продукта с н-гептаном дает 2,0 г 1-ацетоксипроизводного (выход 40%). Его очищают перекристаллизацией из горячей смеси хлороформ/ н-гексан (1:4) и получают чистый сложный эфир; т.пл. 13б-14ос. т/е - 433 (ш) . 33 Н ЯМР (60 МГц )cfJJJg, ч/млн: 7,2 (с. 5Н, ароматика); 6,62 (д,3 1,5Н-1, 1Н, ); 5,97 (д.Т 3, HI , .1Н мета HJ; 5.86 (.д, 3 3HI, 1Н, мета Н); 2,27 (с, ЗН, (6 СН,,-С(0); ; 1,21 (л, J 7Н, 6Н. 1 CHj-C-N, CHj-C-0); 1,+9-,51 (м, 14Н. остальные протоны). 5 В табл. 3 предствлены соединения, подобные полученным.



















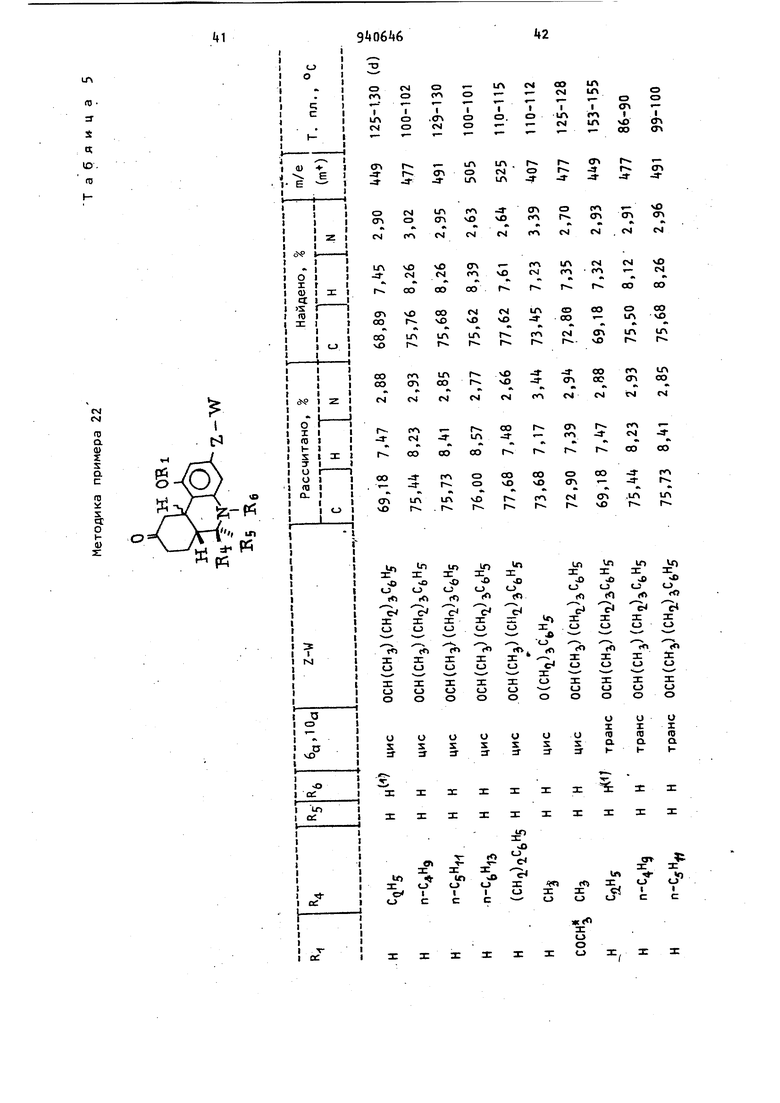
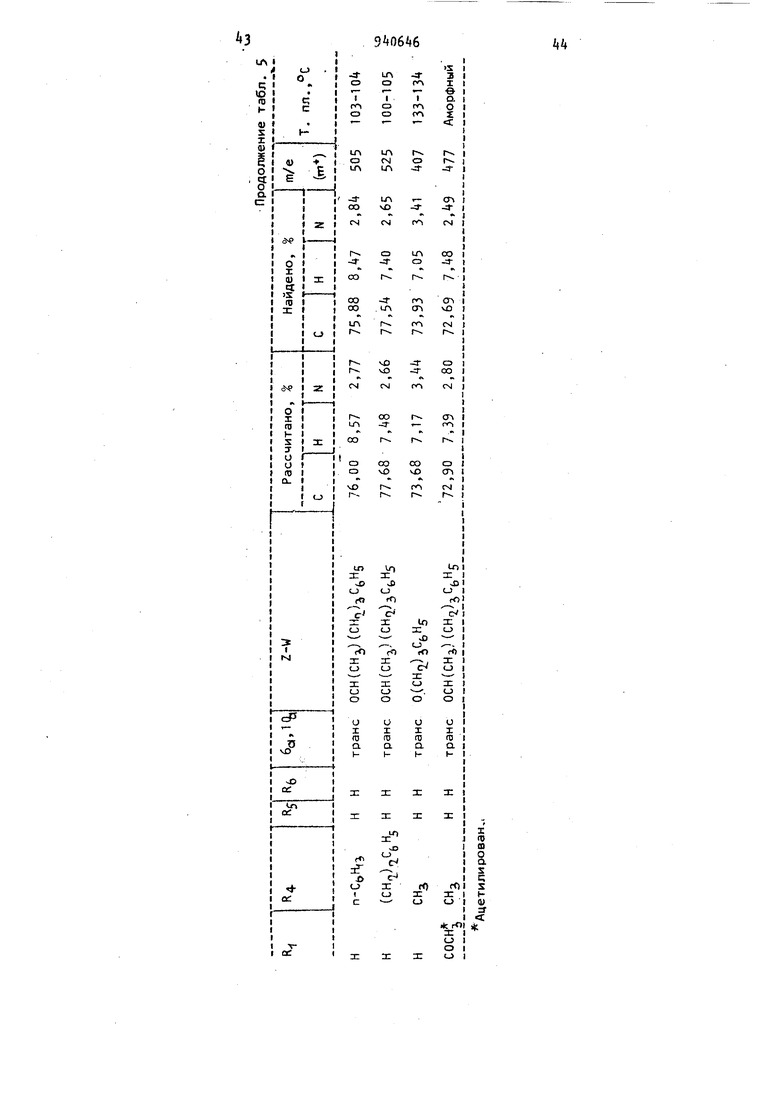
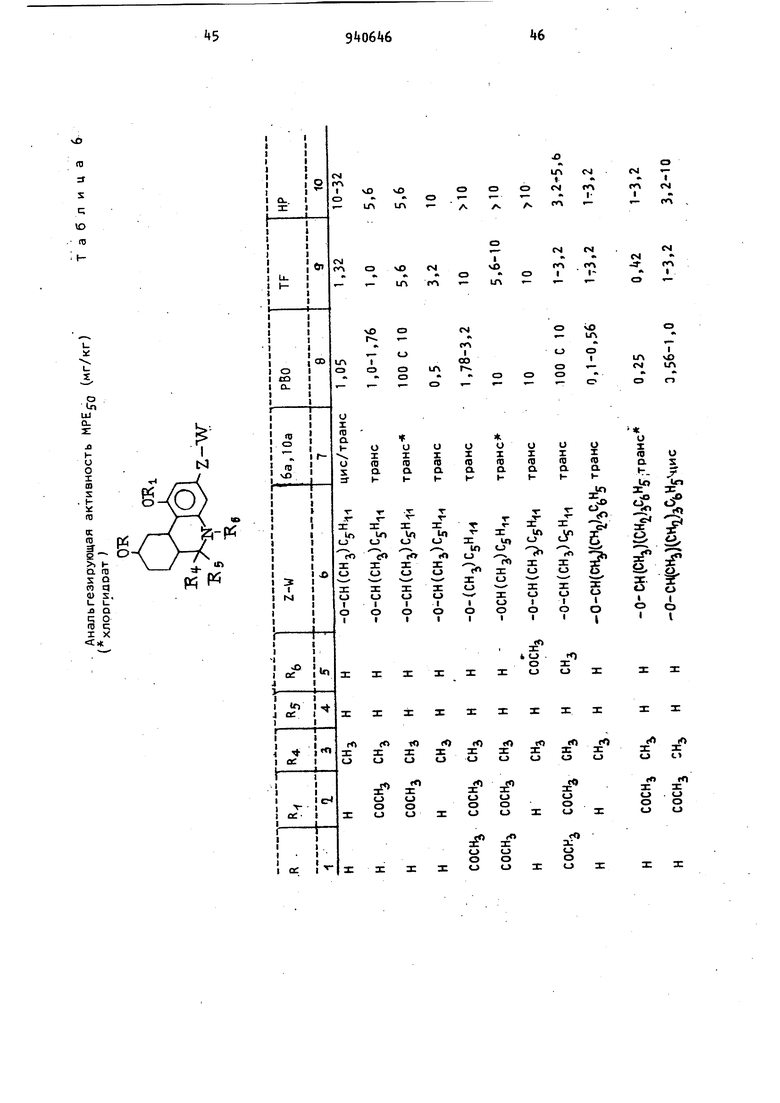

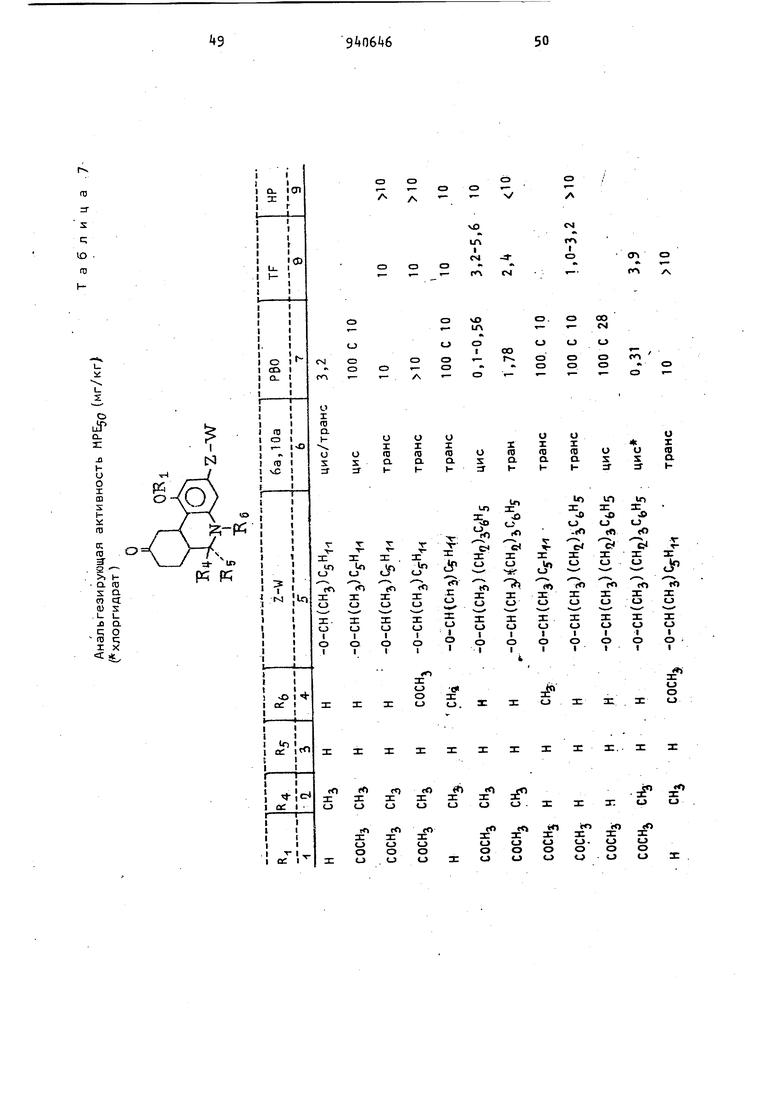



П .р и м е р 18. d, 1-ЦИС-5 ,6 ,6aoL, 7,8,5,10,1 ОасАгОктагидро- 1-ацетокси9|5 гидрокси-6|1-метил-3.{5 фенил-2гпентилокси)бензо- с -хинолин. К раствору d , 1-ЦИС-5 )6 ,6а|3,7 ,1 О, 1Оар-гексагидро-1-ацетокси-6ргметил- 3 (5 Фенил-2-пентилокси)бензо- с1-хинолин-9(8Н)-она (1,0 г; 2,296 ммоль) в сухом тетрагидрофуран (100 мл) при -78С добавляют при перемешивании -втор-бутилборгидрид калия (4,6 мл; 0,5 М; 2,296 ммоль) по каплям за промежуток времени 5 мин. Реакционную смесь перемешивают еще 30 мин при -78°С и затем выливают ,при перемешивании в раствор уксусной кислоты (250 мл) и эфира (500 мл), предварительно охлажденных до . Образующиеся слои разделяют, и водный слой экстрагируют дополнительным количеством эфира (250 мл). Соединенные эфирные экстракты промывают последовательно водой( х 50 мл), насыщенным раствором бикарбоната нат рия (1 X 250 мл) и солевым раствором (1 X 250 мл), сушат (MgS04) и концен рируют в вакууме до получения желтого масла (1, г). Неочищенное масло хроматографируют на силикагеле (100 используя в качестве элюирующего рас ворителя смесь бензол/эфир (3:1). После элюирования менее полярных при месей, выделяют в виде прозрачного масла получаемый продукт (700 мг). Масло растворяют в простом эфире (35 мл) и обрабатывают эфиром, насыщенным газообразным НС1 для получения соли хлористоводородной кислоты указанного соединения (kkS мг). Пример 19. d,1-5,6,6a,7,10, 10а-Гексагидро- 1-ацетокси-6(Ь-метил3(5 фенил-2-пентилокси)бензо- с -хи нолин-9 (8Н)-он , транс--и цис-изомеры Аммоний (1150 мл) конденсируют непосредственно в высушенную на пламени трехлитровую трехгорлую колбу (в атмосфере азота), снабженную механической мешалкой, 500 мл капельной воронкой и хладагентом - твердый COiji (ацетон) (). В нее помещают литиевую проволоку (2,2 г), нарезанную на кусочки С), и немедленно появляется характерная синяя окраска. К перемешиваемому синему раствору при добавляют d,2-5,6,6a,7-тeтpaгидpo- 1-окси-6(Ь-метил-3-( 5-фенил-2-пентилокси) бензо- с -хинолйн-9(8НJон (21,5 г), растворенный в тетрагидрофуране (250 мл ) по капллм в течение 10 мин. После дополнительного перемешивания в течение 10 мин при f78°C реакционную смесь резко охлаждйют дополнительным количеством хлсристого аммония (20 г). Затем охлаждение прекращают, и реакционную смесь медленно нагревают на паровой бане для испарения аммония. Когда он почти весь испарится, добавляют этилацетат (2 л) и воду (1 л), и смесь перемешивают в течение 10 мин. Затем разделяют слои,и водную фазу еще раз . экстрагируют этилацетатом (500 мл). Объединенные органические экстракты промывают еще раз водой (1 л), сушат (МдЗОд) и концентрируют до коричневого полутвердого состояния ( г). Пример 20. d, 1-5,6,6а,7, 10,1 Оа-Гексагидро- 1-ацетокси-6(Ь-метил-3 (1,1-диметилгептил бензо- с -хинолин-9(8Н)-он. Суспензию 2,0 г (5,63 ммoль)d,1,56 ,6а, 7-тетрагидро- -oкcи-6p)-:мeтил 3(1 , 1-диметилгептил)бензо- с1-х.)нолин-9(8Н)-она в 25 мл тетрагидрофурана добавляют по каплям из капельной воронки к интенсивно перемешиваемому растоору 0,236 г литияв жидком аммиаке (120 мл, отогнанных через слой гранулированной гидроокиси калия при -78°С, охлаждение осуществляется с по мощью смеси ацетона и сухого льда. Делительную воронку после окончания добавки Ьполаскивают 10 мл тетрагидро фурана. Смесь перемешивают в течение 10 мин, добавляют к ней Z мг лития и продолжают перемешивание еще 2 ч. Для уничтожения голубой окраски к смеси добавляют г хлористого аммония. После удаления избытка аммиака за счет испарения остаток растворяют в смеси 50 мл воды и 100 мл этилацета та. Этилацетатный слой отделяют, а из водного проводят экстракцию этилацетатом (дважды, порциями по 50 мл). Объединенные экстракты промывают рас солом, высушивают (МдЗОд) и упаривают при пониженном давлении до получения полутвердого коричневого продукта (1,33 г). Остаток затем растворяют в 25 мл метиленхлорида, охлаж дают до 0° (на бане со смесью воды и льда)и добавляют к раствору в течение минуты 0,869 мл триэтиламина, 0,7б2 г диметиламинопиридина и 0,388 мл уксусного ангидрида. Смесь перемешивают при в течение получаса, а затем разбавляют смесью 50 мл метиленхлорида и 25 мл воды. Органическую фазу отделяют, а из вод ной проводят экстракцию 50 мл мети107-110 /435 0, 68,92 7,17 2,86 i(35 0,72 68,7 6,93 3,12
Тонкослойная хроматография, смесь бензол/эфир
(1:1)1 Рассчитано для , %: С 68,71;
Н 7,26; N 2,96.
CHi,
/
-0-CH-itH)Cj,H5 сНз Н СНз Н 94-97°С
Чн,, 3ii
Таблица 2
kkS ленхлорида. Объединенные органические вытяжки промывают последовательно четыре раза насыщенным раствором бикарбоната натрия, порциями по 50 мл, 50 мл рассола и высушивают (MgSOj|.). После отгонки при пониженном давлени1Н растворителя получают темно-коричневый остаток5 который растворяют в. толуоле. Полученный раствор переносят в хроматографическую колонку диаметром 3,8 и высотой 61 см, заполненную 200 г силикагеля. Элюирование осуществляют смесью толуола и эфира, взятых в соотношении 3:1 (объем смеси равен объему колонки), а затем обезгаженной смесью толуола и эфира в том же соотношении. В результате элюирования, контролируемого с помощью тонкослойной хроматографии, получают красного цвета, который концентрируют и обрабатывают сухим НС1. В конечном счете получают хлористоводородную соль целевого соединения (О, г; 17,8%) в виде розового твердого продукта; т.пл. 135-137°С. Данные масс-спектрометрии: т/е - 399 (т); Зб7; 273. Рассчитано, I: С 68,87; Н 8,78; N 3,21. .HCI С 67,85; Н 8,92; Найдено, ; N 3.18. Далее c ютpи примеры 21 и 22 ( т абл. + и 5).
-0-СН-(СНт.)з-С Н5-0-1СНг)4СбН4
Подсчитано для C..LJ).N-НС 1:С, 68,7; Н 7,66; N2,95; С 1,0, CHjOH.
Методика примера 21. .о-сн(сн5)(сн)зСеН5 -0-СН(СНз)(СН) -0-СН(СН)(СН)
СН,, Н CHj Н Масло««9
CHj Н CHj Н 102-103°С
Оо
т. а б л и ц а k
Н 7,«5 N 2,90 с 69,18 Н 7,32 N 2,93 С 75,88 Н 8, HJ н-ан 125-130: 9 н7..7 НИН 153-155 {; O N-HC1 H7,.7 С, Н uH,103-10V505 ( -Н8,57 N2,88 с69,18 N2,88 с76,00
эфир (I:.I),R Q,7k; - - (Ц 0,72
LA
m
s S
EC
Ю.
(0
u
.- 1Л СЧ oo
(M
о in
о .- - CM
о
о о
«г I I I
I I
I
I I о о о .o
о о
т-CM
NO ОЛ
1Л о «M
oo (Г
Г Г- -
r о
г г
r - ил
LA tM -3 Г П г г о
-а- -т
-я-гг
lA
J- 1Л
,NO
о
ГА
стч
cr
LTl
гл
о г
п
г o
«п vD
ггч
CM
см
см
см
01
CM
см
NO
см
1Л ГА
см
vO
ГА
(TV
ГА
см ГА vO
см
Т- «
oo
оо
OO .
оо
oo
оо о
о оо
CM
1А
оо
NO
1А чО
чО
NO
(N4
cs
03
a
Ш
s a с
та
о ь v
LA
оо со
NO
г
-чLT
r r
СП
00 сг
-3NO
СО
CM
CM
см
см
CM
CM
CM
CA.-
1
о
oo
r
CM -3-
LA
-Ч-Яoo oo
00
oo
00
оо
оо
-3oo
о «TV
-3СЭ
rr
-T
N0 NO
о
-
r
LA
г
,LA
vO
см 1
I r
lA
ГА
NO
r
r
. ГX
з: т.
ОС X
X
«
о о о
vO
ra
j s c;
VO
- TO
u
ii:
z
nj
r
s
c;
та Ii
Ы
L.
О
CL.
M
о
О
m s
iC
re
к та
O
S Q.
ct
ej
(U
L. U X D.
: О
ПЗ t;
I X
#. Способ получения производных бен30- с1-хинолинов общей формулы (1) QK, Z-W И, ,ОН где Q -/0 Ci RJJ водород, бензил, бензоил, Ц-(-алканоил, или СО-(СН()р-NRf Rj, где Р - О или Кди Rj одинаковые или разные, водород или С -С -алкил; или RQ и Rj вместе с атомом азота, с которьм они связаны, образуют пяти-или шестичленный гетероцикл, представляюи ий собой пиперидин, пиррол, пирролидин, морфолин или С -С -алкил-пиперазин; R водород С -С -алкил, или (, где Z - целое число Rg - водород, метил и/м этил; R - водород, формил, С(-Сс алкано ил, С-|-С(5-алкил, (СН(2) или COCCHftWCfeHc, где X - целое число 1-V. Z - ,-алкилен или (алк)у1Х-(алк)р , где алк и алк одинако разные ,-алкилен,при условии, что суммарное количество атомов углерода в алк, и алк не превышает 9; m и п - О или 1i где «1 - J мети л- пи ри дил, водород. фтор или хлор, или их солей, отличающийся гем, что соединение общей формулы TI N |Где Rj,R.-R. ,Z и W имеют указанные Значения, восстанавливают, когда (31- в результате реакции о щелочным ме таллом в жидком аммиаке или когда Н ОН ( ,- каталитическим хгидрированием- в присутствии катали:затора - благородного металла, с выделением целевого продукта в свободном виде или в виде соли. Источники информации, принятые во внимание при экспертизе 1.Huchel W. - Ann, 1939, Bd.SfO, Z.157. 2.Ворожцов Н.Н. Основы синтеза промежуточных продуктов и красителей, Н., Госхимиздат, 1955, с. 678.
Авторы
Даты
1982-06-30—Публикация
1977-05-17—Подача