1
Изобретение относится к новым химическим соединениям, конкретно к производным диоксиалкиламиноэ(1)иров общей форьлулы
и-СНгСН ОК СНгСН ОН
где R е 9 ЧЗлкил,
которые являются пенообразователями
в кислых средах.
Известны алкиловые эфиры аминоспиртов, например моноэтаноламина, общей формулы МН2.,ОН,где R С - С, обладающие поверхностноактивными свойствами 1.
Известны также алкилимидазолины в качестве пенообразователей в кислых средах 2.
Однако алкилимидазолины являются лабильными соединениями и способны подвергаться гидролизу.
Цель изобретения - расширение ассортимента поверхностно-активных веществ, которые могут найти применение в качестве пенообразователей в кислых средах, обладающие улучшенными свойствами.
Указанная цель достигается новыми производными диоксиалкиламиноэ( общей формулы (I), где R имеет указанное значение.
10
Предлагаемые соединения получают 0-алкилированием триэтаноламина (ТЭА) н-алкил хлоридом в присутствии гидроокиси натрия при 100-125 0. Процесс ,5 целесообразно проводить при небольшом избытке ТЭА (ТЭА: алкйлхлорид 1,1:1), что позволяет увеличить выход целевых продуктов.
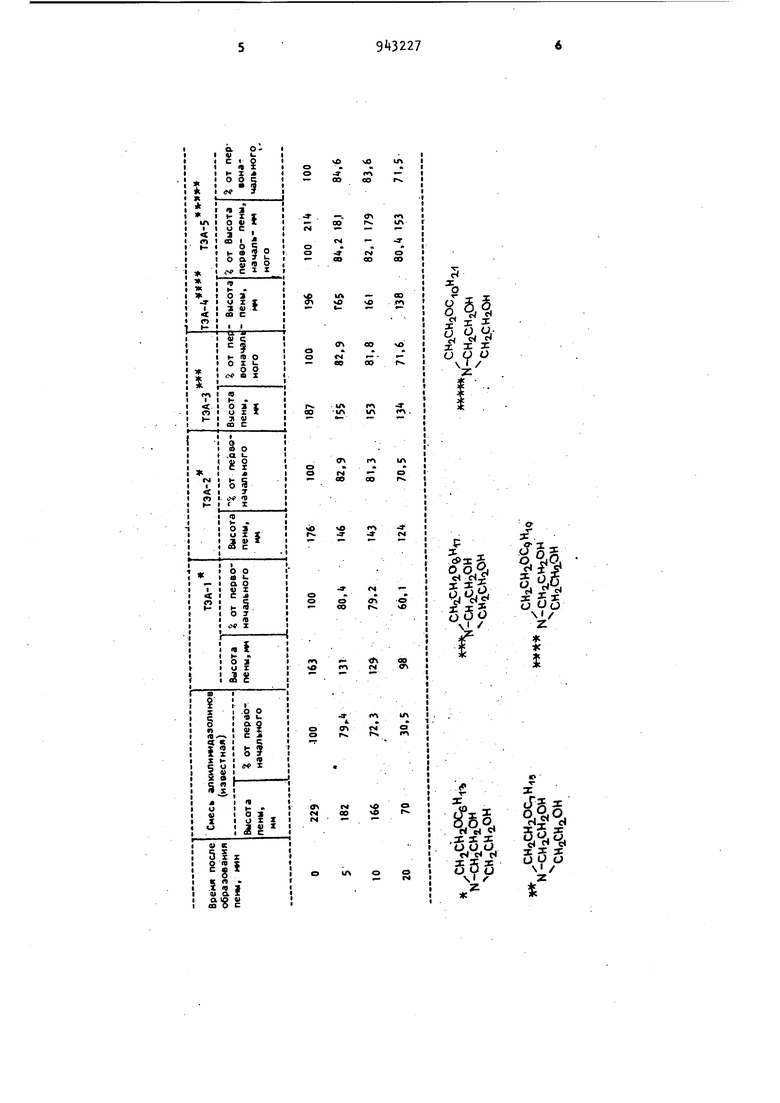
П р и м е р 1. В реакционную кол20бу помещают г (0,5 моль) ТЭА и 20 г (0,5 моль) гидроокиси нат рия. Реакционную смесь перемешивают 1 ч при , после чего добавляют 53,8 г (Q,k моль)хлористого гексила и перемешивают 1 ч при . Моноэфир ТЭА очищают от алкилхлорида переводом в солянокислую соль об работкой соляной кислотой. Водный раствор этой соли обрабатывают аммиаком. Целевой продукт извлекают бензолом, бензольный слой промывают водой до нейтральной реакции и пере гоняют. Выход моногексилового эфира триэтаноламина 35,3 г {k2%) . Полученный продукт представляет собой бесцветную жидкость с т.кип. 153 1 мм рт.ст. п 1,57, 4° . Найдено,%: Аминовое число 150,6, С 61,12,61,48, Н 11,48,11,60,N 5,85 5,90. Вычислено,%: Аминовое число 15б, С 61,75, Н 11,68, N 6,00. Пример 2., Моно.гептиловый эфир триэтаноламина получают аналогично примеру 1. Из 7,6 г (0,5 моль) ТЗА, 53,8 г (0,4 моль) хлористого гептил и 20 г (0,5 моль) гидроокиси натрия получают 4ij,5 г (5) целевого продукта, представляющего собой бесцве ную жидкость с т.кип. 160-161 С/ /1 мм рт.ст., п2С 1,4596, dj° 0,9323. Найдено,: Аминовое число ,5. С 63,06, 62,92, Н ll,62, 11,78, N 5,5(J, 5,58. Вычислено,%: Аминовое число , С 63,10, Н 11,83, N 5,66. Пример 3. Монооктиловый эфир триэтиланоламина получают анало гично примеру 1. Из 7,6 г (0,5 мол|) ТЭА, 59,5 г (0, моль) хлористого октила и 20 г (0,5 моль) гидроокиси натрия получают 41,8 г (40) целевого продукта, представляющего собой бесцвет ную жидкость с т.кип. 170-173С/ /1 мм рт.ст., п 1,4620, dp 0,9321. НайденоД: Аминовое число 13б,1, С 64,03,64,10, Н11,73, 11,79,N 5,32 5,40.. Вычислено, g : Аминовое число 139,6, С 64,30, Н 11,97, N 5,35. Пример 4. Мононониловый эфир триэтаноламина получают аналогично примеру 1. Из 74,6 г (0,5 моль) ТЭА, 65,1 г (0,4 мол) хлористого нонила и 20 г (0,5 моль) гидроокиси . натрия получают 44,1 г (40) целевого продукта, представляющего собой бесцветную жидкость, с т.кип. 180-182°С/ / 1 мм рт.ст., n|f. 1,4640, d 0,9318. Найдено, :. Аминовое число 130,6, С 65,12, 65,20, Н 11,96, 12,00, N 4,92,5,00. Вычислено,%: Аминовое число 132,5, С 65,39, Н 12,09, N 5,08. Пример 5. Монодециловый эфир триэтаноламина (ТЭА-5) получают аналогично примеру 1. Из 74,6 г (0,5 моль) ТЭА, 70,6 г (0,4 моль) хлористого децила и 20 г (0,5 моль)НаОН получают 49,4 г .(34) эфира. Бесцветная жидкость с т.кип. 153-15VO,03 мм рт.ст., п 1,4660, d 0.9295. Найдено,I: Аминовое число 122,0, С 66,25,.66,15, Н 12,01, 12,10, N 4,79, ;83. Вычислено:Аминовое число 126,1, С 66,37, Н 12,21, N 4,84. Предлагаемые соединения формулы являются эффективными пенообразователями в кислых средах, стабильными к гидролизу соединениями, вследствие наличия прочной простой связи, Пенообразующая способность определяется стандартными методами Росса Майлса. В таблице приведена устойчивость пены 0,25%-ных растворов диоксиалкиламиноэфиров в 10|;-ной соляной кислоте при . Как видно из таблицы, предлагаемые соединения, несмотря на менее обильную пену по сравнению с алкилимидазолинами, дают более устойчивую пену. Формула изобретения Производные диоксиалкиламиноэфиров общей формулы iCHjOR СН СНоОМ N-CHiCHoOH СН СН он где R - Сб - С -н-алкил, 7 8 в качестве пенообразователей в средах, Источники информации; принятые во внимание при экспертизе 1- Патент США № 3397238. 2бО-584, опублик. 1968. 2. Авторское свидетельство СССР |Р 486751, кл. А 61 О 1/00, 1972.


| название | год | авторы | номер документа |
|---|---|---|---|
| Четвертичные аммониевые основания на основе эфиров диметилэтаноламина в качестве ингибитора коррозии стали в кислых средах | 1983 |
|
SU1121927A1 |
| СПОСОБ ПОЛУЧЕНИЯ О-АРИЛОВЫХ ЭФИРОВ 2-ТИО- ИЛИ 2-ОКСО-1,3,2-ОКСАЗАФОСФОРИНАНА | 1981 |
|
SU1019823A1 |
| Способ получения циклических алкиленарилфосфитов | 1982 |
|
SU1049495A1 |
| Способ получения моно-окса-бензоацетамидных или -бензамидных соединений,или метансульфонатной соли моно-окса-бензоацетамидных соединений | 1982 |
|
SU1338784A3 |
| Способ получения цис- и транс-изомеров замещенных дигалоидвинилциклопропанкарбоновых кислот или их эфиров | 1976 |
|
SU940644A3 |
| Способ получения бензил-2,2-диметокси ацетамидов | 1976 |
|
SU663299A3 |
| Способ получения производных пиридина | 1976 |
|
SU621317A3 |
| Способ получения эфиров метакриловой кислоты | 1979 |
|
SU910598A1 |
| Способ получения эфиров кислот фосфора | 1975 |
|
SU609471A3 |
| Способ получения производныхдигидРОбЕНзОпиРАНОКСАНТЕНОНОВ | 1979 |
|
SU818485A3 |


Авторы
Даты
1982-07-15—Публикация
1980-10-24—Подача