Изобретение относится к способу получения трипептидамидов - новых .биологически активных соединений, которые могут найти применение в медицине..
В пептидной химии широко используют ступенчатый способ получения пептидов путем нараживания цепи с .С-конца исходной аминокислоты с при.менением активированных производных аминокислот, например, пентафтррфениловых эфиров 1.
Использование известных методов позволяет получить новые соединения, обладающие интересными фармакологическими свойствами.
Цель изобретения - получение новых трипептидамидов, расширяющих арсенал средств воздействия на живой организм.
Поставленная цель достигается способом получения трипелтидамидов общей формулы I.
Glp-X-Y-NH-Л U) где X - Lell, D - Leu, nleu.val,
nval , Thr, Рго,Ь-о -аминобутирил, 1,-о -аминодеканоил, 1,-циклогексилаланил, 1; сА-трет-бутил серил:
Y - Pro;
A - водород, Allc(G, ),
(CH3)(C, -C), при условии, если X - Leu, то A имеет значение, отличающееся от водорода,
или X - His, У - НРго,D - пипеколил, заключающийся в том, что наращивают пептидную цепь, начиная с амида амиtoнокислоты общей формулы И
У - NH - А. (И) где У и А имеют указанные значения, с аминокислотами, их производными
ts или соответствующим дипептидом методом пентафторфениловых эфиров или азидным методом и, в случае использования глутаминовой кислоты, циклизации последней в пироглутамин с
20 последующим снятием защитных групп.
В приведенных примерах использованы следующие сокращения:
Ada - L-2-аминодекановая кислота;
25
Abu - L-2-аминомасляная кислота;
Cha - L-циклогексил-аланин;
Dopa - диоксифени.паланин;
Pip - L-пипеколиновая кислота;
НРго - L-гомопролин; DAK - 2-диметиламиноэтил; DCC - дициклогексил-карбодиимид; PFPOM - пентафторфенол; DCU - дициклогексил-мочевина; DMFA - диметилформамид. Величины оптического вращения из меряют с помощью поляриметра Перкин-Эльмер 141. При тонкослойных хроматографических исследованиях пр меняют силикагельные пластины (Е,Merck). При хроматографии исполь зуют следующие смеси растворителей: .(1) хлороформ:метанол 9:1; С2} этил ацетат: (пиридин: уксусная кислота вода 20:6:11) 9:1; (3)этилацетат : (пиридингуксусная кислота:вода 20:6:11) 8:2; (4)этилацетат :(пиридин:уксусная кислота:вода 20:6:11) 3:2 . Для обнаружения используют раств нингидрина. Пластины после опрыскивания сушат в течение около 5 мин при , Затем хррматограммы обра батывают газообразным хлором, обдувают воздухом и обрызгивают раствором о-толидин- калийиодида. Для хроматографической очистки на колонне применяют силикагель Силикагель (Е.МегсК) с величиной частиц 0,062-0,2 мм. Пример 1. Ь-Пироглутамил-Ь -норлейцил-Ь-пролинамид. 1-я стадия. Раствор 2,28 г (20 ммоль) HProNH, и 3,95 г (10 ммоль) BocNleu OPFPIрастворяют в 40 мл диметилформ амида, после 5 мин стояния упариваю в,вакууме. Полученное в остатке мас растворяют в 50 мл хлороформа, раствор трижды промывают в делительной воронке 10 мл 1 н. раствора соляной кислоты, затем трижды 10 мп 1 н. ра твора бикарбоната натрия и, наконец один раз 10 МП воды сушат над безводным сульфатом натрия и упаривают Остаток растворяют в 5 мл этилацета и раствор смешивают с 10 мл 5 н. ра твора соляной кислоты в этилацетате. Через 30 мин реакционную смесь разбавляют эфиром, выпавший в осадо продукт отфильтровывают и сушат в вакууме над безводной гидроокисыо натрия. Получают 2,48 г HNleu-Pro-NH,, НС1 (94% от теоретического выхода, рассчитанного на BOC-Nleu 70PFP); 0,20. J 2-я стадия: бензилоксикарбонил-L -Пироглутамил-Ь-норлейцил-Ь-пролинамид. Раствор 1,05 г (-4 ммоль) HNleu-Pro-NHj - HCl в 10 мл диметилформам да охлаждают льдом и не снимая охла дения при перемешивании смешивают с 0,56 мл (4 ммоль) триэтиламина и 1,89 г (4,4 ммоль) Z-Glp-OPFP. Чере 5 мин,не прекращая перемешивание, добавляют к смеси 0,56 мл (4 ммоль) триэтиламина, перемешиван ге продолжают еще 20 мин, затем упаривают в вакууме досуха. Остаток растворяют в 40 мл хлороформа, раствор дважды встряхивают в делительной воронке с 10 мл 1 н. соляной кислоты, трижды с 10 мл 1 н. раствора бикарбоната натрия и, наконец, с 10 мл воды, затем сушат над безводным сульфатом натрия и упаривают в вакууме. Полученное в остатке масло кристаллизуют из эфира, полученный сырой продукт (1,52 г) перекристаллизовывают из 8 мл этилацетата. Получают 1,36 г Z-Clp-Nleu-Pro-NH j, (72% от теоретического; т,пл.146-148°С); R 0,32fa/- -79,8 (, в уксусной кислоте) .- Вычислено, %: С 61,00; Н- 6,83; N 11,86 Нд С 60,90 Н 7,04; Найдено,% N 11,87. Мол.вес.472,55. 3-я стадия: Ь-пироглутамил-Ь-норлейцил-Ь-пролинамид. Раствор 1,16 г (2,46 ммоль) Z-Glp-Nleu-Pro-NH в 25 мл метанола смешивают с 0,2 г 10%-ного катализатора палладий/активированный уголь и через раствор в течение 30 мин пропускают газообразный водород. Затем катализатор отфильтровывают, фильтрат упаривают, Твердый аморфный остаток растирают с эфиром, фильтруют. Полученный сырой продукт (0,72 г) растворяют в воде, раствор осветляют активированным углем и прозрачный водный раствор лиофклизуют. Получают 0,66 г Glp-Nleu-Pro-NHj (79,5% от теоретического); R 0,43,rfJ -77,1 (, в уксусной кислоте) . Аминокислотный анализ: Glp 0,96 (1,0), Nleu 1,00 (1,0), Pro 1,00 (1,0). Пример 2. Ь-Пироглутамил-Ь-норвалил-Ь-пролинамид. 1-я стадия: гидрохлорид L-норвалил-Ь-пролинамид. Раствор 2,2 г (20 ммоль) HPro-N% и 3,83 г (10 ммоль) BOC-Nval-OPFP в 40 мл диметилформамида, оставляют на 5 мин, затем упаривают в вакууме. Полученное в остатке масло растворяют в 50 мл хлороформа, раствор трижды встряхивают в делительной воронке с 10 мл 1 н. соляной кислоты, трижды с 10 мл 1 н. раствора бикарбоната натрия и, наконец, один раз с 10 мл воды, -сушат над безводным сульфатом натрия и упаривают. Остаток растворяют в 5 мл этиладетата и раствор смешивают с 10 мл 5 н. раствора соляной кислоты в этилацетате. Через. 30 мин реакционную смесь разбавляют эфиром, выпавший в- осадок продукт отфильтровывают и сушат в вакууме над
безводной гидроокисью натрия. Получают 1,83 г li-Nval-Pro-NHj-HCl (73% от-теоретического выхода, рассчитанного на Boc-Nval-OPFP) ; 0,10.
2-я стадия: бензилоксикарбонил-L-пироглутамил-Ь-норвалил-Ь-пролинамид.
.Взвесь 1,25 г (5 ммоль) H-Nval-Pr-NHj-HCl в 15 мл диметилформамида при охлаждении льдом и непрерывном перемешивании смешивают с 0,7 мл (5 ммол триэтиламина и 2,15 г (5 ммоль) Z-Gl-OPFP, Через 5 мин добавляют 0,7 мл (5 ммоль) триэтиламина, смесь перемешивают еще 20 мин и затем упаривают в вакууме.. Остаток растворяют в 50 м хлороформа, раствор трижды встряхивают в делительной воронке с 10 мл 1 н. соляной кислоты, трижды - с 1U мл 1 н. раствора бикарбоната натрия и, наконец, с 10 мл воды, сушат над безводным сульфатом натрия и . упаривают. Получающееся в остатке масло обрабатывают эфиром,выпавший в осадок продукт 1,8 г отфильтровывают и перекристаллизовывают из смеси этанола и эфира. Получают 1,66 г Z-Glp-Nval-Pro-NHj. (72% от теоретического) , т.пл.166-167с,к / 0,29, -87,5(, в уксусной кислоте)
Вычислено,%: С 60,25;Н 6,59N 12,22.
Найдено, % : С 60,08; Н 6,70;
N 12,15.
Мол.вес.458,52.
3-я стадия: Ь-пироглутамил-Ь-норвалил-Ь-пролинамид.
Раствор 1,42 г (3,1 ммоль) Z-Glp-Nval-Pro-NH2 в 30 мл метанола смешивают с 0,2 г 10%-ного катализатора палладий/активированный уголь и чере раствор в течение 30 мин пропускают газообразный водород. Катализатор отфильтровывают, фильтрат упаривают. Твердый аморфный остаток растирают с эфиром и отфильтровывают; Полученный продукт растворяют в воде, раствор обесцвечивают, обрабатывая активированным углем, и прозрачный водный раствор лиофилизуют. Получают 0.,95 г Glp-Nval-Pro-NHj (94% от тееретического), 0,36,fj -87,0° (, в уксусной кислоте).
Аминокислотный анализ: Glu 0,97 , (1,0), Nval 1,09 (1,0), Pro 1,00 (1,0).
Пример 3. Ь-Пироглутамил-Ь-пролил-Ь-пролинамид..
1-я стадия: гидрохлорид L-пролил-L-пролинамид.
2,28 г ( ммоль) H-Pro-NHa. и 3,81 г (10 ммоль) ВОС-Рго-ЪРРР растворяют в 40 мл диметилформамида, раствор трижды встряхивают в делительной воронке с 10 tui 1 н. соляной кислоты, ТРИХДЫ с 10 МП 1 н.
раствора бикарбоната натрия и один раз с 10 мл воды, сушат над безводным сульфатом натрия и упаривают. Остаток pacTBopsnoT в 5 мп этилацетата и смешивают с 10 мл 5 н. раствора соляной кислоты. Через 30 мин реакционную смесь разбавляют эфиром, выпавший в осадок продукт отфильтровывают и сушат в вакууме над безводной гидроокисью натрия. Получают 2,06 г H-Pro-Pro-NHj-НС1 (83% от теоретического выхода, считая на Boc-Pro-OPFP); 0,05.
2-я стадия: взвесь бензилоксикарбонил- 1-пироглутамил-1-пролил-L-пролинамид.
0,75 г (3 ммоль) H-Pro-Pro-NHa ilCl в 10 мл диметилформамида при охлаждении льдом и постоянном перемешивании смешивают с.О,42 мл (3 ммоль триэтиламина и 1,35 (3,15 ммоль) Z-Glp-OPFP. Через 5 мин добавляют 0,42 мл (3 ммоль) триэтиламина и после 10 мин перемешивания образовавшуюся густую суспензию упаривают в вакууме. Кристаллический остаток растирают с 8 мл этанола и оставляют в холодильнике на 3 ч. Полученный осадок отфильтровывают и сушат. Получают 1,0 г Z-Glp-Pro-Pro-NHg. (73% от теоретического), т.пл. 247-248 v(c разложением), R 0,19; ГаЛ) -82,В (, в уксусной кислоте) .
Вычислено,%: С 60,52Н 6,18; N 12,27.
N4
Найдено, % : С 60,03; Н 6,30/
N 12,20.
Мол.вес 456,50..
3-я стадия: Ь-пироглутамил-Ь-пролил-Ь-пролинамид.
К раствору 1,0 г (2,2 ммоль) Z-Glp-Pro-Pro-NH/j в 50 мл уксусной кислоты добавляют 0,2 г 10%-ный катализатор палладий/активированный угол и через смесь пропускают газообразный водород в течение часа. Катализатор отфильтровывают, фильтрат упаривают и остаток растирают с эфиром. Полученный аморфный сырой продукт (0,60 г) растворяют в воде, обесцвечивают активированным углем и прозрачный водный раствор лиофилизуют. Получают 0,50 г Glp-Pro-Pro-NH ( от теоретического); R 0,10 -223,1° (, в уксусной кислоте).
Пример 4. Ь-Пироглутамил-Ь-валил-Ь-пролинамид.
1-я стадия: гидрохлорид L-валил-L-пролинамид.
Раствор 0,49 г (4,2 мьюль) Н-Рго-NHa. и 0,82 г (2,14 ммоль) Boc-Val-OPFP в 10 мл диметилформамида после 30 мин стояния упаривают в вакууме. Полученное в остатке масло растворяю р 10 мл хлороформа, раствор дважны промывают в делительной воронке 3 м 1 н. соляной кислоты, трижды - 3 мл 1 н. раствора бикарбоната натрия и, наконец, с 3 мл воды, сушат над без водным сульфатом натрия и упаривают Остаток растворяют в 3 мл этилацета та и смешивают с 3 мл 5 н. раствора соляной кислоты в этилацетате. После 1 ч стояния реакционную смесь разбавляют эфиром, осадок ютфильтро вывают и сушат в вакууме над безвод ным едким натром. Получают 0,51 г H-Val-Pro-NHj (95% от теоретического выхода, считая на Boc-Va-1-OPFP) ; 0,10. 2-я стадия: бенэилоксикарбонил-Ь-пироглутамил-Ь-валил-Ь-пролинамид. Взвесь 0,38 г (1,52 ммоль)И-Уа1-Pro-NH2.10 мл диметилформамида при охлаждении льдом и перемешивании смешивают с 0,22 мл (1,52 ммоль) триэтиламина и 0,69 г (1,6 ммоль) Z-Glp-OPFP. Через Ю мин к смеси до бавляют 0,22 мл (1,52 ммоль) триэтиламина и после дополнилгельного 30 мин перемешивания реакционную смесь упаривают в вакууме. Остаток растворяют в 15 мл хлороформа, раствор дважды промывают в делительной воронке 5 мл 1 н. соляной кислоты, трижда 5 мл 1 н. раствора бикарбона та натрия и, наконец, 5 мл воды, су шат над безводным сульфатом натрия и упаривают ввакууме. Масляный остаток кристаллизуют, из эфира получают 0,54 г Z-Glp-Val-Pro-NH, (77% от теоретического), т.пл.ИбИб С, R 0,30, -100,5 (, в уксусной кислоте). 3-я стадия: Ь-пироглутамил-Ь-валил-Ь-пролинамид. Через раствор 9,65 г (21,2 ммоль Z-Glp-Val-Fro-NH2 в 300 мл воды пос де добавления 2 г 10%-ного катализа тора палладий/активированный уголь, в -течение 5 ч пропускают газообразн Водород. Катализатор отфильтровываю фильтрат упаривают. Полученное в остатке масло растворяют в этаноле. Раствор упаривают. Эту операцию повторяют дважды. Полученный аморфный твердый остаток растирают с эфиром, получают 4,47 г Glp-Val-Pro-NHi (Ь5% от теоретического), 0,34, Ы -104,9° (, в уксусной кифюте) . Аминокислотный анализ.: Glu 1,03 (1,01); Val 1,00 (1,0); Pro 0,94 ()- Пример 5. Ь-Пироглу тамил-Е-изолейцил-1,-пролинамид. 1-я стадия:бензилоксикарбонил-Ь Изолейцил-Ь-пролинамид. 51,4 г (0,1 моль) Z-Ile-OPFP и 12,5 г (0,11 моль) H-Pro-NH-i раство ряют в 250 мл диметилформамида.и раствор смешивают с 14,0 мл 0,1 моль) триэтиламина. Реакционную смесь оставляют на ночь при комнатной температуре, затем упаривают в вакууме. Полученное в остатке масло.растворяют в 500 МП хлороформа, раствор последовательно промывают в делительной воронке дважды 100 мл 1 н. соляной кислоты, дважды 100.мл 1 н. раствора бикарбоната натрия и один раз 100 мл воды, сушат над безводным сульфатом натрия и упаривают. Масляный остаток кристаллизуют из смеси 100 мл эфира и 100 мл н-гексана. Сырой продукт (31,7 г) перекристаллизовывают из смеси 60 мл этилацетата и 60 мл н-гексана. Получают 30,32 г Z-Ileu-Pro-NH,2 (84% от теоретического) , т .пл. 127-128С, Rf|- 0,54. 2-я стадия: гидрохлорид L-изолейцил-Ь-пролинамид. К раствору 24,0 г (66,5 ммоль) Z-Ileu-Pro-W в 470 мл метанола добавляют 30 мл 2,4 н. метанольного раствора соляной кислоты и 4 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение часа пропускают газообразный водород. Катализатор отфильтровывают, фильтрат упаривают. Остаток растирают с эфиром, сырой продукт (20 г) перекристаллизовывают из смеси метанола и эфира. Получают 16,05 г H-Ileu-Pro-Nii НС1 (81% от теоретического) , т.пл. 135-140° С, R 0,15.. 3-я стадия: бензилоксикарбонил-Ь-пирогл.утамил-1-изолейцил-Ь-пролинамид. Взвесь 0,90 г (3,5 ммоль) H-Ileu-Pro-NHj- HCl в 20 мл диметилформамида при охлаждении льдом и перемешивании смешивают с 0,49 мл (3,5 ммоль) триэтиламина и 1,57 г (3,7 ммоль) Z-Glp-OPFP. Спустя 5 мин добавляют 0,49 мл (3,5 ммоль) триэтиламина, смесь перемешивают еще 20 мин и упаривают в вакууме. Остаток растворяют в 30 мл хлороформа, раствор последовательно промывают в делительной .воронке трижды 7 мл 1 н. соляной кислоты, трижды 7 мл 1 н. раствора бикарбоната натрия и, наконец,.один раз 7 мл воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло несколько-раз обрабатывают эфиром,эфир декантируют, закристаллизовавшийся продукт отфильтровывают, растворяют в этилацетате и вновь осаждают добавлением, эфира. Получают 1,18 г Z-Glp-Ileu-Pro.-NHj. (71,5% от теоретического), т.пл. 87-89 С, 0,36,V.J -91,4° (, в уксусной кислоте}. Вычислено, %: С 61,00:Н 6,83 N 11,6. «4 . Найдено, % : С 59,19; Н 6,88 N 11,15. Мол.вес 427,55. 4-я стадия: .-пироглутамил-,-изолейцил-1.-пролинамид. К раствору 4,72 г (10 ммоль) Z-Glp-1 leu-rro-NH,j в 100 мл метанола добавляют 1 г 10%-ного катализатора палладий/активированный угол через смесь в течение часа пропуска ют газообразный водород. Катализатор отфильтровывают, фильтрат упари вают и остаток растирают с эфиром. Полученный сырой продукт 3,22 г) растворяют в воде и раствор осветляют активированным углем. Прозрачный водный раствор лиофилизуют, получают 3,3 г Glp-Ileu-Pro-NIia (98% от теоретического), Rf О, 45 ,b;J2 -100,7° (, в уксусной кислоте) Аминокислотный анализ: Glu 95 (1,0), Не 1,00 (1,0), Pro 1,02 (1, Пример 6. L-Пироглутамил-Ь-о -аминобутилил-Ь-пролинамид. 1-я стадия: пентафторфениловый эфир трет .-бутилоксикарбонил-L-: -аминомасляной кислоты. Взвесь 7,7 г (20 ммоль) ВОС-ЛЬи-ОН-ОСНЛ в 60 мл зфира смешивают с 20 мл 2 н. серной кислоты и встряхи вают до растворения суспендированно го вещества. Эфирную фазу отделяют, промывсшзт в делительной воронке 20 2 н. серной кислоты и затем 20 мл воды, сушат над безводным сульфатом .натрия и упаривают. Полученное в остатке масло (4,14 г) и 3,7 г (20 ммоль) пентафторфенола растворя ют в 25 мл этилацетата, раствор охлаждают ниже 5°С и при перемешивани смешивают с 3,92 г (19 ммоль) дициклогексилкарбодиимида. Реакционну смесь перемешивают в течение часа, охлаждая на ледяной бане, отфильтро Бывают выпавшую в осадок дициклогексилмочевину, фильтрат упаривают. По лученное в остатке масло растворяют в н-гексане и раствор оставляют на час в холодильнике. Выпавшую в осад дициклогексидмочевину отфильтровывают и фильтрат концентрируют до объема 20 мл, с началом кристаллизации суспензию оставляют в холодил нике на ночь, затем кристаллы отфильтровывают. Получают 5,57 г Вос-Abu-OPFP (76% от теоретического), т.пл. 83-84°С, 0,8б,Гс;л -32,8 (, в этилацетате). Вычислено, %: С 48,79:Н 4,37/ N 3,79;F 25,7. С,5И,б04 NP Найдено, % : С 48,55;Н 4,28/ N 3,70-, I- 25,44. Мол.вес 369,29. 2-я стадия; гидрохлорид-L-c -аминобутирил-,1,-пролинамид. Раствор 3,2 г (28- ммоль) H-Pro-N и -5,16 г (14 имoль) Boc-Abu-OPFP в 60 мл диметиЛформаглида выдерживают 5мин и затем упаривают в вакууме. Полученное в остатке масло растворяют в 100 мл хлороформа, раствор промывают в делительной воронке дважды 20 глл I н. раствора бикарбоната натрия, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло растворяют в 20 мл этилацетата и смешивают .с 20 мл 6н. раствора соляной кислоты в этилацетате . Через час реакционную смесь разбавляют эфиром, выпавший в осадок продукт отфильтровывают, сушат в вакууме над безводным едким натром. Полученный сырой продукт (3,86 г) растирают с 20 мл холодного (диметилформамида). Получают 2,40 г H-Abu-Pro-N11 (73% от теоретического выхода, считая на Boc-Abu-OPFP), 0,10. 3-я стадия: бензилоксикарбонил-L-пиpoглyтaмил-I,-c -a 1Инoбyтиpил-L-пролинамид. 2,13 г (9 ммоль) H-Abu-Pro-Nll взмучивают в 30 м.п диметилформагшда и при охлаждении льдом и перемешивании смешивают с 1,26 мл (9 ммоль) триэтиламина и 3,95 г (9,2 ммоль) Z-Glp-OPFP. Через 5 мин к смеси добавляют еще 1,26 мл (9 ммоль) триэтиламина и после 20 мин перемешивания реакционную смесь упаривают в вакууме. Кристаллический осадок растирают с 20 мл этанола, оставляют в холодильнике на ночь и фильтруют. Получают 3,30 г L-Glp-Abu-Pro-NH (82% от теоретического)г т.пл.17517600, RJ О, 2 8,raj 25- -99,6(, в уксусной кислоте). 4-я стадия: Ь-пироглутамил-Ь-1-{ -аминобутнрил-L-пролинамид. Раствор 2,67 г (6 ммоль) Z-Glp-Abu-Pro-Nil-jj в 100 мл уксусное кислоты смешивают с 0,5 г 10%-ног катализатора палладий/активированный уголь, через смесь в течение часа пропускают газообразный водорсд. Катализатор отфильтрови.ьа:от, фильтрат упаривают и остаток растирают с эфиром. Полученный продукт (1,82 г) растворяют в воде, раствор обесцвечивают активированным углем и прозрачный водный раствор лиофилизуют.Получают 1,70 г Glp-Abu-Pro-NH(91% от теоретического) ,R-| 0,24,(3, -102,5° (. в уксусной кислоте). П р. и м е р 7. Ь-Пироглутамил-Ь-с6-аминодеканоил-Ь-пролинамид. 1-я стадия: гидрохлорйд L-oC-аминодеканоил-L-пролинамид. Раствор 1,37 г (12 ммоль) Н-Рго-NHi и 2,72 г (6 г-фюль) Boc-Ada-OPFP в 20 МП диметилформамида выдерживают 5 мин,затем упаривают в вакууме.Полученное в остатке масло растворяют в 50 мл хлороформа, раствор промывают в делительной воронке трижды 10 мл 1 н. соляной кислоты, трижды 20 :лп 1 н. раствора бикарбоната натрия и, наконец, дважды Ю мл воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло растворяют в 3 мл этилацетата и раствор смешивают с 5 мл 6 я. раствора соляной кислоты в этилацетате. После 1 ч стояния, реакционную смесь разбавляют эфиром, выпавший в осадок продукт отфильтровывают и сушат в вакууме над безводной гидроокисью натрия. Получают 1,75 г H-Ada Pro-NH - HCl (91% от теоретического выхода, считая на Boc-Ada-OPFP). 2-я стадия: бензилоксикарбонил-L-пироглутамил- Ь-т« -аминодеканоил-Ь-пролинамид. Раствор 1,75 г 5,5 ммоль) H-AdaPro-NHg и 2,58 г (6 ммоль) Z-Glp-OPFP в 30 мл диметилформамида смеши вают с О,77мл (5,5 ммоль) триэтилами на. Спустя 5 мин к смеси добавляют еще 0,77 МП (5,5 ) триэтиламина и после 20 мин перемешивания реакционную смесь упаривают в вакууме. Остаток растворяют в 50 ют хлороформа, раствор промывают в делительной воронке трижды 2Q мл 1 н. раствора соляной кислоты, трижды 20 мп 1 н. рас твора бикарбоната натрия и, наконец, дважды 20 мл воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке вспененное масло растирают с эфиром, образовавшуюся при этом желатинового типа суспензию оставляют стоять в течение 2 ч в холодильнике, затем осадок отфильтровывают и сушат. Сырой продукт (2,61 г) перекристаллизовывают из 20 мл этилацетата. Получают 2,45 г Z-Glp-Ada-Pro-NH. (84% от теоретиче.с кого , т.пл. 103-105°С, Яф 0,19, MJ -63,7 (, в уксусной кислоВычислено,%: С 63,62-, Н 7,63 N 10,60. 4 Найдено, % : С 63,24; Н 7,81, N 19,47. Мол.вес 528,65. . 3-я стадия: Ь-пироглутамил-Ь-оС-аминодеканоил-Ь-пролинамид. Раствор 1,9 г (3,6 ммоль) Z-Glp-Ada-Pro-NHj B 40 мл уксусной кислоты смешивают с 0,2 г 10%-ного катализа(гора палладий/активированный уголь и через смесь в течение часа пропускают газообразный водород. Затем катализатор отфильтровывают, фильтрат упаривают и остаток растворяют в воде. Водный раствор обесцвечивают активированным углем и упаривают. По лученное в остатке масло растворяют в 30 мл хлороформа, раствор сушат над безводнЕЛм сульфатом натрия и упа ривают. Вспененный, аморфный, твердьШ остаток растирают с эфиром, отфилйтровывают и сушат. Получают 1,20 г Glp-Ada-Pro-Nilu (02% от теоретического), 0,.55, -66,2(, в уксусной кислоте). Пример 8. Ь-Г,ироглутамиЛ-Ь-циклогексилаланил-Ь-пролинамид. 1-я стадия: пентафторфениловцй эфир трет-бутилоксикарбонил-Ь-циклогексилала нин. , Суспензию г (20 ммоль) Вос-Cha-OH DCHA в 80 мл эфира смешивают с 20 мл 2 н. серной кислоты. Смесь встряхивают до полного растворения твердого вещества, затем отделяют эфирную фазу, промывают 20 мл 2 н. серной кислоты 20 мл воды, сушат над сульфатом натрия и упаривают. Полученное в остатке масло- (5,7 г) растворяют в 30 мл этилацетата, смешивают с 3,7 г (20 ммоль) PFPOH. смесь охлаждают до и смешивают с 4,12 г (20 ммоль) дициклогексилкарбодиимида. Реакционную смесь перемешивают в течение часа при этой температуре, затем выпавшую в осадок дициклогексилмочевину, фильтрат упаривают и полученное в остатке масло растворяют в 30 мл н-гексана. Раствор оставляют в холодильнике на час, при этом вновь высадившуюся дициклогексилмочевину отфильтровывают и фильтрат разбавляют 70 мл н-гексана. Разбавленный раствор промывают .в делительной воронке пять раз 40 мл 1 н. раствора бикарбоната натрия, дважды 40 мл воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло кристаллизуют. Получают 8,48 г Boc-Cha-OPFP (97% от теоретического), т.пл .75-77С, 0,88. Вычислено,%s С 54,92; Н 5,53; 3,20|Р 21,72. Cг. Найдено, % : С 54,67- Н 5,66N 3,11-,F 21,43:Мол. вас 437,41. 2-я стадия: гидрохлорид L-циклогексилаланил-Ь-пролинамид. Раствор 2,28 г (20 ммоль) Н-Рго-NHj, и 4,37 (10 ммоль) Boc-Cha-OPFP в 40 мл диметилформамида после 5 мин стояния упаривают в вакууме. Полученное в остатке масло растворяют в 80 мл хлороформа, раствор промывают в делительной воронке трижды 20 мл 1 н. соляной кислоты, трижды 20 мл 1 н . раствора бикарбоната натрия и, наконец, .один раз 20 мл воды, -сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло растворяют в 8 мл этилацетата, смешивают с 10 мл 5 н. раствора соляной кислоты в этилацетате ц тереэ час реакционную смесь разб::. -яют Эфиром, йлпавший в осадок .. ст отфильтровывают и сушат в вакууме над безводным едким натром. Получают 2,98 г H-Cha-Pro-Ni.- НС (97% от теоретического выхода, считая на Boc-Cha-OITP). 3-я стадия: бензилоксикарбонил-Ь-пироглутамил-Ь-циклогексилаланилпролинамид. Раствор 2,43 г (8 ммоль) Il-Cha-Pro-Niri- ИС1 и 3,60 г (8,4 ммоль) Z-Glp-OPFP в 25 мл диметилформамида смешивают с 1,12 мл (8 ммоль) триэтиламина. Спустя 5 мин добавляют еще 1,12 глл (8 ммоль) триэтиламина и реакционную смесь перемешивают 20 мин и упаривают в вакууме. Остаток растворяют в 80 мл хлороформа, раствор промывают в делительной воронке трижды 20 мл 1 н. соляной кислоты, трижды 20 мл 1 н. раствора бикарбоната натрия и, наконец, один раз 20 ют воды, сушат над безводным сульфатом натрия и упаривают; Полученное в остатке масло кристаллизуют из эфира, полученный сырой про дукт (3,88 г) перекристаллизовывают из 30 мл этилацетата. Получают 3,32 Z-Glp-Cha-Pro-Nll (81% от теоретического) , т.пл.165-166°С, Rf| 0,17, ij -67,3 (, в уксусной кисло те) . Вычислено,%: С 63,26; Н 7,08; N 10,93. ( Найдено, % : С 63,15- Н 7,04, N 10,91 Мол.вес 512,61. 4-я стадия: Ь-пироглутамил-Ь-циклогексилаланил-Ь-пролинамид. Раствор 3,07 г (6 ммоль) Z-Glp-Cha-Pro-NHi 60 мл этанола, смешива ют с 0,6 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение 2 ч пропускают газообразный водород. Катализатор отфильтровывают, фильтрат упаривают и остаток растирают с эфиром. Получают 2,15 г аморфного твердого Glp-Cha-Pro-NHT. (95% от теоретического 0,50,i:otJ b -70,9°(, в уксусной кислоте). Пример 9. Ь-Пироглутамил-Ь тpeoнил-L-пpoлинa ид. 1-я стадия: гидрохЛорид О-бензил -Ь-треонил-Ь-пролина1 д. Раствор 1,43 г (12,5 ммоль) Н-Рг -NHi и 2,98 г (6,27 ммоль) Boc-Thr( -OPFP растворяют в 20 мл диметилфор амида, выдерживают 5 мин и упариваю в вакууме. Полученное в остатке масл растворяют в 30 мл хлороформа, раст промывают в делительной воронке дваж ды 10 мл 1 н. соляной кислоты, триж ды 10 мл 1 н. раствора бикарбоната натрия, сушат над безводным сульфато натрия и упаривают. Полученное в ос татке масло растворяют в 4 мл этилацетата и смегаивают с 5 мл 5 н. рас твора соляной кислоты в этилацетате. Реакционную смесь выдерживают 1 ч при комнатной температуре и разбавляют эфиром, отфильтровывают осадок и сушат в вакууме над безводным едким натром. Получают 2,05 г H-Thr(B7.1)-Pro-NIIj- HCl (95% от теоретического) , 0,40. 2-я стадия: бензилоксикарбонил-i,-пироглутамил-Ь-О-бензилтреонил-Ь-пролинa 1ид. К раствору 2,05 г (6 ммоль) И-Thr(Bzl)-Pro-NH2-ПС1 и 2,69 г. (6,27 ммоль) Z-Glp-OPFP в 21 мп диметилформамида по каплям прибавляют 0,84 мл (6 ) триэтиламина и после 5 мин стояния добавляют еще 0,84 мл (6 ммоль) триэтиламина, 20 мин реакционную смесь перемешивают, а затем упаривают в вакууме, остаток растворяют в 50 мл хлороформа, раствор промывают в делительной воронке дважды 10 мл 1 н. соляной кислоты и трижды 10 мл 1 н. раствора бикарбоната натрия, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло обрабатывают эфиром и охлаждают, продукт застывает в аморфном состоянии. Полученный продукт (2,76 г) растворяют в этилацетате и раствор обесцвечи- вают активированным углем. Уголь отфильтровывают, фильтрат упаривают и твердый, аморфный, вспененный остаток распирают с эфиром. Получают 2,47 г Z-Glp-Thr(Bzl)-Pro-Kll2 (75% от теоретического). 3-я стадия: Ь-пироглутамил-Ь-треонил-Ь-пролинамид. Раствор 2,04 г (3,7 ммоль) Z-Glp-Thr(Bz:l)-Pro-NIl2. в 40 мл уксусной кислоты смешивают с 0,4 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение 4 ч пропускают газообразный водород. Катализатор отфильтровывают, фильтрат упаривают и остаток растирают с эфиром. Полученный аморфный продукт (1,31 г) помещают в колонку, содержащую 30 г силикагеля (размер частиц: 0,063-0,2 мм) и элюируют продукт смесью растворителей (3). Фракции элюатов, содержащие чистый продукт, объединяют и упаривают, полученный в остатке сырой продукт обрабатывают эфиром. Получают 0,72 г Glp-Thr-Pro-Nll., (59,5% от теоретического), R|- 0,16, loLJ -90,0° (, в уксусной кислоте). Аминокислотный анализ: Glu 1,00 (1,0), Thr 0,99 (1,0), Pro 1,03 (1,0). Пример 10. L-Пироглутамил-О-трет-бутил-Ь-серил-1,-пролинампд. 1-я стадия: 0-трет-бутил-.-серил-пролинамид-полуоксалат. 8,0 г (70 ммоль) H-Pro-NHa, и 16,0 г (34,7 ммоль) Z-Ser()-OPFP растворяют в 120 мл диметилформамида и раствор после 5 мин стояния упаривают в вакууме. Полученное в остатке масло растворяют в 300 мп хлороформа, раствор промывают в де лительной воронке трижды 80 мп 1 н соляной кислоты, трижды 80 мл 1 н. раствора бикарбоната натрия и, наконец, один раз 80 мл воды,сушат на безводным сульфатом натрия и упаривают . Полученное в остатке масло (18 г) и 4,37 г (34,7 ммоль) дигидр та щавелевой кислоты растворяют в 300 мл метанола, раствор смешивают с 3 г 10%-ного катализатора паллади активированный уголь и через смесь в течение часа пропускают газообраз ный водород. Катализатор отфильтровывают, фильтрат упаривают, остаток растирают с этилацетатом и сушат в вакууме.. Получают 10,8 г H-Ser(Ви)-Рго-NH - (СООН)2. (90% от теоретического выхода, считая на Z-Ser(Ви)-OPFP в форме аморфного гироскопичного вещества), RSf 0,22. 2-я стадия: бвнзилоксикарбонил-L -пироглутамил-о-трет-бутил-Ь-серил -L-пролинамид. Раствор 6,43 г (18,5 ммоль) Н-Ser(Bu-t)-Pro-NHi- (СООН) и 3,97 г (18,5 ммоль) Z-Glp-OPFP.в 80 мл ди .-метил формами да смешивают с 5,18 мл (37 ммоль) триэтиламина. После 5 м стояния реакционную смесь упариваю в вакууме и кристаллический остато растираят с эфиром. Полученный сырой продукт (9,53 г) перекристал лизовывают из 120 мп метанола. По.лучают 7,70 г Z-Glp-Ser(But)-Pro-NHi (83% от теоретического), т.пл 226-229с, 0,46,ОО 71,6® (, в уксусной кислоте). I Вычислено, %: С 59,75, Н 6,82; IN 11,15. - / : c, Найдено, % : С 59,55; Н 6,95N 11,09. Мол. вес 502,57. 3-я стадия: L-пироглутамил-О-трет-бутил-Ь-серил-Ь-пролинамид. . 4,02 г (8 ммоль) Z-Glp-Ser(Bu)-Pro-NHj растворяют в 160 мл метаиола и раствор смешивают с 0,8 г ТО%-ного катализатора палладий/активированный уголь, через смесь в течение 30 мин пропускают газообразный водород. Катализатор отфильтровывают, фильтрат упаривают. Полу ченное в остатке масло кристаллизую из эфира, Jкpиcтaллы отфильтровывают и сушат. Получают 2,50 г Glp-Ser(BU -Pro-NHi (85% от теоретического), т.пл.186-187«С , R4 0,45,W: -60,8° (, в уксусной кислоте) Аминокислотный анализ: Glu 1,03 (1,0), Ser 1,00 (1,0), Pro 1,00 (1,0). Вычислено, %: С 55,42:Н 7,66, N 15,21С,7Н2Д% Найдено, % : С 55,07;; Н 7,61; N 14,94. Мол. вес 368,44. .Пример 11. L-Пироглутамил-В-лейцил-Ь-пролинамид. 1-я стадия: пентафторфениловый эфир трет-бутилоксикарбонил-В-лейцил. Раствор 4,62 г (20 ммоль) Вос-D-Leu-OH и 4,23 г (22 ммоль) PFPOH -в 50 мл этилацетата при охлаждении льдом и перемешивании смешивают с 4,12 г (20 ммоль)дициклогексилкарбодиимида. Реакционную смесь перемешивают, охлаждая в ледяной бане, отфильтровывают выпавшую в осадок дициклогексилмочевину, фильтрат упаривают. Полученное в остатке масло растворяют в 100 мл н-гексана, раствор оставляют на час в холодильнике и выпавшую в осадок дициклогексилмочевину отфильтровывают. Фильтрат промывают в делительной воронке пять раз 50 мл 1 н. раствора бикарбоната натрия и дважды 50 мп воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло кристаллизуют в течение ночи. Получают 7,0 г Boc-D-Leu-OPFP (88% от теоретического), т.пл.53-55 С, Л 4-31,7(, в этилацетате) . Вычислено,%: С 51,39; Н 5,07/ N 3,53iF 23,91 С НздОи NFfНайдено, % : С 51,51; Н 4,68; N 3,66; F 23,65. Мол.вес 397,35. 2-я стадия: гидрохлорид D-лейцил-Ь-пролина мид. . Раствор 3,42 г (30 ммоль) Н-Рго-NH и 60,0 г (15 ммоль) Boc-D-Leu-OPFP в 60 МП диметилформамида после 5 мин стояния упаривают в вакууме . Остаток растворяют в 100 мл хлороформа,раствор прогллвают в делительной воронке дважды 20 мп 1 н. раствора соляной кислоты, трижды 20-мл 1 н, раствора бикарбоната натрия и, наконец, один раз 20 мл воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло растворяют в 10 мп этилацетата, раствор сманивают с 15 мп 4 н. раствора соляной кислоты в этилацетате,через час реакционную смесь разбавляют эфиром, осадок отфильтровывают и сушат в вакууме над безводным едким натром. Получают 3,66 г H-D-Leu-Pro-NHg- HCl (92,5% от теоретического выхода, считая на Boc-D-Leu-OPFP), 0,25..
3-я стадия: бензилоксикарбонил-L-пироглутамил-О-лейцил-Ь-пролинамид.
Раствор 3,66 г (13,9 ммоль H-D-Leu-Pro-NHj. НС1 и 6,43 г (15 ммоль) Z-Glp-OPFP в 50 мл диметилформамида при охлаждении льдом и перемешивании смешивают с 1,95 мл (13,9 ммоль) триэтиламина. Смесь перемешивают 5 мин и затем добавляют к ней дополнительно 1,95 мл (13,9 ммоль) триэтиламина, реакционную смесь перемешивают еще 20 мин и упаривают в вакууме. Остаток растворяют, в 120 мл хлороформа, раствор промывают в делительной воронке трижды 30 мл 1 н. раствора соляной кислоты,трижды 30 МП 1 н. раствора бикарбоната натрия и, наконец, 30 ит воды один раз, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло кристаллизуют после обработки эфиром. Полученный сырой продукт (6 г) перекристаллизовывают из 30 мл этанола. Получают 5,48 г Z-Glp-D-Leu-Pro-NHi (77% от теоретического), т.пл.18919.4С VRf 0,48;И25 зз,2 (, в уксусной кислоте).
4-л стадия: Ь-пироглутамил-В-лейцил-Ь-пролинамид.
Раствор 3,78 г (8 ммоль) Z-Glp-D-Leu-Pro-NH в 150 ма метанола, смешивают с 0,8 г 10%-ного катализатора палладий на активированном угле и через смесь в течение часа пропускак т газообразный водород. Катализатор отфильтровывают, фильтрат упаривают и остаток растирают с эфиром. Полученный сырой продукт (2,5 г) растворяют в воде, обесцвечивают активированным углем и прозрачный водный раствор лиофилизуют. Получают , 2,35 г Glp-D-Leu-Pfo-NH (87% от теоретическогоУ, R 0,48,,3 (, в уксусной кислоте).
Пример 12. L-Пироглутамил-Ь-лейцил-Ь-пролин-этиламид.
1-я стадщя: гидрохлорид L-лейцил-L-пролин-этиламид.
Суспензию 1,67 г (7,2 ммоль) Н-Pro-NH-Et-(COOH)i в 20 мл этилаце- тата смешивают с 2,0 мл (14,4 ммоль) триэтиламина и 2,38 г (6 ммоль) Вос-Leu-OPFP. Через 5 мин реакционную -смесь промывагот в делительной воронке дважды 5 мл 1 н. раствора соляной кислоты, трижды 5 мл 1 н. раствора бикарбоната натрия и, наконец, один раз 5 МП воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло обрабатывают 10 МП 5 н. раствора соляной кислоты в этилацетате, через 20 мин смесь разбавляют эфиром, осадок отфильтровывают и сушат в вакууме над безводным едким натрием. Получают 1,46 г гигроскопического H-Leu-Pro-NH-Et-НС1
(83% от теоретического выхода, считая на Boc-Leu-OPFP), R 0,43.
2-я стадия: бензилоксикарбонил-Ь-пироглутамил-Ь-лейцил-Ь-пролин.
1,17 г (4 ммоль) H-Leu-Pro-NH-Et-НС1 и 1,72 г (4 ммоль) Z-Glp-OPF растворяют в 15 МП диметилформамида и раствор смешивают с 0,56 мл (4 ммол триэтиламина. Через 5 ми.н добавляют оставшиеся 0,56 мл (4 ммоль) триэтиламина и смесь упаривают в вакууме.Полученное в остатке масло растворяют в 40 МП хлороформа, раствор промьавают в делительной воронке дважды 10 мл 1 н. раствора соляной кислоты, трижды 10 мл 1 н. раствора бикарбоната натрия и, наконец, один раз 10 мл воды, сушат над безводным сульфатом натрия и упаривают. Остаток растирают с н-гексаном и отфильтровывают. Получают 1,61 г аморфного Z-Glp-Leu-Pro-NH-Et (80,5% от теоретического), «4 0,50,с/.-89,0° (, в уксусной кислоте).
3-я стадия: Ь-пироглутамил-Ь-лейцил-Ь-пропин-этиламид.
Раствор 1,07 г (2,14 ммоль) Z-Glp-Leu-Pro-NH-Et в 30 мл водЫг смешивают с 0,25 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение получаса пропускают газообразный водород. Катализатор отфильтровывают, фильтрат упаривают, масляный остаток растворяют в 20 МП хлороформа, раствор сушат над безводным сульфатом натрия и упаривают . Отверждающийся после вспенивания остаток растирают смесью эфира и н-гексана. Получают 0,52 г Glp-Leu-Pro-NH-Et (66% от теоретического). 0,57ЛЫ35 -94,5 (, в уксусной кислоте).
Пример 13. L-Пироглутамил-Ь-лейцил-Ь-пропил-н-дециламид.
1-я стадия: бензилоксикарбонил-L-пропин-н-дециламид.
Раствор 5,0 г (20 ммоль) Z-Pro-OH в 50 W диметилформамида сманивают с 2,8 мл (20 ммоль)триэтиламина и охлаждают до -10 С. При этой температуре не прекращая перемешивание по каплям добавляют сначала 2,8 мп (21,5 ммоль) изобутилового эфира хлоругольной кислоты и через 10 мин 4,4 МП (22 ммоль) н-дециламина. По окончании добавления смесь в течение 30 мин перемешивают при и затем 2 ч при комнатной температуре. Полученную суспензию фильтруют, фильтрат упаривсцот и остаток растворяют в 100 МП этилацетата. Раствор промывают в делительной воронке четырежды 50 МП 1 н. раствора соляной кислоты, дважды 50 МП воды, сушат над безводHbJM сульфатом натрия и упаривгиот. Получён ное в остатке масло кристаллизуют при обработке н-гексаном. Получают 5,43 г Z-Pro-NH-f Hj (70% от теоретического), т.пл.7880 С, 0,75. .2-я стадия: Ь-пролин н-дециламид-пЪлуоксалат. Раствор 5,0 г (12,9 IMoль) Z-Pro-NH-QpHj и 2,02 г (16 ммоль)дигидрата щавелевой кислоты в 100 мл метанола смешивают с 0,8 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение 2ч.. пропускают газообоазный водород. По окончании ;гидрирования реакционную смесь нагревают, катализатор отфильтровывают и фильтрат упаривают. Крис таллический остаток растирают с эфиром, эфир отфильтровывают. Получают 3,9 г H-Pro-NH-qpH2,-n(COOH)a (88% от теоретического) , т .пл . 152-154С, R 0,16. 3-я. стадия: гидрохлорид L-лейцил-L-пролин-н-дециламид. Раствор 3,44 г (.100 моль) Н-Рго-NH-C,II,-()2. и 2,0 г (5 ммоль) Boc-Leu-OPFP в 30 мл диметилформамида смеишвают с 2,.8 мл (20ммоль) триэтиламина. Через 5 мин реакционную смесь упаривают и полученное в остат ке масло растворяют в 50 мл н-гексана. Раствор промывают в делительной воронке пять раз 30 мл 1 н. раствора соляной кислоты, трижды 30 2УШ 1 н. раствора бикарбоната натрия и, наконец, один раз 30 мл воды и упаривают Полученное в остатке мйсло растворяют в 10 МП 5 н. раствора соляной кислоты в этилацетате, раствор оставля ют на 30 мин и упаривают.-Вспенивающийся в вакууме аморфный остаток растирают с н-гексаном и сушат в вакууме над безводным едким натром.Получают 1,05 г H-Leu-Pro-NH-C H.-,-HCl (60% от теоретического выхода, считая на Boc-Leu-OPFP), . 0,17. 4-я стадия: ббнзилоксикарбонил-L-пнроглутамил-L-лейцил-L-пролин-дециламид. Раствор 1,03 г (2,55 ммоль) H-Leu -Pro-NH-C H,j в 10 мл диметилформa П дa смешивают с 0,36 г-ш (2,55 триэтиламина и 1,1 г (2,55 ммоль) Z-Glp-OPFP .Смесь перемешивают 5 мин, затем добавляют к ней еще 0,36 мл (.2,55 ) триэтиламина и после 20 квдн перемешивания реакционную смесь упаривают в вакууме. Остаток растворяют в 20 мл хлороформа, раствор промывают в делительной воронке пять раз 10 мл 1 н. раствора соляной кислоты, трижды 10 мл 1 н. рас твора бикарбоната натрия и, наконец, один раз 10 M.rt воды, сушат над безводным сульфатом натрия.и упаривают. Полученное масло кристаллизуют из зфира. Получают 1,22 г Z-Glp-Leu-Pro-Nl -C ILj (78% от теоретического), т.пл. 10 8-109 С, Щ 0,50, -74,5(, в уксусной кислоте) . Вычислено, %:С 66,64; Н 8,55; N 9,14. Сн. Найдено, % : С 66,43, Н 8,84, N 9,13. Мол.вес 612,82. 5-я стадия: L-пиpoглyтaмил-L-лeйцил-L-пpoлин-н-дециламид. 1,22 г (2 ммоль) Z-Glp-Leu-Pro-NH-C pHj растворяют в 30 мл метаноа, раствор смешивают с 0,2 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение 30 мин пропускают газообразный водород. Катализатор отфильтровывают, фильтрат упаривают и полученное в остатке масло обрабатывают н-гексаном. Выпавший осадок отфильтровывают. Сырой продукт (0,85 г) перекристаллизовывают из 4 мл этилацетата. Получают 0,74 г Glp-Leu-Pro-NH-C,oH.2 (77% от теоретического), т.пл . 140-141 С, ,,3° (, в уксусной кислоте). Аминокислотный анализ: Glu 0,97 (1,0), Leu 1,00 (1,0), Pro 1,01 (1,0). Пример 14. L-Пироглутамил-L-лeйцил-L-пpoлин-(2-диметиламиноэтил)-амид. 1-я стадия: трет-бутилоксикарбонил-L-пpoлин(2-диметиламиноэтил)-амид. Раствор 11,43 г (30 ммоль) Вос-Рго-ОРРР в 100 мл эфира смешивают с 6,54 МП (60 ммоль) Н,М-диметиламино-этиламкна и оставляют стоять на 10 мин. Смесь промывают в делительной воронке трижды 30 мл воды, водные фазы объединяют добавлением твердого карбоната натрия, устанавливают рН 10 и раствор экстрагируют этилацетатом (4x20 мл). Органические фазы объеди.няют, промывают 20 мл воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло кристаллизуют при стоянии. Получают 6,71 г Вос-Рго-ЫН-СН2 СНгЫ(СНз)/г. (78,5% от теоретического), ,29. 2-я стадия: дигидрОхлорид L-лейцил-L-пpcшин (.2-диметиламиноэтил )амида. 6,71 г (23,5 ммоль) Boc-Pro-NH-Cli,(CE) в течение 30 мин обрабатывают 30 мл 5 н. раствора соляной кислоты в этилацетате, затем смесь упаривают. Получаемое в остатке маело растворяют в 50.мл хлороформа и смешивают с 2,8 мл (20 ммоль) триэтилаг.1ина. Полученный прозрачный раствор сме1.1швают с 6,74 г (17 ммоль) Boc-Leu-OPFP и после 1 ч перемешивания по каплям добавляют еще 2,8 мл (20 ) триэтиламина. Смесь оставляют на ночь и на следующий день упаривают. Полученное в остатке маело растворяют в 50 мл воды, рН значение раствора устанавливают 10 путем добавления твердого карбоната натрия защищенный дипептид экстрагируют из водной фазы зтилацетатом. Этилацетатную фазу отделяют, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло в течение часа обрабатывают 5 н. раствором со-ляной кислоты в этилацетате, реакционную смесь упаривают и остаток растирают с эфиром. После отфильтровывания аморфный, сильно гигроскопич ный продукт сушат в вакууме над безводным едким натром. Получают 4,5 г H-Leu-Pro-NH-CH,CHi-N( ). 2НС1, R 0,05.
3-я стадия: Ь-пироглутамил-Ь-лейцил-Ь-пролин-(2-диметиламиноэтил)-амид.
Раствор 2,6 г (7 ммоль) H-Leu-Pro-NH-CH CH,(CH3-)i- 2НС1 растворяют в 30 млдиметилформамиДа, смешивают с 1,86 мл (14 ммоль) триэтиламина. Выпавший в осадок продукт отфильтровывают и маточник по каплям
iприбавляют при перемешивании к охлаждаемому льдом раствору 3,29 г
I(7,7 ммоль) Z-Glp-OPFP в 10 мл диметилформамида. По окончании добавления реакционную смесь оставляют на
Мчи затем упаривают в вакууме. Полученное в остатке масло растворяют в 50 мл воды, раствор с помощью концентрированной соляной кислоть; подкис ляют до рН 3 и трижды промывают в делительной воронке 20 мл этилацётата. Затем значение рН водного раствора путем добавления твердого карбоната натрия устанавливают на 10 и щелочной раствор экстрагируют этилацетатом (5-30 мл). Органические фазы объединяют, сушат над безводным сульфатом натрия и упаривают. Полученный маслообразный защищенный дипептид (3,05 г, 5,6 ммоль) растворяют в 60 мл воды, раствор смешивают с 5,6 мл 1 н. раствора соляной кислоты и 0,6 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение 30 мин пропускают газообразный водород. После отфильтровывания катализатора фильтрат упаривают,полученное в остатке масло растворяют в смеси из 50 мл хлоро,форма и 20 мл 1 н. раствора бикарбоната натрия. Фазы разделяют, хлороформенный слой сушат над безводным сульфатом натрия и фильтруют. Полученный аморфный продукт (2,0 г) растворяют в воде, раствор обрабатывают активированным углем и прозрачный водный раствор лиофилизуют. Получают ,12 г Glp-Leu-Pro-NHCH CH2,N(CH, (60% от теоретического), 0,06, ,l° (,. в уксусной кислоте)
Аминокислотный анализ: Glu 1,02 (1,0), Leu 1,00 (1,00), Pro 1,03 (1,0).
Пример 15. Амид L-пироглутамил-L-гистидил-П-пипеколиновой кислоты .
1-я стадия: амид бензилоксикарбонил-В-пипеколиновой кислоты.
Раствор 13,15 г (50 Фюль) Z-D-Pip-OH в 100 мл этилацетата смешивают с 7,0 мл (50 ммоль) триэтиламина. Смесь охлаждают до -20С и при этой температуре при перемешивании ней по каплям добавляют 6,5 мл (50 ммоль) изобутилевого эфира хлоругольной кислоты. После 15 мин пере мешивания при -10°С в смесь в течен полутора часов пропускают газообразный аммиак. Осадок отфильтровывают, маточник промывают в делительной воронке 1 н. раствором соляной кислоты, затем 1 н. раствором бикарбоната натрия и, наконец, водой, сушат над безводным сульфатом натрия и упаривают. Остаток кристаллизуют из смеси этилацетата и эфира, по- , лучают 11,5 г Z-D-Pip-NlIj (88% от теоретического), т.пл.114-115°С, R 0,50,,0 (с 1, в уксусной кислоте).
исчислено,%:N 10,68.
Q4lUO N5.
Найдено,%:. N 10,63
Мол. вес 262,30.
2-я стадия: П-пипеколиновой кислоты амид.
Раствор 3,93 г (15 ммоль) Z-Pip-NH в 75 мл метанола смешивают с 0,5 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение-часа пропускают газообразный водород. Катализатор отфильтровывают. Маточник упаривают и остаток растирают с эфиром. Получаю 1,70 г H-D-Pip-NH.2 (90% от теоретического), т.пл.1б1-1бзс ,,IO,
Г(,0° (, в метаноле).
З-я стадия: бензилоксикарбонил-Ь-глутаминил-Ь-гистидин-гидразид.
71,0 г (0,165 моль) Z-Gln-His-ОМ pacTBopsnoT в 700 мл диметилформамид и раствор смешивают с 33,6 мл (0,495 моль) гидраэингидрата. Реакционную, смесь оставляют на 3 дня, затем разбавляют 600 мл этилацетата и ночь выдерживают в холодильнике. На следующий день осадок отфильтровывают. Полученный сырой продукт (71,65 г) перекристаллизовывают из 1800 мл метанола. Получают 55,1 г Z-Gln-His-:N2.H3 (78% от теоретического), т.пл.198-200с, R| 0,28.
Вычислено, %: С 52,90; Н.5,84; N 22,72
Ч
Найдено, % : С 51,21; Н 5,73,
N 22,7.
Мол. вес 431,40.
4-я стадия: амид бензилоксикарбонил-Ь-глутаминил-Ь-гистидил-Ь-пипеколиновой кислоты.
Суспензию 5%39 г (12,5 ммоль) Z-Gln-His-N2 H в 100 мл диметил.формамида смешивают с 4,6 мл (37,5 ммоль) 8,1 н. раствора соляной кислоты в диоксане. Полученный раствор охлаждают до -20С, температуру поднимают до , при перемешивании по каплям добавляют к нему 1,63 МП (13,7 ммоль) трет-бутилнитрил-а. Реакционную смесь перемешивают при в течение 20 мин, затем по каплям к смеси добавляют 3,5 мл (25 ммоль) три:;тиламина, раствор 1,57 г (12,5 ммоль) H-D-Pip-NHj. и, наконец, еще 1,75 мл (12,5 ммоль) триэтиламина. Затем реакционную смесь перемешивают при -10 С в течение часа и оставляют на ночь в холодильнике при 2°С. На следующий день осадок отфильтровывают, маточник упаривают в вакууме. Аморфный остаток растирают с этилацетатом, Получемный сырой, продукт вносят на колонку с силикагелем и продукт элюируют смеI СЬЮ растворителейй (2). Фракции, содержащие чистый продукт, объединяют и упаривают, остаток растирают с эфиром и отфильтровывают. Получают 2,.76 г аморфного Z-Gln-His-D-Pip-NHi (42% от теоретического).,R 0,101
5-я стадия; амид Ь-гЙгроглутамил- -гистидил-В-пипеколиновой кислоты.
. Раствор 2,63 г (5 ммоль) Z-Gln -His D-Pip-NH2 мл уксусной кислоты, смеишвают с 0,5 г 10%-ного катализатора палладий/активированный уголь и через раствор в течение часа пропускают газообразный водород. Катализатор отфильтровывают, маточник нагревают до 60-70 С, смесь выдерживают 30 мин при этой температуре и затем упаривают в вакууме. Оста.ток растворяют в воде, раствор обрабатывают смолой Dowex-2 в ОН-форме и упаривают. Полученный сырой продукт вводят в колонку с силикагелем и элюируют смесью растворителей (1). Фракции, содержащие чистый продукт, . объединяют и упаривают, остаток растворяют в воде, раствор осветляют активированным у1лем и прозрачный водк раствор упаривают. Аморфный остаток сушат в вакууме над фосфорным ангидридом. Получают 704 мг Glp-His-D-Pip-NHa (51% от теоретического), RW 0,10,,0°(, в воде).
Аминокислотный aнaлиз:Glu 1,03 (1,0), His 1,00 (1,0), Pip 0,96 vl,07 .
П р и и е р 16 .Ь-Пироглутамил-Ь-гистидил-Ь-гомопролинамид.
1-я стадия: трет-бутилоксикарбонил-Ь-гомопролинамид.
2,29 г (10 ммоль;ВоС-HPго растворяют в 30 мл этилацетата, раствор смешивают с 1,4 мл (10 г.1моль) триэтиламина и охлаждают до . Поддерживая температуру реакционной смеси -10°С, по каплям добавляют 1,3 мл (10 ммоль) изобутилового эфира хлоругольной кислоты. После 15 мин перемешивания при в реакционную смесь в течение получаса пропускают 0 газообразный , после чего смесь оставляют на 2 ч при температуре от О до 5°С. Затем отфильтровывают осадок, фильтрат упаривают и полученное в остатке масло растворяют в 30 мл 5 хлороформа. Раствор промывают в делительной воронке дважды 10, мл 1 н. раствора соляной кислоты, затем дважды 10 мл 1 н. раствора бикарбоната натрия и, наконец, один раз 10 мл Q воды, сушат над безводным сульфатом натрия и упаривают. Полученное в остатке масло кристаллизуют из н-гексана. Полученный сырой продукт (1,96 г) перекристаллизовывают из 5 смеси этиладетата эфира. Получают 1,78 г Boc-HPro-NIi, (78% от теоретического), т.пл. 138-140 С; R 0,43,,85(, в уксусной ки.слоте),.
Вычислено, %: С 57,87; Н JB,83; N 12,27.
ОмН,,„О N5.
Найдено, % : С 57,6.0; Н 8,89, N 12,.11.
Мол.вес 228,29.
5 2-я стадия: гидрохлорид L-гомопролинамид.
1,6 г (7 ммоль) Boc-HPro-NH растворяют в 10 мл этилацетата при нагревании. Раствор охлаждают до 0 комнатной температуры и смешивают . с 10 мл 6 н. раствора соляной кислоты в этилацетате. Реакционную смесь оставляют на час, затем разбавляют эфиром, полученный осадок растирают 5 и фильтруют. Получают 1,05 г Н-НРго-NH/ -НС1 .(91% от теоретического), т.пл. 178-180°С, 0,32,ro(j25 +26,2(, в метаноле).
3-я стадия: бензилоксикарбонил 1- глутаминил-Ь-гистидил-Ь-гомопролинамид.
Суспензию 5,39 г (12,5 ммоль) Z-Gln-.His-N2.H (см.пример 15, 3-я стадия) в 100 мл диметилформамида
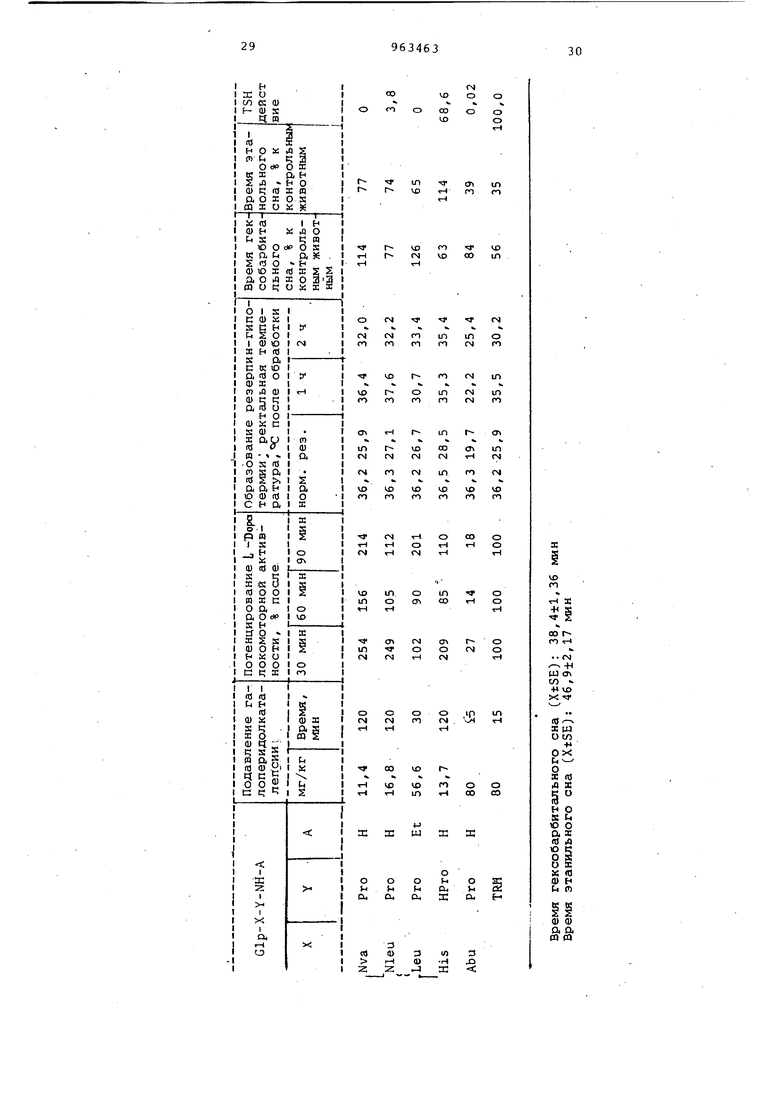
5 смешивают с 4,6 мл (37,5 ммоль) 8,1 н, раствора соляной кислоты в диоксане. Полученный раствор охлаждают до -20с, затем температуру поднимают до и при перемешива0 НИИ к реакционной смеси по каплям добавляют 1,63 глл (13,7 ммоль) трет-бутилнитрила. Реакционную смесь перемешивают 20 мин при -10с, затем смешивают с 3,5 мл (25 ммоль) три5 этиламина.Раствор 2,07г (12,5 ммоль) ll-MPro-Ntl - ll(;i в 10 мл диметилформамида спешивают с 1,75 мл (12,5 ммол триэтиламина. Осадок отфильтровывают. Полученный раствор охлаждают до -10°С и по каплям добавляют к азидно му раствору и, наконец, к смеси добавляют 1,75 мл (12,5 ммоль) триэтил амина. Реакционную массу в течение часа перемешивают при и после этого оставляют на ночь при 2 С. На следующий день осадок отфильтровывают, фильтрат упаривают в вакууме и аморфный остаток растирают с этилаце татом. Полученный сырой продукт вводят в колонку с силикагелем и элюируют смесью растворителей (2). Фракции, содержащие чистый продукт, объе диняют и упаривают, а остаток растирают с эфиром. Получают 2,35 г Z-Gln -His-HPro-NH (36% от теоретического 0,30. 4-я стадия: Ь-пироглутамил-Ь-гистидил-L-гомопроли намид. Раствор 2,1 г (4 ммоль) Z-Gln-His -HPro-NH. в 40 мл уксусной кислоты смешивают с 0,4 г 10%-ного катализатора палладий/активированный уголь и через смесь в течение часа пропуск ют газообразный водород. Катализатор отфильтровывают маточник нагревают до температуры от 60 до и при ,, этой температуре выдерживают 30 мин и затем упаривают в вакууме. Получен ный в остатке сырой продукт обрабаты вают ионообменной смолой, как описано в примере 15, 5-я стадия, и чистят на колонне с силикагелем. Получают 618 мг Glp-His-HPro-NHi (56% от теоретического), R 0,08,,0 (, в метаноле). Аминокислотный анализ: Glu 0,97 (1,0),- His 1,00(1,0), HPro 0,91 (1,0 Полученные согласно изобретению трипептиды с помощью описанных ниже биологических методов были проверены на их фармакологические действия. 1. Подавление галоперидол-каталепсии у крыс. Животным подкожно вводят 40 мг/кг галоперидола-4-(р-хлорфенил)-1-rt 3- (р-фторбензоил) -пропил -пиперидин-4-ола и через 120 мин контролируют наступление каталепсии, затем крыс разделяют на группы по 10 живот ных в каждой и внутривенно вводят до зами TRH и соответствующие трипептиды. Животных контрольной группы обрабатывают физиологическим раствором поваренной соли. Через 15,30,90 и 120 мин после обработки проверяют устраняющее каталепсию действие отдельных соединений. Каталептическими считают тех животных, которые, если передними лапами установить на колонну высотой 7 см. Не меняют своего положения в течение 30 с. Опыты проводят с WiStar-крысами, самцами весом от 160 до 180 г. 2 . Потенцирование локомоторной активности у мышей. Животным, внутрибрюшинно вводят каждой вначале 40 мг/кг Ы-метил-Ы-пропаргил-бензиламина, затем 20 мг/кг TRU соответственно равные дозы исследуемых новых трипептидов и, наконец, 100 мг/кг L-Dopa. Через 30,60 и 90 мин после обработки измеряют локомоторную активность животных, определенные значения указаны в таблице в процентах (сравнивают со значениями, полученными на животных,обработанных TRH). Для опытов используют по 15 мышей самцов весом от 18 до 22 г. . . 3.Peзepпин-гипoтep шя-oбpatцaющee действие у мышей. Мышей-самцов весом от 18 до 22 г делят на группы по 10 штук в каждой, внутрибрюшинно вводят 5 мг/кг резерпина, через 16 ч животных обрабатывают дозами по 20 мг/кг TRH и соответствующего трипептида. Ректальную температуру животных измеряют перед обработкой их резерпином. В таблице приведены средние значения ректальных температур, измеренных у каждых 10 мышей. 4.Влияние на продолжительность сна, вызванного с помощью гексобарбитала. Мышай-самцам, разделенным на группы по 10 штук в каждой, внутривенно вводят по 60 мг/кг гексабарбитал-Na, затем через 10 мин внутрибрюшинно вводят TRH соответствующие изучаемым трипептида в-дозе по 20 мг/кг. В таблице указано время сна в процентах по отношению к значениям, измеренным у животных контрольной группы (средние значения из 10 животных) . 5.Этанольный наркоз. Мышам смешанного пола весом от 18 до 22 г, разделенным на группы по 20 животных в каждой, внутрибрюшинно вводят по 4,5 г этанола, через 10 мин животным внутрибрюшинно вводят изучаемые трипептиды дозами по 20 мг/кг. В таблице приводятся периоды сна в процентах по отношению к значениям, измеренным у животных контрольной группы (средние значения т,1э 20 животных). 6.Гормональная активность (TRHдействие)у крыс.. Wistar-крысы-самцы весом около 200 г делят на группы по 7-8 животных в каждой и внутривенно вводят дозами по 20 мг/кг TRH и соответствующих изучаемых трипептидов, TRHреакцию животных измеряют через 15 мин после обработки с TRH и соответствующими изучаемыми соединениями из плазкы животных с помощью радиоиммуиного исследования. Относительный уровень действия вычисляют по четырехточечному методу с помощью ТОА 101 Computer, причем уровень действия TRH рассматривают как 100.
Данные биологических действий некоторых соединений общей формулы I, определенные по вышеописанным фармакологическим методам, сведены в таблице. . .
Из данных таблицы видно., что путем замены His на алифатическую аминокислоту с прямолинейной или разветвленной углеродной цепью в TRH-молекуле вызывается прекращение или значительное снижение выделения TSH, причем, например, подавление вызванной галоперидолом кадалепсии QTaновится сильнее в 2-7 раз. Некоторые новые TRH-аналоги обнаруживают также существенное потенцирование локомоторной активности соответствующее
понижение периода сна, вызванного гексобарбиталом или этанолом.
Получаемые согласно изобретению новые трипептиды, а также их Фармацевтически применяемые соли или Комплексы могут быть применены в форме обычных лекарственных препаратов в терапии. Эти лекарственные препараты содержат активные.вещества в сопровождении пригодных для кишечного или парентерального введения неорганических или органических носителей. Лекарственные препараты могут быть изготовлены, например, в форме твердых лиофилизатов, в которые добавляют не вступающие во взаимодействие с пептидами соединения в качестве носителей, например, углеводы, также они могут быть изготовлены в виде концентрированных или разбавленных суспензий или эмульсий или таблеток или препаратов дпя инъекций. 319634 Формула изобретения Способ попучения трипептидамидов общей формулы i. . Glp-X-Y-NH-A (Т) 5 где X - Leu, D-Leu, Nleu, lieu, Val, Nvai. Thr, Pro, L-rf-аминобу-. терил,Ь-а-аминодеканоил, Ь-циклогексилаланил,1-«:-трет-,„ -бутилсерил- tt - 10 vr Г) . . , А - водррод/ А1К(С;( -0,0) , (CHj) NA1K() , . при условии, если X - Leu, то А имеет значение, отличающееся от водорода или X - His, Y НРго, D-пипеколил, отличающийся тем, что , наращивают пептидную цепь,начиная 3-32 с амида аминокислоты общей формуv мн д(ri- к - iNn - rt Ш где Y и А имеют указанные значения, с аминокислотами, Их производными ™ соответствующим дипептидом мето«° пентафторфениловых эфиров или азидным методом и, в случае использования глутаминовой кислоты, циклизации последней в пироглутамин с последующим снятием защитных групп. Источники информации, принятые во -внимание при экспертизе 1. Боданский М., Клаузнер Я.С. Активированные эфиры и стратегия пептидного синтеза.- Химия полипептидов. Под ред. П.Катосояниса. М., Мир, .1977, с.30-51.














| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения трипептидов | 1980 |
|
SU1085505A3 |
| Способ получения октапептидов | 1981 |
|
SU993816A3 |
| Способ получения пептидов в виде кислотно-аддитивных солей | 1982 |
|
SU1277903A3 |
| Способ получения метиловых эфиров октапептидов | 1981 |
|
SU1041030A3 |
| Способ получения пептидов или их солей | 1977 |
|
SU664560A3 |
| СПОСОБ ПОЛУЧЕНИЯ БУСЕРЕЛИНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2442791C1 |
| ПЕПТИДНЫЕ СУБСТРАТЫ ЦИСТЕИНОВЫХ ПЕПТИДАЗ СЕМЕЙСТВА ПАПАИНА | 2018 |
|
RU2717689C2 |
| Способ получения производных пироглутамил- -гистидил-3-алкилпролинамида | 1976 |
|
SU619101A3 |
| Способ получения пептидов | 1978 |
|
SU845773A3 |
| СПОСОБ ПОЛУЧЕНИЯ НОНАПЕПТИДЭТИЛАМИДА | 1995 |
|
RU2086561C1 |


Авторы
Даты
1982-09-30—Публикация
1980-06-26—Подача