(З) СПОСОБ ПОЛУЧЕНИЯ БИЦИКЛИЧЕСКИХ ПРОСТАГЛАНДЙН08 ИЛИ ИХ СОЛЕЙ
Изобретение относится к способу получения бициклических про7-1Hw-(lH-(cJH.)p-Il а,(нг) СА -(Щпг L i где R - свободная или этерифицированная карбоксильная группа; Z - водород или галоген; р - О или целое число .от 1 до 7 i q - 1 или 2;
Н Zi(44c} Н
-dHa -ci-cl-; (. и C-d.
стагландинов общей формулы
Z г (транс) -()„-R / R - водород, ОКСИ-, С -С -алкокСИ-, ap-C -Cg-алкокси-; ацилоксигруппа; Y - радикал, выбираемый из следующей группы: где Z - водород или галоид; одна из групп R и водород, ,-алкил, С -С -алкенил, С2-С -алкинил или арил, или другая - окси-, Ц-С -алкокси-, ар-С -С -алкоксигруп па, или Rg вместе образуют оксо группу; каждая из групп , которые являются одинаковыми или различными, может быть водородом, (,-алкилом ;или фтором. каждое из п и п, которые одинак вы или различны, равно О или является целым числом от 1 до 6; X - выбран из группы, состоящей и -0-, -S и -(СН)-, где га равно О или 1; R - выбран из группы, состоящей 13 (а) водорода, (Ь) С -С -алкила, (с) С -Сд-циклоалифатического радикала, незамещенного или замещенного .X dH-dHCdэ cd Ьн .заключающийся а том, что ацетиленовый карбинол формулы .чД и подвергают взаимодействию с -метокси-2-метилаллилхл6ридом в присутствии этилмагнийбромида и хлорной меди Cl /Однако в литературе отсутствуют сведения о способе получения фармакологически активных бициКлических простагландинов общей формулы (I). Цель изобретения - расширение ассортимента фармакологически активных простагландинов. Поставленная цель достигается тем, что согласно способу получения бицикли.ческих простагландинов общей формулы (I) или их солей соединения общей формулы 2it ()р-11 O-Cs. (И) одним или более заместителями, выбранными из группы, состоящей из С -Сб-алкила и С -С -алкоксигруппы (d)арила, незамещенного или замещенного одним или более заместителями, выбранными из группы, состоящей из галоида, галоид-С -С -ал.кила, Ц-С алкила или С -С -алкоксигруппы, и (e)тетрагидрофурила, тетрагидропиранФ1ла, пирролила, пиразолила, оксазолила, изоксазолила, пиридила, пиразинила, пиридазинила, пиримидинила незамещенных или замещенных одним или более заместителями, выбранными изгруппы, состоящей из галоида, галоид -С,-С,-алкила, С.|-С -алкила и G,- С -алкоксигруппы, или их солей, обладающих фармакологической активностью. Известен способ получения аналога по строению - соединения формулы i - о енз где R, р, Z, q и R имеют указанные значения подвергают взаимодействию с соединением формулы Тг f.5 (Ml) Е-(J-d о-№2)й,-х-( 6 где Е - Группа (С(,Н) или группа () 0,, где каждый из 1Г одинаковый или различный, алкил или арил; Z, Rj, R, п:,, Oj, X и Rg имеют указанные значения, полученные соединения формулы (|), где Re и R, взятые вместе, образуют оксогруппу; Y - -СН CZfj где 22 имеет указанные значения, подвергают восстановлению с получением соединения формулы (I), где одна из групп R. и Rj является водородом, а другая является оксигруппой; Y СН , где Z имеет указанные знамения, или при необходимости, восстанавливают соединение формулы (О) где R 2 и R, взятые вместе, образуют оксогруппу; Y -СН а 2, где 2п имеет указанные значения в соединение формулы (I), где одна из групп Ry- оксигруппой, а другая С -С -алкил, С -С -алкенил, С2 С -алкинил или арил, или при необходимости зтерифицируют соединение формулы (I), где одна из групп R и Rj -- оксигруппа, а другая - водород, C-j-Cfi-алкил, C-,-Ci,-an кенил, С -Сь-алкинил или арил; Y - -СИ CZj-, где Zj имеет указаниые значения-, с получением соединений формулы (I), где одна из групп RI и Rj- Ц-С -алкокси- или ар-С,, алкоксигруппа, а другая - водо-род, Сч-С()-алкил, С -С -алкенил, С2Cg-алкинил или арил; Y - -СН , где 2 имеет указанные значения, и или при необходимости гидрируют сое динение формулы (1), где Y - -СН , где Zj - водород, в соединение формулы (|),.где Y - -СН2СН2-, или при желании дегидрогалоидируют соеди нение формулы (I), где Z 2 водород; Y - СН CZ2-, где 2.- галоид, до получения соединения формулы (f), где Y - С С-; Z - водород или при необходимости гидрируют соединение формулы (I) и выделяют целевые продукты в свободном виде или в виде соли. Реакцию между альдегидом формулы (II) и соединением формулы (11J) проводят с избытком соединения форму лы (Ml), используют по крайней мере 1,01-молярный эквивалент соединения формулы (111) на каждый молярный эквивалент соединения формулы (II). Процесс осуществляют в инертном растворителе, таком как линейные и циклические эфиры, например этиловый эфир, тетрагидрофуран, диоксан, диметоксиэтан, алифатические или ароматические углеводороды, например Н-гептан, н-гексан, бензол, толуол, или галоидированные углеводороды, на пример метиленхлорид, тетрахлорэтан, а также смеси этих растворителей. Те пература реакции изменяется между температурой замерзания и кипения растворителей. Когда реакцию проводят с соединением формулы (III), где Е представляет собой (R«|0), предпочтитель ной температурой является комнатная а именно 10-25°С. В случае соединения формулы (Ml), в котором Е представляет собой (CqiH5), предпочтительной является температура кипения растворителя. Продукт реакции между соединением формулы (и) и соединением формулы 111) представляет собой смесь соеди нения формулы (I), где Y - транс-СН ,где Z2 имеет указанные значе 97 t ния, и соединения формулы (I), где Y - цис-СН , где Z имеет ука занные значения в соотношениях, меняющихся между примерно 90:10 и Восстановительное дегалоидирование соединения формулы (I), у которого Z., - галоид, приводящее к соединению формулы (I), в которой Z водород, осуществляют путем обработки например, ацетатом двухвалентного хрома или гидридом, таким как, три-(н-бутил)-оловогидрид, или, каталитическим гидрированием. Когда восстановительное дегалоидирование проводят ацетатом хрома, этот реагент прибавляют при перемешивании к охлажденному раствору соединения формулы (|), в которой Z - галоид, в смеси этанола и водного раствора гидроокиси натрия или калия в атмосфере азота. Когда дегалоидирование проводят с три-(н-бутил)-оловогидридрм, используют примерно 1,2 эквивалента восстановителя на каждый эквивалент соеди- нения формулы (), в которой Zt| галоид. Подходящими растворителями для этой реакции являются ароматические углеводороды, такие как бензол или толуол, а температура предпочтительно находится между комнатной и примерно 70°С. Каталитическое гидрирование соединения формулы (|), в которой 2, галоид, для получения соединения формулы ( I ), в которой Z - водород и Y , может быть проведено или при комнатной .температуре, или при нагревании этого соединения, например, при С, или при атмосферном давлении, или при давлении например, атм, в г растворителе, таком как, например, низший алифатический спирт, тетрагидрофурЗн, диоксан, бензол, толуол, в присутствии катализатора, такого как палладий или платина на угле или на СаСО, а в некоторых случаях в присутствии аммонийной соли, а именно ацетата аммония или пропионата аммония. Дегидрогалоидирование соединения формулы (И, где 2 - водород; Y -СН CZ2-, где галоид, для получения соединения формулы (f), в которой 2 - водорбд; Y - -С ЕС-, проводят с использованием дегидрогалоидирующих агентов, предпочтительно выбранных из группы, состоящей из диметилсульфинилкарбаниона диазобициклоундецена, диазобйциклононена, амида или алкоголята щелочного металла. Можно применять от 1 до 5 а предпочтительно от 1,5 до 1,8-молярного. эквивалента основного дегидрогалоидирующего агента на каждый моль соединения формулы {I).
Процесс дегидрогалоидирования предпочтительно проводят в отсутстви атмосферного кислорода, в инертном растворителе, таком как диметилсульфоксид, диметилформамид, гексаметилфосфоротриамид, линейном или цикличе ком простом эфире, таком как диметок сиэтан, тетрагидрофуран, диоксан, ар матическом углеводороде, например бензоле, толуоле, или жидком аммиаке, или в смеси этих растворителей. Температура реакции изменяется от температуры жидкого аммиака до 100 С но предпочтительна комнатная. Гидрирование соединения формулы (|), в которой У - -СН CZ2-, где Zo - водород, для получения соединения формулы О) в которой Y - -CHij-CH - Г1РОВОДЯТ, например, предпочтительно в спиртовом растворителе в присутствии платины или.палладия на угле в качестве катализатора при температуре примерно до . Восстановление соединения формулы (О, где Rn 5 взятые вместе оксогруппа; Y - -СН CZ, где Z2 имеет указанные значения, для получения соединения формулы (О, где уСН CZ2-, где Zg имеет указанные значения; один из Rg- водород, а другой - гидроксил, превращение соединения формулы (1), где R,j, и R, взятые вместе, - оксогруппа Y - -СИ CZj-, где 1 имеет указанные значения, в соединение формулы (I), где Y - -СИ CZ2-, где Zg имеет указанные значения; один из ВдИ R гидроксил, а другой - C-j-Сб-алкил, С -С -алкенил; С2-С,-алкинил или арил, заключается в 1,2-молярном присоединении к карбонильной труппе. Восстановление полученного соединения формулы (О, где R2 и R, взятые вместе - оксогруппа; Y -- -СИ CZ, где Iq имеет указанные значения для получения соединения формулы (I), где Y СН , где Z2 имеет указанные значения, для получения соединения формулы (г), в которой Y - -СН CZ2-, где Z2 имеет указанные значения; один из R и R - водород, а другой - гидроксил, предпочтительно проводят с помощью боргидрида щелочно го или щелочноземельного металла, предпочтительно натрий-, калий-, литий-, кальций-, магний- или цинкборгидрида, используя 0,5-6 моль восстанавливающего агента на каждый 1 моль соединения формулы (|). Восстановление можно осуществлять как в водном, так и в безводном инертном растворителе, таком как линейные или циклические простые эфиры, например этиловый эфир, тетрагидрофуран, диметоксиэтан, диоксан, алифатические или ароматические углеводороды, такие как Н-гептан или бензол, или галоидированные углеводороды, например хлористый метилен, или гидроксилсодержащие растворители, например метанол, этанол или изопропанол, или смеси этих растворител й. Температура реакции может меняться от -kQ°C до точки кипения использованиого растворителя, но предпочтительно температура находится в интервале от -20 до -125 С. Это восстановление приводит к смеси , ..-ОН ОН Д9УХ эпимеров ) и R(C - ) --.H спиртов, из которой могут быть выделены отдельные эпимеры, если это желательно, путем фракционной кристаллизации , например , из диэтилового эфира, Н-гексана, н-гептана, циклогексана, но предпочтительно с помощью хроматографии или на силикагеле, или на силикате магния, хроматографии на колонке или препаративной тонкослойной хроматографии, элюируют, например, хлористым метиленом, этиловым эфиром, изопро,оиловым эфиром, этилацетатом, метилацетатом, бензолом, циклогексаном или их смесями или же разделение проводят с помощь-ю высокоскоростной жидкостной хроматографии. Превращение соединения формулы (I), в которой RJ и RJ, взятые вместе, - оксогруппа; Y СН CZ2-, где Z2 имеет указанные выше значения в соединении формулы I, в которой один из R и Rj- С -С -алкил, Cj-CgалкениЛ, Сд-С -алкинил или арил, проводят путем обработки реактивом Гриньяра формулы R MgHaE, ГД9 Наб галоид; пр едпочтительно бром или йод; R - (-алкил, С -С -алкинил, С2-С -алкенили или ария, предпочтительно метил, винил, этинил, фенил. Реакцию Гриньяра проводят с 1,052 моль магниевого производного на каждый моль кетона, в безводном растворителе, который может быть линейным или циклическим простым эфиром, например этиловым эфирбм, тетрагидрофураном, диоксаном, диметоксиэтаном, или алифатическим или ароматическим углеводородом, например н-гептаном, н-гексаном, бензолом, толуолом, при до температуры кипения использованного растворителя. Предпочтитель но температура реакции находится в интервале от -60 до +10°С. Получение простого эфира соединения формулы (I), где У - СН CZ, где Z2 имеет указанные значения; один из R2 и R5 гидроксил, а другой - водород, С -С -алкил, Crj-C алкенил, ,-алкинил или арил, что бы получить соединение формулы (I), 8 которой Y - СН CZrj,, где l имеет указанные значения, один из Р17.и Rj- алкокси- или аралкокси, другой водород, С -С -алкил, С2-С -алкенил, С2 С алкинил или арил, может быть осуществлено, например, при взаимоде ствии соответствующего диазоалкана в присутствии катализатора, такого как фторборная кислота или трехфтористый бор, в среде органического раствори теля, такого как хлористый метилен, или путем взаимодействия гидроксильной группы в свободном виде или в ви де соли, с алкил- или аралкилгалоидо в присутствии основания, такого как окись серебра в среде такого растворителя , как диметилсульфоксид или диметилформамид. Соединения формулы (J) обладают гипотензивной активностью на млекопитающих и отличаются более высокой химической стабильностью. Из-за гипотензивного и сосудорасширяющего де йствия соединения формулы (I) являются полезными для лечения гангрены нижних конечностей, при нарушениях периферических заболевани сосудов, при профилактике и лечении таких болезней, как флебиты, гепаторенальный синдром, артериальная проходимость , непрепятствующая брыжеечная ишемия, артриты и ишемические изъявления ног. Среди соединений общей формулы (I 6 Н-производные обладают высокой про тивоагрегирующей способностью, и по95 . 10 этому являются особенно полезными средствами для ингибирования скоплений тромбоцитов, для профилактики.и лечения тромбозных образований и для уменьшения слипаемости тромбоцитов, для лечения и профилактики тромбозов и инфарктов миокарда, при лечении атеросклероза, а также при всех синдромах, этиологически основанных или ассоциированных с нарушением баланса липидов или гиперлипедемией, а также для лечени герпартритов, для профилактики мозговых йшемических эпизодов и для долгосрочного лечения после инфаркта миокарда. Соединения общей формулы {I) являются также полезными для стимуляции родов, для изгнания мертвого зародыша у беременной самки (как для людей, так и в ветеринарии), не обладают такими нежелательными побочными действиями природных простагландинов как понос и рвота. Эти соединения расширяют шейку матки, облегчая терапевтический аборт. Соединения общей формулы (I), в особенности соединение dl-6/ H-6,9«зC-oкиcь-16-м-xлopфeнoкcи-w -тетранор, обладают также способностью влиять на образование желтого тела и, следовательно, являются полезными для контроля оплодотворения. Цитопроектированная способность является общей отличительной чертой для всех соединений формулы (|). Соединения общей формулы (О являются полезными также для лечени обструктивных болезней дыхательных органов, таких как бронхиальная астма, так как они обладают значительной бронхорасширякнцей активностью., Пример I. К раствору 1,0 г dl-5 р -гидроксиметил-2с/. , ot-дигидрбксициклопентан-1ot-уксусная кислота-у-лактон-4-п-фейилбензоата в 8 мл бензол-ДМСО (75/25) добавляют при перемешивании 0,89 г дициклогексилкарбодиимида. При комнатной температуре добавляют 1 , мл раствора трифторацетата пиридиния, полученного из 1 мл трифторуксусной кислоты и 2 мл пиридина, доведенного до объема 25 мл с.помощью смеси бензолдиметилсульфоксид(ДМСО) в соотношении 75/25. Через 3 ч добавляют 19 мл бензола и смесь по каплям обрабатывают раствором 0,3 г дигидрада оксалиновой кислоты в 3,8 мл воды. Приблизительно через 15 мин перемешивания смесь отфильтробывают и органическую фазу промывают водой до нейтральной реакции, концентрируют до объема 2 мл и затем разбавляют 5 мл изопропилового эфира. Продукт выделяют фильтрацией и перекристаллизовывают из изопропилового эфира с получением 0,8 г- б1-5э-формил-2о{.,о -дигидроксицикл6пентан-1с -уксусная кислота- лактон- -П-фенилбензоата, т. пл. 129-13l C. Раствор 800 мг этого соединения в 2,8 мл безводного метанола обрабатывают 0,62 мл метилортоформиата и 18 мг моногидрата П-толуолсульфокислоты. Через 1 ч добавляют 0,01 мл пиридина и раствор выпаривают досуха. Остаток растворяют в этилацетате; промывают 1,0 н.раствором МаОН и затем насыщенным растворсУм NaCl до нейтральной реакции. Растворитель отгоняют при пониженном давлении и остаток перекристаллизовывают из метанола с получением 800 мг d1 -5 |b -диметоксиметил-2о, WL дигидроксициклопентан-1о -уксусная кислота- у-лактон- -п-фенилбензоата, т.пл. 108110°С.V
60 мг К-СО добавляют к раствору этого вещества в мл безводного метанола. Через k ч перемешивания при комнатной температуре раствор отфильтровывают, затем .его упаривают до малого объема и подкисляют насыщенным раствором NaHnPO. Метанол отгоняют и остаток переносят в этилацетат. Его промывают насыщенным раствором NaC до нейтральной реакции, сушат над безводным , фильтруют и. выпаривают лри пониженном давлении с образованием 480 мг dl-З/Ь-диме токсиметил-2с{.,4с1-дигиАроксициклопентан- lot-уксусная кислота- лактона.
Раствор этого вещества в 4 мл обрабатывают 0,32 мл 2,3-Д.игидропирана и ,8 мл п-толуилсульфокислоты. Через 4 ц пребывания при комнатной температуре добавляют пиридин и раствор выпаривают при пониженном давлении. Сырой продукт реакции отфильтровывают на 5 г силикагеля с помощью-смеси циклогекса,й/этиловый эфир (50/50) вкачестве элюента с образованием ЗВО мл d1-5/i-Димeтo.кcиметил-2с, с1-диг«дроксициклопентан-1с1-уксусная кислота-д лактон- -тетрагидропиранилозого эфира. Используя в качестве исходного вещества А-эфир 5/ь-диметоксиметил-2сЦ4о дигидроксициклопентан- 1е(1 уксусная кислота-у-лакт.она, например -П-фенилбензоат,
т. пл. 128-13000,00130 -85. или -эфир 5ct-гидpoкcимeтил-2p,i f дигидроксициклопентан-lot-уксусная кислота -рлактона, например «-iv-фенилбензоат, т. пл. 127-129°C,WJD +8,5.
По аналогичной методике получают следующие вещества: 5р диметоксиметил-2(., о дигидроксициКлопентан-1«/.-уксусная кислота- лактон- -тетрагид0 ропираниловый эфир и 5с(-диметоксиметил-2р, р-дигидроксициклопентан-1о -уксусная кислота- лактон- -тетрагидропираниловый эфир. Если вместо 2,3 дигидропирана исполъзуют 1,4-ди5 окс-2-ен получают соответствующие производные 4-диоксанилового эфира.
Пример 2. Раствор 21б мг 5/Ь-диметоксиметил-2(4оСгдигидроксициклопентан-1с/-уксусная кислота-jp0 -лактона, oi 3;р -16, (С 1,0 снеIj), а 1,6 мл диметилформамида обрабатывают О,3 мл триэтиламина и затем 291 мг диметил -трет-бутилхлорсилана. Через 1 ч
5 смесь разбавляют 8i,3 мл воды и экст.рагируют гексаном. Органическую фазу промывают водой и сушат над Na,-S0. с образованием 310 мл 5Д-Диметоксиметил-2Ы,с дигидроксициклопентан-1о(.0 -уксусная кислота-у-лактон- -диметил-трет-бутилсилилового эфира.
Пример З.-К раствору d I -5 /Ь -гидроксиметил-2о,tot-дигидроксициклопентан- lot-пропанОвая кислота-(лактон -4-П-фенилбензоата- (1 г) в 8 мл смеси бензол:ДМСО (75:25)добавляют 0,86 г дициклогексилкарбодиимида и затем 1,37 мл свежеприготовленного трифторацетата пиридиния(см. пример U.Через 3 ч добавляют 18 мл бензола, затем по каплям раствор 0,29 г дигидрата оксалиновой кислоты в 3,7 мл воды. Через 13 мин перемешивания дициклогексилмочевину удаляют фильтрацией и органическую фазу промывают водой до нейтральной реакции. Затем эту фазу концентрируют до объема приблизительно 2 мл и добавляют изопропиловый эфир. Получают 0,793 г dl-5 фopмил-2о,о.-дигидроксициклопентан-Ы-пропионовая кислота- р-лактон- -п-фенилбензоата.
Раствор 780 мг этого вещества в 2,7 мл безводного метанола обрабатывают 0,59 мл метилортоформиата и 17,3 мгп толуолсульфокислоты. Приблизительно через 1 ч добавляют 0,01 мл пиридина и раствор выпаривают досуха. Остаток переносят в этилацетат; органическую фазу промывают 1 н.раствором NaOH и затем насыщенным раствором NaCI до нейтральной реакции. Выпаривание досуха дает 7б9 мг d -5 -димeтoкcимeтил-2ot,W-дигидроксициклопентан-1оС-пропионоваякислота-у-лактон- -п-фенилбензоата. Это вещество растворяют в S, мл безродного метанола и добавляют 75 мг . После ч перемешивания при комнатной температуре и фильтрации раствор упаривают до небольшого объема и подкисляют насыщенным раствором . Метанол выпаривают и водную фазу обрабатывают этилацетатом затем органическую фазу промывают насыщенным раствором NaCl до нейтральной реакции , сушат и выпаривают в вакууме с образованием d 1 -5(5-Диметоксиметил-2оЬ, Wr дигидроксициклопентан-lot-лропановая кислота -у-лактона. Раствор этого вещества в Ц мл обрабатывают 0,3 мл 2,3 -дигидропирана и 4,5 мг п -толуилсульфокислоты. Через 4 ч при комнатной температуре добавляют 0,01 мл пиридина и раствор выпаривают досуха Продукт реакций очищают на силикагеле, используя в качестве элюента смесь циклогексана с этиловым эфиром (50:50) с образованием 480 мг d} -5/Ь-диметоксиметил-2Ы,4с дигидроксициклопентан- 1о1.-пропановая кислота-Т лактон-тетрагидропиранилЬвого. эфира. Используя в качестве исходных веществ 4-эфир 5 -гидрокси-метил-2оС, 4о1-дигидроксициклопентан-1о.-пропановая кислота-у лактона и 4-эфир Soi-гидроксиметил-2/5,4ргдигидроксииикло пентан- 1(/-пропановая кислота- лакто на (например, 4-п-фенилбензоат), по аналогичной методике получают следующие вещества: 5(Ь Диметоксиметил-2с W-дигидроксициклопентан- 1е/.-пропановая кислота-сЛ-лактон-4-тетрагидропираниловый эфир; 5о диметоксиметил-2 4(Ъ-дигидроксициклопентан-1 Ь-пропановая кислота-с/ лактон-4-тетрагидропираниловый эфир. Если вместо 2,3-Дигидропирана используют 1,4-диокси-2-енj то получаю соответствующие производные 4-диокса нилового эфира. Пример 4. Раствор 1 г 5/Jr -формил-2йЬ-гидроксициклопентан-1оС-уксусная кислота-} лактона в 6,5 мл езводного метанола обрабатывают 1,74 мл метилортоформиата и 52 мг п-толуилсульфокислоты. Приблизительно через 1ч добавляют 0,04 мл пириина и раствор выпаривают досуха. статок переносят в этилацетат и промывают 1 н.раствором NaOH и затем насыщенным раствором NaCl до нейтральной реакции. Выпариванием в вакууме получают 1 г 5 диметоксиметил-2о -гидроксициклопентан-1с гуксусная кислота- лактон, Cci -1б°. По аналогичной методике из 5/ формил-2с6-гидроксициклопентан-lot-пропионовая кислота- Л-лактона получают 5|5-формилдиметоксиметил-2с -гиддроксициклолентан-lot-лропионовая кислота-у-лактон. Пример 5. К раствору 960 мг d, 1-5|Ь диметоксиметил-2о1,4Ы-дигидроксипентан-lot-уксусная кислота-} лактон-4-тетрагидропиранилового эфира в 1б мл толуола, охлажденному до -70°С, добавляют 8,5 мл 0,5 н.раствора диизобутилалюминийгидрида в толуоле, в течение 30 мин. В течение последующих 30 мин при перемешивании при -70° по каплям добавляют 10 мл 2 М толуольного раствора изопропансла. Раствор нагревают до 0°С и обрабатывают 3 мл 30 -ного раствора NaHgPO. Через 1 ч перемешивания добавляют 12 г безводного Na2S04. Фильтрацией и вупариванием растворителя получают 900 мг dl-5fb димeтoкcимeтил-2о{.,4о(.-дигидроциклопентан-1о -этаналь-2 -лактол-4-тетрагидропираниловогоэфира. Пример 6. Следуя методике примера 5, раствор 400 мг 5/Ь-диметоксиметил-2о1,4 -дигидроксициклопентан-Ы-уксусная кислота-}1-лактон-4-диметил-трет-бутилсилилового эфира в П мл толуола, охлажденный до -70°С, обрабатывают добавлением по каплям. 5,9 мл 0,5 М толуольного раствора диизобутилалюминийгидрида с образованием 0,43 г 5/Ь Диметоксиметил-2о1, 4с1.-дигидроксицйклопентан-1с/-этаналь-г лактол-4-диметил-трет-бутилсилилового эфира. Пример 7. В атмосфере азота раствор 629 мг 5/ггдиметоксиметил-2оЛ, 4о4.-дигидроксициклопентан-1 ot-пропановая кислота-с лактон-4-тетрагидропиранилового эфира в 11 мл толуола, охлажденный до -70°С, обрабатывают, добавляя по каплям 5,9 мл 0,5 М то- луольного раствора диизобутилалюми;15 97нийгидрида. Через 30 мин при по каплям добавляют 10,9 мл 2 М толуольного раствора изопропанола, Температуру повышают до и добавляют 2 мл 30 -ного . Через 1 ч перемешивания добавляют 3,3 г безводного . и смесь фильтруют. Выпаривание органической фазы в вакууме дает 620 мг 5/5 диметоксиметил 2о1.,. 4о6-Аигидроксициклопентан-1(А-пропаналы -с -лактол-4-тетрагидропиранилового эфира. Пример 8. Используя .одну из методик, описанных в примерах , получают -ацеталь(4-тетрагидропираниловый эфир; -диоксаниловый эфир) и Л-димеТилбутилсилиловый эфир еледующих соединений: 5/Ь-Диметоксиметил-2о1,с -дигидроксициклопентан-1о -этаналь-у-лактол, а также его оптически активную форму (или паt-форму); Soi-диметоксиметил-2/3,/5-дигидроксициклопентан-1р1-этаналь-2Г-лактол (или ent-фсрму); 5 5Диметоксиметил-2о6, Ы-дигидроксициклопентан-1о1-пропаналь-сЛ-лактол в его d оптически активной форме (или nat); 5о -диметОксиметил-2р,4/ь-дигидроксициклопентан-1р-пропаналь-сГ-лактол (или ent-форму) . Пример 9. 0,29 мл абсолютнoгo этанола в 3,5 мл толуола по каплям добавляют k раствору 5 х натрий (2-метоксиэтокси)-алюмипий гидрида, 1,4 мл 70%-ного бензольного раствора, разбавленного 5 мл толуола и охлажденного до . 8,2 мл полученного таким рбразом раствора, добавляют . при -30°С к 0,98 г dl-5p-бeнзилоксиметил-2о6-тидроксициклопентан-lot-пропионовая кислота-с/ -лактона в 22 кл толуола. Через 45 мин избыток реагента охлаждают 6 мл 0,5 М толуольного раствора изопропанола. См.есь нагревают до 0°С, добавляют k мл 30 -ного и полученную смесь перемеши вают в течение 2 ч. Неорганические соли удаляют фильтрацией и раствор выпаривают досуха с образованием 0,94 г dC-5 -бензил6ксиметил-2о6-гидроксициклопёнтан-lci-пропанол-сЛ-лактола. . ., Используя описанную выше методику или одну из методик примеров 4-7,из соответствующих р-лактонов получают следующие соединения: 5/5-бензилоксиметил-2о(ггидроксициклопентан-1(-этаналь- -лактол; 5 -бензилоксиметил-2ог.-гидроксициклопентан-1с -пропа516наль-у-лактол; 5р-диметоксиметил-2о6-гидроксициклопентан-ТЫ-этаналь- у-лактол; 5|Ь-диметоксиметил-2(/-гидроксициклопентан-Ы-пропаналь-/Ь-лактол, . , Пример 10. При перемешиваниц и внешнем охлаждении для поддержания температуры реакции 20-22°С раствор 1,05 г трет-бутилата калия в 10 мл ДМСО по каплям добавляют к раствору 1,8 г -карбоксибутил-трифенилфосфонийбррми а и 0,38 г 5 -Диметоксиметил-2о1,юб-дигидроксициклопентан-Ы-этаналь-у-лактол- -тетрагидропиранилового йфира. После добавления смесь выдерживают при комнатной температуре в течение 1 ч и затем разбавляют 16 мл смеси лед - вода. Водную фазу экстрагируют эфиром (5x8 мл/ и смесью эфира с бензолом (70:30, 5x6 мл); неорганические слои после экстракции 0,5 М раствором NaOH (2 х х 10 мл) отбрасывают. Объединенную щелочную водную фазу подкисляют до рН ,8 NaH2P04 и затем экстра гируют смесью этиловый эфир; пентан (1:1; 5 х 1$ мл); из объединенных органических фаз после сушки и удаления растворителя получают 0, 5гцис-7-(2о1 ,/ c -дигидpoкcи-5/ -димeтоксиметилциклопентан-1о -ил)гепт-5-еновая кислота- -тетрагидропиранилового эфира. Его в свою очередь превращают в соответствующий метиловый эфир обработкой раствором диазометана в эфире. Аналитичёский образец ГОТОВЯТ адсорбцией 100 мг сырого продукта на 1 г силикагеля и элюированием смесью бензо; : этиловый эфир (85: l5). ЯМР: ( 5;4b м.д (мультиплeт. Пример 11. В безводной атмосфере азота суспензию 0,39 г масляной дисперсии NaH в ДМСО (13,5 мл) нагревают до 60-65 С в течение 3 - ч. После охлаждения до комнатной температуры и при поддержании температуры реакционной смеси 2022С в указанном порядке добавляют следующие растворы: 2,66 г Зкарбоксипропилтрифенилфосфонийбромида в 6 мл ДМСО и 0,6 г 5 диметоксиметил-2d-, гидроксициклопентан- lot-npoпаналь- /-лактол-4-тетрагидропиранилового эфира в 3 мл ДМСО. Смесь перемешивают в течение 3 Ч и затем разбавляют 35 мл воды. Водную фазу экстра179гируют этиловым эфиром (5 X 12 мя) и смесью этиловый эфир:бензол (70:30 7 X 12 мл). Объединенный органический Экстракт после повторной экстракции 0,5 н.растворбм NaOH (2x15 мл) отбрасывают , объединенный и елочной вод ный экстракт подкисляют до рН ,3 водным раствором NaHnPO и экстрагируют смесью этиловый эфир: пентан (1:1) с образованием, после промывки до нейтральной реакции, сушки Na2S04 и удаления растворителя, 0,71 г -бис-7-(2о1,4(А-дигидрокси5г диметоксиметил-4иклопент-1с -ил)-гепт- -еновой кислоты. После обработки диазометаном получают соот ветствующий метиловый эфир. Пример 12. Метиловый эфир следующих кислот получают из лактолов, следуя методикам примеров -8, в результате йбработки реагентом Виттига (получен из кapбoкcибyтилтрифенилфосфонийбромида или Зкарбок сипропилтрифенилфосфоний бромида) и последующей этерификации диазометаном, в виде оптически активных форм |-бис-.7-(2Ы-гидрокси-5/Ь-бензилоксиметилциклопент-1о1-ил)-гепт- -еновую;-цис-7-(2 о -гидрокси-5/5-диметоксиметилциклопент-1Ы-ил)-гепт- -еновую;5-бис-7-(2Ы-гидрокси-5/5-диметок симетилциклопент-1о -ил)-пент-5-еновую;5-бис-7-(2о6-гидрокси-5А -бензило симетилциклопент-1 oi -ил) -гепт-5-еновую; I 5-бис-7- (2ot ,kci -дигидрокси-5/Ь -диметоксиметилциклопент-1о4-ил)-геп -5-еновую и их -диоксаниловые, тетр гидропираниловые и диметил-трет-бути силиловые эфиры; -цис-7-(2(У-,Ас4.-дигидроксй-5/3-д метоксиметилциклрпент-1 oi-ил) -renT-i -еновая и ее Л-(диоксаниловый, тетра гидропиранилбвый и диметил-трет-бутил силиловый эфир; -цис-6-(2с51,|о -дигидрокси-5/Ь-диметоксимет.илцикл6пент-1о -ил)-гекс-4-енбаая и ее -тетрагидропира ниловый эфир. 5-бис-8-(2о1,|Ы-дигидрокси-5/Ъ-диметоксиметиЛциклопент-1с -ил)-окт -5-еновая и ее -тетрагидропираниловый эфир П р им е р 13. Раствор 1,06 г метилового эфира 5-аис-7-(2о6,Vd.-дигидрокси-5/Ь-диметоксиметилцикло5 . 18 ент-1 с/-ил)-гепт-5-еновая кислота -тетрагидропиранилового эфира в мл метанола добавляют к 0,8ft г ацеата ртути в метаноле. Через 30 мин ри комнатной температуре, при переешивании и внешнем нагревании добавяют раствор 250 мг боргидрида натрия в 2 мл воды. Через 20 мин перемешивания смесь подкисляют до рН 6,5 водным раствором мононатрийфосфата, метанол отгоняют в вакууме, и остаток переносят в смесь вода/этиловый эфир. Из органической фазы после удаления растворителя получают 1,02 г 5(6-Экзо-диметоксиметил-7-эндо-гидрокси-2-окса-бицикло Г3,3.0 октан-3-ил)-пентановой кислоты: метиловый эфир-у-тетрагидропиранилового эфира. Пример 14. Раствор 1,59 г «-цис-у- (2oL , с6-дигидрокси-5р -ди-. метоксиметилциклопент-1 о1-ил)-гепт- -еновая кислота, метиловый эфир- -тетрагидропиранилового эфира в 6 мл тетрагидрофурана добавляют к раствору 1 ,2б г ацетата ртути .в мл воды, разбавленной k мл ТГФ. Смесь перемешивают в течение 1-2-ч до прекращения выпадения осадка. Затем добавляют 180 кг боргидрида натрия (в 2,5 мл воды) и полученную смесь перемешивают в течение 30 мин. Раствор отделяют от осадка, который затем промывают ТГФ. Водно-органический раствор концентрируют при пониженном давлении и остаток экстрагируют этилацетатом. Объединенный органический экстракт после промывания водой до нейтральной реакции и после отгонки растаорителя дает 0,98 г 4-(у-эйзо-диметоксиметил-8-эндо-гидрркси-2-окса-бицикло 3,,0 нонан-3 -ил)бутано8Ой кислоты метиловый эфир-8-тетрагидропиранйловогб эфира. П р и м е р .15. Используя в качестве исходных веществ эфиры,полученные согласно описанному в примерах 9 11, по реакции с солью ртути и последующим восстановительным димеркурированием, согласно кетрдике, описанной в примерах 13 и 1, получают следующие бициклические производные; 5-(6-экзо-бензилоксиметил-2-окса- -бициклo 3,3 oктaн-3f-ил)-пeнтaнoвoи. кислоты метиловый эфир; 5-(6-экзо-диметоксиметил-2-окса-бициклоСЗ.З.О -октан-3 ил)-пентановой кислоты метиловый эфир; 99 «-(7-экзо-бчнэилоксиметил)-2-окса -бмциклоС3. t k о Знонан-3 f -ил) -бутановой кислоты метиловый эфир . (7-экзо-Аимет,ок ;иметил-2-окса-бицикло 3,.0 нонан-з|-ил)бутановой кислоты метиловый эфир эфир 7 ацетапя{тетрагидропиранило вый эфир, диоксаииловый эфир) и. 7-ди нетил-трет-бутилсилиловый эфир 5-(6-экзодиметоксиметил-7-эндо-гидрокси-окса-би4икло13,3,01-октан-3 -ил)-пентановой кислоты метиловый эфир; эфир 8-ацеталя(тетрагидропиранило вый эфир, .пиоксаниловый эфир) и 8-диметил-трет-бутилсилиловый эфир k-(7-экзо-диметоксиметил-8-эндотидрокси-2-окса-би4иклоСЗ, , О -нонан-3 -ил)-бугановой кислоты метиловый эфир; (6-экзо-диметоксиметил-7-эндогидрокси-2-окса-бицикло 3,3,0 1-октан-3 -ил)-бутановой кислоты метиловый эфир-7 тетрагидропираниловый эфи 5 {7Экзо-диметоксиметил-8-эндо-гидрокси-2-окса-бицикло 3,.,0Знонан )-пентановой кислоты г тиловый эфир-8 тетрагидропираниловый эфир. Все эти соединения получают в dl, nat- и ent-формах. Пример Тб. Раствор 0, г брома в 5 мл .хлористого- метилена по каплям добавляют при перемешивании . к раствору 0,27 г пиридина и 1,2 г 5-бис-7 {2с,4о дигидрокси-5(Ь-диметок симетилциклопент-1с|С-ил)-гепт-5-еновой кислоты метиловый эфир- -тетрагидропиранилового эфира в 6 мл хлористого метилена, охлаждённого до . Перемешивание продолжают в течение 10 мин .после добавления. Органическую фазу промывают 5 мл буферного paQTBopa с рН 7 представляющего собой раствор тиосульфата нутрия, а затем водой до нейтральной реакции. После сушки , удаления растворителя, получают 1,38 г 5 бром-5(6-экзо-диметоксиметил-7 эндо-гидрокси-2-окса-бициклоСЗ,3 ОЗоктан-3 ил)пентановой кислоты метиловый эфир -7 тетрагидропиранилового эфира. Пример 17. 1,2 г N-иодосукцинимида добавляют к раствору 2 г 5-ЦИС-7- (2ot, Ы-дигидрокси-5;|Ь Аиметоксиметилциклопент- 1оСгил -гепт-Звеновой кислоты метиловый эфир- -тетрагидропирЬнилового эфира в 15 мл четыреххлористого углерода. Смесь перемешивают в течение 3 ч и добавляют 30 мл этилового эфира. Органическую фазу 20 .промывают 1 н.растворрм Ha,, и заМW „ Z .1 тем водой до нейтральной реакции.. В результате удаления растворителя по|лучают 2, г 5-иодо-5-(6-экзо.-димето| симетил-7Эидо-гидрокси-2-о«са-бициклоСЗ..3 ОЗоктан-Зf тил) -лентановой кислоты метиловый эфир-7-тетрагидропираниловйго эфира. Пример 18. 422 мг N-бромосукцинимида добавляют при пере мешивании к раствору 0,78. г 1 -цис-7-(2с .-дигидрокси-Зргдиметоксиметилци клопент-lot-ил)-гепт- -еновой кислоты . метиловый эфир-.4-тетрагидропиранилового эфира.в 11 мл СС. Через 4 ч перемешивания добавляют этиловый эфир раствор затем промывают водой, 1 н. Na2S20 и снова водой до нейтральной реакции. Выпаривание досуха дает 0.98 г. -бром-4-(7-экзо-диметоксиметил-8-эндо-гидрокси-2-окса-бицикло3,,О Знонан-3f -ил)-бутановой/ кислоты метиловый эфир-8-тетрагидропиранилового эфира. Пример 19. К-суспензии 0,25 г сухого CaCOj в растворе мг 5-бис-7-(21/.-гидрокси-5(5-бензилоксиметилциклопент-lot-ил)-гепт-5-еноврй КЙС.ЛОТЫ в 10 мл ССР4 охлажденной до , добавляют лри перемешивании раствор 75 мг хлора в 3 мл После .перемешивания в течение 2 ч неорганические .соли удаляют фильтрацией. Раствор промывают 7%-ным водным раствором КЗ и Na2S20 и затем водой до нейтральной реакции. Остаток после выпаривания досуха адсорбируют на силикагеле и элюируют смесью циклогексан:этиловый эфир (80:20) с получением 0,27 г 5-хлор-5(6-экзо-бензилоксиметил-2-окса-бициклоСЗ 3,ОЗоктан-3 -ил)-пентановой кислоты метилового эфира. П р и м ё р J10. Раствор 0,39 г 5-ЦИС-7-(2о,4еЬ-дигидрокси-5/%-Диметоксиметилцинкопент-lot-ил)-гепт-5-еновой кислоты метиловый эфир-5-диоксанилового эфира и 98 мг пиридина в 10 мл дихлорметана охлаждают до -kO°C. Затем добавляют раствор 81 мг хлора в 6 мя в течение 30 мин. После 10 мин перемешивания смесь наг гревают до комнатной температуры. Органическую фазу промывают 7%-ным раствором К1 и затем водой до нейтральной реакции. В результате удаления растворителя получают 0,39 г 5 хлор-5-(6-экзо-метоксиметил-Jf-эндo-гидpoкcи-2-oкca-бици cno3,3,OCoктaн-Зf-ил)-пeнтaнoвoй кислоты метиловый эфир- -диоксаниловогб эфира. . П р и м е р 21. 280 мг иода в ССВ добавляют в раствор 0,39 г -цис-7-(2о1, о1-дигидрокси-5-Диметоксиметилциклопент-lot-ил )-гепт- -еновой кислоты метиловый эфир-«-тетрагидропиранилового эфира и 82 мг пиридина в 10 мл Перемешивание продолжают до исчезновения окраскиj затем добавляли 30 мл этилового эфира. Органическую фазу промывают водой, затем 7%-ным раствором К1 и , и снова водой до нейтральной реакции. В результате удаления растворителя получают О,W г А-иод-4-(7-экзо-диметоксиметил-8-эндо-гидрокси-2-окса-бицикло 3,|,0 нонан-3| -ил)-бутановой кислоты метиловый эфир-8-тетрагидропиранилового эфира. Пример 22. К раствору 0,3 5-бис-7(2о1-гидрркси-5р-бензилоксиметилциклопент-1с ил)-гепт-5-еновой кислоты метилового эфира в 6 мл м(ета нола добавляют при перемешивании раствор 0,325 г ацетата ртути в смеси вода:ме1ганол (1:9,6 «л). Смесь перемешивают в течение 15 мин, концентрируют в вакууме до объема 3 ил и затем добавляют 5 мл насыщенного раствора NaC в воде. Затем полученный осадок экстрагируют хлористым метиленом. Органическую фазу промывают водой и выпаривают досуха с образованием 0,52 г сырого 5-хлорртуть-5(6-экзо-бензилоксиметил-2-окса-бицикло 3 3,Й -октан-3 -ил)-пентановой кислоты метилового Э( Растйор этого вещества в метияенхлориде (10 мл) обрабатывают 80 мг пири дина в 2 мл и затем по каплям при перемешивании раствором 150 мг Вг в . Через 20 мин перемешивания прикомнатной температуре органическую фазу промывают водой, затем раствором К1 и На2$20з и снова водой до нейтральной реакции. В результате упаривания досуха получают 0,3 г 5-вром-5-(6-экзо-бензилоксиметил-2-окса-бицикло 3 3,0 октан-Зб -ил)-пентановой кислоты метилового эфира. Масс-спектр: М , 26 т/е; М - НВг ЗН т/е; М - СНВг (СН УзСОгСНз 231 т/е. Пример 23. 10,5 мг моногид рата п-толуилсульфокислоты добавляют к раствору 0,26 г 5-иод-5-(6-экзо-ди 97 метоксиметил-7-эндо-гидрокси-2-оксабицикло 3,3,0|октан-3 У-ил)-метилового эфира пентановой кислоты-7-тетрагидропиранилового эфира и полученную смесь оставляют при комнатной температуре на 30 мин. Затем добавляют 10 мг пиридина и раствор выпаривают досуха. Остаток переносят в смесь этиловый эфир/вода« После сушки органическая фаза после выпаривания растворителя дает 0,23 г сырого ЗИОД-(&-экзо-д №1етоксиметил-7-андо-гид- рокс14-2-оксгйицикло- 3.3.0}октан-3 -. -ил)-1т№ Нтановой кислоты метилового эфиpa- Разделение хроматогрсн| ированиемна силикагеле с гюмощью смеси хлористый метилен:этиловый эфир (75:25) в качестве элюента приводит к образованию 8 мг 5 иод-5-(6-экзо-диметоксиметйя-7-э«до-гидрокси-2-вкса-бициклоСЗ.З.О октан-3|-эндо-ил)-пентановой кислоты, метилового эфира и 55 «г 3-экзо-изомера. Согласно данным спектрометрии будут использоваться следующие наименования простагландинов. Так, например, Iупомянутые диастереоизомеры могут быть названы как эндо-диастереоизо;мер - 6/iH- б,9(/-окись-11Ы-гидрокси-12})тдиметокси-формила411еталъ- ш( 43) тетранорпростановой кислоты метиловый эфир, а экзо-диастереоизомер6 - d Н-6, 9ot-окис ь -11 об-гидрокси -12 -диметокси-формилацеталь- о(20- 13) тетранорпростановой кислоты метиловый эфир. Аналитическйе данные. Эндо-диасТереоизомер: тонкослойная хроматография более полярная - одно пятно. Масс-спектр (га/е, интенсивности фрагмента); 442 0, 3 5/314 3 М - иод/Н 283 11 315-СНзОЯ; . /.ОСНз 75 100 СН. ЯМР (растворитель , внутрйенНИИ стандарт TMS), ч./млн.: 3;49 и ,OCMj 3,S2 S; ЗН/ЗН. СИС., 3,64 S, 3 Н, 4,0 ЗН (протоны ОНС, ). 4,29 d, ОСИэ Ч Э 4,60 m, 1 Н 6(&H. СНР (20 НГц, раствор , внутренний стандйрт TMS), ч./ипн.: 72,9; 36,5 33,.1; 25,6; 41,8; 81.Oi 38,1; 55,5; 83,1; ,5; 7,2; ЦЧ.б-. tOS.O; 5,2; 51.0. Экзо-диастереойзомер: тонкослойная хронатография менее полярная одно пятно. . , Масс-спектр: Й2 0,01 М, 366 З М СИ СН (ОСИэ)2; 315 i М - 1; 283 10 1 - CHjOH; jun; 75 100СН(ОСН CHCoCHj) ЯМР; ррга:-3,3« и 3,37 3 H/3tH 3,5 и t, m, 1 Н и 2 Н протоны Cg, Сд, С неопределенного назначения; 3,65, s,, 3 Н, 1,21, dlH, СН(ОСН)2; ,35 т, 1 Н, 6ctH. , ppni: 173,0; 37,0; 33,1 25,51 0,1; 8,4; 39,7; 57,2; 83,7; 40,3; 76,5; ,0; 107,3; 5,0; 53,8; 51,1. П р и м е р 2. Раствор 980 мг 4-бром-4-(7-Экзо-диметоксиметия-8-эндо-гидрО1$си-2-окса-би4иклоСЗ,,0 нонан-3| -ил)-бутановой кислоты метиловый эфир-8-тетрагидропирйнилового эфира в 6 мл безводного метанола обрабатывают при комнатной темпег ратуре в течение 30 мин 48 мг п-толуолсульфокислоты. Добавляют водный раствор NaHCOj и смесь экстра гируют этиловым эфиром. Из органичес кой фазы после промывки до нейтральной реакции и выпаривания растворите ля получают 0,68 г сырого продукта, который после очистки на силикагеле при использовании в качестве элюента смеси хлористый метилен: этиловый эфир (80:20) дает 0,30 г 4-бром-47 -(7 экзо-диметоксиметил-8-эндо-гидрокси-2-окса-бицикло 3,4,0Знонан-З -экзо-ил)-бутановой кислоты метилово го эфира и 0,29 г 3-зндо-изомера. Пример 25. Используя в качестве исходных веществ кислрты, полученные согласно методике примера 11, и осуществляя их галоциклизацию согласно Описанному в одном из примеров 16-22, получают следующие галобициклические соединения: 5-хлор-5-(6-экзо-диметоксиметил-7 эндо-гидрокси-2-оксабицикло 3,3,0 октан-3| -ил)-пентановая кислота; метиловый эфир-7-тетрагидропираниловый 9 ,24 эфир (и 7-диоксаниловый зфир, а также 7-ДИмётилбутилсилиловый эфир); 4-хлор-4-(7-экзо-диметоксиметил-8-эндо-гидрокси-2-оксабициклоСЗ,4,0 ;HOHaH 3f -ил)-бутановая кислота, ме-тиловый Зфир-8-тетрагидропираниловый эфир (и 8.-диоксаниловый эфир, а такт же о-диметилбутилсилиловый эфир); 5-хлор-5-(6-экзо-диметоксиметил-2-окса-бицикло13,3,О октан-3§-ил)-пентановая кислота, метил(овый эфир; 5 хлор-5-(6-экзо-бензилоксиметил-2-окса-бицикло 3,3,0 октан-36-ил)-пентановая кислота, метиловый эфир; 4-хлор-4-(7-экзо-диметоксикетил-2-окса-бицикло 3,4,01-нонан-3 -ил)-бутановая кислота, метиловый эфир; 4-хлор-4-(7-экзo-бeнзилoкcимeтил- 2-окса-бицикло ГЗ,4,0 3-нонан-З.ил)-бутановая кислота, метиловый эфир; 5 бром-5-(6-экзо-диметоксиметил-7-эндо-гидрокси-2-оксабициклоС3,3,0 октан-ЗС-ил)-пентановая кислота, метиловый эфир-7 тетрагидропираниловый ;эфир (7-диоксаниловый и 7-диметилбутилсилиловый эфиры); 4-бром-4-(7-экзо-диметоксиметил-8-эндо-гидрокси-2-оксабицикло 3,4,0 нонан)-36-ил)-бутановая кислота, метиловый эфир-8-тетрагидропираниловый эфир (8-диоксаниловый и 8-диметилбутилсилиловый эфиры); 5-бром-5-(6-экзо-диметоксиметил-2-окса-бициклоСЗ,3,0 -октан-3 -ил)-пентановая кислота, метиловый эфир; 5-6pOM-5f(6-экзb-бeнзилoкcимeтил-2.-oкca-бициклo 3,3,03-oктaн-3 -ил)-пeнтaнoвaя кислота, метиловый эфир; 4-бром-4-(7-экзо-диметоксиметил-2-окса-бицикло 3,4,0 -нонан-3f-ил)-бутановая кислота, метиловый эфир; 4-бром-4-(7-зкзо-бензилоксиметил-2-окса-бицикло- 3,4,0 ионан-3 -ил)-бутановая кислота, метиловый эфир; 5-иод-5-(6-экзо-диметоксиметил-7-эндо-гидрокси-2-окса-бицикло 3,3,0 октан-ЗБ-ил)-пентановая кислота, метиловый эфир-7-тетрагидропираниловый эфир (а также 7-Диоксаниловый и 7-Диметилбутилсилиловый эфиры); 4-иод-4-(7-зкзо-диметоксиметил-8-эндо-гидрокси-2-о1«са-бицикло 3,4,0 нонан-.)-бутановая кислота, метиловый зфир-8-тетрагидропираниловый у эфир (а также 8-диоксаниловый и 8-диметилбутилосилиловый эфиры); 5-иод-5-(6-экзо-диметоксиметил-2-окса-бици1сгюСЗ,3,01-октан-3| ил)-пентановая кислота, метиловый эфир; 2597 5-ИОД-5-(6-экзо-бензилоксиметил-2-окса-бицикло 3,3,0.-октан-3 -ил)-пентановая кислота, метиловый эфир; 4-И6Д-4-(7-экзо-бензилоксиметил.-2-окса-бицикло ГЗ .i, О -нонан-З -ил) i-бутановая кислота, метиловый эфир; «-ирд- -{7-:Экзо-чиметоксиметил-2-окса-бицикло 3, , О -нонаи-36-ил) -бутановая кислота, метиловый эфир; Пример 26. Селективной деацетализацией или десилилизацией эфи ров, описанных в примере 25, согласно методике примеров 23 и получаю производные 3-оксиран-гидроокись-фор милацеталей, которые после разделения изомеров дает следующие соединеметиловый эфир 5-хлор-5-(6-экзо-диметоксиметил-7-эндогидрокси-2-окс-бициклоСЗ,3,0 октан-3 -ил)-пентановой кислоты, а также ее индивидуальные 3-экзо- и 3-эндо-изомеры; -хлор-4-(7-экзо-диметоксиметил-8-эндо-гидрокси-2-окса-бициклоС3,,0 нонан-3 ил)-бутановой кислоты метиловый эфир, а также его индивиду альные 3-экзо- и 3-эндо-изомеры; метиловый эфир 5 -бром-5-{6-экзодиметоксиметил-7-эндо-гидрокси-2-окса-бицикло 3,3,0 октан-3|-ил)-пентановой кислоты, а также его индивидуальные З -экзо- и З -эндоизомеры. Эндо-изомер: ТСХ на Si Со более полярная - одно пятно. ЯМР, fCOCe,), ч./млн.: 3, d, 6 Н сн(оснз)2; 3,65, S, 3 Н сОаСНз; /,00 т, 4 Н (протоны С4, Cj, €9, .ОШз . с-,-,); ,17 d, 1 СН; V Н, , 13cMPl M73,0; 35,0; 33,3; 23,6; 59,; 80,6; 36,4; 55,6; 83,3; 41,6; 74,3; 44,5; 108,0; 54,5; 54,2; 51,1. Зкзо-изомер; ТСХ на SiO менее полярная - одно пятно. ЯМР, (СОСез) ч./млн.: 3,37, 6 Н3,66, 3 Н, сОдСНз; 4,00, 4 Н, .протоны С4, Су, Cj, 4,32; 1 Н,.6 Н. «,5 т СМР: 173,0; 35,5; 33,3; 23,6; 7,7; 8,2; 38,2; .57,9; 83,6; kQ; 76,0;.43,9; 107,2; 53,8; 51,0. 4-Бром-4-(7-экзо-димётоксиметил-8-эидо-гидрокси-2-окса-бициклоГЗ, ионан-3§-ил)-бутановой кислоты метиовый эфир, а также его индивидуальные изомеры 3-экзо и 3-эндо; 5-иод-5-(6-экзо-диметоксиметил-7эндо-гидрокси-2-окса-бицикло 3,3,0 октан-3 -ил)-пентановой кислоты метиловый эфир, а также его индивидуальные 3-экзо- и Зэндо-изомеры; -иод- -(7-экзо-диметоксиметил-8-эндо-гидрокси-2-оксабицикло 3,4,0 нонан-3 -ил)-бутановой кислоты метиловый эфир, а также его индивидуальные 3-зкзо- и ЗЭндо-изЬмеры. Пример 27. При перемешива- НИИ в атмосфере азота бензольный рас вор (30 мп) 2,8 г 5-иод-5-(6-экзо-диметоксиметил-7-эндо-гидрокси-2-окса-бииикло 3-3.0 октан-3- ия)-пентановой кислоты метиловый эфир-7-тетрагидропиранилового эфира обрабатывают раствором 2,8 г трибутилолова гидрида в 8 мл беизола. Смесь выдерживают при в течение 8 ч и зате« в течение ночи при ко««1атной температуре. Бензольный слой промывают 2 х 10 мл 5%ного раствора NaHCO и затем водой до нейтральной реакции. Остаток после 1мпаривания растворителя адсорбируют на 10 г силикагеля и элюируют бензолом и смесью бензол :этилош(й э(1р (85:15) с образованием 1 ,Э« г 5-(6-экзо-диметокси«етил-7-эндо-гидрок у4--2-окса-биаикж)3,3,0 октан-3f-ия)-пентановой кислоты метиловый эфир-7 тетрагидропиранилового эфира. Л р и м е р 28. 60 нг п-тояуилсульфокисяоты добавляют к раствору 1,98 г 5(6-экзодиметоксиметил-7 -SHfio-гиярокси-2-окса-бицикло З,3,0 октан-З ил)-пентановой кислоты метиловый эфир-7-тетрагидропиракилового эфира в 10 мл безводного метанола. Через 30 w«H стояния при комнатной тектературе эту смесь добавляют к 20 мл 20 -ного водного раствора КаНСО. Смесь экстрагируют этиловым э 1 «ром; объединенный эфирный экстракт после сушки над Na2SO выпаривают досуха. Остаток адсорбируют на 100 г силикагеля и элюируют хлористым метиленом: этихювым эфиром (94:6) с образованием 0,64 г 5-(6-экзо-диметок279симетил-7Эндо-гидрокси-2-окса-бицик лоГЗ,3,0 октан-3 -экзо-ил)-пентановой кислоты метилового эфира, 0,52 г 3-эндо изомера и 0,12 г . Эндо-изо « р ЯМР (COCtjj, ч./млн.: 4,6 т, 1 Н, 6(iH. тех более полярная./ Экзо-изомер. ЯМР (CDC€i), ч./млн. k,3 т. Н, брН. тех менее полярная. 0,32 г 3 эндо-изомера растворяют в пиридине (0,8 мл) и обрабатывают в течение 8 ч при комнатной температуре 0,3 мл уксусного ангидрида. Затем смесь выливсиот в ледяную воду, и, после подкисления до рНЧ,2, ее экстратруют этиловым эфиром. Объеди ненный экстракт после промывания до нейтральной реакции выпаривают с образованием 0,315 г 5-(6-экзо-диметоксиметил-7 эндо-гидрокси-2-окса-би4иклоСЗ Э,0}октан-3|-экзо-ил)-пентановая кислота-метиловый эфир-7-ацетата. П р и м е р 29. Раствор 1,32 г (7-экзо-диметоксиметил-8-эндо-гидрокси-2-окса-бицикЛо 3,,О нонан-3f -ил)-бутиловой кислоты метиловый эфир -8-трет-бутилметилсилилового эфира в 10 мл безводного метанола обрабатываюТ 55 мг п-толуилсульфокислоты в течение 2 ч при комнатной температуре. Добавляют 0,1 мл пиридина, растворитель .отгоняют в вакууме и остаток переносят в смесь вода/этиловый эфир. Органическая фаза/после удаления растворителя даёт 1,1 г сырого 8-гид1Х кси-3 -ил производного. Хроматографйрованием его на силикагеле испоЛьзуя в качестве элюента смесь бензол: этиловый эфир (80:20), это произеодное разделяют на 4-(7-экзо-диметоксиметил-8-эндо-гидрокси-2-окса-бици Сло З 4,01-ионан-3| -эндо-ил)бутановой кислоты метиловый эфир (0,42 г) и 3 f -экзо-ил-изомер (0,34 г). Пример 30. Используя методику примеров 28 и 29, метанолизом эфиров (ацеталей или силиловых), описанным в примере 15, получают соответ ствующие свободные спирты. Пример ЗЬ Ацетилированием в присутствии пиридина (0,6 мл) и уксусного ангидрида(0,3 мл)0,2 г 5-иод-5-(6-экзо-диметоксиметил-7тэндо-гидрокси-2-окса-бицикло 3,3,03-октан-3 -эндо-ил)-пентановой кислоты метилового эфира получают 0,21 г соответствующего 7-ацетоксипооизводного. 5 ЯМР (COCtj), ч./млн.: 2.035 ЗН, ОСИ OCOCHj; 3,36-3,40 S, ЗН, си V осн 3J56. S, ЗН, 4,00 m 2Н. про/ -xOCHj тоны С5,Сэ; 4,27 d, 1Н; СН. -.4,63, ГН, 6(i Н; 5,0т 1Н, протон С. (Спектрометрические данные для 6oLH изомерного ацетата: 2,03 3,34-3,33, 3,66 Чгп4Н COgCHj и один из Сс, Сд-протонов; 4,1т 1Н другие С5,Сэ-протоны; 4,2, 4,2т 1Н, , 5,1). Раствор 5-иод-З-эндо-ацетата в бензоле (5 мл )обрабатывают О,4 г трибутилолова гидрида в течение 10 ч при 50С. После промывания бензольной фазы 5%-ным раствором NaHCO и водой, упаривания растворителя и очистки на силикагеле (10 г), используя в качестве элюента смесь бензол: этиловый эфир (80:20), получают 0,105 г 5-(6-экзо-диметоксиметил-7-эндо-гидроксй-2-окса-бицикло 3 3,ОЗоктан-3 -эндо-ил)-пентановой кислоты метиловый эфир-7-ацетата, идентичного во всех отношениях образцу, полученному по методике примера 28. -- Прим е р 32. Согласно методике примеров 27 и 31 восстановлением гидридом трибутилолова одного из галогенпроизводных, синтезированных в припримерах 16-26, получают соответству«чее производное, в котором атом галогена зам гачен на водород. Такие соединения во всех отношениях идентичны соединениям, полученным согласно методикам примеров 15, 28, 29 и 30. Пример 33. 5,4мг гидрохинона и раствор 1,63 г оксалиновой кислоты в 48 мл воды добавляют к раствору 4 г 5(6-экзo-димeтoкcимeтил-7-эндo-гйдpoкcи-2-oкca-би4иклo3,3,03-октан-35-ил)-пентановая кислота-метилового эфира в iSO мл ацетона. Через.. 12 ч при 40 С ацетон удаляют при пониженном давлении и смесь экстрагируют этилацетатом (3 х 25 мл) Объединенный органический экстракт промывают до нейтральной реакции 10%-ным раствором сульфата аммония и сушат над Na2S04 В результате удаления растворителя получают 3,21 г 5-(6-экзо-формил-7-эндо-гидрркси-22997
.-оксабицикло 3,3,0 октан-3 -ил)-пентановой кислоты метилового эфира, 6-экзо-формил-З-эндо и 7-экзо-формил-3 экзо-производные получают из соответствующих индивидуальных изомеров.
Пример З. Согласно методике примера 33, используя в качестве исходных веществ соответствующие бицикло 3,3,0 октан-6-экзо-диметоксиметил- и бицикло 3,,0 нонан-7-экзо-диметоксиметилпроизводные, получают следующие вещества (либо в виде индивидуальных 3-экзо- и 3 эндо-, либо в виде 3f-изомеров):
5-(6-экзо-формил-2-окса-бицикло 3, 3,3,0)октан-3-ил) -пентановая кислота, метиловый эфир;
метиловый эфир 4-(7-экзо-формил-2-окса-бицикло 3,,0 -нонан-3-ил)-бутановой кислоты;
метиловый эфир 5-(6-экзо-формил-7-эндо-гидрокси-2-окса-бицикло 3,3,0 октан-3-ил)-пентановой кислоты;
метиловый эфир -(7-экзо-формил-8-эндо-гидрокси-2-окса-бицикло 3,,0 нонан-3-ил)-бутановой кислоты;
5-хлор-5-(6-экзо-формил-2-окса-бицикло 3,3,0 jOKTaH-3-ил)-пентановая кислота, метиловый эфир;
t-хлор- -(7-экзо-формил-2-окса-бицикло 3,,0 нонан-3-ил)-бутановая кислота, метиловый эфир;
5-хлор-5-(б-экзо-формил-7-эндо-гидрокси-2-окса-бицикло C3,3 0 oктан-З-ил)-пентановая кислота, метиловый эфир;
А-хлор- - (7-экзо-формил-8-эндо-гидрокси-2-окса-би1ДиклоСЗ,гО нонан-3-ил -бутановая кислота, метиловый эфир;
5 бром-5-1б-экзо-формил-2-окса-бицикло 3,3,0 октан-3-ил)-пентановая кислота, метиловый эфир:
k-бDO л- - (7-экзо-формил-2-окса-би14иклоСЗ,,0 нонан-3-ил)-бутановая кислота, метиловый эфир;
5 бром-5-(6-экзо-формил-7-эндо-гидрокси-2-окса-бициклоСЗ,3,0 октан-3-ил)-пентановая кислота, метиловый эфир;
А-брОМ- -(7-ЭКЗО-ФОРМИЛ-8-ЭНДО-гидрокси-2-окса-бицикло 3,,0 нонан -3-ил)-бутановая кислота, метиловый
эфир;. ..
5-иод-5-(6-экзо-формил-2-окса-5ициЛоСЗ,3,.0 октан-3-ил)-пентановая кислота, метиловый эфир;
-иод-4- (7-экзо-формил-2-окса-бицикло 3,,О J-нонан-Зил)-бутановая кислота, метиловый эфир;
30
5-иод-5-(6-экзо-формил-7 эндо-гидрокси-2 -окса-бицикло( 3,3,0 октан- 3-ил -пентановая кислота, метиловый эфир;
-иод- -(7-экзо-формил-8-эндо-гидрокси-2-окса-би4икло 3, , О нонаи-3-ил)-бутановая кислота, метиловый эфир;
5-(6-экзо-формил-7-эндо-гидрокси-2-окса-биаикло 3,3,0 октан-3-ил)-пентановая кислота, метиловый эфир-7-ааетат;
5-ИОД-5-(6-экзo-фopмил-7 эндo-гидpoкcи-2-oкca-биi4иклofЗ,3 0}oктaн-3-ил)-пeнтaнoвaя кислота, метиловый эфир-7-ацетат;
5-(7 экзо-формил-8-эндо-гидрокси-2-окса-биаикло- 3,,0 нонан-3-ил)-пентановая кислота, метиловый эфир;
4-{6-экзо-формил-7-эндо-гидрокси-2-окса-бицикло- 3,3,О октан-3-ил)-бутановая кислота, метиловый эфир.
Пример 35. К раствору 1,2 г метилового эфира 5-(6-экзо-бензилоксиметил-2-окса-бицикло 3,3 0 oKtан-3 -ил)-пентановой кислоты в снеси метанол:метилааетат (10 мл:10 мл) добавляют 2 мл 0,1 н.раствора НСЕ в метаноле. После добавления 0,13 г PtOi2 смесь гидрируют при комнатнс температуре и атмосферном давлении до поглощения 1-молярного эквивалента водорода. После удаления газа в вакууме и промывки азотом суспензию фильтруют, нейтрализуют и )И8ают досуха. Остаток переносят в смесь вода/этилацетат и из органической фазы получают 0,8 г 5(6-экзо-гидроксиметил-2-окса-бицикло 3,3,0 октан-3§-ил)-пентановой кислоты метилового эфира. Это соединение затем окисляют в 6-экзо-формилпроизводное по методике примера 1, используя дициклогексил-карбодиимид в смеси ДМСО бензол (25:75).
Пример 36. К раствору 18,1 5 -тетрагидроггиранилоксиметил-2 А,1№1-дигидроксициклопент- lci-уксусная кислота-у-лакТон-|-тетрагидропиранило вого эфира а 150 мл толуола, охлажденному до -70°С, добавляют за ЗР 128 мл 5 М раствора диизобутилила/иомнийгидрида (1,2 М/М). Через 30 мин при -70°С добавляют 128 мл 2 М толуольного раствора изопропанола и раствор нагревают до 0 .Затем добавляют 10 мл насыщенного водного раствора NaHflPO и смесь перемешивают в течение 1 ч. После добавления 10 г безводног
Ыа2520з и 10 г фильтрующей земли, раствор отфильтровывают и выпаривают досуха с образованием 18,1 г Нэагидропиранилоксиметил-2о, W-ДИГИДР окси-циклопент-1о -этанель-у-лактол- s -t-тетрагидропираноилового эфира. (Раствор этого соединения в 2 мл безводного ДМСО добавляют по каплям к раствору, полученному следующим образом: г 8,0 -ного гидрида натрия в Ю 300 мл ДМСО нагревают в течение ч при затем после нагревания смеси до 18-20°С добавляют 67 г 4-карб- оксибутилтрифенилфосфонийбромида, , растворенного в 80 мл безводного ДМСО, 5 поддерживая при этом температуру в интервале 20-22 С для появления яркокрасного цвета. После k ч перемешивания добавляют 600 мл воды и смесь экстрагируют смесью этиловый эфир: 20 бензол (70:30) для удаления окиси трифенилфосфина. Бензольную органимческую фазу повторно экстрагируют 0,1 н,раствором NaOH и затем водой до нейтральной реакции; затем ее от- 25 брасывают. Щелочную водную фазу подкисляют до рН 3-,8 и затем экстрагируют смесью этиловый эфир:пентан (1:1) с образованием 21,6 г 5 бис-7-( 2c3t,-дигидрокси-5(3-тетрагидропи- jo ранилоксиметил-циклопент-ТсА-ил)-гепт-6-еновой кислоты -тетрагидропиранилового эфира, который можно превратить в метиловый эфир обработкой диазометаном в эфире. г этого эфираjj в 28 мл тетрагидрофурана добавляют по каплям к желтовато-коричневой суспензии, полученной добавлением 28 мл ТГф к раствору 6,13 г ацетата ртути в 28 мл воды. После перемешивания 40 смеси в течение 20 мин при комнатной температуре ее охлаждают в бане с ледяной водой и по каплям добавляют 810 мг NaBH в 14 мл воды. Происходит осаждение элементарной ртути, суспензию декантируют, тетрагидрофуран выпаривают при пониженном давлении и остаток экстрагируют этиловым эфиром. Б результате удаления растворителя получают 7,5 г 5-(6-экзо-тетрагидропиранилоксиметил-7 гидрокси-2-окса-бицикло ,3iO -октан-3-ил)-пентановой кислоты метиловый эфир-7-тетрагидропиранилового эфира; затем добавляют 0,42 г п-толуилсульфокислоты к раствору этого соединения в 30 мл метанола. Через 2 ч при комнатной температуре раствор концентрируют в вакууме и добавляют воду. После экстракции
эфиром и хроматографии на силикагеле, используя этиловый 31ФИР в качестве элюента, получают 2,k г 5-(6-экзо-гидроксим6тил-7-гидрокси-2-окса-бицикло 3,3,0 октйн-3-экзо-ил)-пентановой кислоты метилового эфира и 2,6 г 3-эндо-изомера. «
Пример 37. 2,5г N-иодсукцинимида добавляют к раствору 4,26 г 5-цис-7-(2Ы,4о -дигидроксй-5 тетрагидроксипиранилоксиметил-циклопент-1 о6-ил-гепт-5-еновая кислота 4-тетрагидропиранилового эфира в (10 мл + 10 мл) и полученную в результате смесь перемешивают в течение 4 М. Добавляют 30 мя безводного метанола, содержащего 130 мг п -толуолсульфокислоты, и перемешивание продолжают в течение 2 ч. Добавляют 0,2 мя пиридина, смесь концентрируют до небольшого объема и Остаток переносят в смесь вода/этилацетат. После промывания и затем водой до нейтральной реакции органическую фазу выпаривают досуха с образованием остатка, который адсорбируют на силикагеле и элюируют этиловым эфиром с образованием 2,2 г 5-иод-5-(6-экзо-гидроксиметил-7-гидрокси-2-окса-бицикло3,3,ОЬктан-3-экзо-ил)-пентановой кислоты метилового эфира и 1,85 г 3-эндо-изомера. .
Пример 38. Следуя методике примера 37, но используя метиловый эфир вместо кислоты и N-бромацетамид вместо N-иод-сукциНимида, получают метиловый эфир 5-бром-5-(6-экзогидрокси-метил-7-гидрокси-2-оксабициклоСЗ,3,0 октан-3-ил)-пентановой кислоты. Хроматографией на силикагеле это вещество разделяют на 3-экзои 3-эндо-изомеры.
П р и м е р 39. Раствор 0,86 г пиридина и 2,2 г 5-цис-7-(2о1,4с6-дигидрокси-5-(5тет.рагидропиранилоксиметил-циклопент- loL-ил) -гепт-5-еновой кислоты метиловый эфир-4-тетрагидропиранилового эфира в дих орметане (20 мл) охлаждают до и добавляют 0,38 г хлора в 10 мл ССе :СН2Се2 (1:1). Смесь перемешивают в течение 2 ч, нагревают до комнатной температуры и промывают 2 н.раствором N2804 и затем водой до нейтральной реакции. После упаривания растворителя остаток растворяют в метаноле (10 мл) и обрабатывают 0,1 г п -толуолсульфокислоты. Затем полученный раствор концентрируют, разбавляют водой и J39 экстрагируют этилацетатом. В результате удаления растворителя иочистки остатка на силикагеле получаст 0,6 г 5-хлор-5-(6-экзо-гидроксиметил-7-эндо-гидрокси-2-окса-бицикло 3,3,0 октан-3-экзо-ил)-пентановой кислоты и 0,71 г 3 эндо-изоме|1а. Пример 4р, К раствору 0,36Л г 5-ИОД-5-(6-экзо-гидроксиметил-7-эндо-гидрокси-2-окса-бициклоС5,3.0 октан-3-экзо-ил)-пентановой кислоты метилового эфира в ,8 мл бензол:ДМСО (75:25) добавляют последовательно 0,28 г дициклогексилкарЬодиимида и О, мл раствора трифторацетата пиридиния (см. пример 1). Через 3 ч перемешивания добавляют 8 .мл бензола и затем водный раствор оксалиновой кислоты (Э мл в 1,2 мл) Осадок удаляют фильтрацией и бензоль ...,.-.-. . .-- ныи раствор промывают водой до нейтральной реакции. В результате удаления растворителя получают 0,32 г 5 -иод-5(6-экзо-формил-7-эндо-гидрокси-2-окса-бицикло 3,3,0Зоктан-З-экзо -ил)-пентановой кислоты метилового эфира. Пример tl.B результате оки сления 6-экзо-гидроксиметил-7-эндогидроксипроизводных, полученных согласно примерам 36-39, следуя методике примера ijO, получают соответствую щие производные 6-экзо-формила. Пример 2. Раствор З, г (2-оксо-гептил) диметоксифосфоната в 50 мл диметоксиэтана по каплям добавляют к суспензии 0,«5 г 80%-ного раствора NaH (дисперсия в минеральном масле). После перемешивания в течение 1 ч добавляют раствор метилового эфира 5(6-экзоформил-7 эндо-гидрокси-2-окса-бициклоСЗ,3,0 Зоктан -3fил)-пентановой кислоты в lO мл диметоксиэтана. В течение 10 Мин этот раствор раз бавляют 50 мл 30 ;-ного водного растiBOpa одноосновного фосфата натрия. Органическую фазу отделяют, водную фазу повторно экстрагируют и объединенный органический экстракт выпаривают. Очисткой сырого продукта на 50 г силикагеля (циклогексен:этиловый эфир 50:50) получают 1,1 г 3.-t6-экзо-(3-оксо-окт-1-транс-ен-1-ил)-7-эндо-гидрокси-2-окса-бицикло, 3,3,3 октан-3-эндо-ил-пентановой кис ты метилового эфира или 13t-6 -6(90 -окись-11о.-гидрокси-15-OKco-npocT-l 3 еновои К11слоты метилового эфира и ,98 г 5-Сб-экзо-(3-оксо-окт-1-транс1-ил)-7-эндо-гидрокси-2-оксаг&1Цико 3 3,0)октан-3 экзо-илj-пентановой : ислоты метилового эфира или 13t-6(iH6 (9ct) -окись-11Ы.-гидрокси-15-оксопрост-13 еновой кислоты метилового фира плюс 0,9 г смеси двух изомеров соотношении 1:1(3-экзо- и Зэндо ли боСН и 6jiH), Такую смесь разделяют а два изомерных компонента методом ех с помощью этилового эфира. Эти зомеры имеют следующие абсорбционные арактеристики: 280 им, t 13,070; f 228 нм, Е 12,200. ямр (сосез):о,91 зн С2о-с«з; 3,68 s, ЗН, С02СН ; 6, Ibd, Ш, еинильный протон C( 6,71q - 1Н винильный протон (Ji3 9 Гц). Согласно аналогичным методикам из соответствующих 5-Н- и 5-галосоединений получают следующие производные простеновой кислоты: 1 3t-6ctH-6(9oL)-oKHCb-15-OKco-npocT-13 еновая кислота метиловый эфир; метиловый эфир 13t-6ci H-6(9-ot) -окись-5-хлор-15-оксопрост-13-еновой кислоты; метиловый эфир 1 Зt-6ciH-6(9cO-oкиcь-5 бpoм-15 oкco-npocт-1 3 еновой кислоты; метиловый эфир 13t-6aW-6()-OKMCb -5-иод-5 иод-15-оксо-прост-13-еновой кислоты; метиловый эфир 13t-6cilH-6(9oO-окись-5-хлор-ПЫ-гидрокси-15ОКСо-прост-13еновой кислоты; 131-6о6Н-6(9о)-окись-5-бром-11о1-гидрокси-15 оксопрост-13 еновой кис лоты, ЯМР: 3,67s ЗН 3,95т ЦН Cg, C5, протоны и Н /Н протон k, 3m 1Н 6otH; 6,l6d 1Н С.,4 протон; 6,63 g 1Н С13. протон; 1 31-6аШ-6(9о1)-окись-5-иод-(1 loL-гидрокси-15-оксо-прост-13-еноваякислота, метиловый эфир, ЯМР: 0,9s ЗН С-щСНз; 3.53 m 1Н протон Сс; 3,6s ЗН CQjCHj; 3,9m Н протон 4,1 m 2Н протон Сд, ,; 4, m 1Н 6Н; 6,2d 1Н протон С-,4; 6,75 g IP протон 13t-6f H-6(9ot)-ОКИСЬ-15-оксо-прост-13-еновая кислота, метиловый эфир; Зt-6эн-6-(9ol)-oкиcь-5-xлop-15-оксо-прост-13 еновая кислота, мети ловый эфир; 13t-6/5H-6(9oi) -окись-5-бром-15-ок со-прост-13 еновая кислота, метилов эфир; 13t-6/Ы -6(9ot)-oкиcь-5-иoд-T5-oкco -прост-13-еновая кислота, метиловый эфир; 1 3t-6/jH-6 (9ot)-окись-5-хлор-1 loi- -гидрокси-15-оксо-прост-13-еновая кислота, метиловый эфир; 13t-6 -6(9ot)-окись-5-бром-lloi-гидрокси-15 оксо-прост-13-еноваякислота, метиловый эфир; ЯМР:, 3,65s ЗН CQjCH ; 4,00m ЗН протон Cg, CQ С, Ц,()т 1Н 6,2 d 1Н протон 6,6 q 1Н протон С,; 131-6/&Н-6(9Ы)-окись-5-иод-11о -гидрокси-15 оксо-прост-13-еноваякислота, метиловый эфир, ЯМР: 3,66s ЗН С02СН,; 3,96 m ЗН протоны Сд, Ц-i и Су; ,6 m 1Н 6/ЗН; 6,21d 1Н протон i ,/ q 1H протон Пример 3- Раствор 2,16 г (2-оксо-октил) диметилфосфоната в 20 мл бензола по каплям добавляют к суспензии 292 мг NaH ( дисперсия в минеральном масле) в 30 мл бензола. Через 30 мин перемешивания раствор 2,6 г метилового эфира 4-бpoм-it-(7-экзo-фopмил-8-эндo-гидрокси-2-окса-бицикло 3 , ,02нонан-3 -ил)-бутановой кислоты в 20 мл бензола по каплям добавляют к этой смеси. Перемешивание продолжают еще в течение 30 мин и добавляют 2 мл 30% ного водного раствора NaHgPO. Отделяют органическую фазу и водную фазу повторно экстрагируют бензолом. Органические слои объединяют и выпаривают досуха. Остаток очищают на силикагеле (50 г) , используя в ка.честве элюента смесь СН2СС2 :этиловый эфир (120: 0) с образованием 0,52 г/ -бром- -(7-экзо-оксо-окт-1-1-енил-8-эндо-гидрокси-2-окса-бициклоСЗ,,О нонан-3-эндо-ил)-бутановая кислота, метилового эфира или 13-транс- -бром-5рН-5 (9oi)-окись-11Ы -гидрокси-15 оксо-прост-13-еноваякислота, метилового эфира и 1 , г метилевого эфира -бром-4-(7-экзо3-оксо-1-транс-1-енил)-8-эндо-гидрокси-2-окса-бициклоСЗ.,0 нонан-3 Э зо-ил}-бутановой кислоты или 13 -транс- -бром-5с Н-5(9о1-)-окись-11сА-гидрокси-15 оксо-прост-13-еноваякислота, метилового эфира, Метаноль9 .36 . ные растворы двух этих соединений МйОН поглощают в УФ-области при ; Л ,нм, е 10, и 229 нм, g 11,600 соответственно. Используя в качестве исходных веществ 4-Н- и 4-галобициклопроизводные, по аналогичной методике получают следующие вещества: 13-транс-5(Ь-Н-5(9оО-окись-15-оксо-прост-13-еновая кислота, метиловый эфир; масс-спектр: М 350; М - Н20 332; М - ОСНз 319; М -(СН2)4СНз.27Э; . метиловый эфир 13-транс-5рН-3 (9)-окись-11-гидрокси-15-оксо-прост -13-еновой кислоты; масс-спектр: М- 366; М З+В; М - ОСИ, 335; М.-(СН2)4 СНз295; метиловый эфир 13-транс-4-хлор-5/b-H-5(9oi)-окись-15-оксо-прост-1 3-еновой кислоты; метиловый эфир 1 З-.транс- -хлор-5рН-5(9оС)-окись-1 lot-гидрокси-15-оксо-прост-1 3-еновой кислоты; метиловый эфир ТЗ-транс- -бром-5pH-5(9oi)-окись-15-оксо-прост-1 3-еновой кислоты; метиловый эфир 1 З-транс- -бром-5рН-5(9о(-)-окись-11о(-гидрокси-15-оксо-прост-13-еновой кислоты; метиловый эфир 13-транс-4-иод-5pH-5(9oi) -окись-1 5-оксо-прост-1 3-еновой кислоты; метиловый эфир 13-транс- -иод-5(ЗН-5 (900-окись-llcir-гидрокси-15-оксо-прост-13-еновой кислоты; метиловый эфир 1 3-транс-5о1Н-5 -() -окись-15-оксо-прост-13-еновой кислоты; масс-спектр: М 350; . М - HgO 332; М ОСНз 319; М (СН2)4 СНз 279; метиловый эфир 13-транс-5сШ-5 (9oi}-окись-1 lot-гидрокси-15-оксо-прост-13-еновой кислоты; массспектр М 336; М - НаР 348; м ОСН, 335; М - (СН2.)4 метиловый эфир 13-транс-4-хлор-5в1Н-5(9) -окись-15-оксо-прост-13-еновой кислоты; метиловый эфир 13-транс-4-хлор-5с(Н-5 (9ot) -окись-1 lot-гидрокси-15-оксо-прост-13-вновой кислоты; метиловый эфир 13-траис- -бром-5 iH-5 (9dL) -окись-15-оксо-прост-13-ено-, вой кислоты; метиловый эфир 13-транс- -бром-5бШ-5 (9оО -оки сь-11о1 гидрокси-15-оксо-прост-13-еноаой кислоты; 3797 метиловый эфир П-транс- -иод-бсАН-5 (9ot) -окись-15-оксо-прост-13-еновой КИСЛОТЫ; метиловый эфир 1 3-тренс- -иод-5о1Н-5(9о6)-окись-11с/.-гидрокси-15-оксо-прост-13-еновой кислоты. Пример tf. По методике примера 2, по реакции между 620 мг (2-оксо-З-метил-4-бутоксибутил) фосфоната и мг NaH (75), и 0,3 г 5-(6-экзо-формил-7-эндо-гидрокси-2-окса-бицикло 3,3,0 октан-3-ил)-пентановая кислота, метилового эфира в диметоксиэтане, получают после хроматографирования на силикагеле (25 г), используя в качестве элюента смесь этиловый эфир:гексан в соотношении 1:1, 0,15 г 13t-6rilH-6(9oL)-окись-llot-гидрокси-15-оксо-16-метил-1б-бутокси-18,19,20-тринор-прост-13-еновая кис/ 1 меон лота, метилового эфира ( Q, 228 нм, Е 14,500), а также 300 м 61ЬН-изомера ( Л 227 нм, t 12,280). Масс-спектр: т/е tlO М ; т/е 392 М - Н20; т/е 379 М - OCHj , We 295 115; т/е 115 CHj-CH O-C-vHg.. Спектры двух изомеров аналогичны при минимальном различии уровней вторичной фрагментации. Используя такую же методику, получают 5-хлор-5-бром- и 5-иодпроизводные метилового эфира 1Зt-6 H-6(9cO-oкиcь-1 1о(-гидрокси-15-оксо-1б-метил -1б-бутокси-Т8, 19,20-тринор-прост-13-еновой кислоты. Для 5-Св массспектр; М «46/ +, 428/42б; 391, 276 Для 5-Вг масс-спектр; М 490/4(8; 472/470; 391; 276 Для 5-1-масс-спект М 536; 518; 3S1; 276. Пример 45. Согласно методике примера 44 из (7-экзо-формил-7-эндо-гидрокси-2-окса-бициклоСЗ , ,0 нoнaн-ЗS-ил)-бyтaнoвaя кислота, мети ... лового эфира и 4-иод-биаиклического производного получают следующие вещества:метиловый эфир 13t-5pH-5(9ct)-окись-1 IcL-гидрокси-15-оксо-1б-метил -16-бутокси-18,19,20-тринор-прост-13-еновой кислоты; масс-спектр: И 410; 392; 379; 295; 229 6 1 4000; , метиловый эфир 131- -иод-5 Н-5(9сОокись-11о.-гидрокси-15-оксо-1б-метил16-бутокси-18,19,20-тринор-прост-13-еновой кислоты; М 536; 518; 391; 76;Л 228 нм, е M,kQQ; метиловый эфир 131-5е(,Н-5(9о)-окись-1 loi- гидрокси-15-оксо-16-метил-16-бутокси-18,19,20-тринор-прост-13-еновой кислоты; 892; 379; 295; УФ:А,т1с.х 227 нм, g 11,800; метиловый эфир 13t- -иoд-5c H-5 (9о1.)-окись-11о1-гидрокси-15-оксо-16-метил-1б-бутокси-18,19,20-тринор-noocT-l3-еновой кислоты; М 536; 518; 391; 276;,,, 226 ни, е 10,300. Пример W.K суспензии k мг NaH 80 в 10 мл бензола добавляют раствор 375 мг (2-оксо-З,3-диметилгептил)-диметилфосфоната в 10 мл бензола и через 30 мин раствор 0,305 г 5-ИОД-5-(6-экзо -формил-2-оксабицикло 3,0 oктaн-3 -ил)-пeнтaнoвaя кислота, метилового эфира. Посл перемешивания в течение kS мин смесь разбавляют водным раствором NaHJO. Органическую фазу промывают до нейтральной реакции, сушат и концентрируют до небольшого объема. Адсорбцией на силикагеле и элюированием смеСЬЮ циклогексан:этиловый эфир 90:10 получают 0,12 г 131-5-иод-6 Н-Ы9ои-окись-15-оксо-1б,16-димeтил-пpocт-13-eнoвaя кислота, метилового эфира и 0,095 г 131-5-иод-6оШ-6(9оОокись-15-оксо-16,16-диметил-13-еновая кислота, метилового эфира. Пример 47. В результате замещения в методике примера 46 формильных производных,.полученных согласно примеру 3, получают следующие 16,16-диметилпроизводные; 13t-6 H-6(96t)-окись-15-оксо-1б, 1б-диметил-прост-13-еновая кислота, метиловый эфир; 131-6/ьН-6(9о1)-окись-1 laL-гидрокси-15-оксо-16,16-диметил-прост-13-еновая кислота, метиловый эфир; метиловый эфир 13t-5(iH-5(9oO-окись-15-оксо-16,1б-диметил-прост-13-еновой кислоты;А.| 226им; t ..-X. ....«...iil- ллл е 15,000; метиловый эфир 13t-5(5H-5(9oO-окись-1 let- гидрокси-15-оксо- 1б, 16-диметил-прост-13-еновой кислоты; 226 нм; 8 13,050; метиловый эфир 131-5-хлор-6(ЬН-6 ()-окись-15-оксо-16,16-диметил-прост-13 еновой кислоты; 39 метиловый эфир 13t-5-xnop-6|5H-6 (Sbi) -окись-11 1-гидрокси-15-оксо-16, 1б-диметил-прост-13-еновой кислоты; метиловый эфир 13t- -xлop-5 -5 {9оО-окись-15-оксо-16,Тб-диметил-прост-13-еновой кислоты; метиловый эфир Зt- -xлop-5f -5 (9oi)-окись-Цо -гидрокси-15-оксо-16, 1б-диметил -прост-ТЗ-енрвой кислоты; метиловый эфир 13t-5-6pOM-e H-(9oi)-окись-15-оксо-16,16-диметил-прост-13-еновой кислоты; метиловый эфир 13t-5-6poM-6pH-6 (Э) -окись-1 Ы-гид роке и-15-оксо-16, 1б-диметил-прост-13 еновой кислоты; метиловый эфир 13t- -6poM-5/bH-5 (900-окись-15-оксо-16,1б-диметил-прост-13-еновой кислоты; метиловый эфир 13t-4-6poM-5/iH-5 (9ot-) -окись-1 lot-гидрокси-15-оксо-16 1б-диметил-прост- 13-еновой кислоты; метиловый эфир 131-5-иод-6рН-6 (9ci)-окись-1 5-оксо-16 ,1б-диметил-прост-13-еновой кислоты; метиловый эфир 131-5-иод-6/ъ Н-6 {9оО-окись-11о6-гидрокси-15-оксо-16, 16-диметил-прост-13-еновой кислоты; метиловый эфир 13t-4-иoд-5(ЬH-5 (9ot) -окись-15-оксо-16,16-диметил-прост-13-еновой кислоты; метиловый эфир 1 Зt-4-иoд-5/iH-5 (9оО-окись-11о -гидрокси-15-оксо-16, 1б-диметил-прост-13-еновой кислоты метиловый эфир 13t-6otH-6(9ciO-окись-15-оксо-1б,1б-диметил-прост-13-еновой кислоты; метиловый эфир 1 3t-6oLH-6(9ot)-окись-1 lot- гидрокси-15-оксо-16,16-диметил-прост-13-еновой кислоты; метиловый эфир 13t-5om-5(9oi)-окись-15-оксо-16,16-диметил-прост-13-еновой кислоты; Лnioix 229 им j е. 1,500; метиловый эфир 13t-5oH-5(9cO-окись-11о6-гидрокси-15-оксо-1б, 16-диметил-прост-13 еновой кислоты; 228 нм ,€ 13,250; пюлметиловый эфир 131-5-хлор-6а. Н-6 (9ot) -окись-15-оксо-16,16-диметил-прост-13-еновой кислоты; , метиловый эфир 131-5-хлор-6о1Н-6 {9оО-окись-11о6-гидрокси-15-оксо-16 , 16-диметил-прост-13-еновой кислоты; метиловый эфир 131- -хлор-5о1Н-5 (9оС) -окись-15-оксо-16 ,16-диметил-прост-13-еновой кислоты; метиловый эфир 13 -А-хлор-5ЫН-5(9ci) -окись -1 lot- гидрокси-15-оксо-16, 16-диметил-прост-13-еновой кислоты; 5 метиловый эфир 13t-5-6pOM-6ctH-6 (9of) -окись -15-оксо-16,16-диметил-прост-13-еновой кислоты; метиловый эфир 13t-5-6pOM-6dH-6 (9oit).-окись-Hot-гидрокси-15-ОКСО-16, 16-диметил-прост-13-еиовой кйслотм; метиловый эфир 13t- -6pOM-5oLH-5 {9od) -окись-15-ЙКСО-16, 1б-диметил-прост-13-еновой кислоты; метиловый эфир 13t-4-6pOM-5otH-5 (9ot)-1 lot-гидрокси-15-оксо-16,16-диметил-прост-13-еновой кислоты; метиловый эфир 13t-5-иoд-6otH-6 (9ot)-OKHCb-15-OKco-l6,1б-диметил-прост-ГЗ-еновой кислоты; метиловый эфир 13t-5-иoд-6oiH6 (9ot)-окись-11 ot-гидрокси-15-оксо-16, 16-диметил-прост-13-еновой кислоты; метиловый эфир 131- -иод-5о1-Н-5 (9oL) -окись-15 оксо-16 , 1б-диметил-прост-1Звеновой кислоты; метиловый эфир 1 31- -иод-5о1Нб(9о)-окись-11ot-гидpoкcи-15-оксо-16, 16-диметил-прост-13-еновой кислоты. Пример 48. К суспензии 178 мг NaH ( дисперсия в минеральном масле) в 15 мл бензола добавляют по каплям раствор 1,55 г (2-oKco-3(S, К)-фтор- -циклогексилбутил)-диметилфосфоната в 10 мл безводного бензола. Через 30 перемешивания добавляют раствор i г метилового эфира 5-(6-экзо-формил-7-эндо-гидрокси-2-окса-бицикло 3,3,03-oкtaн-3f-ил)-пентановой кислоты и перемешивание продолжают еще в течение 1 ч. Смесь нейтрализуют 30%-ным водным раствором NaH2P04 и органическую фазу отделяют , концентрируют и адсорбируют на силикагеле. Элюирование смесью CHgCPg Et20 (90:10) дает 0,62 г метилового эфира 13t-6ciLH-6(9oi)-окись-1 lot-гидрокси-15-оксо-1б-($, R)-фтор-17-Цикло«-ексил-Т 8,19,20-тринор-прост-13-еновой кислоты ( А то,ж: -238НМ, е 12,765) и 0,31 г б Н-изомера ( AJS 238 нм, е 9,870). Данные ЯМР для первого соединения (). М.Д.: 3,6; S ЗН СОаСН ; 3,8 (т) ТНСа протон; 1,03 (q) 1Н протон С.,4; ,3(т) 1Н боШ; 3,00 и 5,5 (t) 1/2Н 1/2Н (ЗНР 55 Гц); 6,5 (q) 1Н протон С|4; 6.9 (а) 1Н. C-ii JHilrH-f 3,5 Гц, JMi3-H 2l5,5 Гц. . 978 .: Обработкой. этого соединения пири дином и уксусным ангидридом его превращают в 11с -вчетоксипроизводное, для которого данные ЯМР-анализа имеют следующий вид (CHCPj) м.д.: 2,02s, ЗН OCOCHj; S ЗН С02СНа; 3,8 протон Сд; «,25 m 1Н 6 Н; Ц,66 5,22 tt 1/2Н, 1/2Н протон С ; ,97q Н протон С,,; 6,51 протон С 6,90 протон . . Для диастереоизомерных гидроксикетонов масс-спектр дает следующие значения масс: М k2 ш/е и датем М - М - HI; М - CHjOH/CH O; M- -СН2 -СНОН (базисный ион); М J15; и М2-- (СНСНз-С Н.). В масс-спектре экзо-диастереоизоме ,ра превалируют следующие значения масс: М - и М - 4t,28; для ;эндодиастереоизомерз превалируют еледующие значения: -««-18 Из 5 бромпроизводного получают метиловый эфир 1 Зt-5-бpoм-6(H-6(9ot)-oкиcь-11о -гидрокси-15-оксо-1б(5, R)фтор-17-Циклогексил-18,19,20-тринорI - МеОИ -прост-13-еновой кислоты. А„. ..ШС1А 235 нм; е 12,900. Пример Э. Заменяя в методике примера «В реагенты фосфонатом , выбранным из (2-оксо- -циклогексилбутил)-диметилфосфоната и (2-оксо- -фенилбутил)-диметилфосфоната, получают следующие соединения; 13t-6jjH-6(9ot)-окись-1 Ы-гидрокси-15-оксо-17-Циклогексил-18,19,20-тринор-прост-13 еновая кислота, метило вый эфирД 223 нм; 9,780; метиловый 13t-6BH-6(9ot).-окись-11 А-гидрокси-15-оксо-17-Фенил-18,19,20-тринор-прост-13-еновой кислоты;Атс«х 238 нм; g 9,9$0 Я их 6о1Н-изомеры, ,Yiax 230 нм 11,950. Пример 50. К суспензии .178м NaH ( дисперсия в минеральном масле) в безводном тетрагидрофуране при добавляют по .каплям при пере мешивании раствор 1,63 г 2-оксо-З-(м -хлорфенокси)-пропил-диметилфосфонат в 10 мл безводного ТГФ. Через 30 мин перемешивания добавляют раствор 1 г метилового эфира 5-(6-экзо-формил-7-эндо- 2-оксабициклоСЗ ,3,0 }-октан-3 -ил)-пентановой кислоты и перемешивание продолжают еще в течение 1 ч; Смесь подкисляют водным раствором NaHjPO, органическую фазу отделяют , . Ц2 и водную фазу повторно экстрагируют ензолом. Из объединенного органичесГО экстракта после хроматографирования на силикагеле, используя в качестве элюента смесь CHnC n:EtrtO (95:5), получают 0,3 гметилового эфира 131-6о(Л-6(9сО-окись-1 lct-гидрокси-15 оксо-1б-м-хлорфенокси-17.18,19э 20-тетранор-прост7 З-еновой кислоты 227 нм, С. 16,800 и 0,11 г 6/1Н-изомера (, :224 нм, 16,300) Оба диастереоизомера демонстрируют массовый пик т/е «36, соответствующий Этот ион дает следующую йг 1нтациюГн -НО; и ОСНз/СНзОН м - ЦЦ; К - (O-CfeH Ce); Н+НоО( ) и М -(CHj)- , цуо дополнительно подтверждает предположенную структуру, Два этих дистереоизомера имеют следующие различия: экзо-6(1Н изомер демонстрирует пик при М -32 и мало ин 11 тенсивный пик при К - kk, эндо-6 -изомер демонстрирует пик при М -31 и интенсивный пик Н . Пример 51 Замена фосфоната в методике примера 50 на 2-оксо-З(м-трифторметилфенокси)-пропил-диметилфосфоиат и 2-оксо-З- (п -фторфенокси -пропил-диметилфосфонат приводит к получению следующих соединений соответственно: метилового эфира 13t-6j3H-5(9ci) -окись-1 lot-гидрокси-15-оксо-16-«-трифторметилфенокси-17,18,19,20-тетранор-прост-13-еновой кислоты; метилового эфира 13t-6pH-6(9ot)-окись -1Тобтидрокси- 5-оксо-1б-п-фторфенок - ,, ,о ,« f:.:.l : : °: Ip ::°p: p r/ ° вой кислоты и их 6о1Н-изомеров. Масс-спектры всех соединений согласуются с предполагаемой структурой, например, в том, что демонстрируют массовый пик М - 115; интересное различие между эндо и экзо-трифторметиловыми аналогами заключается в том, что пики массы М - и М CfjCj Hg-OH присутствуют в спектре экзо изомера, а пик массы М и М - СГд-С Н -О- - в спектре ёндоизомера. Пример 52. Замена фосфоната в методике примера 48 на (2-оксо-З-метилбутил)-диметилфосфонат дает метиловый эфир 131-6рН-6(9оО-окись-11о6-гидрокси-15-оксо-1б5-метил-прост-13-еновой кислоты и его боШ-изомер. К раствору 2,2 г 6 9Н-изомера в 2,6 мл 3 97 пиридина, охлажденному до , добавляют 1,05 мл уксусного ангидрида/ Раствор выдерживают при О С в течение мочи и затем его добавляют к избытку холодной 0,05 н.серной кислоты. Экстракция ЭТИЛ09ЫМ эфиром и выпаривание досуха приводят к образованию 2,3 г 13t-6/5H-6(9oi)-oкиcь-not-гидpoкcи-15-оксо-1б$-метил-прост-13-еновая кислота, .метиловый эфир-П-ацетата ( 229 нм, е 12,050). 875 мг брома в ледяной уксусной кислоте по каплям добавляют к раствору последнего соединения в 10 мл ледяной уксусной кислоты до появления светло-оранжевой окраски. Затем добавляют 1,52 г безводного карбоната калия и полученную смесь выдерживают при 80°С в течение k-S ч до завершения осаждения бромистого калия. Избыток уксусной кислоты удаляют в вакууме , добавляют воду и устанавливают рН 6,8 с помощью гидроокиси щелочного металла. Затем полученную смесь экстрагируют этиловым эфиром и органическую фазу концентрируют до небольшого объема. В результате абсорбции на силикагеле и элюирования смесью хлористого метилена и этилового эфира (70: 30 получают 2,01 г 13t-6fЗH-6(9o(.)-oкиcь-1 loi-гидрокси-14-бром-15-оксо-16s метил-прост-13-еновая кислоТа, метиловый эфир-11-ацетата (Д , нм таий аЛып-11-л;|ртата (Л. . :7ftQi-ik е 11,400). Аналогичным образом получают бс Низомер. Пример 53- Раствор 2,06 г {2-оксо-З-метилгептил)-диметилфосфоната в 20 мл диметоксиэтана по каплям добавляют к суспензии 0,265 г NaH ( дисперсия в минеральном масле) в ДМЭ (10 мл). После перемешиЬания в течение 30 мин добавляют 1,6 г Н-бромсукцинимида и интенсивное перемешивани продолжают в течение 10 мин Затем добавляют 1,35 г метилового ;Эфира 5-(6-экзо-|формил-7-эндо-гидрокси-2-окса-бициклЬСЗ,3,ОЗоктан-3- ил) пентановой кислоты в 5 мл диметоксиэтана. Полученную смесь перемешивают в течение 1 ч и добавляют 20 мл 30 -ного NaH2P04. После обычной обработки получают сырой 1 -броменон. Разделение на силикагеле с помощью смеси хлористый метилен:этиловый Эфир (Н5:15) приводит к образованию 0,9 г метилового эфира 13t-6 H-6(9ot)-окись 5ЦЦ -1и-гидрокси-14-бром-15-оксо-1б5-метил-прост-13-еновой кислоты и о,92 г 6о4Н-изомера. В ходе обработки О, мл пиридина и 0,2 мл уксусного ангидрида 0,2 г брН-изомера получают 0,205 г 11-ацетоксипроизводного, идентичного во всех отношениях соединению полученному по методике примера 52. Пример 5. Раствор 0,3 г (2-оксо-октил)-диметилфосфоната в 10 мл бензола по каплям добавляют к суспензии 5 мг NaH (80%-ная дисперсия в минеральном масле) в 5 мл бензола. 4ejpe3 1 ч сразу после прекращения выделения Н добавляют 0,32 г N-бромсукцинимида. К полученному карбаниону(1-бром-2-оксо-октил)-диметилфосфоната добавляют раствор 270 мг метилового эфира 5-(6-экзо-формил-7-эндо-гидрокси-2-окса-бицикло 3,3,0}октан-3 -ил)-пентановой КИСЛОТЫ В 8 мл бензола. Через 30 мин реакцию прекращают добавлением 20 мл 10%-ного раствора NaH2P04. Органическая фаза после промывания до нейтральной реакции дает 0,31 г метилового эфира I3t-6fН-6()-окись-1 lot-гидрокси-1 -бром-1.5-оксо-20-метил-прост-1 3 -еновой кислоты; затем этот эфир разделяют на 6otH- ( А нм; € 13,500) и б Н-йзомеры. П р и м е р 55. В результате замены (2-оксо-октил)-диметилфосфоната в методике примера 5 на (2-оксо- -циклогексилбутил)-диметилфосфонат и (2-оксо-4-фенилбутил) -диметилфосфонат получают следующие соединения: метиловый эфир 13t-6(5H-5(9eO-окись-11о -гидрокси-1 -бром-15-оксо-17-циклогексил-18,19,20-тринор-прост-13 еновой кислоты; нм; метиловый эфир 13t-6/Wi-6(9ot)-окись-1 lot-гидрокси-14-бром-15-оксо-1 7 фенил-18,19,20-трйнор-прост2 47 нм; -13 ено80Й кислоты, Л е И,500. Пример 56. В результате замены формильных производных в примерах 5355 на метиловый эфир 5-иод-бт(6-экзo-фopмил-7-эндo-гидpoкcи-2-oкca-бициклoCЗ,3,0 oктaн-Зy-ил)пeнтaнoвoй кислоты, метиловый эфир It-иод-«-(7-экзо-формил-В-эндо-гидJSрокси-2-окса-6ициклоСЗ, ОТ Р эн-3fил)-бутановой кислоты и соотве ствующее tH-npoMSBdAHoe получают следующие соединения: метиловый эфир 13t-5-иoд-6 H-6 (9ot) -окись-1 lot- гидрокси-1 4-бром-1 $-оксо- 1б5.-метил-пррст-13-еновой ,МеОН кислоты; Д нм; е 12,300; метиловый эфир 131- -иод-5 Н-5 (9оО -окись-11pi-гидрокси-Т -бром-15 -оксо-1б$-метйл-прост-13-еновой ки 235 ни; € 11,950: лоты; А метиловый эфир 13t-5ftH-6(9rf)-окись-11Ы-гидрокси-14-бром-15-оксо-1б5-метил-прост-13:еновой кисло МеОН 245 нм; е 10,350; метиловый эфир 131-5-иод-6|&Н-6 (9сО-окись-Hot-гидрокси-Н-бром-15-ОКСО-20-метил-прост 13-.еновой кислоты; Л 239 им; 6 13,2 метиловый эфир 131-4-иод-5/5Н-5 (9«i)-окись-Hot-гидрокси-11 -бром-15 -оксо-20-метил-прост-13-еновой кис .МеОН 2 нм; е 12,650; метиловый эфир 13t-5/5H-5(9oO, - . I -окись-lloi-ГИДРОКСИ-1i.-6pOM4 5-окс -20-метил-прост-13-еновои кислоты wa°x нм; € 14,500. метиловый эфир 1 31-5-иод-6/ Н-6 (9ot)-окись-1 loi-гидрокси-14-бром-15 -оксо-17-циклогексил-18,19,20-трин I- -прост-13-еновой кислоты; X 235 нм; е 12JOO; метиловый эфир 13t-5jaH-5C9ot) -окись-1 lot- гидрокси-1 -бром-15-окс -17-аиклогексил-18,19,20-тринорМвОН-прост-13-еновой кислоты; А max 231 нм; е 11,750; метиловый эфир 1;31-5-иод-6)-6 (9оО-окись-1 lot-гидрокси-14-бром-15-оксо-17-фенил-18,19,20-тринор -npqcT-13-еновой кислоты; Л 248 нм; е 13,100; метиловый эфир 13t-5/bH-5(9oO-окись-11 -гидрркси-1 -бром-15-оксо-17-феиил-18,19,20-тринор-прост-18-еновой кислоты; 1. 11,100. Л р и м е р 57. Раствор 0,61 г 2-оксо-октил-трифенилфосфонийбромида в 6 мл ДМСО добавляют к раствору 0,15 г трет-бутилата калия в 3 мл {ДНСО, поддерживая при этом темпера туру реакции 1б-19 С. Затем добавляют 0,27 г метилового эфира 5( -формил-7-эндо-гидрокси-2-окса-бициклоСЗ,7,0 октан-31 ил)-пентановой кислоты в 8 мл безводного тетрагкдрофургжа. Через 30 мин перемешивания добавляют равный объем воды и смесь экстрагируют этиловым эфиром. Объединенный органический экстракт промывают до нейтральной реакции и выпаривают растворитель. В результате роматрграфирования на силйкагеяе (циклогексан:этиловь й эфир iO:60) получают 9,2t г метилового 13t-6 H-6(9oO-окись-11 о(-гидрокси-15-оксо-20-метип-прост-13-еновой кислоты. Препаративной тонкослойной |)(роматографией (SiOjj-EtjO) эту смесь разделяют на и -изомеры. Пример 53. Раствор метилового эфира dE-13t-6ciH-6(9oO-oKMCb-11ob-гидрокси-15-оксо-13-еновой кислоты I имк I I J rvnwjiiM я (экзо-изомер с большим значением R) ( г) в сухом этиловом эфире(30 1 добавляют к перемешиваемому 0,1 М раствору 2п (ВН4}г в cyxo этиловом эфире (30 мл) за 15-минутный промемуток времени. Через 2 ч избыток гента разлагают осторожным добавлением насыв|енмого раствора NaCf и 2 и. водного раствора серной кислотм. Органический слой отделяют, промывмот до нейтральной реакции и выпаривают досуха с получением остатка, который адсорбируют на силикагеле и элюируют этиловым эфиром с образованием 0,38 г метилового эфира t3t-6(iH-6(9oO-OKHCb-Hot, 15й-гидроксипростеновой кислоты в виде маслянистой жидкости и О,(2 г метилового эфира dl-13t-6otH-6(9cd-вкись-11 155-дигидроксипростеновой кислоты, т. пл. 69-71°С. Массспектр: 350 М -18; 319 М - 18-СНзО; 318 М. -18-СНзОН. Раствор этого эфире в метаноле (4 мл) обрабатывают 60 мл гидроокиси лития и вод0 «7 (0,8 мл) в течение 8 ч при комнатно температуре. Метанол отгоняют в вак уме, остаток разбавляют водой и экс рагируют этиловым эфиром для удаления нейтральных примесей. Щелочную фазу обрабатывают водным насыщенным раствором NaH2P04 до рН 5 и затем экстрагируют этиловым эфиром. После ние органические фазы собирают с получением после выпаривания раство рителя свободной dE-13t-6otW-6(9ot -окись-1Ы, 155-дигидроксипростеновой кислоты, т. пл. 105-106 С, 15-гидроксисоединение представляет собой не способное кристаллизоваться масло. Аналогичным образом, используя 15-кетосоединение с реакции восстановления Zn (ВН4)2 получают кроме 15-эписпирта, метиловый эфир nat-13t-6o K-6 (9сО -окись- Hoi, 155-дигидроксипростеновой кислоты, т.пл 71-72 С ,CctJx) +10, CoiJ365 +32,2° (GHCe), и после омыления эфира получают свободную кислоту, т. пл. lOI-IOZ C, Cotjj) +6,34°, Wbfcff +33,2С ). Используя 8 качестве исходных ве ществ эндо-диастереоизомеры (более полярные соединения), получают следующие эфиры: метиловый эфир t3t-6pH-6(9oO -окись-1 lot, 15К-Яигидрокси-простеновой кислоты (dB, nat, ent, масла); метиловый эфир 13t-6/lH-6(9oi)-окись-1 lot, 155-дигидрокси-простеновой кислоты (dE, nat, +2,, МъьВ +52,9° (CHCe), масло; ent WJj) -22°, масло) и после омыления получают следующие свободные кислоты; 13t-6jiH-6(3o -окись-11й1,15К-дигидрокси-простеновую кислоту (dP, nat, ent, масла); 13t-6 H-6(9Ы)-oкиcь-no,15S-дигидроксипростеновую кислрту (dB, масло, nat , т.пл. 78-80°С WJj) 32,5°,CcstJ3fe5 -11,б (EtOH), ent. Т, пл; 78-79°С, (EtOH). Пример 59-8 условиях, ког да температуру реакционной смеси по держивают примерно от -5.до , .раствор 153 мг NaBH4 в 7 мл пропан-ола постепенно добавляют к раствору 0,332 г безводного СаСЪг в пропан -2-оле (7 мл)| затем при перемешивании раствор сложного метилового эфира 13t-6o(H-6(9()-оксид-1 lot-окси-15-оксо-1б(5, К)-фтор-17-циклогексил-18,19,20-тринор-прост-13-еновой кислоты (0,38 г) в 3 мл пропан-2-ола добавляют к приготовленному ранее Са(ВН4)2 в течение около ЦО мин. Температуру реакционной смеси поддерживают при перемешивании около , затем избыток реагента разлагают, добавляя 5 мл ацетона и 2 мл воды. Растворитель выпаривают в вакууме, а остаток распределяют между водой , 0,1 н. H-SO и этилацетатом. Органические экстракты собирают, промывают до нейтрализации и после выпаривания растворителя остаток хроматографируют на силикагеле (30 г), используя в качестве элюента смесь этиловый эфир в соотношении 70:30. В элюате получают 0,21 г сложного метилового эфира 13t-.6oiH-6(9ot)-оксид-1 lot, 15К-диокси-1б(5, R) -фтор 7циклогексил-18,19,20-тринор-прост-13-еновой кислоты и 0,1 г 155-эпимера, т.пл. (из этилового эфира). АН а-; логичным способом восстановление б Н-изомера (220 мг) приводит к получению сложного метилового эфира 13t-6рН-6 (9ot) -оксид-1 lot, 15К-Диокси-16 (S, R)-фтop-17-Циклoгeкcил-18,19,20-тpинop-пpocт-13-eнoвoй кислоты (0,1 г), т. пл. 63-64°С (из изопропилового эфира) и 60 мг 15S-cn ipTa. Для 6/5Н-155-спирта определение 16S-фторизомера дает Coijj) +7° (EtOH). Пример 60. Раствор сложного метилового эфира 13t-6otH-6(9oi)-оксид-11о -окси-15-кето-1б-метил-1б-бутокси-18,19,20-тринор-простеновой кислоты (0,15 г) в метаноле (5 мл) охлаждают при температуре от -5 до и восстанавливают, добавляя раствор NaBH (30 мг) в воде (0,5 мл) Реакционную смесь нейтрализуют, до бавляя 15%-ный водный раствор МаН2Рр4 через 15 мин, а затем выпаривают в вакууме. Водный остаток экстрагируют этиловым эфиром, в результате чего получают неочищенную смесь эпимерных 15R,15S-спиртов. После хроматографического разделения на силикагеле (в качестве элюента используют смесь -этиловый эфир в соотношении 70:80) получают соответственно сложный метиловый эфир 13t-6efH-6(9oO-оксид-11о, 15В-Диоксит 16-метил-16-бутокси-18,13,20-тринор-простеновой кислоты (5 мг) и 155-окси-эпимер. 9 X ). Масс-спектр: М k}2; М . Н,р М - 376; Пример 61. Восстанавливая сложный эфир 13t-5otH-5(9ot)-оксид-lU-окси-15-кето-16-метил-16-6утокси-18, 19,20-тринор-простеновой кислоты в e же условиях, что и в примере 60, ё- 4 ослвду«|цмм-хромато{ч афиче ским.фаз делением эпимерных спиртов (300 мг) на силикагеле (12 г), используя в качестве элюента смесь метиленхлоридэтиловый эфир 75:25, получают 100 мг сложного метилового эфира 13t-5oiH-5 .(9о)-оксид-1 Ы,15К-диокси-1б-метил-1б-бутокси-18,19,20-тринор-простеновой кислоты и 110 мг 155-эпимера, Масс спектр: Нсн:, И -HjO М -2Н20 376; 0-(4Н9297. Посл CHj их омыления получают соответствующие свободные кислоты. Пример 62. К перемешиваемому 0,12 М раствору цинкборгидрида в этиловом эфире (8 мл) по каплям добавляют раствор 0,135 г 13t-5-6poM-6otH-6 (9ot) -оксид-1 loi-окси-15-оксопротеинбвой кислоты сложного метилового эфира в 2 мл безводного Et-O Полученную смесь перемешивают в течение 2 ч и избыток реагента разлагают водной 2 H.. Органические фазы разделяют, промывают до нейтрализации и выпаривают досуха. После тонкослойной хроматографии на силикагеле с использованием в качестве элюента смеси этиловый эфир отилацетат в соотношении 90:10 получают ЗВ мг сложного метилового эфира 131-5-бром-6о Н-6(9.о)оксид-1Ы,15Я-диоксипростеновой кислоты и 46 мг 155-эпимера. Пример 63. Используя в качестве исходного соединения О,2 г сложного метилового эфира 131-5,1 -дибром-6 Н-6{9оООКСИД-llot-окси-15-оксопростеновой кислоты и при хром тографическом разделении на силикаг ле в качестве элюента смесь CHjCj этиловый эфир в соотношении 60 iW, получают 0,056 г сложного метиловог эфира 13t-5,1t-дибpoм-6pH-6(9oO-оксид- 1 lot, 15Н-диоксипростеновой кисло ты и 0,098 г 155-изомера. . .92 . 50 , Затем раствор этого продукта в етаноле гидролизуют водным раствором i ОН, в результате чего получают 2 мг 131-5,1 -Дибром-6о Н-6(9«А)-окид-11о1,155-диоксипростеновой кислоты. Пример . Согласно примеру 0, используя в качестве растворитея изопропанол и Na ВН (S мг), в езультате восстановления 0, г ложного метилового эфира 13t-6pH-6 -6(9о)-окси -1 ЬЬ-ркси-15-оксо-1б- метарифторметил)-фенокси-17,1В,19,20-тетанор-прост-13 еновой кислоты получат 0,20 г сложного метилового эфира 13t-6&H-6 (9вО -оксид-1 lot, 155-диокси-16-(мета-трифторметил)-фенокси-17, 18,19,20-тетранор-прост-13-еновой кислоты, otjjj « +33,3 (МеОН) и 0,18 г 15К-эпимера. Эпимерный 6oW-155-спирт представляет собой масло +12 (МеОН). Пример 65. Раствор сложного метилового эфира 131 1б5-метил-6оШ-6 (9oi) -оксид-1 lot-окси-15-оксо-прост-13-еновой кислоты (0,002 М, 0,72 г) в сухбм этиловом эфире (20 мл) до- бавляют к перемешиваемому раствору цинкборгидрида в эфире (0,01 Н, 100 мл). Спустя мин избыток реагента разлагают, добавляя 2 н.серную кислоту в насьйцеином водном растворе NaCv. Органическую фазу про « 1вают до нейтрализации и выпаривают досуха. Остаток хроматографируют на силикагеле (25 г), используя в качестве элюента смесь метиленхлорид:этиловый эфир в соотношении 80:20, в результате чего получают(7,5 , 0,27 г) 15К-окси-изомер и (1,1-10 М; 0,38 г) 15S-спирт:сложный метиловый эфир 131-1б5-метил-6о Н-6()-оксид-1 Ы,155-диокси-прост-13-еновой кислоты. По этой же методике получают .сложные метиловые эфиры следующих кислот: (9aO-оксид-1б5-метил-1 lot, 155-Аиокси-прост-13-еновой кислоты; } 3t-6/ H-6 (9оО -оксид-16,16-диметил-1 let, 155-диокси-прост-13-еновой кислоты; М 131-6ой1-6(9оО-оксид-20-метил-1И., 155-диокси-прост-13-еновой кислоты, т.пл. 57-59 С, Cb(-3D ,tot 365 (СНСбз); 13t-6pH-6(9cL)-оксид-205-метил-1 let, 155-диокси-прост-13-еновой кислоты, т. пл. 38-39 С, +21,7°, CotJsbS - +77 в СНСЕз; 51 13t-5-6poM-6 -6(9ot)-оксид-16Sметил-1 Idt, 155-диокси-проет-13-енов хислоты; V3t-5-6poM-6pH-6(9c)-оксид-16 -метил-1W,155-яиокси-прост-I3-енов кислоты; 13t-5-6pOM-6/3H-6(9oZ)-oKCMfl-J6,t6 -диметил-1 lei, 155- ДИокси- прост-13-ен вой кислоты; 13t-5-6poM-6ptH-6()- оксид-П у. 155-диокси-20-метия-прост-13-еновой кислоты, +38; метиловый эфир 13t-5-иoд-6/ H-6 (9оО -оксид-1 loi, 155-диокси-прост-13-еновой кислоты; М М - НоО 476; 2Н20 458; 131-1б5-метил-5-иод-6рН-6 (9oi) -ок сид-1 tot, 155-диокси-прост-13-еновой кислоты; М 508; М - HgO 490; И --2Н20 472; 131-20-метил-5-иод-6 -6(9оО ОКСИД- 11 ot, 155-диокси-прост- 3-еновой кислоты; 23; Шз(, (cнceэ ; 13t-5-nofl-6{bH-6{9of}-оксид-1 lot, 15$-диокси-18,19,20-тринор-17-Циклогексил-прост-13-еноврй кислоты (;d(.Jjj +26 (EtOH); 13t-5-HOA-6odH-6 (9ot)-оксид-Г Ы, 155-диокси-18,19,20-тринор-17-цикло гексил-прост-13-еновой кислоты; tdL2-D +17° (EtOH); 131-5-иод-6 5Н-6(ЭоО-оксид-Hot, 155-диокси-18,19,20-тринор-17-фенок си-прост-13-еновой кислоты; roLJj) +21° (EtOH); 13t-5-иoд-6oiH-6(9ot)-oкcид-11ot, 155-яиокси-18,19,20-трин6р-17-фенокси-прост-13-еновой кислоты; oijj) +8° (EtOH); 13t-5-иpд-6/5H-6 (9оО-оксид-15S-OK си-прост-13-еновой кислоты; М 478; М - HQO 460;. 13t-5-иoд-6oltH-6(9o)-оксид-15S-OK си-прост-13-еновой кислоты; М 478; М 460; 13t-5-иoд-6pH-6(9op-оксид-tloi, i55-диокси-прост- 1 йновой кислоты Н 492; М - W; 13t-5-иoд-6otH-6(9oO-оксид-Mot, 155-диокси-прост-13-иновой кислоты; М 492; М - НпО 474; 5-иод-6рН-6(9Ы-оксид-1б5-метил-1 155-диокси-прост-13-иновой кислоты; М 506; М - НоО 488; 5-иод-6/ Н-6(9оО-окси -20-метил-1 loi, 155-диокси-прост-13-)новой кис лоты; WJj) +20 (СНСЕэ)ГМ 506М - 488; метиловый эфир 13t-5-6pOM-6otH-6 (9с)-оксид-11о,155-диокси-18,19,20-тринор-17-ЦИКлогексил-прост-13-еновой кислоты и 5-6poM-6/iH-6(9ot)-оксид производное; М 488/486; М - Н„0 470/468; . метиловый Афир 5-6poM-6juH-6(9ot)-оксид-1 lot, 155-диокси-18,19,20-тринор -17-циклогексил-прост-13-иновой кисг/ лоты; М 486/484; М 468/466; 6-бром-6рН-6 (9oi) -оксид-1 lot, 155-диокси-простановой кислоты, М 450/ 448; М - HgO 432/430; 13t-6-6pOM-6|bH-6(9ot)-оксид-11о, 155-диокси-прост-13-ено8ОЙ кислоты; М- 448/4 6; М - HjO 430/428; М N20 412/410; 13t-20-мeтил-5-б|X)м-6pH-6 (9о) -оксид-1 lot, 155-диокси-прост-13-еновой кислоты; М 462/460; М - HjO 444/442 13t-15-мeтил-6-бpoм-6pH-6(9в)-оксид- 1 lot, 155-диокси-прост-13-еновой кислоты; М 462/460; М - Н«0 444/ 442; 13t-15-метил-5-бром-6сШ-6 (9ot) -оксид-1 lot, 155-диоксй-прост-13-еновой кислоты; М 462/460; М -HjO 444/442; 13t-l6S-мётил-5-бpoм-6 H-6 (9 0-оксид-11 оС, 155-диокси-прост-13-еновой кислоты; М 462/460; М - НпО 41,4/ 442; 1 3t-5- 6pOM- -6(9ot) -оксид-1 lot, 155-диокси-18,19,20-тринор-17-цикл6гексил-прост-13-еновой кислоты; мэсс-спектр (метиловый М 4188/486; М - HjO470/468; 13t-5-6poM-60H-6 (9oi)-ОКСИД-.11 ot, 155-диокси-17,18,19,20-тетранор-16-w-трифторметилфенокси-прост-13-еновой кислоты; М 533/536; М - 520/518; 13t-5-иoд-6pH-6(9o()-oкcи-16S-мeтил-1 lot, 155-диокси-прост-13-еновой кислоты; М 508; М - Н,0 490; М 2 НаО 472; 13 t-5-иод-б -б (9вО-оксид-16R-Meтил-1 lot, 155-диокси-прост-13-еновой кислоты; Н 508; М - 490; М 2 472; 13г-5-иод-6/ Н-6 (9ot) -оксид-16,16-диметил-1 lot, 155-диокси-прост-13-еновой кислоты; TЗt-5-иoд-6 -6(9cO-oкcид-11ot, 155-диокси-20-метил-прост-13-еновой кислоты; С ot J D - 23, - +78 (снсез); 13t-5-xnop-6pH-6(9oO-оксид-16S-метил-1 lei, 155-диокси-прост-13-еновой кислоты; 539 13t-5fiH-5(9ot)-оксид-1б5-метил-11 4 155-диокси-прост-13-еновой кислоты; М 368; М - 350; ZHjjO 332, , М - 283; 131-5/ Н-5(9оО-оксид-1б,16-диметил -1 lot, 155-Дио1 си-прост-13-еновой кислоты; М. 382; М - Hjd М - 2Н« М - 283; . 13t-4-бpoм-5fSH-6(9c/)-16S-мeтил-no 155-диокси-прост-13-еновой кислоты; 13t-4-6pOM-5 -5 (9А)-оксид-16R-метил-11о6,155-диокси-прост-13-еново кислоты; 13t-i -6pOM-6pH-5(9ot) -оксид-16,16-диметил-1 Ы,15$-диокси-прост-13-ено вой кислоты; 1 31 - i - иод-5/ Н - 5 (9()-оксид-16 S-метил-11с/., 155-диоксй-прост-13-еновой кислоты; 131-4-хлор-5(5Н-5(9оО-оксид-1б$-метил-1 Ы, 155-диокси-прост-13-еновой кислоты; 131-6/1Н-6(9о)-оксид-1б5-метил-1Ы 155-диокси-1 -бром-пр6ст-13-еновой , кислоты;. 13t-6pH-6{9ot)-оксид-1бЯ-метил-По1 155-диокси-1 -бром-прост-13-еновой кислоты; 131-6(ЬН-6(9с)-оксио-20-метил-гЫ, 155-диокси-1 4-бром-прбст-13-еновой кислоты; 1 3t-6/.H-6(9« 0-оксид-)5(S, R)-20-диметил-11 ci, 155-диокси-1 t-бром-прост-13-еновой кислоты; 131-5 Н-5(9оО-оксид-1б5-метил-1 lot, 155-диокси-1 -бром-прост-13-еновой кислоты, M l48/ 6; M HjO 430/ 28; М - 2Н20 t 12AlO; М+ - Вг 367; 131-5 -5(9о1)-оксиц-1бК-метил-11о, 155-диокси-1 «-бром-прост-13-еновой кислоты; М М - ЗОА28; М - ZHnO М - Вг 367; 13t-5f5H-5{9ol)-оксид-го-метил-Hot, 155-диокси-1 -бром-прост-13-еноаой кислоты; М kkB/klt6; М - М - 2НпО , М - ВгЗб7 13t-5 H-5 9oi)-оксид-16(S, R)-Meтил-20-метил-1 lot, 15S-диoкcи-1 -бpoм-пpocт-13-eнoвoй кислоты: М 62/ДбО .М - k /kЦ2l - i 26/i«2i, М. - Вг 381; 13t-5-6pOM-6 H-6(9оО-оксид-16S -метил-1 lot, 155-диокси-1 i-бром-прост-13-вновой кислоты; 13t-5-6poM-6/5H-6 (9oi) -оксид- 16R-метил-1 let, 155-диокси-14-бром-прост-13-еновой кислоты; 5 131-5-бром-6|Ж-6(94-окси/ 0-меил-11о(.,155-дйокси-1 -6ром-прост-13еновои кислоты; 13t-5-6poM-6/ H-6 (9о6-оксид-16 (S, R), 20.-диметил-11в6,15S-диoкcиH-6poм-пpocт-13 eнoвйй кислоты; 131- -бромг5{Ш-5(9оО-оксид-1б5-метил-1 Ы, 155-диокси-1 -6ром-.прост-13-еновой кислоты; 13t-4-6poM-5pH-5 (9оО-16В-метил-1 lot, 155-диокси-1 ij-GpoM-npocT-13-еной кислоты; ,. 131- -бром-5(Н-5(9о13-оксид-20-метил-1 lot, 155-диокси-1 -бром-прост-13-еновой кислоты;: 1 3V-4-6poM- -5 (9«4 -оксид-16(5,И), 20-диметил-1 let, 155-диокси-1 -бром-прост-13-еновой кислот-ы; вместе с их 1З -эпимерными спиртами, когда соответствующие 15-кетосоединенйя подвергают восстановлению с последукяцим хроматографическим разделением. Исходя из 6dtH- и 5ой -диа- стереоизомериых 15-кетосреяинений. получают соответствующие 15S- и 15Rспирты. Все эти соединения прдверга- ют омылению до получения соответствующих свободоых кислот. Пример 66. Раствор слржного метилового эфира 13t-5 -иод-6 6{9 i) -оксид-16R-мeтил-15-оксо-прост-. -13-еновой кислоты (0,32 г) в этиловом эфире (8 мл) добавляют к перемешиваемому раствору цинкборгидрида в этиловом эфире (25 мл). Спустя 30 мин избыток реагента разлагают, добавляя насыщенный раствор NaCt и 250 . После обычной обработки выделяют органическую фазу и сырой остаток хроматографируют Haj. силикагеле, используя в качестве элюента смесь CHoCt этиловый эфир, в результатечегополучают 0,16 г сложного метилового эфира 131-5-иод-6(ЬН-6(9оО-оксид-16R-метил-15$-окси-прост-13-еновой кислоты и 0,095 г 15R-эпимepa. По этой же методике получают сложные метиловые эфиры следующих кислот; 13t-6pH-6(9oO-оксид-15S-OKCH-16S-метил-прост-13-еновой кислоты; 131-60Н-6(9ЬО-оксид-155-окси-1бЛ-метил-прост-13-еновой кислоты; 131-6рН-6(9с)-оксид-155-окси-1б, 1б-диметил-прост,-13-еновой кислоты;. 131-6 -5(9оО-оксид-155-окси-1б5-метил-прост-13-еновой кислоты; М 352г И - М - 267 J Ut-5(H-5 (9ot) -оксид-15$-окси-16R-метил-прост-13-еновой кислоты; м 352; м - HgO м + - СбНтз 26 13t-5pH-5(9oi)-oKCHfl-15S-oKCM-l6, 1б-диметил-прост-13 еновой кислоты; М 366; М -Н20 М - С4Н 52б7; 1 3t-5-6poM-6/J H-6 (Sbi) -оксид-15S-окси-1б5-метил-прост-13 еновой кис лоты; 13t-5-6poM-6|JH-6 (9о) -оксид-15S-ClKcи-16R-мeтил-npocт-13 eнoвoй кис лоты; 1 3t-5-6pOM-6f5H-6 (Зо)-оксид-15S-окси-16,16-диметил-прост-13-еновой кислоты; 13t-5-6pOM-6p H-6(9oO-оксид-15S-окси-20-метил-прост-13-еновой кислоты;13t-5-бpoм-6 iH-6(9ot)-oкcид-15Sокси-1б$-20-диметил-прост-13-еновойкислоты вместе с их 15К-эпимерными, спиртами когда восстановлению подвергают соответствующие 15-кетасоединения с последующим хроматографическим разделением. Исходя из 6oiH- и 5о6Н-диастереоиз мерных 15-кетосоединений получают соответствующие 15S- и 15К-спирты. Пример 67. После восстановления соответствующих 15-кетосоединений по одной из методик, описанных в примерах 58-66, получают следующие сложные метиловые эфиры 15S-. окси-9о -оксид-простановых кислот вместе с их 15К-эпимерными спиртами 1 3t-6f H-6(9oO-оксид-11oi,15S-flnoK си-13-Простеновую кислоту; +32° (EtOH); масс-спектр: М 368; М - Н20 360, 2Н20 338; 13.t-l 4-6ром-бАН-6 (9ой -оксид-1 lot, 155-диокси-13 простеновую кислоту: масс-спектр: 448/446; 480/528; 41 2/410; . 13t-14-xлop-6 H-6(9cэO-оксид-Itoi, 155-диокси-13-простеновую кислоту; масс-спектр: 404/402, 386/334; 368/366; Зt-5,14-дибpoм-6/ЭH-6{SoO-oкcид-iloi, 155-диокси-13-простеновую кислоту; 528/526/524; 510/508/506; 492/490/488; (9oi)-oкcий-t Gd, 155-диокси-20-метил-13-простеновую кислоту; 382; 364; 352. 13t-14-6ром-6рН-6(9оО-оксид-1Ы, 15$-диокси-20-метил-1 3-прост,ановую кислоту; 462/460;. 444/442; 426/424; Зt-6,T4-дибpoм-6jf H-6(9ot)-oкcид.-1 loi, 155-диокси-20-метил-13-просте95 новую кислоту; 5 2/5 0/538; S2k/b2o; 506/504/502; 131-5-иод-6 Н-6(9оО-оксид-11о/,155-диокси-20-метил-13-простеновую кислоту, 508, 490; 472; 13t-5-иoд-14-бpoм-6/ H-6(9od)-оксид-1 lot, 155-диокси-20-метил-13-простеновую кислоту; 588/586; 570/568; 552/550; 13t-l4-6poM-6pH-6(9oO-оксид-1Ы, 155-диокси-1б($, Я)-фтЬр-17-циклогексил-18,19,20-тринор-прост-13-еновую кислоту; 506/504; 488/486; 470/468; 131-6,14-дибром-6|5Н-6 (9oi)-оксид-1 55-диокси-16 (S, R) - DTOP- 1 7-циклогексил-18,19,0-тринор-прост-13-еновую кислоту; 586/584/582; 568/566/564; 13t-5-6poM-6 H-6(9oO-оксид-Hot, 155-диокси-1б (S, Я).-фтор-17-циклогексил-18,19,20-тринор-прост-13-еновую кислоту; 506/504; 488/486; 1 (9ot)-оксид-Пс,155-диокси-1б-ди({)тор-17-Циклогексил-18,19,20-тринор-про.ст-13 еиовую кислоту; 444, 426, 408; 1 3t-l 4-бром-6|ЬН-6(9оО-оксид-1 lot, 155-диокси-1б-дифтрр-17-ииклогексил18,19,20-тринор-прост-13-еновую кислоту; 524/522; 506/504; 488/486; 131-6рН-6(9о()-оксид-11ог, 155-диокси-1б(5, R)-фтор-17-фенил-18,19,20-тринор-прост-13-еновую кислоту; . 420; 402; 384; 13 13t-l4-6pOM-6/5H-6(9ot)-оксид-11 155-диокси-16 {S, К)-фтор-17-фенил-18.19,20-тринор-прост-13-еновую кислоту; 500/498 482/480; 464/462; 13t-6pH-6(9oO-оксид-Hot, 155-диокси-17-циклопентил-18,}9 20-тринор-прост-13-еновую кислоту; fot3jj +25 (EtOH); масс-спектр: 394, 376, 358; 13 t-6ifbH-6 (9ot) -оксид-1 lot, 155-диркси-17-циклогексил -l8,19,20-тринор-прост-1 3-еновую кислоту; +26 (EtOH).; масс-спектр: 408, 390, 372; 13t-14-бром-6рН-6 (9ot)-оксид-1 lot, 153-диокси-17-Циклогексил-18., 19 20-тpинop-пpocт- 3-eнoвyю кислоту; 488/486; 470/468; 13t-5,14-дибpoм-6/ H-6(9oO-oкcид-1 lot, 15$-диокси-17-Диииклогексил-18,19,2О-тринор-прост-13-еновую кислоту; 568/566/564; 550/548/546; Зt-5-бpoм-6/ H-6(9ot)-oкcид-llclt, 155-диокси-17-Чиклогексил-18,19,20-тринор-прост-13-еновую кислоту; 488/486 470/468; 5.797 131-5-хлор-6(ЬН-6(9оО-оксид 11о6, 155-диокси-17-циклогексил-18,19,20-тринор-прост-13-еновую кислоту; kkZ/kk2; i l8Al6; 13t-6-MOA-6/5H-6(9oO-OKCMfl-11(/, 155-диокси-1б-метил-1б-бутокси-18, 19,20-тринор-прост-13-еновую кислоту; 510,«82. kSk; 1 31-5-иод-6/ЬН-6 ( -оксид-11 0 155-диокси-1б-метил-1б-пропокси-18, 19,20-тринор-прост-13 еновую кислоту , 68, Зt-5-иoд-6(bH-6(9ot)-оксид-1Ы 155-диокси-1б-метил-1б-амил-окси-18, 19,20-тринор-прост-13-еновую кислоту S2k; «496; . 1 31-6-иод-6 Н-6(9оО-оксид-noi, 155-диокси-17-ЦИКлогептил-18,19,20-тринор-прост-1Э-еновую кислоту; 530; 512; 13t-6((9oO-оксид-nod-155-диокси-16-(л-фтор)-фенокси-17,18,19,20-тетранор-13-простеновую кислоту; 422, kOk, 386; TotJu - +30°; 13t-6 H-6(9ot)-оксид-1 lot, 15$-диокси -1б- фенокси-17,18,19,20-тетранор-13-простеновую кислоту; kQk 386; 368; 1 3t-6/)H-6(9oO-оксид-lloi, 155 диокси-1б-циклогексилокси-17,18,19,20-тетранор-13-простеновую кислоту; 410/392/37 ; 13t-6/5H-6(9o)-оксид-Hot, 155-диокси-16-(м-хлор)-фенокси-17,18,19,20 -тетранор-13-простеновую кислоту; 440/438; 422/420; 404/402; Ы +31°; 131-6(-6(90 -оксид-11oi,155-диокси-16- (м-трифторметил)-фенокси-17,18 19,20-тетранор-13-простеновую кислоту; 472; 454, 43б; fcJL3j 131-14-бром-6|1Н-6(9оО-оксид-11о, 155-диокси-16-(п-фтор)-фенокси-17,18 19,20-тетранор-13-простеновую кислоту; 502/500; 484/482; 13t-l 4-бром-6/ -6 (9oi) -оксид-1 lof, 155-диокси-1б-фенокси-17,18,19,20-тетранор-13-простеновую кислоту; 484/482; 466/464; 13t-l4-6poM-6/JH-6(9ot)-оксид-Hoi, 155-диокси-1б-(и-хлор )-фен6кси-17,18 19,20-тетранор-13-простеновую кисло ту; 520/518/516; 502/500/478; 13 -14-бром-6рН-6(9о)-оксид-11о 155-диокси-1б-(м-трйфторметил)-фенокси-17,18,19,20-тетранор-13-простеновую кислоту; М 552/550, М Н20 534/532; 131 - 5-иод-6/зН - 6 V Sot)-о КС и д-11 oi, 155-диокси-1б-(п-фтор)-фенокси-17, 18,19,20-тетранор-13-простеновую кислоту; М 548; М 530; 131-5-иод-6/ЗН-6 (9of)-оксид-1 Ы, 155-диокси-16-фенокси-17,18,19,20-тетранор-13-простеновую кислоту; М - 530; M - HgO 512; 131-5-иод-6|ЬН-6 {9oi)-оксид-n о, 155-диокси-16-циклогексйлокси-17,18, 19,20-тетранор-13-простемовую кислоту; М 536; М - 518; 13t-5-иoд-6/ H-6{9o -оксид-Ног, 155-диокси-16-(к-хлор)-фенокси-17, 18,19,20-тетранор-13-простеноеую кислоту, 566/564, М- - 548/546 13t-5-иoд-6 bH-6 {9сО-ОКСИД-Hoi, 155-диокси-1б-(м-трифторметил)-фенокси-17, 18,19,20-тетранор-13-простеновую кислоту; 598; 580; 552: 131-5рН-5(9оО-оксид-1Ш,15$-диокси-13-простеновую кислоту; 358; 350, 338; . 1 3t-l4-6poM-5/iH-6 (9ог.)-оч:сид-1Ы, 155-диокси-13-простеновую кислоту, 448/446; 430/428; 412/410; 131-14-хлор-5/ьН-5(9й:)-оксид-1Го, 155-диокси-13-простеновую кислоту; 404/402, 386/384; 368/366; 13t-4,14-дибром-5/5Н-5 (9oi)-оксид-1 lot, 155-диокси-1З-простеноеую кислоту; 528/526/524; 51 /508/506. 492/490/488; 13t-6/iH-5(9oi)-оксид-1Ы,155-диокси-20-метил-1З-простеновую кислоту; 382, 364, 352; 13t-14-6poM-5/2 H-5(9ot)-оксид-11,15-диокси-20-метил-13-простеновую кислоту; 462/460; 444/442, 426,.424; 131-4,14-ди6ром-5/5Н-5 (9оЛ-окСид-1 loi, 155-диокси-20-метил-1 3-простеновую кислоту; 542/540/538; 524/522/ 520, 506/504/502; Зt-4-иoд-5pH-5(9oO-оксид-Hot, 155-диокси-20-метил-1 3-простеиовую кислоту; 508; 490; 472; Зt-4-иoд-14-бpoм-5pH-5(9ot)-oкcид-11 ot, 155-диокси-20-метил-13-простенозую кислоту; 588/586; 570/568, 552/550; 131-14-бром-6/5Н-5(9о)-оксид-11Ч 155-диокси-1б($, К)-фтор-17-аиклогексил-18,19,20-тринор.-прост-13-еновую кислоту; 506/504; 488/486; 13t-4,14-дибром-5/1Н-5(9оО-оксид-11о6,155-диокси-1б-(5, К)-фтор-17- -ииклогексил-18,19,20-тринор-прост-13-еновую кислоту; 586/584/582; 568/566/564; 59 13t-4-6poM-6/iH-6(9o6j-оксид-lIoZ, 155-диокси-1б(5, К)-фтор-17-Циклоге сил- 18,19,20-тринор-прост-13-еновую кислоту; 506/50 ; 88/486; 13 t-5/5-H-5 Od} -оксид-1 Ы, 155-дио окси-1б($, Я)-фтор-17-фенил-18,19,2 -тринор-прост-13-еновую кислоту, 20, , 384; . 13t-U-бpoм-5/ H-5(9o)-oкcид-1Ы, 155-диокси-16(5, R)-фтор-17-фенил-18, Т9,20,гтринор-прост-1 3-еновую кислоту, 500Л98; 482/480; k6k/k62; 13t-5/5H-5(9С.О -оксид-1 loi, 155-диокси- 7-циклопентил-18,19,20-тринор-прост-13-еновую кислоту; 376; 358; 13t-5/aH-5(9oi)-оксид-1 Ы,Т55-диокси-17-ииклогексил-18,19,20-тринор-прост-13-еновую кислоту; Ц08, 390; 372; 13t-l А-бром-5/5Н-5 (9cxJ -оксид-1 loi, 155-диокси-17-циклогексил-18,9,20-тринор-прост-13-еновую кислоту; М ВБЛаЭ; - НуО 1 31-, 14-дибром-5/2 Н-5 (9od) -оксид-1 loi, 155-Аиокси-17-циклогексил-18, 19,20-тринор-прост-13-еновую кислоту; 568/566/564; 550/5t8/5 6; 13t-5/У -5{9oi)-oкcид-11o6,155-диокси-1б-фенокси-17,18,19,20-тетранор-13 простемовую кислоту; - 404; К - НаО 386; М - 2Н20 368; 131-4-иод-5 Н-5(9ой-оксид-11о, 15$-диокси-1б-фенокси-17,18,19,20-тетранор-1З-простеновую кислоту; HjO 512; М 2Н20 13 t-4-иoд-5f н-5 (9оО-оксид-11 ot, 155-диокси-1б-циклогексилокси-17,18, 19,2О-тетранор-1З-простеновую кислоту; М 536; Н - 518; М - 2Н20 518; М - 2Н20 500; 131-4-иод-5/ЗН-5(9од-оксид-1 Ы, 155-диокси-1б-(м-хлор)-фенокси-17,18 19,20-тетранор-13-простеновую кислоту; М 566/564; М - N,0 548/546; 131-4-иод-5|ЗН-5(9с)оксид-1Ы,15$-диокси-16- ((И-трифторметйл) -фенокси-17,18,1Э,20-тетранор-1Д-простено8ую кислоту; .M- - 598; - НлО 580; 2Н20 562. .. Аналогичным образом получают диастереоизомерные oi. Н-9 ойОксид-15S- и о Н-9о -оксид-15К-спирты, если в качестве исходных соединений используют о6Н-9сА-оксид-15-кето-диастереоизомер. Все эти сложные эфиры подвергают далее омылению до получения свободных кислот. 560 Прим ер 68. 0,6 г сложного метилового эфира 13t-6pH-6(9of)-оксидi-1 б5-метил-1 lot-окси-15-оксо-прост-13-еновой кислоты обрабатывают пиридином (2 мл) и уксусным ангидридом (1 мл). Спустя 6 ч при комнатной температуре смесь разбавляют рассолом, подкисляют до рН , и экстрагируют этиловым эфиром. Соединенные органические фазы выпаривают досуха, получают 0,48 г 11-aцeтoкcипpoизвoд ° (mS 229 нм, 6 11,058). Затем раствор этого соединения в этиловом эфире добавляют по каплям к раствору Zn/BH /2 в этиловом эфире. Спустя 30 мин избыток реагента разлагают 1 н.раствором HySO и после обычной обработки получают 0,47 г сложного метилового эфира 13t-5/5H-5 (9oi)-оксид-1б5-метил-1 Ы, T5(SR)-диокси-13-простеновой кислоты-11-ацетата, М+ 424; М -Н20 405; М 339- Раствор этой смеси в (5 мл) охлаждают до температуры примерно -5 до , обрабатывают раствором эфирата BFg (1,2 х М) в CHnCS, а затем раствором диазометана в до получения желтой окраски. Затем реакционную смесь выпаривают до половинного объема в вакууме, промывают водным раствором NaHCO, и водой до нейтрализации и выпаривают досуха, в результате чего получают 0,47 г 13t-5|3H-5 (9ot)-оксид-1б5-метил-11с|1-окси-15 (S, К)-метокси-прост-13-еновая кислота- 1 1 -ацетата (M-f 438; СНзСО 379; М - Of,Н 3 353), который разделяют на индивидуальные изомеры, используя хроматографию на силикагеле и применяя в качестве элюента смесь бензол-этиловый эфир в соотношении 85: 15- С другой стороны, 0,21 г смеси 15 (S, Я)-метоксипроизаодных растворяют в сухом метаноле (4 мл) и селективно деацетилируют, используя обработку 20 мг К2СОз в течение 4 ч при комнат,иой температуре. После нейтрализации путем разбавления водным Na НпРО метанол выпаривают в вакууме и остаток экстрагируют этиловым эфиром (2x5 мл), этилацетатом (2x6 мл). Соединенные органические фазы выпаривают досуха, в результате чего получакуг 180 мг сырого метилового сложного эфира 13t-5рН-5 (9oi) -оксид-1 б5-метил-1 lot-окси-15 (S, К)-метокси-простеновой кисло 619 ты (М 396; М - 378; М+ - 311), который потом легко разделяют с помощью хроматографии на колонке с силикагелем, используя в качестве элюента смесь - этиловый эфир в соотношении 80:20, в результате чего получают два чистых изомера: 15$-метокси- и 15К метокси, Используя ту же с,амую методику, полу чают следующие сложные метиловые эфиры: 13t-6pH-6(9oi)-оксид-16S-метил-1W -окси-155-метокси-прост-13 еновой М - 378; кислоты; 396; м- - 311; 13t-6/ R-6(9Dd)-oкcид- 6R-мeтил-11о -окси-155-метокси-прост-13-еновой кислоты; 13t-6 H-6(Эoi)-okcид-20-мeтил- 1ot-окси-155-метокси-прост-13 еновойкислоты; 13t-5-6pOM-6pH-6 (9ot)-оксид-20-метиЛ-11о -окси-15$-метокси-прост-13 еновой кислоты; 13t-5-6poM-5(bH-6(9oi)-оксид-ТЫ-ок си-155-метс)кси-прост-13 еновой кислоты;13t-5-бpoм-6/ H-6(9oi)-oкcид-l6S-метил-11о окси-155-метокси-прост-13 еновой кислоты; метиловый эфир 1Ы-окси-155-метокси-6 5Н-6 (So) -оксид-1 б5-метил-прост-13 иновой кислоты, rotjj) +2 (Eton); этиловый эфир 1 cзt-oкcи-15S-эт6кcи-6 H-6(9ot.)-oкcид-16-мeтил-пpocт-13-инoвoй кислоты Co(.3D +26(EtOH и их эпимерные 15Р -метоксисоединени получают, используя в качестве исходных соответствующие 11-ai eтoкcи-15 кeтocoeдинeния. По этой же мето дике, но используя {АН-диастереоизомер вместо (ЬН-диастереоизомера, получают также соответствующие .-метокси соединения. Эту же методик МОЖНО использовать для любого из оп санных ранее 15-кетосоединений и аналогично другие диазоалканы можно использовать вместо диазометана. Пример 69. К раствору 0,26 сложного метилового эфира 13t-6|bH-5 :(9rf)-оксид-15 (S, К)-окси-1б$-метил -прост-13 еновой кислоты в метиленхлориде, обработанному 0,3 мл раствора эфирата BFj в метиленхлориде, охлажденному до температуры от -10 до , добавляют раствор диазометана в метиленхлориде до образовани устойчивой желтой окраски. Раствори тель выпаривают в вакууме, а остато роматографируют на силикагеле, исользуя в качестве элюента смесь этиовый эфир:метиленхлорид в соотношеии 10:90, в результате чего получат О,П 5 г сложного метилового эфира 131-6рН-6(9о6)оксид-155-этокси-1б5метил-протеиновой кислоты и 0,1 г 15К-этоксиизомера. Когда смесь 15S, 15(1-спиртов, например T3t-6/iH 6(9oi)-оксид-nqt, 15(S, Я)-диокси-1б$-метил-простеновую кислоту, содержащую св;ободные 11 -окси группы, подвергают обработке По методике примеров 68 и 69. происходит также одновременное алкоксилирование 11-спиртовых функциональных группJ что приводит к получению дийзометана, например, после хроматографического разделения полу-чают 13t-6/bH-6(9ci)-оксид-1Ы, 155-диметокси-1б$-метилпростеновой кислоты сложный метиловый эфир, кроме 15К-эпимерного производного. Аналогичным образом получают следующие 15Sалкоксипроизводные... i , 13t-5/iH-5(9oO -оксид-1 Jot, 155-диметокси-простеновая кислота, М J82i М - СуН-г -ЗП; 13 (9ot)-оксид-11 oi, 155-диметокси-простеновая кислота; 131-6рН-6(9{)-оксид-5-бро«-11й1, 155-диметокси-простеновая кислота; 1 3t-5A H-S(9ot)-оксид-}55-метокси-1б5-метил-простеновая кислота, И 366; М - 281; 13t-6p H-5(9oi) -оксид-155-«етокси-1б$-метил-простеновая кислота; 1 3t-6/3H-6{9oi)-оксид-155-метокси-1бЯ-метилпростановая кислота; 131-6/аН-6()-155-метокси-16-метил-1б-бутокси-18-19,20-тринор-про стеновая кислота (М 396; М 281) и их 15К-эпимеры, а после их омыления LiОН в метаноле получают свободные кислоты. Тем же способом можно получить диастереоизомерные eiH-9ot-оксидные производные, . . 70. К перемешиваемоПримерму раствору 1,33 г 13t-6/5H-6(9oi)-OKсид-1 Ы-окси-16-оксо-прост-1 З-еновой кислоты сложный метиловый эфир-11-ацетатй в 6 мл толуола и S мл бен- . зола, охлажденному , добавляют раствор 1,б7 г метилмагниййодида в этиловом эфире. Спустя 20 мин избыток реагента разлагают ледяным 20%ным раствором хлористого аммония в воде. После разбавления одним объемом этилового эфира органическую фазу промывают водой, бикарбонатом натрия и водой, сушат над сульфатом магния, обрабатывают 0,1 мл пиридина и выпаривают досуха, в результате чего получают 1,2 г 13t-6/3H-6{9oi)-оксид-1 lot, 15{S, R)-диокси-15-метил-простеновой кислоты сложный метиловый эфир-11-ацетата, из которого 0,2 г выделяют а виде чистого компонента с помощьютонкослойной хромато графии на силикагеле, используя в качестве элюента смесь бензол:зфир в соотношении . 1 г смеси двух спиртов растворяют в безводном метаноле (20 мл) и перемешивают в течение 4 ч с 0,25 г К2СО, Смесь выпаривают досуха, остаток распределяют между этиловым эфиром и водным 15 ным HaHij PO. Органическую фазу выпаривают в вакууме, а остаток абсорб руют на силикагеле (200 г). После элюирования .смесью этиловый эфир:изо пропиловый эфир -в соотношении 80:20 получают 20 г 13t-6ciH-6(9ot)-oкcид- 1 15К-диокси-15 мётил-прост-13-еновой кислоты сложного метилового эфира и 0,36 г 155-эпимера. 0,16 г этого соединения растворяют в 12 мл метанола и обрабатывают 0,8 мл воды и 0,2 г . После выстаивания в течение 5 м при комнатной температ уре метанол выпаривают в вакууме, остато обрабатывают 20%-ным и этилацетатом. Органическая фаза содержит 0,1 г Зt-6/lH-6(9oi)oкcид-1 loi, 15S-диокси-15-метил-прост-13-еновой кис лоты; Cot JI5(мeтилoвый эфир) +6,2 (СНСбз)- Соответствующие 1б/гН-изомер получают таким же способом. Для мети лового эфира 13t-6/5H-6(9oi)-oкcид-11oi 15$-диокси-15-метил-прост-13 еновой кислоты Cot-3j)- +19,62° (СНСЕ2). П р и м е р 71. К 1,79 г 13t-5otH 5(9ciO ОКСИД-11с|.-окси-15 оксо-прост-13 еновой кислоты сложный метиловый эфир-11-ацетата е 20 мл безводного тётрагидрофурана добавляют 50 мл 0,3 М этилм.агнийбромида в безводном тетрагидрофуране. Встряхивают в течение 1 ч, удаляют избыток реагента, обрабатывая насыщенным раствором , концентрируют органическую фазу в вакууме и извлекают этиловым эфиром, в результате чего получают 1,62 г (9pi)-оксид-Hot, 15 (S, R)-Диокси-15-этинил-прост-13-еновой кислоты сложный метиленовый эфир-11-ацетата, который растворяют в 25 .б. безводном метаноле и обрабатывают в 250 мг безводного карбоната калия в течение 3 ч при встряхивании. Выпа.ривают в вакууме и разбавляют водным NaHjPO и этиловым эфиром. После выпаривания растворителя из .органической фазы получают 1,1 г сложного метилового эфира 13t-5otH-5 (9oi)-оксид-1 lot, 15(S, R)-диокси-15-этинил-простеновой кислоты (масс-.спектр: М 392; М - М -СуН 321), который разделяют на два чистых 155-окси- и 15К окси-эпимера с помощью хроматографии на силикагеле, используя в качестве элюента смесь бензол:этиловый эфир, взятые в соотношении 1:1, и после омыления 155-окси-эпимера К2СО в метаноле получают 13t-5otH-5(9oO-оксид-1 Ы, 15$-диокси-15-этинил-простеновую кислоту. Масс-спектр: Н 378 М - HgO 360; М - CsH 307. Пример 72. К раствору в безводном тетрагидрофуране (25 мл) ,Ц г 131-5-бром-6/ЭН-6(9о -оксид-15-оксо-прост-13-еновой кислоты сложного метилового эфира, добавляют 0,5 М раствор магнийвинилбромида в тетрагидрофуране (25 мл) при и оставляют выстаиваться в течение k ч при комнатной температуре. Разлагают избыток реагента насыщенным раствором хлористого аммония, разбавляют тетрагидрофураном в вакууме и извлекают этиловым эфиром. Органическую фазу абсорбируют на силикагеле и элюируют смесью метиленхлорид: этиловый эфир, в результате чего получают 0,41 г сложного метилового эфира 131-6-бром-бАН-6(9о)-оксид-15К-окси-15-винилпростеновой кислоты и 0,62 г 155-изомера, который после омыления LiOH в метаноле дает 0,49 г чистой 13t-5-6poM-6/bH-6(9o -оксид-153-окси-15 винил-простеновойКИСЛОТЫ. Пример 73. Раствор 0,98 г 13t-5-6pOM-6|3H-6(9oO-оксид-11о гокси-15-оксо-20-метилпростеновой кислоты сложный метиловый эфир-Т1-айетата в 30 мл смеси бензол:толуол (85:15) охлаждают до и к этому раствору добавляют раствор 0,92 г фенилмагнийбромида в смеси этиловый эфир:бензол. Оставляют выстаиваться в течение 5 ч при комнатной температуре, затем разлагают избыток реагента ледяным 15 -ным раствором повторно промывают органическую фазу водой для нейтрализации, а затем выпариптчют. Сырое 15-фенил-15(5, R) -оксипрриз водное растворяют в безводном метаноле, к которому добавляют 0,25 г KjCOj, продолжают встряхивание в течение 2 ч. Выпаривают досуха,разбав ляют водным NaHftPO и этиловым эфиром и из органической фазы лрсле выпаривания растворителя, получают 0,81 г сложного метилового эфира 13t-5-бpoм-6f H-6(9oi)-oкcид-1 lot, 15(5, К)-диокси-15-фенил-20-метил-простеновой кислоты, который после разделения на силикагеле этиловым эфиром в качестве элюента дабт индивидуальные 155- и 15К-изомеры. Пример 7. Подвергая взаимо действию соответствующие 15-оксопрои водные с реагентом, выбранным из гру пы галогенидов:метилмагния, этилмагния, винилмагния, этинилмагния и фенилмагния, и.действуя в соответств с методиками, описанными в примерах 70-73, полумают следующие метиловые сложные эфиры: 13 t-6/ЬН-б (9od)-оксид-155-окси-15-метил-простеновой кислоты; 13 t-6fiH-6 (9ct) -оксид-155-окси-15, 20-диметил-простеновой кислоты; 13t-6(bH-6(9c()-оксид-155-окси-15-этил-простеновой кислоты; 13t-6fbH-6()-оксид-155-окси-15 -этинил-простеновой кислоты 13t-6|bH-6(9ci)-оксид-1 lot, 15$-диок Си-15-метил-простеновой кислоты; 13t-6(jH-6(9o(.)-оксид-1 Ы, 155-диок си-15-этил-простеновой кислоты; 13.t-6pH-6{9ot) -оксид-1 loi, 155-диок си-15-винил-простеновой кислоты; 131-6/ Л-6(9о)-оксид-11о, 15S-диoк cи-15-этинил-простеновой кислоты; 13 t-6pH-6 (9оО -оксид- 1Ы, 155-диок си-15-фенил-простеновой кислоты; 131-6рН-6(9Ы)-оксид-1Ы,155-диок си-15,20-диметил-простеновой кислот 13t-5-6poM-6/5H-6(9o(.)-оксид-Hot, 155-диокси-15-метил-простеновой кис лоты; 13t-5-6pOM-6pfl-6 (9оО -оксид-1 loi, 155-диокси-15-винилпростеновой кисл ты; 13t-5-6pOM-6pH-6(9oi)-оксид-Hot, 155-диокси-15-этинил-простеновой ки лоты ; 13t-5-6pOM-6(jH-6 (9од -оксид-1 lot, 155-диокси-15-этил-простеновой кислоты ; 1 3t-5-6pOM-6 H-6 (9о)-оксид-1 W, 155-диокси-15-фенил-простеновой кисоты;131-4-бром-5/ЗН-5(9о)-оксид-11, 155-диокси-15-метил-простеновой кисоты;13 t- -6poM-5/5H-5 Oci) -оксид-1 Ы, 155-диокси-15,20-диметил-простеноой кислоты; 131- -бром-5р Н-5(9о)-оксид-По, 155-диокси-15-этинил -простеновой ислоты; 13t-5fiH-5{9b)-оксид-1 W, 155-диоки-15-метил-простеновой кислоты; 368; М - Н«0 350; М - 2Н20 332 - 13t-5/2rf4-5 (9oi) -оксид-1 lod, 155-дикси-15,20-диметил-простеновой кисоты; М 382; М - И 2Н20 М - CfeH 2Э7 13t-5/JH-5{9ot)-оксид-1Ы, 155-диокси-15-фенил-простеновой кислоты; М 430; М - «12; М - М - СуН 359; 3t-5/bH-5(9oO -оксид-1 Ы, 155-диокси-15-этинил-простено8Ой кислоты; М- 378; М - 360; М - ZHgO М - 307; 13t-5fiH-5(9ot)-оксид-1 loi, 155-диокгси-15-винил-простеновой кислоты; М 380; М - HjO 362; М н - , 309; 13t-6pH-5(9ot)-оксид-1 lot, 155-диокси-15-метил-простеновой кислоты и их 15ЛОкси-эпимеры. Аналогично, исходя из otH- (9ot) -оксид-15-кетосоединений получают соответствующие otH-(9сО-оксид-15 замещенные спирты. Пример 75. В атмосфере инертного газа к перемешиваемому раствору 0,Ц6 г 131-1 -бром-6/5Н-6(9ой-6ксид-155-метокси-1б5-метил-прост-13 еновой кислоты метилового сложного эфира в безводном диметилсульфоксиде (5 мл) добавляют трет-бутилат калия (0,15 г), и затем продолжают перемешивать в те«1ение 30 мин. Реакционную смесь разбавляют 2 объемами воды и перемешивают в течение 15 мин, затем экстрагируют этиловым эфиром. Органические фазы повторно экстрагируют 2 X 15 мл, 0,2 H.NaOH, а затем водой до нейтрализации, и выпаривают досуха в результате чего получают 30 мг слож- ного метилового эфира 6/5Н-6(9oi)-оксид- 155тметокси- -16$-метил-прост-13-инЬвой кислоты, +21° (EtOH). Соединенные водные фазы подкисляют 6797872 до рН 5,1 и экстрагируют этиловым эфиром. После выпаривания растворителя получают 0,28 г 6/ЗН-6(9о)-оксид-15S-метокси-1б5-метил-прост-13 иновойкислоты, foiJD +19 ,{EtOH). 5 П р и мер 76. В атмосфере инертного газа при перемешивании и интенсивном удалении влаги к безводному раствору в диметилформамиде 0, г 131-6о1Н-6(9)-оксид-Н-бром-1бЯ-ме- 10 тил-прост-13-еноаьй кислоты добавляют 0,8 г триметилсилилимидазола. Перемешивание продолжают в течение 30 мин, а затем добавляют раствор О,1Э г К-трет-бутилата. После перемешивания еще в течение 30 мин смесь разбавляют 3 объемами воды и перемешивают ее в течение более 2 ч. После подкисления до рН ее экстрагируют смесью этиловый эфир:гексан в соотношении 80:20 20
и органические экстракты сушат и выпариваадт досуха, в результате чего получают 0,31 г 5oiH-5(9ot)-оксид-16Я-метил-прост-13-иновой кислоты, Cot}n +21° .(EtOH).
П р и м е р 77. К раствору метилсульфинилкарбаниона натрия, полученному при нагревании при 60°С в течение 3 ч 30 мин суспензии 50 мг NaH () в 8 мл безводного диметилсульф оксида, при интенсивном, перемешивании в атмосфере инертного газа при 18-20°G, добавляют раствор сложного метилового эфира 13t-6/bH-6(9oO-оксид-Ио, 155-диметокси-Н-бром-1б(5, R -фтор20-метил-прост-13 еновой кислоты (0,86 г) в 5 мл диметилсульфоксида- Спустя lO мин перемешивания приливают избыток 25 -ного и полученную смесь экстрагируют этиловым эфиром, в результате чего полу чают сложный метиловый эфир 6}iH-6(9o -ОКСИД Ы,Т55-диметокси-1б(5, R)-фтор-20-метил-прост 13-иноврй кислоты (0,51 г), roi3j3 t-Zbij EtOH). Пример 78. К раствору 80 мг амида в 10 мл диметилсульфоксида добавляют раствор 13t-H-6pOM-5oiH-6 (9ct)-оксид-;1 lot, 15S-диoкcи-16- 4тpифтopмeтилфeнoкcи-17, 18,19,0-тетранор-прост-13-еновая кислота-11,15 -биотетрагидропиранила простого эфира (0,65 г) в 5 мл диметилсульфоксида. Полученную смесь перемешивают в течение 2 ч, а затем разбавляют водой и экстрагируют этиловым эфиром. Эфирные экстракты после повторного экстрагирования щелочью сливают. Водные щелочные экстракты под ,I 1$
19 20-тетранор-п эост-13- шовоЛ кислоты, Cotjjjs: +15° (EtOH); Проводят деацетилиэацию других 0,2 г продукта, растворенного в 5 мл ацетона, и обрабатывают 3,5 мл 0,2 н.цавелевой кислотой в течение 8 ч при , после того, как ацетон выпаривают, в вякууме, экстрагируют-водную фазу этиЛОВЫ1 эфиром и хроматографируют на 68 кисляют до рН 4,5 и экстрагируют этиловым эфиром, в результате чего пояучают Q,5k г простого эфира SdH-5T9oit)-оксид-1 iol, 155-диокси-1б-#1-трифторметилфенокси-Г7И8,19,20-тетрамор-прост-13-иновая кислота-11,15 бис-тетрагидропиранила. Раствор этого соединения (0,23 г) в безводном этаноле (5 мл) и 2,2-диэтоксипирана (3 мл) обрабатРЫвают 20 мг пара-трлуолсульфокислоты. Спустя 5 ч при комнатной температуре смесь нейтрализуют водным NaKCO, выпаривают в вакууме и остаток распределяют межт ду водой и Зтиловым эфиром. Органические фазы выпаривают и после пропускания остатка через силикагель получают 0,1 г сложного этилового эфира (9с)-оксид-1 lot, 155-диокси-1б-мета трифторметил-фенокси-17,18, силикагеле, испольауя в качестве элюента смесь этиловый эфир:этилацетат в соотношении 95:5, получают свободную кислоту (95 мг), fot3j) + 16,5 (EtOH). Таким же способом исходя из 13t-14-хлор-6в1Н-6( 9с)л-оксид-llei, Т 5S-диокси-17-4иклогексил-IВ,19,20-тринор-пррст-12 в«овая кислота-11,15-бис-диоксанилового эфира получают . 6ciH -6 (9оО д-11dL, 15S -диокси -17-циклогексил 18,19г20-тринор-прост-13-иновую кислоту, toijj) 27,2° (EtOH); метиловый эфир IdLJD ,2° (EtOH), Пример 79. К раствору сложного метилового эфира 13t-1 -6poM-брН-б() -оксид-1 lot, 15S-диокси-16-циклогексилокси-17,18,19,20-тетранор-прост-13-еновой кислоты ( О, г) в 3 мл безводного диметилсульфоксида добавляют через 30 мин раствор 1,5-яиазабицикло 3,,0 ундец-5-ена (Oj25 г) в 2 мл безводного диметилформамида, и реакционную смесь выдер живают в течение 6ч при 65°С. Ее разбавляют .водой, поокисляют до рН 4,5, экстрагируют этиловым эфиром. Из ор ганической фазы после выпаривания растворителя и очистки на 69 силикагеле (продукт элюируют смесью бензол+этиловый эфир в соотношении 80:20) получают 0,29 г сложного метилового эфира 6рн-6 (9оООКСИД-1 loi, 155-диокси-1б-циклогексилокси-17 18 19,20-тетранор-прост-13-иновой кислоты, ГоСЗ 33 +17,1° UtOH). Пример Во. По методикам, описанным в примерах с.7В по В2, и используя в качестве исходных соответствующие 13t-1t-гaлoид-пpocт -13 еновые кислоты, получают следующие прост-13 иновые кислоты; брН-б (3oi) -оксид-1 lot, 155-диокси-прост-13 иновую кислоту, +25 (EtOH); 6(5Н-6 (9oO-оксид-11 0 155-диокси-прост-1 3-иновую кислоту, +37° (EtOH); 6/ЬН-6(9оО-оксид-15-метокси-прос -13-иновую кислоту, 27° (EtOH); 6|ЬН-6 (9ot)-оксид-11о4,155-диокси-1б5-метил-прост-13-иновую кислоту Cot3D 22,5 (EtOH); 6|5Н-6(9оО-оксид-1 Ы, 5S-диoкcи-16S,20-димeтил-пpocт-13инoвyю ки лоту, CotJj) +23° (EtOH); 6/JH-6 (9ci) -оксид-11 oi, 155-диокси-1бК-метИл-прост-13-иновую кислоту CoLJ +36° (EtOH); (9о)-оксид-1 loi, 5S-диoкcи-16S-фтop-пpocт-l 3-иновую кислоту, CoLJD +25° (EtOH)i 6|iH-6(9dL)-оксид-11 з6,155-диокси18-дифтор-прост-13-иновую кислоту, CotJB +16. (EtOH); 6/JH-6(9oO-оксид-1 lot, 15$-диокси-20-метип-прост-13-иновую кислоту, CotJD +16° (EtOH); (9oi) -оксид-1 left, 155-диокси-циклогексил-1В,19,20-тpинop-пpocт -13-инoвyю кислоту, ot) +21 (Е tOH) ; метиловый эфир, ei. р +2б (EtOH), зб (EtOH); 6рН-6(9oi) -о сид-Hot, 155-диокси-1б-фтор-17-циклогексил-18,19,20-т нор-прост-13-иновую кислоту, dLJjj +23° (EtOH); 6fbH-6 (9dO-оксид-Hot, 155-диокси-1б-г1ара-фторфенокси-17,18,19,20-т ранор-прост-13-иновую кислоту, WT +17° (EtOH); Н-6 OcL) -оксид-1 }а, 15$-диокси-фенил-18,19,20-тринор-прост-13-ин вую кислоту, (EtOH); (9ot) -оксид-1 Ы, 155-диокси-1 б5-метил-г1рост-13иновую кислоту CoLJD +19° (EtOH); 5|iH-5 (9oQ -оксид-1 lot, 155-диокси-16s,20-диметил-прост-13-иновую кислоту, +20,5 (EtpH); 5jW-6 (9сО -оксид-11,155-диокси-16Я-метил-прост-1Зиновую кислоту, toCJD +39° (EtOH); 5рН-5 (9«i) -оксид-not, 155-диокси1б5-фтор-прост-13-инову|р кислоту, CotJD +23,5° (EtOH); 5pH-5(9oi)-оксид-11сЛ,155-диокси-прост-13-иновую кислоту, cijti +29° (EtOH); 5|ЬИ-5(9оО--оксид-1 Ы, 155-дж)кси-20-метил-прост-13-иновую кислоту, +27° (EtOH) . Исходя изо Н-19о4)-оксидсоединений по той самой методике получают эпимерные oiН-(9оО-оксид-13-иновые соединения-. Пример 81. 0,12 г сложного метилового эфира 131 -1 lot, Т 5S -диокси-6(ЬН-6(9оО-оксид-прост-13-еновой кислоты в 6 мл метанола подвергают взаимодействию с 0,5 н.водным .раствором литийгидрата (2 мл). Спустя 6 ч метанол отгоняют в вакууме. Остаток разбавляют водой (2 мл) и экстрагируют этиловым эфиром для удаления нейтральных примесей. Щелочную водную фазу подкисляют, обрабатывая k мл 30«-ного водного , и несколько раз экстрагируют этиловым эфиром. Потом соединяют эфирные экст ракты и промывают водой (2 х 1 мл) и высушивают; после удаления растворителя получают 91 мг 13t-11oC,15S-диокси-6рН-6(9оО-оксид-прост-13-еновой кислоты, т. пл. 78-80С, otjQ +31 (EtOH). Эту процедуру испопьзуют для омыления сложных эфиров из предыдущих примеров до соответствующих свободных кислот. П р им е р 82. 11о,155-диокси-6рН-6(9оО-оксид-1б5-метил-прост-13-иновую кислоту (0,11 г/ э метиленхлориде обрабатывают 1,5-молярными эквивалентами диазометана в метил;. хлориде. Спустя 15 мин растворитель отгоняют в вакууме, а остаток абсор бируют на силикагеле. После элюирования смесью этиловый эфир:бензол в соотношении 70:80 получают 12 мг сложного метилового эфира Пс -окси-155-метокси-6/ЬН-6 (9оО -оксид- 16S-метил-прост-13-иновой кислоты, otjjj (EtOH), и 78 мг сложного метилового эфира 1 lot, 155-диокси-6|5Н-6 (9оО -оксид-1б5-метил-прост 13-иновой кислоты, C«i3 D +21 ,5 (EtOH). Используя-по
71978725
этой методике вместо диазометана диазоэтан, получают сложный этиловый эфир По(гокси-155-этокси-60Н-6{9о)-оксид-16$-метил-прост-13 иновой кислоты, CO-JD .О fEtOH), S
l (dHz)p-R
оГв .№Ч
-Y-C-CCH,),;
R - свободная или этирифицированная карбоксильная группа;
Z водород или галоген;
0или целое число от 1 до 7; Р
1или 2;
q
Н
-6it-ciHz-; -(i«cJr- d e где Z2 - водород или галоид; одна из групп R и R - водород, алкил, С2-С -алкенил, С -С -алкинил или арил, или другая - окси-, С -С -алкокси-, ,-аякоксигруп па, или R и Rj вместе образуют оксо группу; каждая из групп RgH R, которые являются одинаковыми или различными, может быть водородом, С -С -алкилом или фтором; каждое из п и п, которые одинаковы или различны, равно О или является целым числом от t до 6; X - выбран из группы, состоящей из-0--, -S- и (2)п где m равно О или 1; Rf - выбран из группы, состоящей из (а) водорода, (Ь) С -С -алкила, (с) Сд-Сд-циклоалифатичёского радика ла, незамещенного или замещенного одним или более заместителями, выбран ными из группы, состоящей ,из С,-СА-алкила и С -С -алкоксигруппы, (d) арила, незамещенного или замещенного одним или более заместителями, выбранными из группы, состоящей из галоида, галоид-С -С -алкила, C-j-C -алкила или С -С -алкоксигруппы, и (е) тетрагидрофурила, тетрагидропиранила, пирролила, пиразолила оксазолила, изоксазолила, пиридила, пирази72 изобретения
Формула
Способ получения
бицикличесобщей форких простагландинов мулы 1
()n-R,
- водород, ОКСИ-, с,,-С -алкокСИ-, ар-С -С -алкокси-,ацилоксигруппа;
- радикал выбираемый из следующей группы;
н
2|(«л)
с-С
Zffrpene) нила, пиридазинила, пиримидинила, незамещенных или замещенных одним или более заместителями, выбранными из группы, состоящей из галоида, гало- алкила и Ц-С -алкоксигруппы;или их солей, отличающийс я тем, что соединения формулы (М) ) И R имеют значения, указанные ранее, подвергают взаимодействию с соединением формулы (ill) Т (оЧЙС,)й,С-Х-((Н,)„-В. где Е -- группа () pt+ - или группа (), где каждый из Rtj


































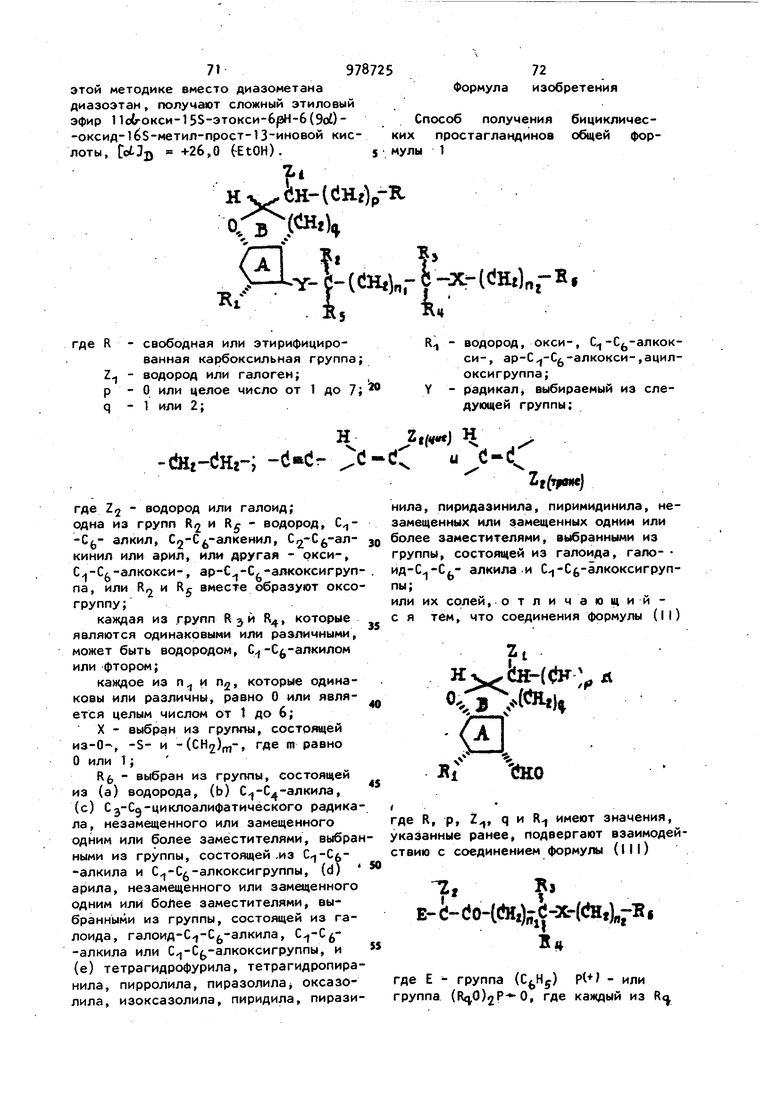



Авторы
Даты
1982-11-30—Публикация
1977-12-30—Подача