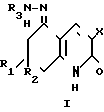
Изобретение относится к области химии соединений хинолинового ряда и касается неописанных ранее биологически активных химических соединений арилгидразонов 5, 6, 7, 8-тетрагидрохинолиндиона-2, 5 общей формулы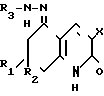 (1) где, если Х есть CN-группа,
(1) где, если Х есть CN-группа,
то R1 = R2 = CH3, R3 = C6H5 (Iа);
R1 = R2 = H, R3 = C6H5 (Iб);
R1 = R2 = H, R3 = C6F5 (Iв);
R1 = H, R2 = R3 = C6H5 (Iг);
если Х есть CONH2-группа
то R1 = R2 = CH3, R3 = C6H5 (Iд);
R1 = R2 = H, R3 = C6H5 (Iе).
Соединения общей формулы I обнаружили кардиотоническую активность.
Ближайшими структурными аналогами заявляемых соединений являются производные 5, 6, 7, 8-тетрагидрохинолиндиона-2,5 нижеследующей формулы 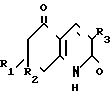 , но о биологической активности этих соединений сведения в литературе отсутствуют.
, но о биологической активности этих соединений сведения в литературе отсутствуют.
В ряду производных тетрагидрохинолинона в настоящее время неизвестны соединения, обладающие кардиотонической активностью.
В настоящее время в ряду кардиотоников, имеющих в основе своей химической структуры замещенный пиридиновый-2 цикл, который обуславливает наличие каридиотонических свойств, известно два препарата - амринон, милринон [3- 4- 5] . Они применяются в клинической практике. Наиболее эффективный из них является милринон - 3-цианат-5-(пиридинил-4)-6-метилпиридон-2 формулы А,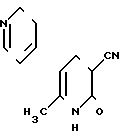 (А) который выбран авторами в качестве фармакологического аналога заявляемых соединений. Милринон применяют для лечения хронической сердечной недостаточности.
(А) который выбран авторами в качестве фармакологического аналога заявляемых соединений. Милринон применяют для лечения хронической сердечной недостаточности.
Однако следует отметить его сравнительно невысокую кардиотоническую активность.
Цель изобретения - новые производные тетрагидрохинолинового ряда, содержащие замещенный пиридиновый 2-цикл.
Поставленная цель достигается химической структурой новых арилгидразонов 5, 6, 7, 8-тетрагидрохинолиндиона-2,5 общей формулы I.
Заявляемые соединения представляют собой кристаллические вещества желтого цвета, трудно растворимые в воде, спиртах, растворимые при нагревании в диметилсульфоксиде и диметилформамиде и не растворимые в неполярных растворителях.
Способ получения соединений общей формулы I основан на известной реакции конденсации арилгидразинов с карбонильными соединениями [7] .
Заявляемые соединения I получают путем взаимодействия производных 5, 6, 7, 8-тетрагидрохинолиндиона-2,5 общей формулы II, где R1, R2 и Х имеют вышеуказанные значения, с арилгидразинами общей формулы III, где R3 имеет вышеуказанные значения, в среде ледяной уксусной кислоты в температурном интервале от 30оС до температуры кипения реакционной массы, согласно схеме: 
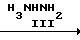
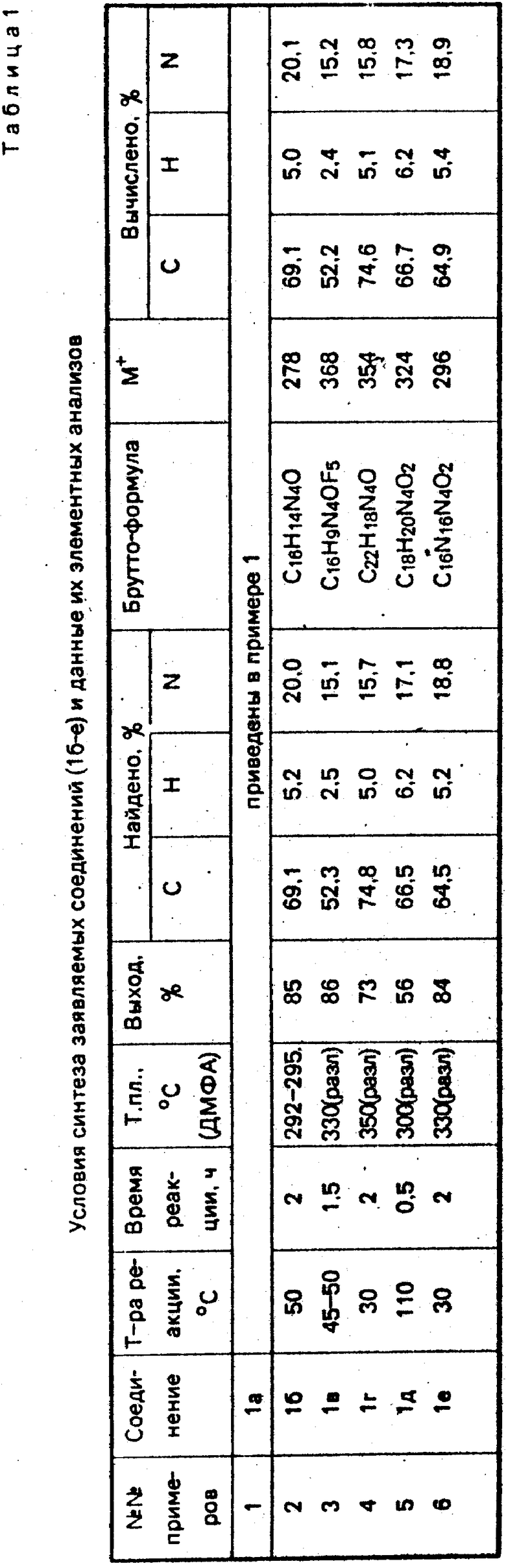
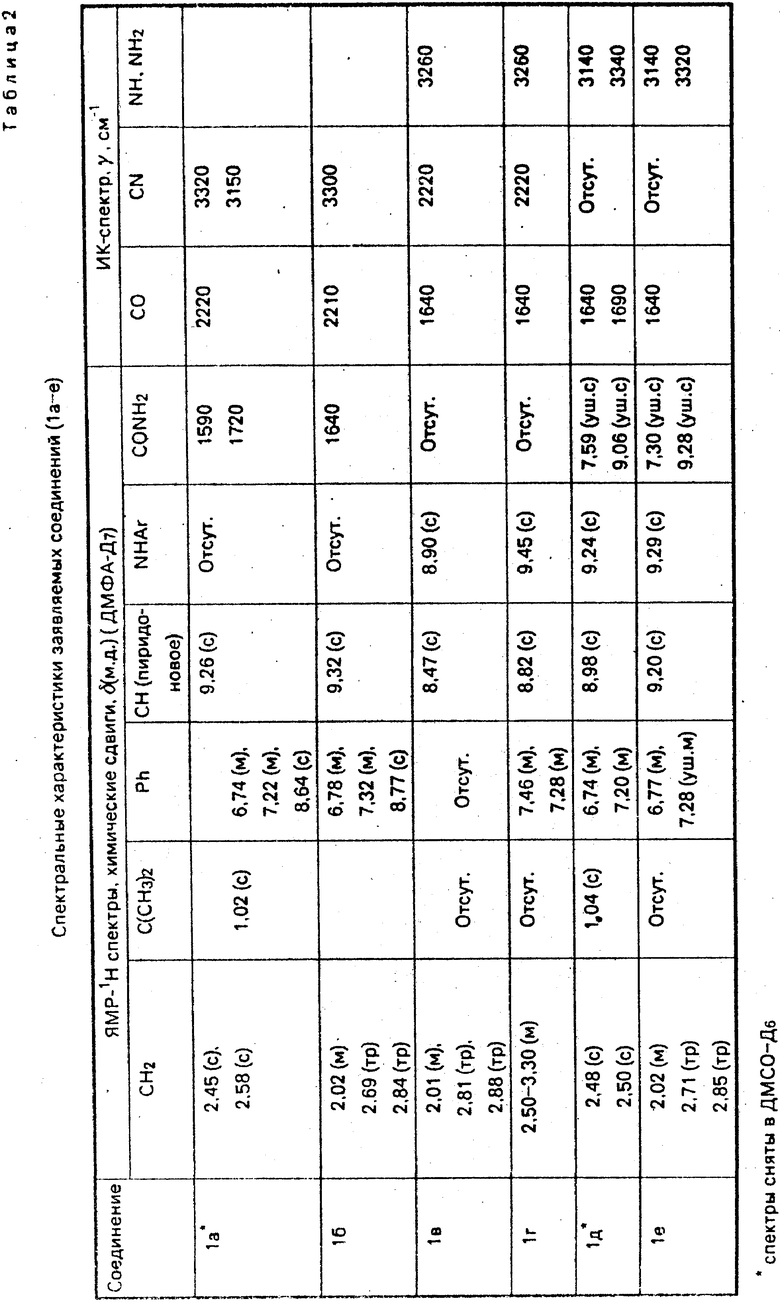
Структура заявляемых соединений подтверждена элементным анализом и спектральными данными (см. табл. 1 и 2).
Исходные соединения и способ их получения описаны в литературе [1, 2] .
Нижеследующие примеры иллюстрируют получение заявляемых соединений.
П р и м е р 1. Получение 5-фенилгидразона 3-циано-7, 7-диметил-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 (Iа).
К суспензии 2,16 г (0,01 моль) 3-циано-7, 7-диметил-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 в 14 мл ледяной уксусной кислоты постепенно прибавляют 2,16 г (0,02 моль) фенилгидразина. Смесь перемешивают 30 мин при кипении реакционной массы, охлаждают. Выпавший осадок отфильтровывают, промывают водой до нейтральной реакции, сушат на воздухе.
Получают 1,59 г (52 % ) 5 -фенилгидразона 3-циано-7, 7-диметил-5, 6, 7, 8-тетрагидрохинолиндиона-2,5, т. пл. > 300о (разл) (ДМФА), М+ 306.
Найдено, % : C 70,7; H 6,0; N 18,0.
C18H18N4O.
Вычислено, % : C 70,6; H 5,9; N 18,3.
Исходя из соответствующих исходных соединений II и III, в условиях, аналогичных примеру 1 получают:
5-фенилгидразон 3-циано-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 (Iб);
5-пентафторфенилгидразон 3-циано-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 (Iв);
5-фенилгидразон 3-циано-7-фенил-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 (Iг);
5-фенилгидразона 3-карбамидо-7, 7-диметил-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 (Iд);
5-фенилгидразон 3-карбамидо-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 (Iе).
Физические константы, условия реакции, выходы и аналитические характеристики заявляемых соединений (Iб-е) приведены в табл. 1, а спектральные данные в табл. 2.
Биологическая часть.
Исследование кардиотонической активности предлагаемых соединений проводились на следующих объектах:
на изолированных спонтанно сокращающихся правых предсердиях морских свинок [8] ;
на бодрствующих крысах по влиянию на модифицированный индекс Верагута по известным методикам [9] .
Соединения общей формулы I изучались в сравнении с близким по биологическому действию препаратом милриноном (А).
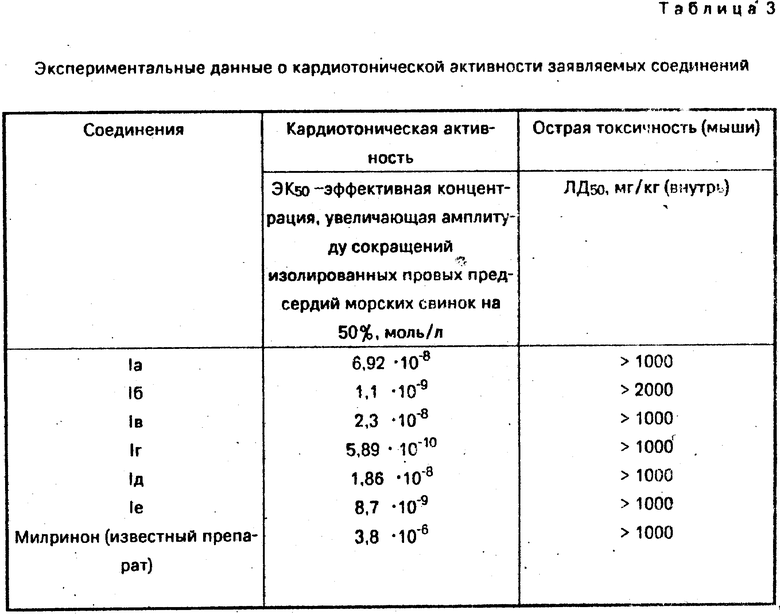
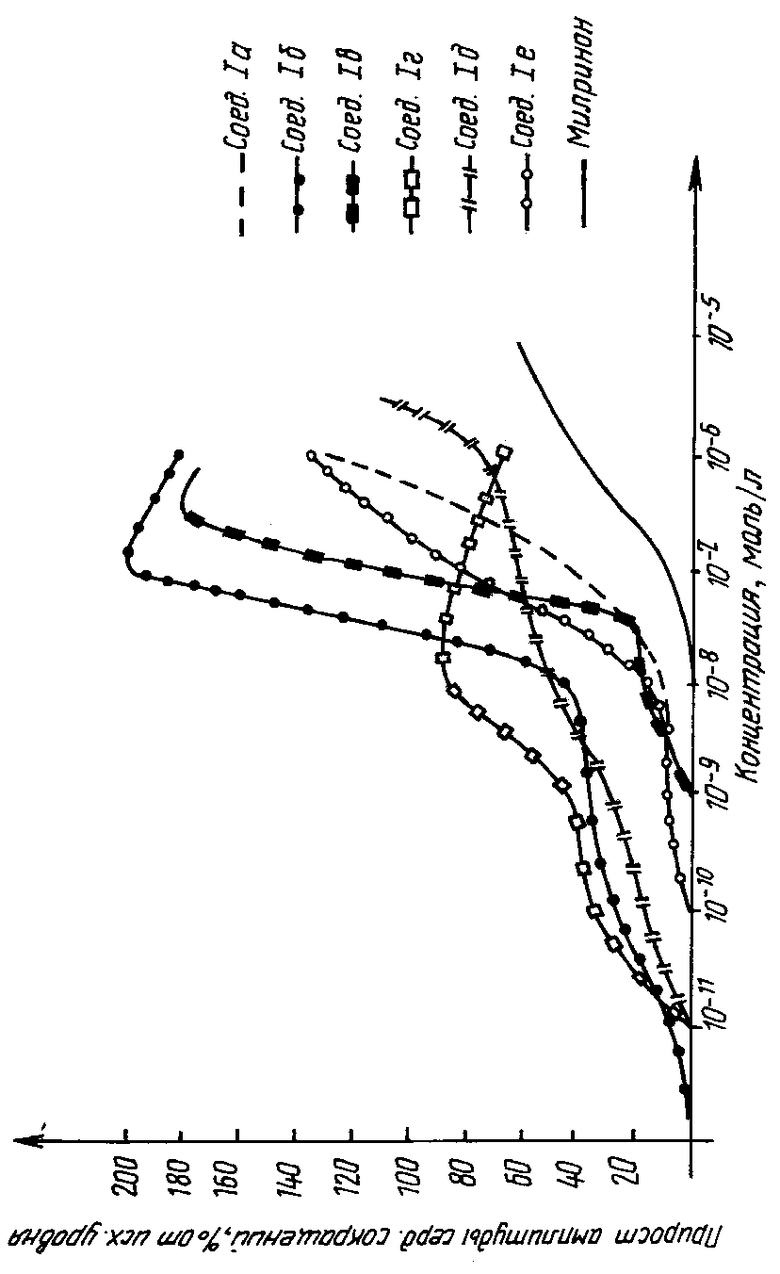
Результаты исследования представлены на фиг. 1 и в табл. 3.
Как видно из табл. 3, по положительной инотропной активности (показатель ЭК50) на изолированных правых предсердиях морских свинок все заявляемые соединения значительно превосходят известный препарат милрион.
Наиболее активным из них оказалось соединение 1 г (ЭК50 - 5,89 ˙ 10-10 моль). По данным острой токсичности все соединения относятся к группе малотоксичных веществ [10] (ЛД50 1000 мг/кг внутрь), при этом одно из них -Iб имеет ЛД50 200 мг/кг, это позволяет предположить, что данное соединение обладает большей широтой терапевтического действия по сравнению с другими заявляемыми соединениями. Кроме того, данные экспериментов показали, что соединение Iб вызывает наибольший прирост амплитуды сердечных сокращений по сравнению с милриноном и остальными заявляемыми соединениями (фиг. 1).
С учетом полученных вышеуказанных данных исследования соединение Iб выбрано для более глубокого изучения, которое было проведено на левых предсердиях морских свинок с навязанным ритмом и в условиях целого организма - бодрствующих нормальных крысах и крысах с кобальтовой кардиомиопатией.
Результаты исследований на левых предсердиях с навязанным ритмом показали, что и при данной остановке опыта (с более жесткими условиями) соединение Iб проявляло на порядок большую активность, чем милрион (ЭК50 Iб - 1,64 ˙ 10-8 моль, ЭК50 милриона - 1,4 ˙ 10-7моль).
Исследование кардиотропной активности соединения Iб на бодрствующих крысах.
Объект и методы исследования.
Работа проведена на бодрствующих нормальных крысах и крысах с кобальтовой кардиомиопатией. Кобальтовую кардиомиопатию вызывали путем поения крыс раствором сульфата кобальта (1 мг/мл) в течение 3 мес.
Животным предварительно вживляли катетеры в левый желудочек, аорту и яремную вену. Левожелудочковое (ЛЖД) и аортальное давление (АД) регистрировали с помощью электроманометров. Кривые ЛЖД и АД анализировали с помощью программы для обработки физиологических сигналов в реальном времени BEAT на микрокомпьютере Zabtam 3015. Для оценки кардиотропной активности испытываемых соединений использовался модифицированный индекс Верагута.
Соединение Iб вводилось внутривенно в дозах от 5 мг до 50 мкг на 1 кг массы. Препарат сравнения милринон (Sterling-Wintrop, США) вводилися в дозах от 3 до 1000 мкг/кг.
Результаты исследования
У контрольных крыс пороговая доза кардиостимуляторного эффекта для милринона составила 8 мкг/кг, максимальный эффект выявлялся в дозе 300 мкг/кг. ЕД50 для индекса сократимости (dp/dt/Pd) 37,3 ± 4,3 мкг/кг.
Соединение I, вызывало дозозависимое кардиостимуляторное и гипотензивное действие: пороговая доза кардиостимуляторного действия составила в среднем 15 ± 4 нг/кг, максимальное повышение индекса сократимости левого желудочка (dp/dt/Pd) выявлялось в дозе 3 ± 0,5 мкг/кг; введение больших доз препарата вызывало увеличение продолжительности эффекта.
ЕД50 для индекса сократимости (p/dt/Pd) 196 ± 8,3 нг/кг, что, примерно, в 200 раз меньше, чем милринона (Р < 0,001).
У крыс с кобальтовой кардиомиопатией различия в кардиотропной активности двух соединений увеличились.
Таким образом, заявляемые соединения - соединения впервые найденные в хинолиновом ряду, а именно 5-арилгидразоны 3, 7-замещенных-5, 6, 7, 8-тетрагидрохинолиндиона-2,5 общей формулы 1, обладают кардиотонической активностью, причем более высокой, чем известный препарат кардиотонического действия милрион.
Представленные данные свидетельствуют о том, что соединения общей формулы I представляют интерес в плане поиска потенциальных высокоэффективных сердечно-сосудистых лекарственных препаратов в вышеуказанном ряду соединений. (56) 1. Мosti L. , Schenone P. , Menozzi G. - Reaction of 2-Dimehylaminomethylene-1,3-diones with Dinucleophyles. V. Synthesis of 5-Acyl-1, 2-dihydro-2-oxo-3-pyridinocarbonitriles and 1, 2, 5, 6, 7, 8-Hexahydro-2,5-dioxo-3-qyinolinecarboxamides - J. Heter. Chem. , 1985, 22 (6), 1503-1509.
2. Junek H. , Wolfbeis O. S. , Sprintschnik H. , Wolny H. - Synthesen von Alkyl-bzw. Cycloalkylpyridinen und Naphthyridinen. Beitrage zyr Chemie der Enaminoketone, 13 mitt - Monatsh Chem. , 1977, 108 (3), 689-702.
3. Пат. 4004012, 1977, США / Chem. Abstr. 1977, v. 86, N 189725 e.
4. Пат. 4276293, 1981 США / Chem Abstr. 1981, v 95, N. 2039482 z.
5. Пат. 4305948, 1982 США / Сhem. Abstr. 1982, v. 96 N 122642 p.
6. Jonnd R. A. , Ward A. - Milrinone A preliminary review of its pharmacologycal properties and therapeutic yse-Drugs, 1988, 36, 158-192.
7. Китаев Ю. П. , Бузыкин Б. Н. - Гидразоны, Москва, "наука", 1974.
8. San Feliciano A. , Medarde M. , Caballero E. et al. - Synthesis and Evaluation of Cardiotonic Activity of Simple Butenolides. - Eur. J. Med. Chem. , 1990, 25, 413-417.
9. Medvedev O. S. , Proshkin S. D. , Savchenko A. V. et. al. - BEAT - a system for multicannel processing of physiological signals in real time - Proceeding of the ISMM International Symposium: Mini and Microcomputers and their application, Lugano, Switzerland, June, 19-21, 1990, 29-31.
10. Саноцкий И. В. - Методы определения токсичности и опасности химических веществ, М. : Медицина, 1970.
Использование: в качестве препарата, обладающего кардиотонической активностью. Сущность изобретения: соединение ф-лы 1, где, если X-CN-группа, то R1=R2=CH3, R3=C6H5 (1а); R1=R2=H, R3=C6H5 (1б); R1=R2=H, R3=C6H5 (1в); R1=H, R2=R3=C6H5 (1г), если X-CONH2-группа, то R1=R2=CH3, R3=C6H5 (1д). R1=R2=H, R3=C6H5 (1с). 1 табл.
Арилгидразоны 5,6,7,8-тетрагидрохинолиндионы-2,5 общей формулы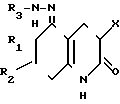
где X - CN - группа;
R1 и R2-CH3, R3-C6H5;
R1 и R2-H, R3-C6H5;
R1 и R2-H, R3-C6F5;
R1-H, R2 и R3-C6H5
если X - CONH2 - группа,
то R1 и R2 - CH3, R3-C6H5,
R1 и R2-H, R3-C6H5,
обладающие кардиотонической активностью.
Авторы
Даты
1994-03-15—Публикация
1991-12-16—Подача