Изобретение относится к способам получения низкоатомных линейных спиртов из синтез-газа при давлениях не выше 100 атм в присутствии катализатора.
Получение смеси спиртов С1-С6 из синтез-газа в настоящее время является актуальной задачей, так как позволяет решить проблему экологически чистого и высокооктанового автомобильного топлива за счет использования альтернативных источников сырья путем добавок спиртов (до 10 об.) к бензинам.
Основным требованием к таким смесям является малое содержание воды (не более 0,2 мас.), так как незначительное увеличение воды приводит к расслоению спиртово-бензиновых смесей и, соответственно, неприменимости их в качестве моторного топлива.
Известны [1, 2] способы получения спиртов по синтезу Фишера-Тропша с получением наряду со спиртами углеводородов, что приводит к образованию конденсата, содержащего более 30 мас. воды. В этом случае требуется удаление воды из смеси спиртов, что приводит к существенному удорожанию процесса.
Значительно меньшее количество воды образуется в процессах синтеза спиртов, протекающих на катализаторах синтеза метанола, модифицированных щелочными добавками. Прежде всего это процессы проводимые на модифицированном ZnO-Cr2O3-К2О катализаторе при высоких давлениях (до 200 атм) и повышенных температурах (350-390оС). Основными продуктами являются метанол и изобутанол, в то время как этанол и пропанол образуются в незначительных количествах. Содержание воды в конденсате составляет 8-25 мас. в зависимости от температуры процесса [3]
Кроме того, для синтеза смеси метанола с высшими спиртами предложены CuO-ZnO-M2O3 (M=Al, Cr или Ga) катализаторы с щелочными добавками. Процесс на них осуществляется при более низких температурах и давлениях (270-310оС, 50-80 атм). Содержание воды в конденсате составляет 3,0 мас. селективность по спиртам 76-84% количество спиртов С2+-ОН равно 22-36% Катализатор состава Cu/Zn/Cr (Al или Ga)=30/45/25 мол. получают путем терморазложения гидроксокарбоната меди-цинка-хрома, структура которого идентична структуре природного минерала гидроталькита с формулой Mg6Al2(OH)16CO3x4H2O. Гидроксокарбонат меди-цинка-хрома получали совместным осаждением из растворов азотнокислых солей соответствующих металлов карбонатом натрия [4] (прототип). Основным недостатком данного процесса является присутствие воды в конденсате в значительном количестве (до 3 мас.), что не позволяет напрямую использовать спирты в качестве высокооктановой добавки к бензинам.
Задача, решаемая изобретением получение из синтез-газа смеси спиртов С1-С6 с содержанием воды в смеси не более 0,2 мас.
Предлагаемый способ синтеза спиртов заключается в следующем: Синтез-газ, содержащий 50-65 об. СО, 30-50 об. Н2 и 10 об. N2, проходит через слой катализатора при температуре 250-320оС и давлении 50-80 атм. Образующиеся продукты реакции охлаждаются и разделяются на газообразные и жидкие. Конденсат, состоящий из смеси спиртов, является целевым продуктом, а газовая смесь, содержащая непрореагировавший СО, СО2 и некоторое количество углеводородов, проходит через аппарат удаления СО2 и направляется на смешивание с исходным газовым потоком, т.е. осуществляется рециркуляция газа. Оксидный катализатор содержит ионы меди, цинка, хрома или алюминия и щелочные добавки, количество компонентов в пересчете на металлы составляет медь 20-40 ат. цинк 45-75 ат. хром или алюминий 5-15 ат. количество щелочных добавок в виде калия, натрия или цезия составляет 0,1-5,0 ат.
Предлагаемый способ синтеза отличается тем, что катализатор для процесса синтеза спиртов, приведенного выше состава, получают путем терморазложения гидроксокарбоната меди-цинка-хрома (или алюминия) со структурой типа гидроцинкита [5] с формулой Zn5-x-yCuxCry(OH)6(CO3)2. Терморазложение осуществляют в токе воздуха при 300-400оС. Для получения гидроксокарбоната меди-цинка-хрома (или алюминия) с заданной структурой необходимо на стадии осаждения обеспечить химическое взаимодействие компонентов, что достигается совместным осаждением растворов нитратов металлов (Cu, Zn, Cr или Al), смешанных в заданном соотношении, карбонатом натрия в условиях постоянных рН 6,5-7,5 и температуры 60-75оС с последующей отмывкой от ионов натрия до содержания не более 0,01% Введение щелочного компонента в катализатор осуществляют пропиткой высушенного на воздухе образца раствором карбоната щелочного иона в заданном количестве. Затем катализатор сушат на воздухе при 100оС и прокаливают в указанном выше режиме.
П р и м е р 1. Процесс синтеза спиртов осущетвляется путем взаимодействия оксида углерода с водородом в соотношении 2:1 при температуре 270оС и давлении 75 атм. конверсия СО=30% объемная скорость подачи газа 3000-5000 ч-1.
Процесс проводят на оксидном катализаторе, содержащем ионы меди, цинка, хрома и цезия в ат. Сs/Сu/Cr/Zn=1/40/15/45, полученном терморазложением в токе воздуха при температуре 350оС гидроксокарбоната меди-цинка-хрома со структурой типа гидроцинкита.
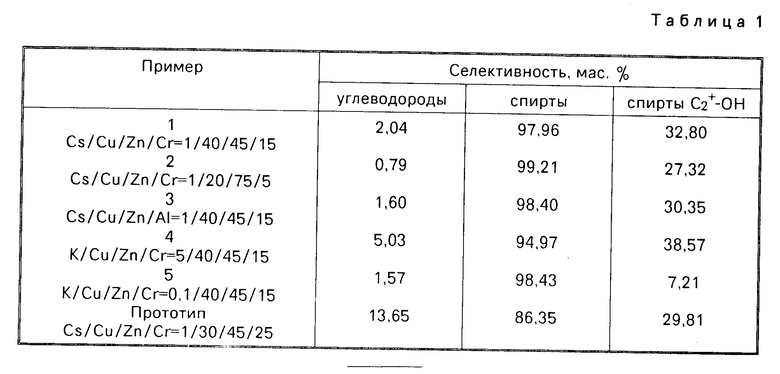
Активность и селективность процесса синтеза спиртов С1-С6 приведена в табл. 1 и 2.
Анализируя свойства катализаторов, приведенных в табл. 1 и 2, можно отметить, что увеличение щелочной добавки до 5% снижает производительность по спиртам, однако содержание воды в конденсате практически не зависит от содержания щелочного иона.
Получение гидроксокарбоната с заданной структурой обеспечивается условиями синтеза и соотношением компонентов. Гидроксокарбонат меди-цинка-хрома образован при совместном осаждении ионов металлов из растворов их нитратов раcтвором карбонатa натрия при рН, равном 6,9, и температуре 75оС. Идентификация структуры полученного гидроксокарбоната меди-цинка-хрома, проведенная методом рентгенофазового анализа, показала, что структура полученного соединения полностью идентична структуре гидроцинкита [5] После чего образец был пропитан раствором карбоната цезия, высушен и прокален как указано выше.
Селективность и производительность процесса, а также содержание воды в конденсате приведены в табл. 1, 2.
П р и м е р 2. Аналогично примеру 1, но соотношение элементов составляет Cs/Cu/Zn/Cr= 1/20/75/5, гидроксокарбонат меди-цинка-хрома со структурой типа гидроцинкита получен осаждением при рН 6,5, температуре 60оС, терморазложение проводили при 300оС.
П р и м е р 3. Аналогично примеру 1, но вместо хрома используется алюминий, гидрокcoкарбонат меди-цинка-хрома со структурой типа гидроцинкита получен осаждением при рН=7,5, температуре 70оС, терморазложение проводили при 400оС.
П р и м е р 4. Аналогично примеру 1, но вместо цезия используется калий в количестве 5 мас. в пересчете на металл.
П р и м е р 5. Аналогично примеру 4, но количество калия составляет 0,1%
Как видно, что все катализаторы, полученные терморазложением гидроксокарбоаната меди-цинка-хрома (или алюминия) со структурой типа гидроцинкита, обепечивают синтез спиртов с содержанием воды в конденсатe значительно меньшем, чем катализатор, полученный терморазложением гидроксокарбоната меди-цинка-хрома со структурой типа гидроталькита (прототип).
Таким образом, предлагаемый способ синтеза смеси спиртов С1-С6 обеспечивает получение конденсата, содержание воды в котором не превышает 0,2% что позволяет напрямую использовать полученные спирты в качестве высокооктановой добавки к бензинам, тем самым сделать процесс синтеза спиртов экономически выгодным, так как не требуется дополнительная стадия разгонки.
Применение спиртов в составе моторных топлив позволит: уменьшить на 10-15% расход бензина, отказаться от использования канцерогенного антидетонатора тетраэтилсвинца, в несколько раз снизить содержание СО, углеводородов и оксидов азота в выхлопных газах автомобилей.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ НИЗКОТЕМПЕРАТУРНОГО СИНТЕЗА МЕТАНОЛА | 1997 |
|
RU2161536C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПРОЦЕССА КОНВЕРСИИ ОКСИДА УГЛЕРОДА ВОДЯНЫМ ПАРОМ | 1993 |
|
RU2046656C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛФОРМИАТА, КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА | 2000 |
|
RU2185370C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА КОНВЕРСИИ ОКСИДА УГЛЕРОДА ВОДЯНЫМ ПАРОМ | 1997 |
|
RU2118910C1 |
| КАТАЛИЗАТОР И СПОСОБ СЕЛЕКТИВНОГО ГИДРИРОВАНИЯ АЦЕТИЛЕНОВЫХ УГЛЕВОДОРОДОВ | 2000 |
|
RU2180611C1 |
| КАТАЛИЗАТОР И СПОСОБ ПАРОВОЙ КОНВЕРСИИ МОНООКСИДА УГЛЕРОДА | 2005 |
|
RU2281805C1 |
| СПОСОБ ФАЗОВОГО АНАЛИЗА ТВЕРДЫХ ВЕЩЕСТВ | 1990 |
|
RU2056635C1 |
| КАТАЛИЗАТОР ОКИСЛЕНИЯ НА ОСНОВЕ ОКСИДА СО СТРУКТУРОЙ ПЕРОВСКИТА И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1993 |
|
RU2065325C1 |
| КАТАЛИЗАТОР ОКИСЛЕНИЯ ОКСИДА УГЛЕРОДА И УГЛЕВОДОРОДОВ (ВАРИАНТЫ) | 1996 |
|
RU2100067C1 |
| КАТАЛИЗАТОР ОКИСЛЕНИЯ АММИАКА | 1996 |
|
RU2100068C1 |

Использование: в производстве автомобильного топлива. Сущность изобретения: продукт C1-C6-спирты, содержащие воды не более 0,2 мас. Реагент 1: окись углерода. Реагент 2: водород. Условия реакции: температура 270 310°С, давление 50 80 атм в присутствии катализатора, полученного терморазложением гидроксосоединения со структурой типа гидроцинкита, в котором содержание элементов в пересчете на металлы составляет меди 20 40 ат. хрома или алюминия 5 15 ат. цинка 45 75 ат. цезия, калия или натрия 0,1 5,0 ат. 2 табл.
СПОСОБ ПОЛУЧЕНИЯ СМЕСИ СПИРТОВ C1-C6 путем взаимодействия оксида углерода с водородом при температуре 270 310oС, давлении 50 80 атм в присутствии катализатора, содержащего одновременно медь, цинк, хром (или алюминий) и один из щелочных элементов, отличающийся тем, что используют катализатор, полученный терморазложением гидроксосоединения со структурой типа гидроцинкита, в котором содержание элементов в пересчете на металлы составляет, ат.
Медь 20 40
Хром или алюминий 5 15
Цинк 45 75
Цезий, калий или натрий 0,1 5,0
| Chose S | |||
| Acta Cryst., 17, 1051, 1964. |
Авторы
Даты
1995-08-09—Публикация
1992-07-22—Подача