Изобретение относится к области биотрансформации, в частности к новому способу получения оптически активного S-(+)-2,2-диметилциклопропанкарбоксамида, причем в рацемическом R,S-(±-2,2-диметилциклопропанкарбоксамиде R-(-)-2,2-диметилциклопропанкарбоксамид биотрансформируется в R-(-)-2,2-диметилциклопропанкарбоновую кислоту, и при этом выделяется желательный S-(+)-2,2-диметилциклопропанкарбоксамид.
В последующем 2,2-диметилциклопропанкарбоксамид сокращенно обозначается как 2,2-ДМЦПКА, а 2,2-диметилциклопропанкарбоновая кислота как 2,2-ДМЦПКК.
Оптически чистый S-(+)-2,2-ДМЦПКА служит в качестве исходного материала для получения ингибитора дегидропептидазы циластатина, который в терапии используется вместе с антибиотиками по-немногу, соответственно карбопенемного типа, чтобы препятствовать дезактивации антибиотиков в почках благодаря ренальной дегидропептидазе (см. европейский патент 048301).
До сих пор известны только химические способы получения S-(+)-2,2-ДМЦПКА. Эти способы имеют тот недостаток, что они дорогостоящие и протекают через несколько стадий (европейский патент 155779).
Задача настоящего изобретения состояла в том, чтобы разработать биотехнологический способ, с помощью которого, исходя из легко получающегося рацемического R, S-(±)-2,2-ДМЦПКА, в одну стадию можно получать желательный изомер высокой чистоты.
Эта задача решается с помощью нового способа и с помощью новых штаммов бактерий.
Предлагаемые согласно изобретению бактерии способны в рацемическом R, S-(±)-2,2-ДМЦПКА биотрансформировать R-(-)-2,2-ДМЦПКА в R-(-)-2,2-ДМЦПКК, причем выделяется оптически активный S-(+)-2,2-ДМЦПКА.
Эти бактерии можно выделять, например, из почвенных проб, ила или сточных вод при помощи традиционных микробиологических способов.
Для получения S-(+)-2,2-ДМЦПКА можно применять все бактерии, которые используют в качестве субстрата R-(-)-ДМЦПКА.
Их получают по следующему селекционному методу:
а) бактерии, которые используют в качестве N-источника 2,2-ДМЦПКА, в виде рацемата или его оптических изомеров и в присутствии C-источника, выращивают обычным образом;
б) из выращенных культур затем отбирают те, которые стабильны и используют 2,2-ДМЦПКА в виде рацемата или его оптических изомеров в качестве единственного источника азота.
Целесообразно проводить селекцию бактерий, которые акцептируют R-(-)-2,2-ДМЦПКА в качестве N-источника.
В качестве C-источника бактерии могут использовать, например, сахар, сахароспирты, карбоновые кислоты или спирты. Из сахаров можно использовать, например, фруктозу или глюкозу. Из сахароспиртов эритрит, маннит или сорбит. В качестве карбоновых кислот можно применять моно-, ди- или трикарбоновые кислоты, как, например, уксусная кислота, малоновая кислота или лимонная кислота. В качестве спиртов одно-двух- или трехатомные спирты, как, например, этанол, гликоли или глицерин. Предпочтительно в качестве C-источника используется трехатомный спирт глицерин.
Целесообразно, чтобы C/N соотношение в селекционной среде находилось в области 5:1 10:1.
В качестве селекционной среды можно использовать известные в мире специалистов среды для отбора, например среда с минеральными солями, описанная у Kulla et al. Arch. Microbiol. 135, 1 7, 1983.
Предпочтительными бактериями, которые растут с помощью рацемата 2,2-ДМЦПКА или его оптических изомеров, в качестве N-источника и в присутствии C-источника, являются:
Comamonas acidovorans A: 18 (DSM N 6315), Comamonas acidovorans TG 308 (DSM N 6552), Pseudomonas sp. NSAK:42 (DSM N 6433) и бактерии Bacterium sp. VIII: II (DSM N 6316) (Corynebacterium aquaticum), а также их потомки и мутанты.
Штаммы DSM NN 6315 и 6316 с 29.1.1991, штамм DSM N 6433 с 25.3.1991 и штамм DSM N 6552 с 6.4.1991 хранятся в немецкой коллекции микроорганизмов и клеточных культур ГмбХ, Mascherodeweg 1B, D-330, Braunschweig.
Научное описание Comamonas acidovorans A:18 (DSM N 6315).
Бактерия Comamonas acidovorans A:18 (DSM N 6315) имеет типичные для бактерий рода Comamonas признаки, а именно является грам-отрицательной; морфологические признаки: форма клеток в виде палочек с полярными жгутиками, культуральные признаки: рост при 37oC, а также другие признаки: в качестве субстрата использует ацетат, адипат и капрат.
Табл. 1 10 поясняют изобретение.
API 20NE _→ Cs.acidovorans 99,0%
Научное описание Comamonas acidovorans TG 308 (DSM N 6552):
Бактерия Comamonas acidovorans TG 308 (DSM N 6552) имеет типичные для микроорганизмов рода Comamonas признаки, а именно является грам-отрицательной; морфологические признаки: форма клеток в виде палочек; культуральные признаки: оптимальный рост при температуре 37oC, а также другие признаки: способность к понижению нитрата и ассимиляции глюконата.
Научное описание Pseudomonas sp. NSAK:42 (DSM N 6433):
Бактерия Pseudomonas sp. NSAK (DSM N 6433) имеет типичные для микроорганизмов рода Pseudomonas признаки, является грам-отрицательной; морфологические признаки: форма клеток в виде палочек; культуральные признаки: оптимальный рост при температуре 37oC, а также другие признаки: в качестве субстрата использует гликолят, лактат или лавулинат.
Научное описание Bacterium sp. VIII:II (Corynebacterium aquaticum) (DSM N 6316):
Микроорганизм Bacterium sp. VIII:II (Corynebacterium aquaticum) (DSM N 6316) имеет типичные для микроорганизмов рода Corynebacterium признаки, а именно является грам-положительным; морфологиеские признаки: неравномерные палочки; а также другие признаки: неполярные липиды.
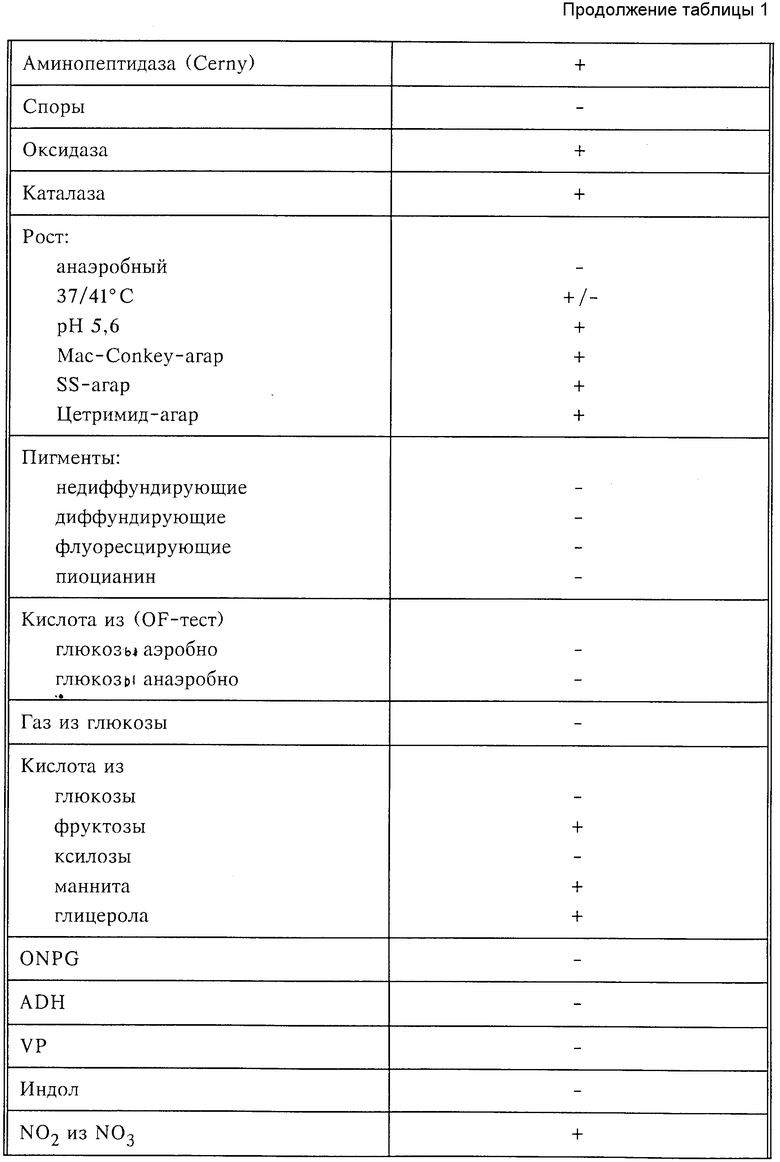
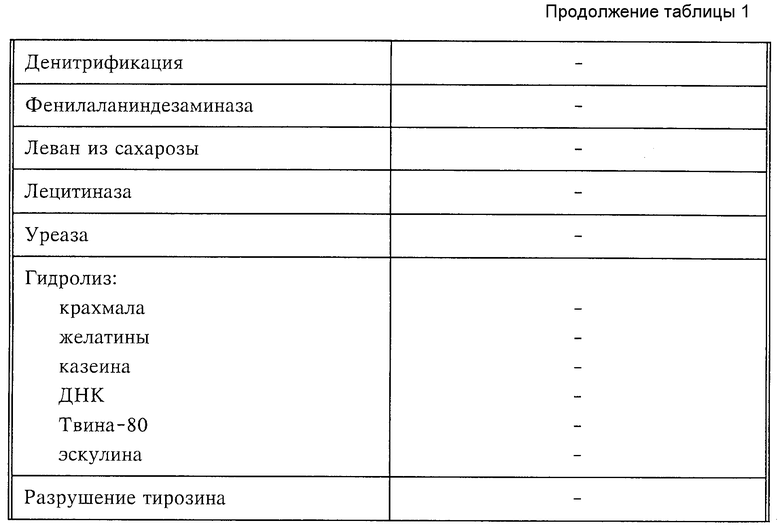
Дополнительные свойства штамма DSM 6316:
Характеристика: грам-положительные, неравномерные палочки, аэробный рост
Подвижность: +
Споры: -
Каталаза: +
Мезо-диаминопимелиновая кислота в стенке клеток: нет
Пептидогликан тип B2γ, [L-Dab] D-Glu-D-Dab
Полярные липиды: DPG, PG, G1, G2
Изопреноиды: МК-10 (28%), МК-11 (17%)
Основные компоненты в клеточных жирных кислотах: ai-15:0, ai-17:0, i-16: 0
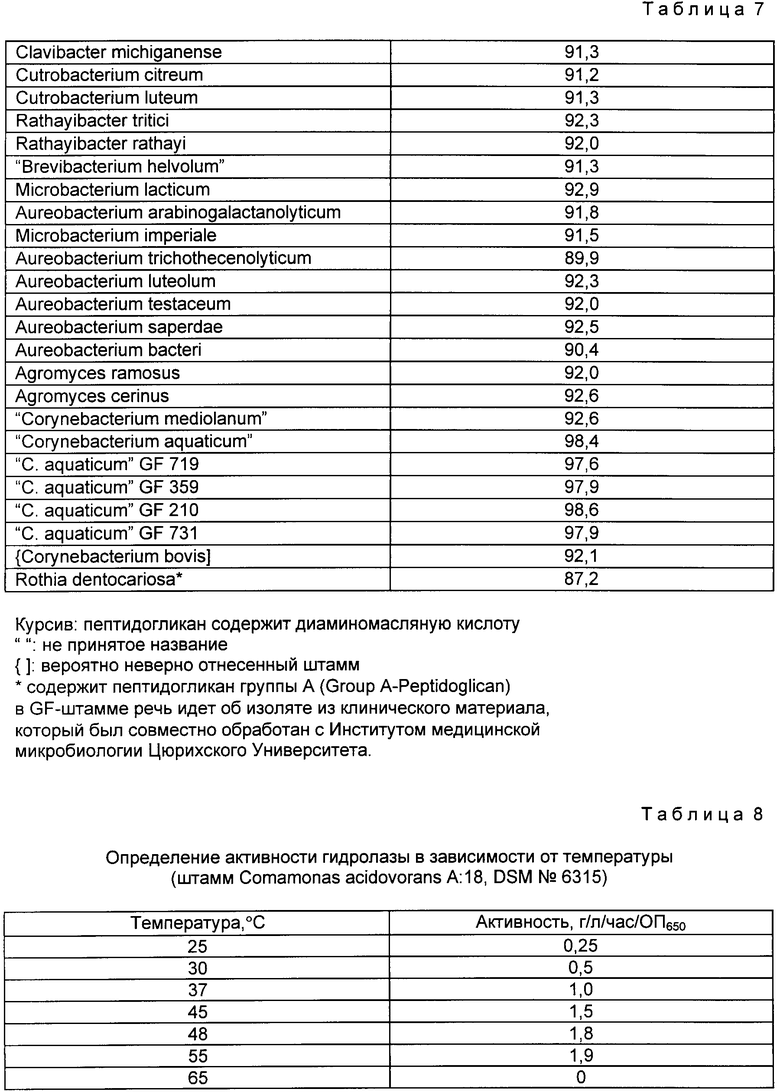
Примечание: было произведено выделение фрагментов 16S pDHK. Результаты представлены в приложенной таблице. Согласно результатам штамм VIII-II однозначно относится к виду Corynebacterium aquaticum. Однако скорее всего речь идет о новом виде, который должен быть описан.
Сходство последовательности pDHK штамма DSM 6316 с другими актиномицетами, имеющими пептидогликан группы B (Group B-Peptidoglycan) (табл. 7).
Предкультура
Обычно по способу селекции получают среду для культивирования этих бактерий, которую затем инфицируют культурами этих бактерий.
Эту предкультуру можно выращивать (культивировать) в тех же самых средах, с таким же C/N-соотношением и с такими же соединениями в качестве C-источника, как и в способе селекции.
Предпочтительно среда для культивирования имеет либо состав, указанный в табл. 9, либо состав, который указан в табл. 10, с или без содержания универсального пептона.
В качестве N-источника для предкультуры можно применять следующие N-источники; предпочтительно в качестве N-источника используется соль аммония, как, например, сульфат аммония.
Целесообразно, чтобы pH при культивировании составляло 4 10 при температуре 20 40oC.
После культивирования, как правило, в течение 10 100 ч бактерии индуцируются и подготавливаются для биотрансформации.
Индукция
Обычно с помощью полученной культуры инфицируется индукционная среда, которая вплоть до N-источника имеет такой же состав, как и среда для культивирования.
Целесообразно, чтобы среда для индукции содержала активные ферменты микроорганизмов 2,2-ДМЦПКА в виде рацемата или его оптических изомеров, которые могут служить как в качестве N-источника, так и в качестве индуктора ферментов.
Однако в качестве индукторов возможны также другие соединения, как, например, циклопропанкарбоксамид, капролактам, бензамид, циклогексан-карбоксамид, амид никотиновой кислоты или амид кротоновой кислоты. Индукцию осуществляют 0,05 0,15 мас. предпочтительно 0,1 0,15 мас. 2,2-ДМЦПКА в форме рацемата или его оптически активных изомеров. После обычной продолжительности индукции 15 18 ч бактерии можно выделять, например, путем центрифугирования или ультрафильтрации и затем снова суспендировать в среде, описанной в заявленном способе.
Биотрансформация
Собственно способ получения S-(+)-2,2-ДМЦПКА согласно изобретению осуществляется таким образом, что в рацемическом R,S-(±)-2,2-ДМЦПКА R-(-)-2,2-ДМЦПКА биотрансформируется в R-(-)-2,2-ДМЦПКК, причем выделяется оптически активный S-(+)-2,2-ДМЦПКА, и его изолируют.
Рацемический R,S-(±)-2,2-ДМЦПКА можно получать, например, химически или ферментативно из нитрила R,S-(±)-2,2-диметилциклопропанкарбоновой кислоты.
Целесообразно осуществлять биотрансформацию либо с помощью бактерий, либо с помощью ферментов в несодержащей клеток системе.
Ферменты для бесклеточной системы можно получать путем обычного разрушения клеток бактерий. Для этой цели можно применять, например, ультразвуковой, French-Press- или лизоцимный методы. Эти бесклеточные ферменты затем можно иммобилизовать на пригодном носителе.
Для способа особенно пригодны бактерии вида Comamonas acidovorans A:18 (DSM N 6315), Comamonas acidovorans TG 308 (DSM N 6552), Pseudomonas sp. NSAK:42 (DSM N 6433) и вида Bacterium sp. VIII:II (Corynebacterium aquaticum) (DSM N 6316), их потомки и мутанты, а также другие бактерии, которые отбираются описанным здесь способом. Также пригодны ферменты из этих бактерий.
Предпочтительно способ осуществляется либо с находящимися в состоянии покоя клетками бактерий (не растущие клетки), которым не нужен никакой источник углерода и азота, либо с ферментами в бесклеточной системе, причем эти ферменты получаются как описано выше, например, путем разрушения индуцированных бактерий.
Целесообразно, чтобы среда содержала рацемический 2,2-ДМЦПКА в количестве 0,2 5 мас. предпочтительно 0,2 2 мас.
В качестве среды могут служить обычные среды, как, например, низкомолекулярный фосфатный буфер, вышеописанная среда с неорганическими солями или HEPES-буфер (N-2-гидроксиэтилпиперазин-2'-этансульфоновая кислота).
Предпочтительно способ осуществляется в низкомолекулярном фосфатном буфере.
Значение pH среды может быть в области 6 11, предпочтительно 6,5 10.
Целесообразно осуществлять биотрансформацию при температуре 15-55oC, предпочтительно при 20 40oC.
После обычной продолжительности превращения 1 30 ч, предпочтительно 5 -25 ч, R-(-)-2,2-ДМЦПКА полностью превращается в соответствующую кислоту, причем выделяется оптически чистый S-(+)-2,2-ДМЦПКА.
Таким образом, полученный S-(+)-2,2-ДМЦПКА затем можно изолировать, например, путем экстракции, электродиализа или благодаря высушиванию.
Пример 1
Изоляция и селекция бактерий с помощью R-(-)-2,2-ДМЦПКА-гидролазы
К размельченным образцам из почвы (1 г) добавляют изотонический раствор хлорида натрия (9 мл) и все оставляют стоять в течение примерно 5 мин. После этого надосадочную жидкость (0,5 мл) пересевают в среду с неорганической солью (25 мл) (Kulla et. al. Arch. Microbiol. 135, 1 7, 1983), которая содержит глицерин и R,S-(±)-ДМЦПКА в C/N-соотношении 5:1. Затем эту культуру инкубируют вплоть до образования смешанной культуры, которая может использовать R,S-(±)-2,2-ДМЦПКА в качестве N-источника.
Чистые культуры этих бактерий получают при помощи традиционных микробиологических способов.
Полученные таким образом штаммы бактерий затем испытывают на их рост на агаровых пластинках на R,S-(±)-2,2-ДМЦПКА, S-(+)-2,2-ДМЦПКА и R-(-)-2,2-ДМЦПКА, чтобы исключить нежелательные штаммы, одинаково быстро растущие на обоих изомерах [R-(-)-2,2-ДМЦПКА и S-(+)-2,2-ДМЦПКА]
Остальные штаммы испытывают далее. Ими затем засевают среду для культивирования. Полученные в этой предкультуре бактерии переводят в среду из неорганических солей и после этого испытывают на их способность селективно использовать R-(-)-2,2-ДМЦПКА в качестве единственного N-источника, причем надосадочную жидкость исследуют с помощью GC на образование R-(-)-2,2-ДМЦПКК и на обогащение S-(+)-2,2-ДМЦПКК.
Пример 2
Определение активности R-(-)-2,2-ДМЦПКА-гидролазы
Для определения активности гидролазы в суспензии бактерий устанавливают оптическую плотность 0,5 при 650 нм. В качестве среды служит фосфатный буфер (10 ммоль), pH 7,0, с 0,2 мас. R,S-2,2-ДМЦПКА. Эту суспензию инкубируют в течение 3 ч при 30oC и при встряхивании. Выделившийся за счет гидролилазы NH4 + или R-(-)-2,2-ДМЦПКК измеряют и активность выражают в виде граммов превращенного R-(-)-2,2-ДМЦПКА (л/ч) оптическая плотность при 650 нм, предполагая, что 1а ммоль образовавшегося NH4 + равен 1 ммолю превращенного R-(-)-2,2-ДМЦПКА.
Пример 3
Получение S-(+)-2,2-ДМЦПКА
Comamonas acidovorans A:18 культивируют на агаровых пластинах в среде из неорганических солей, с глицерином в качестве C-источника и сульфатом аммония в качестве N-источника в течение 2 дней при 30oC. Состав этой среды из неорганических солей указан в табл. 10. С помощью этих, выращенных на агаровых пластинах бактерий засевают среду для культивирования такого же состава и инкубируют 2 дня при 30oC.
Такую же среду из неорганических солей с Na2SO4 вместо (NH4)2SO4 (100 мл), содержащую 0,2 мас. глицерина и 0,15 мас. R,S-(±)-2,2-ДМЦПКА, засевают с помощью 5 мл этой культуры для индукции и инкубируют в течение 45 ч при 30oC. Затем клетки собирают путем центрифугирования и обрабатывают 0,9%-ным раствором NaCl.
После суспендирования клеток в 10 мМ фосфатом буфере (800 мл), pH 7,0, устанавливают оптическую плотность при 650 нм, равную 1,3, и добавляют 2 мас. R, S-(±)-2,2-ДМЦПКА. После инкубирования в течение примерно 25 ч при 37oC R-(-)-2,2-ДМЦПКА полностью превращается в R-(-)-2,2-ДМЦПКК, что соответствует оптической чистоте (ее) 100% и аналитически измеренному выходу S-(+)-2,2-ДМЦПКА 46,7% За протеканием реакции следят, руководствуясь выделением NH4 + и GC-анализом надосадочной жидкости.
После отделения путем центрифугирования клеток в недосадочной жидкости устанавливают pH-значение 9,5 и продукт выделяют путем экстракции с помощью этилацетата.
Пример 4
Аналогичным образом, как и в примере 1, выделяют микроорганизм Bacterium sp. VIII:II (Corynebacterium aquaticum).
Длительность предкультивирования в случае этих бактерий составляет 4 дня и продолжительность индукции 3 дня при прочих равных условиях, как в примере 3.
В противоположность примеру 3, биотрансформация этой бактерии осуществляется с помощью 0,2 мас. R,S-(±)-2,2-ДМЦПКА, причем активность гидролазы определялась до 0,13 г/л/ч/ОП650 нм.
Пример 5
Аналогичным образом, как и в примере 1, выделяют Pseudomonas sp. NSAK:42 (DSM N 6433). Длительность культивирования составляет 2 дня, продолжительность индукции составляет 18 ч, при прочих равных условиях, как в примере 3, за исключением того, что индукционная среда содержит 1 мас. глицерина (вместо 0,2 мас. ) и дополнительно еще 0,3 мас. универсального пептона (Merck).
Биотрансформация осуществляется с помощью 0,2 мас. R,S-(±)-2,2-ДМЦПКА, причем активность гидролазы определяется до 0,34 г/л/ч/ОП650 нм.
Пример 6
Comamonas acidovorans TG 308 (DSM N 6552) культивируют в течение 2 дней при 30oC в комплексной среде (4 мл) "Nutrient Broth" (Oxoid Ltd. Великобритания). С помощью этих бактерий засевают среду из неорганических солей (табл. 10) и инкубируют 2 дня при 30oC.
Затем собирают клетки соответственно примеру 3.
В противоположность примеру 3 биотрансформация осуществляется в 10 мМ HEPES-буфера (pH 7,0) с 0,5 мас. R,S-(±)-2,2-ДМЦПКА при прочих равных условиях, как и в примере 3.
После инкубации в течение 4,5 ч при 37oC R-(-)-2,2-ДМЦПКА полностью превращается в R-(-)-2,2-ДМЦПКК, что соответствует аналитически измеряемому выходу S-(+)-2,2-ДМЦПКА 45,5% и оптической чистоте (ее) 99,0%
Пример 7
Получение S-(+)-2,2-ДМЦПКА с помощью ферментов в несодержащей клеток (бесклеточной) системе
После индукции клетки Comamonas acidovorans A:18 концентрируют до оптической плотности при 650 нм 210 до 95 мл в HEPES-буфере (10 мМ, pH 7,0). Затем клетки разрушают French-процессом под давлением 1200 бар, двукратно, для того, чтобы получить несодержащий клеток ферментный экстракт, затем все центрифугируют при 20000 об/мин в течение 20 мин.
В этом, не содержащем клеток ферментном экстракте определяют количество протеинов (измеряя по методу Бредфорда) до 39,3 мг протеина/мл.
Для определения активности этих, не содержащих клеток, ферментов 20 мкл (примерно 0,8 мг протеина) экстракта фермента обрабатывают (растворяют) в 4 мл фосфатного буфера (10 мМ, pH 7,0), содержащего 0,2 мас. R,S-(±)-2,2-ДМЦПКА, и инкубируют при 30oC. При этом в несодержащем клеток экстракте 2,5 г R-(-)-2,2-ДМЦПКА/ч/г протеина (3,64 мкмоль/мин/г протеина) превращается в соответствующую кислоту.
Пример 8
Получение S-(+)-2,2-ДМЦПКА с помощью иммобилизированных клеток
После индукции (соответственно примеру 3) собирают клетки Comamonas acidovorans A: 18. Эти клетки иммобилизуют благодаря обработке полиэтиленимином с глутаровым альдегидом (соответственно патенту Чехословакии 251111). Иммобилизированный биокатализатор имеет активность 1,6 мкмоль/мин•г сухого веса. Сухой вес биокатализатора соответствует 32% мокрого веса.
Затем биокатализатор (с 55 г мокрого веса) суспендируют в 800 мл борной кислоты (10 мМ, pH 9,0) с 16 г R,S-(±)-2,2-ДМЦПКА.
После времени инкубации 68,8 ч при 37oC и при скорости перемешивания 200 об/мин R-(-)-2,2-ДМЦПКА полностью превращается в R-(-)-2,2-ДМЦПКК, что соответствует оптической чистоте (ее) 98,2% и аналитически измеряемому выходу S-(+)-2,2-ДМЦПКА 40%






Использование: биотехнология. Сущность изобретения: описывается новый микробиологический способ получения S-(+)-2,2-диметилциклопропанкарбоксамида. Для этого способа селекционированы и выделены новые микроорганизмы, которые способны в рацемическом 2,2-диметилциклопропанкарбоксамиде R-(-)-2,2-диметилциклопропанкарбоксамид биотрансформировать в R-(-)-2,2-диметилциклопропанкарбоновую кислоту. Этот способ затем можно осуществлять либо с помощью этих микроорганизмов, либо с помощью бесклеточных ферментов из этих микроорганизмов. 5 с. и 6 з.п. ф-лы, 10 табл.
| EP, заявка, 0048301, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| EP, заявка, 0155779, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1997-11-20—Публикация
1992-01-30—Подача