Изобретение касается способа получения динитротолуола путем нитрования толуола.
Известно, что нитрование ароматических углеводородов проводят в смеси кислот, а именно, смеси азотной и сорной кислот. Однако, эти системы смесей кислот требуют поддержания нужной концентрации после реакции нитрования. Эта стадия повторного создания концентрации требует время, энергии и использования дорогих материалов для конструкций. Кроме того, использование серной кислоты для нитрования имеет тенденцию давать значительное количество побочных продуктов, нитрокрезола и цианида, удаление которых требует дорогой обработки отходов водой.
Из-за этих недостатков стараются отказаться от применения системы смеси азотной и серной кислот, а вести газофазное или жидкофазное нитрование в концентрированной азотной кислоте в отсутствии серной кислоты. Известен (патент США N 4064147) способ получения мононитросоединения (такого как мононитробензол) жидкофазной реакцией с азотной кислотой при концентрации кислоты 70-100 мас.% при температуре реакции 0-80oC.
При использовании в качестве исходного соединения относительно реакционноспособного соединения, такого как бензол или толуол, предпочтительна концентрация азотной кислоты 70-90 мас.%. Согласно патенту отношение азотной кислоты плюс воды к органическим компонентах должно быть не ниже 3 при использовании 70%-ной азотной кислоты и не ниже 8 при использовании 100%-ной азотной кислоты.
Известно также (патент США 3928395) использование концентрированной азотной кислоты для нитрования ароматических соединений, необязательно в присутствии диполярного апротонного растворителя, инертного относительно нитрующего агента. Согласно патенту, реакцию останавливают разбавлением реакционной смеси диполярным апротонным растворителем после достижения требуемой степени нитрования. Однако, использование таких растворителей или в процессе реакции, или для остановки реакции вызывает необходимость ликвидации отходов.
Поскольку динитротолуол является промежуточным продуктом при получении ТД1, очень важны новые способы селективного получения этого промежуточного продукта, позволяющие избежать вышеупомянутые недостатки. Это достигается предложенным способом, который заключается в получении динитротолуола путем нитрования толуола в жидкой фазе безводной азотной кислотой в реакторе при температуре от 0 до 60oC в течение менее 15 мин при молярном соотношении азотной кислоты плюс воды к толуолу между 10:1 и 15:1, причем процесс проводят в отсутствии серной кислоты, а также без апротонного диполярного растворителя, как на стадии процесса нитрования, так и на стадии остановки процесса с получением динитротолуола в смеси продуктов с последующей перегонкой этой смеси в вакууме при отсутствии любого апротонного диполярного растворителя для удаления непрореагировавшей азотной кислоты от вышеназванной смеси продуктов, получен тем самым вышеназванный динитротолуол.
Таким образом, согласно способу настоящего изобретения реакция нитрования проводится при использовании безводной азотной кислоты в отсутствии серной кислоты. Используемый здесь термин "безводная азотная кислота" означает азотную кислоту концентрации 95-100 мас.%, предпочтительно, по крайней мере, 98 мас. %, остальное вода. Желательно, чтобы количество воды в реакционной смеси было минимальным, так как вода вызывает остановку реакции нитрования на стадии мононитрования в реакции толуола и мешает нитрованию бензола до мононитробензола.
Способ настоящего изобретения является одностадийной реакцией, проводимой в однофазной жидкой среде и не включает образование двухфазных эмульсий, наблюдаемое при обычном способе нитрования смесью серной и азотных кислот. Кроме того^ реакция проводится при умеренных условиях реакции с получением прекрасного выхода требуемого мононитробензола или динитротолуола. Таким образом, реакцию удобно проводить при температуре реакции, не превышающей 80oC, предпочтительно между 0 и 60oC, более предпочтительно между 10 и 60oC, особенно предпочтительно между 20 и 30oC. Реакцию удобно проводить при атмосферном давлении, хотя, если требуется, может быть использовано давление выше атмосферного. Время реакции обычно составляет менее получаса, предпочтительно менее 15 мин и более предпочтительно менее 5 мин.
Для реакции толуола до динитротолуола молярное соотношение азотная кислота плюс вода к толуолу используется обычно между 10:1 и 15:1, предпочтительно между 11:1 и 12:1.
Это позволяет достичь максимальный выход целевого продукта с минимальным содержанием побочных продуктов.
После окончания реакции и образования целевого продукта, избыток (непрореагировавшая) азотной кислоту удаляется из реактора, предпочтительно перегонкой в вакууме, что обеспечивает перегонку при низкой температуре и давлении. Подходящие температуры перегонки варьируют от 30 до 6ОoC. Подходящие значения давления для перегонки изменяются от 50мм Hg до 300мм Hg.
После удаления избытка безводной азотной кислоты, выделение ДНТ (динитротолуол) из кубового остатка после перегонки проводят с помощью разделения фаз, осуществляемого добавлением небольшого количества воды или разбавленной азотной кислоты. Очищенный ДНТ получают промыванием водой и щелочным раствором. Промывные воды свободны от примесей нитрокрезола, содержащиеся в отработанной воде, полученной после обычного способа получения ДНТ со смесью серной и азотной кислот. Водная азотная кислота со стадии разделения фаз может быть очищена экстракцией толуолом, толуольная фаза возвращается на стадию реакции и 60-70%-ную водную азотную кислоту повторно концентрируют, затем продают или используют для производства других продуктов.
Следующие примеры иллюстрируют, но не ограничивают объем настоящего изобретения.
Пример 1. Синтез динитротолуола.
Четырехмиллилитровую ампулу, снабженную магнитной мешалкой и силиконовой мембраной, погружают в баню с водой. Реакционный сосуд продувают азотом со скоростью 20 см3 мин, продувку подсоединяют к 100 мл стеклянной приемной колбе, погруженной в баню с водой и льдом. Реакционную ампулу загружают 50 мл 98% HNO3 (75,0 г, 1,13 моль) и 10 мл (8,67 г, 0,094 моль) толуола. Скорость подачи составляет 0,60 мл HNO3/мин и 0,12 мл толуола/мин и контролируется насосом Sage Instrument Syringe, модели 351 и 355. Содержимое реактора регулируют на уровне 2 мл с помощью регулировки высоты линии выхода у реактора в реакционной ампуле так, чтобы время пребывания в реакторе составляло 2,8 мин.
Температуру водяной бани поддерживают 15±5oC периодическим добавлением льда в течение прибавления реагентов. После окончания прибавления реагентов содержимое реактора перемешивают 3 мин, затем удаляют приемник. Получают 83,31 г светло-желтого раствора продукта, который перегоняют (53oC, 75-160 мм Hg) и получают 38,75 г светло- желтой кислоты, анализ которой титрованием стандартизованным NaOH показывает 100% HNO3. Резервуар содержит 44,2 г светло-желтого раствора, 0,42 г HNO3 остается на стенках химической посуды, 0,43 г продукта теряется с парами NO2 при перегонке. Содержимое резервуара разбавляют 21,72 г воды, экстрагируют 33,30 г толуола. Разделение слоев дает 48,74 г слабой водной кислоты и 48,11 г раствора ДНТ в толуоле. Органический слой промывают один раз 20 мл воды, сушат над MgSO4/, и фильтруют. Выход извлеченного ДНТ рассчитывают 86% и по ГХ анализу продукт содержит 0,02 мас. % 4-нитротолуола, 17,36% 2,6-ДНТ, 0,48% 2,5 ДНТ, 78,47% 2,4-ДНТ, 1,65% 2,3-ДНТ, 1,92% 3,4-ДНТ и 0,09% ТНТ. Количество HNO3 в виде выделенной слабой кислоты и эквивалент ДНТ составляет 99%.
Пример 2. Дополнительный синтез динитротолуола.
По способу, описанному в примере 1, в реакционный сосуд подают 100 мл 98% HNO3 (150,0 г, 2,38 моль) и 21 мл (18,2 г, 0,20 моль) толуола со скоростью соответственно 0,80 мл/мин и 0,17 мл/мин. Получают 166,26 г светло-желтого жидкого продукта. Продукт нагревают 2 ч. при 55- 60oC, затем охлаждают, разбавляют 46,5 г ледяной воды. Образовавшуюся суспензию экстрагируют 41,5 г толуола, затем повторно 46,3 г толуола. Объединенные экстракты толуола экстрагируют 3х15 мл 5%-ным раствором гидроокиси натрия. Экстракты объединяют, полученный желтый щелочной экстракт охлаждают, подкисляют разбавленной серной кислотой, экстрагируют 3х10 мл хлористым метиленом. После упаривания основного объема хлористого метилена, экстракт хлористого метилена, содержащий кислые органические соединения от первоначального ДНТ продукта, характеризуется газо-хроматографической масс-спектрометрией. Не обнаружены мононитро- или динитрокрезолы (минимальный уровень обнаружения рассчитывают при 2 ppm) (частей на миллион) от начального веса полученного ДНТ).
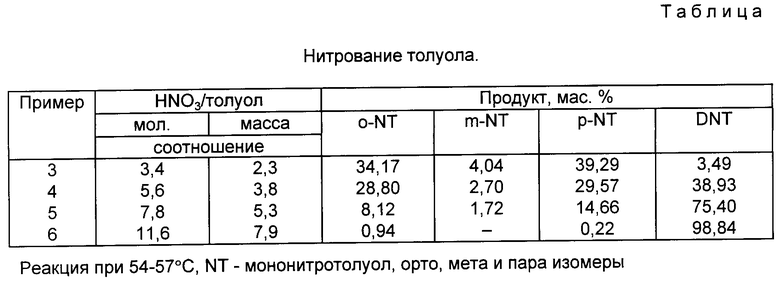
Дополнительные эксперименты выполняют для определения соотношения реагентов, пригодного для селективного синтеза ДНТ. Эти данные сведены в таблице для различных молярных соотношений HNO3 к толуолу.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИНИТРОТОЛУОЛА | 1995 |
|
RU2100347C1 |
| СПОСОБЫ ОТДЕЛЕНИЯ КИСЛОТНОЙ ПРИМЕСИ ОТ РАСТВОРА И СПОСОБ ОТДЕЛЕНИЯ АЗОТНОЙ КИСЛОТЫ ОТ РАСТВОРА | 1991 |
|
RU2061671C1 |
| СПОСОБ УДАЛЕНИЯ И РЕГЕНЕРАЦИИ СМЕСЕЙ НИТРУЮЩИХ КИСЛОТ ИЗ ПРОЦЕССОВ НИТРОВАНИЯ И ПРОМЫШЛЕННАЯ УСТАНОВКА ДЛЯ НИТРОВАНИЯ | 2006 |
|
RU2356885C2 |
| СПОСОБ ПРОМЫВКИ ДИНИТРОТОЛУОЛА | 2013 |
|
RU2627308C2 |
| СПОСОБ ДВУХСТАДИЙНОГО ПОЛУЧЕНИЯ ДИНИТРОТОЛУОЛА | 2004 |
|
RU2330836C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА ХЛОРА (ВАРИАНТЫ) | 1992 |
|
RU2104247C1 |
| СПОСОБ ВЫДЕЛЕНИЯ 4-НИТРОТОЛУОЛА | 2014 |
|
RU2560882C1 |
| Способ получения 3,3 @ -динитро-4,4 @ -дигидроксибензофенона | 1988 |
|
SU1606507A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОНИТРОТОЛУОЛОВ | 1995 |
|
RU2119909C1 |
| СПОСОБ ГАЗОВОЙ ДЕЛИГНИФИКАЦИИ ДРЕВЕСНОЙ ПУЛЬПЫ | 1994 |
|
RU2097461C1 |
Изобретение описывает способ нитрования толуола для получения динитротолуола, характеризующийся жидкофазной реакцией нитрования, отличающийся тем, что это реакция безводной азотной кислоты с толуолом в реакторе при температуре реакции между 20oС и 30oС за время реакции менее 15 мин при молярном соотношении азотная кислота плюс вода к толуолу между 10 : 1 и 15 : 1, причем вышеназванная реакция проводится в отсутствии серной кислоты и любого апротонного диполярного растворителя при проведении реакции и при отсутствии любого апротонного диполярного растворителя для остановки реакции для получения вышеназванного динитротолуола в смеси продуктов без примеси нитрокрезола, с последующей перегонкой в вакууме смеси продуктов без использования любого апротонного диполярного растворителя для удаления непрореагировавшей азотной кислоты из вышеназванной смеси продуктов, получая тем самым динитротолуол. 7 з.п. ф-лы, 1 табл.
Авторы
Даты
1998-03-10—Публикация
1993-06-01—Подача