Изобретение касается обеспечения клеток человека или животного биологически активными веществами, в частности средства для переноса нуклеиновых кислот или их производных в клетки человека или животных.
Известно средство для переноса нуклеиновой кислоты, или ее производного, или кодирующей ее последовательности в гепатоциты, представляющее собой конъюгат модифицированного в случае необходимости поликатиона, преимущественно полилизина, или кодирующей поликатион последовательности и гликопротеина, связываемого имеющимся на поверхности гепатоцитов рецепторами (G.Y.Wu, C.H. Wu, J.Biol. Chem.,т.263, N 29, с.14624-14624, 1988).
Недостаток известного средства состоит в том, что оно пригодно только для введения нуклеиновых кислот или их производных в гепатоциты. Следовательно, эксплуатационные возможности известного средства ограничены.
Задачей изобретения является расширение эксплуатационных возможностей, направленное на то, что биологически активные вещества можно вводить в самые различные клетки человека и животных.
Данная задача решается предлагаемым средством для переноса нуклеиновых кислот или их производных в клетки человека или животных, содержащим поликатион и гликопротеин в виде конъюгата, отличительная особенность которого заключается в том, что из поликатионов оно содержит полилизин, или протамин, или гистон, а из гликопротеинов - трансферин при мольном соотношении трансферина и поликатиона, равном (10,5 : 1) - (1 : 4).
Трансферины представляют класс родственных связывающих металл транспортных гликопротеинов со специфичностью на живом организме для железа. Были идентифицированы различные трансферины млекопитающих животных, причем трансферин плазмы снабжает железом большинство тканей тела. Основным производителем трансферина является печень.
Трансферин имеет молекулярный вес около 80000, 6% которого приходятся на сахарные остатки. Одна молекула трансферина может связывать две молекулы железа, причем связывать две молекулы железа, причем связывание требует присутствия ионов карбоната или бикарбоната.
Рецептор трансферина, от которого на различных клетках в незначительном количестве (предположительно в группе углеводов) имеются отклонившиеся друг от друга формы, представляет трансмембранный гликопротеин с молекулярным весом около 180000, причем одна молекула рецептора может связывать одну или возможно две молекулы трансферина.
Рецептор трансферина при физиологическом значении рН 7,4 имеет очень высокое средство к Fe2-трансферину, меньшее сродство к Fe-трансферину и практически не имеет сродства к апотрансферину, хотя последний при рН 5 образует очень стойкий комплекс с рецептором.
Рецепторы трансферина были обнаружены особенно в большом количестве в предшественниках эритроцитов, плаценте и печени, в измеримом количестве также во многих других тканях тела. Особый интерес представляет собой наблюдение о том, что рецептор в растущих клетках можно регулировать в плюсовую сторону. Наблюдали также, что количество рецептора в опухолевой ткани в живом организме в противоположность доброкачественным поражениям значительно повышено, что указывает на повышенную потребность в железе. Механизм поглощения рецепторами комплекса трансферина и железа и его внутриклеточный цикл хорошо исследованы.
Молярное соотношение трансферина и вышеуказанного поликатиона в рамках вышеуказанных предельных величин выбирают таким образом, что происходит комплексообразование с нуклеиновой кислотой и гарантируется, что образованный комплекс связывается рецептором трансферина и переносится в клетку, что от случая к случаю можно проверять просто осуществляемыми опытами.
Соответственно, выбранное соотношение зависит, прежде всего, от размера молекулы вышеуказанного поликатиона, а также от числа и распределения положительно заряженных групп, критериев, которые согласуются с размером, структурой и возможно имеющимися модификациями переносимой нуклеиновой кислоты.
Протамины представляют собой небольшие (молекулярный вес приблизительно до 8000), сильно основные протеины, у которых положительно зараженные аминокислотные остатки (прежде всего аргинины) обычно расположены группами и которые на основании поликатионного характера нейтрализуют отрицательные заряды нуклеиновых кислот.
Применяемые в рамках изобретения протамины могут быть природного происхождения, или их можно получать рекомбинатным путем, причем можно изготовлять многократные копии или производить модификации относительно размера молекул и последовательности аминокислот. Соответствующие соединения можно также синтезировать химическим путем. При синтезе искусственного протамина можно, например, поступать таким образом, что аминокислотные остатки, которые при природном протамине имеют функции, нежелательные для функции переноса (например, конденсация ДНК), заменяют другими подходящими аминокислотами и/или на одном конце предусматривают аминокислоту (например, цистеин), которая делает возможной конъюгацию с трансферином.
Гистоны - это имеющиеся в хроматине небольшие связывающие ДНК протеины с высоким процентом положительно заряженных аминокислот (лизин и аргинин), который делает их способными независимо от последовательности нуклеотидов связываться с ДНК и складывать их в нуклеосомы, для чего особенно пригодны богатые аргинином гистоны H3 и H4.
Размер вышеуказанных поликатионов предпочтительно выбирают таким образом, что сумма положительных зарядов составляет около 20 - 5000, он согласуется с переносимой нуклеиновой кислотой.
Связь поликатиона с трансферином можно осуществлять химическим или, если поликатион представляет полипептид, рекомбинантным путем. Связь химическим путем можно осуществлять известным для связывания пептидов способом, причем, если требуется, отдельные компоненты перед реакцией связывания снабжают связывающими веществами (эта мера необходима тогда, когда с самого начала не имеется подходящей для связывания функциональной группы, например меркаптогруппы или спиртовой группы. При связующих веществах речь идет о бифункциональных соединениях, которые сначала вступают в реакцию с функциональными группами отдельных компонентов, после чего осуществляют связывание модифицированных отдельных компонентов.
В зависимости от требуемых свойств предлагаемого средства (в дальнейшем "конъюгат"), особенно ввиду его стабильности, можно осуществлять связывание через
а) дисульфидные мостики, которые в восстанавливающих условиях могут снова расщепляться (например, при применении сукцинимидилпиридилдитиопропионата):
б) в основном стойкие в биологических условиях соединения (например, простые тиоэфиры, реакцией малеимидо-связывающих веществ с сульфгидриловыми группами связанного с вторым компонентом связующего вещества):
в) неустойчивые в биологических условиях мостики, например эфирные связи, или неустойчивые в слабо-кислых условиях ацетальные или кетальные связи.
Связывание рекомбинантным путем дает то преимущество, что можно получать точно определенные, однородные соединения, в то время как при химическом связывании образуются смеси конъюгантов, которые следует разделять.
Рекомбинантные связывание можно осуществлять по известным для получения химерных полипептидов методам. При этом поликатионные пептиды можно изменять относительно их размера и последовательности аминокислот. Получение методом генной инженерии дает также то преимущество, что можно модифицировать трансферин в конъюгате, например, за счет того, что благодаря подходящим мутациям можно повышать способность связывания с рецептором или же за счет того, что трансферин может находиться только в ответственной для связывания с рецептором части молекулы. Особенно целесообразным для рекомбинантного связывания является применение вектора, который содержит кодирующую трансферин последовательность и полилинкер, в который вводят соответственно необходимую кодирующую поликатионный пептид последовательность. Таким путем можно получать набор экспресионных плазмид, из которого в случае необходимости содержащую желаемую последовательность плазмиду используют для экспрессии предлагаемого конъюгата.
У переносимых в клетку нуклеиновых кислот речь может идти о ДНК или РНК, причем относительно последовательности нуклеотидов не существует никаких ограничений. Нуклеиновые кислоты могут быть модифицированы при условии, что модификация не причиняет ущерба полианионному характеру нуклеиновых кислот: к таким модификациям причисляют, например, замещение фосфодиэфирной группы фосфоротиоатом или применение нуклеозидных аналогов.
В качестве нуклеиновых кислот в рамках настоящего изобретения принимают во внимание прежде всего такие нуклеиновые кислоты, которые с целью торможения специфических генных последовательностей должны переноситься в клетку. К ним причисляют противочувствительные олигонуклеотиды и рибоцимы, в случае необходимости вместе с нуклеиновой кислотой-носителем.
Относительно размера нуклеиновых кислот изобретение также позволяет применять его в широких пределах. Относительно нижнего предела не существует никакого обусловленного предлагаемым коньюгатом ограничения: возможное ограничение получается по специфике применения, так как, например, противочувствительные олигонуклеотиды приблизительно ниже 10 нуклеотидов едва ли могут применяться в расчет ввиду слишком небольшой специфичности. С помощью предлагаемого конъюгата можно переносить также в клетку плазмиды, причем прежде всего имеют практическое значение небольшие плазмиды, которые по своей функции применяются в качестве нуклеиновой кислоты - носителя (например, ретровирусные носители до 5000 пар оснований (далее п.о.).
С помощью предлагаемого коньюгата также возможно переносить в клетку одновременно различные нуклеиновые кислоты.
Другое преимущество настоящего изобретения заключается в том обстоятельстве, что для трансферина и рецептора существуют полиморфизмы, которые могут использовать для целенаправленного переноса тормозящих нуклеиновых кислот в определенные клетки.
В рамках настоящего изобретения смогли показать, что конъюгаты трансферина и поликатиона эффективно поглощаются живыми клетками и вводятся внутрь. Предлагаемый конъюгат или его комплекс с нуклеиновой кислотой не являются вредными для роста клеток. Это делает возможным повторное применение и тем самым постоянно высокую экспрессию введенных в клетку генов.
Далее, можно было обнаружить, что конъюгаты поликатиона и трансферина могут функционально заменять нативный комплекс трансферина и железа.
Тот факт, что комплексы трансферина и поликатиона с ДНК поглощаются клеткой через рецептор трансферина, был подтвержден с помощью гена люциферазы в качестве ДНК-компонента. Было показано, что нативный трансферин эффективно вытесняет комплекс трансферина и поликатиона с ДНК, что измерялось на основании уменьшения активности люциферазы в клетке.
Благодаря осуществленным в рамках настоящего изобретения опытам могли также показать, что ген т-РНК и рибоцима (рибоцим был направлен против последовательности V-erbB) при помощи предлагаемого конюъгата может вводиться в трансформированные erbB куриные клетки и ослаблять трансформирующее действие онокогена. Этот результат тем значительнее, что в этих опытах применяли только небольшое количество рибоцимного гена.
Соотношение нуклеиновой кислоты и конъюгата может колебаться в широких пределах, причем не обязательна нейтрализация всех зарядов нуклеиновой кислоты. Это соотношение от случая к случаю в зависимости от таких критериев как, размер и структура переносимой нуклеиновой кислоты, размер поликатиона, число и распределение его зарядов, можно регулировать таким образом, что существует благоприятное для соответствующего применения отношение между способностью переноса и биологической активностью нуклеиновой кислоты. Это соотношение сначала можно регулировать грубо, например на основании замедления скорости миграции ДНК в геле, или центрифугированием с соблюдением градиента плотности. После получения этого предварительного соотношения может оказаться целесообразным, принимая во внимание максимальную имеющуюся в клетках активность нуклеиновой кислоты, осуществление опытов по переносу в клетку радиоактивно меченного комплекса и, в случае необходимости, до такой степени, чтобы остающиеся отрицательные заряды нуклеиновой кислоты не препятствовали переносу в клетку.
Получение комплекса конъюгата трансферина и поликатиона с нуклеиновой кислотой можно осуществлять методами, известными для комплексообразования полионных соединений. Одна возможность предотвращения неконтролируемого скопления или осаждения состоит в том, что оба компонента сначала смешивают при высокой (около I-молярной) концентрации хлористого натрия и затем диализом или разбавлением доводят до физиологической концентрации хлористого натрия. При реакции комплексообразования преимущественно не применяют слишком высокие концентрации ДНК и конъюгата (более 100 мкг/л), чтобы избежать осаждения комплекса.
Предпочтительной нуклеиновой кислотой в комплексе конъюгата трансферина и поликатиона с нуклеиновой кислотой является противочувствительная РНК или рибоцим или кодирующий его ген. При применении рибоцимов и противочувствительных РНК особенно выгодно вводить гены, кодирующие тормозящую функцию РНК РНК-азы предпочтительно вместе с геном-носителем. Введением гена в клетку в противоположность абсорбции РНК как таковой гарантируют значительное увеличение числа РНК и тем самым запас, достаточный для желаемого торможения биологической реакции. Особенно подходящими генами-носителями являются необходимые для транскрипции полимеразой III транскрипционные единицы, например гены т-РНК. В последние можно включать, например, рибоцимные гены таким образом, что при транскрипции рибоцим представляет часть компактного транскрипта полимеразы III. С помощью предлагаемого конъюгата можно усиливать действие этих генетических единиц за счет того, что повышенная исходная концентрация гена в клетке гарантируется.
Изобретение иллюстрируется нижеследующими примерами.
Пример 1. Получение конъюгатов трансферина и полилизина 90.
Связывание производят аналогично известным из литературы методам введением дисульфидных мостиков после модификации сукцинимидилпиридилдитиопропионатом.
а) Модифицированный 3-(2-пиридилдитио)пропионатом трансферин
6 мл фильтрованного через гель сефадекс Г-25 раствора 120 мг (1,5 ммоль) трансферина (из белка куриного яйца, кональбумина типа 1, не содержащего железа) в 3 мл 0,1 - молярного буфера фосфата натрия (pH 7,8) смешивают при сильном встряхивании с 200 мкл 15 ммолярного этанольного раствора сукцинимидил-3-(2-пиридилдитио)-пропионата (3 ммоль, далее SPDP) и смесь оставляют стоять в течение часа при комнатной температуре и при случайном встряхивании, через колонку с гелем (сефадекс Г-25, размер 14 х 180 мм, 0,1 - молярный буферный раствор фосфата натрия с pH 7,8) отделяют низкомолекулярные продукты реакции и остатки реагентов и получают при этом 7 мл фракции продукта: содержание связанных с трансферином остатков пиридилдитиопропионата устанавливают при помощи аликвота после восстановления дитиотреитолом путем фотометрического определения количества высвободившегося пиридин-2-тиона. Оно составляет около 2,6 мкмоль.
Идентичным образом модифицируют трансферин человека (не содержащий железа).
б) Модифицированный меркаптопропионатом полилизин 90 (далее pL 90)
Раствор 18 мг (около 1,0 мкмоль) гидробромида поли-L-лизина, меченного изотиоцианатом флуоресцеина (далее FITC) с молекулярным весом около 18000 (соответствует средней степени полимеризации около 90) в 3 мл 0,1-молярного фосфата натрия (pH 7,8) фильтруют через сефадекс Г-25 (флюоресцентную маркировку осуществляют в буферном растворе бикарбоната натрия с pH 9 в течение 3 ч). Раствор полилизина разбавляют водой до 7 мл, смешивают при хорошем встряхивании с 270 мкл 15-ммолярного этанольного раствора SPDP и смесь оставляют стоять в течение часа в темноте при комнатной температуре и при случайном встряхивании. После добавки 0,5 мл 1-молярного буферного раствора ацетата натрия (pH 5,0) низкомолекулярные вещества отделяют фильтрацией через сефадекс Г-25 (элюент: 20 ммоль буферного раствора ацетата натрия с pH 5,0). Фракцию продукта (окрашивание нингидрином, флюоресценция) сгущают в вакууме, pH среды доводят примерно до 7 добавкой буфера, добавляют раствор 23 мг (150 мкмоль) дитиотреитола в 200 мкл воды и смесь оставляют в темноте на один час при комнатной температуре в атмосфере аргона. Дальнейшей гель-фильтрацией (на сефадексе Г-25 колонка размером 14 х 130 мм, 10 ммоль буферного раствора ацетата натрия с pH 5,0) отделяют избыточный восстановитель и получают 3,5 мл раствора полилизина с флюоресцентной маркировкой, содержащего 3,8 мкмоль меркаптогрупп (фотометрическое определение с помощью реактива Эллмана, 5,5 - дитиобис-2-нитробензойной кислоты).
в) Конъюгаты трансферина и полилизина
Полученный на стадии а) раствор модифицированного трансферина (7 мл в 0,1 - молярном буферном растворе фосфата натрия с pH 7,8, около 1, 5 мкмоль трансферина, содержащего приблизительно 2,6 мкмол остатков пиридилдитиопропионата) промывают аргоном; добавляют 2,0 мл полученного на стадии б) раствора меркапто- модифицированного полилизина (в 10 ммоль буферного раствора ацетата натрия с pH 5,0, это соответствует приблизительно 0,6 мкмоль полилизина приблизительно с 2,2 мкмоль меркаптогрупп), промывают аргоном, встряхивают и в атмосфере аргона оставляют стоять в темноте на 18 ч при комнатной температуре. Реакционную смесь разбавляют водой до 14 мл и разделяют ионообменной хроматографией (содержащая ионит моно S колонка HR 10/10, градиентная элюация, буферный раствор А:50 ммоль HEPES с pH 7,9, буферный раствор Б: А+3 моль хлористого натрия, 0,5 мл/мин, фиг. 1). Неконъюгированный трансферин элюируют вначале, фракции продукта приблизительно при 0,66-1,5 моль хлористого натрия. Получают конъюгаты, которые имеют усредненное (по всем фракциям) соотношение трансферина и полилизина, равное 1,3:1.
Конъюгированные продукты (окрашивание нингидрином, абсорбция протеина в ультрафиолете при 280 нм и измерение флюоресценции маркированного FITC полилизина при 495 нм) собирают в 6 фракций с содержанием каждая приблизительно 10 мг трансферина.
Фракции сначала подвергают диализу относительно 100 ммоль раствора цитрата железа (III) (бикарбонатом натрия доводят до pH 7,8) и после этого еще дважды диализуют относительно 1 ммоль буферного раствора HEPES (pH 7,5).
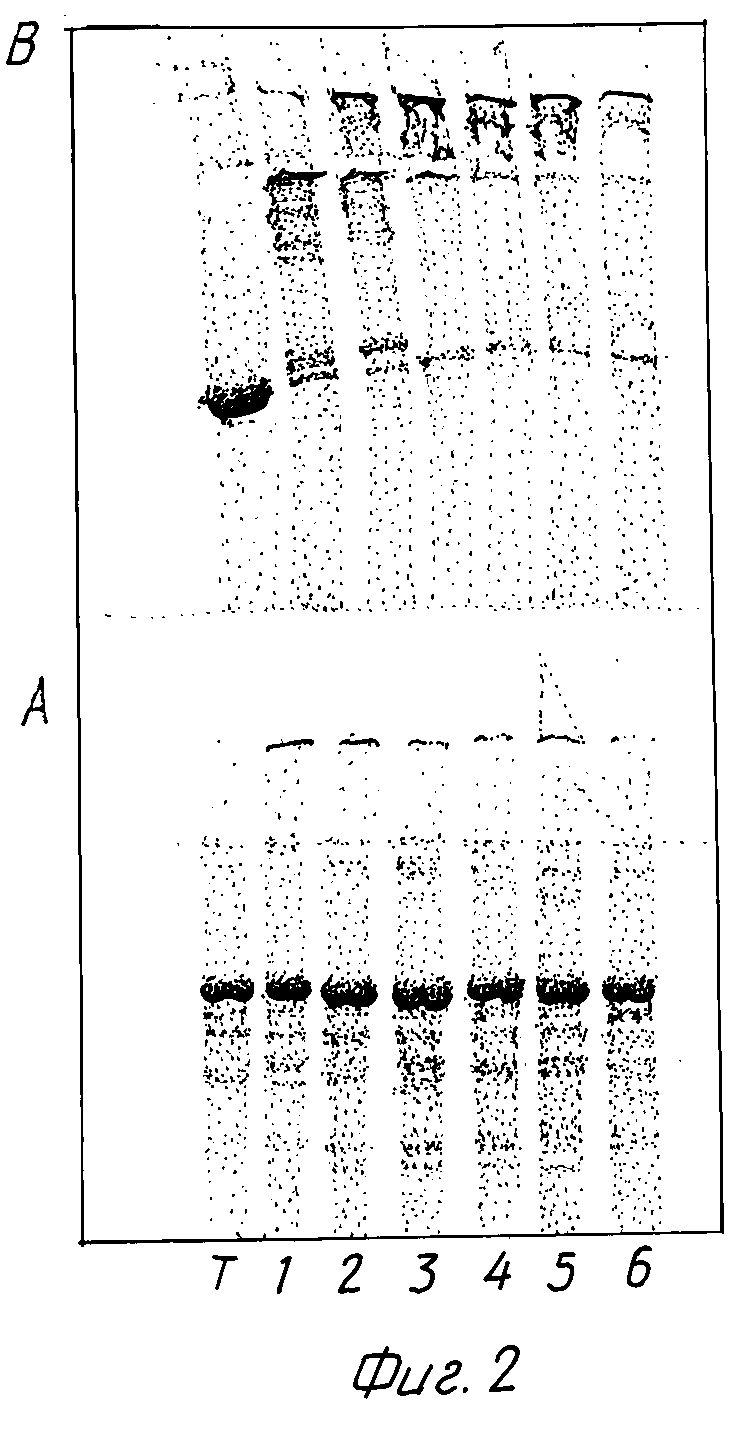
После предварительной обработки 2-меркаптоэтанолом гельэлектрофорез с применением 10% додецилсульфата натрия (далее SDS; 8% полиакриламидного геля, см. фиг. 2) показывает во всех 6 фракциях приблизительно одинаковое содержание трансферина (см. фиг. 2А), в то время как в невосстановленных пробах обнаруживают не полосы для свободного трансферина, а только менее далеко переходящие коньюгаты (см. фиг. 2B, T - необработанный трансферин: 1-6= фракции 1-6 конъюгатов).
Пример 2. Получение конъюгатов трансферина и полилизина 270 и трансферина и полилизина 450 (далее конъюгаты TfpL 270 и TfpL 450)
а) Получение модифицированного трансферина осуществляют аналогично примеру 1(а).
б) Получение модифицированного полилизина 270 и полилизина 450
Отфильтрованный на геле раствор 0,33 мкмоль полилизина 270 (со средней степенью полимеризации, равной 270 остаткам лизина, с флюоресцентной маркировкой или без нее: соответственно 19 мг гидробромидной соли) в 1,2 мл 75-ммолдярного буферного раствора ацетата натрия доводят до pH 8,5 при помощи буферного раствора карбоната натрия. При интенсивном перемешивании добавляют 182 мкл 15-ммолярного этанольного раствора SPDP (1,9 мкмоль). Через час добавляют 200 мкл 1-молярного ацетата натрия с pH 5; после фильтрации на геле с применением 20 ммоль ацетата натрия получают раствор, который содержит 0,27 мкмоль полилизина 270 с 1,3 мкмоль меркаптогрупп (4,8 связующего вещества на одну цепь полилизина).
Аналогичным образом 0,20 мкмоль полилизина 450 (со средней степенью полимеризации, равной 450 остаткам лизина) модифицируют при помощи 2,25 мкмоль SPDP, причем получают продукт 0,19 мкмоль полилизина 450 с 2,1 мкмоль меркаптогрупп (II связующих веществ на одну цепь полилизина). Аналогично примеру 1б) дитиопиридиновые группы восстанавливают дитиотреитолом, чтобы получить свободные сульфгидрильные группы.
в) Получение конъюгатов трансферина и полилизина
1,0 мкмоль модифицированного трансферина в 100 ммоль буферного фосфатного раствора с pH 7,8 смешивают с 0,14 мкмоль модифицированного полилизина 270 (в 20 ммоль буферного раствора ацетата натрия) при исключении кислорода в атмосфере аргона. После 18 ч при комнатной температуре реакционную смесь разбавляют водой до объема 10 мл и подвергают катионообменной хроматографии (содержащая ионит моно S колонка HR10/10: градиентная элюация, буферный раствор A: 50 ммоль HEPES c pH 7,9: буферный раствор Б: А+3 моль хлористого натрия: абсорбция в ультрафиотеле при 280 нм и измерение флюоресценции, активация при 480 нм, эмиссия при 530 нм). При этом сначала элюируют избыток несвязанного трансферина. Фракции продукта элюируют между 30 и 50% градиента Б и собирают в виде 3 фракций (молярные соотношения трансферина и полилизина: фракция A: 5,5:1: фракция Б: 3,4:1: фракция В: 1,8:1). Конъюгаты получают со средним выходом 0,23 мкмоль трансферина с 0,075 мкмоль полилизина 270.
Подобным образом получают конъюгаты трансферина и полилизина 450, причем исходят из 1,2 мкмоль модифицированного трансферина по примеру 1(а) (в 20 ммоль буфера HEPES с pH 7,9, содержащего 80 ммоль хлористого натрия) и 71 нмоль меркапто-модифицированного полилизина 450 при примеру 2(б) в ацетатном буфере.
Очистку реакционной смеси проводят с помощью гель-проникающей хроматографии (содержащая ионит супероза 12 колонка, 1 моль хлористого гуанидина с pH 7,3) и диализа (20 ммоль буфера HEPES с pH 7,3, содержащего 100 ммоль хлористого натрия). Получают конъюгаты трансферина и полилизина, содержащие 0,40 мкмоль трансферина и 33 нмоль полилизина 450.
Вставку железа осуществляют таким образом, что на 1 мг трансферина в конъюгате добавляют 6-12 мкл 100 ммоль буферного раствора цитрата железа (содержащего бикарбонат натрия, pH 7,8).
Пример 3.
а) Получение конъюгатов трансферина и протамина
Получение модифицированного трансферина осуществляют аналогично примеру 1(а).
б) Получение модифицированного 3-меркаптопропионатом протамина
К раствору 20 мг (3 мкмоль) трифторацетатной соли протамина (полученной ионообменной хроматографией выделенного из спермы лосося протамина в виде сульфата (продукт "сальмин" инофирмы Сигма, DE) в 2 мл диметилсульфоксида и 0,4 мл изопропанола, содержащего 2,6 мкл (15 мкмоль) этилдиизопропиламина, добавляют несколькими порциями в течение одного часа раствор 30 мкмоль SPDP в 250 мкл изопропанола и 250 мкл диметилсульфоксида. После 3,5 ч при комнатной температуре раствор упаривают в высоком вакууме и поглощают в 0,5%-ной уксусной кислоте с содержанием 10% метанола. В результате гель-фильтрации (ионит: сефадекс Г-10: 0,5%-ная уксусная кислота с 10% метанола) получают после лиофилизации 16 мг (2,5 мкмоль) ацетатной соли протамина, модифицированной 2,5 мкмоль дитиопиридинового связующего вещества. Восстановление 1,75 мкмоль протамина (содержащего 1,75 мкмоль связующего) при помощи 16 мл дитиотреитола в буферном растворе бикарбоната натрия с pH 7,5 в течение одного часа в атмосфере аргона, последующее доведение pH до 5,2 и гельфильтрация с применением сефадекса Г-10 и 20 ммоль буферного раствора ацетата натрия с pH 5,2 дают раствор протамина, модифицированного 1,6 мкмоль меркаптопропионата.
в) Получение конъюгатов трансферина и протамина
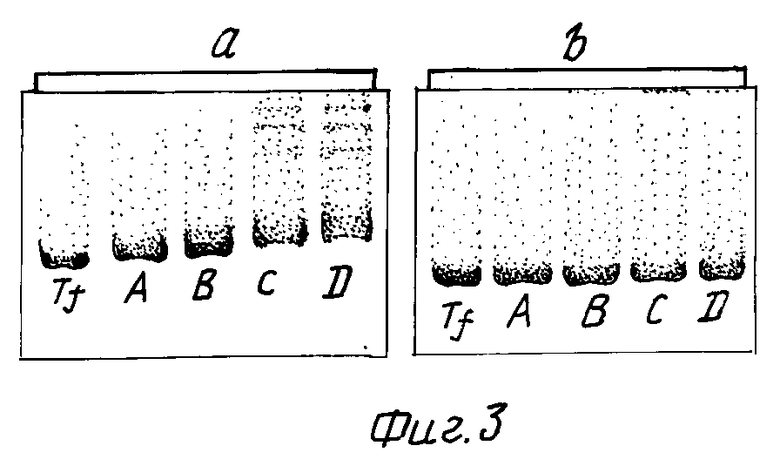
В результате реакции полученного на стадии (б) раствора протамина (1,6 мкмоль связывающего агента) с 1,34 мкмоль трансферина (модифицированного при помощи 3,1 мкмоль дитиопиридинового связующего вещества) и последующей очистки катионообменной хроматографией, описанной выше для конъюгатов трансферина и полилизина, получают четыре последовательно элюируемые фракции A-D, содержащие соответственно 90, 320, 240 и 120 нмоль модифицированного трансферина с возрастающими количествами протамина (определенными посредством гель-электрофореза: 10% SDS, 8% полиакриламидного геля, окрашивание коомасси-синим). Фиг. 3 показывает результат гель-электрофореза. Фракции A-D конъюгата трансферина и протамина, в которых соотношение трансферина и протамина составляет 1:1, 1:4, 1:3 и 1:1,5 соответственно, показывают медленно мигрирующие полосы (а), в то время как в восстановленных меркаптоэтанолом пробах (b) обнаруживается только полоса трансферина. Диализ и вставку железа осуществляют тем же образом, что и описано в примере 2 для конъюгатов TfpL 270 и TfpL 450.
Пример 4. Получение коньюгата трансферина и гистона H4.
а) Получение модифицированного трансферина
Процесс осуществляют аналогично примеру 1 (а).
б) Получение модифицированного 4-меркаптобутиримидатом гистона H4
В атмосфере аргона к раствору 2,7 мг (0,24 мкмоль) гистона H4 в 0,8 мл буфера (200 мМ HEPES, pH 8,5, 5мМ ЭДТУК) добавляют 12 мкл 100 мМ раствора 2-имунотилана (в 100 мМ HEPES, pH 8,5; 5 мМ ЭДТУК). Через час при 37oC раствор фильтруют на сефадексе Г-25 (колонка размером 14 х 130 мм; элюент: 30 мМ буфера ацетата натрия с pH 5,0).
Получают 0,20 мкмоль модифицированного гистона H4, содержащего 0,20 мкмоль свободных меркаптогрупп.
в) Получение конъюгата трансферина и гистона H4
Реакцию продуктов стадий (а) и (б) осуществляют аналогично примеру 1 (в), причем трансферин используют в количестве 0,75 мкмоль. Полученный в результате хроматографии продукт подвергают диализу с применением буфера 25 мМ HEPES, pH 7,3, содержащего 300 мМ хлористого натрия. Получают конъюгат, состоящий из 85 нмоль трансферина и 85 нмоль гистона H4.
Пример 5. Получение комплексов конъюгатов трансферина и поликатиона с ДНК
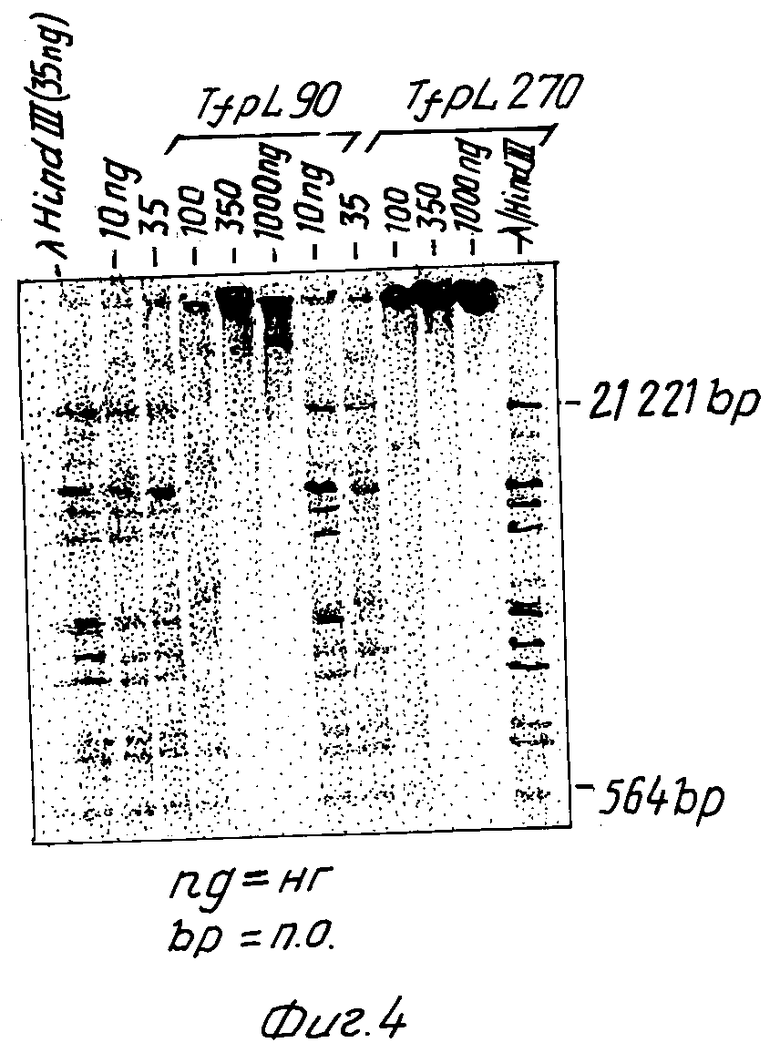
Комплексы получают в результате того, что разбавленные растворы ДНК (30 мкг/мл или меньше) смешивают с конъюгатами трансферина и поликатиона. Для предотвращения осаждения комплексов применяют не содержащий фосфата буферный раствор (фосфаты снимают растворимость конъюгатов). Связывание ДНК с конъюгатами в физиологических ионных условиях подтверждается результатами опыта по определению скорости миграции в агарозном геле с применением на 3-конце 32 р-меченной λ- ДНК, разрезанной при помощи EcoR1/Hind 111 (см. фиг. 4). К каждой пробе с 1 мкл (35 нг) ДНК добавляют 3 мкл 100 ммоль буферного раствора HEPES с pH 7,9, содержащего 1 моль хлористого натрия, и пробы смешивают с возрастающими количествами (10 - 1000 нг) конъюгатов трансферина и поликатиона в 11 мкл водного раствора, что дает конечную концентрацию хлористого натрия 200 ммоль. Электрофорез на 1%-ном агарозном геле с применением буфера 1 x TAE осуществляют при 50 В (45 мА) в течение 2,5 ч; гель сушат с последующей авторадиографией в течение 2 ч при -80oC с применением пленки XAP.
Пример 6. Перенос конъюгатов и полилизина в живые клетки.
Для подтверждения того, что конъюгаты трансферина и полилизина по примеру 1 эффективно вносятся в живые эритробласты, применяют FITC-меченые конъюгаты. Известно, что FITC-меченый трансферин после нескольких часов инкубации с эритробластами, которые предварительно были лишены трансферина, обнаруживается в пузырьках внутри клетки (исследование с флуоресцирующим микроскопом).
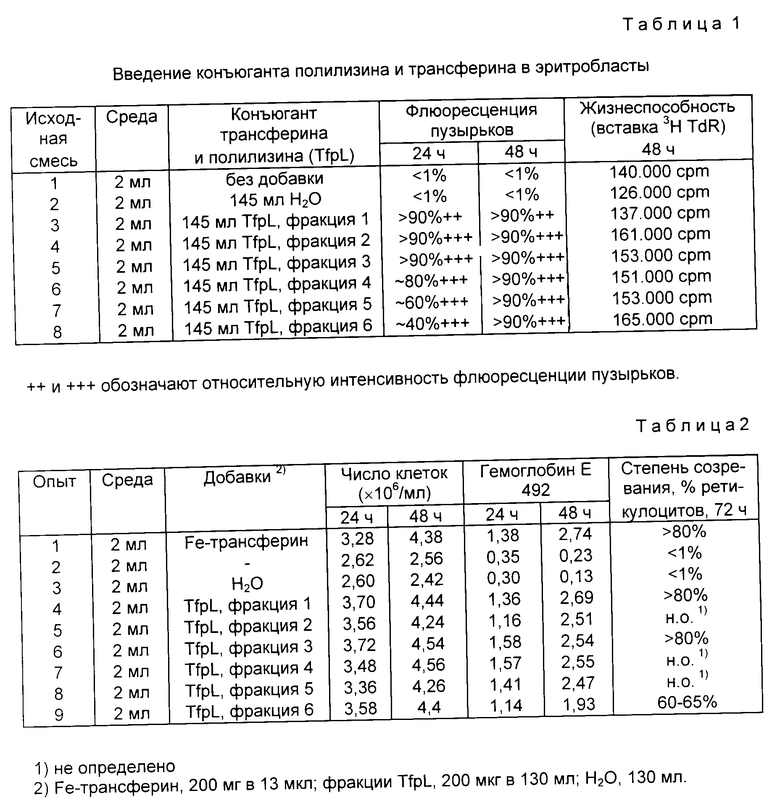
В настоящем примере эритробласты (трансферированные ретровирусом рецептора эпидермального фактора роста (далее EFG)) инкубируют 18 ч в не содержащей трансферина среде для дифференцирования по Ценке и др. (Cell 52, 1988, с. 107-119) при 37oC (концентрация клеток 1,5 • 106/мл). После добавки различных конъюгатов трансферина (или, как контроль, соответствующего количества бидистиллированной воды) клетки инкубируют при 37oC в присутствии 10 нг/мл EGF (чтобы поддерживать трансформированное состояние). После 24 и 48 ч отбирают около 5 • 105 клеток, промывают 1 раз в содержащем фосфатный буфер физиологическом растворе хлористого натрия (далее: раствор PBS, pH 7,2), фиксируют 50-кратным объемом смеси 3,7% формальдегида и 0,02% глутарового альдегида в растворе PBS при температуре 40oC в течение 10 мин, промывают 1 раз раствором PBS, вводят в элванол (=искусственная смола на основе поливинилового спирта) и исследуют в флуоресцирующем микроскопе. Одновременно в других аликвотах различных исходных смесей определяют скорость роста клеток. Для этого отбирают 100 мкл клеточной суспензии и определяют вставку 3H-тимидина (8 мккюри/мл, 2 ч). Из фиг. 5 вытекает, что инкубированные вместе с конъюгатом трансферина и полилизина эритробласты через 24 ч имеют флюоресцирующие пузырьки, которые нельзя обнаружить в контрольных пробах. Табл. 1 показывает, что за исключением фракции 6 все конъюгаты поглощены практически всеми клетками.
Были сделаны снимки флуоресценции куриных эритробластов, которые были инкубированы 24 ч без конъюгатов трансферина и полилизина. При возбуждении синим светом (для обнаружения FITC) можно отчетливо различать несколько флуоресцентных пузырьков в каждой клетке. Специфичность этой флуоресценции дозировалась тем, что флуоресценция пузырьков при возбуждении зеленым светом, при котором можно видеть подобную неспецифическую флуоресценцию клеток, как в случае опыта без конъюгата, не появлялась.
Тот факт, что клетки во всех пробах растут одинаково быстро (как измерено вставкой тритированного темидина (далее 3H TdR; см. табл. 1), доказывает, что клетки не повреждаются конструктами и тем самым исключено неспецифическое поглощение (например, через ставшие проницаемыми оболочки клеток).
Пример 7. Опыты направлены на подтверждение того, что предлагаемые конъюгаты трансферина и полилизина используются клеткой как нативный трансферин, т. е. нормальный цикл трансферина проходит с подобной эффективностью. В качестве тест-системы для этого особенно пригодны эритробласты, которые "отключением" трансформирующего онкогена можно индуцировать для созревания в нормальные эритроциты. Из литературы вытекает, что такие клетки для нормального созревания требуют высоких концентраций комплекса трансферина и железа (100- 200 мкг/мл), концентрации в 3 раза меньше препятствует созреванию клеток и приводят через несколько дней к отмиранию клеток (см. Ковенц и др. 1986, Mod. Trends in Human Leukemia VII, издательство Шпрингер, DE, с. 199-209). Кроме того, известно (см. Шмидт и др. Cell 46, с. 41-51, 1986), что "рециркуляция", т.е. повторное применение рецепторов трансферина и тем самым протекающий с оптимальной скоростью цикл трансферина необходим для нормального в пробирке дифференцирования.
Эритробласты (трансформированные ретровирусом рецептора EGF) индуцируют для дифференцирования лишением EGF и добавкой оптимального количества частично очищенного куриного эритропойэтина (не содержащего трансферина; далее EPO). Инкубацию осуществляют при концентрации клеток 1 • 106/мл в не содержащей трансферина среде для дифференцирования при 42oC и 5% CO2. В начале инкубации добавляют или комплекс нативного трансферина и железа (100 мкг/мл) или насыщенные железом конъюгаты трансферина и полилизина концентрация также 100 мкг/мл). Рост и состояние созревания клеток анализируют через 24 и 48 ч следующим образом:
1) определение числа клеток;
2) определение распределения размеров клеток и
3) фотометрическое измерение содержания гемоглобина в клетках.
Кроме того, аликвоты исследуемых смесей центрифугируют через 72 ч в цитоцентрифуге на предметном стекле и подвергают гистохимическому определению гемоглобина (окрашивание нейтральным бензидином и ускоренное окрашивание для клеток крови по Бойч и др., Cell 23, 1982, с. 907-919).
Результаты табл. 2 ясно показывают, что клетки, которые в присутствии фракции 1-5 конъюгатов полилизина и трансферина индуцируются для дифференцирования, так же эффективно и с одинаковой скоростью созревают, что и клетки, которые инкубируют вместе с комплексом нативного трансферина и железа. В противоположность этому, клетки в не содержащих трансферина контрольных пробах показывают сильно замедленный рост и накапливают только небольшие количества гемоглобина. Исследование клеточного фенотипа с применением окрашенных цитоспиновых препаратов показывает, что инкубированные вместе с конъюгатами полилизина и трансферина клетки точно также созревают до поздних ретикулоцитов, как и клетки, обработанные нативным трансферином, в то время как инкубированные без трансферина клетки представляют смесь дезинтегрированных и незрелых, похожих на эритробласты клеток.
Только обработанные фракцией 6 конъюгаты трансферина и полилизина показывают меньшее содержание гемоглобина и больший процент незрелых клеток (табл. 2). Это показывает, что конъюгированная с особенно большим количеством полилизина фракция 6 менее хорошо функционирует в цикле трансферина. Одновременно этот результат указывает и на чувствительность данного опыта.
Пример 8. Подобным образом, как в примере 7, различные конъюгаты трансферина и полилизина и трансферина и протамина исследуют на способность к функциональной замене комплекса нативного трансферина и железа при созревании куриных эритробластов до эритроцитов.
Уже было показано, что терминально дифференцирующие куриные эритробласты требуют оптимально функционирующего цикла трансферина: т.е. без трансферина или при торможении "рециркуляции" рецептора трансферина клетки отмирают. Так как обычно применяемый частично очищенный EPO содержит еще трансферин, его заменяют не содержащим трансферина, частично очищенным эритроидным фактором роста (далее: фактор REV), чтобы сделать возможным эритроидное дифференцирование. В качестве целевых клеток размножают эритробласты, трансформированные ретровирусом, содержащим рецептор человеческого EGF вместе с термочувствительным онкогеном V-myb, причем процесс проводят в среде CFU-E в присутствии 20 нг/мл EGF. Эти клетки стимулируются EGF к нормальному размножению, лишение EGF при одновременной добавке фактора REV способствует тому, что клетки вступают в нормальное дифференцирование. После двукратной промывки в не содержащей трансферина среде клетки высевают в не содержащую трансферин среду и добавляют различные количества насыщенного железом трансферина или конъюгатов трансферина и поликатиона (перед или после их комплексообразования с плазмидной ДНК). Через 1,2 и 3 дня инкубации при 42oC устанавливают состояние дифференцирования клеток цитоцентрифугированием и гистохимическим окрашиванием или количественным определением гемоглобина.
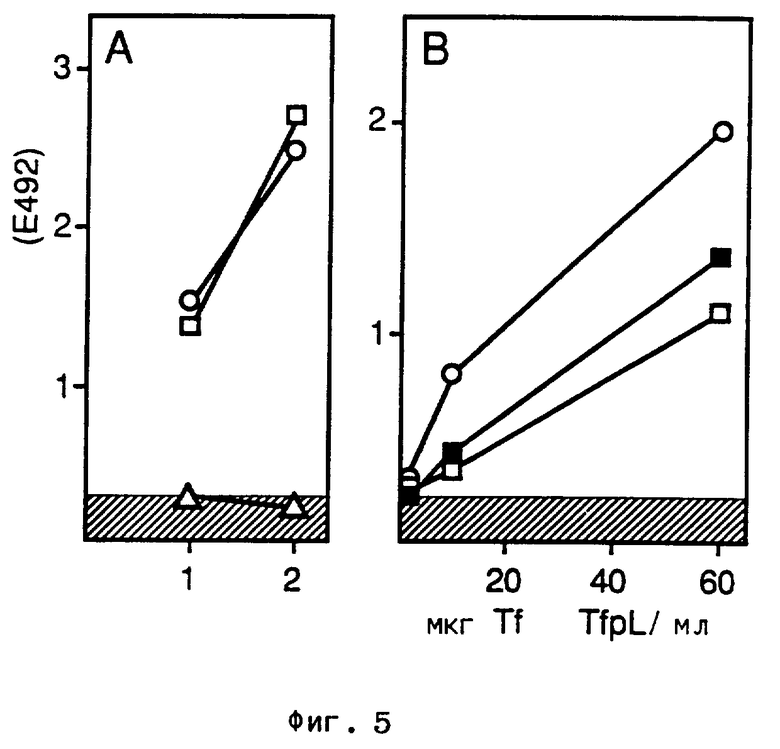
Результаты этих опытов представлены на фиг. 5 и в табл. 3 соответственно.
Клетки (1•106/мл) в несодержащей кональбумина среде для дифференцирования по Ценке, дополненной 1 мкг/мл инсулина и фактором REV, при оптимальной концентрации (разбавление 1:5,000) вносят в чашки диаметром 14 мм. При этом первая проба (треугольники) не имеет добавок, вторая проба (круги) содержит 100 мкг/мл насыщенного железом кональбумина, а третья проба (четырехугольники) содержит 100 мкг/мл насыщенных железом конъюгатов TfpL270. После инкубации в течение 24 и 48 ч измеряют фотометром содержание гемоглобина в аликвотах объемом 100 мкл. Заштрихованная область указывает содержание гемоглобина выращенных в отсутствии трансферина клетках (средняя величина из 4 опытов: фиг. 5А).
Чтобы анализировать эритроидное дифференцирование как функцию концентрации трансферина или концентрации конъюгата трансферина и полилизина, клетки вносят в вышеописанную среду, содержащую указанные количества насыщенного железом кональбумина (открытые круги), конъюгата TfpL90 (открытие четырехугольники) или конъюгата TfpL270 (закрытые четырехугольники), и через 2 дня определяют фотометром содержание гемоглобина (фиг. 5B).
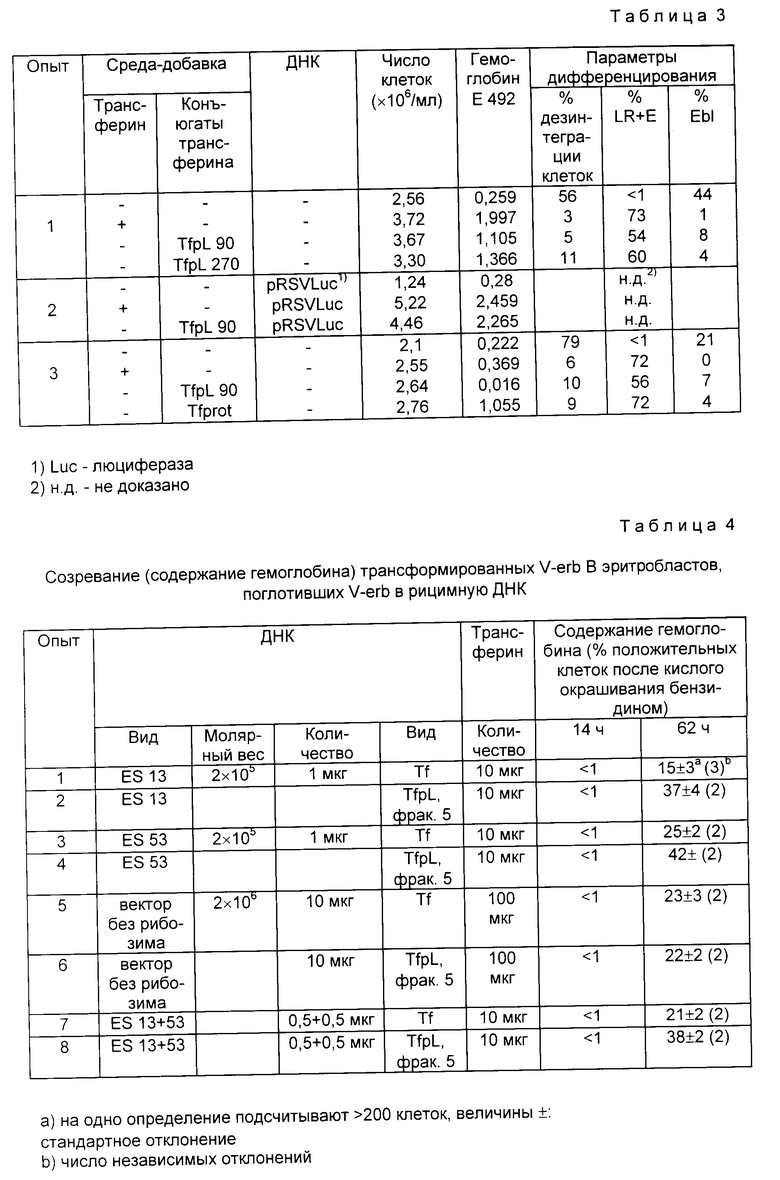
Таблица 3. За эритроидным дифференцированием следят с помощью фотометрического определения гемоглобина (ср. фиг. 5), определения числа клеток или цитоцентрифугирования и последующего нейтрального окрашивания бензидином (для определения гемоглобина) и гистологическими красителями.
Конечные концентрации трансферина и конъюгатов составляют в опыте 1 60 мкг/мл: в опытах 2 и 3 - 100 мкг/мл. Концентрация ДНК в опыте 2 составляет 10 мкг/мл. Число дезинтегрированных клеток, зрелых клеток (LR: поздние ретикулоциты: E: эритроциты) и незрелых клеток (Ebl) определяют по методам, описанным Бойгом и Шмидтом в вышеуказанных литературных источниках. Полученные результаты показывают, что два различных конъюгата трансферина и полилизина (TfpL90 или TfpL270), как и конъюгат трансферина и протамина, способны к функциональной замене нативного трансферина, за счет того, что они гарантируют быстрый перенос железа в дифференцирующие красные клетки, причем их удельная активность в 1,5-2 раза ниже (ср. фиг. 5). Комплексообразование ДНК с конъюгатами трансферина и полилизина 270 и трансферина и протамина не изменяет существенно биологическую активность конъюгатов. В контрольном эксперименте устанавливают, что при добавке полилизина или протамина, смешанного с соответствующим количеством цитрата железа вместо указанных коъюгатов, клетки не могут дифференцировать и отмирают, подобно клеткам в сравнительных пробах, которые инкубируют без трансферина.
В целом, опыты по примерам 7, 8 показывают, что оба вида коъюгатов поликатиона и трансферина переносят железо лишь незначительно менее эффективно, чем нативный трансферин.
Пример 9. Конъюгаты полилизина и трансферина содействуют поглощению ДНК в куриных эритробластах.
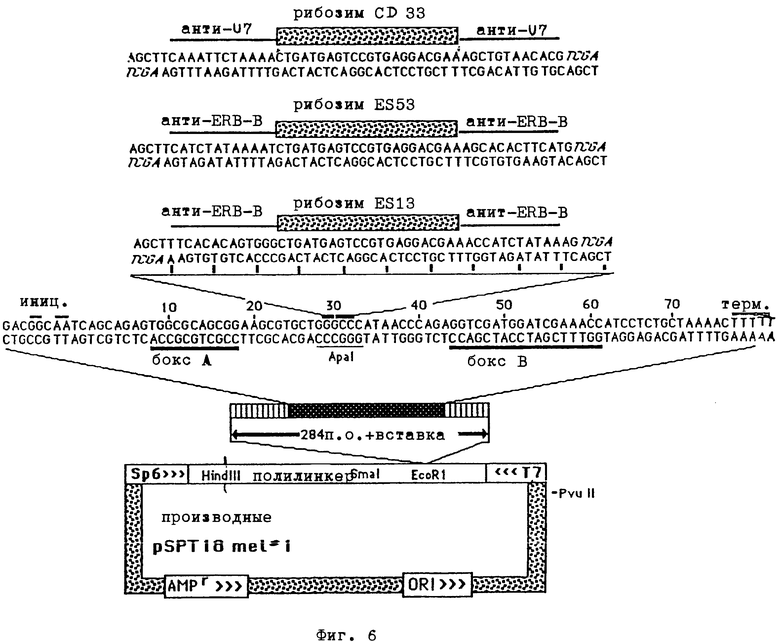
В настоящем примере исследуют вопрос о том, может ли ДНК размером, соответствующим размеру рибоцимов тДНК (ср. фиг. 6), эффективно вноситься внутрь клетки конъюгатом трансферина и полилизина. В настоящем примере применяют тДНК со вставкой последовательности
CGTTAACAAGCTAACGTTGAGGGGCATGATATCGGGCC
CCGGGCAATTGTTCGATTGCAACTCCCCGTACTATAGC,
имеющую молекулярный вес около 300,000 и 32Р АТР концевую маркировку. Приблизительно 0,3 мкг этой ДНК, растворенной в 20 мкл буфера ТЕ, смешивают или с 10 мкг нативного трансферина, растворенного в 50 мкл бидистиллированной воды, содержащей 400 мкг/мл сывороточного альбумина крупного рогатого скота, или с 10 мкг фракции 3 конъюгата трансферина и полилизина, растворенной в 50 мкл бидистиллированной воды, содержащей 400 мкг/мл сывороточного альбумина крупного рогатого скота, или с 50 мкл указанного растворителя без трансферина. Полученные смеси добавляют к 2 мл не содержащей трансферина среде для дифференцирования, к которой добавляют 4•106 куриных эритробластов, трансформированных ретровирусом рецептора EGF и предварительно инкубированных в не содержащей трансферина среде в присутствии EGF, после чего смеси инкубируют 8 ч при 37oC и 5% CO2. После этого клетки центрифугируют, отбирают надосадочную жидкость и промывают клетки 3 раза в не содержащей трансферина среде. Клеточный осадок и питательную среду поглощают в среде, содержащей 1% SDS, 1 мг/мл протеиназы K, 300 ммоль хлористого натрия, 20 ммоль трис с pH 8,0, 10 ммоль ЭДТУК (далее: буфер PK/SDS), инкубируют 30 мин при 37oC, экстрагируют смесью фенола и хлороформа и выделяют ДНК путем осаждения этанолом. Выделенную ДНК с радиоактивностью всего 2000 cpm разделяют на неденатурирующем 3,5%-ном акриламидном геле (с применением буфера TBE), и ДНК доказывают авторадиографией. При этом обнаруживают, что в обработанной конъюгатом трансферина и полилизина клеточной пробе поглощено клетками приблизительно в 5-10 раз больше ДНК, чем в контрольных пробах с нативным трансферином.
Пример 10. Конъюгаты полилизина и трансферина содействуют поглощению и экспрессии плазмидной ДНК в куриных эритробластах
В этих опытах применяют плазмидную ДНК, содержащую ген люциферазы Photinus pyralis в качестве гена-репортера, чтобы исследовать перенос гена и экспрессию. Для этого плазмидную ДНК pRSVluc, получаемую традиционным лизисным методом с применением тритона X с последующим градиентным центрифугированием, осуществляемым с применением хлористого цезия и бромистого этидия, обесцвечиванием бутанолом-1 и диализом относительно 10 ммоль буфера трис/HCl c pH 7,5, содержащего 1 ммоль ЭДТУК. Для комплексообразования по 10 мкг коньюгата трансферина и полилизина (далее конъюгат TfpL) или коньюгата трансферина и протамина (далее коньюгат Tfprot) медленно добавляют при осторожном перемешивании к 3 мкг плазмидной ДНК pRSVluc в 250 мкл 0,3 молярного хлористого натрия. (Было установлено, что при сохранении этих условий можно применять до 100 мкг коньюгата трансферина и поликатиона и 30 мкг плазмидной ДНК в конечном объеме 500 мл, без осаждения комплексов коньюгата с ДНК). После 30 мин при комнатной температуре комплексы добавляют к 5 - 10 • 106 клеток HD 3 (0,5 - 1 • 106 клеток на 1 мл, среда EBM + H, 37oC, 5% CO2) и инкубируют в течение 16-48 ч (в качестве клеточной линии применяют трансформированную ts-v-erb B клеточную линию HD3 куриных эритробластов). Клетки собирают (5 мин при 1500 х g, 4oC), дважды промывают фосфатным буферным солевым раствором (далее буфер PBS) и поглощают в 100 мкл 0,25-молярного трис/HCl с pH 7,5. Клеточные экстракты получают 3 циклами замораживания и оттаивания с последующим высокоскоростным центрифугированием (15 мин, 18000 х g, 4oC). Аликвоты таких клеточных экстрактов люминесценцией исследуют на наличие активности люциферазы.
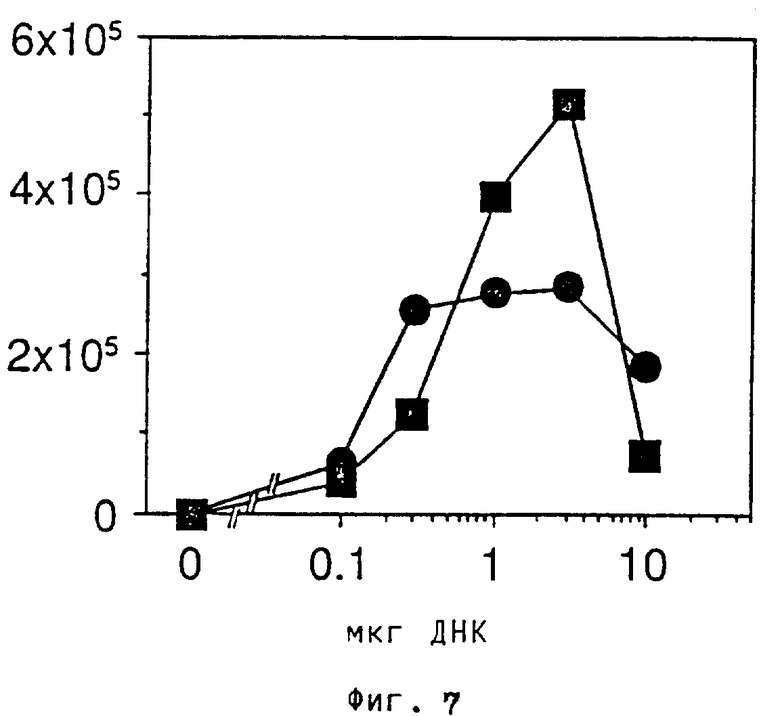
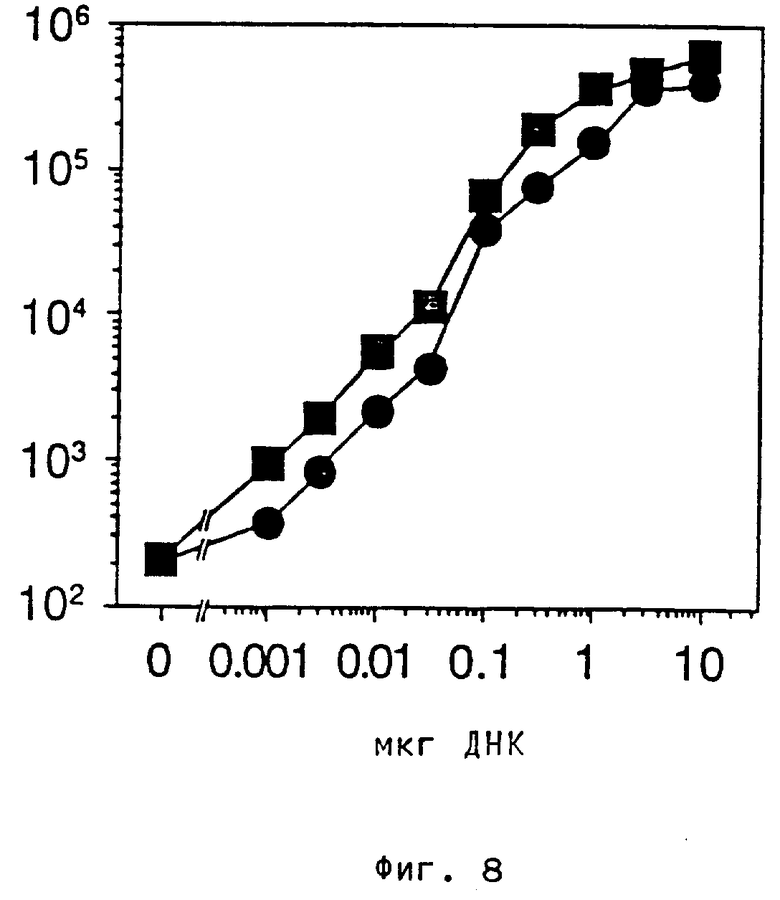
Было установлено, что присутствие комплекса конъюгата трансферина и поликатиона с ДНК в питательной среде не оказывает вредного влияния на рост клеток и на размножение клеток. Как видно из фиг. 8, достигают максимальной активности люциферазы, если применяют 3 мкг ДНК /10 мкг TfpL и 0,3 - 1 мкг ДНК /10 мкг Tfprot. Предполагая, что все образованные комплексы конъюгатов с ДНК являются идентичными, это соответствует молярному соотношению 25 или 75 молекул конъюгата на молекулу плазмидной ДНК. Отсюда моно заключить, что ДНК в комплексе целиком связана с молекулами конъюгата, а именно при соотношении конъюгата и ДНК, которое, очевидно, обеспечивает электронейтральность (в пересчете на положительные заряды в поликатионе, требуемые для нейтрализации отрицательных зарядов фосфатных групп в ДНК).
Это предположение совпадает с тем наблюдением, что по сравнению с конъюгатом трансферина и полилизина требуется в три раза больше менее сильно положительно заряженного конъюгата трансферина и протамина для оптимального комплексообразования и переноса гена. Это предположение совпадает также с полученным в примере 5 результатом для соотношения конъюгата и ДНК, которое требуется для эффективного комплексообразования.
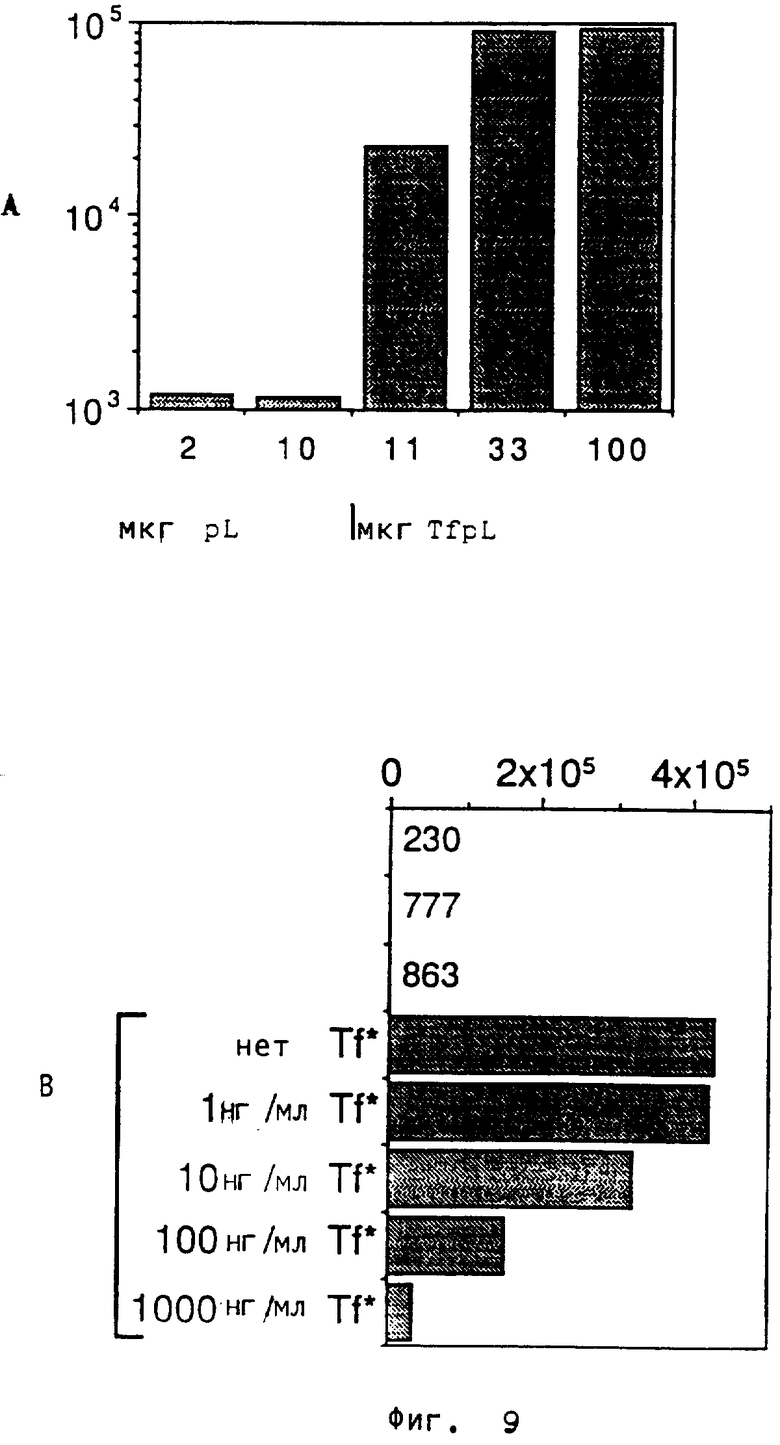
При применении оптимированного таким путем соотношения конъюгата TfpL и ДНК для комплексообразования определяют чувствительность этой системы переноса гена. Результат этих опытов показан на фиг. 8: менее чем 1 нг кодирующей люциферазу плазмидной ДНК еще показывает обнаруживаемый сигнал. Применение более чем 2 мкг плазмидой ДНК в виде комплекса с 6 мкг TfpL или 20 мкг Tfprot не приводят к дальнейшему росту активности люциферазы, по всей вероятности, ввиду насыщения системы. Далее установлено, что для комплексообразования не требуется особой концентрации соли или ионов, так как комплексы TfpL и ДНК, которые образуются при различных концентрациях соли (0, 20, 50, 100, 200 ммоль NaCl) в экспериментах одинаково эффективны (фиг. 7,8: круги = комплекс конъюгата Tfprot и ДНК, а четырехугольник = комплекс конъюгата TfpL и ДНК). Показано, что прием клетками комплексов конъюгата трансферина и поликатиона с ДНК протекает через рецептор трансферина. Сначала, как показано на фиг. 9A, установлено, что достигаемая комплексами конъюгата TfpL и ДНК активность люциферазы по меньшей мере в 100 раз выше, чем активность, которую измеряют для комплексов полилизина и ДНК. Сравнительный опыт показал, что одна смесь полилизина и трансферина не облегчает поглощение клеткой плазмидной ДНК. В дальнейшем опыте к постоянному количеству комплекса конъюгата TfpL и ДНК добавляют избыток нативного трансферина. Фиг 9B показывает, что содержащийся в среде свободный трансферин эффективно конкурирует с конъюгатом TfpL, обеспечивающим перенос ДНК в клетку, о чем свидетельствует снижение активности люциферазы. Отсюда можно заключить, что поглощение клеткой комплекса конъюгата TfpL с ДНК через рецептор трансферина.
Пример 11. В предварительных опытах на основании трансфекции куриных фибробластов посредством erb B ДНК ES установлено, что рибоцим т-ДНК ES экспримируется в куриных клетках.
При помощи этого примера можно показать, что рибоцимы с т-ДНК, которые направлены против erbB онкогена, могут вносится в трансформированные erbB куриные эритробласты и ослаблять трансформирующее действие онкогена.
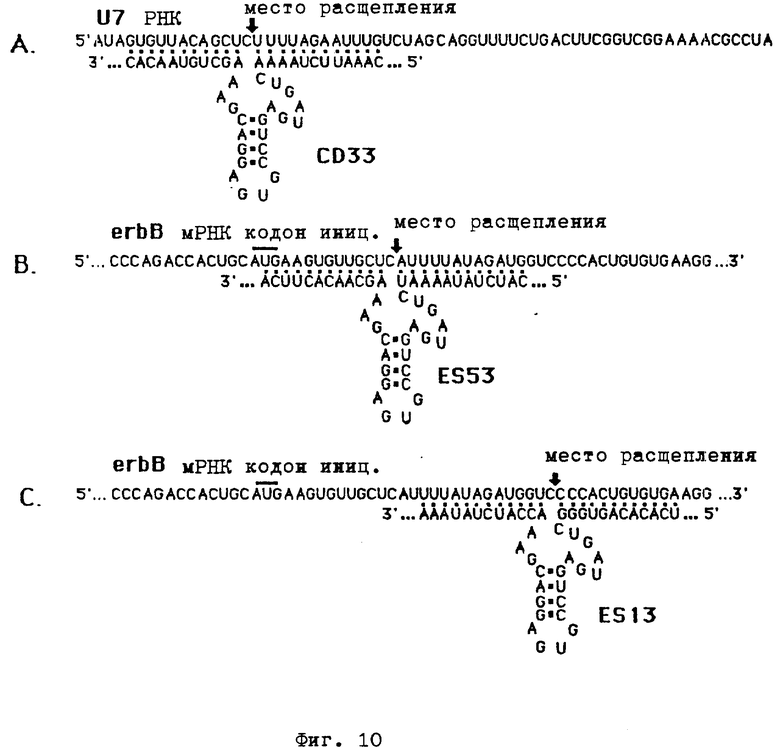
Конструируют (ср. фиг. 6, 10) два рибозимных гена с т-PHK, направленных против трансляционной иницирующей области erbB. Около 100 мкг каждой содержащей ген плазмиды переваривают EcoPI, чтобы высвободить рибоцимный ген с т-PHK на фрагменте длиной 325 п. о. Продукты переваривания маркируют на концах фрагментом Кленова и очищают при помощи электрофореза на 2%-ном агарозном геле с применением буфера TBE. Векторный фрагмент и фрагменты рибозимного гена с т-PHK локализуют окрашиванием бромидом этидия, вырезывают и выделяют электроэлюацией, экстракцией смесью фенола и хлороформа и хлороформом и осаждением этанолом. При использовании предлагаемого конъюгата трансферина и полилизина очищенные, радиоактивно маркированные фрагменты ДНК применяют для определения поглощения и торможения erb B-PHK. В качестве контрольной ДНК применяют вектор pSPT 18.
В качестве тест-клеточной системы выбирают клеточную линию куриных эритробластов, трансформированную термочувствительным мутантом (ts 34) вируса AEV эритробластоза птиц.
Так же экспримируемый в этих клетках erbA онкоген можно тормозить специфическим ингибитором протеинкиназы (ингибитор H 7). Установлено, что v-erb A онкоген в живом организме и в пробирке (т.е. как бактериально экспримированный протеин) в двух местах, а именно Ser 28 и Ser 29, фосфорилируется протеинкиназой C или зависящей от сАМР протеинкиназой. Мутация этих серинов до аланинов препятствует фосфорилированию и снимает активность v-erb A онкогена. H 7 представляет специфический ингибитор этих обеих киназ, который в содержащих v-erbA и v-erbБ эритробластах может избирательно снимать вызываемые v-erbА изменения (например, блокаду дифференцирования).
Известно, что эритробласты, erb B-онкоген которых инактивируют, например, повышением температуры в случае термочувствительного erb B-мутанта, индуцируются для созревания до эритроцитов.
Одним из первых признаков для этого процесса является индукция синтеза гемоглобина, который можно доказать чувствительным анализом (кислое окрашивание бензидином) на уровне индивидуальной клетки. Как фенотипное действие направленного против erb B рибозима в этой тест-системе можно было бы, следовательно, ожидать специфического повышения числа бензидин-положительных клеток.
Лежащую в основе этого примера серию опытов проводят следующим образом: различные препараты ДНК (см. выше и табл. 4), растворенные в 30 мкл буфера TE, смешивают соответственно с 10 мкг комплекса нативного трансферина и железа и конъюгата трансферина и полилизина (растворенного в бидистиллированной воде) и инкубируют 30 мин при 37oC.
В случае векторной ДНК (10 мкг) применяют соответственно больше (100 мкг) препаратов трансферина. Исходные смеси добавляют к 1 мл не содержащей трансферина среды для дифференцирования по Ценке. Тест-клетки (3•106 в каждом опыте) инкубируют перед опытом 60 мин в не содержащей трансферина среде для дифференцирования при 42oC (этот прием позволяет улучшать поглощение трансферина) и добавляют к содержащим ДНК и трансферин исходным смесям. Через 6, 18 и 68 ч (обработку клеток см. ниже) отбирают пробы, которые описанным выше образом разделяют на надосадочную жидкость и клеточный осадок, поглощают в буфере PK/SDS и анализируют ДНК.
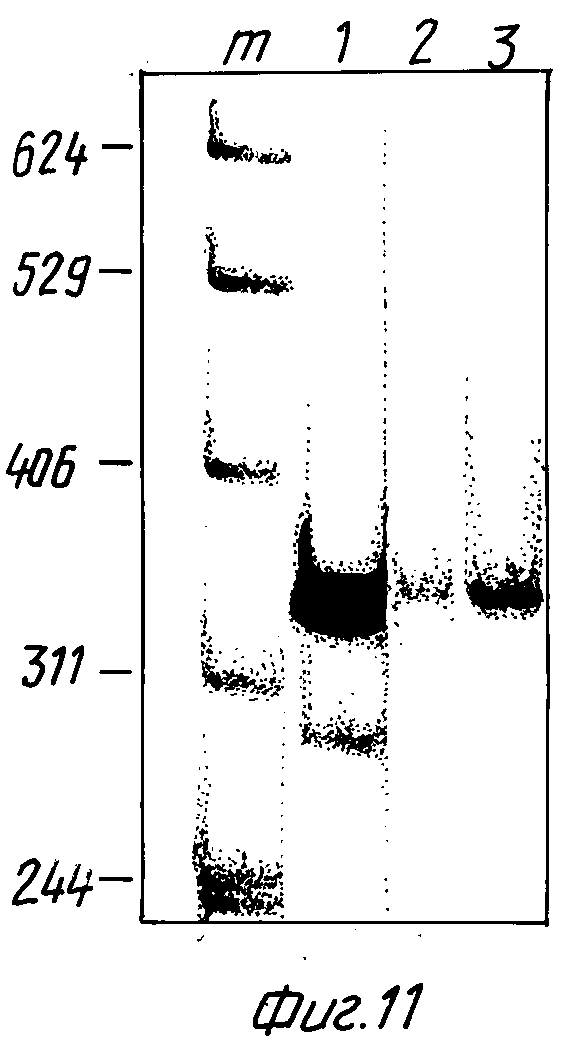
Фиг. 11 показывает, что аналогично примеру 8, в обработанной конъюгатом трансферина и полилизина пробе клетками поглощается приблизительно в 5 - 10 раз больше ДНК, чем в контрольных пробах с нативным трансферином.
След m: маркер молекулярного веса: ДНК pBP322, расщепленная Hpa11 и с применением фрагмента Кленова ДНК полимеразы радиоктивно маркированная альфа - 32P-СТР.
След 2: клетки, отработанные комплексом трансферина и ES13.
След 3: клетки, отработанные комплексом конъюгата трансферина и полилизина с ES 13.
После окончания инкубация (6 ч) клетки центрифугируют и инкубируют еще 2 ч в содержащей трансферин среде для дифференцирования, содержащей эритропоиетин и инсулин (2мл на исходную смесь и при 37oC, т.е. в присутствии активного v - erb B протеина).
Получают следующие результаты:
1. Подобно примеру 8, можно наблюдать усиленное поглощение ДНК в размере ДНК ES в обработанных трансферином и полилизином клеточных пробах (приблизительно в 5 раз).
2. Табл. 4 показывает, что во всех случаях, в которых ДНК ES вносят в erb B трансформированные эритробласты с помощью конъюгата полилизина и трансферина, процент бензидинположительных клеток значительно повышен, приблизительно в 2 раза, (в качестве эталона служат пробы, которые обработаны векторной ДНК и в которых применение конъюгатов полилизина и трансферина, как и следовало ожидать, не приводит к повышению числа бензидин-положительных клеток).
Пример 12. Эффективное связывание и интернализация комплексов конъюгата трансферина и полилизина с ДНК в гематопойетических куриных клетках.
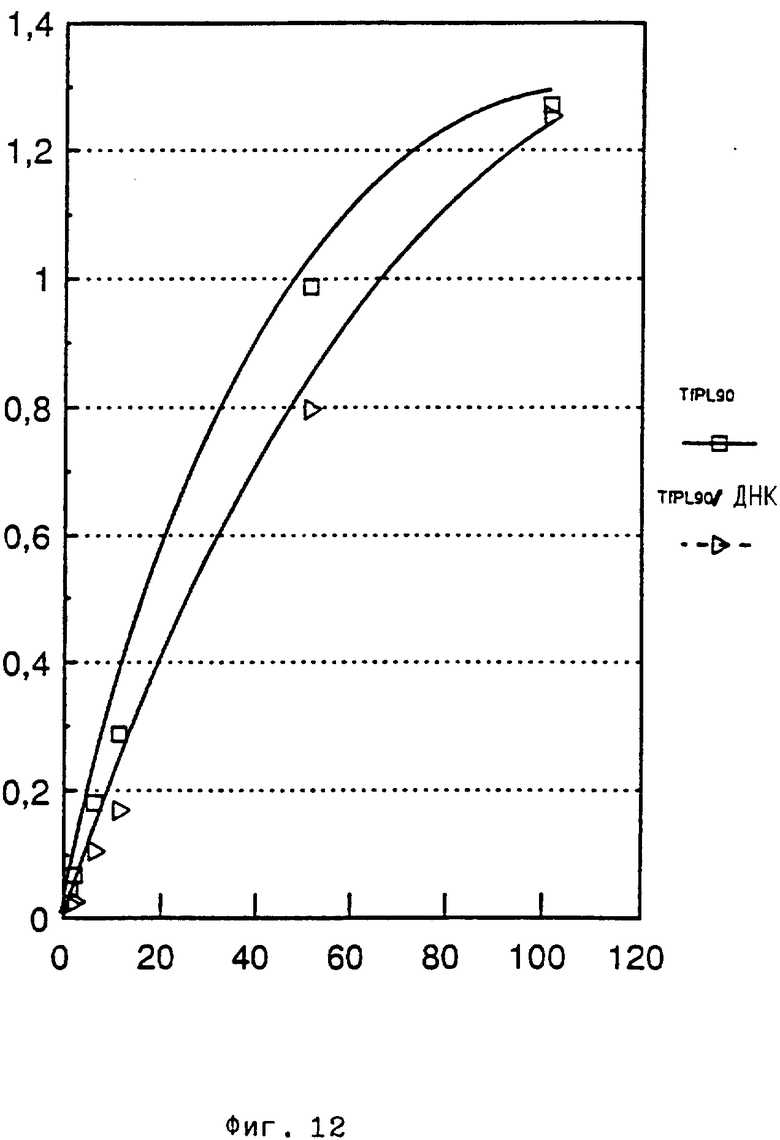
Связывание конъюгата TfpL и комплекса конъюгата TfpL с ДНК с рецепторами на поверхности клеток измеряют при помощи меченных тритием веществ по методу, описанному Штейном и др. , 1984, J. Biol. Chem. 259, 14762-14772. 3H-меченый конъюгат TfpL получают конъюгацией меченого полилизина с трансферином по описанному в примере 1 методу. Маркировку полилизина 90 осуществляют обработкой формальдегидом и 3H-меченым бораном натрия.
Результат этих опытов представлен на фиг. 12. Меченый конъюгат TfpL 90 (четырехугольник) или меченый конъюгат TfpL 90 в виде комплекса с ДНК PB-SK-, получаемого при помощи лизиса с применением тритона X, центрифугирования в равновесных условиях при соблюдении градиента плотности, применяя хлористый цезий и бромид этидия, обесцвечивания 1-бутанолом и диализа относительно 10 ммоль буфера трис/HCl с pH 7,5, содержащего ЭДТУК, (треугольник) исследуют на их специфическое связывание с рецептором трансферина клеток HD3. Для этого добавляют конъюгаты или комплексы (0,1 - 100 нмоль) к клеткам HD3 (1•106/мл в среде МЕМ (= Eagle's Minimum Medium), содержащей 1% альбумина сыворотки крупного рогатого скота, и инкубируют 3 ч. Фиг. 12 показывает, что как конъюгаты, так и комплексы связываются с клетками HD3 таким образом, что происходит насыщение. Вычисленные из этих данных мнимые константы связывания составляют 22 нМ для конъюгата TfpL и 43 нМ для комплекса конъюгата TfpL с ДНК немного выше, эти величины относительно хорошо совпадают с величинами для нативного трансферина (15 нмоль).
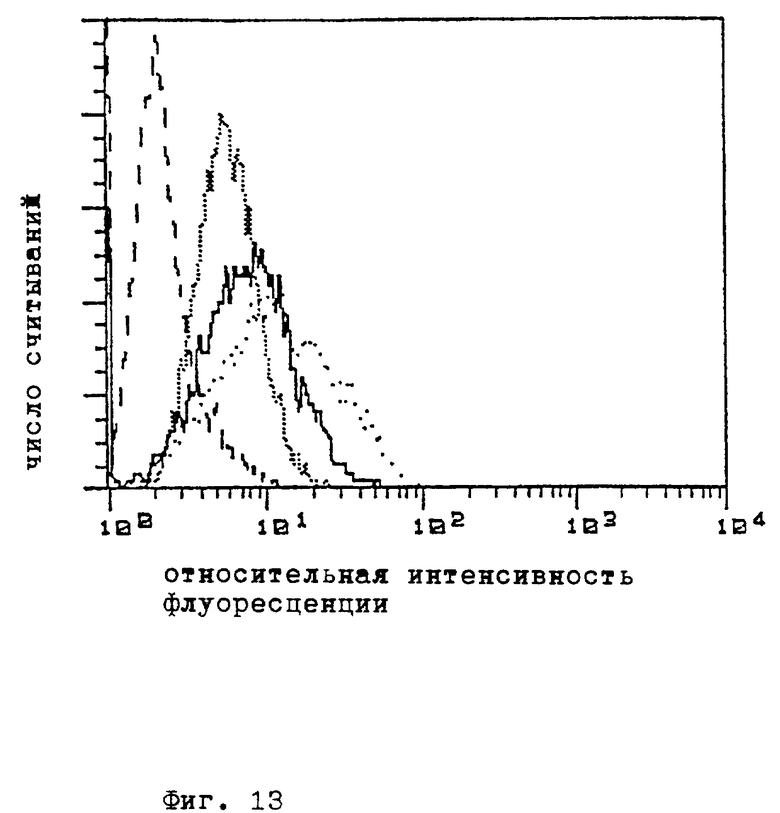
Для определения поглощения комплекса конъюгата TfpL с ДНК во внутриклеточных пузырьках сначала инкубируют клетки HD3 в не содержащей трансферина среде для дифференцирования при 37oC в течение 18 ч. После добавки меченого FITC трансферина или конъюгатов TfpL (меченых FITC на полилизине, образующих в некоторых экспериментах комплексы с ДНК) инкубируют клетки еще 18 ч. Клетки цитоцентрифугируют, обрабатывают смесью 3,7%-ного формальдегида и 0,02%-ного глутарового альдегида, промывают буфером PBS, подают в мовиол 4,88 (поливиниловый спирт) и исследуют в флюоресцентном микроскопе. В качестве контроля применяют меченое FITC антитело козы - антимыши (0,1 мг/мл) (ср. пример 6). Для количественного определения FITC-Tf, FITC-TfpL и FITC-TfpL/ДНК клетки в течение 6 ч инкубируют вместе с соответствующим препаратом Tf: 40 мкг/мл; конъюгат TfpL 270; 50 мкг/мл; комплекс конъюгата TfpL270 с ДНК pB-SK-, получаемый при помощи лизиса с применением тритона X, центрифугирования в равновесных условиях при соблюдении градиента плотности, применяя хлористый цезий и бромид этидия, обесцвечивания 1-бутанолом и диализа относительно 10 ммоль буфера трис /HCl с pH 7,5, содержащего 1 ммоль ЭДТУК в 50 мг/мл или 16 мг/мл буфера связывания, промывают 3 раза холодным буфером PBS, содержащим альбумин сыворотки крупного рогатого скота, и подвергают количественному анализу, аминокислотных последовательностей с помощью прибора Бектона/Дикинсона. Фиг. 13 показывает, что как с TfpL, так и с TfpL-ДНК все клетки имеют более чем в 10 раз повышенную относительную флюоресценцию, что указывает на то, что конъюгаты или комплексы поглощаются более чем 95% клеток (Tf: ...; TfpL: ...; TfpL/ДНК: ___; буфер связывания: ---).
Пример 13. Экспрессия ДНК, которая вносится в клетку при помощи конъюгата TfpL.
В предшествующих примерах доказано, что перенос гена посредством конъюгата TpL отрицательно не влияет на рост клеток. В данном же примере исследуют действие комплексов конъюгата TfpL с ДНК, которыми продолжительное время обрабатывают клетки (в качестве ДНК применяют плазмидную ДНК, содержащую ген люциферазы; см. пример 10). В этом опыте одинаковую концентрацию клеток HD3 инкубируют 1-4 дня с ежедневным дополнением комплекса конъюгата TfpL с ДНК или без ежедневного дополнения.
В различные промежутки времени аликвоты исследуют на активность люциферазы описанным в примере 10 образом. В культурах с повторной добавкой комплексов измеряют относительно высокую величину экспрессии гена люциферазы (от 100.000 до 200.000 световых единиц/107 клеток), которая в течение всего периода исследования, где не наблюдают никаких цитотоксических действий, остается в основном постоянной. Если клетки только один раз нагружают комплексами, то активность люциферазы между 2-м и 4-м днем снижается в 10-20 раз. Эти результаты показывают, что несмотря на очевидно проходящую экспрессию гена люциферазы, вносимого в клетку с помощью предлагаемых конъюгатов, повторной добавкой можно сохранять постоянно высокую экспрессию вводимого гена.
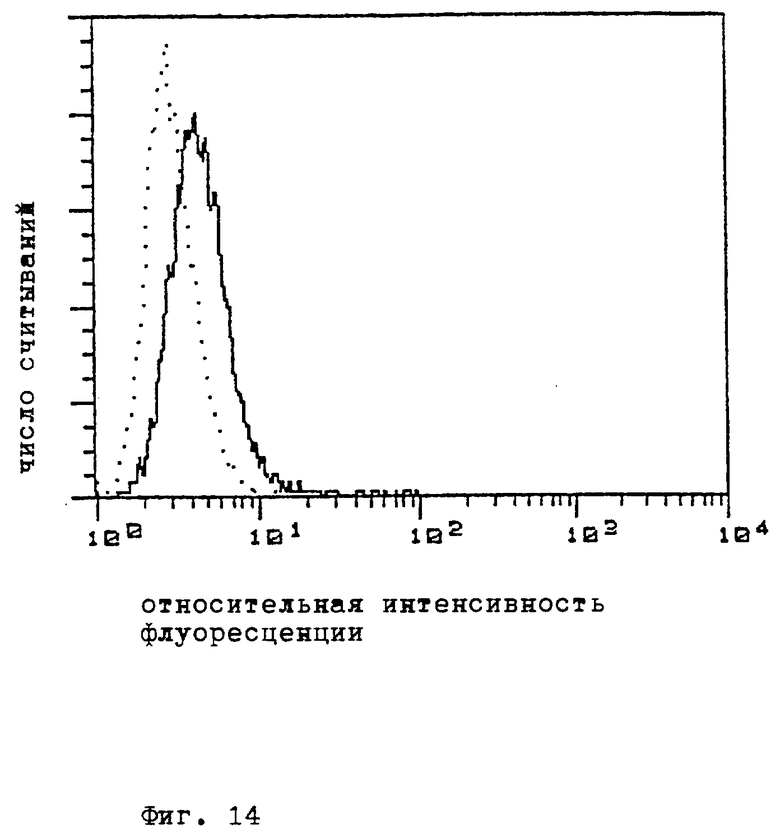
Пример 14. Для определения количества клеток, которые действительно экспримируют плазмидную ДНК, вводимую инфекцией трансферином, клетки HD3 инкубируют вместе с комплексами конъюгата TfpL с ДНК описанным в предыдущих примерах образом. В качестве ДНК применяют плазмидную ДНК pRSV- β Gal (_____ __). Экспрессию этого гена-репортера исследуют затем в отдельных клетках при помощи анализа аминокислотной последовательности согласно Нолану и др., Proc.NatI.Acad.Sci.85, 1986, 2603-2607.
В качестве контроля применяют комплекс конъюгата TfpL с ДНК pB-SK- (... ).
Для этого флюоресцирующее вещество, флуоресцеин-ди-β d-галактопиранозид (далее FDG), вводят посредством осмотического шока и исследуют распределение клеток, которые содержат флуоресцеин, который в результате энзиматической активности высвобождается из FDG. Равномерное распределение содержащих флуоресцеин клеток допускает вывод о том, что большое количество клеток экспримирует ген-репортер β Gal. Результат этих опытов показан на фиг.14.
При стимулировании индуцированного в пробирке созревания эритробластов конъюгат полилизина и трансферина может функционально заменять нормальный трансферин.
Пример 15. Получение конъюгатов трансферина и полилизина.
Раствор 102 мг (1,28 мкмоль) трансферина человека (не содержащего железа) в 3 мл 30 ммольного буфера ацетата натрия с pH 5 подвергают гель-фильтрации на колонке Сефадекс Г-25. Получают 3,8 мл раствора, который охлаждают до 0oC, после чего добавляют 80 мкл 30 ммольного буфера ацетата натрия с pH 5, содержащего 4 мг (19 мкмоль) периодата натрия. Получаемую смесь оставляют стоять в темноте на ледяной бане в течение 90 мин. Для удаления низкомолекулярных продуктов осуществляют дальнейшую гель-фильтрацию на вышеуказанной колонке. При этом получают раствор, содержащий примерно 82 мг (1,03 мкмоль) окисленного трансферина (содержание трансферина определено путем абсорбции ультрафиолетовыми лучами при 280 нм и осуществления анализа с помощью нингидрина). Для доказательства окисленной формы, которая содержит альдегиды и при взаимодействии с анисовым альдегидом приводят к цветной реакции, пробы каплями подают на тонкослойную силикагельную пластинку, после чего сушат, пластинки погружают в смесь п-анисового альдегида, серной кислоты и этанола в соотношении 1: 1: 18, сушат и нагревают. Раствор окисленного трансферина быстро (в течение 10 - 15 мин) добавляют к раствору, содержащему 0,50 мкмоль меченного флуоресценцией полилизина, имеющего среднюю длину цепи 300 лизиновых мономеров (получаемого взаимодействием 34 мг гидробромидной соли с 130 мкг изотиоцианата флуоресцеина в буфере бикарбоната натрия pH 9 и последующей гель-фильтрацией) в 4,5 мл 100 мМ ацетата натрия с pH 5 при интенсивном размешивании. Через 20 мин величина pH раствора доводится до 7,5 путем добавления 1 М буфера бикарбоната натрия. К получаемой смеси за 4 ч каждый час добавляют по 9,5 мг (150 мкмоль) цианоборана натрия. Через 18 ч добавляют 1,9 л 5 М хлористого натрия с тем, чтобы довести раствор до общей концентрации примерно 0,75 М. Реакционную смесь подают на катионообменную колонку марки Моно S HR 10/10 и фракционируют при градиенте 0,75-2,5 М хлористого натрия с постоянным содержанием 25 мМ HERES pH 5,3. Высокая концентрация соли при нагрузке колонки и с начала осуществления градиента является существенной для получения желаемых конъюгатов. Несколько трансферина (примерно 30%) вместе со слабой флуоресцентной активностью элюируют при проходе. Основное количество меченного флуоресценцией конъюгата элюируют при солевой концентрации между 1,35 М и 1,9 м. После двухкратного диализа с применение 2 л 25 ммольного буфера HERES с pH 7,3 последовательно получают первую фракцию, содержащую конъюгат трансферина и полилизина в мольном соотношении 3:1 (далее TfpL 300 А), вторую фракцию, содержащую конъюгат трансферина и полилизина в соотношении 2,3:1 (далее TfpL 300 Б), и третью фракцию, содержащую конъюгат трансферина и полилизина в мольном соотношении 1 : 1,3 (далее TfpL В). Общий выход составляет 50% в пересчете на трансферин и 62% в пересчете на полилизин. Получаемые конъюгаты можно хранить в не содержащей железа форме после предварительного быстрого замораживания в среде жидкого азота при -20oC. Перед включением железа пробы (0,5-1 мг) доводят до физиологической солевой концентрации (150 моль) путем добавления хлористого натрия. Включение железа осуществляют путем добавления 6 мкл 10 ммольного буфера цитрата железа (III) (содержащего 200 нмоль цитрата, доведенного до pH 7,8 путем добавления бикарбоната натрия) на мг трансферина. Перед применением для комплексообразования с ДНК железосодержащие конъюгаты распределяют на небольшие аликвоты, которые быстро замораживают и хранят при температуре -20oC в среде жидкого азота или смеси сухого льда и этанола.
Пример 16. Трансфекция эукариотных клеток комплексами ДНК и конъюгатов трансферина и полилизина.
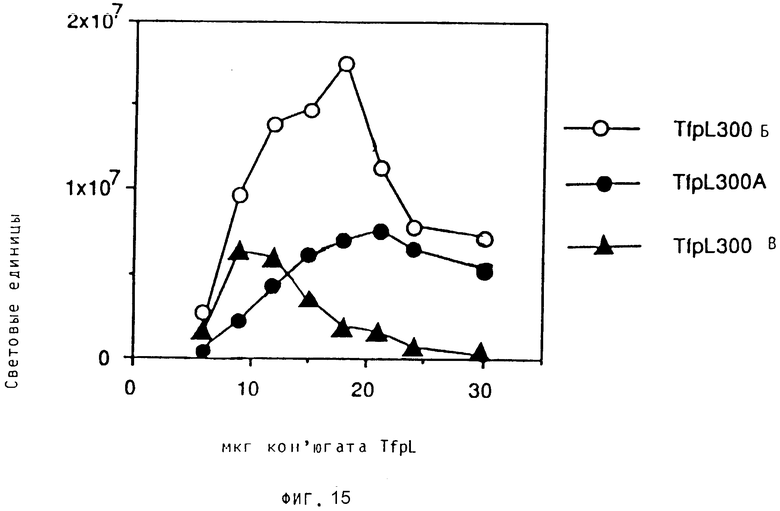
Клетки клеточной линии эритролейкемии K 562 (ATCC CCL 243) в виде суспензии в среде RPMI 1640, содержащей 10% эмбриональной телячьей сыворотки, 100 единиц/мл пенициллина, 10 мг/мл стрептомицина и 2 ммоль глутамина, выращивают до достижения плотности 500000 клеток/мл и затем два раза промывают свежей средой. За 20 ч до трансфекции клетки в количестве примерно 200000/мл подают в свежую среду, содержащую 50 мкмоль дезферриоксима. Перед трансфекцией клетки собирают, в количестве 250000/мл снова подают в свежую среду, содержащую 10% эмбриональной телячьей сыворотки и 50 мкмоль дезферриоксима, и получаемую суспензию подают в чашку, снабженную 24 плюсковидными углублениями (2 мл/углубления). Обработка дезферриоксимом служит для 5-кратного увеличения числа рецепторов трансферина, чем улучшается поглощение ДНК. 6 мкг плазмидной ДНК p-RSVL (содержащей ген люциферазы Photinus pyralis под контролем вируса Rous Sarcoma LTR) в среде 330 мкл буфера HPS (150 ммоль хлористого натрия, 20 ммоль HEPES, pH 7,3), смешивают с конъюгатами TfpL 300 A-B в 170 мкл буфера HPS. Конъюгаты берут в представленных на фиг.15 количествах. Через примерно 30 мин при комнатной температуре 50 мкл смеси добавляют к клеткам K 652 (за 10 мин до добавления комплекса ДНК и конъюгата все клеточные пробы обрабатывают хлорохином до конечной концентрации 100 мкмоль с тем, чтобы тормозить разложение ДНК внутри клетки). После 4-часовой инкубации при температуре 37oC клетки промывают предварительно нагретой свежей средой (без добавки хлорохина) и инкубируют при температуре 37oC. 20 ч после трансфекции клетки собирают и перерабатывают для получения экстрактов, которые исследуют на активность люциферазы. Результаты представлены на фиг.15.
Использование: медицина, ветеринария. Сущность изобретения: путем объединения модифицированного трансферрина с модифицированным полилизином, протамином или гистоном получают конъюгат с молярным соотношением трансферрина и поликатиона от 10,5:1 до 1:4, который после обработки нуклеиновой кислотой дает комплекс, обеспечивающий перенос указанной нуклеиновой кислоты в клетки человека или животных. 15 ил., 4 табл.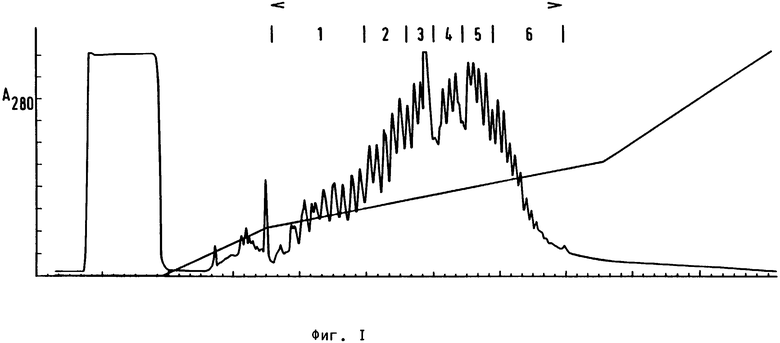
Средство для переноса нуклеиновых кислот или их производных в клетки человека или животных, содержащее поликатион и гликопротеин в виде конъюгата, отличающееся тем, что из поликатионов оно содержит или полилизин, или протамин, или гистон, а из гликопротеинов - трансферрин при молярном соотношении трансферрина и поликатиона от 10,5 : 1 до 1 : 4.
| G.Y.Wu, C.H.Wu, J.Biol | |||
| Chem., т | |||
| Железнодорожный снегоочиститель на глубину до трех сажен | 1920 |
|
SU263A1 |
| Круглый ткацкий станок | 1928 |
|
SU14624A1 |
Авторы
Даты
1998-06-20—Публикация
1992-03-20—Подача