Предлагаемое изобретение относится к органической химии, а именно к способам получения пептидов, в частности, L-глутамил-L-триптофана и его солей, которые могут найти применение в фармацевтической промышленности. L-глутамил-L-триптофан, известный
также под названием "Тимоген" (Временная фармакопейная статья. ВФС N 42-1981-90), является одним из регуляторных пептидов и находит применение, например, в качестве иммуностимулирующего средства для лечения больных с иммунодефицитными состояниями (патент РФ N 1582393, кл. A 61 K 37/02). В отличие от других пептидов, выделенных из тимуса (тималина, тимопоэтинов I и II и др.), тимоген может быть синтезирован химическим путем.
Основой для синтеза L-глутамил-L-триптофана являются глутаминовая кислота
и триптофан
Синтез L-глутамил-L-триптофана обычными методами пептидной химии многостадиен и должен включать стадии защиты γ-карбоксильной и α-аминогруппы глутаминовой кислоты, получение активированного эфира с α-карбоксильной группой глутаминовой кислоты, с которым взаимодействует триптофан, и деблокирование защитных групп и выделением L-глутамил-L-триптофана. При этом индольную группу триптофана в ряде случае также следует защищать [H. Ueba, V. Doi, M. Inoue T. Ishida // Biochem. Biophys. Res. Commun. 1988. Vol. 154, N 1. P. 199-204: H. Iyo, H. Hitoshi, J. Isami, I. Kafuku, M. Doi, M. Inoue T. Ishida // Chem. Pharm. Bull. 1991. Vol. 39, N 1. P. 2483-2486: И.Д. Рябинина, И.В. Мирошниченко, А.А. Ярилин. Иммунология. 1991. N 6. С. 20-23].
Известны также методики проведения отдельных стадий. Так, для защиты α-аминогруппы глутаминовой кислоты берут ее γ-бензиловый эфир, который получают путем этерификации глутаминовой кислоты бензиловым спиртом с последующим гидролизом дибензилового эфира в присутствии солей меди [R.L. Prestidge, D. R.K. Hardino, J.E. Battersby, W.S. Hancock // J. Org. Chem. 1975. Vol. 40, N 22. P. 3287-3288], или бензилированием солей медного комплекса глутаминовой кислоты бензилгалогенидами [R. Ledger, F.H.S. Stewart // Austral. J. Chem. 1965. Vol. 18 N 9. P. 1477-1484; W.A.R. van Heesvijk, M.J.D. Eenink, J. Feijen // Synth. 1982. N 9. P. 744-747].
Обычные методы пептидной химии дорогостоящи, многостадийны и дают низкий процент выхода целевого продукта.
L-глутамил-L-триптофан очень мало растворим в воде и изотоническом растворе хлорида натрия (для растворения взвесь обрабатывают ультразвуком в течение 2 мин) и мало растворим в 0,01 М растворе гидроксида натрия (ВФС 42-1981-90). Обработка ультразвуком приводит к частичному разрушению молекулы L-глутамил-L-триптофана, а 0,01 М раствор гидроксида натрия имеет pH 12; то и другое нежелательно при использовании растворов L-глутамил-L-триптофана в качестве лекарственного препарата.
Наиболее близким по совокупности существенных признаков к заявляемому способу является способ получения L-глутамил-L-триптофана и его мононатриевой соли, включающий стадии: (1) защиты α-аминогруппы глутаминовой кислоты, (2) активации α-карбоксильной группы глутаминовой кислоты путем образования сложного активированного эфира, (3) взаимодействие сложного активированного эфира с триптофаном, (4) отщепления защитных групп от продукта, полученного на стадии (3), гидрированием в присутствии палладиевого катализатора, вещества-донора водорода и гидрокарбоната натрия, (5) выделения целевого продукта [А.П. Ерюхина, С.В. Куликов. Ж. общей химии. 1995. Т. 65, Вып. 10. С. 1735-1738].
Согласно прототипу, на стадии защиты α-аминогруппы глутаминовой кислоты используют глутаминовую кислоту с защищенной γ-карбоксильной группой, полученную из калиевой соли диглутамата меди взаимодействием с бензилбромидом в присутствии триэтиламина; γ-бензиловый эфир глутаминовой кислоты взаимодействует с O-бензилоксикарбонил-N-гидроксисукцинимидом в присутствии триэтиламина и дает γ-бензиловый эфир N-бензилглутаминовой кислоты с защищенной α-аминогруппой. Полученное соединение взаимодейтвует с N-гидроксисукцинимидом. Полученный сложный активированный эфир взаимодействует с триптофаном в присутствии триэтиламина. N-бензилоксикарбонил-γ- бензилглутамил-триптофан, полученный из предыдущей стадии, растворяют в спирте и гидрируют на палладиевом катализаторе в спиртоводной смеси в присутствии бикарбоната натрия и формиата аммония (донор водорода). Полученный в результате деблокирования L-глутамин-L-триптофан выделяют в виде мононатриевой соли. Для получения L-глутамин-L-триптофана раствор его мононатриевой соли подкисляют, например, соляной кислотой до pH 3,5. L-глутамин-L-триптофан, плохо растворимый в воде, выпадает в виде осадка.
Известный способ имеет ряд недостатков. Способ многостадиен; реакция получения исходного γ-бензилового эфира глутаминовой кислоты идет с выходом, не превышающим 45% по массе; на стадии получения вещества с защищенной α-аминогруппой протекает побочная реакция, продукт которой не пригоден для дальнейших превращений и должен быть отделен. Все это приводит к низкому выходу L-глутамин-L-триптофана или его мононатриевой соли, в расчете на исходную глутаминовую кислоту. Многостадийность, низкий промежуточный выход, побочная реакция на одной из стадий, а также высокая стоимость используемых реагентов, особенно имидов, приводят к очень высокой себестоимости L-глутамин-L-триптофана и его мононатриевой соли, получаемых по способу-прототипу.
Технический результат, достигаемый в заявляемом способе, выражается в упрощении и удешевлении процесса получения L-глутамин-L-триптофана, а также в достижении более высокого выхода целевого продукта в расчете на исходную глутаминовую кислоту.
Указанный технический результат достигается тем, что в способе получения L-глутамин-L-триптофана и его солей, включающем стадии защиты α-аминогруппы глутаминовой кислоты, активации α-карбоксильной группы глутаминовой кислоты путем образования сложного активированного эфира с триптофаном, отщепления защитных групп гидрированием продукта взаимодействия с триптофаном с палладиевым катализатором и донором водорода и выделения целевого продукта, защиту α-аминогруппы глутаминовой кислоты осуществляют взаимодействием непосредственно глутаминовой кислоты с избытком карбоксибензохлорида в щелочной среде. Активацию α-карбоксильной группы глутаминовой кислоты осуществляют взаимодействием полученной на предыдущей стадии бензилоксикрабонил-L-глутаминовой кислоты и избытком полиформальдегида с получением 3-(N-бензилоксикарбонил-оксазолидин-5-он-4-ил)пропионовой кислоты, продукт гидрирования в спиртоводном растворе обрабатывают эквивалентным количеством кислоты или неорганического соединения щелочного или щелочноземельного металла.
В качестве соединения щелочного или щелочноземельного металла используют соль натрия в виде, например, бикарбоната натрия, соль калия в виде бикарбоната калия, соединения магния в виде гидроксида магния или кальция в виде гидроксида кальция и др. Кислоту или неорганическое соединение берут в эквивалентном количестве для того, чтобы получить однозамещенную соль.
Согласно заявляемому способу глутаминовая кислота реагирует с избытком карбоксибензохлорида в щелочной среде, давая N-бензил-оксикарбонил-L-глутаминовую кислоту (с защищенной α-аминогруппой). N-бензил-оксикарбонил-L-глутаминовая кислота реагирует с полиформальдегидом в бензоле в присутствии, например, паратолуолсульфокисилоты, превращаясь в 3-(N-бензилоксикарбонил-оксазолидин-5-он-4-ил)пропионовую кислоту. Последняя конденсируется с триптофаном в присутствии триэтиламина или ацетата натрия или карбоната калия и бромида тетрабутиламмония. В результате конденсации получается N-бензилоксикарбонил-N-гидроксиметил-L-глутамил-L-триптофан. Деблокирование последнего проводят обработкой формиатом аммония (или формиатами метиламмония или диметиламмония) в спиртоводной смеси в присутствии палладиевого катализатора (5-10% Pd на угле или палладиевая чернь). Продукт деблокирования в спиртоводной смеси обрабатывают эквивалентным количеством кислоты или бикарбоната натрия, бикарбоната калия, гидроксида магния или гидроксида кальция и выделяют в виде L-глутамил-L-триптофана или моносолей L-глутамил-L-триптофана общей формулы: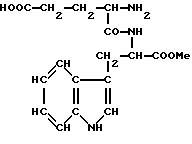
где
Me = Na, K, Mg, Ca и др.
Магний и кальций координируют два аниона L-глутамил-L-триптофана.
Способ иллюстрируется примерами.
Пример 1 (контрольный по прототипу).
а) Получение γ-бензилового эфира глутаминовой кислоты.
58,8 г (400 mM) глутаминовой кислоты растворяют в 1500 мл воды. Раствор нагревают до 75 - 80oC и при перемешивании добавляют к нему 36 мл уксусной кислоты, а затем небольшими порциями 88,4 г (400 mM) основного карбоната меди. Суспензию высаждающегося диглутамата меди интенсивно перемешивают до охлаждения и оставляют на двое суток. Осадок фильтруют, промывают водой и высушивают в вакуум-эксикаторе над пятиокисью фосфора.
59,7 г (406 mM) глутаминовой кислоты растворяют в 300 мл воды и при охлаждении к раствору добавляют 44,8 г (800 mM) KOH. К полученному раствору добавляют 300 мл диметилформамида и 98 г (200 mM) полученного диглутамата меди и перемешивают до растворения. К полученной смеси добавляют 11,2 мл (80 mM) триэтиламина, затем 105 мл (882 mM) бензилбромида, перемешивают в течение 5 часов при температуре 18 - 20oC и оставляют на 5 суток. Выпавший осадок фильтруют и промывают. Выход γ-бензилового эфира глутаминовой кислоты - 85,5 г (45%).
б) Защита γ-аминогруппы.
80,4 г (339 mM) γ-бензилового эфира глутаминовой кислоты суспендируют в 432 мл диоксана, добавляют 47,5 г (339 mM) триэтиламина и 85,4 г (343 mM) o-бензилкарбоксикарбонил-N-гидроксисукцинимида. Смесь оставляют при перемешивании и температуре 18-20oC на ночь. После этого диоксан отгоняют в вакууме. Остаток растворяют в этилацетате; γ-бензиловый эфир N-бензилоксикарбонилглутаминовой кислоты и экстрагируют из этилацетатного раствора водой и дважды - насыщенным раствором NaHCO3. Водный слой подкисляют серной кислотой до pH 2,0 и продукт экстрагируют этилацетатом. Органический слой промывают насыщенным раствором хлористого натрия, сушат сульфатом магния и упаривают. Выход 114 г (90,6%).
в) Активация α-карбоксильной группы глутаминовой кислоты.
27,0 г (264 mM) γ-бензилового эфира N-бензилоксикарбонилглутаминовой кислоты растворяют в 267 мл сухого диметилформамида, добавляют 30,4 г (264 mM) N-гидроксисукцинимида, охлаждают льдом и добавляют при интенсивном перемешивании раствор 54,3 г (264 mM) дициклогексилкарбодиимида в 200 мл диметилформамида. Смесь перемешивают в течение часа при температуре 0oC и оставляют при перемешивании при комнатной температуре на 16 час. Выделившуюся дициклогексилмочевину отделяют фильтрованием. Активированный N-гидроксисукцинимидный эфир N-бензилоксикарбонил-γ-бензилглутаминовой кислоты, не выделяя из раствора, используют на следующей стадии.
г) Конденсация с триптофаном.
К раствору N-гидроксисукцинимидного эфира N-бензилоксикарбонил γ-бензилглутаминовой кислоты в диметилформамиде, полученному на стадии (в), добавляют 64,1 г (314 mM) триптофана и 44,3 мл (316 mM) триэтиламина. Смесь перемешивают в течение 16 ч при температуре 18-20oC. Реакционную массу фильтруют, разбавляют 2,5 л воды и N-бензилоксикарбонил-γ-бензилглутамил-триптофан экстрагируют 2 раза 700 мл этилацетата. Органический раствор промывают водой, 2 H раствором серной кислоты и насыщенным раствором хлористого натрия, затем сушат сульфатом натрия и отгоняют этилацетатом под вакуумом. Выход - 132,5 г (93%) и N-бензилоксикарбонил γ-бензилглутамилтрипфтофана.
д) Деблокирование и выделение мононатриевой соли L-глутамил-L-триптофана.
135,5 г (251 mM) и N-бензилоксикарбонил-γ- бензилглутамилтриптофана растворяют при нагревании в 450 мл спирта и охлаждают до комнатной температуры. К раствору добавляют 250 мл воды и при интенсивном перемешивании добавляют 21,1 г (251 mM) бикарбоната натрия или 39,6 г (629 mM) формиата аммония. Затем медленно добавляют суспензию 22%-ного палладия на угле в 200 мл воды. Смесь перемешивают в течение 5 часов, катализатор отделяют фильтрованием, спирт отгоняют в вакууме. Водную фазу фильтруют через силикагель и упаривают до кристаллизации массы. Кристаллы разбавляют 1 л ацетона, перемешивают и оставляют на 16 час при температуре 0-5oC. Продукт фильтруют, промывают ацетоном, сушат, перекристаллизовывают из смеси воды с этанолом и получают 83,6 г (97%) мононатриевой соли L-глутамил-L-триптофана.
При исследовании продукта определяют:
- ультрафиолетовый спектр 0,01% раствора в воде в области 250 нм;
- спектр протонного ядерного резонанса 0,05 моль/л раствора в дейтерированном фосфатном буфере;
- прозрачность по ГФ ХI, вып. 1, с. 198;
- цветность по ГФ ХI, вып. 1, с. 194;
- растворимость по ГФ ХI, вып. 1, с. 175.
Выход соли L-глутамил-L-триптофана в расчете на исходную глутаминовую кислоту составляет 36%.
Пример 2 (заявляемый способ).
а) Защита α-аминогруппы.
44 г (299 mM) глутаминовой кислоты суспендируют в растворе 50 г (595 mM) NaHCO3 в 230 мл воды при сильном перемешивании; суспензию охлаждают льдом и добавляют 2 H раствора NaOH до pH 9.
Получают раствор глутамата натрия, к которому при температуре 5oC в течение 1,5 час добавляют по каплям 48 мл (338 mM) карбоксибензохлорида, pH реакционной смеси поддерживают равным 9 добавлением 2 H раствора NaOH. По окончании добавления перемешивают 2 часа при комнатной температуре.
Реакционную смесь дважды промывают диэтиловым эфиром, подкисляют 18%-ной соляной кислотой до pH 2, выпавшую бензилоксикарбонил-L-глутаминовую кислоту отделяют фильтрованием, промывают водой и сушат. Выход 78 г (93%).
б) Активация α-карбоксильной группы глутаминовой кислоты.
28,1 г (100 mM) бензилоксиркабонил-L-глутаминовой кислоты, 6 г (200 mM) полиформальдегида ("Параформ" фирмы SERVA, Германия) и 1,2 г (6 mM) пара-толуолсульфокислоты растворяют в 400 мл бензола и кипятят 1 час с насадкой Дина-Старка. Добавляют 100 мл этилацетата, промывают 0,3 М водным раствором карбоната калия и трижды - водой, сушат сульфатом магния, упаривают и высушивают в вакуум-эксикаторе над KOH/P2O5. Получено 27,8 г (95%) 3-(N-бензилоксикарбонил-оксазолидин-5-он-4-ил)пропионовой кислоты.
Индивидуальна по данным тонкослойной хроматографии в системе хлороформ-метанол-уксусная кислота (17:2:1).
в) Конденсация с триптофаном.
27,8 г (95 mM) 3-(N-бензилоксикарбонил-оксазолидин-5-он-4-ил)пропионовой кислоты растворяют в 50 мл диметилформамида, добавляют 20,9 г (102/5 mM) триптофана и 28,6 мл (205 mM) триэтиламина. Смесь перемешивают при температуре 18-20oC, затем фильтруют, разбавляют 500 мл воды, промывают эфиром, водный слой отделяют, подкисляют, наслаивают хлористым натрием и продукт экстрагируют тремя порциями этилацетата. Вытяжки объединяют, промывают насыщенным раствором хлористого натрия, сушат сульфатом натрия и упаривают под вакуумом. Получившийся маслообразный продукт сушат под вакуумом. Получено 43,4 г (92%) N-бензилоксикарбонил-N-гидроксиметил-L-глутамил-L-триптофана.
Индивидуален по данным тонкослойной хроматографии в системах хлороформ-метанол-25% аммиак-вода (15:10:2:3) и хлороформ-метанол-уксусная кислота (17:2:1).
г) Деблокирование и выделение мононатриевой соли L-глутамил-L-триптофана.
43,4 г (85,5 mM) N-бензилокси-карбонил-N-гидроксиметил-L-глутамил-L-триптофана растворяют в 150 мл изопропилового спирта. К полученному раствору добавляют раствор 13,5 г (214 mM) формиата аммония в 85 мл воды, затем суспензию 10% палладия на угле в 68 мл воды. Смесь перемешивают при температуре 18-20oC в течение 5 часов, после чего катализатор отделяют фильтрованием. К фильтрату добавляют 7,2 г (85,5 mM) NaHCO3, перемешивают до растворения и из раствора отгоняют изопропанол. Водный раствор фильтруют через 20 г силикагеля и упаривают до кристаллизации массы. Кристаллы перемешивают с 340 мл ацетона, выдерживают в течение 16 ч при температуре 4oC и продукт отделяют фильтрованием. Продукт растворяют в 100 мл воды, доводят pH раствора до 6,5 и фильтруют через 200 г окиси алюминия (pH сорбента - 9,5). Фильтрат упаривают и перекристаллизовывают из смеси воды с изопропиловым спиртом.
Получают 30 г (выход 99%) мононатриевой соли L-глутамил-L-триптофана.
Продукт исследуют как в примере 1. Выход готового продукта в расчете на исходную глутаминовую кислоту составляет 80%.
Пример 3.
Синтез ведут как в примере 2, но на стадии деблокирования после гидрирования и отделения катализатора фильтрованием к фильтрату добавляют 85,5 мл 1 М раствора HCl (85,5 mM). Осадок L-глутамил-L-триптофана отделяют, промывают на фильтре и сушат.
Пример 4.
Синтез ведут как в примере 2, но на стадии деблокирования, после гидрирования и отделения катализатора фильтрованием, к фильтрату добавляют 8,6 г (85,5 mM) KHCO3. Далее как в примере 2.
Пример 5.
Синтез ведут как в примере 2, но на стадии деблокирования, после гидрирования и отделения катализатора фильтрованием, к фильтрату добавляют 2,5 г (42,75 mM) Mg(OH)2. Далее как в примере 2.
Пример 6.
Синтез ведут как в примере 2, но на стадии деблокирования, после гидрирования и отделения катализатора фильтрованием, к фильтрату добавляют 3,2 г (42,75 mM) Ca(OH)2. Далее как в примере 2.
Как видно из приведенных примеров, заявляемый способ получения L-глутамил-L-триптофана и его моносолей более простой, не содержит ни стадии с низким выходом, ни стадии, на которой образуются побочные продукты. Это приводит к значительному увеличению выхода целевого продукта. В синтезе не используются дорогостоящие имиды, что вместе с сокращением и упрощением процесса и увеличением выхода продукта приводит к снижению себестоимости продукта в 3-5 раз.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2136277C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОНАТРИЕВОЙ СОЛИ ИЗОГЛУТАМИЛ-ТРИПТОФАНА | 2019 |
|
RU2703991C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРЫХ РЕСПИРАТОРНЫХ ВИРУСНЫХ ЗАБОЛЕВАНИЙ И ГРИППА | 1995 |
|
RU2107498C1 |
| ПЕПТИД, ОБЛАДАЮЩИЙ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1995 |
|
RU2091389C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДОВ, ОБЛАДАЮЩИХ ТКАНЕСПЕЦИФИЧЕСКОЙ АКТИВНОСТЬЮ, И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2000 |
|
RU2161501C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 1999 |
|
RU2165254C2 |
| ПЕПТИД, ОБЛАДАЮЩИЙ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ, И ПРЕПАРАТ НА ЕГО ОСНОВЕ | 1997 |
|
RU2142958C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2438694C1 |
| ПЕПТИДНЫЙ СОПОЛИМЕР, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2009 |
|
RU2402576C1 |
| ТЕТРАПЕПТИД, РЕГУЛИРУЮЩИЙ ФУНКЦИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ, ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2001 |
|
RU2177802C1 |
Предлагаемое изобретение относится к химии пептидов. Способ получения L-глутамил-L-триптофана и его солей включает последовательные стадии защиты α-аминогруппы глутаминовой кислоты, активации α-карбоксильной группы глутаминовой кислоты путем образования сложного активированного эфира, взаимодействия с триптофаном сложного активированного эфира, отщепления защитных групп гидрированного продукта взаимодействия с триптофаном в присутствии палладиевого катализатора и донора водорода и выделения готового продукта. Технический результат, состоящий в упрощении и удешевлении процесса и увеличении выхода целевого продукта, достигается тем, что защиту α-аминогруппы глутаминовой кислоты осуществляют взаимодействием глутаминовой кислоты с избытком карбобензоксихлорида в щелочной среде. Активацию α-карбоксильной группы глутаминовой кислоты осуществляют взаимодействием бензилоксикарбонил-L-глутаминовой кислоты с избытком полиформальдегида с получением 3-(N-бензилоксикарбонил-оксазолидин-5- он-4-ил)пропионовой кислоты, а продукт гидрирования в спиртоводном растворе обрабатывают эквивалентным количеством кислоты или неорганического соединения щелочного или щелочноземельного металла. В качестве неорганического соединения щелочного металла используют бикарбонаты натрия и калия, а в качестве щелочноземельного металла - гидроксиды магния и кальция. 4 з.п. ф-лы.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| RU, патент, 1582393, A 61 K 38/05, 1992 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Ueba H., Doi v | |||
| at.al | |||
| Biochem | |||
| Biophys | |||
| Res | |||
| Commun | |||
| Механическая топочная решетка с наклонными частью подвижными, частью неподвижными колосниковыми элементами | 1917 |
|
SU1988A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Jyo H., Hitoshi H | |||
| at.al | |||
| Chem | |||
| Pharm Bull | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Рябинина И.Д | |||
| Мирошниченко И.В., Ярилин А.А | |||
| Иммунология, 1991, N 6, с.20-23 | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Prestige R.L., Hardino D.R.R | |||
| at.al | |||
| J.Org.Chem | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Ерюхина А.П., Куликов С.В | |||
| Ж | |||
| "Общая химия", 1995, т.65, вып.10, с.1735-1738. | |||
Авторы
Даты
1998-10-20—Публикация
1996-08-01—Подача