Изобретение относится к биохимии, в частности к применению 4,4-дигалоидпроизводных 3,5-дизамещенных пиразол-1,2-диоксидов общей формулы I: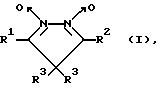
где
R1 и R2 - метил или фенил;
R3 - атом хлора или брома,
в качестве активаторов растворимой формы гуанилатциклазы (рГЦ).
Вышеуказанные соединения могут найти использование в биохимии для изучения механизма регуляции рГЦ и других ферментов.
Гуанилатциклаза/КФ 4.6.1.2. ; гуанозин-5'-трифосфат-пирофосфатлиаза (циклизующая)/является ферментом, катализирующим биосинтез гуанозин-3',5'-циклофосфата(цГМФ)- универсального регулятора внутриклеточного метаболизма [1].
ГЦ существует в двух формах - мембранной и растворимой. В настоящее время установлено, что в рГЦ является основной мишенью фармакологического действия наиболее распространенных нитровазодилятаторов (нитроглицерина, нитросорбида, нитропруссида натрия) и играет ключевую роль в регуляции таких физиологических процессов, как сокращение и расслабление гладких мышц кровеносных сосудов и агрегация тромбоцитов. Показано, что лечебный эффект вышеуказанных фармпрепаратов связан со стимуляцией активности рГЦ в результате взаимодействия оксида азота, образующегося при их биотрансформации, с атомом железа гема, входящего в состав фермента, и образования комплекса нитрозил-гем.
Существенным недостатком известных вазодилятаторов на основе органических нитратов является возникновение толерантности при их длительном применении. В связи с этим изучение молекулярного механизма регуляции активности рГЦ с помощью новых соединений, способных генерировать NO в живом организме и/или вызывать активацию фермента NO-независимым путем, является перспективным подходом для поиска и создания новых более эффективных антигипертензивных и антиагрегантных фармпрепаратов.
Известен 3-фенил-4-хлор-1,2,5-оксадиазол-2-оксид, вызывающий активацию рГЦ в присутствии цистеина, используемого в концентрации 5 мМ [2].
Недостатком данного соединения является его низкое активирующее действие на рГЦ (в концентрации 5•10-4 М оно активирует фермент ≈ в 2,3 раза).
Наиболее близкими к описываемым являются известные соединения - 3,5-дизамещенные пиразол-4-он-1,2-диоксиды, в частности 3,5-дифенилпиразол-4-он-1,2-диоксид(см. вышеуказанную формулу I, где R1=R2-фенил и R3 + R3 = 0)[3]). Данное соединение является тиол-зависимым донором оксида азота и активатором рГЦ.
Недостатком данного соединения является сравнительно невысокая степень активации рГЦ.
Целью описываемого изобретения является поиск соединений в ряду известных замещенных пиразол-1,2-диоксидов, более эффективно активирующих рГЦ.
Указанная цель достигается применением известных 4,4-дигалоидпроизводных 3,5-дизамещенных пиразол-1,2-диоксидов вышеуказанной общей формулы I, где R1, R2 и R3 имеют вышеуказанные значения, в качестве активаторов рГЦ.
Данные соединения были получены известным способом при взаимодействии соответствующих 3,5-дизамещенных 1-гидроксипиразол-2-оксидов или диоксимов β-дикетонов с N-бром- или N- хлорсукцинимидом или N-бромацетамидом в водно-органической или водной среде при охлаждении [4].
Действие описываемых соединений на рГЦ до настоящего времени не исследовалось.
Изобретение иллюстрируется следующими примерами.
Пример 1. Активирующее действие производных пиразол-1,2-диоксида на рГЦ.
Препарат рГЦ получали из тромбоцитов человека, выделенных из венозной крови доноров известным способом. Активность фермента определяли по количеству образовавшегося цГМФ иммуноферментным способом с использованием наборов реактивов для количественного определения цГМФ АО "Биоиммуноген" (Россия).
Инкубационная смесь для определения активности (общий объем пробы 150 мкл) приготавливалась при 0-4oC и содержала 50 мМ Трис-HCl (pH 7,6),1 мМ ГТФ, 4 мМ MgCl2, 4 мМ креатинфосфат, 100 мкг (50 ед/мг) креатинфосфокиназы, 10 мМ теофиллин, ферментный препарат (супернатант 105000 g, 10-20 мкг белка). При определении активирующего действия в среду инкубации вносили изучаемое соединение в виде раствора в водном диметилсульфоксиде (DMCO). Концентрация соединения в пробе составляла 1•10-5 M, DMCO - 0,02 об.%. Контрольная проба показала отсутствие влияния DMCO в указанной концентрации на базальную активность рГЦ. Пробы инкубировали в водяном термостате при 37oC в течение 15 минут. Реакцию останавливали перенесением проб на 2 минуты в кипящую водяную баню с последующим охлаждением в ледяной бане. После отделения денатурированного белка центрифугированием (10 минут при 1500g) в полученном супернатанте определяли количество образовавшегося цГМФ вышеуказанным способом.
Определение белка проводили по способу Лоури, в качестве стандарта использовали бычий сывороточный альбумин.
Эффективность активирующего действия изучаемых соединений в концентрации 1•10-5 M оценивали в сравнении с аналогичным эффектом наиболее близкого известного соединения - 3,5-дифенилпиразол-4-он-1,2-диоксида (соединение I). Степень активации рГЦ в вышеуказанных условиях для соединений данного изобретения находилась в интервале 280-500%. В частности, для 3,5-дифенил-4,4-дихлорпиразол-1,2-диоксида она составила 380% (ср.250% для соединения I).
Пример 2. Генерация оксида азота производными пиразол-1,2-диоксида. Для определения оксида азота использовали известный способ, основанный на реакции оксида азота с кислородом воздуха в водной среде с образованием нитрита, количество которого измеряли по окрашенному продукту реакции азосочетания [5] с помощью спектрофотометра. Проба конечным объемом 400 мкл содержала 50 мМ калий-фосфатный буфер (pH 7,4) 1 мМ цистеин, изучаемое соединение в концентрации 0,1 мМ и 0,2% DMCO. В качестве отрицательного контроля использовался водный раствор DMCO в концентрации 0,2%, а в качестве положительного контроля 0,1 мМ раствор нитрата натрия, содержащий 0,2% DMCO. Пробы инкубировали 1 час при 20oC и добавляли последовательно 50 мкл 3 M раствора ацетата натрия, 300 мкл 0,92% раствора сульфаниловой кислоты в 30% уксусной кислоте и 300 мкл N-нафтилэтилендиамина. Пробы инкубировали 10 минут и измеряли оптическую плотность при длин волны 554 нм на спектрофотометре.
3,5-Дифенил-4,4-дихлорпиразол-1,2-диоксид в вышеуказанных условиях генерировал 0,081 моль нитрита на моль соединения (в отсутствие цистеина образования нитрата не происходит). Известное соединение I в вышеуказанных условиях генерировало 0,053 моль нитрита на моль соединения.
Как вытекает из данных примера 1, соединения настоящего изобретения оказывают более выраженное активирующее действие на рГЦ и расширяют ассортимент специфических регуляторов активности данного фермента.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДОНОР ОКСИДА АЗОТА И АКТИВАТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 1997 |
|
RU2123046C1 |
| ДОНОР ОКСИДА АЗОТА И АКТИВАТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 1998 |
|
RU2139932C1 |
| СПЕЦИФИЧЕСКИЙ РЕГУЛЯТОР АКТИВНОСТИ НУКЛЕОТИД-ЗАВИСИМЫХ ФЕРМЕНТОВ | 1997 |
|
RU2130490C1 |
| АКТИВАТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 1997 |
|
RU2123526C1 |
| ПРОИЗВОДНЫЕ 1,2,5-ОКСАДИАЗОЛО-[3,4-D]-ПИРИДАЗИН-5,6-ДИОКСИДА В КАЧЕСТВЕ АКТИВАТОРОВ РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ И СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1997 |
|
RU2165256C2 |
| ИНГИБИТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 2001 |
|
RU2196175C2 |
| ПРОИЗВОДНЫЕ 1,4,2,5-ДИОКСАДИАЗИНА | 2001 |
|
RU2212409C1 |
| ИНГИБИТОР NO-ЗАВИСИМОЙ АКТИВАЦИИ РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 2001 |
|
RU2189392C1 |
| ДОНОР ОКСИДА АЗОТА, АКТИВИРУЮЩИЙ РАСТВОРИМУЮ ФОРМУ ГУАНИЛАТЦИКЛАЗЫ, ИНГИБИРУЮЩИЙ АГРЕГАЦИЮ ТРОМБОЦИТОВ И ОБЛАДАЮЩИЙ СПАЗМОЛИТИЧЕСКИМ И СОСУДОРАСШИРЯЮЩИМ ДЕЙСТВИЕМ | 2001 |
|
RU2208438C1 |
| ИНГИБИТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 1999 |
|
RU2151799C1 |
Изобретение относится к биохимии, может быть использовано для изучения механизма регуляции растворимой формы гуанилатциклазы (рГЦ). Сущность изобретения заключается в применении 4,4-дигалоидпроизводных 3,5-дизамещенных пиразол-1,2-диоксидов общей формулы I в качестве активаторов растворимой формы гуанилатциклазы (рГЦ). Степень активации рГЦ для соединений данного изобретения находилась в интервале 280 - 500%. В частности, для 3,5-дифенил-4,4-дихлорпиразол-1,2-диоксида она составила 380% (ср. 250% для известного соединения 3,5-дифенилпиразол-4-он-1,2-диоксида). Соединения настоящего изобретения оказывают более выраженное активирующее действие на рГЦ и расширяют ассортимент специфических регуляторов активности данного фермента. 1 з.п. ф-лы.
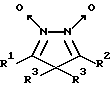
где R1 и R2 - метил или фенил;
R3 - атом хлора или брома,
в качестве активаторов растворимой формы гуанилатциклазы.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| DE 4322545 A1, 12.01.95 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Ferioli R., Folco G.C | |||
| et al | |||
| "A new class of furoxan derivatives as NO donors: mechanism of action and biological activity" Brit | |||
| J | |||
| Pharmacol | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| Способ получения борнеола из пихтового или т.п. масел | 1921 |
|
SU114A1 |
| Топка генеративного типа для мелкого топлива | 1923 |
|
SU816A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Hansen J.F., Kim Y.L | |||
| et al | |||
| "Halogenation of N-oxygenated pyrazoles | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Org | |||
| Chem | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| Аппарат, предназначенный для летания | 0 |
|
SU76A1 |
Авторы
Даты
1998-11-27—Публикация
1997-10-31—Подача