Изобретение относится к способу получения алкиленгликолей. Алкиленгликоли используются в производстве растворителей, пластификаторов, компонентов для низкозамерзающих, антиобледенительных, гидравлических и гидротормозных жидкостей, а также для получения материалов, применяемых в промышленности пластических масс, пестицидов, лаков и красок.
Известен способ получения алкиленгликолей некаталитической гидратацией оксидов алкилена в реакторе вытеснения при 160-210oC и 1,5-2,1 МПа. Мольное соотношение вода:оксид в смеси, поступающей на гидратацию, составляет 15-17: 1 (концентрация оксида алкилена в исходном растворе 13-18 мас.%). В этих условиях получают водный раствор гликолей с концентрацией 18-20 мас.% и выходом моноалкиленгликолей не более 91,5 мол.%. (Дымент О.Н., Казанский С.К., Мирошников А. М. Гликоли и другие производные окисей этилена и пропилена. - М.: Химия, 1976).
Однако по данному способу образуются разбавленные растворы алкиленгликолей, что требует больших энергетических затрат на отгонку воды.
Известен способ получения алкиленгликолей взаимодействием алкиленоксида с водой в присутствии каталитической системы, включающей в себя твердый материал, имеющий электроположительные центры, которые координированы с анионами иными чем металлат- или галоген-анион. Когда твердым материалом является анионообменная смола с четвертичными аммониевыми группами, а анионом - бикарбонат, процесс проводят практически в отсутствии диоксида углерода (заявка PCT WO 95/20559, 03.08.95). Лучшими твердыми материалами в данном способе являются материалы, содержащие низшие триалкиламиновые и триметилбензиламмониевые группы.
И в этом случае получают относительно разбавленные растворы алкиленгликоля, что требует энергетических затрат на отгонку воды.
Известен способ получения алкиленгликолей каталитической гидратацией оксидов алкилена при температуре 20-250oC и давлении до 3 МПа в присутствии анионита в хлор-форме и диоксида углерода. Используемый как катализатор анионит Dowex MSA-1 в качестве электроположительных центров содержит атомы азота бензилтриметиламмониевых групп. Мольное соотношение вода:оксид алкилена в смеси, подаваемой на гидратацию, составляет 1:0,66 (концентрация оксида алкилена в исходной смеси - 62 мас.%). В этих условиях получают водный раствор гликолей с концентрацией не более 87 мас.% и содержанием в продуктах реакции 1-1,5 мас. % карбонатов алкиленоксидов (патент JP 57-139026, 27.08.82).
Недостатком способа является сложность выделения гликолей из смеси с карбонатами из-за близости температур кипения дигликолей и карбонатов.
Наиболее близким аналогом предложенного способа является способ получения алкиленгликолей гидратацией оксидов алкилена при 80-130oC и 0,8-1,6 МПа в присутствии алкиленгликолей, диоксида углерода (при концентрациях даже таких низких как 0,01 мас.%) и катализатора-анионита в гидрокарбонатной форме, содержащего в качестве электроположительных центров атомы азота четвертичных бензилметиламмониевых групп, связанные с полимерной матрицей через бензильную группу (марки АВ-17-8 и АВ-17Т). Согласно данному способу возможно с высокой селективностью (93-96%) получать концентрированные растворы, содержащие 65-90 мас. % гликолей (патент RU N 2002726, приоритет 19.05.92, опубл. 15.11.93).
Однако способ имеет относительно низкую удельную производительность, которая не превышает 0,22 кг превращенного оксида этилена с литра катализатора в ч [0,22 кг ОЭ/(л kt•ч)] и 0,35 кг превращенного оксида пропилена с литра катализатора в ч [0,35 кг ОП/(л kt•ч)]. Кроме того, используемые каталитические системы, содержащие четвертичные триметилбензиламмониевые группы, имеют относительно низкую термическую стойкость и при температуре более 120-130oC постепенно теряют свою каталитическую активность и селективность. Время стабильной работы данных каталитических систем при температуре 120-130oC без потери активности и селективности образования моногликолей обычно не превышает 5-30 ч.
Предлагаемый способ позволяет повысить удельную производительность процесса. Кроме того, используемые в данном способе каталитические системы обладают повышенной термостойкостью и могут работать длительное время (как правило, свыше шести месяцев) при температурах, превышающих 130oC без потери активности и селективности.
Неожиданно было установлено, что гидратация оксидов алкилена эффективно протекает в присутствии каталитической системы на основе ионообменных полимерных материалов, содержащих в качестве электроположительных центров атомы азота, координированные с анионами, отличающийся тем, что один или более электроположительных центров связан двумя или более атомами, отличными от атома углерода метильной группы.
Ионообменные полимерные материалы, у которых электроположительные центры связаны с двумя или более атомами углерода, отличными от атома углерода метильной группы, известны и имеют коммерческое значение. Например, подходящими исходными материалами для получения каталитической системы по изобретению являются ионообменные полимерные материалы:
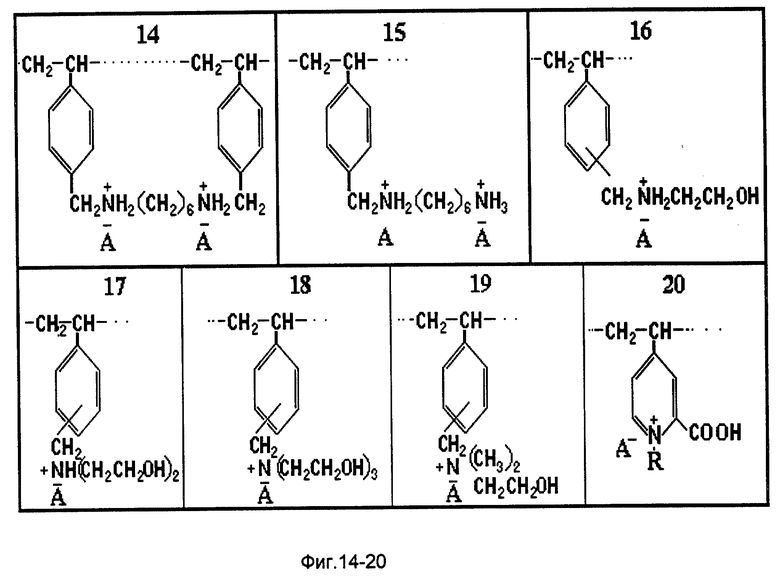
- АВ-29-12П, АДМ, А11-500 (фирма DOW) (фиг. 19), у которых атом азота связан с бензильной, β- оксиэтильной и двумя метильными группами;
- АМЭ-1 (фиг. 16), у которого атом азота связан с двумя атомами водорода, β- оксиэтильной и бензильной группой;
- АД-1 (фиг. 17), у которого атом азота связан с атомом водорода, двумя β- оксиэтильными и одной бензильной группой;
- АТ-1 (фиг. 18), у которого атом азота связан с тремя β- оксиэтильными группами и одной бензильной;
- АМП (фиг. 9), у которого атом азота связан с бензильной группой и двумя атомами углерода пиридинового кольца,
а также ряд других ионообменных полимерных материалов.
Активные каталитические системы могут также содержать в сочетании с вышеперечисленными другие функциональные группы, например хлорметильные: -CH2-Cl, хлорбензильные: -C6H4CH2Cl, гидроксиметильные (фиг. 7), карбоксильные (фиг. 20).
В качестве аниона (A-), координированного с электроположительным центром, могут выступать анионы неорганических : соляной, фосфорной, угольной, сернистой, серной, борной, кремниевой кислот и/или органических карбоновых и дикарбоновых кислот, содержащих 1-20 атомов углерода. Предпочтительным анионом является гидрокарбонат.
Кроме того, каталитические системы могут быть получены из других известных ионообменных полимерных материалов их последовательной обработкой:
- кислотой и/или смесью кислот и оксидом алкилена и солями кислот и/или диоксидом углерода;
- галогенорганическими соединениями и солями кислот и/или диоксидом углерода;
- алкилсульфатами и солями кислот и/или диоксидом углерода;
- оксидами алкилена и солями кислот и/или диоксидом углерода.
Аналогичный результат может быть достигнут при другой последовательности обработки ионообменных полимерных материалов. Кроме того, две или более из перечисленных стадий обработки ионообменного полимерного материала могут быть совмещены в одну стадию.
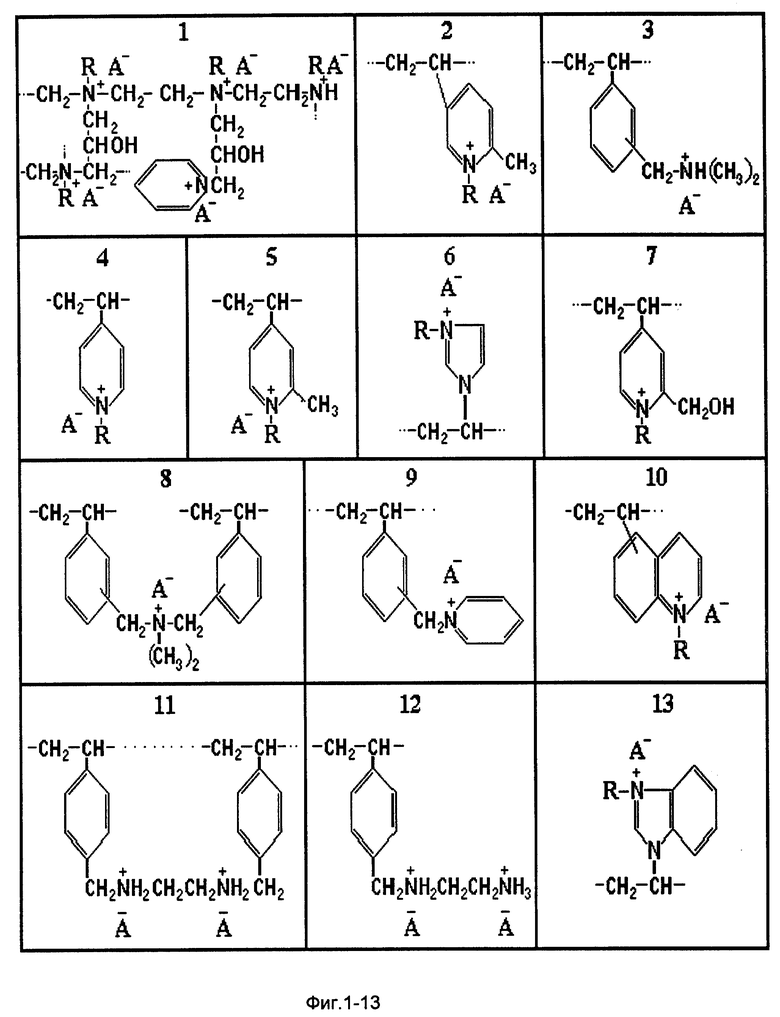
Структуры активных центров некоторых каталитических композиций, используемых в данном способе, приведены на фиг. 1-20.
Предпочтительно процесс гидратации оксидов алкилена проводят в присутствии кислот и/или их солей и/или диоксида углерода при их содержании в исходном водном растворе алкиленоксида в интервале 0,00001-1 мас.%. Предпочтительно 0,001-0,01 мас.%. В качестве кислот используют сернистую, угольную, ортофосфорную кислоты, борную, кремниевую, карбоновые и дикарбоновые кислоты, содержащие 1-20 атомов углерода. В качестве солей используют дигидро-, гидро- и ортофосфаты, сульфиты и гидросульфиты, карбонаты и гидрокарбонаты, формиаты, мета- и тетерабораты, силикаты, ацетаты и оксалаты натрия, калия и аммония.
Предпочтительно в качестве карбоновых кислот используют муравьиную, уксусную, щавелевую, малоновую и янтарную кислоты.
Наиболее предпочтительно проводить реакцию в присутствии диоксида углерода. По предлагаемому способу процесс эффективно протекает, когда диоксид углерода присутствует в реакционной массе в количестве большем или равном 0,1 мас. %. Предпочтительно, однако, чтобы диоксид углерода присутствовал в реакционной массе в количестве, меньшем или равном 0,5 мас. %, более предпочтительно 0,2 мас.% Наиболее предпочтительное количество диоксида углерода, присутствующего в реакционной массе, находится в интервале от нижнего уровня 0,01 мас. %, более предпочтительно 0,05 мас.%, до высшего уровня 0,2 мас.%, более предпочтительно 0,1 мас.%.
Следующие примеры иллюстрируют изобретение.
Пример 1
Процесс осуществляли в трубчатом реакторе вытеснения объемом 50 мл, заполненном каталитической системой - ионообменным полимерным материалом, содержащим три типа электроположительных центров (фиг. 1), у которых атомы азота, связаны:
- с оксипропильной группой и двумя атомами углерода пиридинового кольца;
- с тремя атомами углерода полимерной матрицы и атомом углерода метильной группы (R=CH3-);
- с тремя атомами углерода полимерной матрицы и атомом углерода оксиэтильной группы (R=-CH2-CH2OH);
- с атомами тремя атомами углерода полимерной матрицы и атомом углерода этильной группы (R=CH3CH2-),
и которые координированы с гидрокарбонат - анионом (HCO
На вход реактора подавали исходную смесь состава, мас.%: вода - 73,14; оксид этилена (ОЭ) - 26,74; диоксид углерода (CO2) - 0,12, со скоростью 105 г/ч. Мольное соотношение вода:оксид = 6,7. Температуру в реакторе поддерживали в интервале 20-140oC. Давление 1,0 МПа. На выходе из реактора отбирали смесь состава, мас.%: ОЭ - 2,14; этиленгликоль (ЭГ) - 34,1; диэтиленгликоль (ДЭГ) - 0,56; CO2 - 0,12; вода - остальное. Степень конверсии (Х) оксида этилена - 92,0%. Селективность образования моногликоля (Ф) - 98,1 мол. % . Удельная производительность по превращенному оксиду этилена (Gу) составляет: 0,52 кг ОЭ/(л kt•ч).
Пример 2
В трубчатый реактор вытеснения объемом 50 мл, заполненный ионообменным полимерным материалом, содержащим электроположительные центры (фиг. 2), у которых атомы азота связаны с двумя атомами метилпиридинового кольца и с атомом углерода метильной группы, которые координированы с карбонат-анионом ( (NaCO
На вход реактора подавали исходную смесь состава, мас.%: вода - 62,039; оксид пропилена (ОП) - 37,96; CO2 - 0,001 со скоростью 97 г/ч. Мольное соотношение вода: оксид= 5,3. Температура в реакторе 60 -140oC. Давление - 1,9 МПа. На выходе из реактора отбирали смесь состава, мас.%: ОП - 2,66; пропиленгликоль (ПГ) - 44,9; дипропиленгликоль (ДПГ) - 1,18; CO2 - 0,08; вода - остальное. Степень конверсии ОП - 93%. Селективность образования моногликоля - 97,1 мол.%. Удельная производительность по превращенному оксиду пропилена составляет 0,68 кг ОП/(л kt•ч).
Пример 3.
Процесс осуществляли в каскаде, состоящем из трех последовательно соединенных реакторов вытеснения объемом 24, 24 и 40 мл соответственно, заполненных ионообменным полимерным материалом, содержащим электроположительные центры (фиг. 3), у которых атом азота, связаны с атомом углерода бензильной группы, с двумя атомами углерода метильных групп и атомом водорода. Электроположительные центры координированы с гидрокарбонат анионом. Обменная емкость по гидрокарбонат-аниону - 1,3 мг-экв/мл. Общий объем реакторов каскада 88 мл. Температуру в реакторах поддерживают в интервале 50-130oC. Давление 2,6 МПа. На вход первого реактора каскада подали смесь состава, мас. %: вода - 74,739; ОЭ - 25,1; CO2 - 0,2 со скоростью 75 г/ч. Реакционную смесь, выходящую из первого реактора, смешали с 17 г/ч оксида этилена и направили на вход второго реактора каскада. Аналогично, к потоку, выходящему из второго реактора, добавили 23 г/ч оксида этилена и направили на вход третьего реактора каскада. На выходе из третьего реактора каскада отбирали смесь продуктов реакции со скоростью 115 г/ч. Степень конверсии ОЭ - 99,1%. Селективность образования моноэтиленгликоля 93,1%. Суммарная концентрация моно-, ди-, и триэтиленгликолей - 71 мас.%. Производительность по превращенному оксиду этилена составила 0,67 кг ОЭ/(л kt•ч).
Пример 4
Процесс осуществляли в каскаде реакторов, описанном в примере 3 и заполненных ионообменным полимерным материалом, содержащим два типа электроположительных центров (фиг. 11 и 12), у которых часть атомов азота связана с атомом углерода бензильной группы и двумя атомами водорода, а другая чть связана с тремя атомами водорода. Кроме того, два соседних электроположительных центра связаны между собой мостиковой -CH2-CH2- группой. Электроположительные центры координированы с гидрокарбонат анионом. Обменная емкость по гидрокарбонат-аниону - 1,8 мг-экв/мл. На вход первого реактора подали смесь состава, мас. %: вода - 72,89; ОП - 27,1; CO2 - 0,01 со скоростью 56 г/ч. На вход второго и третьего реакторов дополнительно подали оксид пропилена в количестве 27 и 39 г/ч. Температура в реакторах 40-140oC. Давление 1,6 МПа. На выходе из третьего реактора отбирали продукты реакции со скоростью 122 г/ч. Степень конверсии ОП - 99%. Селективность образования монопропиленгликоля 92,5%. Суммарная концентрация моно-, ди- и трипропиленгликолей - 85 мас.%. Производительность по превращенному оксиду составила 0,91 кг ОП/(л kt•ч).
Пример 5
Процесс осуществляли в каскаде реакторов, описанном в примере 3 и заполненных ионообменным полимерным материалом, содержащим электроположительные центры (фиг. 6), у которых атом азота связан с атомом углерода диазольного кольца и с атомом углерода бензильной группы. Электроположительные центры координированы с гидрокарбонат анионом. Обменная емкость по гидрокарбонат-аниону - 2,4 мг-экв/мл. На вход первого реактора подали смесь состава, мас. %: вода - 71,9; ОП - 27,1; CO2 - 1,0 со скоростью 65 г/ч. На вход второго и третьего реакторов дополнительно подали оксид пропилена в количестве 32 и 46 г/ч. Температура в реакторах 60-150oC. Давление 2,5 МПа. На выходе из третьего реактора каскада отбирали смесь продуктов реакции со скоростью 143 г/ч. Степень конверсии ОП - 98,5%. Селективность образования монопропиленгликоля 92,8%. Суммарная концентрация моно-, ди- и триэтиленгликолей - 85 мас.%. Производительность по превращенному оксиду пропилена составила 1,07 кг ОП/(л kt•ч).
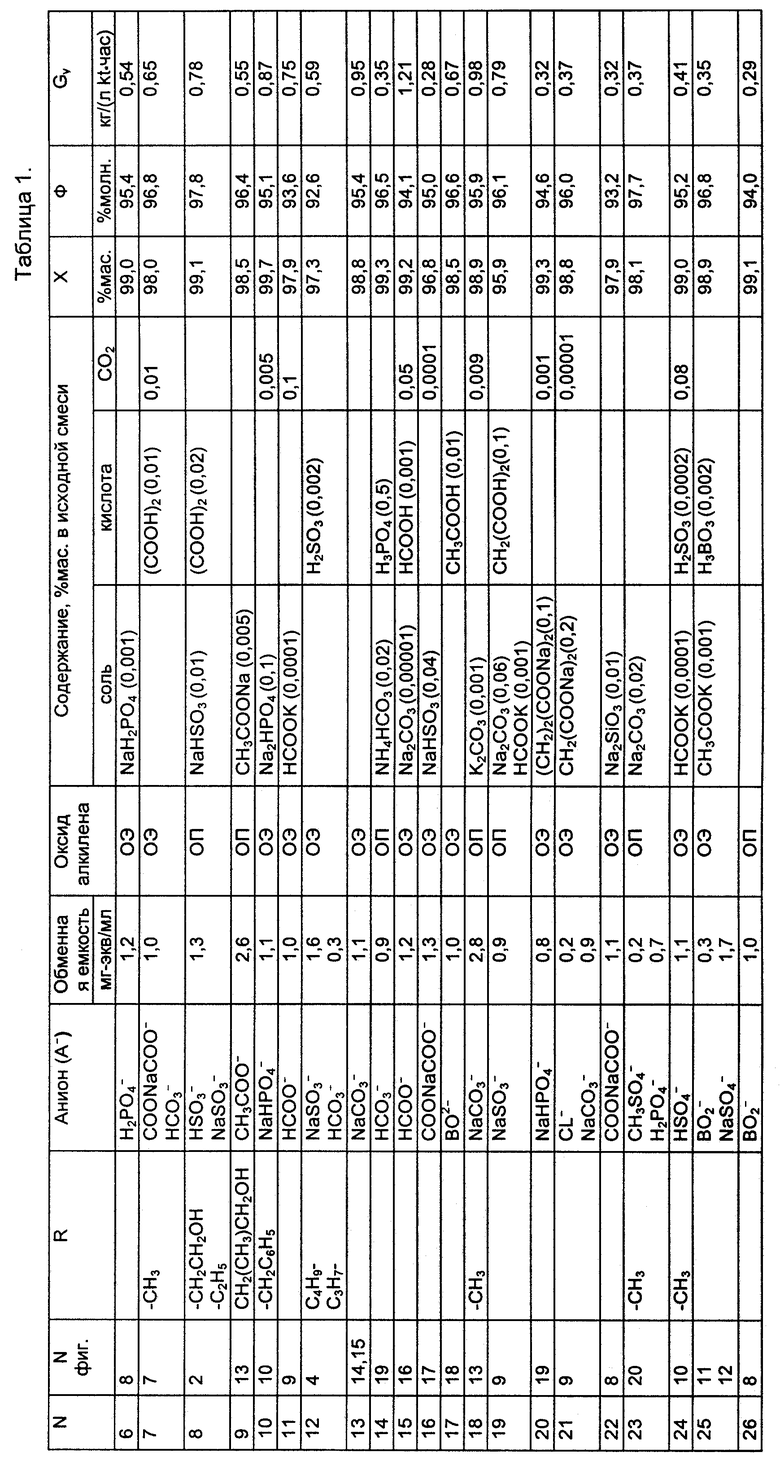
Примеры 6-26
Иллюстрируют процесс гидратации оксидов этилена и пропилена в трубчатом реакторе, описанном в примере 1, в присутствии других каталитических систем. Температуру в реакторе поддерживали в интервале 20-200oC. Давление 0,6-5,0 МПа. Объемная скорость подачи 1,0-3,0 ч-1. Мольное отношение вода:оксид 1 - (5:1). Условия и результаты проведения процесса приведены в таблице.
Таким образом проведение процесса описанным в настоящем изобретении способом позволяет увеличить удельную производительность для оксида этилена с 0,22 до 0,28-1,21 кг ОЭ/(л kt•ч) и для оксида пропилена с 0,35 до 0,45--0,98 кг ОП/(л kt•ч) и получать концентрированные растворы гликолей до 71-85 мас. %. Кроме того, используемые каталитические системы позволяют работать без потери активности и селективности в течение длительного времени (более 0,5 года). Данный способ применим для гидратации других α- оксидов, например глицидола, оксидов циклогексена, дивинила и др.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 1999 |
|
RU2149864C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 2006 |
|
RU2317971C1 |
| СПОСОБ РЕГЕНЕРАЦИИ ОСНОВНЫХ АНИОНИТНЫХ КАТАЛИЗАТОРОВ | 2006 |
|
RU2322295C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКОКСИУКСУСНЫХ КИСЛОТ ИЛИ ИХ СОЛЕЙ | 1999 |
|
RU2181714C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 2004 |
|
RU2284985C2 |
| СПОСОБ ПЕРЕРАБОТКИ ЛАКТАТА АММОНИЯ В МОЛОЧНУЮ КИСЛОТУ И ЕЕ СЛОЖНЫЕ ЭФИРЫ | 2012 |
|
RU2535680C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛАКТИДА | 2005 |
|
RU2301230C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 1999 |
|
RU2222522C2 |
| СПОСОБ ГИДРОЛИЗА АЛКИЛЕНОКСИДОВ С ИСПОЛЬЗОВАНИЕМ ДОБАВКИ, СТАБИЛИЗИРУЮЩЕЙ КАТАЛИЗАТОР | 1999 |
|
RU2230728C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ И КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1999 |
|
RU2233261C2 |
Изобретение относится к каталитическим способам получения алкиленгликолей. Способ получения алкиленгликолей гидратацией оксидов алкилена в присутствии каталитической системы на основе азотсодержащих ионообменных полимерных материалов, содержащих в качестве электроположительных центров атомы азота, координированные с анионами. Причем один или более электроположительных центров связан с двумя или более атомами, отличными от атома углерода метильной группы. Атомами, отличными от атома углерода метильной группы, в каталитической системе могут быть атомы углерода алкильных, бензильных, оксиалкильных, фенильных и алкилфенильных групп, атомы углерода гетероциклических соединений, а также атомы водорода и азота. Гидратацию оксидов алкилена можно проводить при 20-200oC и 0,6-5,0 МПа. Предпочтительными являются диапазоны температур и давлений 100-140oС и 1,0-2,0 МПа соответственно. Указанный способ позволяет повысить удельную производительность процесса. Кроме того, используемые в данном способе каталитические системы обладают повышенной термостойкостью и могут работать продолжительное время при температурах более 130oС без потери активности и селективности. 19 з.п. ф-лы, 20 ил., 1 табл.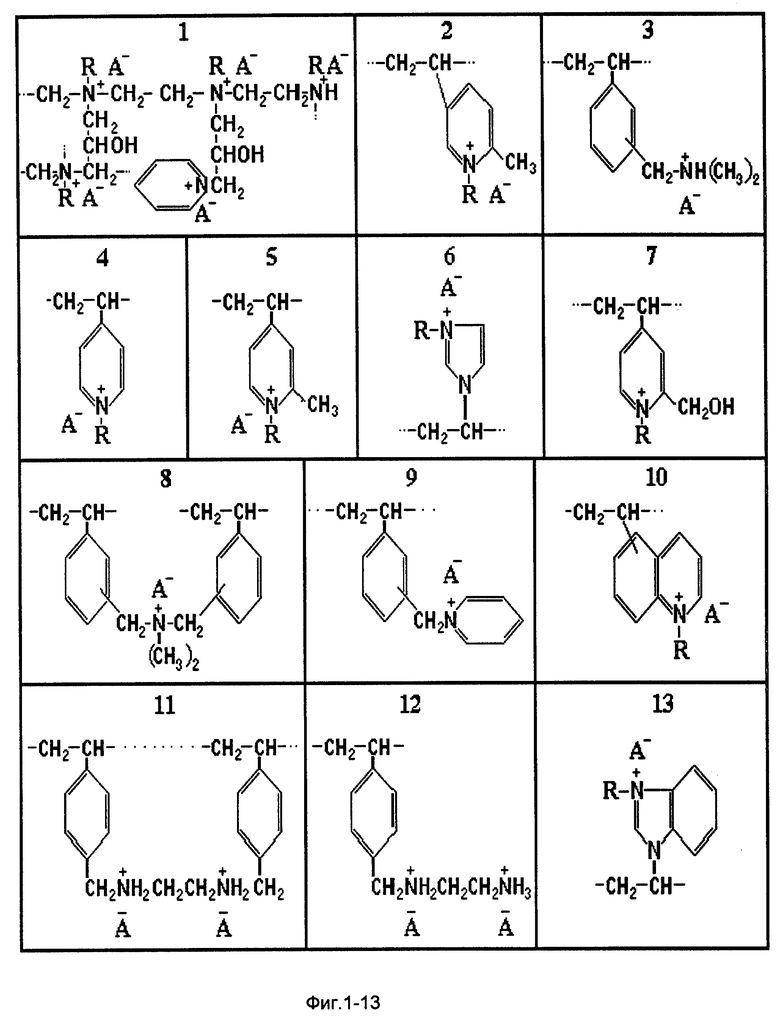
| RU 2002726 C1, 1993 | |||
| RU 2001901 C1, 1993 | |||
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| 0 |
|
SU160330A1 | |
| 0 |
|
SU156447A1 | |
| US 4393254 A, 1983. | |||
Авторы
Даты
1998-12-10—Публикация
1997-09-09—Подача