Настоящее изобретение относится к промышленно выгодному способу выделения цефаклора из реакционной смеси ферментативного ацилирования путем осаждения цефаклора из смеси в виде соли с антрахинондисульфокислотой в соотношении 2:1.
В патенте США N 3816253 описан ферментативный способ получения цефалоспоринов путем конденсации производного аминокислоты и ядра 7-аминоцефалоспорина. В патентной заявке США N 07/874257 от 24 апреля 1992 г (X-8505) описан улучшенный ферментативный способ получения цефалоспоринов, в частности относящийся к конденсации соответствующего ядра 7-аминоцефалоспорина с аминокислотой. До сих пор представляющее интерес вещество, цефаклор, после такой реакции ферментативного ацилирования находилось в сложном окружении, которое содержало не только ядро, но и фенилглицин, D-фенилглицинметиловый эфир и их соли. Вследствие сложного характера данной смеси цефаклор выделяли на ряде колонок. Конечно, это приводит к потере продукта, а также занимает много времени.
Ввиду вышесказанного требуется способ селективного удаления цефаклора из сложной реакции ацилирования.
Обнаружено, что можно селективно выделять цефаклор или его соль из смеси реакции ферментативного ацилирования, которая содержит ядро, фенилглицин и D-фенилглицинметиловый эфир, а также их соли, путем обработки реакционной смеси после ферментативного ацилирования антрахинон-1,5-дисульфокислотой или ее солью с щелочным металлом. Хотя антрахинондисульфокислота будет образовывать соли с иными перечисленными выше соединениями, добавление кислоты приводит к селективному осаждению соли цефаклора в соотношении 2:1, образованной с антрахиноном-1,5-дисульфокислотой, из смеси ферментативной реакции, что обеспечивает эффективный и требующий меньших затрат времени способ выделения цефаклора из смеси реакции ферментативного ацилирования. Удивительно то, что соль цефаклор/ кислота осаждается из смеси с высокой селективностью. Сама по себе соль цефаклор/кислота описана в Европейкой патентной заявке N 341991, опубликованной 15 ноября 1989 г.
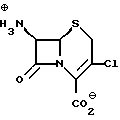
Способ по изобретению можно использовать для выделения цефаклора или его соли формулы I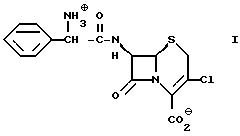
Ферментативный процесс протекает по схеме I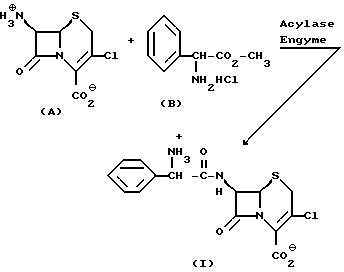
Используемый в ферментативном процессе фермент ацилаза может быть получен из любого известного микробного источника. Среди них есть микроорганизмы следующих родов: Xanthomonas, Pseudomonas, Aeromonas, Escherichia, Arthrobacter, Corynebacterium и Bacillus. Предпочтительно использовать пенициллинацилазу, полученную из Escherichia Coli АТСС 9637.
Ферментативное ацилирование и последующее выделение осуществляют в водной системе. Однако можно использовать подходящие органические растворители, и они включают этиленгликоль, низшие спирты (например метанол, этанол, изопропанол, 2-бутанол), ацетон и т.п. Ферментативное ацилирование можно проводить при температурах, описанных на уровне техники, а последующую стадию осаждения/выделения можно осуществлять при температурах между примерно 0o и примерно 25oC. Предпочтительный температурный диапазон составляет от 0o до 10oC.
Антрахинон-1,5-дисульфокислоту добавляют к смеси реакции ацилирования в количестве между примерно 0.5 моль и примерно 2 моль на моль цефаклора, которой нужно выделить. Предпочтительное мольное количество лежит между 0.5 моль и 0.7 моль кислоты на моль цефаклора, который нужно выделить. Кислота может быть в форме соли с щелочным металлом (натрий или калий).
Стадию осаждения/выделения можно осуществлять при pH между примерно 1.0 и примерно 4.0. Предпочтительный диапазон pH составляет от около 1.3 до около 1.7. pH можно контролировать добавлением подходящей кислоты, такой как соляная кислота, и/или основания, такого как триэтиламин.
После выделения соли цефаклор/кислота по известным методикам может быть образован моногидрат цефаклора. Например, соль можно растворить в смеси ДМФА/вода и для кристаллизации из нее сольвата цефаклор-ДМФА pH смеси можно поднять до примерно 5.7. После этого сольват ДМФА можно добавить в воде с низким pH (0.5-1.0) для растворения смеси и кристаллизовать из нее моногидрат цефаклора при pH 3.5.
Следующие неограничивающие примеры иллюстрируют изобретение.
Синтез I
7-(D-2-аммоний-2-фенилацетамидо)-3-хлор-3-цефем-4-карбоксилат, внутренняя соль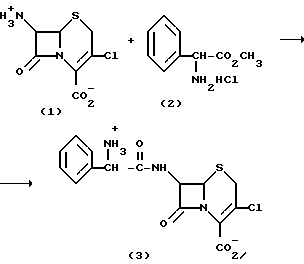
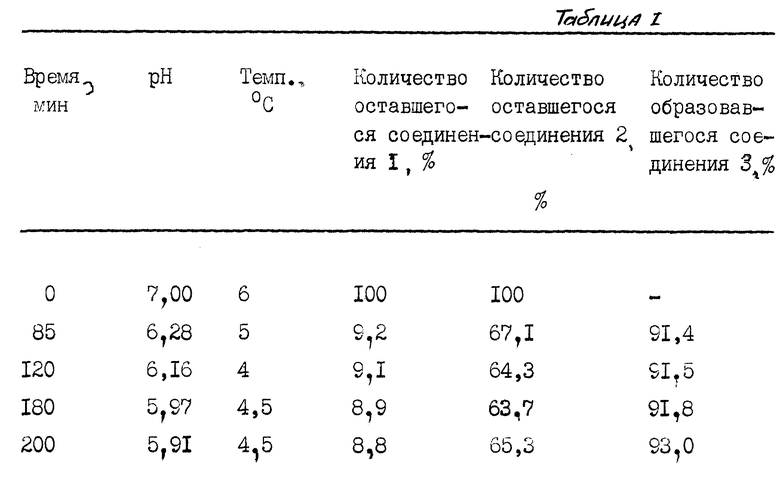
7-АССА (1) (0.9388 г, 4.0007 моль) и 96.0 мл H2O соединяют в химическом стакане. pH составляет 4.123. В стакан добавляют трехмолярный NH3 (1.78 мл). pH составляет 7.57. В стакан добавляют гидрохлорид D-фенилглицинметилового эфира (2) (4.7594 г, 23.602 ммоль). pH составляет 5,68. Смесь охлаждают до 5oC и для поднятия pH до 7.00 к смеси добавляют трехмолярный NH3 (1.90 мл). Добавляют фермент (6,1442 г, 940 м.е./г ядра). Согласно анализу ЖХВД достигнуты следующие результаты по скоростям реакции (таблица).
Когда время = 200 минут, смесь фильтруют (для удаления иммобилизованного фермента) с выходом указанного в заголовке продукта in situ 93%.
Пример 1
7-(D-2-аммоний-2-фенилацетамидо)-3-хлор-3-цефем-4-карбоксилат, внутренняя соль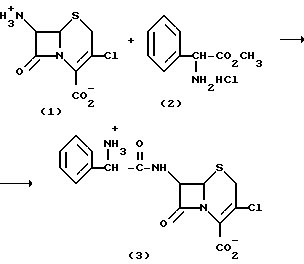
A. Ацилирование
(1) 7-АССА (1) (4.8338 г, 20 ммоль) и 150 мл H2O объединяют в химическом стакане. pH составляет 3,67. В стакан добавляют трехмолярный NH3 (8.40 мл). pH составляет 8.20. В стакан добавляют гидрохлорид D-фенилглицинметилового эфира (2) (23.0 г, 114 ммоль). pH составляет 5,29. Смесь фильтруют через гифлофильтр и промывают 10.0 мл воды. Объем смеси составляет 310 мл. Смесь переносят в стакан большего размера, с пропиткой ее 5 мл H2O. Смесь охлаждают до 1oC и к смеси добавляют трехмолярный NH3 (16,6 мл) для того, чтобы повысить pH до 7,28. Добавляют фермент (15,34 г, 500 м.ед./г ядра). Через 145 минут реакционную смесь фильтруют для удаления фермента. Выход продукта (3) in situ составляет 89.8%.
Б. Выделение
Реакционную смесь охлаждают до 5oC, и она имеет pH 6,65. Добавляют двунатриевую соль антрахинон-1,5-дисульфокислоты (72.3% чистоты, 10 ммоль) и смесь перемешивают в течение 5 минут. Температура смеси равна 4oC, pH=6.72. Добавляют концентрированную HCl (2.3 мл), что приводит к pH 2,4, и в смесь вносят затравку соли цефаклор/антрахинон-1,5-дисульфокислота. Смесь перемешивают еще 2 минуты, и pH составляет 3.3. Добавляют концентрированную HCl (3,9 мл), и pH смеси составляет 1.5. Смесь перемешивают еще 30 минут, и она имеет температуру 1oC и pH 1.4. Твердый осадок отфильтровывают и промывают 75 мл H2O, а затем 50 мл ацетона. Фильтрат содержит фенилгилицин и соединения (1) и (2). Осадок, соль соединения (3) с антрахинон-1,5-дисульфокислотой состава 2:1, содержит in situ 99.8% (3).
Пример 2
Выделение цефаклора в виде сольвата с ДМФА
В 250 мл химический стакан помещают соль цефаклор/антрахинон- 1,5-дисульфокислота (11.06/18.5 ммоль) и добавляют 123 мл раствора ДМФА/H2O 85/15. pH составляет 3,85. В смесь вносят затравку соли цефаклор/кислота и в течение 15 минут добавляют триэтиламин для того, чтобы довести pH до примерно 5.7. Смесь охлаждают до 18oC, добавили триэтиламин, и смесь перемешивают, поддерживая температуру около 20oC. Смесь фильтруют, и твердое вещество промывают 35 мл раствора ДМФА/H2O 85/15, а затем 20 мл ацетона, после чего твердое вещество сушат под вакуумом при 30oC.
Пример 3
Образование моногидрата цефаклора
Сольват цефаклора из примера 2 добавляют к раствору, содержащему 39 мл H2O, 0.07 г натриевой соли этилендиаминтетрауксусной кислоты в 1.88 мл концентрированной соляной кислоты, предварительно охлажденной до температуры между 15 и 20oC. Добавляют концентрированную соляную кислоту, после чего - триэтиламин. В смесь вносят затравку моногидрата цефаклора и перемешивают. При необходимости добавляют триэтиламин и смесь охлаждают до 0 - 5oC и перемешивают. После этого смесь фильтруют и твердое вещество промывают 20 мл охлажденной H2O. Твердое вещество оставляют сушиться на воздухе в вытяжном колпаке, с получением моногидрата цефаклора.
Изобретение относится к способу выделения цефаклора из реакционной смеси ферментативного ацилирования путем добавления антрахинон-1,5-дисульфокислоты или ее соли с щелочным металлом к названной смеси с последующим при необходимости подкислением соляной кислотой для выделения соли цефаклор/ антрахинон-1,5-дисульфокислоты в соотношении 1:2. Данное изобретение обеспечивает эффективный и требующий меньших затрат времени способ выделения. 1 с. и 8 з.п. ф-лы, 1 табл.
3. Способ по п. 2, отличающийся тем, что указанная реакционная смесь включает фенилглицин или его соль.
| Способ выделения цефалоспорина с | 1972 |
|
SU468430A3 |
| US 3676434 A, 11.07.72 | |||
| US 3816253 A, 11.07.74 | |||
| ЗАЖИМ ДЛЯ КРЕПЛЕНИЯ КАНАТА | 0 |
|
SU341991A1 |
Авторы
Даты
1999-02-20—Публикация
1994-02-07—Подача