Изобретение относится к медицинской микробиологии, в частности к технологии получения иммуномодулятора из коринебактерий неспецифического, инактивированного жидкого, способствующего иммунокоррекции. Кроме коррекции нарушений иммуносистемы неспецифические иммунопрепараты могут оказаться весьма ценными в комплексном лечении больных с онкологическими заболеваниями для усиления специфической химио- и радиолучевой терапии.
Из патентной литературы известен способ получения инактивированной вакцины, включающий выращивание микроорганизма на питательной среде с последующим его инактивированием /см. Mara M, Inter, Medcor Microbiol. Virol Parasitol. Infect. des, 1994, v. 288 (4), pp. 549-555/.
Предлагаемый способ получения неспецифического инактивированного жидкого иммуномодулятора из коринебактерий /Модкор/ включает выращиванием штаммов на питательной среде с последующим инактивированием. Предлагаемая технология отличается тем, что используют в качестве модифицированной питательной среды - сухой питательный агар /СПА/ по ФС 42Д-057ВС-96 с /0,2±0,05/% глюкозы и /0,15±0,05/% твина, pH /7,7±0,1/ при режиме стерилизации /112±1/oC в течение 30 минут, а в качестве выращиваемых штаммов используют штаммы Corynebacterium KT, получают микробную массу в пробирках, вскрывают ампулы с лиофильновысушенными культурами Corynebacterium KT, вносят в ампулы /0,25±0,05/ мл стерильного 0,9% раствора хлорида натрия, pH /7,2±0,1/, высевают каждый штамм после регидратации и получения взвеси на скошенный питательный агар, инкубируют посевы при температуре /336±0,5/oC в течение /46±2/ часов, просматривают выросшие культуры визуально на наличие характерного роста производственных штаммов и возможной контаминации другими видами бактерий, осуществляют контроль чистоты посевных культур микроскопией мазков, окрашенных по Граму, пересевают чистые культуры Corynebacterium, содержащие полиморфные грамположительные палочки /C. KT N 226/ и грамположительные коккобациллы /C. KT N 227/ с характерным дифтероидным расположением, на пробирки со средой, инкубируют при /36±0,5/oC /46±2/ часов, осуществляют повторную проверку на контаминацию, смывают 0,9% раствором хлорида натрия /полученная суспензия представляет собой исходную посевную, маточную культуру/, осуществляют массовый посев пробирок с плотной питательной средой, инкубируют посевы при /36±0,5/oC в течение /46±2/ часов, смывают выросшую культуру с каждой пробирки после визуального просмотра на однородность и типичность 0,9% раствором хлорида натрия и сливают каждый штамм в отдельности в стерильный стеклянный сосуд, доводят полученные густые суспензии до 10 единиц мутности по ОСО 42-28-59-85 ГИСК им. Л.А. Тарасевича, соединяют суспензии в равных объемах и прогревают в водяной бане при температуре /80±1/oC в течение 1 часа для инактивации бактериальной взвеси, высевают инактивированную суспензию на пробирку питательного агара с /0,2±0,05/% глюкозы и /0,45±0,05/% твина для проверки отсутствия специфического роста, препарат разливают по /0,7±0,05/ мл и ампулируют, проводят контроль стерильности и биологический контроль готового препарата.
Достигаемый изобретением результат заключается в получении препарата, способствующего иммунокоррекции, что является важной проблемой в комплексной терапии онкологических заболеваний, т. к. при онкологических заболеваниях происходят нарушения всей иммунной системы организма, как клеточного, так и гуморального иммунитета.
Использование полученного препарата обеспечивает возможность восстановления общей иммунорезистивности организма больных, что возможно, повышает их способность к естественным, физиологическим формам борьбы с гетерогенными для организма факторами. При применении получаемого препарата, относящегося к неспецифическим иммуномодуляторам, в онкологии отмечены: стимуляция лейкопоэза, активность макрофагов и лейкоцитов, увеличение числа и активности лимфоцитов, усиление комплементарной активности крови. Все это приводит к существенному повышению противоопухолевой резистентности организма больного.
Данные экспериментальных исследований и ограниченных клинических испытаний по лечению онкологических больных этим препаратом позволяют сделать заключение об эффективности его применения в комплексном лечении больных, которое проявляется: усилением цитотоксичности, по отношению к клеткам с нарушенными параметрами, ускорением клиренса и перевариванием метаболитов и продуктов разрушения опухолевых клеток, в результате чего, у больных наблюдается исчезновение токсикоза, угнетением роста опухоли и подавлением процесса метастазирования, усилением эффективности и снижением токсичности антибластомных препаратов, сокращением до минимума или отменой переливания крови, кровезаменителей, отменой необходимости длительного применения противоболевых фармацевтических препаратов, увеличением продолжительности жизни больных онкологическими заболеваниями, резким снижением частоты вторичных бактериальных инфекций, связанных с условнопатогенными микроорганизмами.
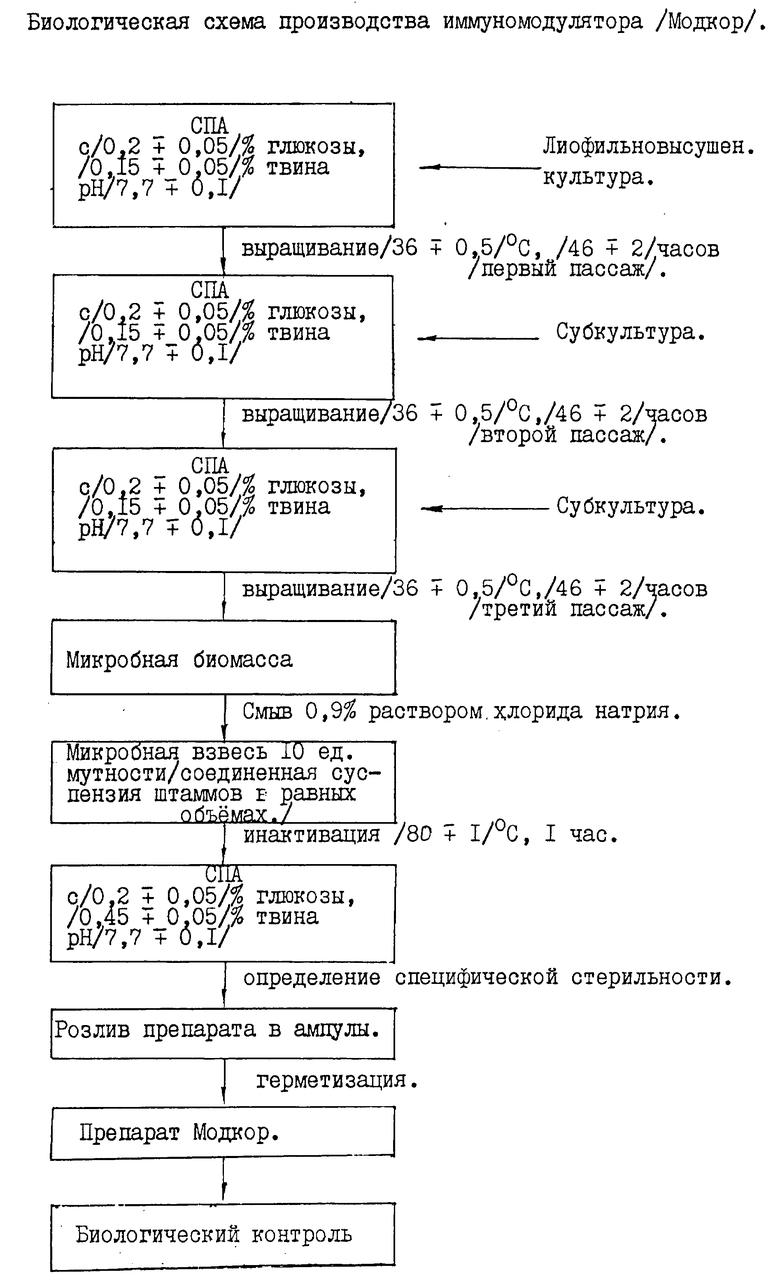
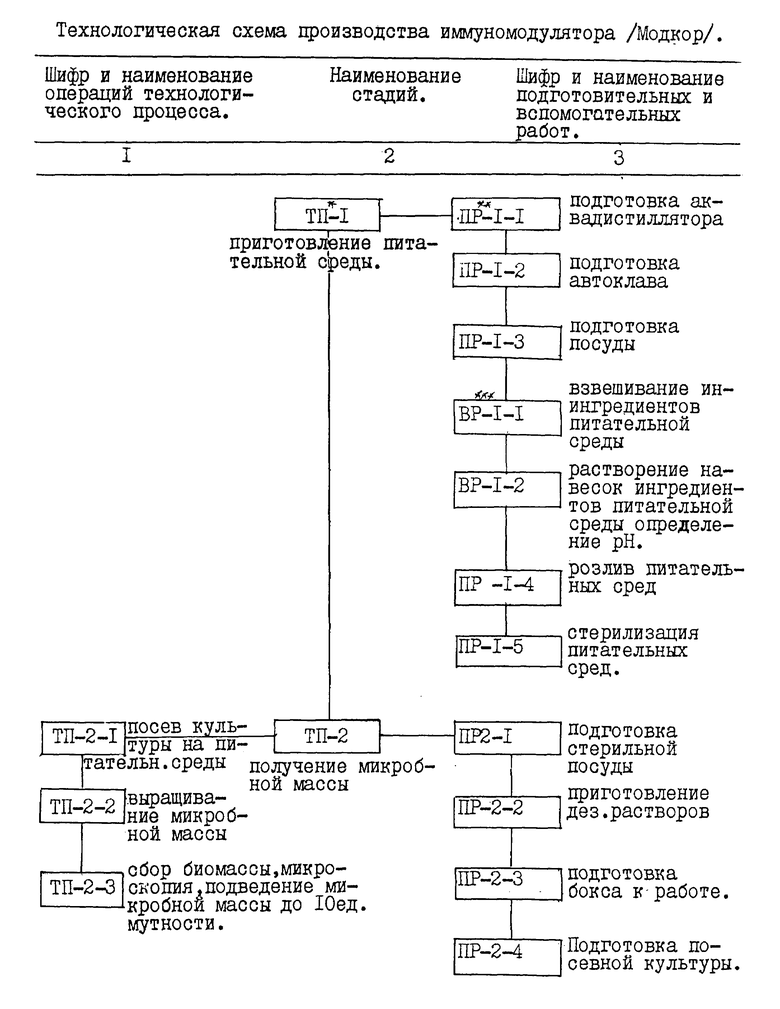
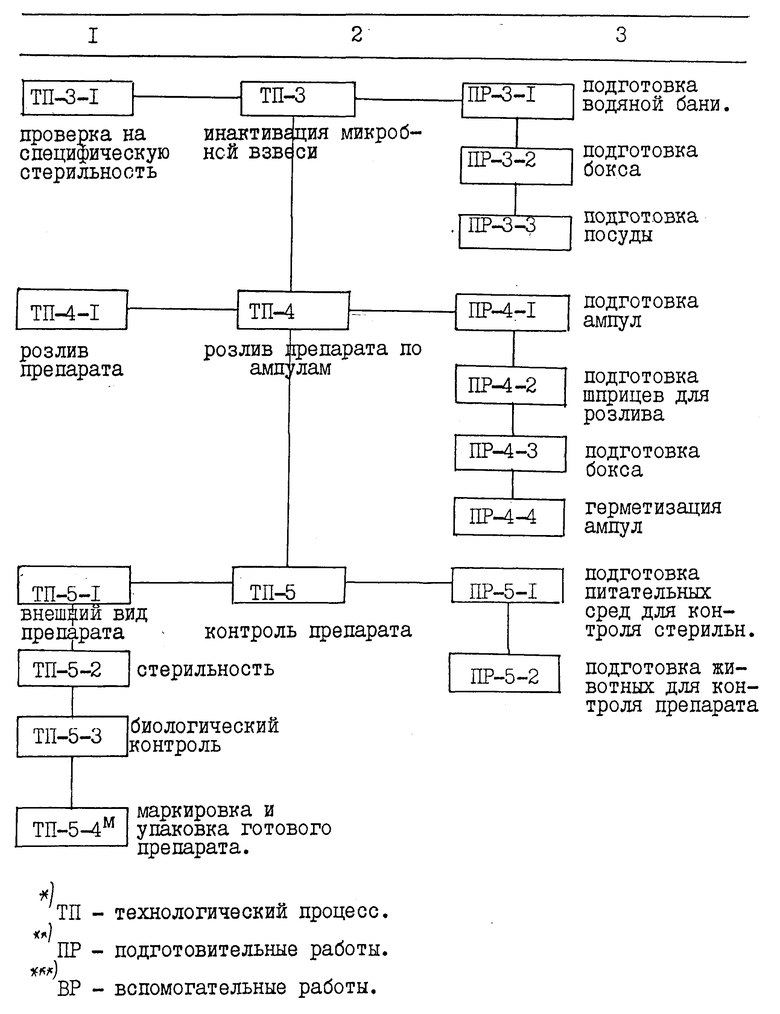
Предлагаемый способ получения иммуномодулятора из коринебактерий неспецифического, инактивированного жидкого /Модкор/ включает следующие основные стадии: приготовление питательной среды; получение микробной массы; инактивацию микробной взвеси; розлив препарата по ампулам; контроль препарата.
Стерилизацию предварительно обработанной посуды из нейтрального стекла, чашек Петри, пробирок, пипеток, флаконов, ампул проводят раствором хлорида натрия и дисциллированной воды при температуре /127±1/oC, в течение /1±0,1/ часа. По этому же режиму проводят обезвреживание инфицированного материала; стерилизацию плотной питательной среды проводят при температуре /120±1/oC, в течение /30±1/ минут; стерилизацию питательных сред с углеводами проводят при температуре /110±1/oC, в течение /20±1/ минут.
Среды готовят в соответствии с указаниями на этикетках. Все ингредиенты перемешиваются и доводятся до полного растворения компонентов в дистиллированной воде при нагревании. Доводят среду до кипения. Питательную среду разливают по флаконам. В питательную среду для получения биомассы СПА добавляют /0,2± 0,05/% глюкозы и /0,15±0,05/% твина; в СПА для контроля специфической стерильности добавляют /0,2±0,05/% глюкозы и /0,45±0,05/% твина.
При изготовлении препарата используют дезрастворы:
1. Раствор перекиси водорода с объемной долей 6% для обеззараживания посуды.
2. Раствор перекиси водорода с объемной долей 3% и моющим порошком с массовой долей 0,5% - для обработки боксов и термальных комнат.
При получении микробной массы ампулы с сухой культурой производственных штаммов обрабатывают ватным тампоном со спиртом и стерильно вскрывают. Во вскрытую ампулу с сухой культурой производственного штамма стерильно в пламени горелки пастеровской пипеткой вносят /0,25±0,05/ мл стерильного 0,9% раствора хлорида натрия. После суспендирования содержимое ампулы пипеткой переносят в пробирки со средой. Пробирки помещают в термостат при /36±0,5/oC на /46±2/ часов.
Выросшую культуру просматривают визуально на наличие характерного роста и контаминацию посторонней флорой. Контроль чистоты посевной культуры осуществляют микроскопией мазков, окрашенных по Граму.
Чистая культура, например, штамм C. KT N 226 представляет собой полиморфные грамположительные палочки, штамм C. K N 227 - грамположительные коккобациллы с характерным дифтероидным расположением. В случае контаминации посторонней флорой пробирки с ростом бракуют. После проверки культуры на чистоту с каждой пробирки делают пересевы на модифицированную плотную питательную среду. Пробирки помещают в термостат, инкубируют при /36±0,5/oC в течение /46±2/ часа.
Далее выросшую культуру с каждой пробирки после проверки на бактериологическую чистоту и типичность морфологии клеток смывают 0,9% раствором хлорида натрия. Полученные суспензии представляют собой посевные /маточные/ культуры для массового посева. Посевы инкубируют при /36±0,5/oC в течение /46±2/ часа.
Выращенные при /36±0,5/oC в течение /46±2/ часа культуры после визуального просмотра смывают со скошенного агара 0,9% раствором хлорида натрия. Микробную суспензию каждого штамма смывают в отдельный стерильный стеклянный флакон.
Суспензию контролируют на биологическую чистоту и типичность морфологии клеток. Полученные бактериальные взвеси не должны быть контаминирорваны посторонней флорой. Густоту полученной микробной суспензии определяют с помощью стандарта мутности ГИСК им. Л.А. Тарасевича. Затем суспензию доводят до 10 единиц мутности по ОСО 42-28-5985. Полученные взвеси соединяют в равных объемах.
Инактивацию микробной взвеси проводят в водяной бане при температуре /80±1/oC. Проверку на специфическую стерильность проводят из каждой емкости инактивированной суспензии после 18-20 часов хранения при температуре /20±2/oC; делают высев на чашки и пробирки со скошенной питательной средой. Посевы инкубируют при /36±0,5/oC в течение 5 суток. Флаконы с суспензией до розлива препарата по ампулам хранят при температуре /8±2/oC.
Используют ампулы типа ШП, стекло марки ОСТ 64-485-85 вместимостью 3 мл. Розлив препарата проводят по /0,77±0,05/ мл. Ампулы после розлива немедленно отпаивают. Запаянные ампулы проверяют на герметичность по РД 42-28-29-86. Контроль стерильности препарата на производстве и в ОБТК /отдел биологического технологического контроля/ проводят по методике, изложенной в ГФ, изд. XI, Вып. 2, с. 183. Проведение биологического контроля осуществляют по ГФ изд. XI, Вып. 2 и по РД 42-28-10-90.
Препарат должен отвечать следующим требованиям: иметь вид бесцветной, мутной жидкости с осадком, легко разбивающимся при встряхивании, в мазке, окрашенном по Граму, должны быть грамположительные полиморфные палочки и коккобациллы с характерным расположением для коринебактерий, быть стерильным, быть не токсичным для белых мышей, морских свинок, обладать иммуногенной активностью, определяемой в тесте гиперчувствительности замедленного типа /ГЗТ/ к эритроцитам барана.
Препарат Модкор должен обладать иммуногенной активностью, которая определяется в тесте гиперчувствительности замедленного типа /ГЗТ/ к эритроцитам барана /ЭБ/. ГЗТ определяют по методике, изложенной в РД 42-28-10-90. Мышей разделяют на 3 группы. Мышей первой группы иммунизируют исследуемым препаратом, мыши второй группы - интактные /положительный контроль/, мыши третьей группы - интактные с введением только разрешающей дозы ЭБ /контроль/. Мышам первой и второй групп вводят ЭБ без адъюванта Фрейнда в дозе 107 клеток/на мышь в объеме 0,2 мл в межлопаточную область подкожно, мышам первой группы параллельно внутрибрюшинно водят исследуемый препарат в дозе 5•106 клеток/на мышь в объеме 0,5 мл. Разрешающую дозу ЭБ 2•107 клеток/на мышь вводят на пятый день в объеме 0,0- мл в подушечку задней лапы, в подушечку контрлатеральной лапы - 0,02 мл 0,9% раствора хлорида натрия всем трем группам животных. При учете результатов местную реакцию на введение разрешающей дозы ЭБ оценивают через 18-20 часов путем определения веса опытной (Pо) и контрольной (Pк) лапок. Интенсивность местной реакции определяют по индексу реакции (ИР), рассчитываемому по формуле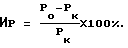
Значение ИР в опытной (первой) группе выше двух его значений в положительном контроле (второй группе) и интактной (третьей) группе следует оценивать как выраженный иммуностимулирующий эффект препарата. Результаты исследований показали, что препарат Модкор оказывает стимулирующее действие на формирование ГЗТ на гетерологичный антиген (ЭЭБ). При оценке специфической иммуностимулирующей активности препарата эффект составлял не менее 50%.
Экспериментальные исследования инактивированного жидкого иммуномодулятора и коринебактерий Модкор на иммунную систему проведены в рамках общей программы изучения безопасности препарата на стадии его доклинического изучения в соответствии с требованиями РД 42-28-10-90 Минздрава РФ. Оценены изменения показателей гуморального и клеточного иммунитета у экспериментальных животных при введении им терапевтической дозы Модкор по следующим тестам: количественное содержание T- и B-лимфоцитов, формирование антителообразующих клеток (АОК) и гиперчувствительности замедленного типа (ГЗТ) на гетерологический антиген (эритроциты барана - ЭБ), фагоцитарная активность макрофагов, функциональная активность лифоцитов по спонтанной и митогениндуцированной бласттрансформации.
1. Показано стимулирующее действие на процесс созревания и формирования T- и B-лимфоцитов, эффект воздействия препарата выявлялся при исследовании через 7 суток после выделения препарата.
2. Модкор оказывал иммуномодулирующее действие на развитие иммунного ответа на гетерологичный антиген - ЭБ, о чем свидетельствует увеличение количества АОК к ЭБ в селезенке мышей в 1,4-1,5 раза.
3. Выявлена стимуляция ГХТ на ЭБ при введении Модкора экспериментальным животным. Индексы реакции составили: 20,5±3,57 и 26,9±1,89% в опытных группах и 12,8±1,11 - в контрольной.
4. Стимуляция фагоцитарной активности отмечена на 7 и 14 день после введения препарата. Значения процента фагоцитоза составили 47,6±3,9 и 42,7±4,5, в контрольной группе 36,0±4,0 и 37,0±2,7, значения индекса стимуляции составили 1,32 и 1,18 соответственно срокам исследования.
5. Препарат Модкор вызывал митогениндуцированную пролиферацию спленоцитов на 7 и 14 сутки. Эффект зависел от вида митогена и срока учета результатов. На основании проведенного экспериментального изучения влияния препарата Модкор на иммунную систему был отобран 1 тест (определение ГЗТ на ЭБ) для внесения в фармакопейную статью для контроля качества серий препарата при их производственном выпуске.
Проведенные исследования показывают, что выбранные тесты подтверждают иммуномодулирующее действие (активность) препарата Модкор.
Изобретение относится к области медицины, а именно к медицинской макробиологии, и касается способа получения неспецифического инактивированного жидкого иммуномодулятора из коринебактерий. Сущность изобретения заключается в выращивании двух штаммов Corymbacterium КТ N 226 и N 227 в отдельных пробирках на модифицированной питательной среде, содержащей сухой питательный агар с 0,2±0,05 глюкозы и 0,15±0,05% твина, рН 7,7±0,1, смывании выросшей культуры с каждой пробирки 0,9%-ным раствором хлорида натрия, доведении полученных густых суспензий до 10 единиц мутности, объединении суспензий в равных объемах и прогревании на водяной бане при температуре 80±1oC в течение 1 ч для инактивации. Технический результат заключается в получении препарата, способствующего иммунокоррекции. 1 з. п.ф-лы.
| Mara M., Jucak J., Bednar M., et al.,Jnt | |||
| J | |||
| Med | |||
| Microbiol | |||
| Virol | |||
| Parasitol | |||
| Jnfed des., 1994, V.288/4/, PP.549 - 555 | |||
| RU 2052502 C1, 1996 | |||
| EP 0433744 A1, 1991.ER 2269961 A1, 1975 | |||
| Руководство по вакционному и сывороточному делу/Под ред | |||
| Бургасова П.Н | |||
| - М.: Медицина, 1978, с.139 - 157, |
Авторы
Даты
1999-03-10—Публикация
1997-12-08—Подача