Изобретение относится к способу селективного окисления олефинов с получением продуктов, содержащих эпоксидные функциональные группы. Главным образом, настоящее изобретение относится к процессам, в которых источники активного кислорода, такие как органические гидроперекиси или перекись водорода, реагируют с этиленово-ненасыщенным веществом в присутствии катализатора на основе цеолитов с относительно большим объемом пор, содержащих титан, с образованием эпоксида. Такой катализатор характеризуется структурой решетки, которая изоморфна, бета-цеолиту, состоящему из кремния и титана, но, практически не содержит решеточного алюминия.
В настоящее время разработано большое число способов получения эпоксидов. Один из таких способов заключается в осуществлении реакции жидкофазного эпоксидирования олефина с использованием в качестве окисляющего агента органической гидроперекиси, а в качестве катализатора - некоторых растворимых соединений переходного металла. Хотя такой подход реализован в промышленном масштабе и, как правило, обеспечивает высокую селективность по эпоксиду, имеется, по крайней мере два характерных признака, которые ограничивают гибкость процесса и повышают стоимость производства. Так, использование органической гидроперекиси приводит к побочному получению спирта, образующего из гидроперекиси в ходе эпоксидирования, на каждый эквивалент эпоксида образуется примерно 1 эквивалент такого побочного продукта. Если рынок сбыта для такого спирта отсутствует, то такой побочный продукт должен быть подвергнут дополнительным химическим превращениям (что вызывает дополнительные производственные расходы) для обратного получения гидроперекисного окислителя, или должен быть реализован способ получения другого соединения, на которое существует коммерческий спрос. Проблематичным представляется также регенерация растворимого металлического катализатора для его дальнейшего использования в рассматриваемом процессе. В связи с этим, существует большая потребность в создании нерастворимого (гетерогенного) катализатора эпоксидирования, обладающего высокой активностью и селективностью действия при его применении с таким окислителем, как перекись водорода, который в ходе реакции не образует органического побочного продукта. В идеальном случае такой катализатор должен в активной форме легко выделяться из реакционной смеси, полученной в результате эпоксидирования путем фильтрации или аналогичных методов, либо должна существовать возможность его применения в виде неподвижного слоя и т.п.
Недавно в трудах Политехнического Университета Валенсии было сообщено о синтезе кремнийалюмината титана, изоморфного бета-цеолиту (см. работу Камблора с сотр. в J. Chem. Soc. Chem. Commun. с. 589-590 (1992), Камблора с сотр. в Zeolites 13, с. 82-87 (1993) и ES 2037596 (опубликованный 6/16/98). Было обнаружено, что такие алюминий-содержащие вещества катализируют окисление алканов в спирты, кетоны и т.п. при использовании и т.п. при использовании в качестве окислителя перекиси водорода. Однако такой тип кремнийалюмината титана в немодифицированной) (полностью протонированной) форме является плохим катализатором реакции получения эпоксидов из олефинев (см. работу Сато с сотр. J.Chem. Soc. Chem. Comm. 1887-1888 (1994).
Авторы настоящего изобретения неожиданно установили тот факт, что титансодержащие цеолиты, характеризующиеся тем, что их матричная структура изоморфна бета-цеолиту и состоит из атомов Si и Ti, но практически не содержит матричного алюминия, может быть получена двумя различными методами синтеза. В одном из таких способов используется комбинация стадий деалюминирования и внедрения титана, тогда как в другом применяются соединения бензил-замещенного аммония. Такие молекулярные сита селективно катализируют эпоксидирование олефинов при использовании органической гидроперекиси или предшественника перекиси водорода.
Изобретение поясняется с помощью представленных рисунков.
На фиг. 1 представлена рентгеновская дифрактограмма образца титансодержащего молекулярного сита, приготовленного согласно методике примера 1. На фиг. 2 представлена рентгеновская дифрактограмма образца титансодержащего молекулярного сита, приготовленного с использованием методики согласно примеру 2. На фиг. 3 представлен спектр 13C-ЯМР бензил-замещенного производного аммония при различном окружении.
В соответствии со способом эпоксидирования по настоящему изобретению олефин контактирует с органической гидроперекисью или перекисью водорода или предшественником органической гидроперекиси или перекиси водорода в условиях реакции, в присутствии каталитически-эффективного количества титансодержащего молекулярного сита. Титансодержащее молекулярное сито, подходящее для использования в настоящем процессе, характеризуется матричной структурой, изоморфной бета-цеолиту. Атомы Si и Ti присутствуют в матричной структуре (как правило, в виде оксидов). Матрица молекулярного сита в значительной степени не содержит алюминия (Al) однако, было установлено, что присутствие значительных количеств алюминия оказывает негативное влияние на молекулярные сита в качестве катализаторов эпоксидирования, если протоны, связанные с алюминием не замещены на аммиак, щелочной металл или катионы щелочноземельного металла. В контексте оказанного выше, термин "практически не содержащий" относится к матричной структуре молекулярного сита, содержащего менее 1000 ч/млн. Al. Предпочтительно, чтобы в матричной структуре присутствовало менее 500 ч/млн. Al. Наиболее предпочтительно, чтобы это количество составляло менее 100 ч/млн. Молярное соотношение Si к Al (Si:Al), предпочтительно, составляет, по крайней мере 750, более предпочтительно, по крайней мере, 1000, однако оно может иметь значение более 3000.
Цеолит-бета характеризуется отверстиями пор из 12-членного кольца и трехмерной взаимосвязанной канальной системой, такая матричная структура наиболее полно раскрыта в патенте США N 3308069, работе Шостака в Handbook of Hobecular Sieres, с. 92-96, работе Хиджина с сотр, в Zeolites 8,446 (1986) и в работе Триси с сотр. в Nature, 332,249 (1988). Таким образом, катализатор по настоящему изобретению имеет структуру, которая фундаментально отличается от структур других титансодержащих молекулярных сит, о которых сообщалось в литературе (например катализатора TS-1, описанного в патенте США N 4410501, который имеет структуру MFI, катализатора TS-2, описанного Редди с сотр. в Appl. Cat 58, 11 (1990), который имеет структуру ZSM-11 полностью окисно-кремниевого Ti/ZSM-48, описанного Серрано с сотр. в J. Chem. Commun 745 (1990).
Согласно предпочтительным вариантам выполнения изобретения титансодержащие молекулярные сита имеют относительно крупные поры (в среднем, имеющие размер 6 ангстрем или более) и характеризуются цеолито-подобной структурой, состоящей из Si и меньшего количества Ti. Обычно для них желательно значение кристалличности более 75%.
Метода синтеза, описанные в указанных выше ссылках, способны обеспечивать кристалличность, превышающую 95%. Предпочтительно, чтобы молярное соотношение Ti:Si составляло 1:99,9-20:80, причем особенно предпочтительные соотношения лежат в интервале 1:99 - 15:85. Предпочтительно, когда титансодержащее молекулярное сито имеет содержание титана - 1-10 вес.%.
Предпочтительная общая формула титансодержащего молекулярного сита имеет вид:
SiO2:Y Ti O2
в которой Y имеет значение в интервале 0,01-0,25 (предпочтительно, 0,02-0,20).
Предпочтительные способы синтеза практически свободных от Al титансодержащих молекулярных сит, являющихся предметом настоящей заявки, включают использование соединений бензил-замещенного аммония. Без конкретных теоретических рассуждений можно предположить, что соединения бензил-замещенного аммония выполняют функции шаблона регулирующего образование требуемого структурного каркаса цеолита-бета из реагентов, служащих источниками Si и Ti. При этом они также обеспечивают получения целевого продукта, действуя как буфер, или структурно-регулирующий агент. Используемый в тексте описания термин "шаблон" не подразумевает, что соединения бензил-замещенного аммония фактически участвуют в матричном механизме. Использование соединений бензил-замещенного аммония для получения катализаторов настоящего изобретения является выгодным в том отношении, что такой метод обеспечивает получение молекулярных сит, которые являются менее кислотными, содержат меньшее количество вне-каркасного Ti (например анатаз) и содержат меньшее число дефектов, чем молекулярные сита, полученные методом деалюминирования/внедрения, который будет описан ниже. Неожиданно было установлено, что лишь соединения бензил-замещенного аммония способны надлежащим образом функционировать в качестве шаблона для указанных целей, такие соединения тетраалкиламмония, как соли тетраэтил аммония, традиционно применяющиеся в качестве шаблонов в синтезах других титансодержащих молекулярных сит, не способны обеспечивать получение высококристаллических продуктов высокой чистоты. Без каких-либо теоретических рассуждений можно предположить, что решающее значение (шаблонов) используемого типа связано с отсутствием в таких синтезах каких-либо соединений алюминия. Предполагается, что бета-структура является неустойчивой кинетической фазой, которая кристаллизуется лишь в очень специфических условиях. Высказанное предположение не согласуется с относительной легкостью получения молекулярных сит, имеющих MFI-структуру (например, TS-1, ZSM-5, силикаты) с помощью матрично-регулирующих методов, такие вещества могут кристаллизоваться при использовании большого числа матриц.
Подходящие соединения бензил-замещенного аммония включают соединения четвертичного аммония, содержащие, по крайней мере, один атом азота, замещенный бензильной группой  Предпочтительным является тот случай, когда каждый азот имеет лишь одну бензильную группу, а другие группы, присоединенные к атому азота, предпочтительно, представляют собой алкильные группы (так например, попытки использования в качестве шаблона гидроксид дибензилдиметиламмония к настоящему времени оказались безуспешными).
Предпочтительным является тот случай, когда каждый азот имеет лишь одну бензильную группу, а другие группы, присоединенные к атому азота, предпочтительно, представляют собой алкильные группы (так например, попытки использования в качестве шаблона гидроксид дибензилдиметиламмония к настоящему времени оказались безуспешными).
Предпочтительные соединения бензил-замещенного аммония, используемые в качестве шаблонов в синтезах свободных от Al титансодержащих цеолитов, имеющих структуру бета, включают дичетвертичные соединения, содержащие два атома азота в одной и той же молекуле, причем каждый атом азота имеет четыре углеводородных заместителя, один из которых представляет собой бензильную группу. Такие атомы азота соединены посредством органического фрагмента, имеющего алифатическую нормальную, разветвленную, циклическую), ароматическую или смешанную алифатически-ароматическую природу. Предпочтительно, атомы азота отделены друг от друга, по крайней мере, двумя, но не более, чем шестнадцатью, углеродными атомами. Согласно особенно предпочтительному воплощению, такой шаблон представляет собой соединения 4,4-триметилен-бис(N-бензил-N-метилпиперидиния), отвечающие структуре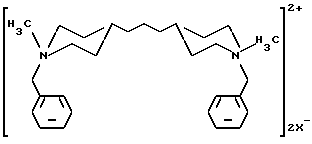
в которой X, предпочтительно, представляет собой галоген (например Br) или гидроксил (OH).
В соответствии с одним из методов, в котором соединения бензил-замещенного аммония могут применяться в качестве шаблона матрицы для синтеза молекулярного сита, являющего предметом настоящего изобретения, солюбилизированный частичный гидролизат получают путем реакции способных к гидролизу соединений кремния и титана с водой в кислых условиях. Используемый в контексте настоящего описания термин "способный к гидролизу" относится к соединению, способному выполнять функции источника SiO2 или TiO2 для структуры кристаллического титансодержащего молекулярного сита в ходе реакции с водой. Хотя такая реакция гидролиза может осуществляться в любом порядке, предпочтительно осуществлять реакцию способного к гидролизу соединения кремния с водой перед гидролизом способного к нему соединения титана.
В качестве способного к гидролизу соединения кремния может использоваться любое соединение, функционирующее, как источник SiO2 (оксида кремния), включающее, например аморфный оксид кремния или белую сажу, либо, что более предпочтительно, такой тетраалкоксисилан, как тетраэтилортосилакат и т.п. Подходящими, способными к гидролизу соединениями титана являются такие соединения, которые служат источниками TiO2 (оксид титана), например, галогенид титана (например TiCl4) или, что более предпочтительно, такой алкилат титана, как тетрабутилат титана и т.п.
Неполный гидролиз указанных выше реагентов катализируется таким кислотным катализатором, как например минеральная или органическая кислота. Лучше всего использовать такую разбавленную (<0,2М) минеральную кислоту, как хлористоводородная кислота. Неполный гидролиз может осуществляться в любом растворителе, способном растворять образующийся неполный гидролизат. В соответствии с особенно предпочтительным вариантом, в качестве растворителя для реакции гидролиза используются вода и/или такой алифатический спирт, как этанол или изопропанол. Температура гидролиза выбирается таким образом, чтобы обеспечить неполный гидролиз, а не избыточный гидролиз, поскольку в результате протекания избыточного гидролиза могут образовываться нерастворимые формы SiO2 и/или TiO2. Для таких целей, как правило, подходят температуры в интервале 0-50oC. Вода контактирует с указанными выше реагентами в течение времени (обычно, 0,5-12 часов), достаточного для образования растворимого неполного гидролизата, который характеризуется отсутствием осажденных диоксидов кремния и титана. Хотя точная структура растворимого неполного гидролизата неизвестна, предполагается, что она включает удлиненный каркас из атомов Si и Ti, связанных друг с другом мостиковыми атомами кислорода, причем такая структура содержит достаточное количество некислородных заместителей, связанных с атомами Si и Ti, таких как алкоксигруппы и т.п., обеспечивающих растворимость каркаса в гидролизной среде.
Затем, растворимый неполный гидролизат обрабатывают каталитическим количеством бензил-замещенного аммония, эффективным для осуществления дополнительного гидролиза, в результате которого образуется твердый аморфный гель SiO2-TiO2. В системе должно присутствовать достаточное количество бензил-замещенного аммония для того, чтобы нейтрализовать кислоту и сделать гидролизную среду щелочной. Обычно указанный гель осаждается из гидролитической среды и его можно выделять такими любыми подходящими способами, как фильтрация, центрифугирование, декантация и т.п. По не вполне понятным причинам, как это было установлено, использование бензил-замещенного аммония, а не других типов оснований, например аммиака, обеспечивает успешное получение кристаллического, свободного от Al, титансодержащего молекулярного сита, имеющего структуру цеолита-бета. Гидролиз растворимого неполного гидролизата приводит к образованию твердого аморфного геля SiO2-TiO2. Такой гель может непосредственно использоваться, как матрица для импрегнирования, или, если это желательно может отделяться от остающихся жидких компонентов (например от растворителя) путем сушки, фильтрации или каких-либо других методов.
Твердый гель приводится в контакт с раствором бензил-замещенного аммония в среде растворителя для получения импрегнированного геля таким образом, чтобы реализовать предпочтительный вариант, когда шаблон главным образом, содержится в порах геля. Общее количество бензил-замещенного аммония на стадиях гидролиза и пропитки, предпочтительно, составляет 50% (более предпочтительно, 20%) от количества, которое необходимо для заполнения имеющегося объема пор геля. В то же время, предпочтительно, чтобы количество растворителя (который, предпочтительно, представляет собой такое полярное соединение, как вода и/или спирт) было достаточным для растворения бензил-замещенного аммония, но не избыточным для того, чтобы приводить к образованию суспензии геля в указанном растворителе (например способной к свободному истечению и перекачке суспензии геля в жидком растворителе). Для указанных целей может с успехом применяться техника влажного импрегнирования. Контактирование твердого геля и бензил-замещенного аммония осуществляется в течение такого времени и при такой температуре, которые обеспечивают внедрение матрицы-шаблона в поры геля (обычно, это время 0,25-24 часа при температуре 0-50oC). Затем импрегнированный гель нагревают при температуре 120-160oC (более предпочтительно, при 130-140oC) в течение времени, являющегося эффективным для получения желаемого титансодержащего молекулярного сита. Как правило высокие выходы продукта обеспечиваются за период 1-14 дней. Предпочтительно, чтобы импрегнированный гель в ходе нагревания не перемешивали.
Относительные соотношения различных реагентов при получении импрегнированного геля могут изменяться по желанию, но так, чтобы оказывалось благоприятное влияние на элементный состав конечного титансодержащего молекулярного сита. Состав импрегнированного геля в терминах молярных соотношений, в том случае, когда бензил-замещенный аммоний представляет собой дичетвертичное соединение, может быть следующим:
DiO2/TiO2 5-20, предпочтительно, 10-100
X-/SiO2 0,002-1, предпочтительно, 0,05-0,6
H2O/SiO2 0,1-10, предпочтительно, 1-5
M+/SiO2 0-0,5, предпочтительно около 0
DQ2+/SiO2 0,005-2,0, предпочтительно, 0,025-1,0
где М+ представляет собой такой металлический катион, как Na+ или K+ (предпочтительно, когда катионы щелочного металла отсутствуют), DQ2+ представляет собой дикатионную часть дичетвертичного соединения аммония, а X- представляет собой анион, связанный с дичетвертичным соединением аммония (предпочтительно, Br2 или OH-).
Согласно альтернативному подходу, титансодержащее молекулярное сито по настоящему изобретению может быть получено с использованием соединения бензил-замещенного аммония в синтезе с применением растворителя. Такой способ предусматривает образование смеси, предпочтительно, в растворе, из способного к гидролизу соединения кремния, способного к гидролизу соединения титана и соединения бензил-замещенного аммония и гидротермальную обработку указанной смеси при температуре 100-200oC (более предпочтительно, при 120-180oC) в течение времени, являющегося эффективным для образования кристаллического титансодержащего молекулярного сита. Наиболее предпочтительно проводить такую гидротермальную обработку в водной среде (которая, помимо воды, может содержать такой смешивающийся с водой органический растворитель, как спирт) в таких условиях, которые обеспечивают гидролиз соединений кремния и титана. Если желательно, то такой гидролиз может катализироваться основанием. Для таких целей могут использоваться любые из описанных ранее способных к гидролизу соединений кремния, титана и соединений бензил-замещенного аммония. В тех случаях, когда в качестве соединения бензил-замещенного аммония используется дичетвертичное соединение, предпочтительные молярные соотношения компонентов в исходном, реагенты могут бить следующими:
SiO2/TiO2 - 5-2000
X-/SiO2 - 0,1-2,0
H2O/SiO2 - 20-200
DQ2+/SiO2 - 0,1-2,0
где X- представляет собой анион, связанный с дичетвертичным соединением аммония, а DQ2+ представляет собой дикатион, связанный с дичетвертичным соединением аммония. Подходящим методом получения указанной смеси может служить следующий: сначала осуществляют неполный гидролиз способного к нему соединения кремния вначале проводят путем реакции указанного соединения с водой, содержащей часть соединения бензил-замещенного аммония (в гидроксидной форме). Затем полученный продукт неполного гидролиза объединяют со способным к гидролизу соединением титана (и, необязательно, с дополнительным количеством способного к гидролизу соединения кремния). Затем добавляют оставшуюся часть соединения бензил-замещенного аммония с образованием геля-предшественника. Любые летучие побочные продукты, которые образуются в результате гидролиза (как, например спирты, образующиеся в том случае, когда способное к гидролизу соединение кремния представляет собой тетраалкилортосиликат, или когда способное к гидролизу соединение титана представляет собой тетраалкилат титана), если это желательно, могут удаляться любыми подходящими способами, например дистилляцией или выпариванием до гидротермальной обработки. Такую гидротермальную обработку лучше всего проводить в автоклаве или в другом закрытом реакторе при автогенном давлении. Как правило, за период от 8 до 20 дней обеспечивается образование титансодержащего молекулярного сита в кристаллической, осажденной форме. Обычно, оптимальные результаты достигаются при длительности гидротермальной обработки около четырнадцати дней. Такие кристаллы, которые обычно содержат матрицу-шаблон из бензил-замещенного аммонийного соединения, могут быть выделены из маточной жидкости такими подходящими способами, как фильтрация, декантация, центрифугирование, затем промыты такой подходящей жидкой средой, как вода, и высушены.
Кристаллический продукт, полученный по описанным методикам, включающий матрицу-шаблон из соединения бензил-замещенного аммония, если это желательно, может быть подвергнут прокаливанию воздуха при температуре выше 400oC для удаления матрицы-шаблона, все еще присутствующей в порах молекулярного сита.
Другой способ получения описанных выше титансодержащих молекулярных сит заключается в том, что цеолит-бета деалюминируют и образующиеся в результате этого решеточные вакансии заполняют атомами титана. Такой способ является относительно быстрым и обеспечивает высокие выходы активного катализатора, по сравнению, например с гидротермальными методами, требующими 1 неделю или более на одну загрузку и дающими более низкие выхода катализатора. Метода деалюминирования после синтеза хорошо известны и включают, например реакцию с минеральными кислотами (например HCl, H2SO4, HNO3) или выщелачивание ими, или реакцию с хелатирующими агентами и гидротермальную, либо паровую обработки (возможно, совместно, с кислотным травлением). В этом отношении можно обратиться к широкому списку публикаций, описывающих методы деалюминирования цеолита, приведенному в патенте США N 4576805, (отрывок от колонки 8, строка 62 до строки 27 в колонке 9), а также в статье Шерзера "Получение и охарактеризирование алюминий-дефицитных цеолитов" ACS Symp. fez 248, 157-200 (1984). В особенно предпочтительном способе используется обработка цеолита-бета такой минеральной кислотой, как азотная кислота (предпочтительно, имеющей концентрацию 2-13 М, наиболее предпочтительно, концентрированной азотной кислотой) при температуре 25-150oC в течение периода времени от 5 минут до 24 часов. Могут использоваться и другие минеральные и карбоновые кислоты, о чем указывается в патенте Великобритании N 1061847, в опубликованном Европейском патенте N 488867, в статье Краушаара с сотр. в Catalysis Letters 1. , 81-84 (1988), в Китайском патенте N 1059701 (Chem. Abst. 117; 114655), в опубликованном Европейском патенте N 95304 и Китайском патенте N 1048835 (Chem. Abst. 115: 52861). Предпочтительно осуществляют суспендирование бета-цеолита или его контактирование каким-либо другим способом, с относительно большим объемом азотной кислоты (предпочтительно, 10-1000 вес. частей азотной кислоты на 1 вес. часть цеолита-бета). Такая операция деалюминирования может повторяться многократно для реализации более полного удаления Al. Подходящие способы деалюминирования такого типа подробно описаны в работе Лами с сотр. в Microporous Materials 1, 237-245 (1993) и в опубликованном Европейском патенте N 488867. Далее деалюминированный материал можно обрабатывать источником титана. Так, например деалюминированный цеолит-бета можно обработать таким летучим источником титана, как TiCl4 в среде азота, в течение 1-24 часов при повышенной температуре (предпочтительно, 250-750oC). Такой жидкофазный источник (титана, как (NH4)2 TiF6 (водн.) или TiF4 (водн.) также может использоваться для внедрения атомов Ti в решеточные вакансии деалюминированного цеолита-бета. Для этих целей также подходят такие твердые источники титана, которые способны испаряться при доступных температурах, например алкилаты тирана (например, Ti (OMe)4. Способы титана в цеолитные материалы после синтеза описаны, например в патенте США N 4576805, патенте США N 4828812, а также в статье Краушаара с сотр. в Catal. Lett. 1, 81- 84 (1988). Далее, желательно проводить обработку титансодержащего молекулярного сита такой солью аммония, как нитрат аммония, раствором кислоты (например водным раствором азотной кислоты) и т.п. для перевода источника титана в кислотную форму (например в водородную или протонную форму) или для удаления избыточного количества алюминия в решетке. Успешными операциями являются также сушка и/или прокаливание.
Титансодержащие молекулярные сита настоящего изобретения характеризуются помимо чрезвычайно низкого содержания Al низкой кислотностью. Однако для улучшения технических характеристик некоторых титансодержащих молекулярных сит, полученных как было описано выше, успешной операцией является контактирование катализатора с соединениями аммиака, щелочного и/или щелочноземельного металла, без каких-либо теоретических рассуждений можно предположить, что такое улучшение может быть приписано нейтрализации некоторых связанных с металлом кислотных центров, присутствующих в титансодержащем молекулярном сите. Предпочтительным способом осуществления такой модификации является растворение соединения аммония, щелочного или щелочноземельного металла в воде или другой подходящей жидкой среде, затем осуществляют стадию интенсивного контактирования полученного в результате раствора с молекулярным ситом. Такой метод, предпочтительно, осуществляется при температуре, достаточно высокой для того, чтобы осуществить частичный (примерно, по крайней мере, 25%) или полный обмен, или замещение аммонием щелочным или щелочноземельным металлом водородных катионов кислотных центров в течение короткого, с практической точки зрения, периода времени (например за 24 часа). Для этих целей обычно достаточно использовать температуры в интервале 25-150oC. Концентрации соединения аммония, щелочного или щелочноземельного металлов могут изменяться, как правило, они составляют 0,001-5М. Оптимальные концентрации могут быть легко установлены методом общепринятого эксперимента. После требуемого катионно-обмена, избыток жидкой среды может быть отделен от титансодержащего молекулярного сита фильтрацией, декантацией, центрифугированием или другими подходящими способами, а полученное модифицированное титансодержащее молекулярное сито (если желательно) промывают водой или другой подходящей жидкостью и затем сушат и/или обжигают перед тем, как использовать в реакции эпоксидирования настоящего изобретения. Если используется соединение аммония, то предпочтительно избегать стадию прокаливания с тем, чтобы минимизировать какое-либо репротонирование катализатора.
Конкретная форма соединения аммония, щелочного или щелочноземельного металла, выбранная для указанного использования, не имеет решающего значения, но предпочтительно, такие соединения представляют собой растворимые в воде вещества и желательно выбирать их из аммиака гидроксидов и оксидов щелочного или щелочноземельного металла (например из гидроксида натрия, гидроксида калия, гидроксида бария, гидроксида кальция) карбонатов аммония, щелочного или щелочноземельного металла (например из карбоната натрия, карбоната калия) бикарбонатов аммония, щелочного или щелочноземельного металла (например из бикарбоната натрия, бикарбоната калия, нитратов аммония, щелочного или щелочноземельного металлов (например из нитрата натрия, нитрата калия), галогенидов аммония, щелочного или щелочноземельного металлов (например из хлорида калия, бромида натрия, хлорида натрия), сульфатов аммония, щелочного или щелочноземельного металлов (например из сульфата натрия, сульфата калия), карбоксилатов аммония, щелочного или щелочноземельного металлов (например ацетат натрия), а также подобных соединений и их смесей. Противоион для соединения аммония, щелочного или щелочноземельного металла следует выбирать таким образом, чтобы он не оказывал вредного влияния на желаемую активность титансодержащего молекулярного сита и на его кристаллическую структуру. Так например, было обнаружено, что при некоторых условиях использование пирофосфатов щелочных металлов может дезактивировать или отравлять катализатор на основе молекулярного сита.
В соответствии с одним из вариантов настоящего изобретения, модифицированное аммонием, щелочным или щелочноземельным металлом, титансодержащее молекулярное сито получают in situ в ходе эпоксидирования в результате использования немодифицированного титансодержащего молекулярного сита в комбинации с соединением аммония, щелочного или щелочноземельного металла, относящимся к описанному выше типу или с буффером, состоящим из карбоксилатов аммония, щелочного или щелочноземельного металлов и т.п. Так например, реакционная среда, в которой олефин контактирует с перекисью водорода, может содержать буфферную систему NaOAc/HOAc (предпочтительно в концентрации 0,1-5М) в среде такого подходящего растворителя, как спирт (например метанол). С другой стороны, можно использовать соединение щелочного металла, как таковое, например ацетат натрия. В периодических процессах, соединения аммония, щелочного или щелочноземельного металлов, могут, например, добавляться, как таковые, до инициирования эпоксидирования, тогда как в непрерывных процессах (как, например, в случав с использованием реактора CSTR), указанные соединения могут комбинироваться с одним из потоков сырья, содержащих один из других реакционных компонентов, например окисляющий газ.
Кислотность поверхности титансодержащих молекулярных сит может, с другой стороны, с успехом понижаться в результате силилирования. Силилирование может осуществляться, например, по реакции с хлортриметилсиланом и т.п.
Количество катализатора, используемое для эпоксидирования олефина не является решающим, однако оно должно быть достаточным для полного завершения реакции за практически приемлемый период времени. Оптимальное количество катализатора будет зависеть от рада факторов, включающих температуру реакции, реакционноспособность олефина и его концентрацию, концентрацию окисляющего агента, тип и концентрацию органического растворителя, а также активность катализатора. Однако, как правило, при периодическом эпоксидировании, количество катализатора составляет 0,001-10 г на моль олефина. В системах с неподвижным слоем катализатора оптимальное количество катализатора зависит от потока реагентов через неподвижный слой (как правило, составлявший 1-100 молей окисляющего агента на кг катализатора в час) Обычно, общая концентрация титана в реакционной смеси эпоксидирования составляет 10-10000 ч/млн.
Такой катализатор может применяться в порошкообразной, гранулированной, микросферической, монолитной, экструдированной или в любой другой подходящей форме. Может быть предпочтительным использовать наполнитель (гель) или подложку в комбинации с титансодержащим молекулярным ситом. Нанесенные или связанные катализаторы могут быть получены методами, известными в данной области техники, как эффективные для цеолитных катализаторов в целом. Так например, катализатор может быть нанесен на оксид титана путем применения методов, описанных в патенте США N 5354875.
Примерами наполнителей и подложек (которые, предпочтительно, имеют не кислотный характер) могут служить оксид кремния, оксид алюминия, системы типа оксид кремния-оксид алюминия, оксид кремния-оксид титана, оксид кремния-оксид тория, оксид кремния-оксид магния, оксид кремния-оксид циркония, оксид кремния-оксид бериллия, а также четырехкомпонентные композиции на основе оксида кремния и других тугоплавких оксидов. Могут также применяться такие глины, как монтмориллониты, каолины, бентониты, галлоизиты, дискиты, накриты и анакситы. Соотношение между титансодержащим молекулярным ситом и наполнителем или подложкой может лежать в интервале 99:1-1:99, предпочтительно 5: 95-80: 20. Рассматриваемый катализатор может быть также импрегнирован или смешан с такими благородными металлами, как Pt, Pd и т.п.
Олефин, подвергаемый эпоксидированию по способу настоящего изобретения, может представлять собой любое органическое соединение, содержащее, по крайней мере, одну этиленовоненасыщенную группу (т. е. углерод-углеродную двойную связь) и может быть олефином циклического, разветвленного или линейного строения. Такой олефин может содержать арильные группы (например фенил, нафтил). Предпочтительно, такой олефин имеет алифатический характер и содержит 2-30 углеродных атомов (т.е. олефин C2-C30. Особенно успешным является использование легких (низкокипящих) моноолефинов C2-C10. В молекуле олефина может присутствовать более одной углерод-углеродной двойной связи, таким образом могут использоваться диены, триены и другие полиненасыщенные субстраты. Двойная связь в олефине может быть концевой или внутри молекулы, либо составлять часть циклической структуры (как это имеет место, например в циклогексене). Другие примеры подходящих субстратов включают ненасыщенные жирные кислоты или их производные, такие, как сложные эфиры глицеридов, а также такие олигомерные или полимерные ненасыщенные соединения, как полибутадиен. Эпоксидированию могут также подвергаться бензильные и стирольные олефины, хотя следует иметь в виду, что эпоксиды некоторых стирольных олефинов, например стирола, могут вступать в последующие реакции изомеризации в условиях настоящего изобретения с образованием альдегидов и т.п.
Олефин может содержать другие заместители, отличные от углеводородных, например галогенид, карбоксилатный, эфирный, гидроксил, тиольный, нитро, циано, кетонный, ацильный, сложноэфирный ангидридный, амино и другие аналогичные заместители.
Примерами олефинов, подходящих для использования в способе настоящего изобретения могут служить этилен, пропилен, бутены, (например, 1,2-бутен, 2,3-бутен, изобутилен), бутадиен, пентаны, изопропен, 1-гекоен, 3-гексен, 1-гептен, 1-октен, диизобутилен, 1-нонен, 1-тетрадецен, пентамирцен, камфен, 1-ундецен, 1-додецен, 1-тридецен, 1-тетрадецен, 1-пентадецен, 1-гекоадецен, 1-гептадецен, 1-октадецен, 1-нонадецен, 1-эйкозен, тримеры и тетрамеры пропилена стирол (и другие винилароматические субстраты), полибутадиен, полиизопрен, циклопентен, циклогексен, циклогептен, циклоктен, циклооктадиен, циклододецен, циклододекатриен, дициклопентадиен, метиленциклопропан, метиленциклопентан, метиленциклогексан, винилциклогексан, винилциклогексен, металлил-кетон, хлористый аллил, бромистый аллил, акриловая кислота, метакриловая кислота, кротоновая кислота, винилксусная кислота, металлил-хлорид, дихлорбутены, аллиловый спирт, аллил-карбонат, аллил-ацетат, алкилакрилаты и метакрилаты, диаллил-малеат, диаллил-фталат, такие ненасыщенные триглицериды, как соевое масло и такие ненасыщенные кислоты, как олеиновая кислота, линоленовая кислота, линолевая кислота, эруковая кислота, пальмитоловая кислота, и рицинолевая кислота, а также их сложные эфиры, включая моно-, ди- и триглицеридные сложные эфиры, и т.п.
Эпоксидированию могут подвергаться смеси олефинов и полученные в результате смеси эпоксидов могут использоваться либо в смешанной форме, либо подвергаться разделению на индивидуальные компоненты.
Способ настоящего изобретения особенно полезен для эпоксидирования олефинов C2-C30, отвечающих общей структуре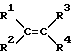
в которой R1, R2, R3 и R4 могут иметь одинаковые или различные значения и их выбирают из группы, состоящей из водорода и алкилов C1-C20.
В качестве окисляющего агента в процессе настоящего изобретения может использоваться источник перекиси водорода, например, сама перекись водорода (H2O2), органическая гидроперекись, или соединение, способное в условиях реакции эпоксидирования образовывать или выделять перекись водорода или органическую гидроперекись. Было установлено, что часто эпоксидирование протекает более легко (т.е. с более высокими скоростями, с более высокой селективностью по эпоксиду) при использовании в качестве окисляющего агента органической гидроперекиси, хотя причины установленного факта, к настоящему времени, не вполне ясны. Этот результат оказался полностью неожиданным в свете недавнего сообщения (Хоу с сотр. J.Catalysis, 149 195-205 (1994), в котором говорится, что другие свободные от алюминия титансодержащие ZSM-5 молекулярные сита ("TS-1") неактивны в качестве катализаторов окисления при использовании органических гидроперекисей и что такая неактивность не связана с относительно мелким размером пор TS-1, а скорее связана с объемом массы органических гидроперекисей при образовании их комплексов с активными центрами Ti.
Соотношение между количеством окисляющего агента и количеством олефина не имеет решающего значения, но лучше всего использовать молярное соотношение окисляющий агент: олефин в интервале 100:1-1:100 в том случае, когда олефин содержит одну этиленовоненасыщенную группу. Молярное соотношение между количеством этиленовоненасыщенных групп в олефине и количеством окисляющего агента предпочтительно выбирать из интервала 1:10-10:1. Теоретически для окисления одного эквивалента мононенасыщенного олефина требуется один эквивалент окисляющего агента, однако, иногда, для улучшения селективности реакции по эпоксиду, желательно использовать избыток одного из реагентов,
Хотя перекись водорода, подходящая для использования в качестве окисляющего агента, может быть получена из любого подходящего источника, отличительным преимуществом способа настоящего изобретения является тот факт, что перекись водорода может быть получена путем контактирования такого вторичного спирта, как альфа-метил-бензиловый спирт, изопропиловый спирт, 2-бутанол, или циклогексанол с молекулярным кислородом, при условиях, которые обеспечивают образование окислительной смеси, состоящей из вторичного спирта и перекиси водорода (и/или предшественника перекиси водорода). Как правило, такая окисляющая смесь будет также содержать такие кетоны, как ацетофенон, ацетон или циклогексанон, соответствующие используемому вторичному спирту (т. е. имеющие тот же углеродный скелет), небольшие количества воды и изменяющиеся количества других форм активного кислорода, например, органических гидроперекисей. Для получения перекиси водорода можно также использовать окисление молекулярным кислородом антрагидрохинона, алкилзамещенных антрагидрохинонов, или воднорастворимых антрагидрохиноновых соединений. Перекись водорода может образовываться in situ непосредственно до или одновременно с эпоксидированием, как это например описано в опубликованном Европейском патенте N 526945 Japanese Kokai N4-352771, в докладе Феррини с сотр. /"Каталитическое окисление алканов с использованием силиката титана в присутствии образующейся in situ. перекиси водорода" ДСМК конференции по селективному окислению в нефтехимии, сентябрь 16-18, 1992, с. 205-213, а также в опубликованном Европейском патенте N 469662.
В качестве органических гидроперекисей, подходящих для использования в качестве окисляющего агента в способе эпоксидирования настоящего изобретения, могут применяться любые органические соединения, содержащие, по крайней мере, одну гидроперекисную функциональную группу (-OOH). Предпочтительными являются вторичные и третичные гидроперекиси, что связано с высокой нестабильностью первичных гидроперекисей и причинами безопасности. Оpгaничeскaя гидроперекись предпочтительно имеет следующую общую структуру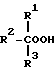
где R1, R2 и R3 могут иметь одинаковые или различные значения и их выбирают из группы, состоящей из водорода, алкилов C1-C10 (например метил, этил, трет-бутил) и арилов C6-C12 (например фенил, алкил замещенный, фенил), при условии, что не более одного из радикалов R1, R2 или R3 представляют собой водород. Примерами органических гидроперекисей могут служить трет-бутил гидроперекиси, трет-амил гидроперекисей, гидроперекись кумила, гидроперекись этилбензола, гидроперекись циклогексила, гидроперекись метил-циклогексила, гидроперекись тетралина, гидроперекись изобутилбензола, гидроперекись нафталина и т.п. Могут также использоваться смеси органических гидроперекисей.
Если желательно, в процессе эпоксидирования настоящего изобретения может дополнительно использоваться растворитель для того, чтобы растворять реагенты, отличные от титансодержащего молекулярного сита с тем, чтобы обеспечивать лучший температурный контроль реакции или благоприятное влияние на скорость и селективность реакции эпоксидирования. В случае его присутствия такой растворитель может составлять 1-99 вес.% от общего количества реакционной смеси эпоксидирований и, предпочтительно, такой растворитель выбирают таким образом, чтобы он представлял собой жидкость при температуре реакции эпоксидирования.
Как правило, предпочтительными для использования являются органические соединения с температурами кипения при атмосферном давлении 25-300oC. Избыток олефина может служить растворителем или разбавителем. Примерами таких подходящих растворителей могут служить кетоны (например ацетон, метил-этил кетон, ацетофенон), простые эфиры (например тетрагидрофуран, бутиловый эфир), нитрилы (например ацетонитрил), алифатические и ароматические углеводороды, галогенированные углеводороды, а также спирты (например, метанол, этанол, изопропиловый спирт, трет.бутиловый спирт, альфа-метил, бензиловый спирт, циклогексанол, трифторэтанол). Было установлено, что использование полярного, но слабокоординирующего растворителя, такого как трифторэтанол, повышает активность и селективность действия катализатора, особенно в том случае, когда окислитель представляет собой такую органическую гидроперекись, как ГПТБ. Важным практическим преимуществом настоящего изобретения является тот факт, что процесс быть может осуществлен практически с использованием таких спиртовых растворителей с повышенной молекулярной массой, как альфа-метил-бензиловый спирт, тогда как при использовании этих же растворителей при применении других титансодержащих молекулярных сит, как TS-1, в качестве катализаторов, достигаются плохие результаты. Такая гибкость процесса минимизирует проблемы, с которыми приходится считаться в других случаях, когда осуществляются попытки выделения эпоксидного продукта из реакционной смеси эпоксидирования. Так, например, количественное отделение метанола от такого, относительно легкого эпоксида, как оксид пропилена, затруднено в связи с близкими значениями температур кипения. Могут использоваться несколько типов растворителей. Вода может также использоваться в качестве растворителя или разбавителя, неожиданно было установлено, что способ по изобретению реализуется при минимальном гидролизе даже в том случав, когда в реакционной смеси эпоксидирования присутствует значительное количество воды. Таким образом, для реализации способа по настоящему изобретению могут использоваться как двухфазные, так и однофазные реакционные системы.
Температура реакции не имеет решающего значения, однако она должна быть достаточной для достижения значительной конверсии олефина в эпоксид за разумно короткий период времени. Разумно проводить реакцию до достижения как можно более высокой степени превращения окисляющего агента, предпочтительно, по крайней мере, 50%, более предпочтительно, по крайней мере 90%, и наиболее предпочтительно, по крайней мере 95%, что должно сопровождаться достижением значительных селективностей. Среди различных факторов, оказывающих влияние на оптимальную температуру реакции, можно отметить активность катализатора, реакционноспособность олефина и окисляющего агента, концентрацию реагента и тип используемого растворителя, однако, как правило, такая температура лежит в интервале 0-150oC (более предпочтительно, 25-120oC). Как правило, подходящими, в зависимости от перечисленных выше факторов, могут служить времена реакции от 1 минуты до 48 часов (более желательно, от 10 минут до 8 часов). Хотя могут использоваться давления выше атмосферного, предпочтительно, (особенно в том случае, когда температура кипения олефина ниже температуры реакции эпоксидирования) проводить реакцию при атмосферном давлении или при повышенном давлении (обычно, 1-100 атм). Обычно, желательно создавать в реакторе эпоксидирования достаточное давление для того, чтобы поддерживать компоненты реакции в жидкой фазе. Так например, проведение реакции эпоксидирования при повышенном давлении способствует повышению растворимости таких газообразных реагентов, как пропилен, в растворителе и перекиси водорода.
Способ настоящего изобретения можно осуществлять в периодическом, непрерывном или полунепрерывном вариантах с использованием реакционных сосудов или аппаратуры соответствующего типа, например реакторов с неподвижным слоем, движущемся слоем, псевдоожиженным слоем катализатора, реактор с перемешивающейся эмульсией, либо CSTR реактор при применении однофазной или двухфазной систем. Известные способы осуществления реакций эпоксидирования олефинов в условиях катализа металлами, при использовании окисляющего агента на основе активного кислорода
также, могут быть использованы для настоящего случая. Так например, реагенты можно объединять все сразу или вводить в реакцию последовательно. Так, например, окисляющий агент может вводиться в реакционную зону частями. Окисляющий агент также может образовываться in situ в той же реакторной зоне, где проходит реакция эпоксидирования. После проведения реакции эпоксидирования до желаемой степени конверсии, эпоксидный продукт может быть отделен или выдели из реакционной смеси с использованием таких соответствующих методов, как фракционная дистилляция, экстрактивная дистилляция, экстракция в системе жидкость-жидкость, кристаллизация и т.п. После отделения от реакционной смеси эпоксидирования любым из методов, например фильтрацией, регенерированный катализатор может экономично использоваться для последующих эпоксидирований. В случае применения катализатора в виде неподвижного слоя продукт экпоксидирования, выносимый из зоны эпоксидирования в виде потока, практически, не содержит катализатора, поскольку последний удерживается в зоне эпоксидирования. В случае некоторых вариантов выполнения настоящего изобретения, предусматривающих получение эпоксида в непрерывном варианте, может оказаться желательным периодически или непрерывно регенерировать все количество или часть используемого титансодержащего молекулярно-ситового катализатора с тем, чтобы сохранить оптимальную активность и селективность. Подходящие для этого методы регенерации включают, например обработку катализатора растворителем, прокаливание катализатора, и/или контактирование катализатора с соединением аммония, щелочного или щелочноземельного металла. Любое количество непрореагировавшего олефина или окисляющего агента может быть подвергнуто аналогичному отделению и рециркуляции. С другой стороны, непрореагировавший окисляющий агент (особенно, в том случае, когда он присутствует в концентрациях, слишком низких для экономически выгодной регенерации) может быть подвергнут термическому или химическому разложению на содержание перекисную цепочку соединения. В тех вариантах выполнения настоящего способа, когда окисляющий агент представляет собой перекись водорода, образующуюся в результате окисления молекулярным кислородом вторичного спирта, сырая реакционная смесь эпоксидирования содержит также вторичный спирт и кетон, соответствующий такому вторичному спирту. После отделения эпоксида от вторичного спирта и соответствующего кетона, последний может быть подвергнут обратному превращению во вторичный спирт путем гидрирования. Так например, такой кетон может реагировать с водородом в присутствии такого катализатора гидрирования на основе переходного металла, как никель Рэнея, хромит меди, рутений, или нанесенный палладиевый катализатор. Реакция гидрирования такого типа хорошо известна специалистам. Вторичный спирт может быть также подвергнут дегидратации, с использованием известных методов, с образованием таких ценных алкенильных продуктов, как стирол.
Описанное в тексте титансодержащее молекулярное сито, помимо его использования в качестве ценного катализатора эпоксидирования может также находить применение в качестве ионообменника, селективного адсорбента - разделителя, или катализаторов других процессов превращения углеводородов, например, таких как: крекинг, селективный реформинг, гидрирование, дегидрирование, олигомеризация, алкилирование, изомеризация, дегидратация, гидроксилирование олефинов или ароматических соединений, окисление алканов, реформинг, диспропорционирование, метанирование и т.п. Молекулярные сита настоящего изобретения особенно полезны для катализа тех же реакций, в которых ранее использовали силикалиты титана (называемые также силикаты титана). Примерами применений такого типа могут служить следующие:
а/ способ получения кетон-оксима, который заключается в реакции такого кетона, как циклогексанон с аммиаком и перекисью водорода в жидкой фазе при температуре 25-150oC, в присутствии каталитически эффективного количества титансодержащего молекулярного сита. Реакция такого типа хорошо известны из литературы и подходящие условия осуществления такой синтетической трансформации в присутствии титан- силикалитного катализатора описаны, например в патенте США N 4745221, статье Роффиа с сотр. Cyclohexanone Ammoximation: A. Breakthroagh in the b. Caprolactam production process в книге "Новые подходы к селективному окислению" ред. Сенти др. с. 43-52 (1990), в статье Роффиа с сотр, "Новый процесс получения циклогексаноноксима" la eh: mica and L. Industria 72, с. 598-603, 1990), патенте США N 4894478, патенте США N 5041652, патенте США N 4794198, в статье Ридди с сотр. "Аммоксимирование циклогексанона на титансиликатных молекулярных ситах" J. Hol. Cat. 69, 383-392 (1991), в Европейской патентной публикации N 496385, в опубликованном Европейском патенте N 384390 и патенте США N 4968842.
б/ Способ окисления парафинового соединения (т.е. насыщенного углеводорода), заключающийся в реакции парафинового соединения при температуре 25-200oC с перекисью водорода в присутствии каталитически эффективного количество титансодержащего молекулярного сита. Реакции такого типа хорошо известны из литературы и подходящие условия для осуществления такой реакции синтеза в присутствии силикалита титана описаны, например, в статье Хайбрехста с сотр. Nature 345, 240(1990), статье Клеричи. Appl. Catal. 68, 249(1991) статье Татсуми с сотр. в J.Chem. Soc. Chem. Comm. 476 (1990), Хайбрехтса с сотр. в Catalysis Zetters 8 237-244 (1991).
в/ Способ гидроксилирования ароматического углеводорода (например фенола), заключающийся в реакции ароматического соединения при температуре 50-150oC с перекисью водорода в присутствии каталитически эффективного количества титано содержащего молекулярного сита с образованием фенольного соединения (например крезола). Реакции такого типа хорошо известны из литературы и подходящие условия для осуществления такой реакции синтеза в присутствии силикалита титана описаны, например в патенте США N 4396783, в статье Романо с сотр. "Селективное окисление в присутствии силикалита Ti ". La Chimica L' Industrim 72, 610-616 (1990) в статье Редди с сотр. Appl. Catalysis 58, 11-14 (1990).
г/ Способ изомеризации арил-замещенного эпоксида в соответствующий бета-фениловый альдегид, заключающийся в контактирования арил-замещенного эпоксида с каталитически эффективным количеством титансодержащего молекулярного сита при температуре 25-150oC. См. например патент США N 4495371 (на который ссылаются в описании).
д/ Способ окисления винилбензольного соединения в соответствующий бета-фениловый альдегид, заключающийся в реакции винилбензольного соединения с перекисью водорода при температуре 20-150oC в присутствии титансодержащего молекулярного сита. См. например патент США N 4609765.
е/ Способ синтеза N,N-диалкил-гидроксиламина, заключающийся в реакции соответствующего вторичного диалкиламина с перекисью водорода в присутствии титансодержащего молекулярного сита. См. например патент США N 4918194.
ж/ Способ окисления алифатического спирта, заключающийся в реакции алифатического спирта с перекисью водорода в присутствии титансодержащего молекулярного сита при температуре 25-150oC с образованием соответствующего кетона или альдегида, соответствующего указанному алифатическому спирту. См. например патент США N 4480135.
з/ Способ синтеза моноалкилового эфира гликоля, заключающийся в реакции олефина, алифатического спирта и перекиси водорода, в присутствии титансодержащего молекулярного сита при температуре 25-150oC. Cм. например патент США N 4476327.
На основании вышесказанного, специалист в данной области может легко оценить существенные отличительные признаки настоящего изобретения, в рамках его объема, осуществить различные изменения и модификации с тем, чтобы адаптировать изобретение к различным областям применения и условиям выполнения.
Следующие ниже примеры дополнительно иллюстрируют способ настоящего изобретения, и, никоим образом, не ограничивают изобретение.
Пример 1.
Настоящий пример иллюстрирует получение титансодержащего молекулярного сита, практически свободного от решеточного алюминия и имеющего решеточную структуру изоморфную структуре цеолита-бета, причем соединения бензил-замещенного аммония используются в качестве матрицы-шаблона.
Матрицу-шаблон 4,4'-триметилен-бис(N-бензил-N-метилпиперидиний)-дигидроксид, готовили следующим образом: к 800 мл этилацетата добавляли 25 г (0,105 моля) 4,4'-триметилен-бис-(1-метилпиперидина). Затем к полученному раствору прикапывали в токе азота 36,8 г (0,215 моля) бромистого бензила. Вскоре образовывался белый осадок и полученную в результате смесь перемешивали в течение ночи в токе азота. Твердый осадок выделяли, промывали этилацетатом и затем подвергали ресуспендированию из пентана. После выделения осадка во второй раз и промывки пентаном полученный продукт сушили в вакууме при 30oC в течение 48 часов. Выход дибромида был близким к количественному. Соль дигидроксида готовили методом ионообменной обработки примерно 50 ммоль соли дибромида с использованием 300 г анионо-обменной смолы БиоРад Ag I-X8. Целевое соединение дичетвертичного аммония получали в виде почти бесцветного водного раствора после низкотемпературного удаления воды с целью концентрации раствора.
К 30 г (0,144 моля) тетраэтилортосиликата прикапывали 0,72 г 0,05 М водного раствора HCl. Полученный в результате прозрачный раствор перемешивали в течение двух часов при комнатной температуре в слабом токе азота. После этого добавляли 30 мл абсолютированного этанола и затем прикапывали 1,53 г (0,045 моля) раствора тетра. н-бутилата титана в 20 мл изопропанола. Далее, прикапывали 2 г 1,27 N раствора триметилен-бис(бензил-метилпиперидина)дигидpoксидa. Полученный раствор сушили при 110oC в течение ночи с образованием 23,3 г сухого белого порошка. В УФ-спектре диффузного отражения высушенного геля наблюдается две сильных полосы поглощения в области 216 и 235 нм.
Дополнительную часть (17 г) указанного выше раствора матрицы-шаблона объединяли с 4 г дважды перегнанной деионизированной воды. Используя метод влажного импрегнирования, полученный в результате разбавленный раствор матрицы-шаблона прикапывали к высушенному гелю.
Количество раствора было несколько большим, чем требуется для начального увлажнения, в результате чего образуется очень жидкая суспензия. Молярное соотношение компонентов геля для суспензии было следующим:
0,144 Si : 0,045 Ti : 0,012 DQ : 0,24 OH : 0,973 H2O
Si/Ti = 32, DQ/Si = 0,084, OH/Si = 0,167, H2O/Si = 6,8
DQ = дикатионная часть соединения дичетвертичного аммония. Полученную суспензию помещали в футерированный тефлоном реактор Парра и нагревали в статическом состоянии в течение 8 дней при 135oC (было установлено, что меньшая продолжительность нагревания приводит к образованию частично аморфных продуктов). После этого твердое вещество выделяли, промывали водой и затем сушили при 110oC в течение ночи. Рентгеновский анализ порошка подтвердили, что высушенное титансодержащее молекулярное сито имеет структуру бета-цеолит и содержит недетектируемые загрязнения другими фазами например ZSM-12. В соответствии с данными ТГА-анализа было установлено, что при 800oC наблюдается потеря веса 26,1%, связанная с потерей матрицы-шаблона, что соответствует 3,3 молекулам матрицы-шаблона на 64 атома Ti. ДСК-анализ показал одну экзотерму (до 700oC) с центром при 432oC и началом при 382oC. В соответствии с литературными данными / Ван-дер Вааль с сотр. J. Chem. Soc. Chem. Comm. 1241-1242 (1994) окиснокремний-борный цеолит-бета содержит значительные количества кокса после прокаливания при 400oC, причем для удаления такого кокса требуется прокаливание при температуре 700oC. Однако такое прокаливание вызывает потерю кристалличности. В отличие от этого, титансодержащий цеолит-бета, полученный в соответствии с настоящим изобретением, можно обжигать при 550oC в течение 8 часов в атмосфере сухого воздуха с полным удалением всего количества матрицы-шаблона (о чем свидетельствуют данные элементного анализа). Данные рентгена - анализа прокаленного вещества (фиг. 1) свидетельствуют о сохранении и кристалличности.
Элементный анализ прокаленного вещества показал наличие 32% Si, 2.0 Ti<100 ч/млн. Al, 0,025% Na (Si/Ti=27.3 Si/Al 3500). Прокаленное вещество имеет объем микропор 0,269 мл/г (N2, измерение согласно БЭТ), что хорошо согласуется со значением 0,266 мл/г, полученным для полностью кремний-содержащего цеолита-бета. Адсорбция толуола составила 230 мг/г по сравнению с 170 мг/г для H-Al/бета, что подтверждает более гидрофобный характер первого образца. Данные ДР УФ-спектроскопии позволили обнаружить сильное поглощение в области 216 нм и второй меньший пик при 232 нм. Небольшой пик в области 330 нм, присутствующий в спектре свидетельствует о небольшой степени загрязнения анатазой. В ИК-спектре прокаленного молекулярного сита наблюдается умеренно сильный резонанс при 953 см-1, который был приписан возмущению в ячейке SiO4 в результате абсорбции фрагментов TiO4.
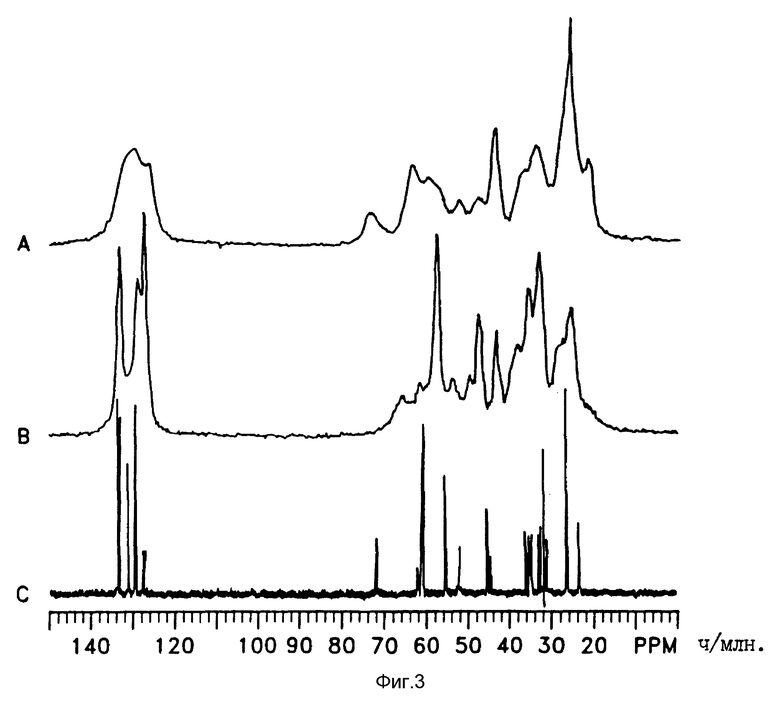
Данные 29Si МАСС-ЯМР-анализа синтезированного (непрокаленного) молекулярного сита показали, что матрица-шаблон на основе дичетвертичного аммония остается интактной внутри решетки каркаса в ходе гидротермального синтеза 13C МАСС-ЯМР-спектр синтезированного молекулярного сита, представленный на фиг. 3 под индексом A, а также 13C-МАСС-ЯМР -спектр 4,4'-триметилен-бис(бензил-метилпиперидиний)-дибромида (B на фиг. 3) и 13C МАСС-ЯМР-спектр дибромида в растворе d6-ацетона (C на фиг. 3) дали дополнительное подтверждение присутствия соединения дичетвертичного аммония. В спектре 13C МАСС-ЯМР прокаленного молекулярного сита проявляется полоса Q3 (-101 ч/млн.) интенсивности которой выше в 2,5 раза, чем у полосы Q4 (-110 ч/млн.), что аналогично соотношению, наблюдаемому для TS-1 (MF 1) силикалитов титана. Это указывает на тот факт, что молекулярное сито настоящего изобретения не содержит ощутимо большего числа дефектов центров силанола (SiOH), чем TS-1. SEM-анализ синтезированного молекулярного сита показал наличие гомогенных, небольших (субмикронных) частиц сферической морфологии и не дал свидетельств о наличии аморфного материала.
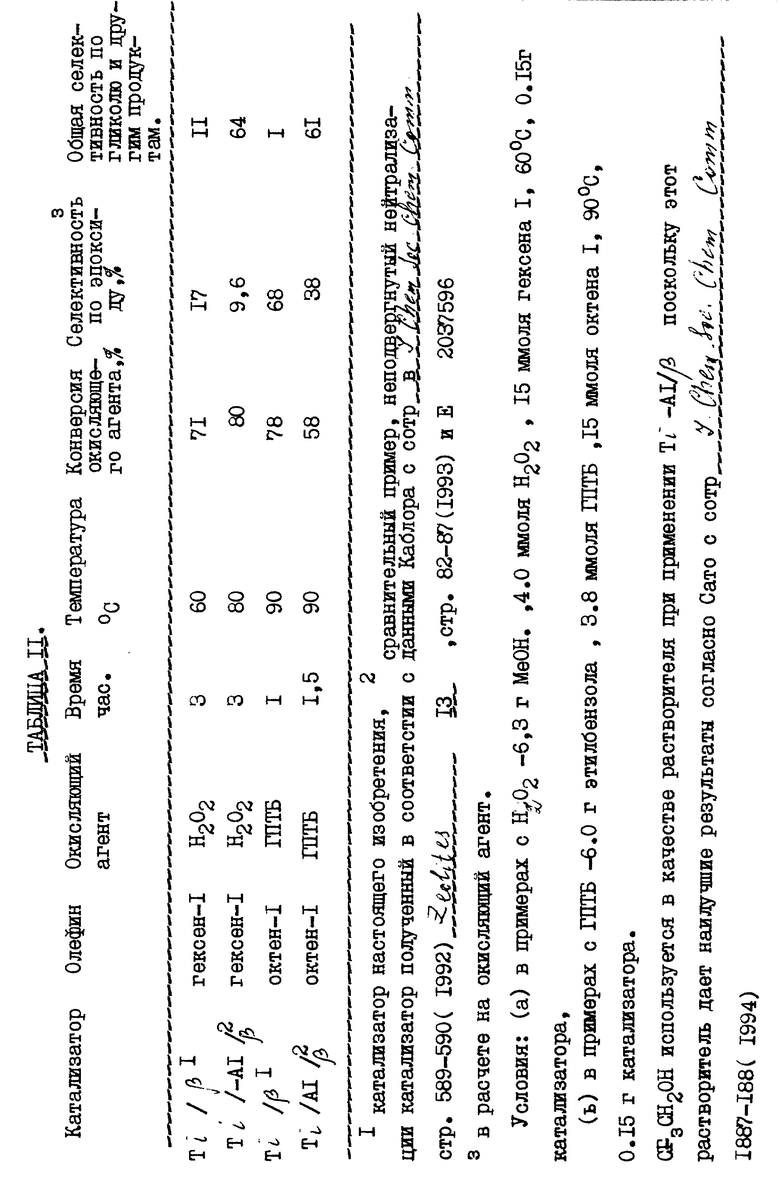
Было обнаружено, что прокаленное титансодержащее молекулярное сито, имеющее структуру цеолита-бета, полученное в соответствии с описанным выше, проявляет активность в качестве катализатора эпоксидирования при использовании водного раствора перекиси водорода или таких органических перекисей, как перекись трет-бутила. Полученные результаты представлены в табл. I и II. Так например, при использовании гексена-1 в качестве субстрата при 60oC в присутствии 50% H2O2 (соотношение олефин: H2O2 = 3,3) в среде метанола через час достигалась конверсия 27%, селективность 37% (в расчете на H2O2) по эпоксиду и 12% селективность по метиловым эфирам. Через 3 часа наблюдалась конверсия 71% при селективности по эпоксиду 17% и селективности по метиловому эфиру гликоля 110 (соотношение эпоксид/гликоли = 3,2). При использовании не-нетрализованного Ti -Al/β (т. е. бета-цеолита, содержащего в структуре матрицы атомы Si, Ti и Al в аналогичных условиях, напротив, наблюдается почти 100% селективность по побочным продуктам раскрытия цикла. С целью определения влияния воды реакционный раствор вначале сушили над сульфатом магния. В условиях, аналогичных описанным выше, было обнаружено, что через 1 час конверсия H2O2 составила 40% при селективности по эпоксиду 40% и селективности по побочным продуктам раскрытия цикла лишь 4% (соотношение эпоксид/гликоли = 10).
Еще лучшие результаты были получены при использовании в качестве окисляющего агента гидроперекиси трет.бутила (90% раствор в смеси трет.бутиловый спирт/вода). При использовании в качестве растворителя этилбензола и октена-1- в качестве олефина при 90oC было установлено, что через 1 час конверсия ГПТБ составила 78% при селективности по эпоксиду 68% и селективности по гликолям менее 1%. Для сравнения следует отметить, что в аналогичных условиях (время реакции 1,5 часа) использование не подвергнутого нейтрализации Ti-Al/β приводит к конверсии ГПТБ 58%, селективности по эпоксиду лишь 38% и селективности по гликолям 61%.
Пример 2.
В этом примере демонстрируется альтернативный способ получения титансодержащего молекулярного сита согласно настоящему изобретению.
Прокаленный цеолит-бета (5 г, Сonteko, 41-89-001), имеющий соотношение SiO2: Al2O3, равное 24, добавляли в 500 мл 13N раствора азотной кислоты. Полученную в результате суспензию нагревали при 80oC в течение четырех часов, при перемешивании. Суспендированные твердые вещества выделяли фильтрацией и дважды подвергали описанной выше обработке свежими порциями 13N азотной кислоты. После выделения фильтрацией твердые вещества промывали деионизированной водой и сушили при 95oC в течение ночи с образованием деалюминированного цеолита-бета с молярным соотношением Si/Al 940.
Деалюминированный бета-цеолит загружали в кварцевую трубку. Трубку в вертикальном положении помещали в печь и начинали медленно (100 см3/мин) пропускать поток азота. Образец нагревали при 400oC, затем нагревали при 600oC и скорость потока азота увеличивали до 300 см3/мин. После установления температуры на значении 600oC образец обрабатывали в течение восьми часов тетрахлоридом титана, путем продувания азота через нагретый (40oC) раствор TiCl4. После этого обработку с помощью TiCl4 прекращали и через образец еще в течение часа при 600oC продолжали пропускать азот. Далее, образец охлаждали до комнатной температуры в течение ночи в токе азота. Охлажденный образен обрабатывали 1М водным раствором нитрата аммония при 80oC в течение четырех часов. Образец выделяли фильтрацией, хорошо промывали водой, сушили при 95oC и затем прокаливали при 550oC в течение 6 часов с получением титансодержащего молекулярного сита, имеющего очень низкий уровень содержания алюминия. Данные Раман-спектроскопии, а также 29Si и 27Al МАСС-ЯМР также подтвердили, что произошло практически исчерпывающее деалюминирование и что титан внедрился в структуру цеолита. Спектр рентгеновской дифракции порошка титансодержащего молекулярного сита представлен на фиг. 2 и систематизирован в табл. III. Элементный анализ показал, что молекулярное сито содержит 200-300 ч/млн. алюминия.
Полученное таким образом титансодержащее молекулярное сито оценивали в качестве катализатора эпоксидирования гексена-1 перекисью водорода с использованием следующих условий: 60oC, 12,2 г метанола (растворитель), 16,5 ммоля гексена-1, 4,5 ммоля перекиси водорода, 0,10 г катализатора.
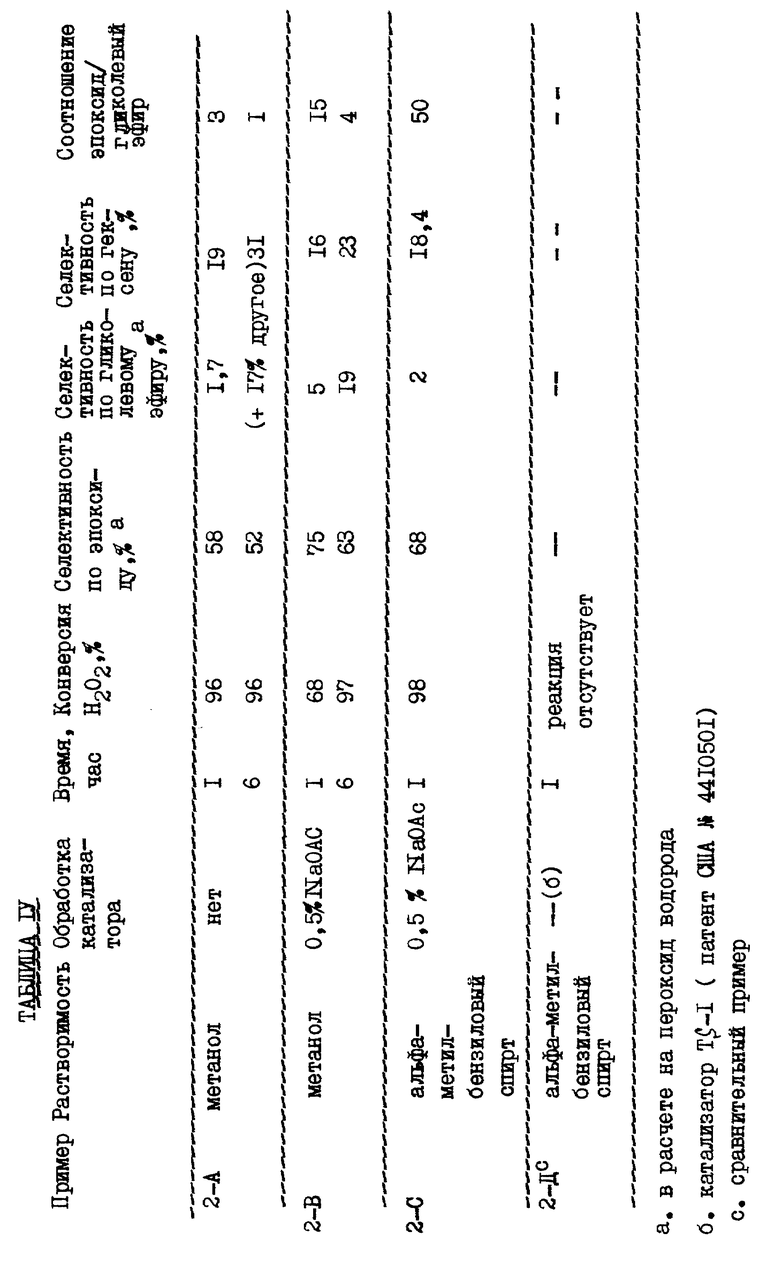
Результаты такой оценки представлены в табл. IV. Пример 2-A показывает, что хорошая селективность по эпоксиду может быть достигнута без модификации катализатора катионами металлов Группы IA или группы IIA, что (как предполагается) связано с чрезвычайно низким содержанием в катализаторе алюминия. Активность такого катализатора достаточно высока, 90% конверсии перекиси водорода достигается уже за один час. При промывании катализатора 0,5% раствором ацетат натрия (пример 2-B) наблюдается не сколько более низкие начальные скорости реакции, оцениваемые по превращению перекиси водорода при улучшенной селективности. Пример 2-C демонстрирует тот факт, что титансодержащее молекулярное сито, подвергнутое обработке ацетатом натрия, также обеспечивает получение вполне удовлетворительных результатов, при замене метанола на альфа-метилбензиловый спирт в качестве растворителя эпоксидирования. В отличие от этого, активностью при использовании альфа-метил бензилового спирта в качестве растворителя (пример 2-Д)
Пример 3.
В следующем ниже примере иллюстрируется альтернативный способ получения свободного от Al титансодержащего молекулярного сита настоящего изобретения с использованием в качестве матрицы-шаблона соединения дичетвертичного аммония.
Раствор 4,4'-триметилен-бис-(N-бензил-N-метилпиперидиний)дигидроксида готовили в соответствии с методикой примера 1 из 30 г соответствующего дибромида. Тетраэтилортосиликат (30 г, 144 моля подвергали неполному гидролизу путем добавления по каплям в 50 мл 0,49 N (по гидроксиду) водного раствора матрицы-шаблона. К такому гомогенному раствору добавляли тетрабутират титана (1,74, 0,00511 мо в 5 г (0,024 ммоля) тетраэтилортосиликата. К полученной в результате мутной жидкости добавляли оставшуюся часть раствора матрицы-шаблона (от 0,0517 моля). После перемешивания при комнатной температуре в течение двух часов этанол, образовавшайся в ходе гидролиза, удаляли выпариванием и предшественнику геля давали стареть в течение ночи. Гель- предшественник имеет следующий состав:
TiO2:10 матриц-шаблонов: 33 SiO2:800 H2O
Прозрачный предшественник геля загружали в футерованный тефлоном реактор и нагревали при встряхивании в течение 9 дней при 135oC. Полученные в результате кристаллические твердые вещества давали спектр рентгеновских лучей, характеристичный для бета-структуры матрицы. После прокаливания, молекулярное сито проявляло две полосы в спектре УФ /VIS при 233 нм и 214 нм с интенсивностями 0,420 и 0,391, соответственно. Элементный анализ подтвердил присутствие 1,9 вес.% Ti, 0,005 вес.% Al и 43 вес.% Si.
Эпоксидирование гексена-1 с использованием перекиси водорода и прокаленного молекулярного сита при 60oC привело через 1 час к 44% конверсии, при селективности 45,3% в расчете на перекись водорода. Органические продукты реакции представляли собой 73,8% оксида гекоена-1 и 26,2% эфиров гликоля. В пробе, отобранной через шесть часов реакции, была установлена 100% конверсия и 31% селективность в расчете на перекись водорода. Образовавшиеся органические продукты представляли собой оксид гексена-1 (42 вес.%) и гликолевые эфиры (58 вес.%).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭПОКСИДИРОВАНИЯ ОЛЕФИНА | 1996 |
|
RU2140415C1 |
| СПОСОБ ЭПОКСИДИРОВАНИЯ ОЛЕФИНА | 1995 |
|
RU2154641C2 |
| ИНТЕГРИРОВАННЫЙ СПОСОБ ПОЛУЧЕНИЯ ЭПОКСИДА И НЕПРЕРЫВНЫЙ ИНТЕГРИРОВАННЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРОПИЛЕНОКСИДА | 1994 |
|
RU2145322C1 |
| СПОСОБ ЭКСПЛУАТАЦИИ УСТАНОВКИ ДЛЯ ЭПОКСИДИРОВАНИЯ ОЛЕФИНА (ВАРИАНТЫ) | 1998 |
|
RU2205181C2 |
| СПОСОБ ЭПОКСИДИРОВАНИЯ ОЛЕФИНА | 1996 |
|
RU2162466C2 |
| СПОСОБ ЭПОКСИДИРОВАНИЯ С - С ОЛЕФИНОВ | 1996 |
|
RU2168504C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ПРОПИЛЕНА С ИСПОЛЬЗОВАНИЕМ СМЕСЕВОГО КАТАЛИЗАТОРА НА ОСНОВЕ ДРАГОЦЕННЫХ МЕТАЛЛОВ, НАНЕСЕННОГО НА КАРБОНАТ ЩЕЛОЧНОЗЕМЕЛЬНОГО МЕТАЛЛА | 1997 |
|
RU2183629C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТИТАНСОДЕРЖАЩЕГО ЦЕОЛИТА | 2001 |
|
RU2256613C2 |
| СИСТЕМА И СПОСОБ КАТАЛИТИЧЕСКОГО КОНВЕРТИРОВАНИЯ | 1997 |
|
RU2181071C2 |
| РЕГЕНЕРАЦИЯ ТИТАНСОДЕРЖАЩЕГО ЦЕОЛИТА | 2014 |
|
RU2673798C9 |



Описывается титансодержащий цеолит со структурой изоморфной структуре бета-цеолита, содержащий атомы кремния и титана и практически не содержащий атомы алюминия в решетке цеолита, и имеющий состав, соответствующий общей формуле SiO2 : у TiO2, где у имеет значение в интервале 0,01 - 0,25. Описывается также способ его получения (варианты), способ эпоксидирования олефинов и дичетвертичное аммониевое соединение для получения титансодержащего цеолита. Технический результат - получение простыми способами (вариантами) молекулярных сит - катализаторов, селективно катализирующих эпоксидирование олефинов с помощью перекиси водорода. 5 с. и 19 з.п. ф-лы, 4 табл., 3 ил.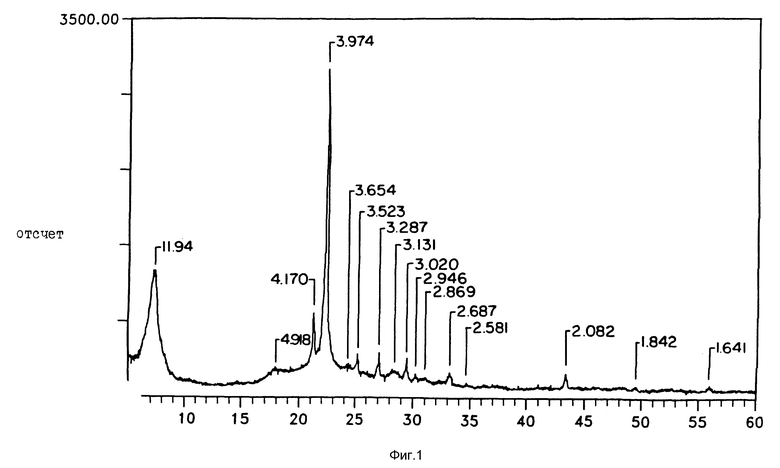
а) осуществляют реакцию способных к гидролизу соединения кремния и соединения титана с водой в кислой среде с образованием солюбилизированного неполного гидролизата, не содержащего осажденных диоксида кремния и диоксида титана; б) контактируют солюбилизированный неполный гидролизат с дичетвертичным аммониевым соединением, в котором каждый атом азота несет один бензильный заместитель, взятым в количестве, эффективном для катализа дополнительного гидролиза, с образованием твердого аморфного SiO2 - TiO2 - геля; в) контактируют твердый аморфный SiO2 - TiO2 - гель с раствором указанного дичетвертичного амониевого соединения в среде растворителя с образованием импрегнированного геля и г) нагревают полученный гель при 120 - 160oC в течение времени, достаточного для образования титансодержащего цеолита.
SiO2/TiO2 - 5 - 200
X-/SiO2 - 0,002 - 1
H2O/SiO2 - 0,1 - 10
M+/SiO2 - менее или равно 0,5
ДQ2+ - 0,005 - 2
где М+ - катион щелочного металла;
Х- - анион дичетвертичного аммониевого соединения, в котором каждый атом азота несет один бензильный заместитель;
ДQ2+ - дикатион указанного дичетвертичного аммониевого соединения.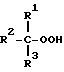
где R1, R2, R3 имеют одинаковые или различные значения и их выбирают из группы, состоящей из С1 - С10 алкила, С6 - С12 арила и водорода, при условии, что не более одного радикала из R1, R2 или R3 представляет собой водород.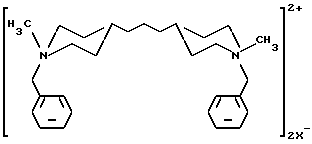
в которой Х представляет собой галоген или гидроксил.
Приоритет по пунктам:
23.12.93 по пп.1 - 5, 10 - 18, 20.
| US 4476327 A, 09.10.84 | |||
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОГО ГАЛЛОСИЛИКАТА С ЦЕОЛИТНОЙ СТРУКТУРОЙ И АТОМНЫМ ОТНОШЕНИЕМ Si/Ga ≥ 5 | 1991 |
|
RU2044690C1 |
| Электромеханическая трансмиссия транспортного средства | 1972 |
|
SU728699A3 |
| US 5474754 A, 12.12.95. | |||
Авторы
Даты
1999-11-10—Публикация
1994-12-22—Подача