Изобретение относится к микробиологии и может быть использовано при контроле результатов специфических биологических реакций (антиген-антитело, фермент-субстрат, ДНК-гибридизация и т.д.).
Биосенсоры (биодатчики) представляют собой миниатюрные устройства, детектирующие специфические биологические или химические взаимодействия за счет электрических сигналов.
По конструкции и принципам работы эти устройства сочетают реакции биологических систем с электронными, оптическими, термочувствительными или другими преобразователями, обеспечивающими съем информации с датчиков в виде специфических сигналов.
Практическое использование биосенсоров открывает широкие возможности быстрого и точного определения содержания определенного вещества в минимальном количестве среди множества ему подобных по свойствам химических веществ или биологических компонентов.
Известны биосенсорные устройства колориметрического типа, основным конструктивным элементов которых являются высокочувствительные электроды с иммобилизованными ферментами, при реакции которых с субстратами выделяются определяемые ионы (Шеллер Ф., Волленберг У., Шуберт Ф. и др./ Прикладные биохимия и микробиология, 1982, т. 18, N4, с. 454-470).
При использовании такого типа биосенсоров с клеточными органеллами, бактериальными клетками и др. макромолекулами, обладающими набором ферментных систем, ухудшается реакционная специфичность и воспроизводимость.
Известны биосенсоры, основным конструктивным элементом которых являются термочувствительные элементы и биологические системы (антиген-антитело). Принцип работы этих устройств основан на изменении величины энтальпии в иммунобиологических, ферментативных, химических реакциях. Недостатком биосенсорных термисторов является чрезвычайно высокая их чувствительность к изменениям температуры.
С внедрением оптико-волоконной технологии активно ведутся разработки оптических биосенсоров. Регистрация биологических реакций проводится по изменению оптических свойств световода с иммобилизованными на его торце биологическими материалами (North J.R.// Trends Biothechnol. 1985. V.3. N7. P. 180-186.).
Практическое использование этого способа требует специального оборудования.
Перспективным является использование МДП транзисторов с селективной мембраной.
Такие биодатчики матричного типа совместимы со средствами вычислительной техники. Однако пока не решена проблема создания высокоселективных мембран (Gronow М.// Trends Biochem. Sci. 1984. V.9. N8. P.337-340).
Наиболее близким к заявляемому является способ детекции макромолекул биосенсорным устройством (Пат. США N4735906, 436/806; 324/711; 05.04.88). Способ включает модификацию поверхности пьезокварцевого резонатора с образованием реакционно-активных групп, ковалентную иммобилизацию макромолекул с необходимым количеством слоев и регистрацию изменений резонансной частоты при изменении массы резонатора.
Недостатком способа являются сложность и длительность модификации поверхности резонатора с образованием реакционно-активных групп для последующей ковалентной иммобилизации макромолекул, процесс которой также длителен и сложен.
При химической обработке поверхности резонатора не исключен гидролиз альдегидных групп в водных растворах, что снижает стабильность резонатора.
Кроме того, пьезокварцевые резонаторы, относящиеся к электрогравитометрическим электронным элементам очень чувствительны к внешним условиям среды (температура, влажность, электропроводность, интенсивность электромагнитного поля).
Во многом недостатки связаны с процессом иммобилизации биологических материалов на поверхности сенсорного устройства и свойственны всем известным типам сенсоров.
При физическом адсорбировании биологических макромолекул или структур на поверхность датчика формируется непрочная связь, количество сорбируемого материала варьирует в широких пределах, при этом появляется возможность неспецифической сорбции.
Усовершенствование процесса иммобилизации биологических материалов ведется в основном в направлении создания условий для ковалентной связи макромолекул с поверхностью сенсора. Известны различные методы модификации поверхности датчика с целью создания на ней реакционно-активных групп для ковалентной иммобилизации.
Например, фиксирование на поверхности сенсорных устройств различных гелей, пленок на основе полиакриламида, агара, желатина, в ячейки которых включают антигены, антитела, ферменты.
Электроды покрывают белковой пленкой, образующейся в результате поликонденсации неспецифических активных белков в присутствии глютарового альдегида.
Известны способы образования на поверхности сенсоров полимерных пленок с использованием вакуумного плазменного напыления (Шеллер Ф. и др./ Прикладные биохимия и микробиология, 1982, т. 18, N4, с. 454-470).
Однако все эти известные приемы сложны технологически и инструментально и кроме того снижают чувствительность датчиков.
При получении иммуносорбентов прочность фиксации биоматериала на поверхности носителя обеспечивается созданием на них покрытия с функционально-реакционными группами, которые образуют с биоматериалом ковалентную связь. Эти покрытия осуществляют различными альдегидами, кетонами путем обработки носителей их растворами. При этом в основном используются пористые носители (полиакриламиды, силикагели), которые не могут полностью реализовать функции сенсора. Кроме того, модификация поверхности носителя в водных растворах неравномерна, альдегиды гидролизуются в водной среде, все это приводит к снижению стабильности сорбента и эффективности его иммобилизации (а. с. СССР, N1517545, C 01 N 33/53, 15.12.93, Бюл. N45-46).
Известен способ обработки поверхностей носителей из разнородных твердофазных непористых материалов для последующей иммобилизации лигандов (Пат. РФ N2070439, B 01 J 20/30, от 20.12.96, Бюл. N35).
По этому способу обработку поверхности твердофазного носителя проводят в парах альдегидов в вакууме в УВЧ-поле мощностью 15-30 Вт в течение 0,5-2,5 мин, под давлением 0,49-0,98 Па.
Способ позволяет значительно повысить сорбционную способность носителей к биологическим препаратам, повысить стабильность носителя, однако детекция осуществляется традиционными методами, так как сорбенты не чувствительны к преобразованию энергии биоспецифических реакций в электрическую, тепловую, световую.
Техническим результатом изобретения является повышение чувствительности и специфичности детекции макромолекул за счет повышения сорбционной способности биосенсора, увеличение срока службы биосенсоров и обеспечение универсальности их использования при контроле различных биологических процессов.
Технический результат достигается тем, что модификацию поверхности пьезокварцевого резонатора с образованием реакционных групп осуществляют парами альдегида в условиях вакуума в УВЧ-поле, ковалентную иммобилизацию макромолекул с необходимым количеством слоев проводят в нейтральном буфере в течение 3-5 мин по каждому слою с последующей обработкой раствором альбумина, регистрацию изменений резонансной частоты при изменении массы резонатора проводят в условиях изоляции электромагнитного поля при постоянной температуре.
Причинно-следственная связь отличительных признаков способа с техническим результатом изобретения проявляется в следующем.
Предварительная активация пьезокварцевого резонатора парами альдегидов в условиях вакуума в УВЧ-поле обеспечивает плазменную полимеризацию альдегидов на поверхности резонатора с высокой степенью адгезии и формированием реакционно-функциональных групп для ковалентного связывания с биологическими компонентами. Благодаря этому повышается сорбционная способность и срок службы резонатора. Обработка в УВЧ-поле обеспечивает безопасные и щадящие температурные условия.
Проведение послойной иммобилизации макромолекул в нейтральном буфере в течение 3-5 мин по каждому слою с последующей обработкой раствором альбумина обеспечивает отмывку биосенсора от несвязавшихся макромолекул и нейтрализацию неспецифических центров, что повышает чувствительность и специфичность детекции.
Проведение регистрации изменений резонансных частот в условиях изоляции от электромагнитного поля при постоянной температуре исключает отрицательные факторы на чувствительность биосенсора, условий окружающей среды и обеспечивает стандартность детекции.
Возможность практического применения заявляемого способа с использованием полной совокупности существенных признаков иллюстрируется примерами конкретного выполнения.
Пример 1. Брали 2 пьезокварцевых резонатора, один из которых является опытным, а другой - контрольным образцами, и замеряли в изолирующей камере, соединенной с генератором частот и частотомером, исходную частоту резонансных колебаний обоих образцов.
Затем опытный образец помещали в вакуумную камеру с источником УВЧ-ионизации и обрабатывали парами бензальдегида, предварительно охлажденного до - 70oC при достижении 0,73 Па и мощности УВЧ-поля 15 Вт до возникновения тлеющего разряда с характерным свечением. Экспозицию в УВЧ-поле продолжали в течение 45 с.
После обработки образцы помещали в изолирующую камеру и измеряли резонансную частоту.
Обработанную поверхность опытного образца покрывали противочумными иммуноглобулинами с концентрацией 20 мкг/мл в объеме 20 мкл, экспонировали 5 мин в нейтральном буфере и обрабатывали несвязанные реакционно-функциональные группы 0,01% раствором альбумина.
В изолирующей камере замеряли резонансную частоту, которая составила ≈6 МГц. Затем на слой лиганда в качестве антилиганда наносили 20 мкл Y.pestis EV. c концентрацией 20 м.к./мл, экспонировали 5 мин, промывали в нейтральном буфере и снова в изолирующей камере измеряли резонансную частоту. Последующие операции нанесения лиганда и антилиганда проводили аналогично опытному образцу, и снимали показания резонансной частоты после каждой последующей операции.
Пример 2. Все операции проводили аналогично примеру 1, за исключением того, что в качестве лиганда использовали F1, а антилиганда - противочумную сыворотку.
Пример 3. Все операции проводили аналогично примеру 1, за исключением того, что в качестве лиганда использовали пероксидазу, подтверждая ее фиксацию на образце наличием ферментативной активности после тщательной промывки образца нейтральным буфером.
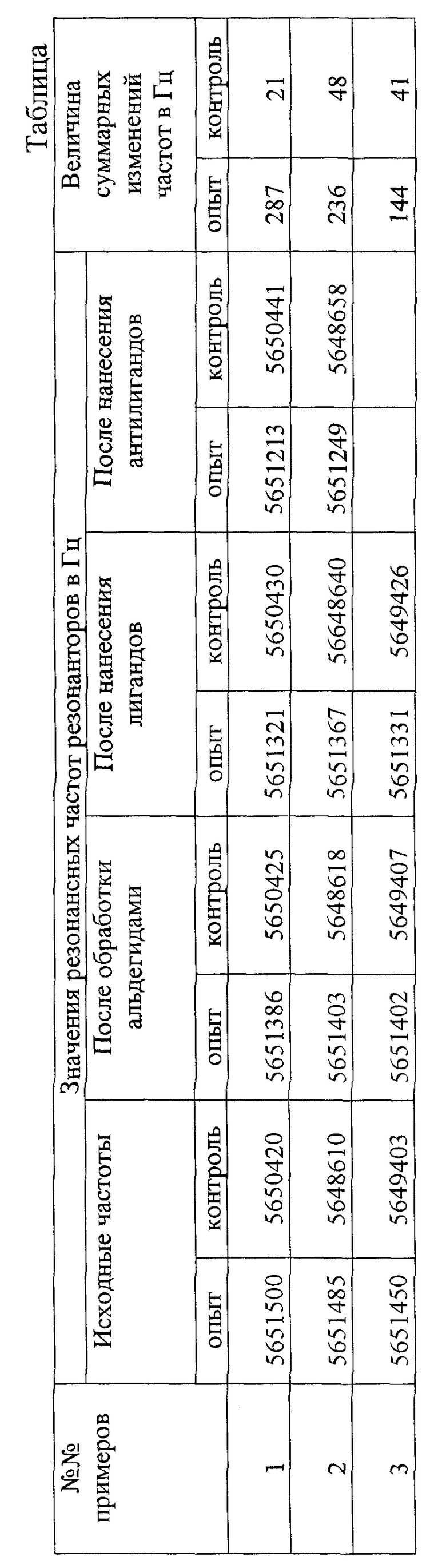
В таблице представлены результаты измерений резонансных частот резонаторов последовательно после каждой операции предлагаемого способа.
Изменение относительной резонансной частоты обратно пропорционально массе биосенсора и его частотным характеристикам. Эти изменения составляют 1-20% от частоты базовых образцов.
Величина суммарного изменения резонансных частот по всем приведенным примерам подтверждает, что опытные образцы обладают значительно более высокой сорбционной способностью, что повышает чувствительность и специфичность детекции макромолекул.
Таким образом, изобретение практически осуществимо, его использование позволит расширить сферу и эффективность биосенсоров в биотехнологии, иммунологии. Значительным преимуществом заявляемого способа перед известными является достижение высокой стабильности биосенсоров, срок их службы достигает 2-3 месяцев.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МИКРОГРАВИМЕТРИЧЕСКОГО ИММУНОСЕНСОРА | 2012 |
|
RU2510830C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТОВ | 1994 |
|
RU2070439C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОМАГНОСОРБЕНТА | 1994 |
|
RU2092854C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОСОРБЕНТА (ВАРИАНТЫ) | 1997 |
|
RU2138813C1 |
| НАНОДИАГНОСТИЧЕСКАЯ ТЕСТ-СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ВИРУСА ГЕПАТИТОВ | 2004 |
|
RU2315999C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОСОРБЕНТА | 2003 |
|
RU2253871C1 |
| СПОСОБ ЭЛЕКТРОИММОБИЛИЗАЦИИ АНТИТЕЛ | 2017 |
|
RU2658350C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАГНОИММУНОСОРБЕНТА ДЛЯ ОБНАРУЖЕНИЯ БАКТЕРИАЛЬНЫХ АНТИГЕНОВ | 2003 |
|
RU2246968C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОМАГНОИММУНОСОРБЕНТА ДЛЯ ОБНАРУЖЕНИЯ БАКТЕРИАЛЬНЫХ АНТИГЕНОВ (ВАРИАНТЫ) | 2003 |
|
RU2271540C2 |
| СПОСОБ ДИАГНОСТИКИ СИФИЛИСА (ВАРИАНТЫ) | 1999 |
|
RU2200327C2 |
Изобретение относится к микробиологии. Способ включает предварительную активацию парами альдегидов поверхности пьезокварцевого резонатора в условиях вакуума в УВЧ-поле, нанесение макромолекул с необходимым количеством слоев и последовательную, после каждой операции, регистрацию резонансных частот при изменении массы резонатора в условиях изоляции от электромагнитного поля и температуры. По этому изменению судят о наличии макромолекул. Это способствует повышению чувствительности и специфичности детекции макромолекул за счет повышения сорбционной способности биосенсора, увеличению срока службы биосенсоров и обеспечению универсальности их использования при контроле различных биологических процессов. 1 з.п. ф-лы, 1 табл.
| US 4735906 А, 05.04.1988 | |||
| US 4314821 А, 09.02.1982 | |||
| US 4236893 А, 02.12.1980 | |||
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТОВ | 1994 |
|
RU2070439C1 |
| Способ получения иммуносорбента | 1986 |
|
SU1517545A1 |
| Львович А.А | |||
| и др | |||
| Высокостабильные кварцевые генераторы на туннельных диодах | |||
| - М.: Связь, 1980, с.16-18 | |||
| Велитов Р.А | |||
| и др | |||
| Пондемоторное действие электромагнитного поля | |||
| - М.: Советское радио, 1975, с.23-32. | |||
Авторы
Даты
2000-04-27—Публикация
1998-04-17—Подача