Изобретение относится к способу связывания CO2 окисями олефинов (оксиранами, эпоксидами) в присутствии катализаторов. Согласно изобретению, в качестве катализаторов этого процесса впервые предложены электрополимеризованные аминозамещенные планарные и сэндвичеобразные фталоцианиновые комплексы переходных и редкоземельных элементов в электрохимически восстановленных формах.
Электрополимеризация фталоцианинов может быть осуществлена практически на любые электропроводящие материалы, как, например, платина, проводящее стекло, различные типы графита и т.п.
Пленки полимерных моно- и дифталоцианиновых комплексов при наложении катодного потенциала, соответствующего переносу одного электрона на каждое мономерное звено, служат эффективными катализаторами реакции связывания диоксида углерода окисями олефинов с образованием циклических алкиленкарбонатов.
Реакция протекает в мягких условиях (атмосферное давление, комнатная температура).
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Известно использование фталоцианинов в качестве катализаторов реакции связывания CO2 эпоксидами. В случае применения электронейтральных фталоцианиновых комплексов реакции протекают при температуре 185oC и давлении 50 атм (патент N 2100355). Использование электрохимически восстановленных форм фталоцианинов позволяет проводить эту каталитическую реакцию в мягких условиях, при комнатной температуре и атмосферном давлении (заявка N 97108659). Применяемые в этих патентах способы введения катализатора в реакцию отличаются низкой эффективностью. Катализатор либо находится в растворе, либо нанесен на окись алюминия (патент N 2100355) или электролитический графит (заявка N 97108659). Это приводит к необходимости использования довольно значительных количеств катализатора. Способ, при котором катализатор находится в растворе, имеет недостаток, поскольку возникает проблема отделения катализатора от продуктов реакции. Более предпочтительными являются каталитические процессы, в которых катализатор нанесен тонким слоем на соответствующую подложку, при этом реакция протекает на границе раздела фаз. Используемый в заявка N 97108659 способ нанесения катализатора на электролитический графит не является оптимальным. Это связано с тем, что, во-первых, процесс недостаточно технологичен (необходимо несколько раз пропитывать электрод раствором, сушить, и т. п. ). Во-вторых, по завершении процесса связывания CO2 эпоксидами, катализируемого электрохимически восстановленными формами фталоцианинов, часть катализатора, нанесенного на графит, все-таки переходит в раствор. Причиной этого является большая растворимость восстановленных форм фталоцианинов по сравнению с нейтральными комплексами. Это сильно ограничивает возможности метода, поскольку опять возникает проблема отделения продукта реакции - алкиленкарбоната - от катализатора.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
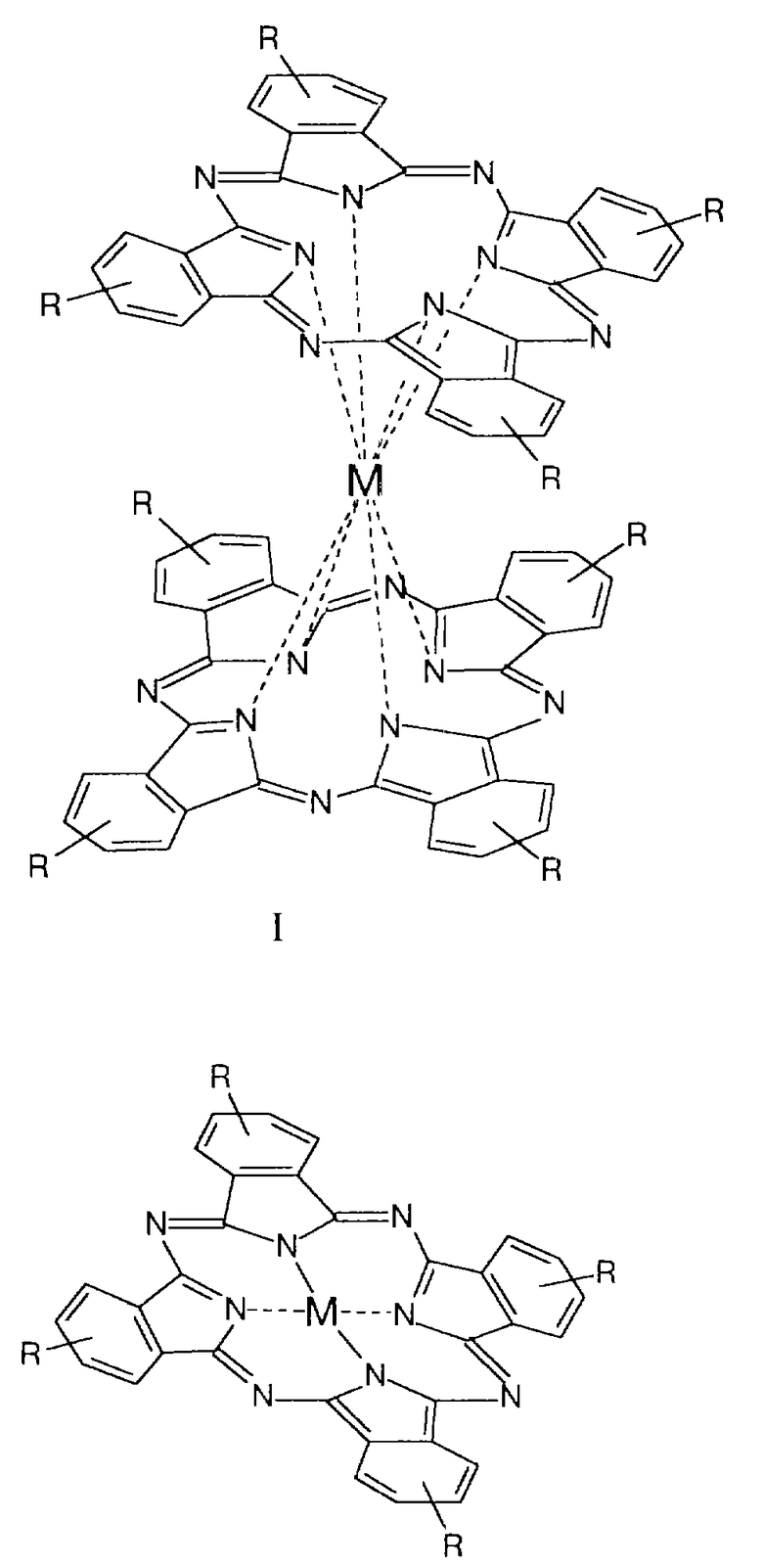
Заявитель указанного изобретения обнаружил, что вышеперечисленные недостатки могут быть устранены, если для приготовления катализаторов процесса связывания CO2 окисями олефинов использовать электрохимическую полимеризацию фталоцианиновых комплексов на различные электропроводящие материалы. В качестве объектов исследования были выбраны тетрааминозамещенные фталоцианины переходных металлов (меди, кобальта, палладия) и октааминозамещенные дифталоцианиновые комплексы редкоземельных элементов (см. формулу I и II в конце описания, где R=NH2, I - дифталоцианины РЗЭ, II - фталоцианины, содержащие двухвалентные металлы).
В результате электрохимической полимеризации этих соединений удается получать пленки полимерных моно- и дифталоцианинов, иммобилизованные на различных типах графита, на платине, проводящем стекле и т.п.
В качестве модельных соединений для связывания CO2 были взяты эпихлоргидрин и окись пропилена. Для осуществления процесса подходит простейшая электрохимическая ячейка любой формы с разделенным анодным и катодным пространством, предусматривающая возможность ввода CO2. При пропускании диоксида углерода через раствор эпоксида в ацетонитриле, в который помещен электрод, модифицированный полимерным фталоцианином, в результате электрокаталитической реакции образуется алкиленкарбонат. Процесс проводится при контролируемом потенциале, таком, чтобы катализатор находился в восстановленной форме, соответствующей переносу одного электрона на каждое мономерное звено.
При использовании фталоцианиновых катализаторов, приготовленных вышеописанным способом, удается превращать диоксид углерода в α- хлорметилэтиленкарбонат с каталитической эффективностью (которая определяется как количество молей продукта на 1 моль катализатора в единицу времени), в 102-103 раз превышающей каталитическую эффективность, полученную при использовании электрохимически восстановленных форм неполимеризованных фталоцианиновых комплексов.
Связывание CO2 протекает по следующей схеме: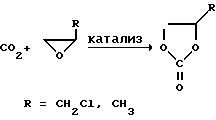
Строение продуктов реакции доказывалось с помощью ИК- и масс-спектроскопии. Характеристичные полосы поглощения в ИК-спектрах, а также массы осколочных ионов, наблюдаемые в масс-спектрах продуктов реакции, полностью совпадали с заведомо чистыми образцами. Для определения числа каталитических циклов, реализующихся в системе в зависимости от условий реакции и природы используемого катализатора, был применен метод калибровочной кривой, позволяющий определить в растворе концентрацию продукта реакции - алкиленкарбоната - с помощью ИК-спектроскопии.
Полимерные фталоцианиновые пленки, получающиеся в результате электрохимического осаждения, которые применяются в качестве катализаторов реакции связывания CO2 эпоксидами, характеризуются значительной адгезией к используемой подложке и хорошей механической прочностью. Это является существенным преимуществом предлагаемого способа связывания диоксида углерода, поскольку в процессе реакции катализатор не переходит в раствор; следовательно, нет необходимости отделять продукт реакции от катализатора.
Таким образом, предлагаемый способ электрокаталитического связывания двуокиси углерода, основанный на приготовлении активной формы фталоцианинового катализатора путем его электрохимической полимеризации на проводящей подложке и последующем электрохимическом восстановлении, имеет ряд преимуществ. Во-первых, по сравнению с другими вариантами нанесения катализатора количество исходного вещества, расходуемое на приготовление каталитически активного материала, сильно уменьшается. Это связано с тем, что сведены к минимуму непроизводительные потери исходного комплекса при его иммобилизации на поверхности электрода. Кроме того, электрополимеризованный катализатор можно использовать в виде очень тонких пленок. Это приводит к тому, что в каталитическом процессе участвует практически весь нанесенный катализатор. В результате этого удается достичь увеличения каталитической эффективности процесса в 102-103 раз по сравнению с применявшимися ранее подходами к иммобилизации фталоцианиновых катализаторов в реакции связывания CO2 эпоксидами. Во-вторых, фталоцианиновый комплекс оказывается прочно закреплен на электроде, поэтому снимается проблема отделения продукта реакции от катализатора. Это безусловно увеличивает технологичность процесса.
Применение изобретения иллюстрируется, но не ограничивается следующими примерами.
Пример 1
В электролитическую трехэлектродную ячейку объемом 7 мл с разделенным анодным и катодным пространством помещали 3 мл CH3CN, 20 мг (0.02 моль/л) Bu4NBF4 и 0.75 мл (1.6•10-2 моль) эпихлоргидрина. Далее в нее помещали рабочий электрод, представляющий собой пластинку из проводящего стекла, на которую путем электрохимической полимеризаци из раствора нанесен катализатор - 4,9,16,23-тетрааминофталоцианин меди (II). Раствор продували аргоном в течение 15 мин, затем включали ток CO2 и после этого начинали электролиз в потенциостатическом режиме при потенциале, соответствующем первой волне восстановления комплекса - 0.70В (отн. насыщенного хлорсеребряного электрода). Через 75 мин ячейку отключали, а содержащийся в ней раствор использовали для определения концентрации продукта реакции с помощью ИК-спектрометра (по интенсивности полосы валентных колебаний νco =1809 см-1). Получено 3.97•10-4 моль α -хлорметилэтиленкарбоната.
Оценка количества катализатора, используемого в реакции, проводилась спектрофотометрически. В данном примере оно составило 1.5•10-9 моль. Зная концентрацию продукта реакции и количество используемого катализатора, определяли число каталитических циклов на 1 моль катализатора, т.е. каталитическую эффективность процесса. Она составляет 2.65•10-5.
Сравнительный пример 2
В условиях, аналогичных примеру 1, за исключением того, что в качестве рабочего электрода использовали графит марки МГ (осч), на который был нанесен неполимеризованный 4,9,16,23-тетрааминофталоцианин меди (II). Катализатор был нанесен путем осаждения из раствора в диметилформамиде при добавлении этанола. Количество иммобилизованного катализатора определяли спектрофотометрически, по изменению поглощения раствора фталоцианина в диметилформамиде до и после нанесения катализатора. Оно составило 2.5•10-7 моль. Получено 9.9•10-5 моль α-хлорметилэтиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 4•102.
Пример 3
В условиях, аналогичных примеру 1, за исключением того, что в качестве катализатора использовали 2.9•10-9 моль 4,9,16,23,4',9',16',23'-октааминодифталоцианина лютеция λmax\= 727 нм) и на электрод подавался потенциал -0.66 В. Получено 4.05•10-5 моль α-хлорметилэтиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 1.4•104.
Сравнительный пример 4
В условиях, аналогичных примеру 2, за исключением того, что в качестве катализатора использовали 1.2 мг (10-6 моль) неполимеризованного дифталоцианина лютеция, который наносили на графитовый электрод путем пропитывания его раствором катализатора в CH2Cl2 и последующего высушивания током воздуха. На электрод подавался потенциал -0.10 В, время реакции составляло 150 мин. Получено 1.25•10-4 моль хлорметилэтиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 1.25•102.
Пример 5
В условиях, аналогичных примеру 1, за исключением того, что в качестве катализатора использовали 8.52•10-9 моль 4,9,16,23,4',9', 16',23' - октааминодифталоцианина эрбия= λmax=720 нм) и на электрод подавался потенциал -0.55 В. Получено 5.95•10-5 моль α-хлорметилэтиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 7•103.
Пример 6
В условиях, аналогичных примеру 1, за исключением того, что в качестве катализатора использовали 8.73•10-9 моль 4,9,16,23-тетрааминофталоцианина кобальта(II) ( λmax = 707 нм) и на электрод подавался потенциал -0.52 В. Получено 4.1•10-5 моль α -хлорметилэтиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 4.7•103.
Пример 7
В условиях, аналогичных примеру 1, за исключением того, что в качестве катализатора использовали 2.6•10-9 моль 4,9,16,23-тетрааминофталоцианина палладия(II) ( λmax = 685 нм) и на электрод подавался потенциал -0.71 В. Получено 2.73•10-5 моль α -хлорметилэтиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 1.05•103.
Пример 8
В условиях, аналогичных примеру 1, за исключением того, что в качестве рабочего электрода использовали пиролизованный полиакрилонитрил (ПАН), на который был нанесен электрополимеризованный 4,9,16,23-тетрааминофталоцианин меди(II). Количество катализатора определяли взвешиванием нитей ПАН до и после нанесения катализатора. Оно составляет 4.2•10-7 моль. Получено 7.6•10-5 моль α -хлорметилэтиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 1.8•102.
Пример 9
В условиях, аналогичных примеру 6, за исключением того, что в качестве рабочего электрода использовали графит марки МГ (осч), на который был нанесен электрополимеризованный 4,9,16,23-тетрааминофталоцианин меди(II). Количество катализатора составляет 2.45•10-7 моль. Получено 9.01 • 10-5 моль α-хлорметилэтиленкарбоната, т. е. число каталитических циклов на 1 моль катализатора равно 4•102.
Пример 10
В условиях, аналогичных примеру 1, за исключением того, что в качестве субстрата использовали 3 мл (4,3•10-2 моль) окиси пропилена. В качестве катализатора было взято 3,5•10-9 моль 4,9,16,23-тетрааминофталоцианина меди(II). Получено 1,8•10-6 моль пропиленкарбоната, т.е. число каталитических циклов на 1 моль катализатора равно 5,15•102.
Другие примеры содержат моно- и дифталоцианиновые комплексы различных металлов.
При увеличении размеров ячейки и каталитической поверхности абсолютные количества исходных веществ и продукта реакции могут быть увеличены во много раз.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭЛЕКТРОКАТАЛИТИЧЕСКОГО СВЯЗЫВАНИЯ ДИОКСИДА УГЛЕРОДА | 1997 |
|
RU2141470C1 |
| СПОСОБ КАТАЛИТИЧЕСКОГО СВЯЗЫВАНИЯ ДВУОКИСИ УГЛЕРОДА | 1996 |
|
RU2100355C1 |
| КОМПЛЕКС ИЗОИНДОЛО[5,6-f]ИЗОИНДОЛ-1,3,6,8(2Н,7Н)-ТЕТРААМИНА, 6,7- ДИФЕНИЛ-2,3-ДИЦИАНОНАФТАЛИНА И Mg И СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА | 2010 |
|
RU2430924C1 |
| НЕПРЕРЫВНЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРОПИЛЕНКАРБОНАТА В РЕАКЦИИ КАРБОКСИЛИРОВАНИЯ ОКИСИ ПРОПИЛЕНА В ПРИСУТСТВИИ ФТАЛОЦИАНИНОВЫХ КАТАЛИЗАТОРОВ | 2003 |
|
RU2228933C1 |
| СПОСОБ ОЧИСТКИ ВОДЫ ОТ РАСТВОРЕННЫХ ОРГАНИЧЕСКИХ ВЕЩЕСТВ | 1996 |
|
RU2117517C1 |
| РЕГЕНЕРАЦИЯ ФТАЛОЦИАНИНОВЫХ КАТАЛИЗАТОРОВ ДВУОКИСЬЮ УГЛЕРОДА В СВЕРХКРИТИЧЕСКОМ СОСТОЯНИИ | 2003 |
|
RU2236290C1 |
| СПОСОБ ПРЕВРАЩЕНИЯ МЕТАНА В ЭТИЛЕН И ЭТАН В ПРОЦЕССЕ ЕГО ОКИСЛИТЕЛЬНОГО ПРЕВРАЩЕНИЯ С ИСПОЛЬЗОВАНИЕМ ФТАЛОЦИАНИНОВЫХ КОМПЛЕКСОВ В КАЧЕСТВЕ ВЫСОКОЭФФЕКТИВНЫХ КАТАЛИЗАТОРОВ | 2008 |
|
RU2412143C2 |
| 6,7-ДИФЕНИЛ-2,3-ДИЦИАНОНАФТАЛИН И СПОСОБ ПОЛУЧЕНИЯ 6,7-ДИФЕНИЛ-2,3-ДИЦИАНОНАФТАЛИНА | 2010 |
|
RU2426725C1 |
| Способ получения сэндвичевых бис(фталоцианинатов) и/или трис(фталоцианинатов) редкоземельных элементов | 2018 |
|
RU2691011C1 |
| ПРОИЗВОДНЫЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-B)ИНДОЛОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1995 |
|
RU2140417C1 |
Описан способ электрокаталитического связывания диоксида углерода путем взаимодействия его с оксиранами в присутствии катализатора, при этом в качестве катализатора используются электрохимически полимеризованные фталоцианиновые комплексы, иммобилизованные на различных проводящих материалах. Эффективность процесса возрастает в 102-103 раз. 1 з.п.ф-лы.
| RU 9718659 А1, 27.04.1999 | |||
| СПОСОБ КАТАЛИТИЧЕСКОГО СВЯЗЫВАНИЯ ДВУОКИСИ УГЛЕРОДА | 1996 |
|
RU2100355C1 |
| Катализатор для окисления сернистых соединений и способ его приготовления | 1980 |
|
SU1041142A1 |
| Способ получения катализатора для удаления окислов азота, окиси углерода и/или остаточных углеводородов | 1987 |
|
SU1657048A3 |
| US 5283356 А, 01.02.1994. | |||
Авторы
Даты
2000-08-10—Публикация
1999-06-03—Подача