Изобретение относится к области медицины, конкретно к профилактической фармакологии, и касается средств, улучшающих умственную и физическую работоспособность как здоровых, так и больных людей, активирующих обмен веществ, ускоряющих регенерацию тканей.
Известны биогенные препараты с широким спектром биологического действия, обладающие различным химическим составом и механизмом действия: 1) адаптогенные препараты из растений (экстракты женьшеня, элеутерококка, родиолы розовой, заманихи, лимонника и др.) и пантов маралов, изюбров и пятнистых оленей (пантокрин), пантов северных оленей (рантарин); 2) средства, активирующие регенерацию тканей и обмен веществ - алоэ, керакол; спленин, глюнат, солкосерил, актовегин, 3) иммуностимуляторы и стимуляторы гемопоэза - церулоплазмин, эритрофосфатид; 4) эндокринные препараты (инсулин); 4) ферментные препараты - фестал; цернилтон и др. [1]; 5) порошкообразный биогенный препарат из окостенелых оленьих рогов и пищевая добавка на его основе [2], пантогематоген жидкий из дефибринированной крови марала, изюбра или пятнистого оленя психостимулирующего действия [3]. Известны пищевые добавки, содержащие биологически активные продукты, представляющие собой концентраты натуральных или идентичных натуральным биологически активных веществ, полученных при переработке растительного и животного сырья, которые предназначены для непосредственного приема с пищей или введения в состав специальных пищевых продуктов с целью обогащения рациона отдельными биологически активными веществами. Так, например, известны пищевая добавка "Пантогематоген жидкий", бальзам, содержащий жидкий экстракт из пантов оленей - пантокрин [4-5].
Применение таких пищевых добавок способствует повышению устойчивости организма к вредным воздействиям внешней среды, что особо необходимо в регионах с неблагоприятной экологической ситуацией.
Известен способ получения биогенного препарата путем сушки недефибринированной крови марала, изюбра или пятнистого оленя, взятой в период с июня по ноябрь, до пастообразной массы при температуре 45-50oC в течение 1,5-2 часов с последующим досушиванием в течение 4-5 часов до влажности 4-5% [6].
Однако биогенный препарат, полученный данным способом, обладает меньшей биологической активностью и широтой действия за счет высокой температуры сушки и содержания фибрина.
Одним из объектов защиты является биогенный препарат, содержащий высушенную дефибринированную кровь.
Вторым объектом защиты является пищевая добавка на его основе. Третьим объектом защиты является способ их получения.
Наиболее близким к первому объекту защиты по составу и спектру действия является биогенный препарат из высушенной недефибринированной крови марала, изюбра или пятнистого оленя, забранной с июня по ноябрь [5,6].
Однако данный биогенный препарат обладает недостаточной биологической активностью и широтой действия из-за наличия фибрина и высокой температуры сушки.
Наиболее близким к второму объекту защиты (прототипом) является пищевая добавка из сухой недефибринированной крови марала, изюбра или пятнистого оленя [5,6,7].
Однако данная пищевая добавка обладает недостаточной биологической активностью и широтой действия из-за наличия фибрина и высокой температуры сушки.
Прототипом к третьему объекту защиты является способ получения биогенного препарата из высушенной недефибринированной крови марала, изюбра и пятнистого оленя, забранной в период с июня по ноябрь [6].
Задачей, решаемой данным изобретением, является создание биогенного препарата и пищевой добавки на его основе, обладающей более высокой биологической активностью и широтой действия.
Эта задача решается с помощью нового биогенного препарата и пищевой добавки из дефибринированной крови марала, изюбра или пятнистого оленя, высушенной в вакуумной емкости с подогреваемыми стенками при температуре не выше 45oC и диапазоне вакуума от 5 до 600 мм рт.ст.
Новым в предлагаемом изобретении является то, что биогенный препарат и пищевая добавка на его основе содержат дефибринированную кровь марала, изюбра или пятнистого оленя, высушенную в вакуумной емкости с подогреваемыми стенками при температуре не выше 45oC и диапазоне вакуума от 5 до 600 мм рт. ст.
Авторами не найдено в проанализированной ими литературе данных существенных признаков. Известно использование жидкой дефибринированной крови марала, изюбра или пятнистого оленя с добавлением сахарного сиропа, фруктовой эссенции, аскорбиновой кислоты в качестве психостимулирующего средства [3]. Однако данное средство не обладает достаточной биологической активностью вследствие быстрого разрушения.
Данный биогенный препарат и пищевая добавка на его основе прошли клинические испытания в НИИ фармакологии ТНЦ СО РАМН. Таким образом, предлагаемый биогенный препарат соответствует критериям изобретения "Новизна", "Промышленная применимость" и "Изобретательский уровень".
Благодаря изобретению получены новый биогенный препарат и новая пищевая добавка с сохранением природной активности исходного продукта и обладающие более высокой биологической активностью по сравнению с прототипом.
Биогенный препарат и пищевую добавку на его основе получают следующим образом: кровь, забранную у здоровых маралов, изюбров или пятнистых оленей, отделяют от фибрина и дефибринированную кровь подвергают сушке в вакуумной емкости с подогреваемыми до температуры не выше 45oC стенками. Глубину вакуума регулируют вручную или автоматически и устанавливают так, чтобы не происходило сильное ценообразование. Диапазон вакуума составляет от 5 до 600 мм рт.ст. Сушку проводят до достижения влажности 4-5%.
Предложенные режимы сушки позволяют получить препарат с наиболее высокой активностью. Сушка при температуре выше 45oC приводит к разрушению части биологически активных веществ. Вакуумная сушка позволяет существенно ускорить этот процесс, не допуская микробного обсеменения сырья. Диапазон вакуума выбран экспериментально, так как на разных стадиях сушки приходится пользоваться различной глубиной вакуума в связи с ценообразованием, существенно ухудшающим технологический процесс.
Биогенный препарат представляет собой порошок буровато-коричневого цвета со специфическим запахом и вкусом. Биогенный препарат и пищевую добавку на его основе можно использовать в виде порошков, капсул, таблеток и любых других лекарственных форм, пищевую добавку можно использовать для добавления в любые пищевые продукты.
Заявляемый биогенный препарат и пищевая добавка на его основе обладают широким спектром действия: ноотропным, адаптогенным, противоязвенным, улучшающим регенерацию тканей, повышающим половую потенцию и более высоким биологически активным действием по сравнению с прототипом.
В экспериментальных и клинических исследованиях изучены фармакологические свойства предлагаемого биогенного препарата и пищевой добавки на его основе. Проведена оценка биологической активности предлагаемого препарата с прототипом и жидкой дефибринированной кровью марала.
В экспериментах на животных было изучено влияние предлагаемого препарата и прототипов на течение острого иммобилизационного стресса по методу Добрякова (8] в нашей модификации (9), нарушение рефлекса пассивного избегания в результате постгипоксической энцефалопатии [9] и влияние препарата на выработку и воспроизведение сложного условного рефлекса с питьевым подкреплением [10).
Эксперименты были выполнены на 120 беспородных мышах самцах массой тела 20-25 г и 48 беспородных крысах самцах массой тела 250-280 г. Исследуемые вещества вводили 7 раз (там, где это не оговорено особо) по 1 разу в день в желудок в виде раствора или взвеси в дистиллированной воде в течение 6 дней и 7-й раз за 1 час до тестирования или до стрессового или гипоксического воздействия, высушенную кровь марала, изюбра или пятнистого оленя (дефибринированную и недефибринированную) - в дозе 50 мг/кг и жидкую дефибринированную кровь в дозе 3,0 мл/кг. Данные дозы были определены в предварительных эксперименгтах как наиболее эффективные для каждого препарата. Во всех экспериментах численность групп животных составляла 12 особей.
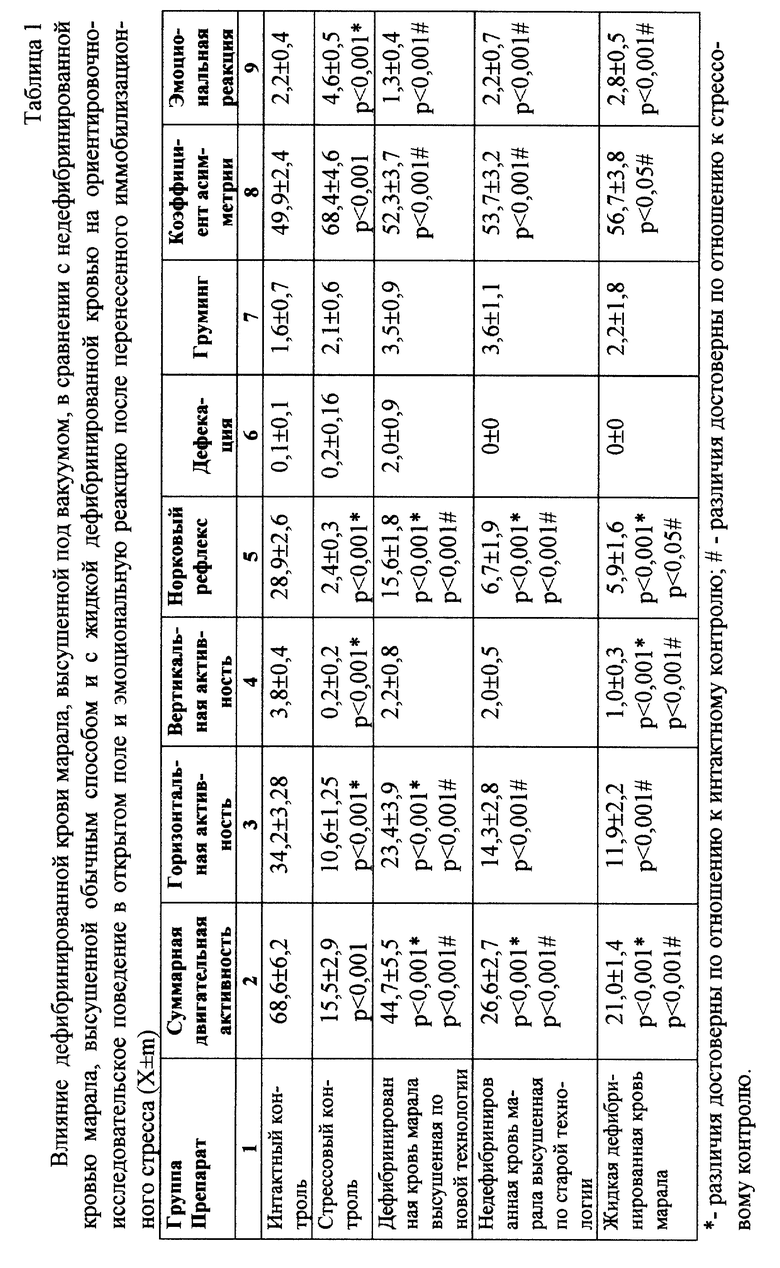
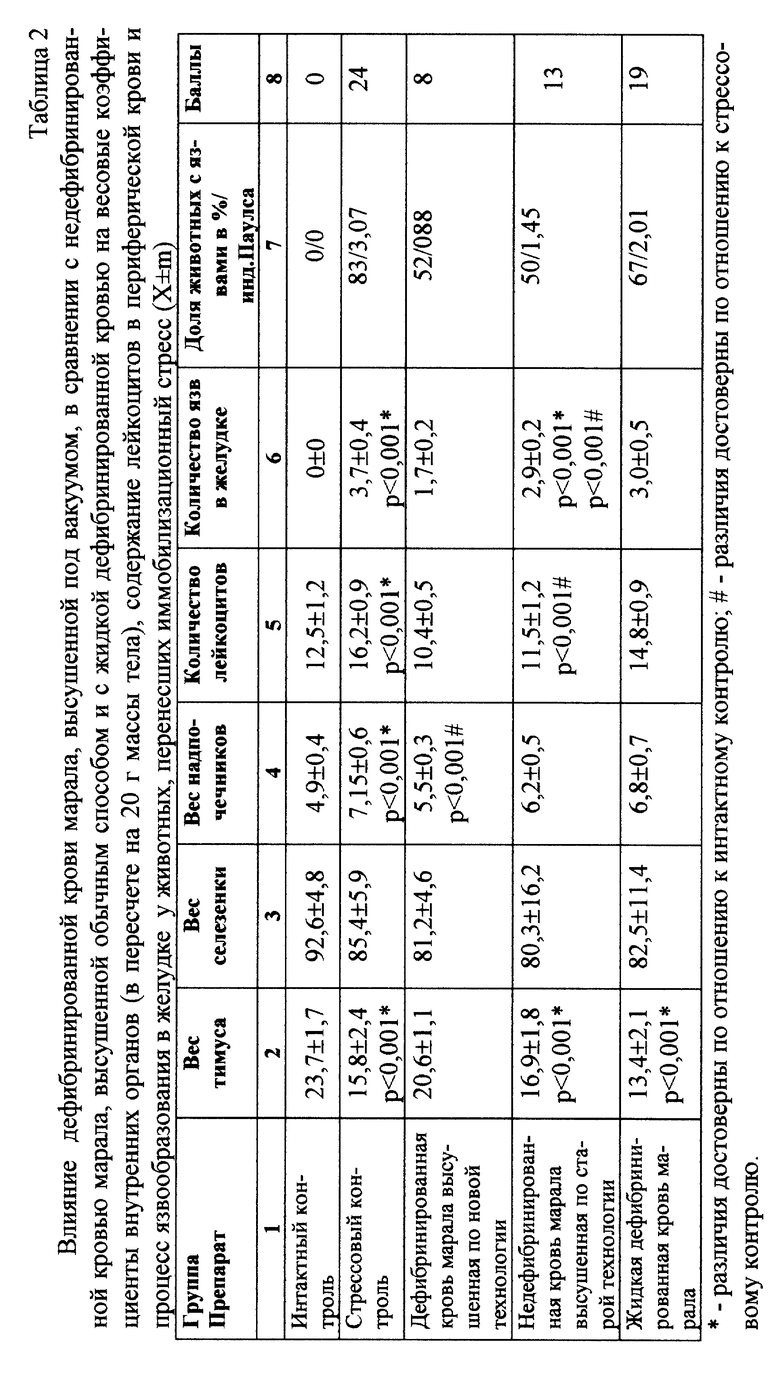
Иммобилизационный стресс создавался подвешиванием животных за шейную складку на 22 часа. По истечении времени животных снимали и через 15 минут после снятия у них изучали ориентировочно-исследовательское поведение, регистрировали эмоциональную реакцию по методу Brady & Nauta [11], определяли количество лейкоцитов в периферической крови, после чего животных забивали и определяли вес селезенки, тимуса, подсчитывали количество язв на слизистой оболочке желудка и рассчитывали весовые коэффициенты органов в пересчете на 20 г массы тела. Затем по методу Ю.И. Добрякова [8] определяли степень выраженности стресса в баллах. При оценке поведенческих показателей использовалась бальная шкала, аналогичная той, что принята в методе Добрякова, разработанная нами. При увеличении двигательной активности за каждые 20% отклонения от соответствующего показателя интактного контроля начислялся 1 балл, если показатель увеличивался более чем на 100%, то начислялось 6 баллов. При продолжительном варианте стресса, когда отмечалось снижение поведенческой активности, за каждые 16,7% снижения активности присваивался 1 балл [9].
Ориентировочно исследовательское поведение изучалось в условиях методики "открытое поле". Экспериментальная установка "Открытое поле" представляла собой камеру размером 40х40х20 см с квадратным полом и стенками белого цвета [12, 13]. Ее пол, разделенный на 16 квадратов, имел в каждом круглое отверстие диаметром 3 см. Сверху камера освещалась электрической лампой накаливания мощностью 100 Вт, расположенной на высоте 1 м от пола. Мышь помещалась в один из ее углов и в течение 2-х минут регистрировали количество перемещений с квадрата на квадрат (горизонтальная активность), количество вставаний на задние лапки (вертикальная активность), количество обследований отверстий (норковый рефлекс), количество умываний (груминг) и количество актов дефекации по количеству фекальных шариков (болюсов), вычислялся коэффициент асимметрии поведения в виде отношения количества горизонтальных перемещений к общей двигательной активности, выраженного в процентах.
Эмоциональная реакция исследовалась по методу Brady & Nauta [11], в нашей модификации для мышей [9], при котором полуколичественным способом оценивалась реакция на 4 вида воздействий - захват в клетке, где животное постоянно живет, захват в руку после помещения животного на плоскую поверхность, реакцию на приближение пинцета, реакцию на толчок пинцетом, при этом дополнительно оценивались дефекация с мочеиспусканием, писк и мышечное напряжение (всего 7 реакций). Каждая реакция оценивалась по 4-х бальной системе, после чего все баллы суммировались, давая общую оценку эмоциональной реакции.
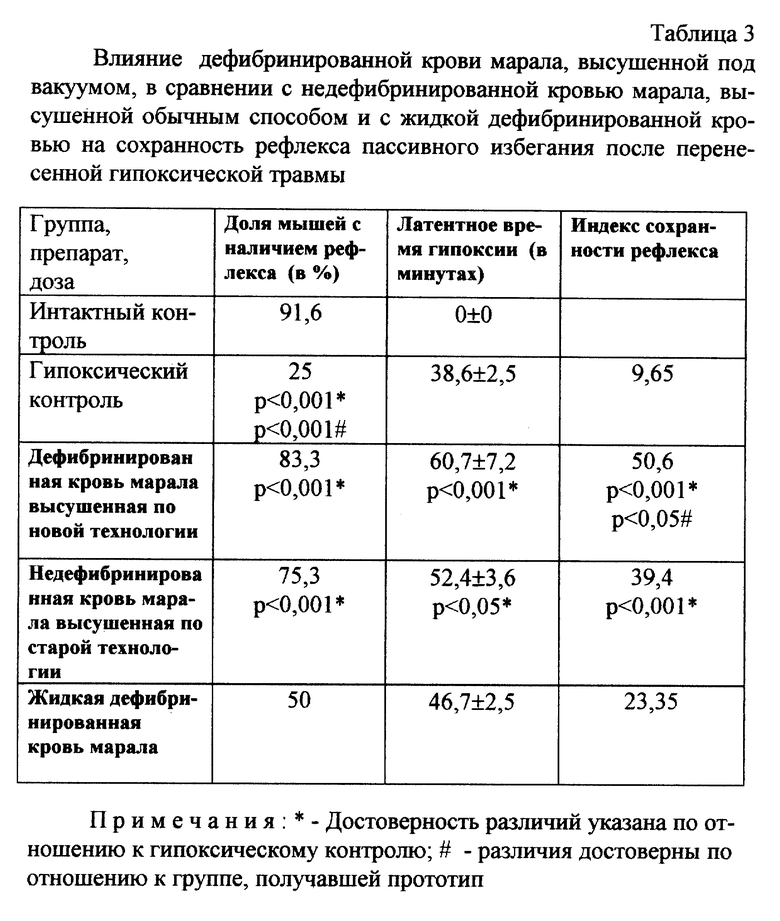
Постгипоксическая энцефалопатия моделировалась с помощью гипоксии гермобъема, ее проявления оценивали по нарушению воспроизведения условного рефлекса пассивного избегания (УРПИ). Использовалась гермокамера объемом 500 мл. Через 1 час после извлечения из гермокамеры, в которой животные находились до появления предсмертного судорожного припадка или первых агональных вдохов, у мышей вырабатывался УРПИ [12]. Проверка воспроизведения рефлекса осуществлялась через 24 часа, 1, 2 и 3 недели после выработки. О качестве рефлекса судили по доле животных с наличием рефлекса. Методика условного рефлекса пассивного избегания основана на подавлении врожденного рефлекса предпочтения темного пространства, имеющегося у грызунов. Экспериментальная установка представляла собой камеру, состоящую из двух отсеков: большого - освещенного и малого - темного. Животное помещалось в светлый отсек и вскоре (через 10-20 с), в силу врожденного рефлекса предпочтения темного пространства, переходило в малый отсек, после чего дверка, соединяющая оба отсека, перекрывалась и на пол темного отсека, состоящего из параллельных чередующихся электродов, подавали электрический ток импульсами продолжительностью 50 Mс, частотой 5 Гц и амплитудой 50 мА. Через 10 секунд дверку открывали и животное могло выскочить в светлый отсек с обычным полом. В результате описанной процедуры у животных вырабатывался условный рефлекс избегания темного пространства. При проверке воспроизводимости рефлекса животных помещали в светлый отсек в угол, противоположный от входа в темный отсек, и наблюдали в течение 3-х минут. Регистрировали время первого захода в темный отсек (латентное время захода), суммарное время пребывания в темном отсеке. Выработанным рефлекс считался, если в течение всех 3-х минут наблюдения животное ни разу не посетило темный отсек или латентное время захода превышало 150 с. Животные, которые после помещения в светлый отсек сохраняли неподвижность, при подсчете результатов не учитывались.
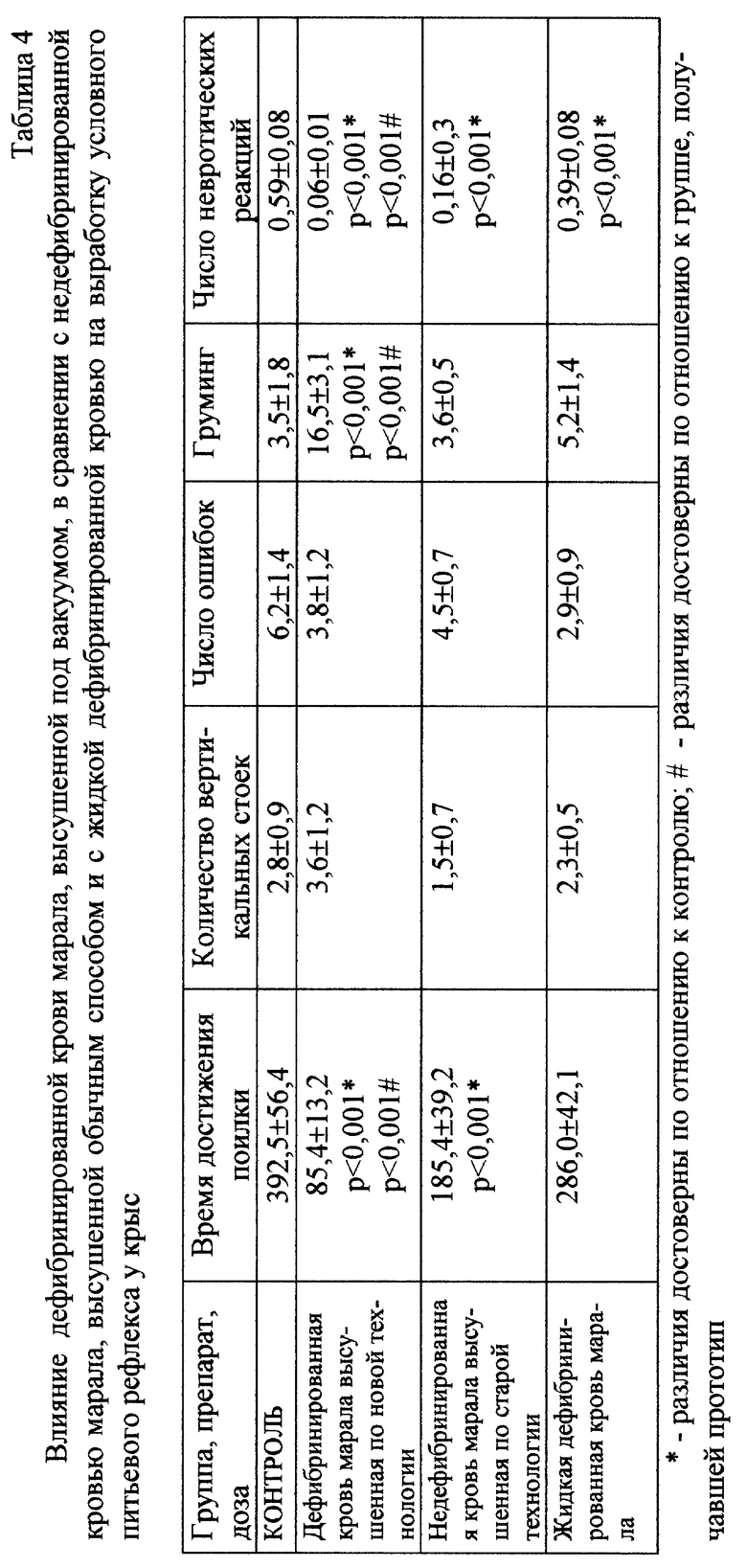
Изучение влияния композиций на выработку и воспроизведение условного питьевого рефлекса у здоровых животных проводилось в Т-образном лабиринте [8]. Опыты выполнялись на крысах на фоне водной депривации. Согласно существующим представлениям, поведение животных в условиях этой методики преимущественно отражает функциональное состояние интегративных механизмов, контролирующихся эмоциональной системой достижения цели или поведенческой активации и являющейся филогенетически самой молодой и сложной поведенческой системой мотивационного характера [14].
Лабиринт представлял собой установку, состоящую из одной стартовой камеры и двух систем коридоров, каждая из которых включала в себя по 3 Т-образных колена, спирально соединенных между собой и заканчивающихся целевыми камерами. Процедура обучения выглядела следующим образом: предварительно крыс оставляли без воды на двое суток. Затем в течение 2-х дней каждую крысу дважды в день на 20 минут с интервалом в 1 час индивидуально помещали в лабиринт, где беспорядочно были расставлены 6 поилок (первый этап обучения). На третий день животное помещалось в стартовую камеру лабиринта, при этом все поилки из последнего были убраны. Крыса начинала искать поилку, выходила из стартовой камеры и делала первый поворот в правую или левую часть лабиринта. Направление первого поворота фиксировалось и считалось предпочтительным направлением поворота для данного животного. Немедленно вслед за этим в целевую камеру, находящуюся в половине лабиринта противоположной той, в которую крыса повернула в первый раз, ставилась поилка. При всех последующих побежках поилка ставилась для данной крысы именно в эту целевую камеру. Это делалось для того, чтобы при становлении условного рефлекса исключить влияние предпочтительного направления поворота на процесс обучения. Каждое животное тестировалось в лабиринте таким образом в течение 15 минут, если оно не находило поилку раньше. Если животное не находило поилки в течение 15 минут, его помещали в целевую камеру, чтобы крыса могла напиться. Крысы, отказавшиеся искать поилку в течение первых 4-х побежек, из дальнейших экспериментов исключались. В тот же день животное через 1 час совершало вторую побежку. Таким образом, каждая крыса обучалась в течение 3-х дней (2-й этап обучения - всего 6 побежек). При этом регистрировались время достижения поилки, количество ошибок (заходы в неправильные рукава лабиринта и тупики), количество вертикальных стоек и груминг. О качестве обучения судили по сокращению времени достижения поилки и количества ошибок. Груминг и вертикальные стойки характеризовали смещенную и ориентировочно-исследовательскую активность соответственно. Об эффекте препаратов судили по разнице показателей 6-й побежки. Отказ от выполнения рефлекса после 2-х удачных нахождений поилки считался проявлением невротической реакции [15] и оценивался как самостоятельный показатель по числу невротических реакций за время обучения, считая после 2-й побежки. Введение препаратов начинали с момента лишения животных воды (всего 7 введений). Полученные экспериментальные данные обрабатывались статистически с использованием параметрического критерия Фишера и непараметрического критерия Вилкоксона [16].
Результаты исследования представлены в табл. 1-4.
В клинике НИИ фармакологии проведены клинические испытания предлагаемого биогенного препарата и пищевой добавки на его основе. Испытания действия заявляемого препарата были проведены в клинических условиях на 162 больных и 30 здоровых добровольцах. Как лекарственное средство и (или) как пищевая добавка сравниваемые препараты (сухая недефибринированная кровь, жидкая дефибринированная кровь, сухая дефибринированная кровь) назначались эквивалентными дозами в перерасчете на цельную кровь. Контрольная группа 228 больных, где в лечении использованы традиционные схемы фармакотерапии.
Клинические группы были представлены следующим образом.
1. Пациенты с хроническими заболеваниями желудочно-кишечного тракта - 41 больной (традиционная терапия - 76, сухая недефибринированная кровь - 12, жидкая дефибринированная кровь - 15).
2. Пациенты с верифицированным диагнозом "нейро-циркуляторная дистония" - 54 больных (традиционная терапия - 45, сухая недефибринированная кровь - 26, жидкая дефибринированная кровь - 18).
3. Пациенты с астеническим синдромом после перенесенных инфекционных заболеваний - 35 больных (традиционная терапия - 58, сухая недефибринированная кровь - 15, жидкая дефибринированная кровь - 13).
4. Пациенты с анемией различного генеза - 32 больных (традиционная терапия - 49, сухая недефибринированная кровь - 18, жидкая дефибринированная кровь - 21).
Исследование проведено в условиях метода слепой рандомизации.
Изучение влияния предлагаемого препарата проводилось путем сравнительного анализа ряда клинических и параклинических методов обследования. До проведения исследования у испытуемых протокольно фиксировались субъективная оценка состояния здоровья, включая оценку сна, засыпания, состояния утомления, деятельность сердечно-сосудистой системы, ряд показателей иммунного статуса, состояние периферической крови, включая анализ ее биохимических параметров, а также данные, характеризующие состояние вегетативной нервной системы.
В результате проведенного исследования было показано, что при включении в комплексную медикаментозную терапию сравниваемых препаратов не было отмечено случаев непереносимости и аллергических реакций.
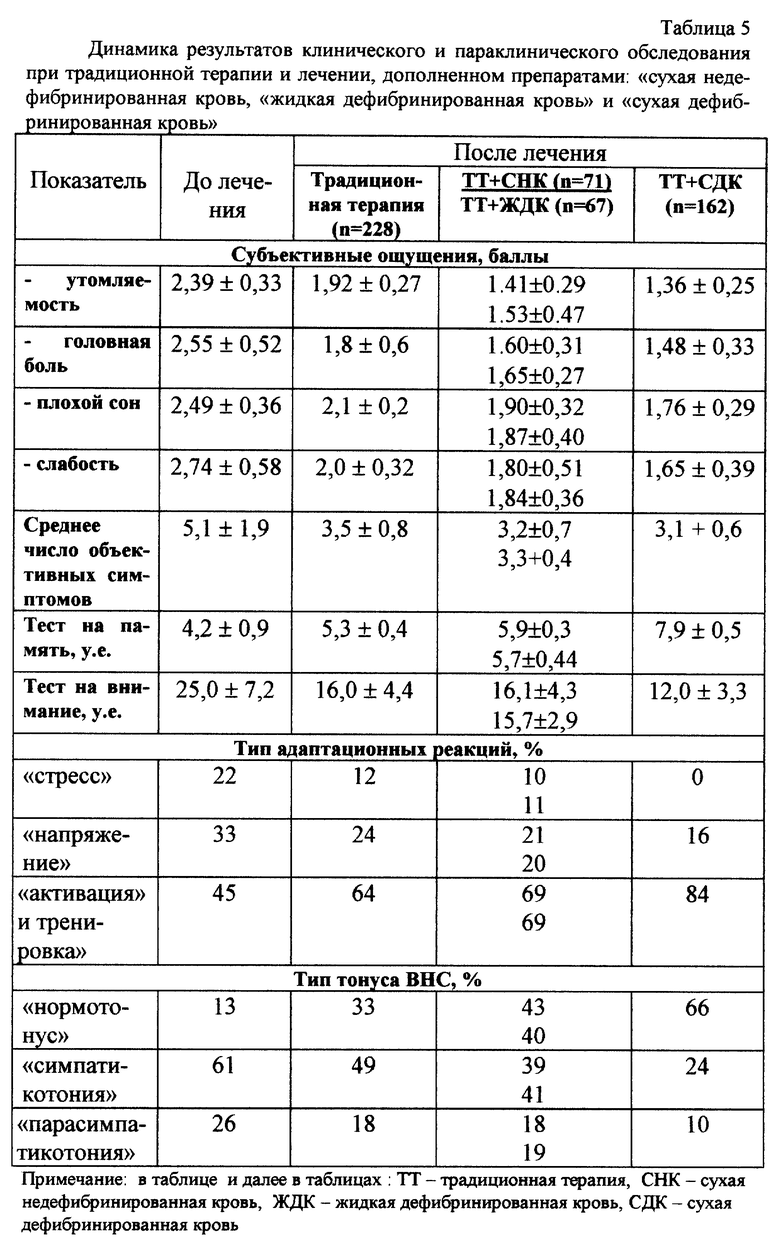
Анализ полученных данных в объединенной группе больных с изучаемыми нозологиями продемонстрировал достаточно выраженное антистрессорное, ноотропное и вегетостабилизирущее действие препаратов. В табл. 5 представлены данные по динамике анализируемых параметров объединенной группы, включившей все рассматриваемые заболевания.
Как видно из приведенных данных, в процессе проведения комплексной терапии имело место улучшение показателей психологических тестов на память, внимание, логическое мышление. При этом терапевтический эффект был выше в группе больных, получавших сухую дефибринированную кровь по сравнению с больными, получавшими сухую недефибринированную кровь и жидкую дефибринированную кровь.
Полученные результаты также свидетельствуют и о более выраженном вегетостабилизирующем действии предлагаемого препарата. Так, в ходе проводимой терапии в группе пациентов, принимающих сухую дефибринированную кровь, по отношению к группам сравнения, имеет место отчетливая тенденция к оптимизации состояния тонуса ВНС, смещающегося в сторону "нормотонии", в то время как у двух других препаратов (сухая недефибринированная и жидкая дефибринированная кровь) эти изменения были менее выраженными.
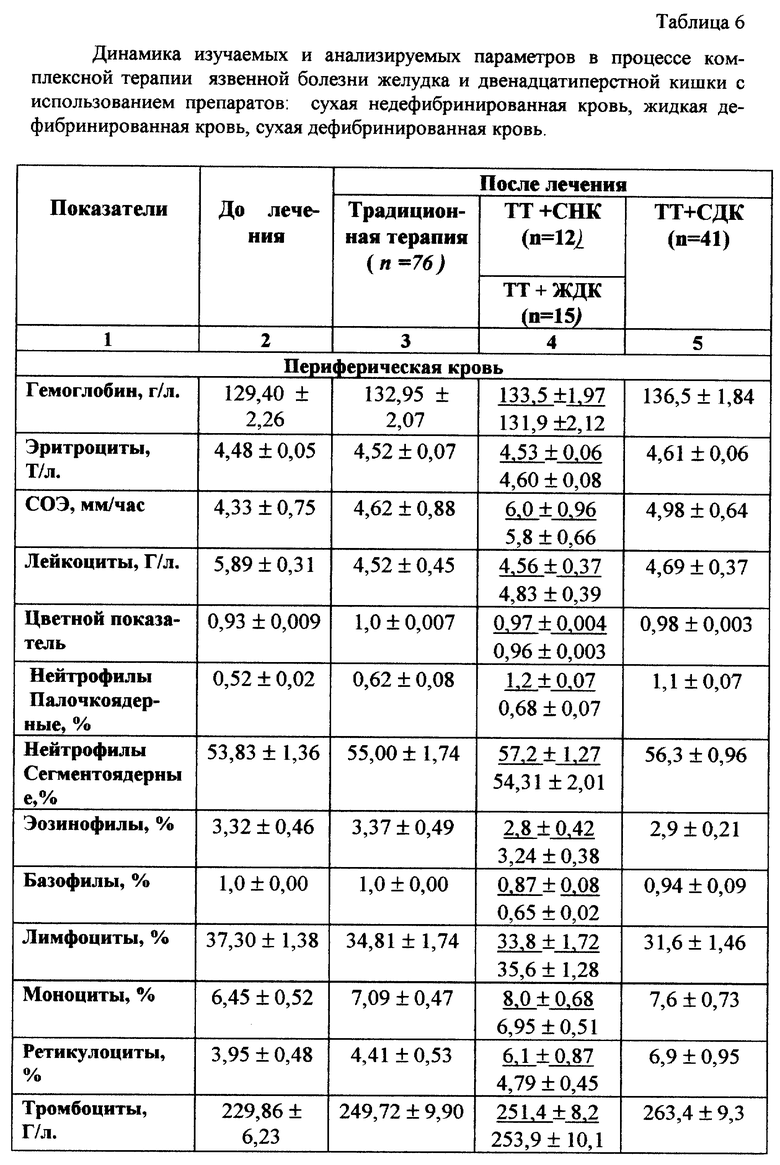
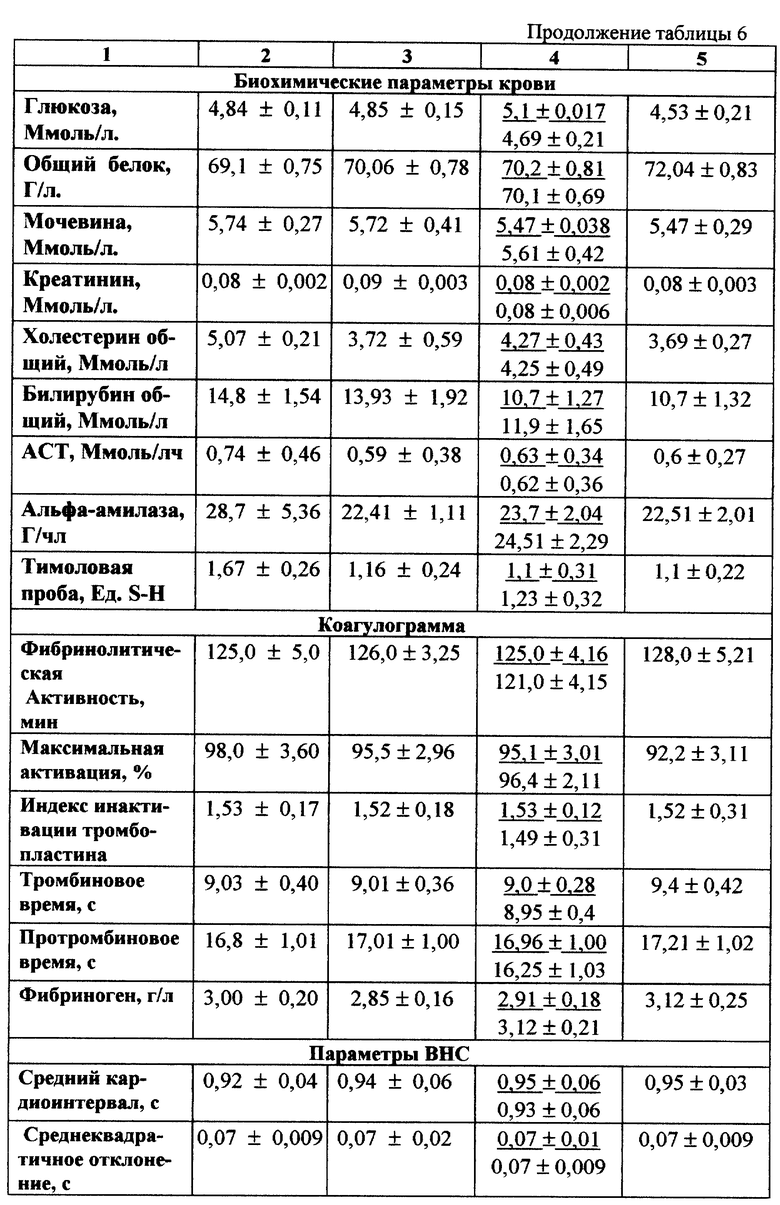
В 1-й группе испытуемых (хронические заболевания ЖКТ) назначение сравниваемых препаратов дополняло общепринятые схемы фармакотерапии. Как видно из приведенных в табл. 6 данных по динамике оцениваемых и анализируемых препаратов, наиболее выраженные положительные изменения претерпевают: в периферической крови - гемоглобин, эритроциты, ретикулоциты и тромбоциты; для биохимических характеристик - холестерин, билирубин, общий белок и тимоловая проба. При этом статистически значимо эти параметры изменяются лишь в группе пациентов, где терапия дополнена приемом препарата - "сухая дефибринированная кровь".
В полученных данных обращает на себя внимание и стабилизирующее действие исследуемого препарата на целый ряд биохимических параметров периферической крови.
Приведенные результаты наглядно демонстрируют сформировавшуюся тенденцию к улучшению ряда биохимических параметров (снижение уровня сахара крови, увеличение общего белка, уменьшение содержания холестерина крови и т.д.), характеризующих физиологически оптимальный обмен веществ в особенности в группе пациентов, где традиционная терапия была дополнена приемом препарата "сухая дефибринированная кровь".
Кроме того, были получены чрезвычайно интересные клинические данные. Так, традиционная терапия привела к закрытию язвенного дефекта на 14-е сутки лишь в 58% случаев, в то время как у больных, дополнительно получавших "сухую дефибринированную кровь " к 14 суткам не только полностью купировались болевой и диспептический синдромы, но и в 73% случаев имело место закрытие язвенного дефекта. Представленная в табл. 2 информация о динамике изучаемых и анализируемых параметров у пациентов данной группы позволяет при расчете представительства фаз ОАС судить о более высоких компенсаторно-приспособительных резервах в группе пациентов, получавших "сухую дефибринированную кровь".
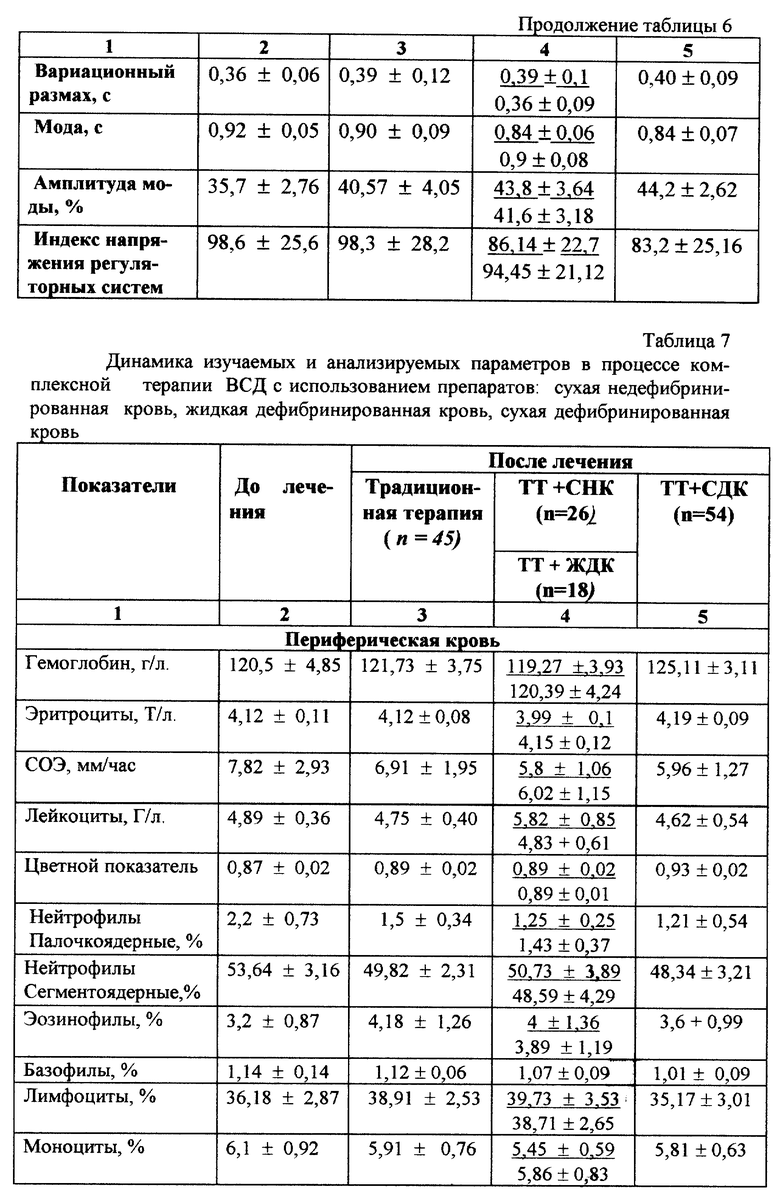
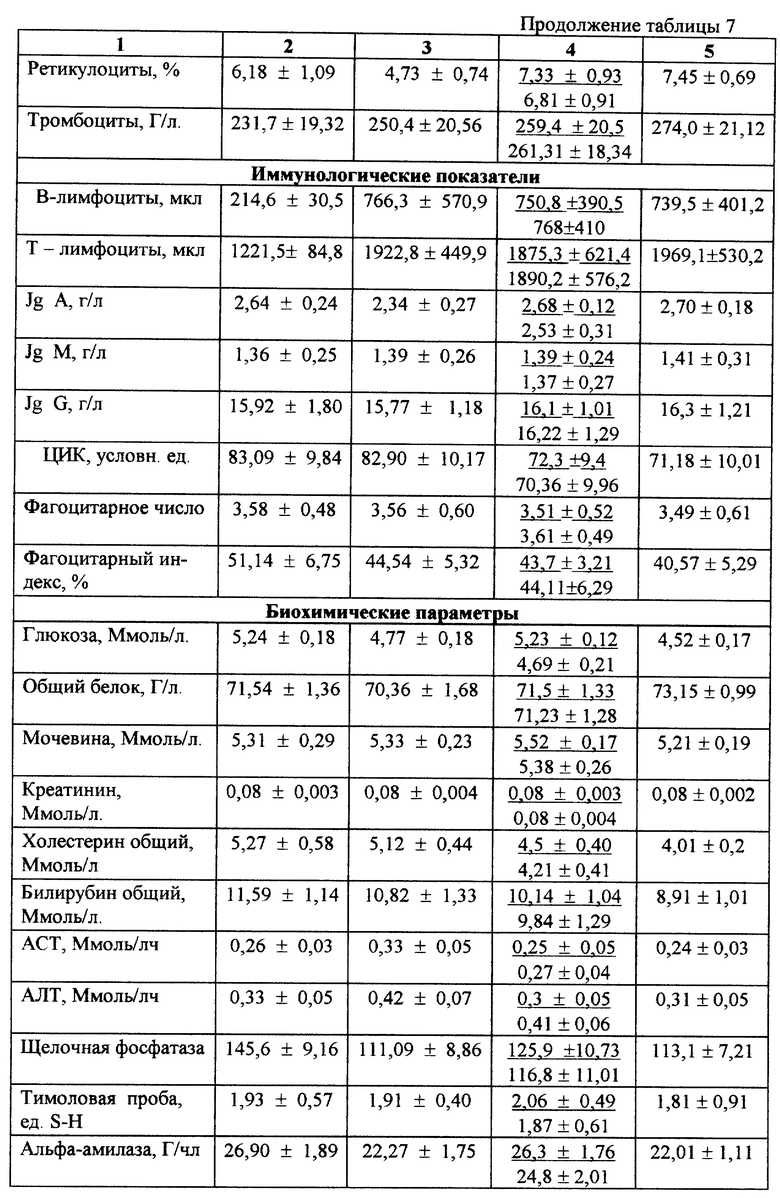
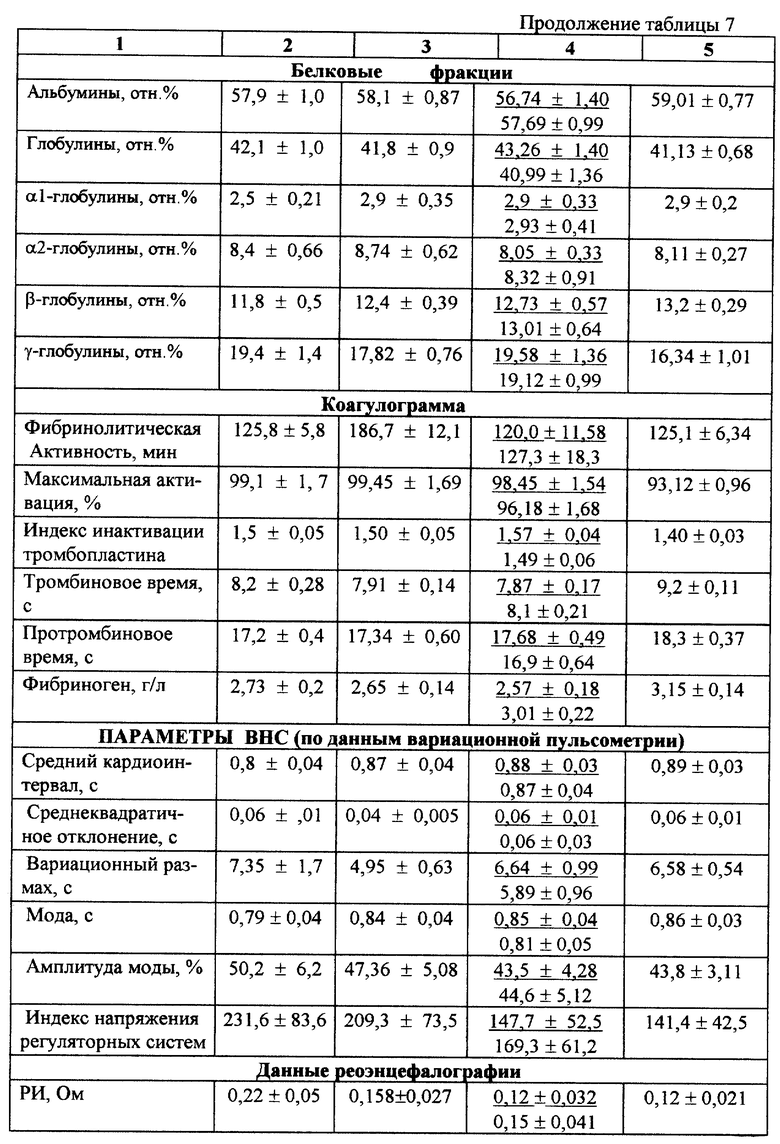
Наиболее представительную группу пролеченных с применением предлагаемого препарата составили пациенты с нейроциркуляторной дистонией по гипотоническому типу. Контроль также был представлен достаточно большой группой сопоставимых по полу и возрасту больных (45 больных для традиционной терапии). Помимо данных о более высоком "темпе" оптимизации уровня артериального давления, купирования жалоб, улучшения самочувствия и повышения работоспособности, у больных из группы, где лечение было дополнено приемом "сухая дефибринированная кровь", уже на 6-7 сутки от начала терапии сформировалась устойчивая "нормотония" и повысилась реактивность ВНС. Наиболее демонстративные изменения зарегистрированы по результатам исследования церебрального кровотока, т.е. сосудистого и гемодинамического "зеркала" течения изучаемого заболевания. Данные оцениваемых параметров приведены в табл. 7.
Как видно из приведенных результатов, в группе пациентов, получавших "сухую дефибринированную кровь", снижение исходно повышенного коэффициента асимметрии, более выражено, а зарегистрированные параметры реоэнцефалограммы в принципе схожи с таковыми, определенными у здоровых лиц. Помимо этого имеет место выраженная положительная динамика в показателях, характеризующих обмен веществ. В группе пациентов, получивших в качестве дополнительного воздействия "сухую дефибринированную кровь", определен выраженный гипохолестеринемический эффект и проявилось иммуномодулирующее действие предлагаемого препарата.
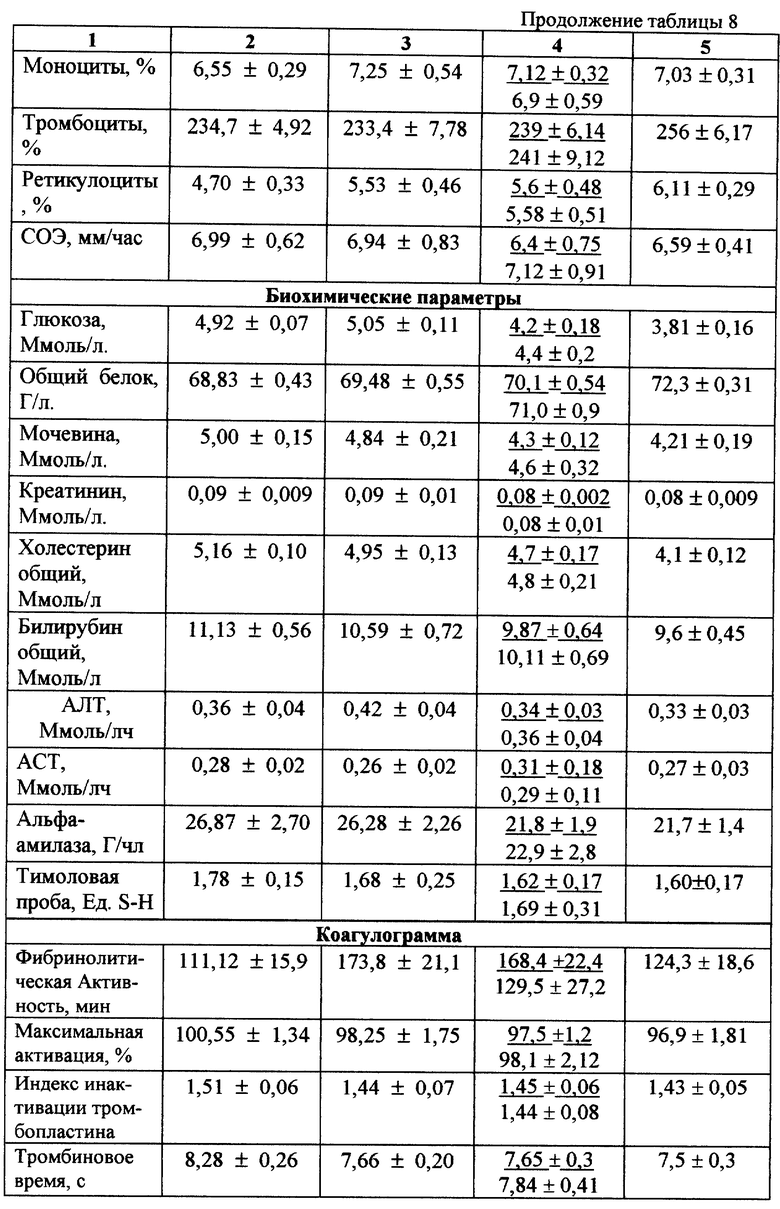
Результаты по динамике анализируемых параметров гомеостаза для групп пациентов с астеническим синдромом в ходе различных схем лечения приведены в табл. 8.
Как видно из представленных результатов, в этой группе пациентов дополнение традиционной терапии приемом препаратов "сухой недефибринированной крови", "жидкой дефибринированной крови" и "сухой дефибринированной крови" приводит к положительным клиническим эффектам. В результате проведенного исследования установлено, что у 96% из пролеченных больных значительно снизился "индекс напряжения", определяемый по данным пульсометрии, уменьшился процент лиц, имеющих отклонение тонуса вегетативной нервной системы либо в сторону преобладания парасимпатического, либо симпатического ее отдела и, следовательно, возрос процент пациентов с "нормальным" ее тонусом. Кроме того, оцененный по соотношению уровней гормонов (инсулин/кортизол) в данных группах пациентов - индекс стрессированности к окончанию терапии у больных, получивших "сухую дефибринированную кровь" статистически значимо снижен. По полученным результатам можно судить о том, что включение "сухой дефибринированной крови" в комплекс терапевтических мероприятий при лечении астенических состояний способствует повышению адаптационных возможностей организма, активации антистрессорных механизмов и за счет этого сокращению сроков клинического выздоровления.
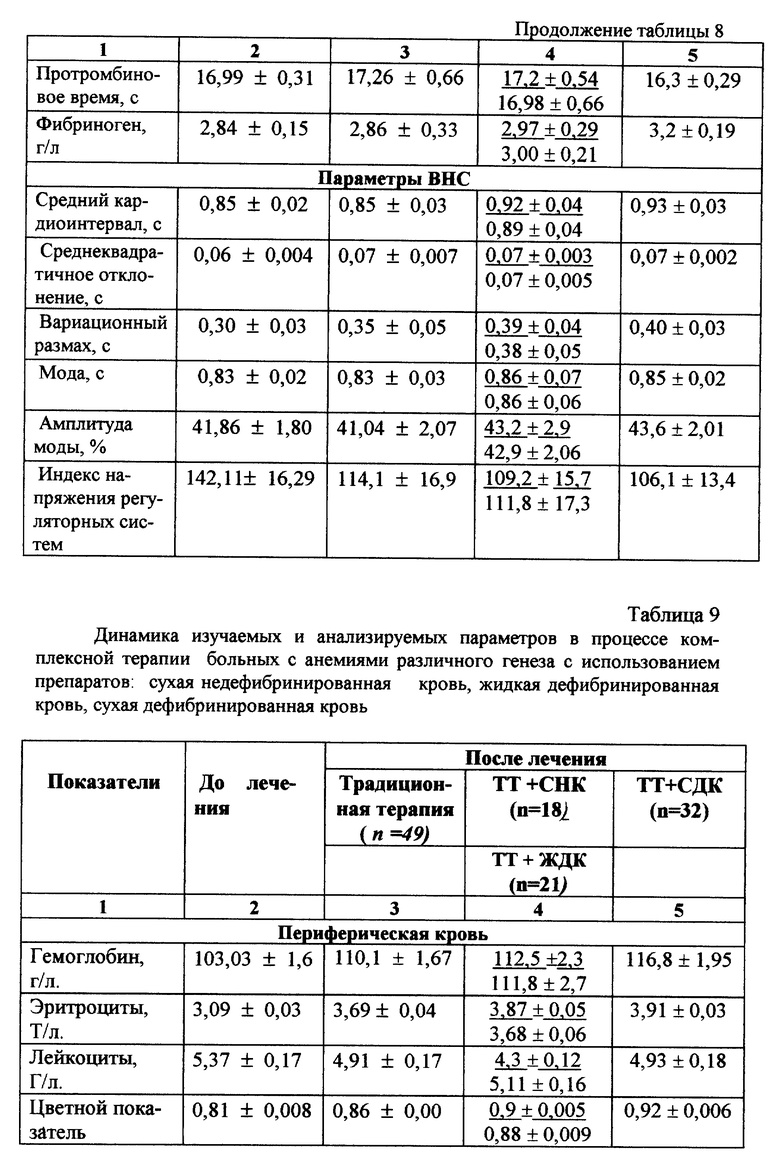
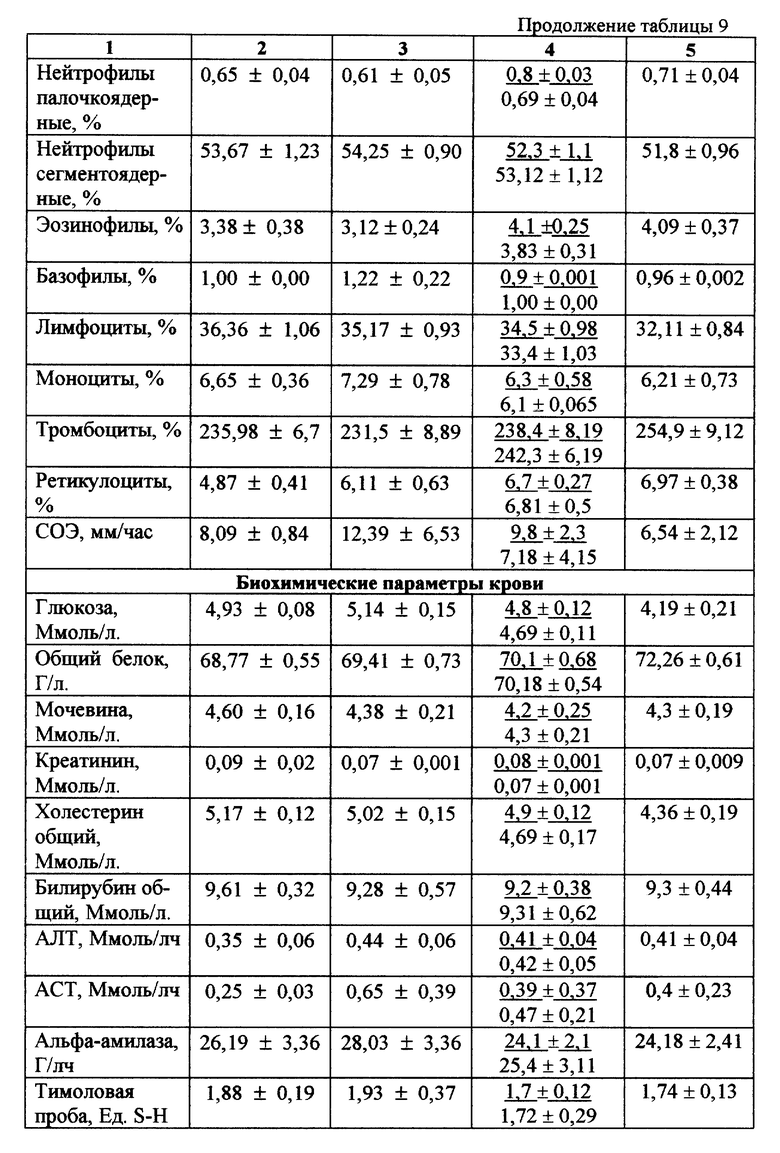
В группе пациентов, где основным диагнозом являлась анемия различного генеза, а классические схемы терапии были дополнены курсовыми назначениями препаратов "сухая недефибринированная кровь", "жидкая дефибринированная кровь" и "сухая дефибринированная кровь" (табл. 9), в динамике анализируемых параметров периферической крови обращает на себя внимание статистически значимое повышение содержания гемоглобина, эритроцитов и ретикулоцитов. Курсовая классическая специфическая терапия пациентов группы контроля приводила к подобным изменениям лишь к 30-м суткам от начала лечения. Помимо этого все пациенты исследуемой группы отмечали значительное улучшение самочувствия и повышение работоспособности, при этом эффект был более выражен также у пациентов, получавших сухую дефибринированную кровь.
В клинике Института фармакологии ТНЦ РАМН в контролируемых условиях стационара проведена клиническая апробация предлагаемой пищевой добавки на пациентах с выраженным астеническим синдромом, сформировавшимся в результате ранее перенесенных инфекционных заболеваний, физических и психических нагрузок. В процессе назначения препарата отслеживался ряд биохимических тестов, характеризующих белковый, липидный и углеводный обмены, иммунный статус. Кроме того, проводилось анкетирование и изучались результаты тестирования на память и внимание. Заявляемая пищевая добавка назначалась 3 раза в день перед едой в течение 14 дней.
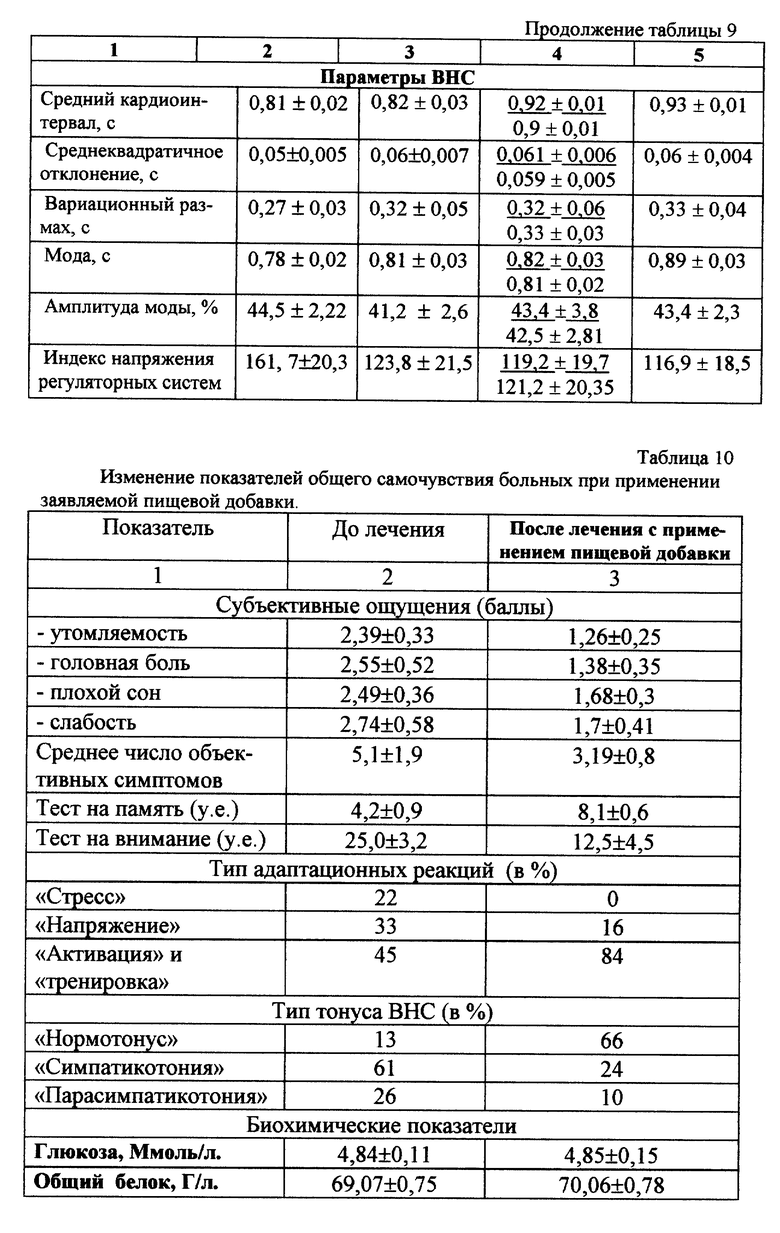
Данные анкетного опроса в изучаемой группе больных показали, что включение предлагаемой пищевой добавки вносило значительные положительные коррективы в предъявляемые жалобы на чувство дискомфорта (табл. 10). Улучшился сон, положительную динамику претерпевали тесты, характеризующие память и внимание. Случаев непереносимости и аллергических реакций на прием предлагаемой пищевой добавки не зарегистрировано.
Наиболее существенная положительная динамика определена в показателях биохимических анализов (табл. 10).
Таким образом, проведенное исследование показало достаточно высокую эффективность использования препарата "сухая дефибринированная кровь" в клинической практике, а также пищевой добавки на ее основе. Активация антистрессорных механизмов, повышение адаптационных резервов организма, отсутствие осложнений и гипохолистеринемический эффекты ставят "сухую дефибринированную кровь" в ряд препаратов, которые могут широко использоваться в терапии целого ряда заболеваний.
Сравнение заявляемого средства с известными показывает, что впервые предложено использование высушенной дефибринированной крови марала, изюбра или пятнистого оленя.
В связи с вышеизложенным можно сделать вывод, что предлагаемый биогенный препарат и пищевая добавка на его основе обладают широким спектром действия, а именно: ноотропным, адаптогенным, противоязвенным, противоневротическим, улучшающим умственную и физическую работоспособность. Как показали клинические испытания, предлагаемый биогенный препарат можно с успехом применять для лечения хронических заболеваний желудочно-кишечного тракта, нейроциркуляторных дистоний, астенических состояний различного генеза, анемий, состояний переутомления и невротических расстройств, умственного и физического переутомления, синдрома хронической усталости.
В результате экспериментальных и клинических исследований было установлено, что дефибринированная кровь, полученная предлагаемым способом, лучше сохраняет природную активность исходного продукта и обладают более высокой биологической активностью по сравнению с известным биогенным препаратом и пищевой добавкой из крови марала, изюбра или пятнистого оленя.
Литература
1. Машковский М.Д. Лекарственные средства: Пособие по фармакотерапии для врачей. - 4.1, 4.2. - М.: Медицина, 1993.- 141 С.
2. Порошкообразный биогенный препарат из окостенелых оленьих рогов и пищевая добавка на его основе. Патент РФ N 2031927.
3. Психостимулирующее средство "Пантогематоген". Патент РФ N 2008008, БИ 4-94.
4. Гольдберг Е. Д. , Дыгай А.М., Суслов Н.И. Новые препараты на основе продуктов пантового мараловодства // Medical Market. Международный медицинский журнал.- 1997. - N 2-3.- С. 54-55.
5. Биологически активная добавка к пище "Пантогематоген сухой". Регистрационное удостоверение N 000147.P. 643.08.98.
6. Положительное решение по заявке N 961139393/14 от 24 ноября 1998 г.
7. Гольдберг Е.Д., Дыгай А.М., Суслов Н.И. Адаптогенные препараты нового поколения на основе продуктов пантового мараловодства // V российский нац. конгр. "Человек и лекарство". Тезисы докладов. - Москва, 21-25 апреля 1998 г. - С. 359.
8. Добряков Ю.И. Скриниговый метод оценки антистрессорного действия препаратов. // Стресс и адаптация: Тез. Всесоюз. Симпоз. - Кишинев: Штиинца, 1978. - С. 172.
9. Суслов Н.И. Патогенетическое обоснование психофармакологических эффектов препаратов природного происхождения (экспериментальное исследование). Дисс...докт мед. наук. - Томск, 1995. - 406 С.
10. Азарашвили А. А. Исследование механизмов памяти с помощью физиологически активных соединений. - М.: Наука. - 1981. - 1983 С.
11. Brady J.V., Nauta W.J.H Subcortical mechanisms in emotional behavioral affective changes following septal forebrain lesions in albino rat. // J. comparative and phisiol. psychol. - 1953. - V. 46.- N 3. - P. 339-341.
12. Буреш Я, Бурешова О., Хьюстон Дж. П. Методики и основные эксперименты по изучению мозга и поведения. / пер. с англ. Под ред. проф. А.С. Батуева). - М.: Высшая школа, 1991. - 398 С.
13. Walsh R.N., Cummins R.A. The open-field test: a critical review. // Psychol. Bull. - 1976, V. 83. - P. 482-504.
14. Грей Дж. Нейропсихология эмоций и структура личности. // Жури. высш. Нервн. деят. - 1987. - Т. 37. - N 6. - С. 1011-1024.
15. Крушинский Л.В. Биологические основы рассудочной деятельности. - М.: Изд-во Московского ун-та, 1986,- 276 С.
16. Зайцев Г.Н. Математическая статистика в экспериментальной ботанике. - М.: Наука, 1984. - 425 С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНЫМ И АДАПТОГЕННЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2130314C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНЫМ И АДАПТОГЕННЫМ ДЕЙСТВИЕМ | 1998 |
|
RU2136292C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИГИПЕРЛИПОПРОТЕИНЕМИЧЕСКОЙ АКТИВНОСТЬЮ, ПИЩЕВАЯ ДОБАВКА НА ЕГО ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ НАРУШЕНИЙ ЛИПИДНОГО ОБМЕНА У БОЛЬНЫХ С СЕРДЕЧНО-СОСУДИСТЫМИ ЗАБОЛЕВАНИЯМИ | 2001 |
|
RU2201239C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И КОРРЕКЦИИ ВОЗРАСТНЫХ НАРУШЕНИЙ ВЫСШЕЙ НЕРВНОЙ ДЕЯТЕЛЬНОСТИ | 2005 |
|
RU2296573C2 |
| СРЕДСТВО ДЛЯ РЕГУЛЯЦИИ МЕНСТРУАЛЬНОГО ЦИКЛА ПРИ ВТОРИЧНОЙ НОРМОГОНАДОТРОПНОЙ АМЕНОРЕЕ И ОЛИГОМЕНОРЕЕ И СПОСОБ ЛЕЧЕНИЯ | 2004 |
|
RU2275923C1 |
| СРЕДСТВО, СТИМУЛИРУЮЩЕЕ ГРАНУЛОМОНОЦИТОПОЭЗ ПРИ ГИПОПЛАСТИЧЕСКИХ СОСТОЯНИЯХ КРОВЕТВОРЕНИЯ | 2001 |
|
RU2182007C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ВАЗОМОТОРНЫХ И ЭМОЦИОНАЛЬНО-ВЕГЕТАТИВНЫХ ПРОЯВЛЕНИЙ КЛИМАКТЕРИЧЕСКОГО СИНДРОМА И СПОСОБ ЛЕЧЕНИЯ | 2004 |
|
RU2274458C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА НА ОСНОВЕ ПАНТОВ ОЛЕНЯ | 1992 |
|
RU2045269C1 |
| ПСИХОСТИМУЛИРУЮЩЕЕ СРЕДСТВО "ПАНТОГЕМАТОГЕН" | 1992 |
|
RU2008008C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПАНТОВОЙ МУКИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ | 1992 |
|
RU2070048C1 |


Изобретение относится к медицине, а именно к фармакологии. Сущность изобретения: биогенный препарат и пищевая добавка на его основе содержат высушенную дефибринированную кровь марала, изюбра или пятнистого оленя. Способ получения биогенного препарата и пищевой добавки заключается в высушивании отделенной от фибрина крови марала, изюбра или пятнистого оленя под вакуумом от 5 до 600 мм рт.ст. при температуре не выше 45°С до влажности 4 - 5%. Технический результат: расширение ассортимента средств, обладающих высокой фармакологической активностью и широким спектром действия, а именно ноотропным, адаптогенным, противоязвенным, противоневротическим, улучшающим умственную и физическую работоспособность. 3 с.п. ф-лы, 10 табл.
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНЫМ И АДАПТОГЕННЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2130314C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО ПРОДУКТА ПАНТОВОГО ОЛЕНЕВОДСТВА, СПОСОБ ЗАБОРА ДОНОРСКОЙ КРОВИ У ПАНТОВЫХ ОЛЕНЕЙ И СПОСОБ ОЗДОРОВЛЕНИЯ ЧЕЛОВЕКА | 1998 |
|
RU2130777C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМАТОГЕНА | 1992 |
|
RU2057536C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ВЛИЯЮЩЕГО НА ГЕМОПОЭЗ ИЗ КРОВИ ЖИВОТНЫХ | 1991 |
|
RU2017493C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ДЛЯ ПРОФИЛАКТИКИ НАРУШЕНИЙ ПРОЦЕССОВ КРОВЕТВОРЕНИЯ | 1990 |
|
RU2014081C1 |
| Способ получения гематогена | 1990 |
|
SU1752393A1 |
| УГЛЕРОДНЫЕ НАНОСТРУКТУРЫ И СЕТКИ, ПОЛУЧЕННЫЕ ХИМИЧЕСКИМ ОСАЖДЕНИЕМ ИЗ ПАРОВОЙ ФАЗЫ | 2011 |
|
RU2579075C2 |
Авторы
Даты
2001-03-10—Публикация
1999-06-17—Подача