Изобретение относится к фармацевтической химии, клинической и экспериментальной медицине, конкретно к пульмонологии, и может быть использовано при получении пролонгированных туберкулостатических препаратов, преимущественно на основе изониазида, применяемых для общего и местного лечения туберкулеза легких.
Данные эпидемиологической статистики свидетельствуют о значительном прогрессировании темпов роста заболеваемости туберкулезом во всем мире и особенно в развивающихся странах. Существующие методы лечения и арсенал противотуберкулезных препаратов за последние десятилетия практически не изменился. В основе базисной терапии этого заболевания по-прежнему используется изониазид (гидразид изоникотиновой кислоты) со свойственными ему побочными эффектами в виде нарушений гемопоэза, функции печени, почек и т.д. Известно, что лишь незначительная часть изониазида попадает в очаг поражения и макрофаги, которые являются основным местом персистенции микобактерий туберкулеза вследствие незавершенности фагоцитоза на стадии слияния фагосомы с лизосомами. Большая часть вводимого изониазида подвергается биотрансформации, не оказывая бактериостатического действия. В связи с этим создание лекарственных препаратов на основе изониазида как наиболее эффективного туберкулостаика, обладающих пролонгированным действием, направленным на различные звенья патогенеза туберкулеза, является весьма актуальной задачей.
Известна композиция, обладающая пролонгированным противотуберкулезным действием, содержащая изониазид, иммобилизованный на декстране с молекулярной массой 20 - 40 кДа (Патент РФ N 2087146, кл. A 61 K 31/455, опубл. 20.08.97, Бюл. N 23). Данная композиция позволяет целенаправленно доставлять туберкулостатик в макрофаги, снизить дозу применяемого препарата и в значительной степени избежать побочных эффектов изониазида. Недостатками известной композиции является ее способность воздействовать лишь на одно звено патогенеза туберкулеза, а именно на очаг персистенции микобактерий, в связи с чем область ее применения ограничивается генерализованными формами заболевания, которые по частоте встречаются значительно реже очаговых форм туберкулеза. При местном применении для санации туберкулезных каверн данная композиция по эффективности практически соответствует неиммобилизованному изониазиду. Наличие в каверне казеозных некротических масс, представленных денатурированными белками и спорами микобактерий, а также морфологические особенности строения стенки каверны, такие как обширные и многослойные участки некротически измененной соединительной ткани с низкой васкуляризацией, практически исключают резорбцию вводимого интракавернозно туберкулостатика.
Известна фармацевтическая композиция, обладающая пролонгированным противотуберкулезным действием, содержащая, мас.%: изониазид - 1,0; плазмозамещающий раствор "Гемодез" - остальное (АС СССР N 1697314, кл. A 61 K 31/455, 1997, Бюл. N 34). Известную композицию получают путем смешения гемодеза с кристаллическим порошком изониазида, взятом в количестве, необходимом для приготовления 1,0%-ного раствора, с последующей фильтрацией полученной смеси через бактериальный фильтр с диаметром пор 0,22 мкм. Недостатком известной композиции является то, что она не обладает лизосомотропным действием и не захватывается селективно макрофагами, вследствие чего не происходит целенаправленной доставки туберкулостатика в зону персистенции микобактерий. Действие препарата направлено лишь на одно звено патогенеза туберкулеза - микобактерии, а при местном применении по эффективности он практически не отличается от немодифицированного изониазида, так как не обладает способностью лизировать ткани, подвергшиеся казеозному некрозу.
Наиболее близкой к заявляемой композиции - прототипом, является композиция для ферментативного гидролиза белков, содержащая следующие компоненты, мас. %: комплекс иммобилизованных на водорастворимом синтетическом полимере нейтральных и щелочных протеиназ из Bac.subtilis с активностью 12-750 ПЕ/г - от 10 до 30, наполнитель - полиэтиленгликоль или гель полиэтиленгликоля с мол. массой 600 - 2000 кДа - от 70 до 90 (Патент РФ N 2003346, кл. A 61 K 37/54, опубл. 30.11.93, Бюл. N 43-44).
Известная композиция представляет собой бесцветную вязкую жидкость без вкуса и запаха, растворимую в воде. Композиция предназначена для использования в медицине для гидролиза белков гнойно-некротических масс, в том числе она применяется в качестве средства для энзиматического очищения каверн при хирургическом лечении деструктивного туберкулеза легких (А.С. N 1688882, кл. A 61 K 37/48, опубл. 07.11.91, Бюл. N 41). Основным недостатком композиции-прототипа является отсутствие прямого туберкулостатического действия, так как она не содержит ни одного из известных противотуберкулезных препаратов. В связи с этим данная композиция применяется только в качестве вспомогательного лекарственного средства в комплексной терапии туберкулеза легких.
Технической задачей изобретения является создание фармацевтической композиции, которая была бы способна осуществлять ферментативный лизис денатурированных белков некротизированных тканей в каверне и обладала бы прямым туберкулостатическим действием.
Поставленная техническая задача достигается предлагаемой композицией, содержащей следующие компоненты, мас.%:
Протосубтилин Г3Х - 1,9-2,1
Изониазид - 0,4-4,0
Полиэтиленоксид 1500 - 8,0-10,0
Буферный раствор с pH 7,5-8,2 - Остальное.
Предлагаемая композиция облучается гамма-излучением или потоком ускоренных электронов с энергией 2 МэВ в дозе 1,0 Мрад для проведения иммобилизации изониазида на полиэтиленоксиде и белках, входящих в состав протосубтилина, в том числе и протеазный комплекс.
Вводимый в состав предлагаемой композиции ферментный препарат протосубтилин Г3Х содержит протеазный комплекс Bac.subtilis, который при воздействии ионизирующего излучения связывается с полиэтиленоксидом 1500, образуя иммобилизованную форму, обладающую стабильностью и пролонгированным терапевтическим действием. При концентрации протосубтилина менее 1,9 мас.% протеолитическая активность получаемой композиции недостаточна для проведения эффективного гидролиза денатурированных белков нек- ротизированных тканей, а при концентрации протосубтилина свыше 2,1 мас. % возможен гидролиз нативных белков и замедление регенеративных процессов в тканях.
В качестве активного туберкулостатического компонента в предлагаемую композицию включен изониазид в количестве 0,4-4,0 мас.%. Диапазон концентраций изониазида выбран исходя из используемых в клинической практике доз данного туберкулостатака, который составляет в среднем от 5 до 15 мг на 1 кг массы тела. При снижении в предлагаемой композиции изониазида менее 0,4% для достижения терапевтической концентрации требуется введение больших объемов жидкости, особенно при парентеральном пути введения, которые могут вызвать гиперволемию. Верхний уровень концентрации изониазида в композиции обусловлен не только стремлением снизить объем вводимой жидкости при парентеральном введении, но и пределом растворимости данного препарата в присутствии белков протеазного комплекса и полиэтиленоксида. При использовании компонентов заявляемой композиции в запредельных количествах эффективность действия последней снижается, а органолептические свойства ухудшаются. При воздействии ионизирующего излучения на предлагаемую композицию происходит связывание изониазида как с полиэтиленоксидом, так и с белками протеазного комплекса.
На чертеже представлены данные хроматографического исследования на ДЭАЭ-целлюлозе связывания изониазида с полиэтиленоксидом 1500 и протосубтилином Г3Х (колонка 0,9 х 20 см, элюент - 0,01 М Трис-HCl буфер с pH 8,5; стрелкой на хроматограмме обозначено начало подачи ступенчатого градиента соли - 3% раствора хлорида натрия, детекция хроматографических фракций по поглощению света при длине волны 290 нм). Исследованию подвергались 3 варианта проб: 1 вариант - протосубтилин Г3Х, иммобилизованный радиационным способом на полиэтиленоксиде 1500 (кривая 1 - ____); 2 вариант - протосубтилин Г3Х, иммобилизованный на полиэтиленоксиде 1500 содержащий несвязанный изониазид (кривая 2 - ..... ); 3 вариант - заявляемая композиция (кривая 3 -  ).
).
Из чертежа видно, что хроматографический профиль пробы 1 варианта (кривая 1) имеет две фракции: первая фракция элюируется в изократическом режиме и содержит основную массу полиэтиленоксида 1500 и часть белков протосубтилина, вторая фракция, неоднородная по своему составу, элюируется при подаче на колонку ступенчатого градиента соли (3% раствора хлорида натрия) и содержит основную часть протеаз, модифицированных полиэтиленоксидом 1500. При добавлении изониазида в пробу 1 варианта появляется добавочный пик несвязанного изониазида (кривая 2), происходит незначительное увеличение поглощения фракции элюируемой в изократическом режиме за счет неспецифического связывания изониазида с полиэтиленоксидом. Поглощение фракции, содержащей протеазный комплекс, остается без изменений за счет отсутствия связывания с изониазидом. При действии гамма-излучения на предлагаемую композицию хроматографическая картина изменяется (кривая 3); происходит значительное увеличение поглощения при 290 нм всех хроматографических фракций, что свидетельствует о связывании изониазида как с полиэтиленоксидом, так и с белками протеазного комплекса.
Предлагаемую композицию получают следующим образом.
Готовят реакционную смесь путем растворения протосубтилина, преимущественно протосубтилина Г3Х, в 0,025 М натрий-фосфатном буферном растворе с pH 7,5 - 8,2, полиэтиленоксида (ПЭО) с молекулярной массой 1500 Да, полученную смесь очищают путем осаждения балластных белков и удаления последних фильтрованием. В фильтрате растворяют изониазид до конечной концентрации от 4 до 40 мг/мл. Полученный раствор фасуют по 10 мл во флаконы вместимостью 15 мл и подвергают облучению гамма-лучами в дозе 1 Мрад.
В результате получают композицию, содержащую иммобилизованные на полиэтиленоксиде 1500 протеазы из Bac.subtilis в комплексе с изониазидом. Протеолитическая активность полученной композиции составляет от 40 до 60 ПЕ/мл, концентрация изониазида от 4 до 40 мг/мл. Композиция представляет собой жидкость желтого цвета.
Определяющим существенным отличием предлагаемой композиции от композиции-прототипа, является то, что она дополнительно содержит изониазид и обладает наряду с протеолитической активностью также прямым антимикобактериальным действием за счет включения в ее состав изониазида.
Изобретение проверено в лабораторных условиях in vitro и in vivo путем проведения ряда опытов на культуре микобактерий туберкулеза и на моделях туберкулеза у экспериментальных животных.
В результате поиска по источникам патентной и научно-технической информации, не выявлено сведений о фармацевтической композиции, обладающей пролонгированным противотуберкулезным действием, аналогичной заявляемой.
Изобретение иллюстрируется следующими примерами приготовления конкретных рецептур заявляемой композиции.
Пример 1.
30 г полиэтиленоксида 1500 растворяют в 300 мл 0,025 М натрий-фосфатного буфера с pH 7,5, добавляют 6,3 г протосубтилина Г3Х, смесь перемешивают при температуре 18 - 20oC в течение 30 минут. Затем проводят осаждение балластных белков методом солевого осаждения. Для этого в смесь последовательно добавляют до полного растворения 1,3 г натрия фосфорнокислого двузамещенного до конечной концентрации 0,45% и 1,9 г хлорида кальция до конечной концентрации 0,63%. После растворения хлорида кальция в реакционной смеси выпадает осадок нерастворимого фосфата кальция, который адсорбирует балластные белки. Смесь выдерживают 12 часов при температуре от 4 до 8oC для полного осаждения балластных белков. Далее реакционную смесь фильтруют через бумажные фильтры ("белая лента"). Объем фильтрата составляет 300 мл. К полученному фильтрату добавляют 12 г изониазида до конечной концентрации 40 мг/мл. Полученный раствор фасуют по 10 мл во флаконы вместимостью 15 мл и подвергают облучению гамма-лучами в дозе 1 Мрад. В результате получают компоцицию следующего состава, мас.%:
1. Протосубтилин Г3Х - 2,1
2. Изониазид - 4,0
3. Полиэтиленоксид 1500 - 10,0
4. 0,025 М Натрий-фосфатный буфер - 83,9
Пример 2.
27 г полиэтиленоксида 1500 растворяют в 300 мл 0,025 М натрий-фосфатного буфера с pH 8,2, добавляют 6,0 г протосубтилина Г3Х, смесь перемешивают при температуре 18 - 20oC в течение 30 минут. Затем проводят осаждение балластных белков методом солевого осаждения. Для этого в смесь последовательно добавляют до полного растворения 1,3 г натрия фосфорнокислого двузамещенного до конечной концентрации 0,45% и 1,9 г хлорида кальция до конечной концентрации 0,63%. После растворения хлорида кальция в реакционной смеси выпадает осадок нерастворимого фосфата кальция, который адсорбирует балластные белки. Смесь выдерживают 12 часов при температуре от 4 до 8oC для полного осаждения балластных белков. Далее реакционную смесь фильтруют через бумажные фильтры ("белая лента"). Объем фильтрата составляет 300 мл. К полученному фильтрату добавляют 6,0 г изониазида до конечной концентрации 20 мг/мл. Полученный раствор фасуют по 10 мл во флаконы вместимостью 15 мл и подвергают облучению гамма-лучами в дозе 1 Мрад. В результате получают компоцицию следующего состава, мас.%:
1. Протосубтилин Г3Х - 2,0
2. Изониазид - 2,0
3. Полиэтиленоксид 1500 - 9,0
4. 0,025 М Натрий-фосфатный буфер - 87,0
Пример 3.
24 г полиэтиленоксида 1500 растворяют в 300 мл 0,025 М натрий-фосфатного буфера с pH 8,2, добавляют 5,7 г протосубтилина Г3Х, смесь перемешивают при температуре 18 - 20o в течение 30 минут. Затем проводят осаждение балластных белков методом солевого осаждения. Для этого в смесь последовательно добавляют до полного растворения 1,3 г натрия фосфорнокислого двузамещенного до конечной концентрации 0,45% и 1,9 г хлорида кальция до конечной концентрации 0,63%. После растворения хлорида кальция в реакционной смеси выпадает осадок нерастворимого фосфата кальция, который адсорбирует балластные белки. Смесь выдерживают 12 часов при температуре от 4 до 8oC для полного осаждения балластных белков. Далее реакционную смесь фильтруют через бумажные фильтры ("белая лента"). Объем фильтрата составляет 300 мл. К полученному фильтрату добавляют 1,2 г изониазида до конечной концентрации 4,0 мг/мл. Полученный раствор фасуют по 10 мл во флаконы вместимостью 15 мл и подвергают облучению гамма-лучами в дозе 1 Мрад. В результате получают компоцицию следующего состава, мас.%:
1. Протосубтилин Г3Х - 1,9
2. Изониазид - 0,4
3. Полиэтиленоксид 1500 - 8,0
4. 0,025 М Натрий-фосфатный буфер - 89,7
Использование предлагаемой композиции позволит по сравнению с композицией-прототипом:
- расширить область применения композиции для лечения как очаговых, так и генерализованных форм туберкулеза легких;
- расширить арсенал медикаментозных средств пролонгированного действия для лечения больных с различными формами туберкулеза.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ТРОМБОЛИТИЧЕСКИМИ, ПРОТИВОВОСПАЛИТЕЛЬНЫМИ И ЦИТОПРОТЕКТИВНЫМИ СВОЙСТВАМИ | 2001 |
|
RU2213557C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМОГО ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА ПРОТЕАЗ | 2004 |
|
RU2270861C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОНИАЗИДА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 1999 |
|
RU2143900C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМОГО ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА | 1998 |
|
RU2137835C1 |
| КОНЪЮГАТ АНТИБИОТИКА И АНТИБАКТЕРИАЛЬНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2007 |
|
RU2371447C2 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, ОБЛАДАЮЩИЙ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2332216C2 |
| ПРОТИВОТУБЕРКУЛЕЗНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2010 |
|
RU2424809C1 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2413517C1 |
| ПРОТИВОТУБЕРКУЛЕЗНЫЙ ПРЕПАРАТ | 2002 |
|
RU2211035C1 |
| МНОГОКОМПОНЕНТНЫЙ КОМБИНИРОВАННЫЙ СОСТАВ, ОБЛАДАЮЩИЙ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2384334C2 |
Изобретение относится к фармацевтической промышленности и медицине, конкретно к фтизиатрии. Изобретение заключается в том, что предложенная фармацевтическая композиция содержит ферментный препарат - протосубтилин ГЗХ, изониазид, полиэтиленоксид и буферную смесь с рН 7,5-8,2 при определенном содержании компонентов. Изобретение обеспечивает широкую область применения и может быть использовано для лечения различных форм туберкулеза. 2 з.п.ф-лы, 1 ил.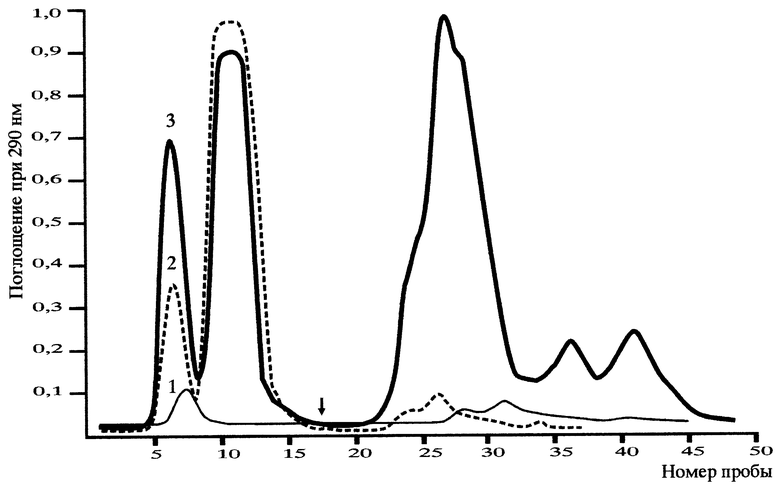
Протосубтилин ГЗХ - 1,9 - 2,1
Изониазид - 0,4 - 4,0
Полиэтиленоксид - 0,8 - 10,0
Буферная смесь - Остальное
2. Фармацевтическая композиция по п.1, отличающаяся тем, что полиэтиленоксид используют с мол.м. 1500 Да.
| СПОСОБ ЛЕЧЕНИЯ ГЕНЕРАЛИЗОВАННОГО ТУБЕРКУЛЕЗНОГО ПРОЦЕССА В ЭКСПЕРИМЕНТЕ | 1993 |
|
RU2087146C1 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, ОБЛАДАЮЩИЙ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2146130C1 |
| RU 2003346, 30.11.1993. | |||
Авторы
Даты
2001-06-27—Публикация
1999-10-26—Подача