Изобретение относится к материалам и методическим рекомендациям по регулированию распространения инфекции вируса гепатита ни-А, ни-В (ВГНАНВ) и, в частности, относится к этиологическому агенту гепатита ни-А, ни-В (ГНАНВ), вирусу гепатита С (ВГС) и полинуклеотидам и их аналогам для диагностики ВГС в биологических средах.
Гепатит ни-А, ни-В (ГНАНВ) - трансмиссивное заболевание или группа заболеваний, которое, как полагают, индуцируется вирусами и дифференцируется с другими заболеваниями печени, индуцированными такими известными вирусами, как вирус гепатита А (ВГА), вирус гепатита В (ВГВ) и дельта-вирус гепатита (ВГД), а также с гепатитом, индуцированным цитомегаловирусом (ЦМВ) или вирусом Эпштейна-Барр (ЭБВ). Впервые ГНАНВ был идентифицирован у индивидуумов, которым производились трансфузии. Передача инфекции от человека шимпанзе и перенос от них возбудителя на других шимпанзе позволяет отнести ГНАНВ к трансмиссивной инфекции, переносимой одним или несколькими переносчиками болезни.
Эпидемиологические данные показывают, что возможны три пути передачи ГНАНВ: водный путь, парентеральный путь (через кровь и иглы взятия крови) и спорадические случаи инфицирования групп людей. Однако число этиологических типов, которые могут привести к заболеванию ГНАНВ, остается невыясненным.
Имеется ряд переносчиков ГНАНВ. См. информацию о них, например, в трудах Принс (1983), Фаинстон и Хуфнагель (1984), Оверби (1985, 1986, 1987), Иварсон (1987). Однако доказательств того, что какой-то из них является этиологическим агентом ГНАНВ не имеется.
Важным является требование к асертике при проведении специфичных методов выявления и идентификации носителей ВГНАНВ, крови и препаратов крови, инфицированных этим вирусом. В 10% случаев гемотрансфузии приводят к пострансфузионному гепатиту (ПТГ), причем около 90% данного заболевания обусловлено ГНАНВ. Главной проблемой этой болезни остается большая частота хронизации процесса поражения печени (25-55%).
Необходимость ухода за больными и предупреждения передачи инфекции ГНАНВ через кровь и ее препараты или через бытовой контакт обусловливают повышение требований к надежности скрининга, диагностики и прогноза с целью выявления нуклеиновых кислот, антигенов и антител, относящихся к ВГНАНВ.
Известны способы выявления определенных полинуклеотидов путем проведения гибридизационных анализов. См. работы, например, Мэттюз и Крика, кн. "Аналитическая биохимия", 1988, т. 169, стр. 1, Ландегрен и соавт., журн. "Сайенс", т. 242, стр. 229: и Миттлин, журн. "Клиническая химия", 1989, т. 35, стр. 1819, патент США 4868105, 9.09.1989, публ. ЕРО 225807, 16.07.1987.
До открытия ВГС заявителем способы выделения и/или детекции определенных полинуклеотидов гибридизацией не могли применяться для скрининга ВГС. В настоящем изобретении представлены материалы и способы получения вирусных геномных последовательностей (см. ниже, а также в межд. публ. РСТ/90/ 14436).
Отличительной особенностью изобретения является процесс выявления ВГС-последовательности в аналит-цепи, имеющей, как полагают, ВГС-полинуклеотид, в которой указанный ВГС-полинуклеотид содержит взятую выборочно область-мишень, содержащий:
а) этап формирования олигомера(ов), способного гибридизировать ВГС-последовательность в аналит-полинуклеотидной цепи, в которой указанный олигомер содержит полинуклеотидную последовательность, взятую выборочно из группы олигонуклеотидов, комплементарных следующим районам ВГС-генома (как показано на фиг. 1): 16-45, 49-78, 82-111, 115-144, 148-177, 211-240, 242-271, 275-304, 332-361, 365-394, 398-427 и 457-486;
b) этап инкубации аналит-цепи с олигомером(ами) (а), дающий возможность сформировать специфические гибридные дуплексы между последовательностью предполагаемой области-мишени и последовательностью выбранной области-мишени; и
d) этап детекции гибридов, сформированных между областью-мишенью, если таковая имеется, и указанным олигоме-ром(ами).
Другой особенностью изобретения является процесс выявления ВГС-последовательности в аналит-цепи, имеющей, как полагают, ВГС-полинуклеотид, в которой указанный ВГС-полинуклеотид содержит взятую выборочно область-мишень, содержащий:
а) этап формирования олигомера(ов), способного гибридизировать ВГС-последовательность в аналит-полинуклеотидной цепи, в которой указанный олигомер содержит полинуклеотидную последовательность, взятую выборочно из группы олигонуклеотидов, комплементарных следующим районам ВГС-генома (как показано на фиг. 1): 16-45, 49-78, 82-111, 115-144, 148-177, 211-240, 242-271, 275-304, 332-361, 365-394, 398-427 и 457-486,
b) этап инкубации аналит-цепи с олигомером(ами) в (а), дающий возможность сформировать специфические гибридные дуплексы между последовательностью предполагаемой области--мишени и последовательностью выбранной области-мишени, и
d) этап детекции гибридов, сформированных между областью-мишенью, если таковая имеется, и указанным олигомером(ами), с другим олигомером(ами), в котором другой олигомер(ы) содержит полинуклеотидную последовательность, взятую выборочно из группы олигонуклеотидов, комплементарных следующим районам ВГС-генома (как показано на фиг.1): 16-45, 49-78, 82-111, 115-144, 148-177, 211-240, 242-271, 275-304, 332-361, 365-394, 398-427 и 457-486.
Следующей особенностью изобретения является способ приготовления крови, не инфицированной ВГС, содержащий:
а) этап получения аналит-нуклеиновых кислот из пробы крови, содержащей, как полагают, область-мишень ВГС-последовательности;
b) этап формирования олигомера(ов), способного гибридизировать ВГС-последовательность в аналит-полинуклеотидной цепи, в которой указанный олигомер содержит полинуклеотидную последовательность, взятую выборочно из группы олигонуклеотидов, комплементарных следующим районам ВГС-генома (как показано на фиг. 1): 16-45, 49-78, 82-111, 115-144, 148-177, 211-240, 242-271, 275-304, 332-361, 365-394, 398-427 и 457-486,
с) этап проведения реакции (а) с (b) в условиях, при которых возможно формирование полинуклеотидного дуплекса между последовательностями предполагаемой области-мишени и выбранной области-мишени, если таковые имеются,
d) этап детекции дуплекса, сформированного в (с), если таковой имеется, и
е) этап сохранения крови, препараты комплексного действия которой не были детектированы в (d).
Очередной особенностью изобретения является способ приготовления крови, не инфицированной ВГС, содержащий:
a) этап получения аналит-нуклеиновых кислот из пробы крови, содержащей, как полагают, область-мишень ВГС-последовательности,
b) этап формирования олигомера(ов), способного гибридизировать ВГС-последовательность в аналит-полинуклеотидной цепи, если таковая имеется, в которой указанный олигомер содержит полинуклеотидную последовательность,
c) этап проведения реакции (а) с (b) в условиях, при которых возможно формирование полинуклеотидного дуплекса между последовательностями предполагаемой области-мишени и выбранной области-мишени, если таковые имеются,
d) этап детекции дуплекса, сформированного в (с), если таковой имеется, с другим олигомером(ами), в котором другой олигомер(ы) содержит полинуклеотидную последовательность, и
е) этап сохранения крови, препараты комплексного действия которой не были детектированы в (d).
На фиг.1 показана составленная сДНК-последовательность ВГС от описанного в данной заявке клона и от составленной сДНК-последовательности, описанной в РCТ/ W 090/14436. Клоны, от которых получена указанная последовательность, представлены в следующем виде: 5'-клон 32, b 114а, 18g, аg 30g, СА205а, СА290а, СА216а, рi 14а, СА167b, СА156е, СА84а, СА59а, К9-1 (также назыв. к9-1), 26j, 13i, 12j, 14i, 11b, 7j, 7е, 8h, 33с, 40b, 37b, 35, 36, 81, 32, 33b, 25с, 14с, 8f, 33f, 33g, 39с, 35f, 19g, 26g, 15е, b5а, 16jh, 6к и р131jh. На фиг. показаны три горизонтальных штриха над последовательностью, обозначающих предполагаемую позицию инициатора метионина кодона. На фиг. показана кроме того аминокислотная последовательность предполагаемого полипротеина, закодированного в сДНК ВГС. Гетерогенности в клонированных ДНК-цепях ВГС1 обозначены аминокислотами над предполагаемой закодированной последовательностью протяженной открытой рамкой считывания (ОРС). Наличие скобок указывает на то, что гетерогенность детектировалась около или в 5'-конце или 3'-конце сДНК ВГС в клоне.
На фиг.2 показаны консенсусные последовательности для пяти различных ВГС изолятов из различных географических районов (Япония и США), где аминокислоты, кодируемые протяженной ОРС ВГС1, обозначены над ДНК-последовательностями.
На фиг. 3 показаны последовательности маркированных зондов для детекции РНК ВГС в биологических средах, примененных в примере 3.
На фиг. 4 показано выравнивание зондов на фиг.3 с ВГС1 в соответствии с нумерацией фиг.1.
Способы осуществления изобретения
Термин "вирус гепатита С" (ВГС) использовался специалистами в данной области в качестве резервного для до сих пор неизвестного этиологического агента ГНАНВ. Изолят-прототип ВГС идентифицирован в пат. заявке США 122714 (см. также европ. пат. публ. ЕРО 318216). Кроме того, термин ВГС включает новые изоляты тех же самых вирусных видов. С целью расширения значения данного термина болезнь, инфицированная ВГС и обозначавшаяся прежде как "сывороточный" гепатит ни-А, ни-В, называется гепатит С. В данной заявке термины ГНАНВ и гепатит С понимаются как равнозначные.
ВГС - вид вируса, патогенные штаммы которого вызывают сывороточный ГНАНВ. Кроме того, могут иметь место ослабленные штаммы или полученные от них дефектные интерференционные частицы. Как показано ниже, геном ВГС состоит из РНК. Известно, что РНК-содержащие вирусы имеют относительно высокие величины спонтанной мутации, т.е., как полагают, порядка 10-3-10-4 на инкорпорированный нуклеотид (Филдс и Кнайп, 1986). Следовательно, поскольку РНК-вирусам свойственны гетерогенность и флуидность, имеют место сложноструктурные штаммы/изоляты, которые в пределах ВГС-вида могут быть вирулентными или авирулентными. Композиции и способы, описанные в данной заявке, обеспечивают возможность распространения, идентификации, детекции и выявления различных штаммов и изолятов ВГС.
Идентифицирован ряд различных штаммов/изолятов (см. РСТ/ W 090/14436), относящихся к ВГС. Один из таких штаммов или изолятов получил наименование CDC/HCVI (также назыв. HCVI ). Информация, полученная от одного штамма или изолята, например, о частичной геномной последовательности, вполне достаточна, чтобы дать возможность специалистам в данной области, используя стандартные методы и приемы, выделить новые штаммы/изоляты и определить являются ли эти новые штаммы/изоляты вирусами гепатита С. Так, например, ниже описывается ряд различных штаммов/изолятов. Эти штаммы, полученные от ряда сывороток человека (притом из разных географических регионов), были выявлены за счет информации, полученной от геномной последовательности ВГС1.
Используя методику, описанную в РCТ/ W 090/14436, были сделаны выводы о геномной структуре и нуклеотидной последовательности РНК-генома ВГС1. Геном, по-видимому, представляет собой одноцепочечную РНК приблизительно из 10000 нуклеотидов. Геном имеет позитивную структуру цепи, непрерывную трансляционную открытую рамку считывания (ОРС), которая кодирует полипротеин до 3000 аминокислот. В ОРС структурный протеин(ы), по-видимому, кодируется приблизительно в первой четверти N-конца участка, с большинством полупротеинов, ответственных за неструктурные протеины. При сравнении со всеми известными вирусными последовательностями наблюдаются небольшие, но важные колинейные гомологии, имеющие неструктурные протеины семейства флавивирусов и пестивирусов (которые в настоящее время также рассматриваются как часть семейства флавивирусов).
Полипротеин флавивируса имеет на участке от амино-конца до карбокси-конца нуклеокапсид протеин (С), матричный протеин (М), протеин оболочки (Е) и неструктурные протеины (NS) 1,2 (а + b ), 3,4 (а+b) и 5. Основываясь на предполагаемых аминокислотах, закодированных в нуклеотидной последовательности ВГС1, в самом конце N-участка полипротеина ВГС появляется небольшой домен, схожий как по размерам, так и по высокому содержанию основных остатков с нуклеокапсид протеином (С), находящимся в конце N-участка флавивирусных полипротеинов. Неструктурные протеины 2,3,4 и 5 (NS 2-5) ВГС и вируса желтой лихорадки (ВЖЛ), по-видимому, имеют аналоги, схожие по размерам и типу гидроманипуляции, хотя имеет место дивергенция аминокислотных последовательностей. Однако регион ВГС, который обычно соответствует регионам ВЖЛ-протеинов, содержащих протеины М, Е и NSI, не только отличается по сиквенсу, но, по-видимому, сильно различим и по размерам, и по гидроманипуляциям. Поэтому, хотя здесь и называются определенные геномные ВГС-домены, такие, например, как NSI или NS 2, следует учитывать, что эти обозначения следует рассматривать как гипотетические; между семейством ВГС и флавивирусами могут быть значительные различия, степень которых еще предстоит выяснить.
Можно предполагать, что в сравнении с ВГС1 различные штаммы, изоляты и подвиды ВГС представляют разновидности аминокислоты и нуклеиновых кислот. Можно также ожидать, что многие изоляты в сравнении с ВГС1 будут показывать большую часть (т.е. свыше 40%) гомологии в общей аминокислотной последовательности. Однако, может быть также показано, что могут иметь место другие, менее гомологичные ВГС-изоляты. Их можно было бы отнести к ВГС-изолятам, исходя из разных критериев, таких как, например, наличие ОРС в пределах приблизительно от 9000 нуклеотидов до приблизительно 12000 нуклеотидов, кодирование полипротеина, схожего по своим размерам с полипротеином ВГС1, закодированный полипротеин с гидрофобными и/или антигенными признаками, подобными признакам полипротеинов ВГС1, и наличие консервированных в ВГС1 колинейных пептидных последовательностей. Кроме того, предполагается, что геном имеет позитивно-цепочечную РНК.
Все ВГС-изоляты кодируют по меньшей мере один эпитоп, который иммунологически поддается идентификации (т.е. иммунологически кросс-реактивен) эпитопа, закодированного в сДНК ВГС, описанными в данной заявке. Эпитоп предпочтительно содержится в аминокислотной последовательности, описанной в данной заявке, и является уникальным по отношению к ВГС, если его сравнивать с ранее известными патогенами. Уникальность эпитопа может быть установлена по его иммунологической реактивности с анти-ВГС антителами, а также по отсутствию иммунологической реактивности с антителами в сравнении с известными патогенами.
Штаммы и изоляты ВГС эволюционно связаны друг с другом. Поэтому можно предполагать, что суммарная гомология геномов на уровне нуклеотида может составлять до 40% или более, с вероятностью до 50% или более, с вероятностью до 60% или более, и даже с большей вероятностью до 80% или более, и кроме того, можно ожидать, что будут иметь место соответствующие соприкасающиеся последовательности с по меньшей мере до 13 нуклеотидов. Следует отметить, что в пределах ВГС-генома имеются переменные и гиперпеременные районы, поэтому можно ожидать, что гомология этих районов будет значительно меньшей, чем гемология генома в целом. С помощью известных методик может быть установлена связь между геномной последовательностью предполагаемого штамма ВГС и, например, CDС /сДНК ВГС1-последовательностью. Эти связи могут, например, быть установлены путем непосредственного сравнения информации о последовательности полинуклеотида от предполагаемого ВГС и описанной в данной заявке информации о сДНК-последователъности ВГС. Кроме того, они могут определяться гибридизацией полинуклеотидов в условиях, при которых формируются устойчивые дуплексы между гомологичными районами (например, те, которые обычно используются до S1 ферментации), за которой следует ферментация путем воздействия однониточной специфичной нуклеазы, после чего определяются размеры фрагментов-стимуляторов.
Вследствие эволюционной зависимости штаммов или изолятов ВГС предполагаемые штаммы или изоляты идентифицируются за счет их гомологии на уровне полипептидов. ВГС-штаммы/изоляты предположительно будут гомологичными по меньшей мере на 40%, гомологичными более чем на 50%, гомологичными с вероятностью более чем на 70% и гомологичными даже с большей вероятностью более чем на 80%, а некоторые могут быть гомологичными более чем на 90% на полипептидном уровне. Известна методика определения гомологии аминокислотной последовательности. Например, аминокислотная последовательность может определяться непосредственно, а затем сравниваться с последовательностями, представленными в данной заявке. С другой стороны, возможно определение нуклеотидной последовательности геномного материала предполагаемого ВГС (обычно через сДНК-посредника), определение закодированной в данной заявке предполагаемой аминокислотной последовательности и сравнение соответствующих районов.
Выражение "полинуклеотид "производный от" указанной последовательности, употребляемое в данной заявке, относится к полинуклеотидной последовательности, которая состоит из последовательно расположенных по меньшей мере приблизительно 6 нуклеотидов, предпочтительно по меньшей мере около 8 нуклеотидов, более предпочтительно по меньшей мере около 10-12 нуклеотидов и даже более предпочтительно по меньшей мере 15-20 нуклеотидов, соответствующих указанной области нуклеотидной последовательности. Термин "соответствующий" означает гомологичный или комплементарный указанной последовательности. Предпочтительно, последовательность района, из которого взят дериват полинуклеотида, является гомологичной или комплементарной последовательности, которая является уникальной ВГС-геному. Более предпочтительно, производная последовательность является гомологичной или комплементарной последовательности, которая является уникальной всем или большей части ВГС-изолятов. Вопрос о том, является ли последовательность уникальной для ВГС-генома, определяется методикой, известной специалистам данной области. Например, последовательность может сравниваться с последовательностями, выбранными из банков данных, например из банка Genebank, с тем, чтобы определить присутствует ли она у неинфицированного хозяина или в других организмах. Кроме того, последовательность может сравниваться с известными последовательностями других вирусных агентов, в том числе тех, которые известны как агенты, индуцирующие гепатит, например, ВГА, ВГВ и ВГД, а также с представителями флавивирусов. Кроме того, вопрос соответствия или несоответствия производной последовательности другим последовательностям может быть решен с помощью гибридизации, проводимой с соблюдением необходимых условий. Известны методика и порядок проведения гибридизации с целью определения комплементарности нуклеиновокислотных последовательностей (см. например, Маниатис и соавт., 1982). Методика гибридизации рассматривается ниже в данной заявке. Кроме того, мисматчи дуплексных полинуклеотидов, сформированных с помощью гибридизации, могут быть определены известными методами, такими как, например, ферментация нуклеазой, например, S1, которая специфично стимулирует одноцепочечные районы дуплексных полинуклеотидов. Районы, из которых могут быть выделены типовые ДНК-последовательности, включают, но не ограничиваются ими, например, районы, кодирующие специфичные эпитопы, а также нетранскрибированные и/или нетранслированные районы.
Выделенный полинуклеотид не обязательно физически выделен из показанной нуклеотидной последовательности, он может генерироваться любым способом, таким, например, как химический синтез или ДНК-репликация или обратная транскрипция или транскрипция. Кроме того, комбинации районов, соответствующих комбинациям указанной последовательности, могут модифицироваться известными способами, согласующимися с предполагаемым использованием.
Под термином "рекомбинантный полинуклеотид", употребляемым в данном контексте, понимается полинуклеотид, имеющий геномное, сДНК, полусинтетическое или синтетическое происхождение, который в силу своего происхождения или манипуляции: 1) не ассоциируется полностью или частично с тем полинуклеотидом, с которым он ассоциируется в природе, 2) связан с полинуклеотидом, кроме того полинуклеотида, с которым он связан в природе, или 3) не встречается в природе.
Термин "полинуклеотид", употребляемый в данном контексте, относится к полимерной форме нуклеотидов любой длины, как рибонуклеотидов, так и дезоксирибонуклеотидов. Этот термин относится только к основной молекулярной структуре. Следовательно, этот термин включает как двухцепочечные, так и одноцепочечные ДНК и РНК. Кроме того, он включает известные виды модификаций, например, известные маркеры, метилирование, "шапки", замена аналогом одного или более встречающихся в природе нуклеотидов, межнуклеотидные модификации, такие, например, как модификации с нейтральными соединениями (напр. метилфосфанаты, фосфотриэфиры, фосфо-амидаты, карбаматы и др.), и с заряженными соединениями (напр. фосфоротиоаты, фосфородитиааты и др.), модификации с боковой составляющей пени, такие как, например, белки (в том числе, например, нуклеазы, токсины, антитела, сигнальные пептиды, поли-L-лизины и др.), интеркалятор-содержащие модификации (напр. акридин, псорален и др.), хелатор-содержащие модификации (напр. металлы, радиоактивные металлы, борон, окислительные металлы и др.), алкилятор-содержащие модификации, модификации с модифицированными соединениями (напр. альфа аномерные нуклеиновые кислоты и др.), а также немодифицированные формы полинуклеотида.
Под термином "чувствительная цепь" нуклеиновой кислоты, употребляемым в данном контексте, понимается, что цепь содержит последовательность, имеющую гомологию сиквенса, относящуюся к мРНК-гомологии. Термин "античувствительная цепь" предполагает цепь, содержащую последовательность, комплементарную последовательности "чувствительной цепи".
Термин "позитивно-цепочечный геном" вируса, употребляемый в данном контексте, подразумевает полинуклеотид РНК- или ДНК-генома, который кодирует по меньшей мере один вирусный полипептид. Примерами позитивно-цепочечных РНК-вирусов являются тогавирусы, коронавирусы, ретровирусы, пикорнавирусы и калицивирусы. В эту группу включены также флавивирусы, которые прежде относились к тогавирусам. Эти вирусы обычно одноцепочечные (см. Филдс и Кнайп, 1986).
Термин "праймер", употребляемый в данном контексте, относится к олигомеру, который в соответствующих условиях способен взять на себя функцию инициатора синтеза полинуклеотидной цепи. Праймер будет полностью или в значительной мере комплементарным району полинуклеотидной цепи, подлежащей копированию. Следовательно, в условиях, благоприятных для гибридизации, праймер ренатурирует комплементарный район аналит-цепи. При добавлении соответствующих реагирующих веществ (напр. полимеразы, нуклеотидных трифосфатов и им подобных) праймер удлиняется с помощью полимеризационного агента и формирует копию аналит-цепи. Праймер может быть однониточным или наоборот частично или полностью двухниточным.
Термины "аналит-полинуклеотид" и "аналит-цепь" относятся к одно- и двухцепочечной молекуле нуклеиновой кислоты, которая, как полагают, содержит последовательность с избранной областью-мишенью и которая может присутствовать в биологической среде.
Термин "олигомер", применяемый в данном контексте, относится к праймерам и зондам. Термин "олигомер" не заключает в себе величину молекулы. Тем не менее, по длине обычные олигомеры не превышают 1000 нуклеотидов, более типичные из них не превышают 500 нуклеотидов, к еще более типичным из них относятся те, которые не превышают даже 250 нуклеотидов, они могут не превышать 100 нуклеотидов, 75 нуклеотидов, а также 50 нуклеотидов.
Термин "зонд", применяемый в данном контексте, относится к структуре, содержащей полинуклеотид, который образует гибридную структуру последовательности с выбранной областью-мишенью, вследствие комплементарности по меньшей мере одного сиквенса в зонде сиквенсу в области-мишени. Полинуклеотидные регионы зондов могут быть ДНК-содержащие, и/или РНК-содержа-щие, и/или содержащие аналоги синтетических нуклеотидов. В пределах зондов имеются т.н. "зонды поглощения" и "зонды"-маркеры". Предпочтительно зонд не содержит последовательность, комплементарную последовательности(ям), используемой для инициации полимеразной цепной реакции (ПЦР).
Термин "область-мишень", применяемый в данном контексте, относится к региону нуклеиновой кислоты, который подлежит амплификации и/или детекции. Термин "последовательность области-мишени" относится к последовательности, с которой зонд или праймер образуют при соответствующих условиях стабильный гибрид.
Термин "зонд поглощения", применяемый в данном контексте, относится к полинуклеотиду, состоящему из одноцепочечного полинуклеотида, соединенного со связующим партнером. Одноцепочечный полинуклеотид содержит полинуклеотидную последовательность предполагаемой области-мишени, которая комплементарна последовательности выбранной области-мишени, подлежащей детекции в аналит-полинуклеотиде. Этот комплементарный регион имеет достаточную длину и комплементарность к сиквенсу области-мишени для обеспечения дуплекса стабильности, достаточного для иммобилизации аналита-полинуклеотида в твердой поверхности (через связывающих партнеров). Связующий партнер специфичен для второго связующего партнера, второй связующий партнер может быть прикреплен к поверхности твердой подложки или может быть косвенно, через другие структуры или связующих партнеров, соединен с твердой подложкой.
Термин "полинуклеотидная последовательность предполагаемой области-мишени", применяемый в данном контексте, относится к полинуклеотидной последовательности, которая содержит нуклеотиды, комплементарные нуклеотидной последовательности выбранной области-мишени, последовательность имеет достаточную длину и комплементарность к сиквенсу области-мишени для образования дуплекса, имеющего достаточную стабильность для осуществления поставленной цели.
Термин "связующий партнер", применяемый в данном контексте, относится к молекуле, способной связывать лиганд-молекулу с высокой степенью специфичности как, например, специфичные антиген и антитело. Специфичные связующие партнеры обычно должны связывать с достаточной степенью сродства для иммобилизации аналит-копии/ комплементарного ниточного дуплекса (в случаях, касающихся зондов поглощения) в условиях изоляции. Известны специфичные связующие партнеры, такие, например, как биотин и авидин или стрептавидин, аллотип IgGu протеин А, многочисленные известные рецепторно-лигандные пары и комплементарные полинуклеотидные цепи. В случае, касающемся комплементарных полинуклеотидных связующих партнеров, такие партнеры обычно имеют по меньшей мере до 15 оснований в длину и могут достигать по меньшей мере 40 оснований в длину. Кроме того, содержание G- и С-остатков у них по меньшей мере около 40% и вплоть до 60%. В состав полинуклеотидов могут входить ДНК, РНК или синтетические нуклеотидные аналоги.
Термин "связанный", применяемый в данном контексте, относится к фиксациям или сцеплениям, производимым с помощью ковалентных связей или сильных нековалентных взаимосвязей (напр. гидрофобные взаимодействия, водородные связи и др. ). К ковалентным связям могут, например, относиться сложные и простые эфиры, сложный фосфоэфир, амид, пептид, имид, углеродно-серные связи и подобные им.
Термин "подложка" относится к любой твердой или полутвердой поверхности, к которой может крепиться требуемый связующий партнер. Соответствующими подложками являются стекло, пластмасса, металл, полимерный гель и подобные им материалы, они могут иметь форму гранул, резервуаров, щупов, мембран и др.
Термин "маркер", применяемый в данном контексте, относится к любому атому или составляющей части, которые могут быть использованы для обеспечения диагностического (предпочтительно поддающегося количественному определению) сигнала, и которые могут крепиться к полинуклеотиду или полипептиду.
Термин "маркерный (меченый) зонд", применяемый в данном контексте, относится к олигомеру, который содержит полинуклеотидную последовательность предполагаемой области-мишени, комплементарную сиквенсу выбранной области-мишени, подлежащему детекции в аналитполинуклеотиде. Этот комплементарный регион имеет достаточную длину и комплементарность к сиквенсу выбранной области-мишени для того, чтобы дать возможность маркеру сдетектировать дуплекс, состоящий из "меченого зонда", и "последовательности выбранной области-мишени". Олигомер связывается с маркером как непосредственно, так и косвенно, через совокупность лиганд-молекул с высокой специфичностью друг к другу. Совокупности лиганд-молекул описаны выше, они также содержат мультимеры.
Термин "мультимер", применяемый в данном контексте, относится к линейным или разветвленным полимерам одной и той же повторяющейся одноцепочечной полинуклеотидной единицы или различным одноцепочечным полинуклеотидным единицам. По меньшей мере одна из единиц имеет сиквенс, длину и композицию, что позволяет ей осуществить целенаправленную гибридизацию представляющей интерес первой одноцепочечной нуклеотидной последовательности, обычно аналит или олигомер (напр. маркерный зонд), связанный с аналитом. Для достижения такой специфичности и стабильности эта единица должна иметь длину по меньшей мере до 15 нуклеотидов, обычно не более чем около 50 нуклеотидов в длину, и предпочтительно иметь длину до 30 нуклеотидов, более того, содержание G- и С-остатков обычно должно быть по меньшей мере около 40% и самое большее около 60%. Кроме указанной единицы(единиц) мультимер включает разнообразие единиц, способных к целенаправленной и стабильной гибридизации второго одноцепочечного нуклеотида, представляющего интерес, обычно меченого полинуклеотида или другого мультимера. Эти единицы обычно имеют примерно такие же размерения и композицию как и мультимеры, о которых говорилось выше. Когда мультимер подлежит гибридизации другим мулътиме-ром, первая и вторая олигонуклеотидные единицы становятся гетерогенными (разнородными) и друг с другом не гибридизуются в условиях выбранного теста. Таким образом, мультимеры могут быть либо мечеными зондами, либо лигандами, которые связывают маркер с зондом.
Термин "вирусная РНК", который включает ВГС РНК, относится к РНК вирусного генома, его фрагментов, транскриптов и мутантных сиквенсов, выделенных из него.
Термин "биологический образец" относится к пробам ткани или жидкости, взятым у индивидуума, включая, но не ограничиваясь ими, например, плазму, сыворотку, цереброспинальную жидкость, лимфатическую жидкость, наружные отсеченные участки кожи, дыхательные пути, кишечник, мочеполовые пути, слезы, слюну, молоко, клетки крови, опухоли, органы, а также образцы ингредиентов клеточных культур в условиях in vitro (включая, но не ограничиваясь условной средой, явившейся результатом роста клеток в среде клеточной культуры, клетки мнимоинфицированные вирусом, рекомбинантные клетки и компоненты клеток).
В практике настоящего изобретения используются, за исключением особо оговоренных случаев, обычные методы и приемы химии, молекулярной биологии, микробиологии, рекомбинантной ДНК, иммунологии, хорошо известные специалистам в данной области. Эти методы и приемы подробно исследованы в научной литературе. См. , например, кн. "Молекулярное клонирование. Руководство по лабораторным работам", авт. Маниатис, Фитш и Сэмбрук, 1982, кн. "ДНК-клонирование", тт. 1, 2, изд. Д.Н. Гловер, 1985, кн. "Синтез олигонуклеотидов", изд. М.Д. Гайт, 1984, кн. "Гибридизация нуклеиновых кислот", изд. Б.Д. Хеймс и С. Д. Хиггинс, 1984, статьи "Методы энзимологии", вып.154, 155, изд. By и Гроссман, Академик Пресс Инк. В настоящем описании даются ссылки на все патенты, пат. заявки и публикации, упоминаемые выше и ниже в тексте.
Применение на практике материалов и процессов, описанных в настоящем изобретении, становится возможным в связи с идентификацией ВГС как этиологического агента "сывороточного" ВГНАНВ и формированием семейства нуклеотидных последовательностей, выделенных из библиотек кДНК, содержащих кДНК-сиквенсы ВГС. Эти библиотеки кДНК были получены из нуклеиновокислотных последовательностей плазмы шимпанзе, инфицированных ВГС. Конструкция одной из таких библиотек, а именно библиотеки "с" (амер. фонд культур (АТСС) 40394) описана в РСТ/ W 090/14436.
Применение описанных выше кДНК-последовательностей ВГС, а также последовательностей, описанных в настоящем изобретении, дает возможность конструировать олигомеры для практического использования в качестве реагентов при детекции вирусных полинуклеотидов в биологических средах. Так, например, используя последовательности, можно синтезировать ДНК-олигомеры из 8-10 или большего количества нуклеотидов, которые можно использовать в качестве зондов гибридизации для детекции присутствия РНК ВГС, например, в донорской крови, фракциях крови, сыворотке трупов при вскрытии с подозрением на носителей вируса, или в системах клеточных культур, в которых реплицируется вирус. Кроме того, новые олигомеры, предложенные в данной заявке, позволяют продолжить изучение свойств ВГС-генома. Полинуклеотидные зонды и праймеры, выделенные из этих последовательностей, могут быть использованы для амплификации последовательностей, находящихся в фондах библиотек кДНК, и/или для скрининга библиотек сДНК с целью дополнительного наложения сДНК-последовательностей, которые, в свою очередь, могут использоваться для получения большего числа наложенных последовательностей. Как указывается в РCТ/ W 090/14436, геном ВГС, по-видимому, является РНК, содержащий главным образом протяженную открытую рамку считывания (ОРС), которая кодирует крупный полипротеин.
В дополнение к вышесказанному ниже приводится информация, которая позволит идентифицировать дополнительные штаммы и изоляты ВГС. Выделение и охарактеризование дополнительных штаммов и изолятов ВГС может быть осуществлено, например, выделением нуклеиновых кислот из компонентов организма, которые содержат вирусные частицы и/или РНК-вирусы, созданием библиотек кДНК, использующих олигомеры, основанные на последовательности ВГС1 для скрининга в библиотеках клонов, содержащих сДНК-последовательности ВГС, описанные ниже, и сравнением кДНК ВГС от новых изолятов с кДНК, описанными в РСТ/ W 0090/14436 и ниже в данном описании. Штаммы и изоляты, которые соответствуют параметрам ВГС, описанным в разделе данного описания, раскрывающем значения терминов и выражений (см. выше), легко идентифицируются. Другие способы идентификации штаммов ВГС будут очевидны специалистам в данной области с учетом информации, представленной в данном описании.
Выделение кДНК-последовательностей ВГС
Олигомеры, описанные в изобретении, содержат регионы, которые формируют структуры гибридных дуплексов с последовательностями областей-мишеней в ВГС-полинуклеотидах. ВГС-полинуклеотидные гибридизационные районы олигомеров могут быть установлены из сДНК-последовательностей ВГС, описанных как в данном описании, так и в РCТ/ W 090/14436. На фиг.1 показан композиционный материал сДНК ВГС от ВГС1, прототипный ВГС. Композиционная последовательность базируется на информации по секвенированию, полученной от ряда кДНК-клонов ВГС, которые были выделены из ряда библиотек сДНК ВГС, в том числе из библиотеки "с" амер.колл. культур (АТСС) 40394, ламбда gt II (λ gt II) и из сыворотки крови человека. Клоны кДНК ВГС были выделены способами, описанными в PCT/W 090/14436. Если изложить существо вопроса кратко, большинство выделенных клонов содержали последовательности из библиотеки "с" кДНК ВГС, которая была построена с использованием смешанной сыворотки от шимпанзе, инфицированных хроническим ВГС, и содержащих высокий титр вируса, т.е. по меньшей мере 106 инфекционных доз/мл, взятых у шимпанзе (СID/ml). Смешанная сыворотка использовалась для выделения вирусных частиц. Выделенные из этих частиц нуклеиновые кислоты использовались в качестве кодирующей нити ДНК для построения библиотек сДНК в геноме вируса. Стартовый клон, 5-1-1, был получен путем скрининга библиотеки "с" сывороткой от зараженных индивидуумов. После выделения стартового клона оставшаяся часть сиквенса была получена путем скрининга синтетическими полинуклеотидными зондами, последовательности которых были получены из 5' -участка и 3' -участка известной сДНК-последовательности ВГС.
Описание способов восстановления сДНК-последовательностей в основном представляет интерес в историческом плане. Последовательности, полученные в результате этих способов, описаны в данной заявке также как и их комплементы, а последовательности или любая их часть может быть подготовлена с использованием синтетических методов или сочетанием синтетических методов с извлечением частичных последовательностей с применением способов, подобных описанным в РСТ/W 090/14436.
Олигомерные зонды и праймеры
Используя ВГС-геном как основу (как показано на фиг.1) и/или предпочтительно неиспользуемые (консервативные) регионы ВГС-генома, можно подготовить олигомеры, состоящие приблизительно из 8 нуклеотидов или более, которые гибридизуют с позитивной нитью(ями) РНК ВГС или ее комплементом, а также с кДНК ВГС. Эти олигомеры могут служить в качестве зондов для детекции (включая выделение и/или маркировку) полинуклеотидов, содержащих нуклеотидные ВГС сиквенсы, и/или в качестве праймеров для транскрипции и/или репликации ВГС последовательностей с выбранными областями-мишенями. Олигомеры содержат полинуклеотидный сиквенс с предполагаемой областью-мишенью, состоящий из нуклеотидов, комплементарных нуклеотидному сиквенсу ВГС с выбранной областью-мишенью, последовательность имеет достаточную длину и комплементарность ВГС сиквенсу для формирования дуплекса, имеющего достаточную стабильность для реализации поставленной цели. Например, если целью является выделение путем иммобилизации аналита, содержащего ВГС сиквенс с выбранной целью-мишенью, олигомеры должны содержать полинуклеотидный регион, имеющий достаточную длину и комплементарность ВГС сиквенсу с выбранной областью-мишенью для обеспечения достаточной дуплексной стабильности с целью иммобилизации аналита на твердой подложке путем его связывания с олигомерами в условиях изоляции. Кроме того, например, если олигомеры должны служить в качестве праймеров для транскрипции и/или репликации ВГС-последовательностей с выбранной областью-мишенью в аналите-полинуклеотиде, олигомеры должны содержать полинуклеотидный регион, имеющий достаточную длину и комплементарность ВГС-сиквенсу с выбранной областью-мишенью, чтобы дать возможность полимеризирующему агенту продолжить репликацию из числа праймеров, находящихся в стабильной дуплексной форме с сиквенсом с выбранной областью-мишенью в условиях полимеризации. Кроме того, например, если олигомеры должны использоваться в качестве меченых зондов или должны быть связаны с мультимерами, полинуклеотидный регион с предполагаемой областью-мишенью должен иметь достаточную длину и комплементарность для формирования стабильных гибридных дуплексных структур с мечеными зондами и/или мультимерами, чтобы дать возможность провести детекцию дуплекса. Олигомеры могут содержать минимум до 4 смежных нуклеотидов, комплементарных ВГС-сиквенсу с выбранной областью-мишенью, обычно олигомеры будут содержать минимум до 8 смежных нуклеотидов, комплементарных ВГС-сиквенсу с выбранной областью-мишенью, а предпочтительно будут содержать минимум до 14 смежных нуклеотидов, комплементарных ВГС-сиквенсу с выбранной областью-мишенью.
Соответствующие нуклеотидные ВГС-сиквенсы с предполагаемой областью-мишенью могут состоять из нуклеотидов, комплементарных нуклеотидам, выбранным из числа сДНК-нуклеотидов ETC, показанных на фиг.1.
Олигомер не должен, однако, состоять только из последовательности, которая комплементарна ВГС-сиквенсу с выбранной областью-мишенью. Он может дополнительно иметь нуклеотидные последовательности или другие составляющие части, соответствующие тем целям, ради которых олигомеры используются. Например, если олигомеры используются в качестве праймеров для амплификации ВГС-сиквенсов путем полимеразной цепной реакции, они могут содержать последовательности, которые, если они имеют дуплексную форму, образуют ферментоограничительные сайты, способствующие клонированию амплифицированных последовательностей. Например, если олигомеры должны также использоваться в качестве "зондов поглощения" при проведении гибридизационных анализов, (описанных ниже), они должны содержать дополнительно связующего партнера, связанного с олигомером, содержащим нуклеотидную последовательность, комплементарную ВГС-сиквенсу с выбранной областью-мишенью. К другим видам составляющих частей или последовательностей, полезных тем, что из них могут составляться или к ним присоединяться олигомеры, относятся те, которые известны как соответствующие различным целям, такой, например, как маркировка нуклеотидных зондов.
Подготовка олигомеров осуществляется известными способами, например, такими как эксцизия, транскрипция или химический синтез. Отбор последовательностей с выбранной областью-мишенью и/или регионов генома, к которым комплементарны полинуклеотиды с предполагаемой областью-мишенью олигомеров, зависят от поставленной цели. Например, если целью является проведение скрининга для выяснения присутствия ВГС в биологических средах (напр. крови), олигомеры предпочтительно должны использоваться в качестве зондов и/или праймеров и осуществлять гибридизацию в резервных (законсервированных) районах ВГС-генома. В данной заявке дано описание некоторых резервных районов ВГС-генома, с которыми олигомеры могут связываться, например районы, которые включают номера нуклеотидов примерно от 5-конца до примерно 200, или примерно от 4000 до примерно 5000, или примерно от 8000 до примерно 9040, как показано на фиг.1, или предпочтительно нуклеотиды от примерно -318 до примерно 174, от примерно 4056 до примерно 4448 и от примерно 4378 до примерно 4902. Особенно предпочтительными являются праймеры и зонды, полученные от нуклеотидов в пределах от примерно -313 до примерно -173 и от нуклеотидов в пределах от примерно 1 до примерно 540, как показано на фиг.1.
Другие резервные районы генома без труда устанавливаются сравнением нуклеотидных последовательностей различных ВГС-изолятов, в том числе ВГС1, как прототипа ВГС. Известны способы проведения сравнений между генотипами с целью определения законсервированных и незаконсервированных районов, примеры этих способов приведены в РСТ/W 090/14436.
При проведении основного гибридизационного анализа нуклеиновых кислот одноцепочечная аналит-нуклеиновая кислота (как ДНК, так и РНК) гибридизуется в зонд нуклеиновой кислоты, а полученные в результате этого дуплексы детектируются. Зонды для ВГС-полинуклеотидов (естественных или производных) представляют собой длину, которая позволяет путем гибридизации детектировать уникальные вирусные последовательности. Длина из 6-8 нуклеотидов может считаться рабочей длиной, последовательности из 10-12 нуклеотидов являются предпочтительными, а последовательности от примерно 20 нуклеотидов и более можно считать оптимальными. Предпочтительно, если эти последовательности будут выделены из регионов, в которых отсутствует гетерогенность. Эти зонды могут быть подготовлены с применением обычной методики, в том числе автоматизированных олигонуклеотидных синтетических методов. Среди зондов, имеющих практическое значение, имеются, например, зонды, полученные от вновь выделенных клонов, предложенных в данном изобретении, а также различные олигомеры, используемые при зондировании библиотек сДНК, рассматриваемые ниже в данном описании. Комплемент к любой уникальной части ВГС-генома будет удовлетворительным. Для использования в качестве зондов желательна полная комплементарность, хотя она может оказаться излишней, поскольку происходит увеличение длины фрагмента.
Для использования таких зондов в качестве агентов для детекции наличия ВГС-полинуклеотидов (например, при скрининге инфицированной крови), по желанию, может быть произведена обработка биологической среды, подлежащей анализу, например крови или сыворотки, для экстрагирования содержащихся в них нуклеиновых кислот. Выделенные из среды нуклеиновые кислоты
могут быть подвергнуты электрофорезу на геле или иному методу разделения величин, с другой стороны, среда нуклеиновой кислоты может быть исследована без разделения методом блотирования отпечатков. Для формирования гибридных дуплексов с учетом последовательности с предполагаемой областью-мишенью в зонде область-мишень аналит-аминокислоты должна иметь одноцепочечную форму. Там где последовательность представлена в естественной одноцепочечной форме, денатурации не потребуется. Однако, там где последовательность представлена в двухцепочечной форме, она подлежит денатурированию. Денатурация может производиться различными известными способами. После денатурации аналит-аминокислота и зонд инкубируются в условиях, способствующих стабильному гибридному образованию последовательности с выбранной областью-мишенью в зонде с мнимой последовательностью, предполагающей область-мишень в аналите, в результате чего происходит детекция дуплексов, содержащих зонд(ы).
Детекция результирующего дуплекса, если таковой имеется, обычно проводится с использованием меченых зондов, с другой стороны, зонд может не маркироваться, а выделяться путем связывания с лигандом, который маркируется как непосредственно, так и косвенно. Известны соответствующие маркеры и способы маркирования зондов, к ним относятся, например, радиоактивные маркеры, которые могут быть увязаны с известными способами (напр. ник-трансляция или киназо-синтез), биотин, флюоресцентные группы, хемолюминесцентные группы (напр. диоксетаны, инициированные диоксетаны), ферменты, антитела и им подобные.
Регион зондов, которые используются в качестве аналит-связывающих средств, может быть создан полностью комплементарным ВГС-геному. Поэтому все работы, связанные с приготовлением, требуют строгого соблюдения правил для предупреждения ложных позитивных результатов. Однако строгого соблюдения правил следует придерживаться только в случаях, когда зонды комплементарны районам вирусного генома с отсутствующей гетерогенностью. Строгость условий проведения гибридизации определяется рядом факторов, соблюдаемых во время гибридизации и промывки, таких как температура, концентрация ионов, продолжительность и концентрация формамида. Эти факторы приводятся, например, у Т. Маниатиса, 1982.
Возможно использование разновидностей этой известной общей схемы, в т.ч. разновидностей, способствующих отделению дуплексов, подлежащих детекции от посторонних материалов и/или разновидностей, амплифицирующих сигнал от меченой составляющей. Ряд этих разновидностей анализируется в работах, например, Мэттюз и Крика, журн. "Анал. Биохим.", 1988, вып.169, стр. 1, Ландегрен и соавт. , журн. "Сайенс",1988, вып.242, стр. 229, и Миттлин, журн. "Клин.Хим. ", 1989, вып.35, стр. 1819. В этих анализах зонды, подходящие для детекции ВГС, состоят из последовательностей, гибридизующих с полинуклеотидными ВГС-последовательностями с выбранными областями-мишенями для формирования дуплексов с аналит-цепью, в которой дуплексы имеют достаточную стабильность для детекции в системе специфичных анализов.
К одной из соответствующих разновидностей относится, например, разновидность, описанная в пат. США 4868105, 9.09.1989 и в европ.пат. Е.Р.О. 225807, 16.06.1987. В этих пат. публ. описывается техника проведения гибридизационного анализа нуклеиновой кислоты в фазе раствора, где аналит-нуклеиновая кислота гибридизуется к набору меченого зонда и набору зонда поглощения (захвата). Комплекс зонд-аналит связывается через гибридизацию с зондом захвата с твердой подложкой, комплементарным набору зонда захвата. Это позволяет удалить из раствора аналит-нуклеиновую кислоту как комплекс твердой фазы. Наличие аналита в виде комплекса твердой фазы способствует при анализе проведению последующих этапов разделения. Набор меченого зонда комплементарен меченому зонду, который связывается через гибридизацию с твердой фазой/ аналит-комплексом.
Обычно предполагают, что последовательности ВГС-генома будут находиться в сыворотке крови инфицированных индивидуумов на относительно низких уровнях, т.е. приблизительно на уровне 102-103 инфекц. доз шимпанзе/мл. Наличие такого уровня может вызвать необходимость использования в гибридизационных анализах метода амплификации. Такие методы известны. Например, "Био-Бридж систем" Энцо Биокемикэл Корпорейшн использует терминальную дезоксинуклеотидную трансферазу для добавления немодифицированных 3' -поли- d Т-"хвостов" к ДНК-зонду. Поли- d Т-"хвостовой" зонд гибридизуется к нуклеотидной последовательности с областью-мишенью, а затем к биотин-модификации поли-А. В PCT/W 084/03520 и ЕРО 124221 описывается техника проведения ДНК-гибридизационного анализа, в котором: 1) аналит ренатурируют в зонд однониточной ДНК, комплементарный олигонуклеотиду, меченому ферментом, и 2) результирующий "хвостовой" дуплекс гибридизуют к олигонуклеотиду, меченому ферментом. В ЕРО 204510 описывается ДНК-гибридизационный анализ, в котором ДНК-аналит контактирует с зондом, который имеет "хвост", например поли- d Т-"хвост", амплификационную нить, имеющую сиквенс, который гибридизуется к "хвосту" зонда, например поли-А-сиквенс, и который способен связать множество маркированных нитей. В ЕРО 317077, 24.05.1989, описывается вид гибридизационного анализа, в котором должны детектироваться сиквенсы на уровне приблизительно 106/мл, и который использует мультимеры нуклеиновой кислоты, связывающие однониточные аналиты нуклеиновой кислоты, а также связывающие множество однониточных меченых олигонуклеотидов. В случае особой необходимости может потребоваться амплификация ВГС-последовательности с областью-мишенью в сыворотках приблизительно 10000-кратном размере (т.е. приблизительно 106 сиквенсов/мл), проводимая в рамках системы гибридизации. Амплификацию можно проводить методом полимеразных цепных реакций (ПЦР), описанным Сайки и соавт., 1986, Муллис, в пат. США 4683195 и Муллис и соавт. в пат. США 4683202. Амплификация может проводиться до или, что предпочтительно, после очистки ВГС-последовательности с областью-мишенью. Например, амплификацию можно применять по методике анализов, описанных в пат. США 4868105, или в случае необходимости продолжения амплификации по системе гибридизации, описанной в ЕРО 317077.
Способы детекции ВГС последовательностей в аналит-полинуклеотидной цепи предпочтительно осуществлять с учетом способов гибридизационной детекции, описанных в пат. США 4868105 и пат. ЕРО 317077. Эти способы предполагают применение анализов сэндвич-гибридизации в фазе раствора, когда используются зонды поглощения (захвата) и маркированные зонды для гибридизации последовательностей с областью-мишенью в аналит-нуклеиновых кислотах. При проведении таких анализов с целью детекции ВГС путем скрининга биологических проб используемые зонды обычно связывают резервные районы ВГС-генома. Зонды поглощения и зонды-маркеры могут быть расположены с разрывами для связывания сиквенсов с областью-мишенью. Как предпочтительный вариант, предлагается использование зондов поглощения и зондов-маркеров в виде наборов, причем зонды одного из наборов не заполняют разрывы в зондах другого набора. В этом варианте, предпочтительно набор(ы) многих зондов поглощения гибридизуют к большинству резервных районов генома, а набор(ы) многих зондов-маркеров могут гибридизовать к районам, которые обнаруживают незначительное число дивергенции. Например, используя прототип ВГС1 сДНК-последовательности, показанной на фиг.1, можно было бы использовать зонды, которые гибридизируются с районами последовательности с нуклеотидами в пределах приблизительно от -318 до приблизительно 174, и/или с нуклеотидами в районе в пределах приблизительно от 4378 до приблизительно 4902, и/или с нуклеотидами в районе в пределах от 4056 до приблизительно 4448. Зонды предпочтительно гибридизовать с последовательностями в 5' -районе BTC-генома, поскольку этот район, как показано ниже, по-видимому, в значительной степени консервативен. Таким образом, предпочтительно зонды могут гибридизоваться, например, с нуклеотидами в пределах от приблизительно -318 до приблизительно 174, как показано на фиг. 1. Можно было бы использовать зонды, которые гибридизируются как к позитивной цепи в законсервированных районах, так и/или к ее комплементу в зависимости от поставленной цели, например для детекции вирусных геномных последовательностей или для детекции сДНК-последовательностей ВГС как результата ампликации полимеразной цепной реакции, или для детекции репликационных промежутков к позитивной РНК-цепи ВГС.
Детекция РНК ВГС и выделенных из нее полинуклеотидов, пользуясь способом ВГС/ПЦР (сРСR)
В вопросах методики детекции РНК ВГС или полинуклеотидов, выделенных из РНК ВГС, весьма полезным для практического применения представляется способ полимеразной цепной реакции ВГС (НСV//сРСR), который является предметом настоящей заявки и использует метод полимеразной цепной реакции (ПЦР), описанный Саики и соавт., 1986, Муллис в пат. США 4683195 и Муллис и соавт. в пат. США 4683202. Способ ВГС/сРСR использует праймеры и зонды, выделенные за счет представленной в данной заявке информации, касающейся природы ВГС-генома.
При полимеразной цепной реакции методика обычно предполагает подготовку коротких олигонуклеотидных праймеров, которые согласуются с противоположными концами требуемой последовательности. Последовательность между праймерами не должна быть известна. Образец полинуклеотида экстрагируется и подвергается денатурации, предпочтительно нагреванием, и гибридизуется с олигонуклеотидныии праймерами, которые имеются в молярном избытке. Полимеризация катализуется матрицезависимой и прайиерозависимой полимеразой в присутствии дезоксинуклеотидных трифосфатов или нуклеотидных аналогов (dNTPs). В результате появляются два "длинных продукта", содержащие соответствующие 5'-концевые праймеры, ковалентно соединенные с новыми синтезированными комплементами первоначальных цепей. Прошедшая репликацию ДНК вновь денатурируется нагреванием, гибридизуется с олигонуклеотидными праймерами, возвращается в состояние полимеризации, после чего инициируется второй цикл репликации. Во втором цикле появляются две первоначальные цепи, два длинных продукта из первого цикла, и два "коротких продукта", реплицированных от длинных продуктов. Короткие продукты содержат последовательности (чувственные или античувственные), выделенные из последовательности с областью-мишенью, фланкирующей 5' - и 3' -концы с праймерными последовательностями. На каждом дополнительном цикле число коротких продуктов экспоненциально реплицируется. Таким образом, этот процесс вызывает необходимость в амплификации специфичной последовательности с выбранной областью-мишенью.
В рассматриваемом способе представлен образец, содержащий, как полагают, РНК ВГС или ее фрагмент. Образец обычно берется от индивидуума, который, как подозревают, болен ГНАНВ, однако имеются образцы (пробы) и от других источников, например кондиционные субстраты или клетки из систем in vitro, в которых реплицирован вирус. Образец (проба), однако, должен содержать нуклеиновокислотный сиквенс с выбранной областью-мишенью.
Образцу затем создаются условия, при которых возможно проведение обратной транскрипции РНК ВГС в сДНК ВГС. Известны условия для обратной транскрипции РНК, такие условия, например, описываются Маниатисом и соавт., 1982, и в кн. "Методы энзимологии". В способе обратной транскрипции предпочтительно используется обратная транскриптаза из разных источников, таких как рекомбинантные молекулы, источники, выделенные, например, из ретровируса, предпочтительно из вируса птичьего миелобластоза (ВПМ), и создаются условия, благоприятные для транскрипции. Продукт сДНК ВГС обратной транскрипции представляет собой гибрид РНК:ДНК, который появляется после первого цикла обратной транскрипции, после этого в результате двух или более циклов транскрипции появляются гибриды ДНК:ДНК.
Продукт сДНК ВГС, как результат обратной транскрипции, затем подвергается ПЦР для амплификации сиквенса с выбранной областью-мишенью. Для выполнения этой задачи кДНК ВГС денатурируется, а разделенные цепи гибридизуются праймерами, фланкирующими сиквенс с выбранной областью-мишенью.
Разделение цепей может осуществляться любым соответствующим способом денатурации, в том числе физическими, химическими или ферментными средствами, известными специалистам в данной области. Предпочтительным является физический метод, представляющий собой нагрев нуклеиновой кислоты до тех пор, пока она полностью (>99%) не денатурируется. Обычная тепловая денатурация происходит при температуре в диапазоне от 80oC до 105oC за период от 1 до 10 минут.
После гибридизации кДНК ВГС праймерами ВГС-последовательности с выбранной областью-мишенью реплицируются с помощью полимеразиционного средства, которое использует праймерный олигонуклеотид для инициирования синтеза репликатной цепи. Отбор праймеров происходит таким образом, чтобы они были комплементарны последовательностям ВГС-генома. Олигомерные праймеры, комплементарные районам чувственных и античувственных ВГС кДНК-цепей, могут быть созданы из ВГС кДНК-последовательностей из композитной кДНК-последовательности, представленной на фиг.1.
Праймеры отбираются таким образом, что их относительные положения на дуплексной последовательности таковы, что выступающий продукт, синтезированный от одного праймера, при отделении его от его матрицы (комплемента) выполняет роль матрицы для удлинения другого праймера с получением репликатной цепи указанной длины.
Праймер предпочтительно является однонитчатым для проведения амплификации с максимальной эффективностью, но альтернативно может быть и двухнитчатым. Если он двухнитчатый, то его сначала обрабатывают для разделения его нитей, до того как он используется для подготовки удлиненных продуктов. Праймер предпочтительно является олигодезоксирибонуклеотидом. Праймер должен иметь достаточную длину, чтобы дать начало синтезу удлиненных продуктов в присутствии агента для гибридизации. Точные длины праймеров будут зависеть от многих факторов, таких как температура и источник праймера и методика. Например, в зависимости от сложности последовательности с выбранной областью-мишенью олигонуклеотидный праймер обычно содержит около 15-45 нуклеотидов, хотя он может содержать большее или меньшее количество нуклеотидов. Молекулы коротких праймеров обычно требуют прохладных температур для формирования достаточно стабильных гибридных комплексов с матрицей.
Праймеры, используемые в данной заявке, отбираются с расчетом, чтобы они были по существу комплементарными различным нитям каждой специфичной последовательности, подлежащей амплификации. Следовательно, праймеры не должны воспроизводить точную последовательность матрицы, но должны быть достаточно комплементарными избирательной гибридизации со своими соответствующими нитями. Например, некомплементарный нуклеотидный фрагмент может крепиться к 5'-концу праймера, причем оставшаяся часть последовательности праймера должна быть комплементарной нити. Некомплементарные основания или длинные последовательности альтернативно могут располагаться с промежутками в праймере при условии, что праймер имеет достаточную комплементарность последовательности одной из нитей, подлежащей амплификации, для гибридизации с ней, и тем самым образовывать дуплексную структуру, которая может быть удлинена средствами полимеризации. Некомплементарные нуклеотидные последовательности праймеров могут включать ограниченные ферментативные сайты. Прикрепление ограниченных ферментативных сайтов к концу(ам) последовательности с выбранной областью-мишенью было бы особенно полезным для клонирования последовательности с выбранной областью-мишенью.
Подразумевается, что термин "праймер", применяемый в данной заявке, может относиться к более чем одному праймеру, в частности, в случае если отмечается противоречивость информации, касающейся концевой последовательности(ей) области-мишени, подлежащей амплификации. Поэтому в понятие "праймер" входит совокупность праймерных олигонуклеотидов, содержащих последовательности, отображающие возможные варианты последовательностей, или нуклеотидов, которые позволяют осуществить обычное спаривание оснований. Один из праймерных олигонуклеотидов в этой совокупности будет гомологичным с концом последовательности с выбранной областью-мишенью. Специфичным является случай, когда используются наборы олигомеров для того, чтобы инициировать амплификацию потенциально вариантного района ВГС-генома.
Можно заранее предположить, что появится целый ряд штаммов или изолятов ВГС с сиквенсами, имеющими отклонения от ВГС1, штамма-прототипа. Поэтому, с целью детекции вариантных штаммов, предпочтительно строить праймеры, гибридизующие резервные районы ВГС-генома. Такие законсервированные районы могли бы определяться путем сравнивания нуклеотида или аминокислотных последовательностей нескольких штаммов/изолятов ВГС. По-видимому, имеется по меньшей мере три района законсервированной аминокислоты в ВГС-геноме, описанных выше, из которых можно выделить праймеры. Считаем, что такие районы имеются. Праймеры, описанные ниже, в примерах, выделены из, как полагают, законсервированных районов ВГС, основываясь на гомологии сиквенса, относящегося к флавивирусам.
Олигонуклеотидные праймеры могут быть подготовлены любым подходящим способом. Известны способы подготовки олигонукле-отидов специфичных последовательностей, они включают, например, клонирование и рестрикцию соответствующих последовательностей, прямой химический синтез. Способы химического синтеза могут включать, например, способ фосфотриэфира, описанный Нарангом и соавт. , 1979, способ фосфодиэфира, предложенный Брауном и соавт., 1979, способ диэтилфосфорарамидата, предложенный Бокажем и соавт., 1981 и способ твердой подложки, описанный в патенте США 4458066.
Праймеры могут, по желанию, быть маркированы с использованием средств, поддающихся выявлению спектроскопическими, фотохимическими, биохимическими, иммунохимическими или химическими средствами.
Матрицезависимое удлинение олигонуклеотидного праймера(ов) катализуется полимеризационным агентом в присутствии адекватных количеств четырех дезоксирибонуклеотидных трифосфатов (dATP, dGTP, dCTP и ТТР) или аналогов в реакционной среде, включающей соответствующие соли, катионы металлов и рН буферную систему. Соответствующими полимеризационными агентами являются ферменты, которые, как известно служат катализаторами праймер-зависимого и матрица-зависимого ДНК-синтеза. К известным ДНК-полимеразам относятся, например, Е. коли ДНК-полимераза 1 или ее Klenow фрагмент, Т4 ДНК-полимераза и Таg ДНК-полимераза. Известны реакционные условия для катализации ДНК-синтеза с указанными ДНК-полимеразами.
Продуктами синтеза являются дуплексные молекулы, состоящие из матричных цепей и цепей праймерных удлинений, включающих сиквенс с областью-мишенью. Эти продукты синтеза, в свою очередь, служат в качестве матриц для другого цикла репликации. Во втором цикле репликации праймерная удлиненная цепь первого цикла ренатурируется ее комплементарным праймером, в результате синтеза получают "короткий" продукт, который крепится на 5'- и 3'-концах праймерными сиквенсами или их комплементами. Повторы циклов денатурации, ренатурации праймеров и удлинение приводят к экспоненциальной аккумуляции области-мишени, образованной праймерами. По времени циклы достаточны, атобы получить потребное количество полинуклео-тидов, составляющих область-мишень нуклеиновой кислоты. Потребное количество полинуклеотидов может варьироваться и будет определяться той функцией, которую должен выполнять продукт полинуклеотида.
Способ ПЦР может проводиться в ряде временных последовательностей. Например, он может проводиться ступенчато, когда после каждого этапа добавляются новые реагенты, или когда одновременно добавляются все реагенты, или он может быть частично ступенчатым, когда свежие реагенты добавляются после данного количества этапов.
Предпочтительным способом является такой, при котором ПЦР проводится в автоматизированном режиме с использованием термостойкого фермента. При таком режиме реакционная смесь циклически повторяется, проходя через участок денатурации, участок ренатурации и участок реакции. Может использоваться устройство, специально приспособленное для использования термостойкого фермента, которое действует по принципу периодического изменения температуры без системы подачи жидкости, поскольку фермент не требует добавления в каждом цикле. Серийно выпускаемое устройство данного типа доступно для приобретения через инофирму Перкин Элмер Цетус Корпорейшн.
После амплификации в ходе ПЦР полинуклеотиды в области-мишени детектируются гибридизацией с зондичным полинуклеотидом, который формирует стабильный гибрид с гибридом сиквенса с выбранной областью-мишенью в условиях от строгого до умеренно строгого режима гибридизации и промывки. Если ожидается, что зондирование будет полностью комплементарным (т.е. около 99% или более) сиквенсу с выбранной областью-мишенью, применяется строгий режим соблюдения условий. Если ожидается некоторое несовпадение (мисматч), например, если ожидается, что результатом использования вариантных штаммов станет то, что зонд не будет полностью комплементарным, требования к строгости условий гибридизации могут быть снижены. Однако условия следует выбирать с таким расчетом, чтобы исключить неспицифичное/случайное связывание. Известны условия, которые воздействуют на гибридизацию и которые выбираются с целью противостоять неспецифичному связыванию, они описываются, например, у Маниатиса и соавт., 1982. Обычно низкая концентрация солей и повышенная температура способствуют точности результатов связывания. Например, обычно считается, что под строгими условиями инкубации в растворах понимаются такие, при которых растворы содержат приблизительно 0,1хssC, 0,1% SDS, при температуре инкубации/промывки около -65oC, а под умеренно строгими условиями понимаются такие, при которых инкубационные растворы содержат приблизительно 1-2 х ssC, 0,1% SDS, при температуре около 50 - 65oC процесса инкубации/промывки. Под нестрогими условиями понимается содержание в растворах 2хssC при температуре 30-50oC.
Зонды для ВГС-последовательностей с выбранной областью-мишенью могут быть выделены из сДНК-последовательности ВГС, показанной на фиг.1, или из новых ВГС-изолятов. Зонды ВГС могут быть любой достаточной длины, перекрывающей область-мишень, но исключающей праймеры и позволяющие гибридизацию области-мишени. Если имеется полная комплементарность, т.е. если штамм содержит сиквенс, идентичный сиквенсу зонда, т.к. дуплекс относительно стабилен даже при строгих условиях, зонды могут быть короткими, т.е. в пределах около 10-30 пар оснований. Если с зондом ожидается некоторая степень мисматча, т. е. если есть опасение, что зонд гибридизует вариантный регион, зонд может иметь большую длину, т.к. длина, по-видимому, уравновешивает некоторое воздействие мисматча(ей).
Нуклеиновая кислота зонда, имеющая последовательность, комплементарную последовательности с выбранной областью-мишенью, может быть синтезирована, пользуясь методами, схожими с описанными выше, в разделе синтеза праймерных последовательностей. В случае необходимости зонд может быть маркирован. Соответствующие маркеры описаны выше.
В некоторых случаях может появиться необходимость в определении длины продукта ПЦР, детектированного зондом. Это может быть особенно справедливо в случае, если есть подозрение, что штаммы вариантного ВГС могут иметь делеции в пределах области-мишени, или если возникает необходимость подтвердить длину продукта ПЦР. В этих случаях предпочтительно подвергнуть продукты размерному анализу, а также гибридизации с зондом. Известны способы определения размеров нуклеиновых кислот, они включают, например, электрофорез на геле, седиментацию ингредиентов и гельисключающую хроматографию.
Наличие последовательности с областью-мишенью в биологической среде детектируется путем определения образовался ли гибрид между зондом полинуклеотида ВГС и нуклеиновой кислотой, подвергнутой методу амплификации ПЦР. Известны способы детекции гибридов, образованных между зондом и нуклеиновокислотным сиквенсом. Например, немаркированная проба для удобства может быть перенесена на твердую матрицу, к которой она крепится, а скрепленная проба ставится в условия, которые позволяют осуществить специфичную гибридизацию с меченым зондом. Если проба маркирована, немаркированный зонд связывается альтернативно с матрицей, и после воздействия гибридизацией при соответствующих условиях матрица исследуется на наличие маркера. Другие формы соответствующих гибридизационных анализов описываются выше.
Определение вариантных ВГС-последовательностей с использованием ПЦР.
С целью идентификации штаммов вариантного ВГС и тем самым разработки зондов для этих вариантов применяется предложенный выше метод ВГС/сПЦР для амплификации вариантных районов ВГС-генома с тем, чтобы можно было определить нуклеотидные последовательности этих районов. Обычно можно ожидать, что вариантные формы ВГС могут проявиться в различных географических регионах, а не в тех, где штамм ВГС1 является доминирующим, например, в Японии, Африке и др. , или у разных видов позвоночных, которые также могут быть инфицированы вирусом. Кроме того, вариантный ВГС может возникнуть при пассаже в системах тканевых культур или в результате спонтанных или индуцированных мутаций.
Для амплификации вариантных областей-мишеней конструируются праймеры для фланкирования подозреваемого района и предпочтительно комплементарные законсервированным районам. Праймеры для двух ВГС-районов, которые предположительно законсервированы, имеют основой модель флавивирусов. При конструировании этих праймеров и зондов может быть использована информация о штамме ВГС1, предложенная на фиг.1.
Анализ нуклеотидной последовательности областей(и)-мишени(ей) может проводиться прямым анализом продуктов, амплифицированных ПЦР. Процедура прямого анализа последовательности продуктов, амплифицированных ПЦР, предложена Саики и соавт., 1988.
Амплифицированная последовательность(и) с областью-мишенью может быть альтернативно клонирована до проведения анализа последовательности. Способ прямого клонирования и анализа последовательности ферментно-амплифицированных геномных сегментов предложен Шарфом, 1986. Согласно его способу праймеры, используемые в ПЦР, модифицируются вблизи 5'-концов с целью образования удобных ограничительных сайтов для прямого клонирования, например, в вектор секвенирования М13. После амплификации продукты ПЦР расщепляются соответствующими ограничительными ферментами. Ограничительные фрагменты лигатируются в вектор М13 и трансформируются, например, в JM 103 хозяина, высеиваются, полученные бляшки фильтруются гибридизацией с меченым олигонуклеотидным зондом. Известны другие способы клонирования и анализа сиквенса.
Универсальные праймеры для флавивирусов и для ВГС.
Изучение ВГС-генома, применение зондов, выделенных от сДНК ВГС, а также сиквенс-информация, содержащаяся в сДНК ВГС позволяют отнести ВГС к флавивирусам. Информация об этих исследованиях дается в РСТ/ W 090/14436. Сравнение ВГС сДНК-последовательности, выделенной из ВГС сДНК-клонов, с известными последовательностями ряда флавивирусов показывает, что ВГС содержит последовательности, гомологичные законсервированным последовательностям в флавивирусах. Эти законсервированные последовательности могут дать возможность создать праймеры, которые могут найти универсальное применение при амплификации областей-мишеней флавивирусов и ВГС. Идентификация видов производится с помощью зонда, специфичного для этих видов. Известны геномы ряда флавивирусов, включающие такие, например, как вирус японского энцефалита (Сумиоси и соавт. , 1987), вирус желтой лихорадки (Райс и соавт., 1985), вирус денге, тип 2 ' (Ханн и соавт., 1988), вирус денге, тип 4 (Макоу, 1987) и вирус западного Нила (Кастл и соавт., 1986). Идентификация ВГС РНК проводится с использованием зонда, специфичного для ВГС, последовательность которого может быть определена представленными в данной заявке сДНК-последовательностями ВГС.
Альтернативно, использование наборов зондов, способных дать объяснение дегенерации кодона и содержащих для этой цели обычные последовательности, относящиеся к флавивирусам и ВГС, определенные путем сравнения аминокислотных последовательностей ВГС с известными последовательностями флавивирусов, позволяет организовать общую систему детекции этих вирусов.
Построение требуемых ДНК-последовательностей
Синтетические олигонуклеотиды могут быть получены с помощью автоматизированного синтезатора олигонуклеотидов, описанного Вагнером, 1984. Синтетические цепи, по желанию, могут быть маркированы 32Р путем обработки полинуклеотидной киназой в присутствии 32Р-АТР при стандартных условиях проведения реакции.
ДНК-последовательности, в том числе выделенные из библиотек сДНК, могут быть модифицированы известными методами, такими, например, как свит-направленный мутагенез, описанный Цоллером, 1982. Если изложить суть дела кратко, ДНК, подлежащая модификации, упаковывается в фаг в виде одноцепочечной последовательности и преобразуется в двухцепочечную ДНК, с ДНК-полимеразой, используя в качестве праймера синтетический олигонуклеотид, комплементарный той части ДНК, которая подлежит модификации, и имея необходимую модификацию как компонент своей собственной последовательности. Образованная в результате этого двухцепочечная ДНК трансформируется в бактерию хозяина в фаге. Культуры трансформированных бактерий, которые содержат репликации каждой нити фага, высеваются в агаре для получения бляшек. Теоретически, 50% новых бляшек содержат фаг, имеющий мутированную последовательность, а оставшиеся 50% имеют первоначальную последовательность. Копии бляшек гибридизуются в меченый синтетический зонд при температуре и условиях, позволяющих проведение гибридизации с правильной нитью, но не с модифицированной последовательностью. Последовательности, идентифицированные гибридизацией, выделяются и клонируются.
Комплекты для скрининга ВГС-выделенных полинуклеотидов
Олигомеры, являющиеся зондами и/или праймерами для амплификации и/или скрининга проб для ВГС, могут укладываться в комплекты. Комплекты для скрининга последовательностей ВГС включают олигомерные зонды ДНК. Комплекты для амплификации ВГС-последовательностей могут включать олигомерные праймеры, используемые при амплификации. В комплектах находятся зонды или праймеры, как правило, с предварительно произведенными измерениями и определением количества, а также другие реагенты и материалы, размещенные соответствующим образом в отдельных емкостях, что обусловлено необходимостью учета и регистрацией при гибридизации и/или амплификации. Так, например, в комплект могут входить стандарты, буферные растворы, подложки, ферменты, субстраты, меченые зонды, связующие партнеры и/или инструкции по технике проведения тестов.
Нижеописанные примеры, относящиеся к настоящему изобретению, приведены только в иллюстративных целях и не ограничивают объем изобретения.
I. Детекция позитивно- и негативно- цепочечной 5 -РНК ВГС в сыворотке крови
РНК в ВГС27, выделенную из сыворотки, исследовали на наличие плюс-цепи и минус-цепи способом ПЦР. В основном, способ ПЦР проводился аналогично описанному выше с некоторыми отличиями, приведенными ниже.
Экстрагированную ВГС 27 РНК обратно транскрибировали в одноцепочечную сДНК, в качестве праймера использовали либо А1ех 90, либо J Н52. Праймер А1ех 90, выделенный из нуклеотидов - 312 до -283 BГC1-генома имеет последовательность:
5' АСС ATG ААТ CАC ТСС СCТ GTG AGG ААС ТАС 3'
Н52 выделен из нуклеотидов ВГС от -93 до -117, номера нуклеотидов указаны в скобках под последовательностями. В праймере JН52 для формирования NOt I-участка мутировали подчеркнутый динуклеотид. Ниже показана последовательность pf JH52:
(Праймер) Наполнитель NOt I ВГС-последовательность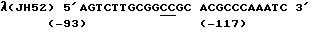
Последовательность Аlех 90 совпадает с указанной в нуклеотидах от -312 до -283 плюс-цепи РНК ВГС, тогда как JH52 совпадает с указанной в нуклеотидах от -117 до -93 минус-цепи. Образованные в результате этого одноцепочечные ДНК ВГС каждую в отдельности амплифицировали ПЦР, применяя Аlех 90 и JH52. Детекцию амплифицированных продуктов проводили саузерн-блоттингом, в качестве зонда применяли А1ех 89. Alex 89 совпадает с РНК ВГС в нуклеотидных номерах от -203 до -175. Ниже приведена последовательность Alex 89:
5' СCA TAG TGG TCT GCG GAA CCG GTG AGT ACA 3'
Исследование показало, что при этом способе сигналы амплифицированных продуктов обеих РНК-цепей были равной интенсивности. Такие результаты дают возможность предположить, что РНК ВГС в 5'-районе может быть в качестве двухцепочечной РНК.
II. Детекция РНК ВГС в плазме с использованием ВГС/сПЦР, праймеров и зондов, выделенных из 5'-района ВГС РНК
Экстракция РНК ВГС из плазмы
Замороженную плазму размораживали оттаиванием в дефростере Р3. 0,2 мл аликвоты пищевой смеси (100 мМ Трис-HCl, 2 мМ ЭДТА, 200 мМ NaCl, 20 г/мл MS2 РНК, 0,5% SDS, и 2 мг/мл концентрации протеиназы К, рН 8) добавляли в 2 мл пробирку микроцентрифуги и предварительно нагревали до 37oС. Затем добавляли плазму (0,2 мл) и смесь инкубировали 1 час при 60oС. Затем добавлялся фенол (0,4 мл), смесь встряхивали три раза по 30 секунд с 30-секундной паузой между каждым встряхиванием. Затем смесь разделялась центрифугированием в течение 5 минут и извлекалась водная фаза. Органическую фазу осаждали в 0,1 мл TES обратным центрифугированием, смешанные водные фазы экстрагировали дважды 1 объемом фенола/хлороформа/ 1АА, затем 1 объемом хлороформа. К экстракту добавляли 1 мкл (2 мг) гликогена (инофирма Борингер-Манхайм Корпорейшн) и 25 мл NаОАс (3 М, рН 5,4), и 1,25 мл холодного EtOH, продукт замораживали на сухом льду и вращали центрифугированием в течение 10 минут. Осадок растворяли в 100 мл дистиллированной воды и в 5 мл NaOAc (рН 5,4) с добавлением 250 мкл холодного EtOH. Раствор замораживали и снова центрифутовали, а образовавшийся осадок растворяли в 10 мл Н2О.
Синтез кДНК
Для синтезирования кДНК из экстрагированной РНК сначала 5 мл растворенной РНК инкубировали в 4 мл воды и 1 мл (1 мг или 166 пмолс 18-мер) праймера RТ. Инкубировали при 70oС 3 минуты и охлаждали намораживанием льда. Ниже показана последовательность праймера RT:
5' ССС ААС ACT ACT CGG СТА 3'
После первичной инкубации в инкубационную смесь добавляли следующие компоненты: 10 мл 5 раз буфера первой цепи (250 мМ трис-HCl, рН 8,3, 375 мМ КСl, 15 мМ MgCl2, 50 мМ дитиотреитола), 2,5 мл трифосфатов дезоксинуклеозида (10 мМ каждого), 2,5 мл обратной транскриптазы (MM LV из BRI, 200 ед. на л) и дистиллированной воды, доводят объем до 50 мл. Смесь инкубируют при 37oС 1 час, прогревают при 90oС 3 минуты и охлаждают намораживанием льда.
Амплификация ПЦР
Амплификация полимеразной цепной реакцией кДНК ВГС, полученной вышеописанным способом, проводилась с использованием контрольно-тестовых реагентов, приведенных ниже, в табл. 1.
В табл. 1 в колонке "РНК" приведена контрольная проба, в которой РНК экстрагировали от индивидуума, не инфицированного BГC1, эта проба проводилась через стадии синтеза сДНК и амплификации ПЦР.
В колонке "cДНК" приведена контрольная проба, которая проводилась через стадии синтеза сДНК и амплификации ПЦР, однако РНК-аликвота в этом случае при синтезировании кДНК заменялась водой.
В колонке "матрица" приведены данные контроля за ПЦР, при которой матрица не использовалась.
В колонке "проба" приведена сыворотка, исследованная на наличие РНК ВГС.
Праймер 1 и праймер 2 были 0,5 мкг/ мкл и 0,42 мг/мл соответственно и имели следующие последовательности:
Праймер 1: 5' АСС АТG ААТ CАC ТСС СCТ GTG АGG ААС ТАС 3'
Праймер 2: 5' АGТ СТТ GCG GGG GСА CGC ССА ААТ С 3
Эти праймеры гибридизуют с консервативным районом на 5'-конце генома ВГС. Пробы содержали 12,5 мл сывороточных эквивалентов кДНК ВГС. Ниже приведены условия, в которых проводился цикл амплификации:
35 циклов: Плавление - при 94oC 1,5 мин
Ренатурация - при 60oС 2 мин
Элонгация - при 72oС 3 мин
Окончат.элонгация - при 72oC 30 мин
Пропитка - при 4oC до удаления
Амплифицированный продукт зондировался с использованием меченой ДНК. Ниже приведена последовательность зонда:
Зонд: 5' RRR СТТ GGA ТСА АСС СGС ТСА ATG CCT GGА 3'
Во время вышеуказанного анализа было исследовано более 200 проб ВГС с позитивной сывороткой. Во внимание принимались только те результаты, в которых контрольные группы были отрицательными. В этом случае все позитивные сывороточные пробы были позитивными также и при анализе ПЦР.
III. Зонды, полученные из мнимого кор- района РНК ВГС
Исследование кДНК-нуклеотидных последовательностей разных ВГС-изолятов свидетельствует, что высокая степень консервативности последовательностей относится к району примерно от нуклеотида 1 до примерно нуклеотида 570, если пользоваться системой нумерации, приведенной на фиг. 1. Этот район предположительно кодирует "кор"-полипептид ВГС. Консенсусные последовательности для пяти различных изолятов из разных географических регионов (Япония и США) показаны на фиг.2, где ВГС1 является прототипом ВГС, аминокислоты, кодируемые протяженной ОРС ВГС1 показаны над консенсусными нуклеотидными последовательностями. Среди последовательностей, показанных на фиг. 2, ВГС- Н любезно предоставлен доктором Тетсу Миямура (Национальный Институт Здоровья, Япония), а вирусы JC -J1 и JC
- J4 взяты из описанных Маюми и соавт., 1990. На фиг. 2 можно видеть, что между консенсусными последовательностями предполагаемого "кор"-района имеется по меньшей мере до 90% гомологии, относящейся к последовательности ВГС1. Ввиду высокой степени гомологии в районе между нуклеотидами +1 и +571 зондирование указанного района будет полезным при скрининге позитивных биологических образцов ВГС.
Набор меченых зондов, которые могут быть использованы для детекции РНК ВГС из района, который предположительно кодирует "кор"-полипептид ВГС, показан на фиг.3. На фиг.3 видно, что "номер зонда" в наборе включает ряд полинуклеотидов с неоднородностями, указанными в группе кода Международного Института Биологии (IUB), показанной на фиг.3. Эти неоднородности (гетерогенности) предназначены для размещения различий нуклеотидных последовательностей, показанных в консенсусных последовательностях различных изолятов. Районы ВГС-последовательностей, к которым комплементарными являются зонды в наборе зондов, показанном на фиг.3, показаны на фиг.4, в которых номера нуклеотидов соответствуют нумерации на фиг.1.
Этот набор зондов использовался при анализе, в котором детектировались ВГС-последовательности. Техника проведения этого анализа описана в РCТ/W 090/14436 в разделе "Примеры", озаглавленном "Зонды для сэндвич-гибридизации ВГС".
Промышленная применимость
Способы, описанные в данной заявке, а также олигомеры как зонды, так и праймеры, полученные из сДНК ВГС, и комплекты для них, практически удобны для точного, относительно простого и экономичного определения наличия ВГС в биологических средах, в частности в крови, которая может быть использована для трансфузий, и у индивидуумов с подозрением на инфекцию ВГС. Более того, эти способы и олигомеры могут быть использованы для обнаружения инфекции ВГС на ранней стадии по сравнению с иммунологическими исследованиями, основанными на использовании рекомбинантных ВГС-полипептидов. Кроме того, амплифицированные полинуклеотидные гибридизационные анализы позволяют осуществить детекцию РНК ВГС в окказиональных пробах, которые являются анти-ВГС негативными антителами. Таким образом, зонды и праймеры, описываемые в данной заявке, могут быть использованы в амплифицированных гибридизационных анализах во взаимодействии с иммуноанализами, основанными на ВГС-полипептидах, для более полной идентификации инфекций, вызванных ВГС, и инфицированных ВГС биологических пробных экземпляров, в том числе крови.
Информация, представленная в данной заявке, позволяет конструировать праймеры и/или зонды, получаемые из консервированных районов ВГС-генома. Создание таких праймеров и зондов делает доступным применение общего способа детекции вариантных штаммов ВГС, который может быть также использован при скрининге крови и ее препаратов.
Если праймеры, применяемые в данном способе, получают из консервированных районов ВГС-генома, способ будет способствовать детекции и/или идентификации вариантных ВГС-штаммов. Это, в свою очередь, должно привести к появлению дополнительных полинуклеотидных реагентов для выявления и обработки ВГС.
Наборы праймеров и зондов, сформированных из консервированных аминокислотных последовательностей флавивирусов и ВГС, позволяют, кроме того, иметь универсальный способ выявления таких инфицированных агентов.
Перечисленные ниже материалы депонируются согласно Будапештскому договору в Американской Коллекции Типовых Культур (АТСС), 12301 Парклоун Драйв, Роквилль, Мэриленд 20852, и им присвоены следующие регистрационные номера ( см. табл. 2).
Кроме того, внесены на хранение 11.05.1989 следующие депозиты (см. табл. 3).
3.05.1989 внесены на хранение следующие производные штамма 1210:
Дериват штамма - АТСС
p CF 1 CS/C8f - 67956
р СF 1AB/C12f - 67952
p CF 1EF/14с - 67949
р СF 1EF/15с - 67954
p CF 1AB/с25с - 67958
p CF 1EF/C33с - 67953
p CF 1EF/с33f - 67050
p CF 1СD/с33g - 67951
р СF 1CD/с39с - 67955
р СF 1EF/с40b - 67957
p CF 1EF/СA 167 b - 67959
12.05.1989 внесены на хранение следующие штаммы:
Штамм - ATCC .
Ламбда gt 11(035) - 40603
Ламбда gt 10 (бета-5а) - 40602
D 1210 (c40b) - 67980
D 1210 (M16) - 67981
23.03.1990 внесены на хранение следующие биологические вещества:
Вещество - АТСС
5'-клон 32 (в pUC 18 S) - 68276
После принятия решения экспертизы о патентоспособности и выдачи патента США по данной заявке будут окончательно сняты все ограничения на пользование этими депозитами, доступ к указанным депозитам будет возможен во время рассмотрения вышеназванной заявки для лица, определенного Комиссаром по патентам как имеющего на это право согласно статьи 37, пункта 1.14 Свода федеральных правил и раздела 35, пункта 1.22 Кодекса законов США. Более того, указанные депозиты будут сохраниться в течение тридцати (30) лет, начиная с даты внесения их на хранение, или в течение пяти (5) лет после последнего запроса о депозите, или на период исковой силы патента США, независимо от того, каким бы долгим он ни был. Депонируемые культуры, упоминаемые в данной заявке, приводятся только для удобства пользования ими и качестве материала ссылочного характера и не могут рассматриваться как признак, относящийся к описанию данного изобретения.






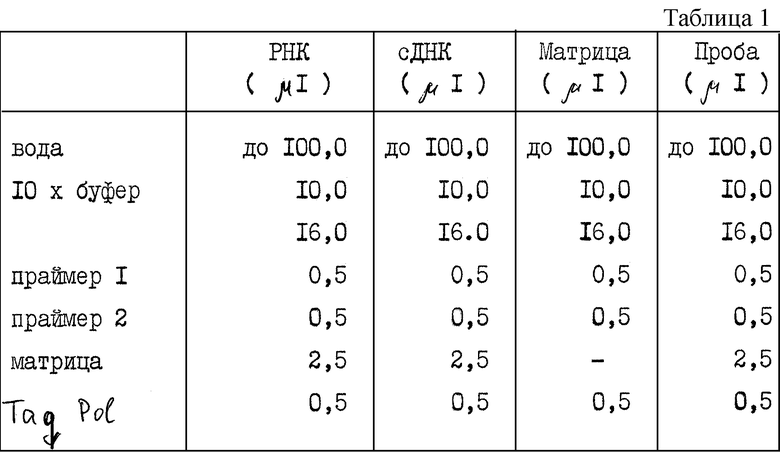
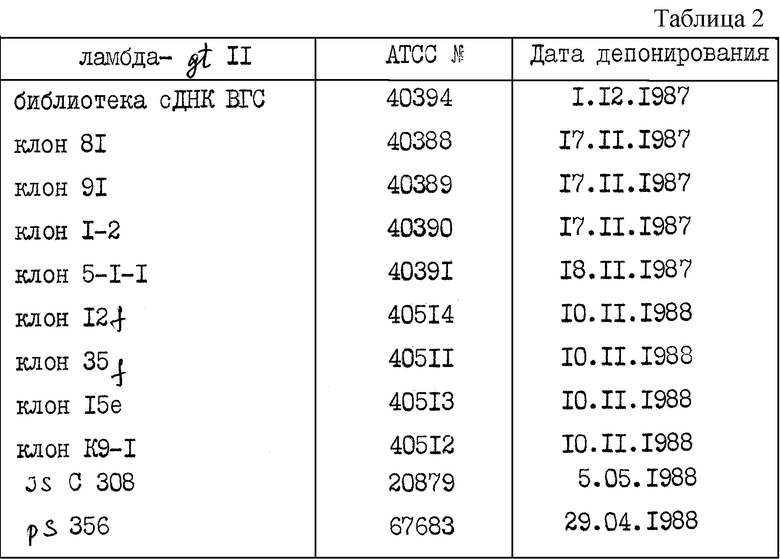
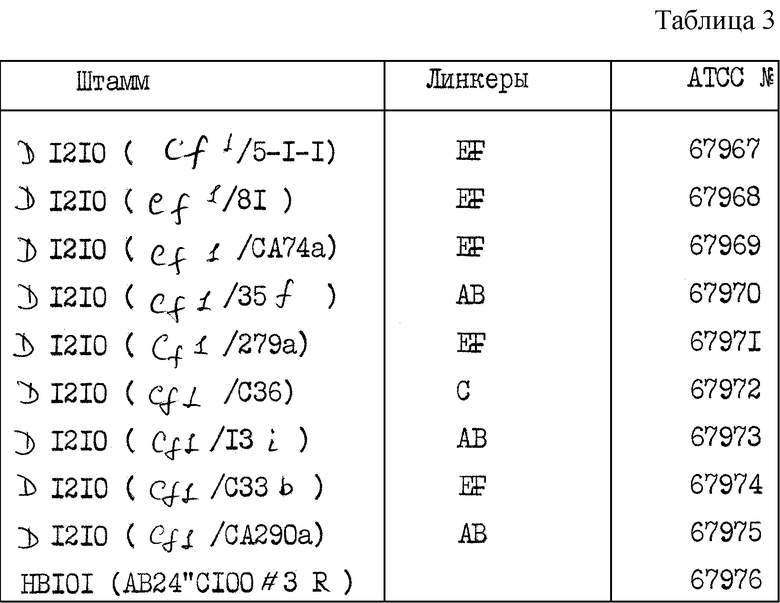











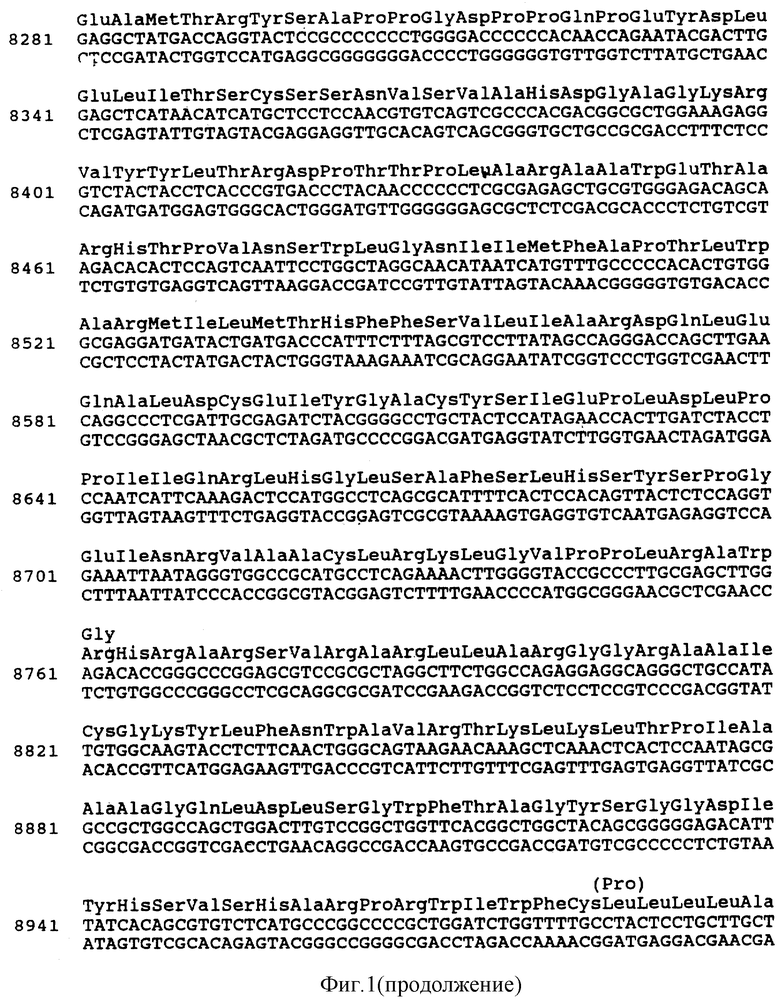






Изобретение относится к области медицины и может быть использовано для диагностики вируса гепатита С в биологических средах. Получены реагенты для выделения, амплификации и детекции вируса гепатита С. Такими реагентами являются олигомеры, состоящие из полинуклеотидных последовательностей, которые способны формировать гибридные структуры с ВГС-полинуклеотидными последовательностями в области мишени. Изобретение позволяет повысить качество и надежность диагностики ВГС в биологических пробах. 5 с. и 5 з.п. ф-лы, 4 ил. , 3 табл.
| СПОСОБ СТАБИЛИЗАЦИИ ГАЛОИДСОДЕРЖАЩИХ УГЛЕВОДОРОДОВ | 0 |
|
SU318216A1 |
| Рекомбинантная плазмидная ДНК @ BLV 51-3, кодирующая кор-антиген вируса гепатита В с экспонированным на его поверхности эпитопом BLV @ 51 (56-103), вируса лейкоза крупного рогатого скота способ ее конструирования и штамм бактерий ЕSснеRIснIа coLI - продуцент кор-антигена вируса гепатита В с экспонированным на его поверхности эпитопом BLV @ 51 (56-103) | 1989 |
|
SU1742331A1 |
Авторы
Даты
2002-03-10—Публикация
1991-08-12—Подача