Изобретение относится к микробиологической и медицинской промышленности, генной и белковой инженерии, биотехнологии.
Целью изобретения является получение рекомбинантных капсидных структур, представляющих собой кор-антиген вируса гепатита В, 39 С-концеаых аминокислот которого заменены на последовательность
BLV gp 51(56 - 103) - белка вируса крупного рогатого скота.
Сконструирован рекомбинантный ген| НВсАд Д - BLVдр 51 (56- t03), кодирующий синтез соответствующего белка и плазмиды pBLV 51-3 для его экспрессии, а также штамм - продуцент Е. coll (pBLV 53 - 3) рекомбинантной структуры НВсАдД - BLV др 51(56 - 103), обеспечивающий выход конемного продукта в количестве не менее 26,7% от суммарного белка Е, coll,
Рекомбинантная плазмида pBLV 51-3 состоит из следующих элементов: ДНК плэзмиды рВс1615, которая представляет собой вариант плазмиды рНВсЗ, содержащей ген НВсАд с оптимизированным участком инициации трансляции, но с мутантным геном НВсАд, содержащим полилинкерную вставку по 144-й аминокислоте и предназначенным для внедрения чужеродных последовательностей по этому участку, протяженность 6900 п.о.; фрагмента генома BLV, соответствующего последовательности между сайтами рестрикции Bgl llsoss и Bam Ш5226И кодиру ющего участок др 51(56- 103) протяженностью 143 п.о.
Размер плазмиды 7000 п.о., мол. м. 4,49 МД. В состав ДНК рекомбинантной плазмиды pBLV 51-3 входят ген НВсАд Л - BLVgp 51(56-103), обеспечивающий синтез конечного продукта, и ген Bla, обеспечивающий устойчивость к ампициллину.
Ген НВсАд Л- BLVgp 51(56-103) находится под контролем тандема промоторов Ptrp,
Плазмида pBLV 51-3 амплифицируется при добавлении в среду хлорамфеникола, неконъюгативна.
Сущность способа конструирования плазмиды pBLV51-3 состоит в том, что фрагмент гена env BLV, именуемый BLVgp 51 (56 - 103), протяженностью 143 п.о., внедряют по сайту рестрикции EcoRV в векторную плазмиду рН Вс 1615 с образованием реком- бинантного гена НВсАдА -др51 (56- 103). В результате делеции в векторной плазмид- ной ДНК утрачивается С-концевая часть гена НВсАд.терминацияжерекомбинантного гена наступает непосредственно за внедренным фрагментом BLV gp 51(56 - 103).
Штамм - продуцент HBcAgA - BLVgp 51(56 - 103) получают трансформацией клеток Е. coll K802 рекомбинантной плазмид- ной ДНК pBLV 51-3.
Морфологические признаки.
Клетки палочковидной формы, грам-от- рицательные.
Культуральные признаки,
Клетки растут на обычно используемых питательных средах, образуют колонии средней величины.
Физико-биохимические признаки.
Оптимальная температура культивирования 37°С, оптимум рН 7,0 - 7,4, В качестве источника углерода используют углеводы, в качестве источника азота - минеральные соли, а также органические соединения в виде пептона, триптона, аминокислот.
Устойчивость к антибиотикам. Устойчив к ампициллину, что обусловлено наличием плазмиды. Присутствие в штамме плазмидной ДНК подтверждается
путем проверки устойчивосчти к ампициллину, а также путем выделения и анализа плазмидных ДНК экспресс-методом.
Штамм депонирован в коллекции Центрального музея промышленных микроорганизмов под номером ВКПМ В-4969.
Пример 1. Конструирование рекомбинантной плазмидной ДНК pBLV 51-3.
2 мкг плазмиды рНВс1615, выделенной стандартным методом, расщепляют частично 2 с д. рестриктазы Е. coRV в 25 мкл раствора А, содержащего 10 мМ трис-HCI, рН 7,5,50 мМ NaCI и 10 мМ MgCl2, в течение 0,5 ч при 37°С. Рестриктазу инактивируют 15- минутным прогреванием при 65°С. Линейную плазмидную ДНК протяженностью 6900 п.о. выделяют из 0,7%-ного агарозного геля и растворяют в 20 мкл Н20 (ДНК 1).
20 мкг плазмиды рНМ 19-3/4 расщепляют 50 ед. Bgl II и 50 ед. Bam HI в 100 мкл
раствора А в течение 2 ч при 37°С, наносят инкубационную смесь на 1,5-й агарозный гель, фрагмент с мол. м. 91 КД (размером 143 п.о.), несущий эпитоп. BLVgp 51(56 - 103), выделяют из агарозного геля известным методом.
Фрагмент растворяют в 10 мкл Н20, липкие концы заполняют в 20 мкл раствора Б, содержащего 50 мМ трис-HCI, рН 7,5, 10 мМ MgCIa, ЮмМ дитиотрейтол, 25 мМ NaCI,
100 М dATP, dCTP, dTTP и dGTP и 5 ед.. ДНК-полимеразы E.coli (фрагмент Кленова), в течение 1 ч при 12°С (ДНК2).
0,25 мкг ДНК 1 и 0,1 мкг ДНК 2 зашивают Т4 ДНК-лигазой в 10 мкл раствора В,
содеражщего 50 мМ трис-HCI, рН 7,5, 10 мМ MgCl2 10 мМ дитиотрейтол, 50 М АТР и 10 ед. Т4 ДНК-лигазы, в течение 12 ч при 37°С. Фермент инактивируют нагреванием при 65°С в течение 15 мин. К реакционной смети
добавляют 100 мкл клеток Е. coll RR1, обработанных 300 мМ CaCIa (конечная концентрация 5 х 10 кл./мл), для трансформации клеток по известному методу.
Отбор клонов осуществляют путем рестрикционного анализа плазмидной ДНК, выделенной экспресс-методом. Плазмида с ожидаемой рекстрикционной картой получает наименование pBLV 51-3.
Пример 2, Штамм-продуцент Е. coif
К802 (pBLV 51-3). Выделение и очистка ре- комбинантного белка НВсАд Л - BLVgp 51(56 - 103).
Штамм-продуцент получают трансформацией клеток Е, coli K802 рекомбинантной
плазмидой pBLV 51-3. Клетки выращивают в солевой среде М9 с добавкой, г/л: казами- новые кислоты 10, глюкоза 2, ампициллин 0,02, до оптической плотности ОПбБО 4-5. Клетки собирают центрифугированием и ли- зируют в четырехкратном объеме буфера, содержащего 0,05 М трис-HCI, рН 8,0, 0,15 М NaCI, 0,1 % тритон Х100, 0,005 М ЭДТА, 2 мг/мл лизоцима. После инкубации в течение 30 мин при 4°С клетки подвергают двух- кратному замораживанию - оттаиванию, добавляют дезоксирибонуклеазу и MgCIa до конечной концентрации 20 мкг/ мл (10 мМ) и инкубируют 30 мин при 4°С. Лизат осветляют центрифугированием (10 000 х д, 4°С).
НВ cAgA - BLVgp 51(56 - 103) очищают следующим образом.
Бесклеточный лизат разбавляют в 4 раза дистиллированной водой и подвергают фракционированию сульфатом аммония. НВсАд А - BLVgp 51(56 - 103) собирают в осадке, полученном при 30% насыщения сульфатом аммония. Осадок растворяют в 0,05 М трис-HCI, рН 8,0, 0.15 М Nad, 0,1% тритоне Х-100 до конечной концентрации белка 25 - 50 мг/мл, и 2 - 4 мл этого раствора наносят на колонку с сефарозой (1,6 х 100 см), уравновешенную тем же буфером, но без тритона Х-100. Фракции, проявляющие HBcAg-активность, собирают и используют либо непосредственно, либо после концентрирования переосаждением 50%-ным . сульфатом аммония.
Пример 3. Определение НВсАд-ак- тивности методом РИД.
Титр НВсАд определяют с помощью радиальной иммунодиффузии по Ухтерлони. Для этого готовят двухкратные серийные разведения клеточного лизата и титруют против анти-НВс антител человека. В каче- стве стандарта используют очищенный НВ сАд, полученный из рекомбинантных бактерий (1 мг/мл). Результаты титрования НВсАд-активности методом РИД приведены в табл. 1.
Пример 4. Определение др 51-актив- ности методом иммуноблотинга. Мол. м. белка НВсАдД - BLVgp 51(56 - 103).
Для иммуноблотинга клетки (6 мг) суспендируют в 100 мкл буфера для нанесения образцов на полиакриламидный гель по Лэммли, содержащего 2%-ный додецил- сульфат натрия (ДСН) и 2%-ный / -меркап- тоэтанол, и лизируют 2 мин прогреванием на кипящей водяной бане. Полученные ли- заты (2-4 мг/мл белка) наносят на полиакриламидный градиентный гель (12 - 18%) размером 150 х 150 х 0,75 мм. Электрофорез проводят в течение 15 ч при силе тока 7 мА.
После электрофореза белки переносят на нитроцеллюлозу. Фильтры инкубируют с моноклональными анти-др 51 антителами ппАК14 в разведении 1:500 на буфере TBS с 1% БСА в течение 15 ч при 20°С. После трехкратной отмывки буфером TBS фильтры инкубируют 2 ч при комнатной температуре с конъюгатом пероксидазы с антителами против иммуноглобулинов мыши в разведении 1:200. Фильтры отмывают буфером ТВ$ (3-5 раз) и проявляют диами- нобензидином. Лизаты клеток штамма - продуцента обнаруживают при этом появление специфических зон окраски, соответствующих белку с мол. м, 21,2 КД (или длиной 200 аминокислот). Контрольные ли- заты клеток E.coli К802(рНВсЗ)таких зон не обнаруживают.
Пример 5. Электронно-микроскопическая характеристика рекомбинантных капсидных структур НВсАд А - BLVgp 51(56
-103).
Препараты очищенного белка НВсАд А
-BLVgp 51(56 - 103) готовят методом негативного контрастирования с применением 1%-ного уранилацетата и исследуют на электронном микроскопе при ускоряющем напряжении 80 кВ и инструментальном увеличении 100000 раз. Белок НВсАд А - BLVgp 51(56 - 103) образует капсиды с диаметром 25 нм.
Пример 6. Определение др 51-активности в составе капсидных структур НВсАдА - BLVgp 51(56 - 103) методом эн- зимоиммунологического анализа на твердой фазе.
В качестве твердой фазы используют полистироловые 96-луночные планшеты для иммунологических реакций. Очищенный белок HBcAgA - BLVgp 51(56 - 103) разводят до определенной концентрации (мкг/мл) в 50 мМ трис-KCI, рН 8.0,0.15 М NaCI и вносят в лунки планшетов - по 100 мкл в каждую. Инкубируют 1 ч при 37°С, после чего раствор удаляют из лунок, планшеты отмывают 4-5 раз дистиллированной водой и высушивают. В лунки вносят монокяональные анти- др 51 антитела мыши (МАК 14) в различных разведениях. После инкубации в течение 1 ч при 37°С планшеты отмывают дистиллированной водой и вносят по 100 мкл коньюгата пероксидазы хрена с антителами против иммуноглобулинов мыши в рёзведении 1:500. После инкубации в течение 1 ч планшеты отмывают и проводят цветную реакцию. В лунки вносят по 100 мкл 0,25%-ного раствора ортофенилендиамина, 2% HCI в 0,1 М цитрате натрия, рН 5,0,0,02% HaOz. инкубируют 30 мин при 20°С, реакцию останавливают добавлением 100 мкл 0,1 н. HCI. Появление коричневой окраски свидетельствует о наличии др 51-активности, для количественной оценки активности измеряют оптическую плотность при 492 нм (табл. 2). Отсутствие реакции в отрицательном контроле (НВсАд) свидетельствует о специфичности связывания анти-др 51 антител рекомбинантными капсидными структурами НВсАд Л - BLVgp 51 (56 - 103).
Пример 7, Определение др 51-активности на поверхности капсидных структур HBcAg A- BLVgp 51(56-103) методом им- муноэлектронной микроскопии.
Капсиды HBcAgA - BLVgp 51(56 - 103) сорбируют на никелевой сеточке, покрытой формваровой пленкой, в течение 15 мин. Сеточку промывают 0,5 мл раствора PBS, содержащего 0,05% Твин-20 (РВЗ-Твин-20) и инкубируют 15 мин в 0,03 мл 0,1%-ного раствора БСА в воде, промывают 0,5 мл РВ5-Твин-20, инкубируют 15 минчв 0,03 мл раствора моноклональных анти-др 51 антител человека МАК14 в разведении 1:100, промывают 0.5 мл РВ5-Твин-20, инкубируют 20 мин в 0,03 мл антител (кролика) против иммуноглобулинов мыши (в разведении 1:500) и промывают 0,5 мл РВ5-Твин-20. Сеточку помещают на 1 ч в 0,03 мл раствора рА-Au, содержащего белок А, который конъ- югирован с частицами коллоидного золота диаметром 5 нм, промывают 0,5 мл PBS- Твин-20 и затем 1 мл НаО. Капсиды окраши- ваютметодомнегативного
констатирования 0,15 мл 2%-ного уранила- цетата. Все операции выполняют при 20°С. В случае поверхностной локализации соответствующих эпитонов капсиды на электронной микрофографии окружены венчиком частиц коллоидного золота. В качестве отрицательного контроля используют капсиды HBcAgA , не несущие эпитоп др 51(56 - 103). Эти капсиды не образуют комплексо- нов с коллоидным золотом. Не образуются комплексы также в отсутствие специфических антител.
Пример 8. Иммуногенная активность рекомбинантных капсид HBcAg A - BLVgp 51(56-103).
Для определения иммуногенности рекомбинантными капсидами HBcAgA - BLVgp 51(56 -103) иммунизируют кроликов. Для этого смешивают 2 мг антигена, растворенного в 1 мл физиологического раствора PBS, с 1,25 мл полного адъюванта Фрейнда
и получают гомогенную эмульсию. Антиген вводят подкожно. Инъекции антигена повторяют на 14-й и 21-й день и с 28-го дня начинают брать кровь. Специфичность антител определяют методом ИФА с использованием двух антигенов: НВсАд (для определения анти-НВс антител) fr-BLVgp 51 (для определения анти-др 51 антител). Титры антител на 28-ный день иммунизации
приведены в табл. 3.
Формула изобретения
1.Рекомбинантная плазмидная ДНК pBLV51-3, кодирующая кор-антиген вируса гепатита В с экспонированным на его поверхности эпитопом BLVgp 51(56 - 103) вируса лейкоза крупного рогатого скота размером 7047 п.о. и мол. м. 4,5 МД, содержащая плаэмидную ДНК рНВс 1615 размером 6900 п.о., обработанную рестриктазой
Е coR V; -Bgl llsoea Bam Hts226 - фрагмент плазмиднойДНКрН М 19-3/4 размером 147 п.о,, кодирующий участок белка др 51(56 - 103) вируса лейкоза крупного рогатого скота, обработанный ДНК полимеразой Е. coli,
уникальные сайты рестрикции и их координаты: Bam H1 (0), Sph 1(101), Sal 1(276), Nru 1(599), Sng 1(1871), Afllll (2098), PstJ 1(3236), Scg 1(3471) Xba 1(5176). Nco 1(5569); гены, генетические маркеры и регуляторные участки: ген HBcAg A - BLVgp 51(56 - 103), обеспечивающий синтез рекомбинантных. капсидных структур -HBcAgA - BLgp 51(56 - 103) (координаты 5087 - 5670: ген Bla, обеспечивающий устойчивость к ампициллину (координаты 2918 - 3778); ген НВсАд А - BLgp51 находится под контролем тандема промотора Ptrp.
2.Способ конструирования рекомби- нантной плазмидной ДНК, кодирующей
кор-антигек вируса гепатита В. экспонированной на его поверхности эпитопом BLVgp 51 (56 - 103) вируса лейкоза крупного рогатого скота, pBLV 51-3, предусматривающий получение фрагмента генома BLV длиной
143 п.о., кодирующего участок др 51(56 - 103), клонирование его в Е coRV-сайт плаз- миды рН Вс 1615, при этом 39 С-концевых аминокислот удаляют в результате делеции, трансформацию рекомбинантными ДНК
клеток Е. coll и отбор клонов, содержащих плазмидную ДНК.
3.Ш.тамм бактерий Escherlchla coll. ВККМ В-4969 - продуцент кор-антигена вируса гепатита В с экспонированным на его
поверхности) эпитопом BLVgp 51(56 - 103) вируса лейкоза крупного рогатого скота.
Та б л и ц а 1



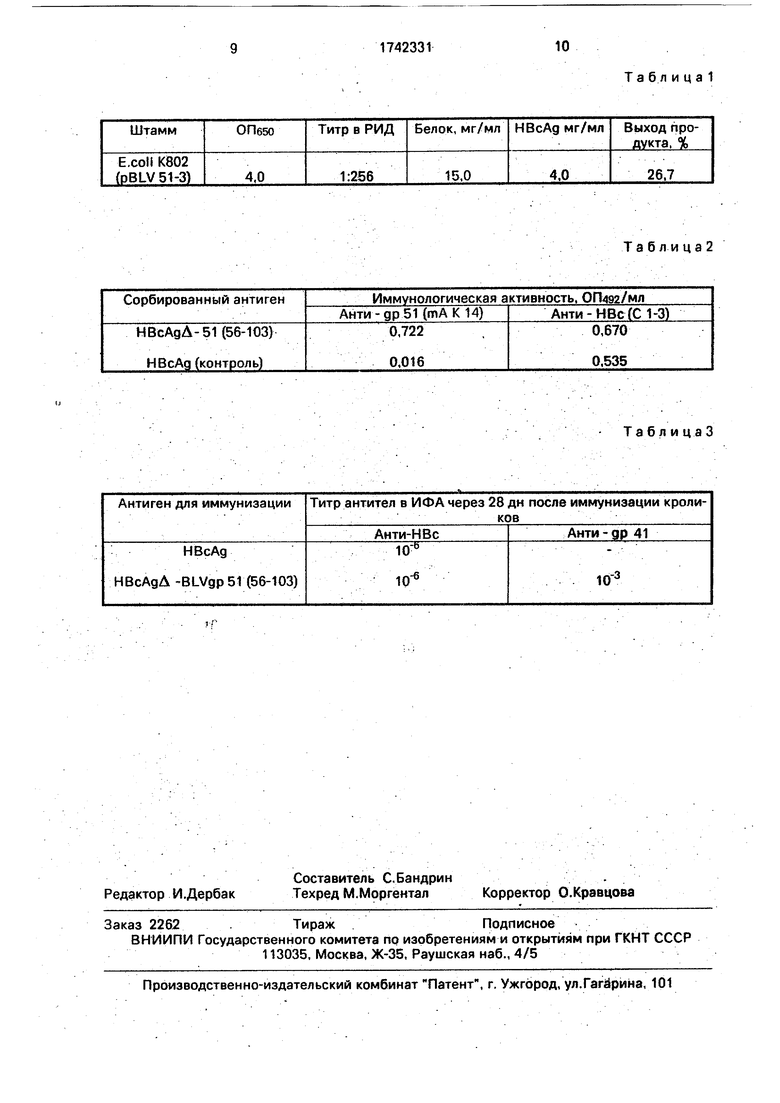
Изобретение относится к микробиологической и медицинской промышленности, генной и белковой инженерии и биотехнологии. Целью изобретения является получение рекомбинантных капсидных структур, представляющих собой кор-антиген вируса гепатита В, 39 С-аминокислот которого заменены на последовательность BLV gp 51 
Таблица2
ТаблицаЗ
| Клапанный регулятор для паровозов | 1919 |
|
SU103A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
1992-06-23—Публикация
1989-08-10—Подача