Изобретение относится к области защиты животных и растений и более конкретно к микробиологическому синтезу и выделению из биомассы авермектинов, используемых для производства антипаразитарных препаратов.
Предшествующий уровень техники
Известно, что актиномицет Streptomyces avermitilis при культивировании в присутствии источников углерода, азота и фосфора при постоянной аэрации продуцирует восемь близких по строению веществ, названных авермектинами, которые обладают резко выраженным антипаразитарным действием (патент GB 1573955, 1980). Все авермектины по химическому строению являются 16-членными макролидами и отличаются между собой заместителями у 5 и 26 атомов углеродного кольца. Индивидуальные авермектины, получившие обозначения A1a, А1b, А2а, А2b, B1a, B1b, В2a и В2b, имеют различную биологическую активность. Наиболее активными являются авермектины B1, особенно B1a.
Известен штамм Streptomyces avermitilis АТСС 31272, продуцирующий в среднем 500 мкг/мл авермектинов (патент US 4310519, 1982). Продуктивность штамма Streptomyces avermitilis ВНИИСХМ-51 (патент RU 2048250, 1995) составляет 700 мкг/мл. Штамм Streptomyces avermitilis ВHИИСХМ-54 продуцирует уже 1500 мкг/мл авермектинов (патент RU 2054483, 1996), причем содержание авермектина B1a достигает 35% и более. Штамм Streptomyces avermitilis CCM 4697, депонированный в Чешской коллекции микроорганизмов в Брно, продуцирует в среднем 2300 мкг/мл авермектинов при размахе изменчивости 2000-3000 мкг/мл.
Во всех приведенных случаях авермектины выделяют из мицелия экстракцией индивидуальным органическим растворителем, смешивающимся с водой, с последующим разделением, например хроматографическим, и получением отдельных авермектинов.
В патенте RU 2054483 (опубл. 1996) описан способ получения авермектинового комплекса экстракцией из высушенной мицелиальной массы с помощью водного раствора этанола с последующей очисткой вымораживанием, обработкой углем и ионообменными смолами. Из полученного спиртового раствора, содержащего 8 индивидуальных авермектинов, готовят различные лекарственные формы ветеринарного назначения.
Сущность изобретения
Предлагаемое изобретение позволяет выделять комплексы авермектинов с различным содержанием индивидуальных авермектинов, различающихся по биологической активности.
Для выделения авермектиновых комплексов различного компонентного состава используют сухую биомассу, полученную при выращивании продуцента в глубинных условиях на известных питательных средах.
Экстракцию авермектинов из биомассы осуществляют смесью, состоящей из воды и низко- и высококипящих растворителей, смешивающихся с водой в неограниченном соотношении. Под низкокипящими подразумеваются растворители с температурой кипения, не превышающей температуру кипения воды, например этиловый, метиловый и изопропиловый спирты или ацетон, в качестве высококипящих используют растворители с температурой кипения выше 150oС: полиэтиленгликоль с молекулярной массой 200 (ПЭГ-200), полиэтиленгликоль с молекулярной массой 400 (ПЭГ-400) или диметилсульфоксид (ДМСО) и др. Экстракты очищают от пигментов и неорганических примесей с помощью катионообменных и анионообменных смол. Затем отгоняют воду и низкокипящий растворитель. Путем отстаивания оставшейся части экстракта в высококипящем растворителе отделяют примеси липидного характера.
Далее из раствора можно в одном случае осадить при помощи воды сразу все присутствующие авермектины и получить суммарный авермектиновый комплекс. В другом случае в присутствии воды и этилового спирта осаждают только часть авермектинов с преимущественным содержанием авермектинов В1а и В1b. Маточный раствор после отделения части авермектинов смешивают с водой, осаждая оставшиеся авермектины.
При этом получают:
1) суммарный авермектиновый комплекс, получивший название аверсектин С, содержащий 8 авермектиновых компонентов в соотношении, %:
Авермектин А1а - 6-12
Авермектин A1b - Следы
Авермектин A2a - 15-25
Авермектин А2b - 2-4
Авермектин B1а - 30-40
Авермектин В1b - 2-12
Авермектин В2а - 14-24
Авермектин В2b - 1-2
или
2) комплекс, получивший название аверсектин В, содержащий в основном авермектины B1a и В1b, %:
Авермектин B1a - 76-83
Авермектин В1b - 12-16
Остальные авермектины - Следы
Авермектин В2а - 0,8-6
Авермектин A1а - 1-6
3) комплекс, названный аверсектином АВ, следующего состава, %:
Авермектин A1a - 4-10
Авермектин A1b - Следы
Авермектин А2а - 25-45
Авермектин А2b - 2,1-4,5
Авермектин В1a - 12-18
Авермектин B1b - 3-9
Авермектин B2a - 25-45
Авермектин В2b - 2,5-5,5
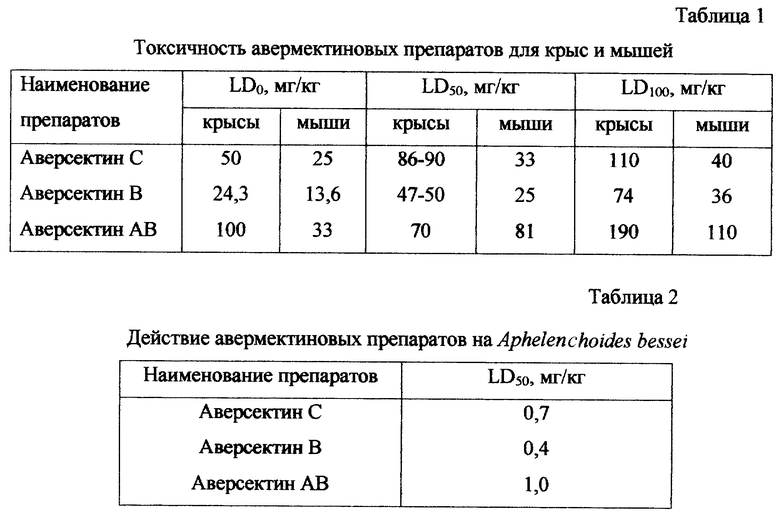
Биологические свойства полученных препаратов представлены в таблицах 1 и 2.
Пример 1
3,5 кг мицелия S. avermitilis ССМ 4697, высушенного на распылительной сушилке, экстрагировали в течение 1 часа при перемешивании и при комнатной температуре смесью 0,5 л ПЭГ-400 и 6,5 л 75% этанола. Осадок отделили фильтрованием на нутч-фильтре под вакуумом и промыли 0,8 л 96% этанола. Фильтрат и промывную жидкость объединили и получили 7,0 л спиртового экстракта, содержащего 500 мл ПЭГ-400 с концентрацией авермектинов 7,7 мг/мл, который затем пропустили последовательно через колонки с 400 г катионита КУ-2x8 в Н+-форме и анионита ЭДЭ-10П в ОН--форме. Колонки промыли 500 мл 96% этанола. Получили 7,15 л очищенного спиртового экстракта (авермектинов 7,5 мг/мл, выход 99,4%), отогнали спирт и воду на роторном испарителе при 55oС в вакууме. Остаток в колбе, нагретый до 65oС, поместили в делительную воронку для отделения липидной фракции.
Нижний слой объемом 580 мл (авермектинов 76 мг/мл) через 3,2 часа отделили и вылили в 1750 мл дистиллированной воды, нагретой до 40oС при интенсивном перемешивании. Смесь перемешивали в течение 3-5 часов для формирования осадка, основную часть надосадочной жидкости отделили декантированием, а остальную часть фильтрованием через стеклянный фильтр под вакуумом. Осадок на фильтре промыли 500 мл холодной дистиллированной воды и высушили в конвекционном потоке теплого воздуха.
Сухой осадок содержал 41 г аверсектина С.
Для оценки биологической активности аверсектина С для теплокровных изучали острую токсичность на белых беспородных крысах и мышах-самцах при однократном внутрижелудочном (пероральном) введении в форме водной суспензии на твине 21 с помощью желудочного зонда. Крысам массой 150-200 г препарат вводили в следующих дозах 50, 70, 84, 90, 110 и 150 мг/кг массы тела. Белым беспородным мышам массой 25-30 г аверсектин С вводили в дозах 7, 10, 25, 40, 50 и 60 мг/кг. Каждую дозу на крысах и мышах испытывали на 6 особях. Для расчета средней летальной дозы применяли метод пробит-анализа по Литчфилду и Уилкоксону (см. , например, Беленький М.Л. Элементы количественной оценки фармакологического эффекта. Л. : Госмедиздат, 1963, стр. 152). Результаты определения острой токсичности аверсектина С для крыс и мышей приведены в таблице 3.
Для оценки биологической активности аверсектина С для беспозвоночных изучали СК50 для Aphelenchoides bessei (рисовая нематода) по методу, описанному в патенте RU 2013053 на "Способ определения нематоцидной активности авермектинов", 1994. Установлено, что СК50 для Aphelenchoides bessei составляет 0,7 мкг/мл.
Пример 2
500 мл экстракта (экстрагент - смесь 75% спирта и ДМСО в соотношении 3: 1) с концентрацией аверсектина С 20 мг/мл очистили, как описано в примере 1, отогнали спирт и воду, как и в примере 1. Липидную фракцию на делительной воронке отделяли через 3 часа. Получили 120 мл нижнего слоя, содержащего ДМСО и аверсектин С - 56 мг/мл (всего 6,72 г аверсектина С - 67,2%).
Раствор аверсектина С в ДМСО вылили в 360 мл дистиллированной воды, перемешивали в течение 4 часов и выделили аверсектин С, как описано в примере 1. Получили 8,2 г сухого препарата, содержащего 79,0% (6,48 г) аверсектина С - выход 64,8%.
Далее провели оценку биологической активности аверсектина С для теплокровных и беспозвоночных так же, как в примере 1. Получены такие же результаты.
Пример 3
3,4 л экстракта, содержащего 3 л 75% спирта и 400 мл ПЭГ-200, очистили от пигментов и неорганических примесей, пропуская последовательно через колонки с ионообменными смолами КУ-2x8 и ЭДЭ-10П. Получили 3,2 л очищенного экстракта.
Экстракт сконцентрировали, как описано в примере 1. После отгонки спирта и воды остаток перенесли в делительную воронку. После отстаивания получили два слоя: нижний слой - ПЭГ-200, содержащий 40 г аверсектина С, и верхний - липидная фракция.
Нижний слой медленно при перемешивании вылили в 1,37 л воды. Выпавший осадок отделили на фильтре, промыли холодной дистиллированной водой и высушили в вакуум-сушильном шкафу. Получили 38,4 г аверсектина С следующего состава, %:
Авермектин
A1а - 11
A1b - Следы
A2a - 23
A2b - 2,1
В1а - 38
B1b - 3,1
В2а - 21
В2b - 1,8
Проверка биологической активности аверсектина С для теплокровных и беспозвоночных такая же, как в примере 1, показала те же результаты.
Получение комплекса с преобладанием авермектинов группы В (аверсектина В) и оценка его биологической активности.
Пример 4
К 200 мл раствора аверсектина С в ПЭГ-400, полученному, как в примере 2 (76 мг/мл аверсектина С), добавили порциями при постоянном перемешивании 400 мл 40% этанола. Смесь перемешивали еще 1 час и оставили для кристаллизации при комнатной температуре на 10 часов. Выпавшие кристаллы отфильтровали через стеклянный фильтр под вакуумом, кристаллы на фильтре промыли 50 мл охлажденного до 10oС 70% раствора спирта в воде и высушили при 60oС до постоянного веса в сушильном шкафу.
Получили 4,1 г аверсектина В с содержанием основных компонентов, %:
В1а - 82,2
В1b - 15,2
B2a - 0,8
A1a - 1,3
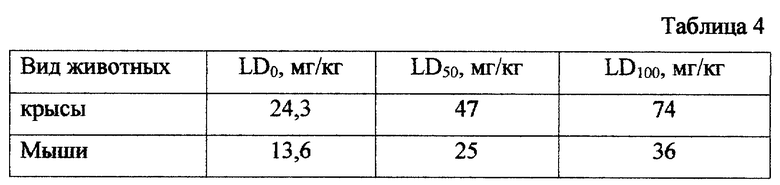
Далее провели оценку биологической активности, как это описано в примере 1. Получены следующие данные при однократном внутрижелудочном (пероральном) введении крысам и мышам-самцам (табл. 4).
При оценке биологической активности аверсектина B для беспозвоночных на примере Aphelenchoides bessei по методу, указанному в Примере 2, СК50 составил 0,4 мкг/мл.
Получение комплекса с преобладанием авермектинов группы А2 и В2 (аверсектина АВ) и оценка его биологической активности
Пример 5
Маточный раствор от кристаллизации аверсектина В и промывку (пример 4) упарили в вакууме. Остаток перенесли в делительную воронку. После отстаивания образовалось два слоя. Нижний слой - раствор аверсектина А в ПЭГ-400 вылили в 600 мл воды. Выпавший осадок отделили на фильтре и высушили. Получили 12,6 г препарата - Аверсектина АВ.
Состав препарата, %:
А1а - 7,1
A1b - Следы
A2a - 27,1
А2b - 2,1
В1а - 12,1
B1b - 3,7
В2а - 44,4
В2b - 3,5
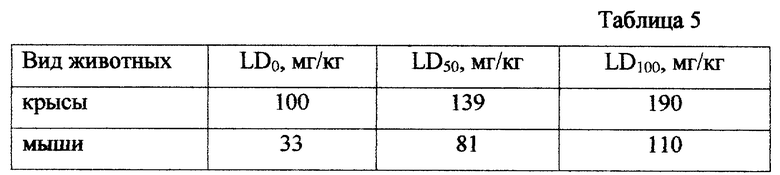
Оценку биологической активности проводили, как описано в примере 1. При изучении острой токсичности на крысах и мышах-самцах получены следующие результаты (табл.5).
CK50 для аверсектина АВ при использовании теста с Aphelenchoides bessei составила 1,0 мкг/мл.
Промышленная применимость
Получаемые аверсектины можно использовать для приготовления лекарственных средств для профилактики и лечения различных паразитарных заболеваний животных и человека.
Аверсектин С и аверсектин В имеют более длительный срок защитного действия. Аверсектин В медленнее выводится из организма, и срок его действия против эктопаразитов будет приблизительно на 7-10 дней дольше чем у аверсектина АВ.
Аверсектин С обеспечивает такой же срок защитного действия против эктопаразитов, как и аверсектин В, но срок ожидания (использования молочных и мясных продуктов после применения препарата) у него находится на уровне 14-21 дня, а у аверсектина В - на уровне 21-28 дней.
Аверсектин АВ обладает высокой активностью против личинок подкожного овода крупного рогатого скота. Он быстрее, чем аверсектин В и аверсектин С выводится из организма животных и не обнаруживается в молоке уже через 3 дня после введения, что позволяет его использовать для профилактики и лечения гиподерматоза на дойном стаде.
На основе аверсектинов могут быть изготовлены различные лекарственные формы (инъекционные, мазевые, оральные, порошкообразные, таблеточные, формы для орошения, пасты), предназначенные для лечения животных, а также жидкие, пастообразные и порошкообразные для борьбы с вредителями сельскохозяйственных культур. Эти препаративные формы на основе аверсектинов могут включать различные вспомогательные и формообразующие вещества.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРЕПАРАТ ДЛЯ ЗАЩИТЫ ЖИВОТНЫХ И РАСТЕНИЙ | 2000 |
|
RU2201244C2 |
| ПРОТИВОПАРАЗИТАРНЫЙ ВЕТЕРИНАРНЫЙ ИНЪЕКЦИОННЫЙ ПРЕПАРАТ | 2000 |
|
RU2201243C2 |
| ШТАММ АКТИНОМИЦЕТА STREPTOMYCES AVERMITILIS ССМ 4697 - ПРОДУЦЕНТ АВЕРМЕКТИНОВ | 1998 |
|
RU2156301C2 |
| СРЕДСТВО ДЛЯ БОРЬБЫ С СИНАНТРОПНЫМИ НАСЕКОМЫМИ | 1999 |
|
RU2159040C1 |
| ПРОТИВОПАРАЗИТАРНОЕ СРЕДСТВО | 1999 |
|
RU2160536C1 |
| КОМПОЗИЦИЯ ДЛЯ БОРЬБЫ С ВРЕДИТЕЛЯМИ РАСТЕНИЙ | 2000 |
|
RU2181244C2 |
| ШТАММ АКТИНОМИЦЕТА STREPTOMYCES AVERMITILIS - ПРОДУЦЕНТ АВЕРМЕКТИНОВ | 1993 |
|
RU2054483C1 |
| АНТИПАРАЗИТАРНЫЙ ПРЕПАРАТ С ИММУНОМОДУЛИРУЮЩИМИ СВОЙСТВАМИ | 2001 |
|
RU2212891C2 |
| ШТАММ STREPTOMYCES AVERMITILIS ФБМ 0004 - ПРОДУЦЕНТ ОЛИГОМИЦИНОВ | 1999 |
|
RU2160780C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕМАТОЦИДНОЙ АКТИВНОСТИ АВЕРМЕКТИНОВ | 1991 |
|
RU2013053C1 |

Изобретение относится к биотехнологии, а именно к микробиологическому синтезу и выделению из биомассы актиномицета Streptomyces avermitilis авермектинов, используемых для антипаразитарных препаратов. Способ включает экстракцию авермектинов из биомассы S. avermitilis, очистку экстракта, отделение липидной фракции и выделение целевого продукта. Экстракцию авермектинов из биомассы осуществляют смесью, состоящей из воды и низко- и высококипящих растворителей, смешивающихся с водой в неограниченном соотношении. Предложенный способ позволяет выделять комплексы авермектинов с различным содержанием индивидуальных авермектинов, активных в биологическом отношении. 4 з.п. ф-лы, 5 табл.
Авермектин А1а - 6-12
Авермектин A1b - Следы
Авермектин A2a - 15-25
Авермектин A2b - 2-4
Авермектин В1а - 30-40
Авермектин В1b - 2-12
Авермектин В2а - 4-24
Авермектин В2b - 1-2
4. Способ по п. 1 или 2, отличающийся тем, что из раствора в высококипящем растворителе после добавления водного раствора низкокипящего растворителя выделяют авермектиновый комплекс со следующим составом компонентов, %:
Авермектин В1а - 76-83
Авермектин B1b - 12-16
Авермектин В2а - 0,8-6
Авермектин А1а - 1-6
Остальные авермектины - Следы
5. Способ по п. 4, отличающийся тем, что из раствора в высококипящем растворителе, оставшегося после отделения авермектина В, выделяют осаждением водой авермектиновый комплекс со следующим составом компонентов, %:
Авермектин А1а - 4-10
Авермектин А1b - Следы
Авермектин А2а - 25-45
Авермектин А2b - 2,1-4,5
Авермектин В1а - 12-18
Авермектин В1b - 3-9
Авермектин В2а - 25-45
Авермектин В2b - 2,5-5,5
| СПОСОБ ПОЛУЧЕНИЯ АВЕРМЕКТИНОВОГО КОМПЛЕКСА И ПРЕПАРАТ АВЕРМЕКТИНОВОГО КОМПЛЕКСА ДЛЯ ПРОФИЛАКТИКИ И КОМПЛЕКСНОГО ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ВЫЗВАННЫХ ЭНДО- И ЭКТОПАРАЗИТАМИ ЖИВОТНЫХ | 1995 |
|
RU2054848C1 |
| US 4429042, 31.01.1984 | |||
| US 5576199, 19.11.1996 | |||
| US 5576200, 19.11.1997 | |||
| EP 0572056, 01.12.1993 | |||
| СПОСОБ ПОЛУЧЕНИЯ АВЕРМЕКТИНА | 1994 |
|
RU2109057C1 |
| ШТАММ СТРЕПТОМИЦЕТОВ ДЛЯ ПРОДУЦИРОВАНИЯ АНТИПАРАЗИТАРНЫХ СОЕДИНЕНИЙ И СПОСОБЫ ПРОДУЦИРОВАНИЯ ЭТИХ СОЕДИНЕНИЙ | 1993 |
|
RU2125609C1 |
| СПОСОБ ПОЛУЧЕНИЯ АВЕРМЕКТИНА И ШТАММЫ STREPTOMYCES AVERMITILIS - ПРОДУЦЕНТЫ АВЕРМЕКТИНА | 1988 |
|
RU2096462C1 |
Авторы
Даты
2002-05-10—Публикация
2000-01-31—Подача