Изобретение относится к области получения новых тетранитрилов гетероциклических тетракарбоновых кислот, которые могут быть использованы для получения не описанных ранее полигексазоцикланов - флуорофоров, бифлуорофоров, трифлуорофоров. Такие полигексазоцикланы перспективны для использования в качестве активных сред жидких и твердых лазеров, сцинтилляторов, особенно для индикации жесткого излучения, для трансформации коротковолнового излучения в длинноволновое при передаче информации по волоконно-оптическим линиям связи, для увеличения мощности солнечных батарей, для защиты ценных бумаг, для изготовления рекламных щитов и т.д.
Известно соединение - пиромеллитнитрил, которое совместно с незамещеным родамином используется для получения флуоресцирующих полигексазоцикланов (Силинг С.А., Феофанов Б.Н., Барашков Н.Н. и др. Полигексазоцикланы на основе гетероциклических диаминов. //Высокомолек. соед. Б. 1988, Т. 30, 4. С. 286-291).
Полученный полигексазоциклан обладает следующими показателями: полоса излучения 532 нм при возбуждении в полосу 312 нм.
Задачей, решаемой настоящим изобретением, является получение новых гетероциклических тетракарбонитрилов.
Заявляются гетероциклические тетракарбонитрилы общей формулы: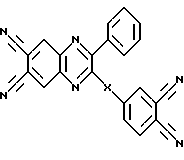
где X = σ-связь,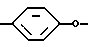
К заявляемым соединениям относятся 2-(3,4-дицианофенил)-3-фенил-6,7-хиноксалиндикарбонитрил (I):
2-[4-(3,4-дицианофенокси)фенил] -3-фенил-6,7-хиноксалиндикарбонитрил (II):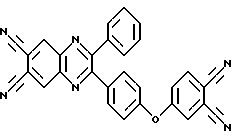
Данные соединения получают реакцией конденсации 4,5-диаминофталонитрила с соответствующим дикетоном по схеме:
Реакцию проводят в среде уксусной кислоты при температуре кипения в течение 1...1,5 часов.
Изобретение иллюстрируется следующими примерами:
Пример 1. В колбу, снабженную обратным холодильником, последовательно загружают 30 мл уксусной кислоты, 1,6 г (0,01 моль) 4,5-диаминофталонитрила, 2,6 г (0,01 моль) 4-(2-оксо-2-фенилацетил)фталонитрила. Реакционную смесь выдерживают при кипении в течение 1,5 часов. Затем реакционную массу выливают в 100 мл воды, отфильтровывают образовавшийся осадок, промывают его 50 мл воды и кристаллизуют из ДМФА.
Получают 3,25 г (85,1% от теории) 2-(3,4-дицианофенил)-3-фенил-6,7-хиноксалиндикарбонитрила (I) - белого кристаллического порошка с т.пл. >300oС.
Найдено, %: С 75,35; Н 2,65; N 21,93
Вычислено, %: С 75,38; Н 2,64; N 21,98 C24H10N6
1H-ЯМР ([2Н6] ДМСО): δ, м.д.: 9,00 (s, 2H), 8,20 (s, 1H), 8,10 (d, 1H, J=7,9 Гц), 7,95 (d, 1H, J=8 Гц), 7,55 (m, 2H), 7,45 (m, 2H)
Пример 2. Реакцию проводят аналогично примеру 1, за исключением того, что в качестве реагента (4-(2-оксо-2-фенилацетил)фталонитрила) соответственно используются эквимолярное количество 4-[4-(2-оксо-2-фенилацетил)фенокси] фталонитрила. Условия и результаты проведенных синтезов приведены в табл. 1.
Пример 3. Конденсация 2-(3,4-дицианофенил)-3-фенил-6,7-хиноксалиндикарбонитрила с родамином 123. В колбу, снабженной мешалкой, термометром, обратным холодильником и капилляром для ввода аргона загружают 3,2 г (0,01 моль) 2-(3,4-дицианофенил)-3-фенил-6,7-хиноксалиндикарбонитрила, 3,8 г (0,01 моль) родамина 123 и 10 г фенола. Полученную смесь медленно нагревают при перемешивании до 175. .. 185oС. Образовавшийся расплав выдерживают при перемешивании в токе аргона до прекращения выделения аммиака. После окончания реакции реакционную смесь выливают в 20 мл этанола, выпавший осадок отфильтровывают, промывают 3 мл этанола и сушат при Т=60oС в течение 2 часов, затем в вакууме над Р2O5. Получают 9,9 г (95% от теории) полигексазоциклана.
Найдено, %: С 75,96; Н 4,09; N 10,71
Вычислено, %: С 75,99; Н 4,07; N 10,74 (C66H42N8O6)n
В ИК-спектре полигексазоциклана отсутствует полоса 2220 см-1 -C≡N, присутствует полоса 680 см-1-C=N.
Структурная формула полигексазоциклана, полученного на основе 2-(3,4-дицианофенил)-3-фенил-6,7-хиноксалиндикарбонитрила и родамина 123:
Полигексазоциклан, полученный на 2-(3,4-дицианофенил)-3-фенил-6,7-хиноксалиндикарбонитрила и родамина 123 имеет следующие спектральные характеристики: максимум спектра излучения - 424 нм при максимумах спектра поглощения - 280 и 337 нм.
Пример 4. Реакцию проводят аналогично примеру 3, за исключением того, что вместо дифталонитрила I используются эквимолярное количество дифталонитрила II.
Условия и результаты проведенных синтезов, а так же спектральные характеристики полученного полигексазоциклана приведены в табл.2.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2,2'-ДИФЕНИЛ-3,3'-(N-ФЕНИЛЕН)БИС(6,7-ХИНОКСАЛИНДИКАРБОНИТРИЛ) | 2001 |
|
RU2200735C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2004 |
|
RU2266289C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2003 |
|
RU2238276C1 |
| 2,3,7,8-ФЕНОКСАТИИНТЕТРАКАРБОНИТРИЛ | 2000 |
|
RU2165417C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2204563C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2183627C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2183628C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2185378C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2004 |
|
RU2266286C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2200733C2 |


Изобретение относится к новым гетероциклическим тетракарбонитрилам общей формулы I
где X = σ-связь,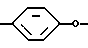
Соединения могут быть использованы для получения полигексазоцикланов - флуорофоров, бифлуорофоров, трифлуорофоров. Такие полигексазоцикланы перспективны для использования в качестве активных сред жидких и твердых лазеров, сцинтилляторов, особенно для индикации жесткого излучения, для трансформации коротковолнового излучения в длинноволновое при передаче информации по волоконно-оптическим линиям связи, для увеличения мощности солнечных батарей, для защиты ценных бумаг, для изготовления рекламных щитов. 2 табл.
Гетероциклические тетракарбонитрилы общей формулы
где Х= σ-связь, 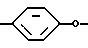
| 2,3,7,8-ТИАНТРЕНТЕТРАКАРБОНИТРИЛ | 2000 |
|
RU2165418C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2000 |
|
RU2165929C1 |
| 4,4'-(ОКСИБИС(N-ФЕНИЛЕНТИО))ДИФТАЛОНИТРИЛ | 1999 |
|
RU2164513C1 |
Авторы
Даты
2002-07-20—Публикация
2001-10-03—Подача