Изобретение относится к области синтеза биологически активных веществ, конкретно - α-токоферола (витамина Е).
α-Токоферол входит в состав витаминов группы Е и является основным липофильным антиоксидантом биологических мембран млекопитающих. Недостаток витамина Е вызывает бесплодие, дистрофию мышц и дегенерацию нервных клеток.
Мировое производство витамина Е составляет 15000-20000 тонн в год. Наиболее крупные фирмы-производители: BASF (Германия), Rhone-Poulene (Франция), Eisai (Япония) и Roche (Швейцария) [T. Netscher, Chimia 50, 11, 563-567 (1996)].
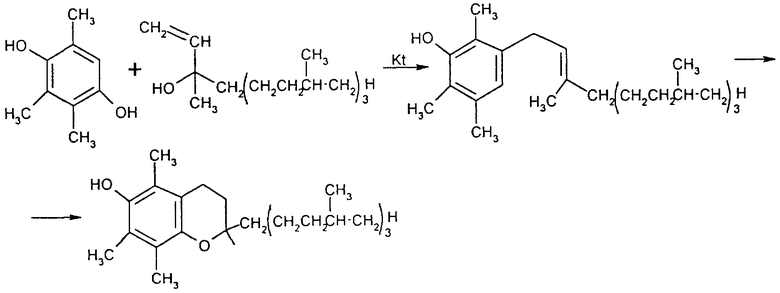
Среди различных форм α-токоферола практическое значение имеет полностью рацемический α-токоферол (синтетический витамин Е). Впервые он был синтезирован Карером с сотрудниками из триметил-n-гидрохинона и фитилбромида в среде бензола или петролейного эфира в присутствии хлористого цинка при 80oС в токе азота. Наиболее известный сегодня и практически значимый метод синтеза α-токоферола основан на кислотно-конденсируемой конденсации рацемического изофитола с триметилгидрохиноном. Реакция протекает по схеме (см. в конце описания).
В качестве катализаторов реакции используют фосфорный ангидрид, муравьиную или уксусную кислоты, хлористый цинк или эфират трехфтористого бора [В. М. Березовский. Химия витаминов.- М.: Пищевая промышленность, 1973, с. 271].
Недостатки использования указанных катализаторов:
1. Дезактивация катализаторов под действием воды, образующейся в процессе реакции.
2. Высокая чувствительность катализаторов к действию влаги и кислорода воздуха и их низкая стабильность при хранении.
3. Необходимость разложения катализаторов водой после завершения реакции и применение больших объемов органических растворителей для проведения процесса экстракции.
Известны способы проведения реакции в условиях гетерогенного катализа с применением в качестве катализатора ионообменной смолы - амберлит-15 [Moroe Tatsuo, Hattori Satohiko, Komatsu Akira, Matsui Takeshi, Kurihara Haruki, пат. США 3459773; С.А. 71, 91307 (1969)].
Кроме того, в качестве катализатора применяют алюмосиликат АШНЦ-3 [Е.И. Захарова, К. А.-В. Шауипов, В.В. Чудинова, С.М. Алексеев, Р.П. Евстигнеева. Биоорганическая химия, 1989, 15, 19, 1268-1273; К.И. Матвеев, Е.Г. Жижина, В. Ф. Одяков. Химическая промышленность, 1996, 3, 29-35], цеолитсодержащие алюмосиликаты АШНЦ-3П и наиболее близкий к предлагаемому изобретению - "Цеокар-2". Реакцию проводят при кипячении в нонане с непрерывным удалением воды [А. А. Щеголев, И.К. Сарычева, Р.П. Евстигнеева. Деп. ВИНИТИ 4779-82 (1982); РЖХим, 1982, 23Е131].
Максимально достижимый выход α-токоферола в известных методах не превышает 82%.
Авторами предлагается новый способ получения α-токоферола, при котором используется катализатор "Цеокар-10" [ТУ 38.1011372-00] - шариковый катализатор крекинга нефтяных фракций, в состав которого в качестве активного компонента (10 мас. %) входит высокомодульный цеолит Y (ОАО "Салаватнефтеоргсинтез").
Сущность изобретения состоит в нагревании в углеводородном или ароматическом растворителях (лучше в нонане) триметилгидрохинона и изофитола, взятых в мольном соотношении 1: 1,1-1: 2 (лучше 1:2) в присутствии катализатора "Цеокар-10". Выход α-токоферола 98-100%, в отличие от максимально достижимых в известных методах не превышающих 82%. [А.А. Щеголев, И.К. Сарычева, Р.П. Евстигнеева. Деп. ВИНИТИ 4779-82 (1982); РЖХим, 1982, 23Е131].
Изобретение поясняется следующими примерами:
Пример 1. К кипящей суспензии 0.2 г (1.32 ммоля) триметилгидрохинона, 0.45 г мелко размельченного катализатора "Цеокар-10" в 6 мл абсолютного нонана, в токе аргона медленно прибавили 0.782 г (2.64 ммоля) изофитола. Реакционную смесь кипятили 5 часов, затем охладили, отфильтровали катализатор, фильтрат упарили. Остаток хроматографировали на колонке с силикагелем. Элюированием гексаном выделили неполярные примеси, затем смесью (10:1) гексан-диэтиловый эфир элюировали α-токоферол. После упаривания элюента получили 0.558 г (98.2%) α-токоферола, чистота ≥97%, nD 24 1,5072 (ср. литерат. [Kirk-Othmer Encyclopedia of Chemical Tecnology Third Edition, 1984, vol. 24, Wiley-Interscience Publication]).
Спектр УФ, λmax,нм(ε): 295 (3800).
Спектр ЯМР 1Н (δ,м.д.): 0.90 м (12 Н, СН3), 1.0-1.9 м (26 Н, СН3-2, СН2, СН), 2.10 с и 2.17 с (9 Н, СН3-Аr), 2.61 т (2 Н, C4H2, J=6.7 Гц), 4.3 с (1 Н, OН).
Спектр ЯМР 13С (δ,м.д.): 11.26, 11.75 и 12.19 (СН3-Аr), 19.67 и 19.75 (СН3-4', СН3-8'), 20.79 и 21.08 (С4), 22.62 и 22.70 (СН3-12', С13), 24.46 и 24.81 (С2', С6', С10'), 27.99 (С12'), 31.60 (С3), 32.75 и 32.83 (С4', С8'), 37.32 и 37.48 (С3', С5', С7', С9'), 39.42 (С11'), 39.91 и 39.97 (С1'), 74.55 (С2), 116.38(C5), 118.51 (С10), 121.05 (С8), 122.64 (С7), 144.57 (С9), 145.63 (С6), (ср. литерат. [ М. Matsuo. S. Wrano // Tetrahedron, 1976, vol. 32, р. 229-231]).
Пример 2. Осуществлено, как описано в примере 1, но реакцию проводят при кипячении в толуоле в течение 6 часов. Выход α-токоферола 0.562 г (99%), чистота ≥97%.
Пример 3. Осуществлено, как описано в примере 1, но реакцию проводят при кипячении в гептане в течение 10 часов. Выход α-токоферола 0.56 г (98%), чистота ≥97%.
Пример 4. Осуществлено, как описано в примере 1, но реакцию проводят при мольном соотношении триметилгидрохинона и изофитола 1:1,1. Выход α-токоферола 0.382 г (67.5%), чистота ≥97%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ИЗОПРЕНОИДНЫХ ПРОИЗВОДНЫХ 2,3,5-ТРИМЕТИЛ-1,4-БЕНЗОХИНОНА | 2000 |
|
RU2197469C2 |
| СПОСОБ ПОЛУЧЕНИЯ (6R,10R)-6,10,14-ТРИМЕТИЛПЕНТАДЕКАН-2-ОНА (ФИТОНА) | 2001 |
|
RU2197465C2 |
| СПОСОБ ПОЛУЧЕНИЯ П-ЦИМОЛА (П-МЕТИЛИЗОПРОПИЛБЕНЗОЛА) | 2001 |
|
RU2200144C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ E3, E8-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]ДЕКАНА И E3, E9-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]ДЕКАНА | 2000 |
|
RU2188813C2 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АЛКОКСИПЕНТАНОНОВ-2 | 1999 |
|
RU2171797C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОР-3-АЦЕТИЛ- И 1,3-ДИХЛОР-5-АЦЕТИЛАДАМАНТАНОВ | 2000 |
|
RU2197467C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-3-(ТРИАЛКИЛСИЛИЛ)АЛЮМАЦИКЛОПЕНТАНОВ | 1999 |
|
RU2157812C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2-(ТРИАЛКИЛСИЛИЛ)АЛЮМАЦИКЛОПРОПАНОВ | 1999 |
|
RU2162851C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-ЭТИЛ-3,3,6-ТРИАЛКИЛЦИКЛОГЕПТАОКСАЛАНОВ И 1-ЭТИЛ-3,3,5-ТРИАЛКИЛЦИКЛОГЕПТАОКСАЛАНОВ | 2001 |
|
RU2197497C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(ДИАЛКИЛАМИНО)-2-(ТРИАЛКИЛСИЛИЛ) АЛЮМАЦИКЛОПРОПАНОВ | 1999 |
|
RU2163907C2 |
Изобретение относится к усовершенствованному способу получения α-токоферола (витамина Е), который является липофильным антиоксидантом биологических мембран млекопитающих. α-Токоферол получают конденсацией триметилгидрохинона с рацемическим изофитолом в условиях гетерогенного катализа в присутствии цеолитсодержащего алюмосиликата "Цеокар-10". Процесс проводят при кипячении в углеводородных или ароматических растворителях (толуол, гептан, нонан) при мольном соотношении триметилгидрохинон : изофитол, равном 1: 2, в течение 5-10 ч. Технический результат - повышение выхода целевого продукта до количественного за счет использования "Цеокара-10".
Способ получения α-токоферола (витамина Е) конденсацией триметилгидрохинона с изофитолом в присутствии цеолитсодержащего алюмосиликатного катализатора в среде органического растворителя, отличающийся тем, что в качестве катализатора используют "Цеокар-10" и процесс проводят в среде ароматического или углеводородного растворителя при мольном соотношении триметилгидрохинон : изофитол, равном 1: 2, в течение 5-10 ч.
| Щеголев А.А | |||
| и др | |||
| РЖХим | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| US 3459773 А, 05.08.1969 | |||
| Захарова Е.И | |||
| и др | |||
| Биоорганическая химия | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Электрический трубочный плавкий предохранитель | 1923 |
|
SU1268A1 |
| СПОСОБ ПОЛУЧЕНИЯ DL-АЛЬФА-ТОКОФЕРОЛА ИЛИ ЕГО АЦЕТАТА | 1994 |
|
RU2098416C1 |
Авторы
Даты
2002-07-27—Публикация
2000-06-28—Подача