Изобретение относится к медицине, а именно к фтизиатрии, и может быть использовано при лечении туберкулеза.
В настоящее время основным способом лечения туберкулеза является химиотерапия. Актуальная проблема лечения туберкулеза - сравнительно ограниченный набор эффективных противотуберкулезных препаратов (ПТП) и быстрое развитие устойчивых к их действию форм микобактерий туберкулеза (МБТ). Поэтому постоянно идет поиск новых ПТП и новых способов лечения туберкулеза (патенты РФ 2080114, A 61 K 31/15, 31/295, 31/455; 2088231, A 61 K 31/505; 2099056, A 61 K 31/505; 2153339, A 61 K 31/513, A 61 P 31/06; 2165761, A 61 K 31/513, A 61 P 31/06).
В стандартной комбинированной химиотерапии туберкулеза в качестве основного и наиболее эффективного препарата используется изониазид - гидразид изоникотиновой кислоты. Поэтому за прототип принят способ лечения туберкулеза с помощью химиотерапии, включающей изониазид (М.Д. Машковский. Лекарственные средства. - М., Медицина. - 1988. - Т.2. - С.315-316). В этом способе в качестве лекарственного препарата используют изониазид в дозах 6-15 мг/кг в сутки, обычно 10 мг/кг. При этом сроки лечения составляют не менее 6-ти месяцев. Применение изониазида бывает ограничено наличием устойчивых форм МБТ к этому препарату, что снижает эффективность лечения и увеличивает его длительность. Известна также высокая токсичность изониазида, приводящая к поражениям печени и периферической нервной системы.
Задача, решаемая заявляемым изобретением, - повышение эффективности лечения туберкулеза, возможность снижения токсического действия изониазида.
Технический результат - уменьшение или исчезновение специфических патологических изменений внутренних органов животных в результате лечения; уменьшение количества положительных посевов МБТ; сокращение сроков лечения за счет ускорения абациллирования и регрессии туберкулезных изменений в легких; излечение туберкулеза, резистентного к изониазиду; возможность использования минимальных доз изониазида.
Для достижения этого технического результата в способе лечения туберкулеза с помощью химиотерапии, включающей изониазид, авторы предлагают дополнительно вводить эффективное и безопасное количество 2,4-диоксо-5-фторпиримидина (фторурацила). Введение фторурацила авторы предлагают проводить в дозе 0,1÷2,5 мг/кг ежедневно не менее 2-х месяцев. Вводить препараты можно одновременно или последовательно. Также авторы предлагают вводить изониазид и фторурацил в виде их смеси. Введение изониазида и фторурацила можно проводить внутривенно.
Экспериментальным путем авторами установлено, что лечение туберкулеза комбинацией изониазида и фторурацила более эффективно, чем лечение одним из этих препаратов, и что введение дополнительно к изониазиду фторурацила в дозе 0,1÷2,5 мг/кг в течение 2-х месяцев является эффективным и безопасным. Использование комбинации изониазида и фторурацила в терапии туберкулеза приводит к тому, что по сравнению с прототипом:
1) после проведенного лечения в органах животных, зараженных как лабораторным, так и клиническим штаммами МБТ, уменьшены или отсутствуют специфические патологические изменения и положительные посевы МБТ; выздоровление наступает в более короткие сроки;
2) у больных с исходно прогрессирующим течением туберкулеза легких, резистентного к изониазиду, в сроки от 1 до 2 месяцев наблюдаются следующие изменения: регресс клинической симптоматики заболевания, абациллирование или снижение интенсивности выделения МБТ, рассасывание инфильтративных изменений, закрытие полостей распада в легких или отграничение процесса в виде формирования фиброза или плотных очагов, за счет чего сокращаются сроки лечения и наступает выздоровление;
3) при сохранении эффективности лечения можно использовать минимальные дозы изониазида (5 мг/кг), что уменьшает его побочное токсическое действие.
Применение фторурацила в дозах, меньших 0,1 мг/кг, не привело к существенным отличиям от прототипа, т. е. не является эффективным, а в дозах, превышающих 2,5 мг/кг, сопровождалось токсическими поражениями организма животных. Лечение менее 2-х месяцев не приводит к выздоровлению. Введение изониазида и фторурацила в виде их смеси удобнее, а при внутривенном введении - еще и менее травматично. Смесь препаратов может быть приготовлена, например, путем смешения соответствующих количеств официнальных растворов изониазида и фторурацила. Острая токсичность ЛД50 смеси, определенная по методу Кербера на 80 белых мышах, составила 267,75 мг/кг, что меньше, чем ЛД50 изониазида (188,4 мг/кг по патенту РФ 2153878, 2000). Внутривенное введение препаратов более эффективно, так как позволяет достичь максимальной концентрации препаратов в крови.
Известно, что фторурацил относится к антиметаболической группе цитостатических средств и применяется при лечении рака в суточных дозах 10-15 мг/кг короткими курсами до 10 дней (М.Д. Машковский. Лекарственные средства. - М. , - Медицина, 1988. - Т. 2. - С. 455). Туберкулостатические свойства фторурацила впервые были обнаружены нами в опытах in vitro (патент РФ 2153339), а его противотуберкулезное действие - в эксперименте in vivo (патент РФ 2165761), где было показано, что фторурацил в дозах 1-2 мг/кг по противотуберкулезному действию не уступает изониазиду и может использоваться для лечения экспериментального туберкулеза в течение длительного времени. Однако в эксперименте (патент РФ 2165761) было установлено, что за время проведенного лечения только одним препаратом (как изониазидом, так и фторурацилом) не обеспечивается элиминация МБТ, у животных сохраняются патологические туберкулезные изменения внутренних органов, что свидетельствует о недостаточной эффективности проведенного лечения каждым из этих препаратов по отдельности.
Известно, что комбинация нескольких туберкулостатических средств не всегда целесообразна из-за взаимного увеличения их токсичности, а также из-за возможной несовместимости и особенностями их воздействия на биологический объект. Эксперименты, проведенные авторами in vitro, показали, что изониазид и фторурацил совместимы при смешивании, при этом туберкулостатическая активность смеси, определенная методом вертикальной диффузии, резко возрастает. Эта смесь оказала туберкулостатическое действие как на лабораторный H37Rv, так и на клинический изониазидоустойчивый штаммы МБТ. Также было установлено, что совместное воздействие изониазида и фторурацила усиливает их противотуберкулезную активность и повышает эффективность лечения туберкулеза, что доказано проведенным хроническим экспериментом при лечении туберкулеза, вызванного лабораторным H37Rv (пример 1) и клиническим изониазидоустойчивым (пример 2) штаммами МБТ у морских свинок, и при клиническом испытании (пример 3).
На фиг. 1-3 представлены результаты исследования легких больной инфильтративным туберкулезом:
Фиг. 1 - при поступлении в клинику: а) рентгенограмма грудной клетки; б) томограмма легкого; в) КТ легкого.
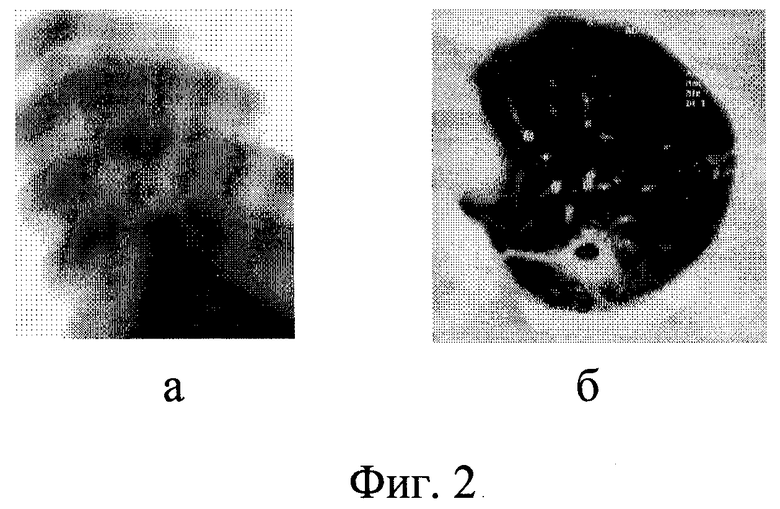
Фиг. 2 - после двухмесячного лечения: а) томограмма легкого; б) КТ легкого.
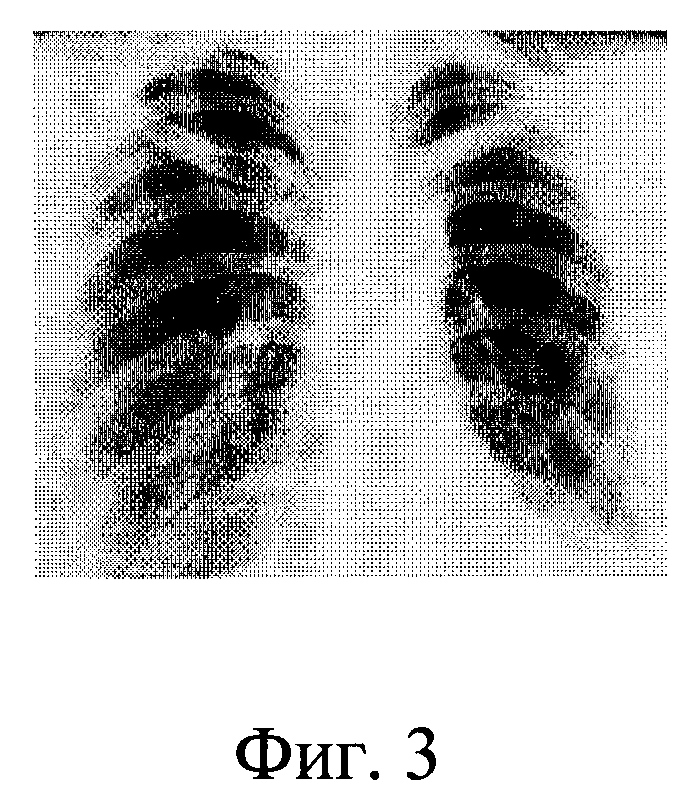
Фиг.3 - рентгенограмма грудной клетки через месяц после операции.
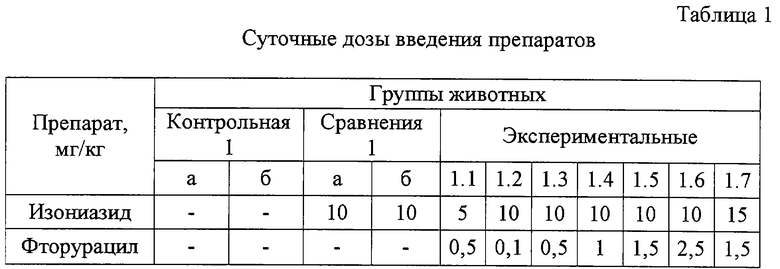
Пример 1. Проведены две серии экспериментов (а и б) продолжительностью по 2 месяца на морских свинках, самцах и самках, массой от 200 до 400 г с формированием однородных групп по массе и полу. Каждая группа состояла из 7 животных, всего 77 животных. Моделирование заболевания проводили путем подкожной инъекции культуры МБТ (лабораторный штамм H37Rv) в дозе 0,025 мг/кг в объеме 0,5 мл в правую паховую область. Лечение начинали через 2 недели после заражения. По группам животные были разделены следующим образом: контрольные группы 1а и 1б - без лечения; группы сравнения 1а и 1б - животные, которым ежедневно внутримышечно вводили изониазид в дозе 10 мг/кг; экспериментальные группы 1.1-1.7 - животные, получавшие ежедневно внутримышечно фторурацил и изониазид как в смеси препаратов, так и раздельно в нижеперечисленных дозах (табл.1).
Методы исследования: прижизненная оценка течения туберкулеза у животных (изменение массы тела в конце эксперимента - табл.2); биохимические и клинические исследования крови; патоморфологические исследования внутренних органов; микробиологическое исследование гомогенатов органов на наличие МБТ методом посева (табл.3).
Результаты исследования. В контрольных группах к окончанию эксперимента пало более 50% животных. В зоне заражения имелись обширные (до 3 см в диаметре) язвы, выполненные некротической тканью со свищами к паховым лимфоузлам. По физическому развитию животные значительно отставали от животных остальных групп (табл. 2). Анализы крови свидетельствовали о наличии анемии, увеличении скорости оседания эритроцитов (СОЭ), резко выраженных изменениях формулы в виде значительного роста числа гранулоцитов и моноцитов, увеличении уровня аспартатаминотрансферазы. При патоморфологических исследованиях у всех животных контрольных групп были обнаружены множественные туберкулезные поражения внутренних органов с многочисленными очагами казеозного некроза. При микробиологическом исследовании гомогенатов внутренних органов во всех случаях был получен рост МБТ (табл.3). Таким образом, у всех животных контрольных групп был выявлен генерализованный туберкулез с характерными лабораторными и патоморфологическими изменениями, МБТ (+).
Все животные, получавшие лечение, выжили. Изменения лабораторных показателей у них не имели существенных различий и не выходили за пределы возрастной нормы за исключением животных групп сравнения 1 и экспериментальной группы 1.6, у которых была выявлена умеренная анемия. Введение изониазида и фторурацила в виде их смеси или раздельно не оказало влияния на результаты лечения.
В конце эксперимента животные групп сравнения 1а и 1б, получавшие только изониазид, по массе превосходили животных контрольных групп 1а и 1б (табл. 2). При исследовании крови в группах сравнения был обнаружен низкий уровень гемоглобина, высокая СОЭ и умеренная лейкопения с соответственным уменьшением числа гранулоцитов и лимфоцитов. При патоморфологическом исследовании в легких были обнаружены единичные, субплеврально расположенные очаги лимфоидной инфильтрации, в двух случаях - пневмонические очаги. В ткани селезенки найдены лимфоидные гранулемы, в интраторакальных и периферических лимофоузлах - очаги крупнопетлистого склероза. При микробиологическом исследовании гомогенатов внутренних органов во всех случаях был получен рост МБТ. Таким образом, у животных групп сравнения 1 через два месяца лечения МБТ (+) и сохранялись признаки заболевания в виде анемии и патоморфологических изменений внутренних органов.
Лечение туберкулеза комбинацией изониазида в дозах 5÷15 мг/кг и фторурацила в дозах 0,1÷2,5 мг/кг (экспериментальные группы 1.1-1.7) в течение 2-х месяцев оказалось более эффективным, чем лечение только изониазидом (группы сравнения 1а и 1б):
- снижено количество положительных посевов МБТ (3 из 7, группа 1.1), отсутствует рост МБТ в гомогенатах внутренних органов (группы 1.2-1.7), см. табл.3;
- уменьшены специфические патологические изменения внутренних органов (группы 1.1; 1.2);
- в группах 1.3-1.7 после проведенного лечения при патоморфологическом исследовании обнаружены лишь остаточные изменения перенесенного генерализованного туберкулеза.
Прирост массы тела животных как экспериментальных групп, так и групп сравнения (табл.2) значительно превышал этот показатель у животных контрольных групп, что свидетельствует об эффективности проведенного лечения. Снижение прироста массы животных группы 1.6 по сравнению с другими животными этой серии, получавшими лечение, вероятно, обусловлено начальными проявлениями токсического действия фторурацила, тем не менее проведенное лечение более эффективно, чем в группе сравнения 1 (табл.3).
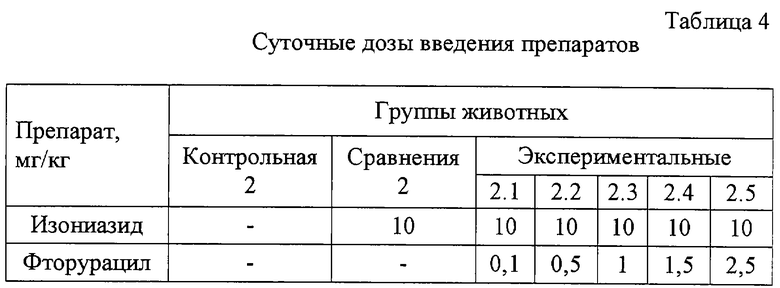
Пример 2. Эксперимент проведен на морских свинках, самцах и самках, массой от 300 до 400 г с формированием однородных групп по массе и полу. Каждая группа состояла из 7 животных, всего 49 животных. Продолжительность эксперимента - три месяца. Моделирование заболевания у животных всех групп проводили путем подкожной инъекции культуры МБТ (клинический изониазидоустойчивый штамм, выделенный из мокроты больного) в дозе 0,025 мг/кг в объеме 0,5 мл в правую паховую область. Штамм идентифицирован и установлена его лекарственная устойчивость к изониазиду в концентрации 100 мкг/мл. Лечение начинали через 2 недели после заражения. По группам животные были разделены следующим образом. Контрольная группа 2 - без лечения; группа сравнения 2 - животные, которым ежедневно внутримышечно вводили изониазид в дозе 10 мг/кг; экспериментальные группы 2.1-2.5 - животные, получавшие ежедневно внутримышечно фторурацил и изониазид как в смеси препаратов, так и раздельно в нижеперечисленных дозах (табл.4).
Методы исследования аналогичны 1-му примеру. Все животные во всех группах выжили. Клиническая картина заболевания во всех случаях была стертой. Изменения лабораторных показателей у исследуемых животных не имели существенных различий и не выходили за пределы возрастной нормы. Результаты посевов гомогенатов внутренних органов на выявление МБТ у всех животных всех групп оказались отрицательными. Изменение массы животных в конце эксперимента приведено в таблице 5. Введение изониазида и фторурацила в виде их смеси или раздельно не оказало влияния на результаты лечения.
Животные контрольной группы 2, не получавшие лечения, по приросту массы значительно отставали от животных остальных групп (табл.5). При патоморфологическом исследовании у всех этих животных были обнаружены множественные туберкулезные поражения внутренних органов с многочисленными очагами казеозного некроза. Таким образом, несмотря на стертую клиническую картину, обусловленную заражением свинок клиническим штаммом МБТ, у всех животных контрольной группы 2 был выявлен генерализованный туберкулез.
По приросту массы тела животные группы сравнения 2, получавшие только изониазид, не слишком отличались от животных контрольной группы 2. При патоморфологическом исследовании в легких у них было обнаружено полнокровие, микроателектазы и множественные лимфоидные фолликулы. В периферических и единичных интраторакальных лимфоузлах обнаруживались казеозно-некротические очаги и крупнопетлистый склероз. В итоге лечения у этих животных было достигнуто некоторое улучшение состояния (по сравнению с животными контрольной группы 2), но при этом отмечался замедленный прирост массы животных и сохранялись патоморфологические изменения внутренних органов.
Добавление к терапии туберкулеза, включающей изониазид, фторурацила в дозах от 0,1 до 2,5 мг/кг повысило эффективность лечения:
- возрос прирост массы животных;
- специфические патологические изменения внутренних органов менее выражены у животных групп 2.1, 2.2, включая отсутствие очагов казеозного некроза в лимфоузлах; у животных других групп не обнаружено каких-либо патологических изменений, что свидетельствует о выздоровлении животных.
В итоге результаты исследований, проведенных на большом количестве животных, показали высокую противотуберкулезную активность комбинации изониазида и фторурацила вне зависимости от характера возбудителя. Преимущества использования данной комбинации препаратов для лечения туберкулеза заключаются как в элиминации МБТ из организма животных в сроки до 2 месяцев от начала лечения на фоне нормализации показателей гомеостаза, так и в уменьшении или отсутствии специфических патологических изменений внутренних органов, т. е. в излечении животных в отличие от результатов, полученных при лечении одним изониазидом (группы сравнения). Применение комбинации данных препаратов также выгодно отличается от использования одного фторурацила (патент РФ 2165761) как по непосредственному результату, так и по менее выраженным побочным проявлениям. При этом экспериментально показано, что возможные дозы дополнительно к изониазиду вводимого фторурацила могут варьироваться в достаточно широких пределах (от 0,1 до 2,5 мг/кг массы животного) и при длительном применении не приводят к осложнениям.
Пример 3. Проведено клиническое испытание противотуберкулезного действия комбинации изониазида (в дозе 10 мг/кг) и фторурацила (в дозе 1÷1,5 мг/кг) на 4-х больных прогрессирующим инфильтративным туберкулезом легких в фазе распада. Объем поражения в двух случаях ограничивался одной долей легкого. У двух других больных имелись очаги обсеменения с противоположной стороны. Во всех случаях была доказана устойчивость МБТ к двум и более основным ПТП. Продолжительность комбинированной химиотерапии у больных до поступления в клинику составляла от 12 до 14 месяцев. В клинике больным была продолжена химиотерапия с обязательным назначением изониазида, который вводили ежедневно внутривенно в дозе 10 мг/кг. Дополнительно к этому назначали фторурацил в дозе 1÷1,5 мг/кг внутривенно ежедневно курсом до 3-х месяцев. Фторурацил вводили как в смеси с изониазидом, так и отдельно. Оценку состояния больных проводили на основании изменений клинической картины заболевания и показателей гомеостаза, динамики рентгенологической картины и сроков прекращения бактериовыделения.
В результате проведения комплексной противотуберкулезной терапии, включающей изониазид с добавлением фторурацила, у всех больных наблюдали положительную динамику процесса, которая выражалась в быстром, до 2-3 недель, купировании симптомов интоксикации и нормализации показателей крови. Через месяц после начала лечения у всех больных отмечался регресс рентгенологических изменений в виде рассасывания инфильтратов, уменьшения размеров или закрытия полостей распада, полного или частичного рассасывания очагов обсеменения. Абациллирование во всех случаях было достигнуто в сроки до 2 месяцев.
Двое больных через 2 месяца после начала лечения были прооперированы - выполнены лобэктомии. В обоих случаях в операционном материале были обнаружены процессы фиброзирования легочной ткани в пределах резецированных участков. Послеоперационная терапия включала только изониазид и фторурацил и продолжалась в течение одного месяца, после чего больные были выписаны под наблюдение фтизиатра. При контрольном обследовании через 12 месяцев признаков реактивации туберкулеза у этих больных выявлено не было.
В двух других случаях лечение ограничили проведением описанной выше химиотерапии. Через три месяца после начала лечения у больных при рентгенологическом обследовании в легких на месте имевшихся полостей распада обнаружены рубцовые изменения с полным рассасыванием инфильтрации. При контрольном обследовании этих больных через 6 и 12 месяцев новых патологических изменений в легких у них не обнаружено.
Клинический пример Больная П., 1972 г.р., поступила с диагнозом: прогрессирующий инфильтративный туберкулез верхней доли левого легкого в фазе распада и обсеменения в пределах доли с поражением дренирующего бронха. МБТ (+). До поступления получила стандартную многокомпонентную противотуберкулезную терапию в условиях стационара в течение 12 месяцев с момента выявления заболевания. Выявлена устойчивость МБТ: S (10), Н (5), R (50), Е (5). При поступлении общее состояние удовлетворительное. Умеренно выражены признаки интоксикации в виде потери веса (10 кг), субфебриллитета, анемии (Нb 107 г/л), лейкоцитоза (7,35•109/л). На рентгенограмме грудной клетки (фиг.1а), томограмме легкого (фиг. 1б) и при КТ легкого (фиг.1в) слева определяется утолщение апикальной плевры, в S1-2 имеется инфильтративный фокус размером 3,5 на 3 см с тяжами в окружающую ткань с расширенным дренирующим бронхом. В инфильтрате имеется полость с четкими внутренними контурами. В пределах верхней доли очаги обсеменения без распада. Правое легкое без изменений.
В течение 2-х месяцев проведена комплексная противотуберкулезная терапия, включающая этамбутол (15 мг/кг), пиразинамид (15 мг/кг) и ежедневное внутривенное введение смеси официнальных растворов изониазида (10 мг/кг) и фторурацила (1,5 мг/кг). В результате проведенного лечения состояние больной улучшилось. Прибавила в весе 12 кг. Нормализовались температура и лабораторные показатели крови, прекращено бактериовыделение. При контрольном рентгенологическом обследовании (фиг. 2) было обнаружено уменьшение размеров инфильтративного фокуса до 2 см, увеличение количества тяжей в окружающую ткань. Полость распада диаметром до 9 мм, контуры ее ровные. Плотность основного фокуса +26 +36 Н. В пределах 1-2 сегментов и в аксиллярных субсегментах сохраняются очаги обсеменения без распада, с четкими контурами. Больной была произведена верхняя лобэктомия слева.
При морфогистологическом исследовании удаленной доли легкого субплеврально в верхушечной области обнаружена полость 1 на 0,5 см, окруженная толстым слоем плотной белесоватой ткани, от которой отходят тяжистые рубцы, в респираторной ткани - мелкие грязно-желтые очаги в пределах верхушечного сегмента. Гистологическое заключение: фиброзирующаяся каверна на фоне туберкулезной инфильтрации в фазе отграничения и формирования неактивных очагов.
Послеоперационный период протекал без осложнений. Лечение продолжено изониазидом (10 мг/кг) и фторурацилом (1,5 мг/кг) в течение одного месяца. При рентгенологическом контроле через месяц после операции патологические изменения в легких не определяются, имеется механический шов левого легкого после верхней лобэктомии (фиг.3). Через 12 месяцев признаков реактивации туберкулеза не выявлено.
Таким образом, проведенные клинико-экспериментальные исследования подтвердили высокую эффективность совместного использования изониазида и фторурацила при лечении прогрессирующего деструктивного полирезистентного туберкулеза.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОТУБЕРКУЛЕЗНЫЙ ПРЕПАРАТ | 2002 |
|
RU2211035C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ТУБЕРКУЛЕЗА | 2000 |
|
RU2165761C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ТУБЕРКУЛЕЗА | 2001 |
|
RU2207127C1 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2004 |
|
RU2269346C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2013 |
|
RU2523792C9 |
| ТУБЕРКУЛОСТАТИЧЕСКОЕ СРЕДСТВО | 2002 |
|
RU2207126C1 |
| СПОСОБ СНИЖЕНИЯ НЕПЕРЕНОСИМОСТИ ПРОТИВОТУБЕРКУЛЕЗНЫХ ПРЕПАРАТОВ | 2009 |
|
RU2412701C2 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА ЛЕГКИХ С ПРЕИМУЩЕСТВЕННО ПРОДУКТИВНЫМ ТИПОМ ТКАНЕВОЙ РЕАКЦИИ | 2000 |
|
RU2204409C2 |
| ТУБЕРКУЛОСТАТИЧЕСКОЕ СРЕДСТВО | 2001 |
|
RU2185170C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФИЛЬТРАТИВНОГО ТУБЕРКУЛЕЗА ЛЕГКИХ, ВЫЗВАННОГО МНОЖЕСТВЕННО-ЛЕКАРСТВЕННОУСТОЙЧИВЫМИ И ВЫСОКОТОКСИЧНЫМИ ШТАММАМИ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2009 |
|
RU2423129C1 |


Изобретение относится к медицине, к фтизиатрии и может быть использовано для лечения туберкулеза. Дополнительно к изониазиду, вводимого в обычной дозе, вводят фторурацил ежедневно в дозе 0,1-2,5 мг/кг не менее 2-х месяцев, при этом изониазид и фторурацил вводят одновременно, или последовательно, или в виде их смеси, или внутривенно. Данное изобретение способствует уменьшению или исчезновению специфических патологических изменений внутренних органов, уменьшению количества положительных посевов МБТ, сокращению сроков лечения за счет ускорения абациллирования и регрессии туберкулезных изменений в легких, излечению туберкулеза, резистентного к изониазиду, позволяет использовать минимальные дозы изониазида для лечения туберкулеза. 4 з. п. ф-лы, 3 ил., 5 табл.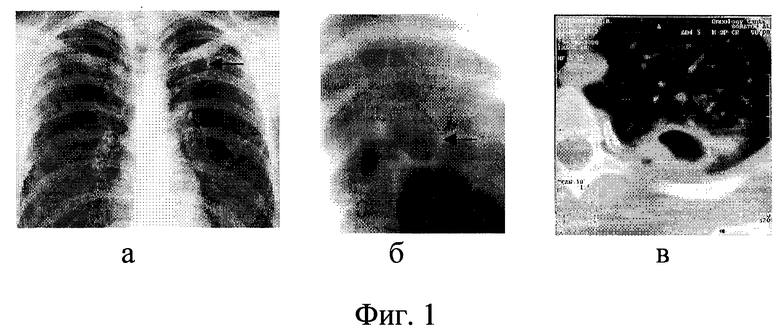
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| Руководство для врачей | |||
| - М.: Медицина, 1988, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 1994 |
|
RU2099056C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ТУБЕРКУЛЕЗА | 2000 |
|
RU2165761C1 |
| ВАСИЛЬЕВА И.А | |||
| Эффективность двухэтапной краткосрочной химиотерапии туберкулеза легких | |||
| Автореф | |||
| дисс | |||
| к.м.н | |||
| - М., 1997, с | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Регистр лекарственных средств России | |||
| Энциклопедия лекарств | |||
| Ежегодный сборник | |||
| Гл | |||
| редактор Г.Л.ВЫШКОВСКИЙ, выпуск 9.- М.:РЛС 2002 (подписано в печать 15.07.2001), с.928, 908 и 909 | |||
| ЧУБАРИН В.Т | |||
| и др | |||
| Дозирование изониазида и рифампицина у больных туберкулезом легких с учетом индивидуальных особенностей фармакокинетики | |||
| Деревянный торцевой шкив | 1922 |
|
SU70A1 |
| Сборник научных трудов, юбилейная научно-практическая конференция | |||
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| СКОРНЯКОВ С.Н | |||
| Фторурацил в комплексной пред- и послеоперационной подготовке больных с лекарственно-устойчивым туберкулезом легких | |||
| Уральский НИИ фтизиопульмонологии, 21.06.2002. | |||
Авторы
Даты
2003-09-20—Публикация
2002-03-18—Подача