Изобретение относится к области синтеза цеолита Бета, который находит широкое применение в качестве катализатора в процессах нефтепереработки, основной и тонкой органической химии, а также в качестве адсорбента.
Все известные способы синтеза цеолита Бета заключаются в том, что состав реакционных смесей, из которых получается цеолит, включает тот или иной органический компонент, представляющий собой органический аммонийный катион.
Наиболее часто встречающимися органическими компонентами реакционных смесей в синтезе цеолита Бета являются соединения тетраэтиламмония. Применение других четвертичных аммонийных оснований, отличных от тетраэтиламмоний катиона, связано со способами синтеза цеолита Бета, не содержащего алюминия в своем составе, таких как цеолит Бета борсиликатного состава [патент США 5166111, B 01 J 29/04, 1992 - бис-(1,4-азониабицикло[2.2.2]октан-α,ω-алкан дичетвертичный аммонийный катион] , титан-содержащего состава [патент США 5527520, С 01 В 37/00, 1996 - 4,4'-триметилен-бис(N-бензил-N-метилпиперидиний) дигидроксид] или цеолит Бета, представляющий собой по своему химическому составу чистую двуокись кремния [J. С. van der Waal, Synthesis of all-silica zeolite beta//Chem. Soc., Chem. Commum., 10, 1241-1242 (1994) - дибензилдиметиламмоний гидроксид]. Синтез этих цеолитных систем затруднен или невозможен в случае использования соединений тетраэтиламмония. Для этих методов, основанных на применении других четвертичных аммонийных оснований, недостатком является нецелесообразность их применения для синтеза цеолита Бета алюмосиликатного состава в силу отсутствия их производства, относительной сложности и многостадийности их синтеза, а также дороговизны исходных реагентов для их получения.
Основной способ синтеза цеолита Бета базируется на применении в реакционных смесях гидроокиси тетраэтиламмония как органического компонента [патент США 3308069, B 01 J 29/28, С 01 В 39/48, 1967]. По данному способу цеолит Бета кристаллизуют из пятикомпонентных реакционных гидрогелей состава Na2O-TEAOH-Al2O3-SiO2-H2O с рекомендованными мольными соотношениями компонентов: SiO2/Аl2О3= 10-200, Na2O/TEAOH=0-0.1, TEAOH/SiO2=0.1-1.0, H2O/TEAOH= 20-75. В качестве источников органического компонента и алюминия указывают гидроокись тетраэтиламмония и алюминат натрия, соответственно. Кристаллизацию ведут в температурном диапазоне 75-200oС за время от 40 дней при минимальной температуре (при этом есть указания, что кристаллизация в реакционной системе была неполной, примеры 2 и 3 патента) до 6 дней при 150oС (пример 7 патента). Мольное отношение SiO2/Аl2O3 в цеолите Бета заявляют в интервале от 10 до 100, хотя максимально достигнутое значение по примерам составляет 75 (пример 2 патента). Недостатком методов, основанных на применении гидроокиси тетраэтиламмония, является относительная дороговизна данного органического компонента в силу особенностей его получения через ионный обмен галоидных солей тетраэтиламмония на сильных анионообменных смолах в гидроксидной форме с последующим упариванием разбавленного раствора гидроокиси тетраэтиламмония при уменьшенном давлении и необходимостью восстановления использованной ионообменной смолы в ОН-форму. Другим недостатком является разложение гидроокиси тетраэтиламмония в ходе гидротермального синтеза на триэтиламин, этилен и воду (расщепление по Гофману) в силу концентрированности реакционной смеси и повышенной температуры.
Замена гидроокиси тетраэтиламмония на более доступные галоидные соли того же органического катиона, такие как тетраэтиламмоний бромид, или тетраэтиламмоний йодид, приводит к образованию других цеолитов, отличных от цеолита Бета, таких как ZSM-5 и/или морденит и/или ZSM-12, наряду с образованием кристаллических модификаций двуокиси кремния, таких как кварц или кристобалит. Образование цеолита Бета из реакционных алюмосиликатных гелей в присутствии галоидных солей тетраэтиламмония осуществляют либо добавлением в реакционную смесь затравочных кристаллов цеолита Бета [патент США 4847055, С 01 В 33/28, 1989; патент РФ 2151101, С 01 В 39/04, 2000], либо добавлением фторидов щелочных металлов [Xiao-Lan Qi и др. Synthesis of b zeolite using tetraethylammonium bromide together with fluoride as composite of template(II) - Studies on crystallization process of b zeolite//Gaodeng Xuexiao Huaxue Xuebao, 21(8), 1161-1166 (Chinese) 2000, CA133:3048342].
Недостатками методов, основанных на применении галоидных солей тетраэтиламмония в присутствии затравочных кристаллов цеолита Бета, являются узкие и жесткие рамки составов реакционной смеси и параметров проведения гидротермального синтеза для устойчивого образования чистой фазы цеолита Бета, что связано с невозможностью образования цеолита Бета в беззатравочном варианте проведения синтеза, а также удорожание процесса синтеза за счет необходимости использования прокаленной формы цеолита Бета для ее использования в качестве затравки для интенсификации процесса.
Недостатками методов, основанных на применении галоидных солей тетраэтиламмония в присутствии фторидов щелочных металлов, являются две особенности. Первая заключается в том, что после синтеза фторид-анион остается в составе полученного цеолита Бета и при дальнейшем отжиге органического компонента происходит локальное разрушение цеолитного каркаса в месте локализации фторид-иона. Вторая заключается в жестких санитарных нормах на содержание фторид-ионов в сточных водах и, как следствие, в необходимости тщательной (и дорогостоящей) очистки образующихся стоков от фторидов. Сюда же примыкает проблема коррозионной устойчивости оборудования к фтористому водороду и очистки от него отходящих газов, образующихся при отжиге цеолита Бета от органического компонента.
Наиболее близким к предлагаемому изобретению является способ синтеза цеолита Бета с применением хлорида тетраэтиламмония [заявка WO 9426663, С 01 В 39/48, 1994]. Способ позволяет получать цеолит Бета без применения затравочных кристаллов. По данному способу цеолит Бета кристаллизуют из пятикомпонентных реакционных гидрогелей состава Na2О-TEACl-Al2О3-SiО2-H2О с рекомендованными мольными соотношениями компонентов: SiO2/А12O3= 10-200, Na+/SiO2= 0.12-0.30, TEACl/SiO2= 0.12-0.32, Н2O/Аl2O3=150-400. Преимущественный диапазон мольных соотношений компонентов указывается следующим: SiO2/Аl2О3= 20-35, Na+/SiO2= 0.14-0.20, TEACl/SiO2= 0.12-0.20, H2О/Аl2О3= 200-360. В качестве источников органического компонента и кремния указывают тетраэтиламмоний хлористый и силиказоль, стабилизированный натрием. Кристаллизацию ведут в температурном диапазоне 140-160oС за время не менее 3 суток. Недостатками данного метода синтеза цеолита Бета являются узкий интервал предпочтительного мольного отношения оксида кремния к оксиду алюминия в реакционной смеси (а следовательно, и в готовом цеолите Бета), низкое допустимое значение для общей щелочности реакционной смеси (выражаемое в патенте отношением Na+/SiO2), что существенно сказывается на возможности интенсификации процесса кристаллизации за счет этого параметра синтеза, а также ограничение сырьевой базы источников алюминия за счет выведения из нее солей алюминия и минеральных кислот, так как для их нейтрализации необходимо дополнительное количество гидроокиси натрия, что с необходимостью приведет к концентрации ионов натрия в реакционной смеси выше допустимых значений Na+/SiO2. Однако основным недостатком данного способа синтеза цеолита Бета является единственность пригодного источника кремния для данного способа, а именно водной дисперсии двуокиси кремния (силиказоль), стабилизированной гидроокисью натрия типа Ludox HS-40 (DuPont Co.), причем с концентрацией по SiO2 не менее 30 мас.%. Кроме того, необходимо отметить существенную дороговизну данного источника кремния.
Изобретение решает задачу упрощения получения цеолита Бета, в том числе и в его различных изоморфнозамещенных вариантах, в широком диапазоне допускаемых химических составов реакционных смесей и выбора реакционных источников для их приготовления без снижения качества получаемого цеолита и без ухудшения эффективности проведения процесса синтеза (температура синтеза и длительность проведения синтеза).
Задача решается способом получения цеолита Бета, включающим гидротермальную кристаллизацию реакционной смеси, содержащей воду, щелочь, источник кремния, источник изоморфнозамещающего кремний элемента и тетраэтиламмонийную соль, анион которой имеет положительную гидратацию, или применяют смесь тетраэтиламмонийных солей, имеющих хотя бы один анион, обладающий положительной гидратацией. Источник изоморфнозамещающего кремний элемента представляет собой соединение алюминия и/или бора, и/или галлия, и/или железа, и/или ванадия, и/или титана, и/или их любую смесь.
По определению Самойлова О.Я. [О.Я. Самойлов, Структура водных растворов электролитов, Изд. АН СССР, 1957] гидратация определяется как влияние ионов на трансляционное движение молекул воды в растворе соли по сравнению с их движением в чистой воде. В случае отрицательной гидратации молекулы воды вокруг иона становятся более подвижными, а в случае положительной гидратации происходит связывание близлежащих к иону молекул воды. Данные по гидратационному влиянию ионов можно получить, например, из релаксационных методов ЯМР (времена переориентации молекул воды), коэффициентов диффузии и самодиффузии воды, вязкости растворов. Так, основываясь на данных по коэффициенту вязкости В [H.D.B. Jenkins, Y. Marcus, Viscosity B-Coefficient of Ions in Solutions//Chemical Rev., 1995, Vol.95, No.8, 2695-2724], гидроксид- и фторид-ионы относятся к группе ионов с положительной гидратацией, бромид- и иодид-ионы относятся к группе с отрицательной гидратацией. Хлорид-ион находится в пограничной области, будучи ионом со слабой отрицательной гидратацией.
Примерами солей тетраэтиламмонийного катиона и кислот, анионы которых имеют положительную гидратацию, можно назвать такие, как тетраэтиламмоний роданистый, тетраэтиламмоний бромат, тетраэтиламмоний формиат, тетраэтиламмоний ацетат и другие соли алифатических кислот, а также соли преимущественно многоосновных кислот, как полностью, так и частично замещенных, такие как тетраэтиламмоний сульфат или гидросульфат, тетраэтиламмоний фосфат или моногидрофосфат или дигидрофосфат, тетраэтиламмоний карбонат или гидрокарбонат, тетраэтиламмоний силикат, тетраэтиламмоний борат, тетраэтиламмоний этилендиаминтетраацетат, тетраэтиламмоний оксалат, тетраэтиламмоний сукцинат, тетраэтиламмоний цитрат и т.п. Предлагаемые органические компоненты для гидротермального синтеза цеолита Бета позволяют получать данный цеолит с использованием самых различных сырьевых источников реакционных компонентов, с различным в широком диапазоне содержанием алюминия в реакционных смесях, а также при температурах и временах синтеза, не превышающих таковые для известных способов и без применения затравочных кристаллов синтезируемого цеолита. Анионы кислот в предлагаемых органических компонентах синтеза цеолита Бета не остаются в составе конечного продукта. Получение предлагаемых органических компонентов синтеза цеолита Бета дешевле и технологически проще, чем получение гидроокиси тетраэтиламмония, поскольку могут использоваться менее основные анионообменные смолы, при проведении процесса ионного обмена снижаются требования по щелочестойкости оборудования и концентрирование элюируемых водных растворов солей органического компонента можно проводить при обычном давлении. Помимо ионообменного способа, соли многоосновных кислот тетраэтиламмония можно получать из галогенидов тетраэтиламмония другими способами, такими как:
- окислительно-восстановительный обмен, например по реакции
2NEt4I+H2O2+H2SO4=(NEt4)2SO4+I2+2H2O
- вытеснение летучих галоидводородов, например по реакции
2NEt4Br+Н3РO4=(NEt4)2HPO4+2HBr
- алкилирование триэтиламина этиловыми эфирами неорганических многоосновных кислот, например по реакции
2NEt3+(C2H5)2SO4=(NEt4)2SO4
- алкилирование триэтиламина этиловыми эфирами поликарбоновых кислот
2NEt3+EtOOCCH2CH2COOEt=(NEt4)2 (CH2COO)2
и другими, приводящими к образованию солей многоосновных кислот тетраэтиламмония.
Сущность изобретения иллюстрируется следующими примерами.
Пример 1 (по прототипу, заявка WO 9426663)
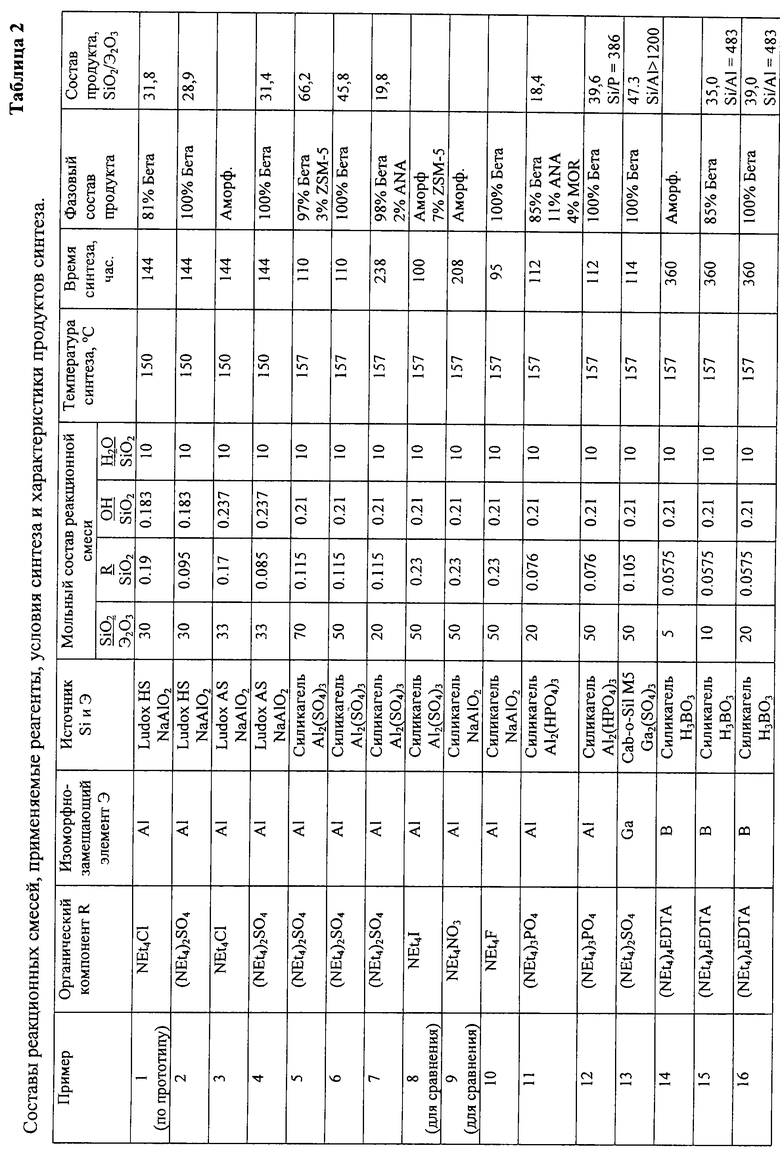
Реакционную смесь, имеющую мольный состав: 0.183 NaOH : 0.19 NEt4Cl : 1/30 Аl2О3 : 1 SiO2 : 10 Н2O, готовят путем смешения раствора, содержащего 1,587 г NaAlO2•1.5 Н2O (46.77 мас.% Аl2О3, 28.43 мас.% Na2O, 24.8 мас.% Н2O), 0,855 г NaOH (98 мас.%), 6,878 г NEt4Cl (91.4 мас.%) и 18,46 г Н2О, и 32,981 г силиказоля Ludox HS-40 (39.8 мас.% SiO2, 0.43 мас.% Na2O, 59.77 мас. % Н2O). После размешивания в течение 30 мин смесь загружают в 100-мл автоклав с фторопластовым вкладышем. Реакционную смесь кристаллизуют при 150oС в течение 6 дней без перемешивания. Осадок после охлаждения смеси отфильтровывают, отмывают водой и высушивают при 100oС. Сухой продукт, выход которого составляет 13,85 г, представляет собой по данным рентгенофазового анализа (диффрактометр HZG-4c, CuKα излучение, область сканирования 2Θ = 4-40o, шаг сканирования - 0,05o, время накопления - 3 с) цеолит Бета со степенью окристаллизованности 81%. Продукт кристаллизации имеет мольное отношение SiO2/Аl2O3=31,8.
Пример 2
К раствору 600 г тетраэтиламмоний йодида в 1000 г воды приливают при перемешивании 290,3 г раствора, состоящего из 168,1 г 23,6% раствора Н2O2 и 122,2 г 17,47 М раствора H2SO4. После перемешивания в течение 30 мин полученную суспензию выделившегося йода в растворе тетраэтиламмоний сульфата отфильтровывают на воронке Бюхнера. Осадок йода на воронке промывают 100 мл воды. Собранный в колбе Бунзена раствор выливают в кристаллизатор, который ставят в сушильный шкаф на упаривание раствора соли тетраэтиламмония и его деколоризацию от следов растворенного йода при 100oС в течение ночи. В результате получают 760 г 54% раствора тетраэтиламмоний сульфата (концентрация раствора определена весовым методом с раствором хлорида бария; выход по катиону тетраэтиламмония - 98%).
Реакционную смесь, имеющую мольный состав: 0.183 NaOH : 0.095 (NEt4)2SO4 : 1/30 Аl2О3 : 1 SiO2 : 10 Н2O, готовят путем смешения раствора, содержащего 1,587 г NaAlO2•1.5 Н2O, 0,854 г NaOH (98%), 13,704 г 54% водн. раствора (NEt4)2SO4 и 12,75 г Н2O, и 32,979 г силиказоля Ludox HS-40. После размешивания в течение 30 мин смесь загружают в 100-мл автоклав с фторопластовым вкладышем. Реакционную смесь кристаллизуют при 150oС в течение 6 дней без перемешивания. Осадок после охлаждения смеси отфильтровывают, отмывают водой и высушивают при 100oС. Сухой продукт, выход которого составляет 14,45 г, представляет собой по данным рентгенофазового анализа полностью окристаллизованный цеолит Бета. Продукт кристаллизации имеет мольное отношение SiO2/Аl2О3=28,9.
Примеры 1 и 2 показывают, что для реакционных смесей одинакового состава в равных условиях проведения синтеза тетраэтиламмоний сульфат дает более окристаллизованный цеолит Бета.
Пример 3
Готовят реакционную смесь по примеру 1, но с увеличенным содержанием щелочи на 30% и с использованием коллоидного раствора двуокиси кремния, стабилизированного аммиаком, путем смешения раствора, содержащего 2,165 г NaAlO2•1.5 Н2O, 2,360 г NaOH (98%), 9,233 г NEt4Cl (91.4 мас.%) и 27,68 г Н2O, и 49,230 г силиказоля Ludox AS-40 (40 мас.% SiO2, 0.16 мас.% NН3). Реакционную смесь, имеющую мольный состав 0.237 NaOH : 0.17 NEt4Cl : 1/33 Аl2О3 : 1 SiO2 : 10 H2O, кристаллизуют при 150oС в течение 6 дней без перемешивания. Сухой продукт, выход которого составляет 21,35 г, представляет собой полностью аморфную фазу по данным рентгенофазового анализа.
Пример 4
Реакционную смесь, имеющую мольный состав: 0.237 NaOH : 0.085 (NEt4)2SO4 : 1/33 Аl2O3 : 1 SiO2 : 10 Н2O, готовят путем смешения раствора, содержащего 2,165 г NaAlO2•1.5 Н2O, 2,360 г NaOH (98%), 34,4145 г 28,86% водн. раствора (NEt4)2SO4 и 4,04 г Н2О, и 49,269 г силиказоля Ludox AS-40. Реакционную смесь кристаллизуют при 150oС в течение 6 дней без перемешивания. Сухой продукт, выход которого составляет 20,85 г, представляет собой по данным рентгенофазового анализа полностью окристаллизованный цеолит Бета. Продукт кристаллизации имеет мольное отношение SiO2/Аl2O3=31,4.
Примеры 3 и 4 показывают, что для реакционных смесей, имеющих одинаковую концентрацию гидроксид-ионов, алюминия и кремния, и приготовленных с использованием стабилизированного аммиаком силиказоля, в равных условиях проведения синтеза тетраэтиламмоний хлорид непригоден для получения цеолита Бета, а тетраэтиламмоний сульфат является эффективным органическим компонентом.
Пример 5
Готовят реакционную смесь, имеющую мольный состав: 0.21 NaOH : 0.115 (NEt4)2SO4 : 1/70 Аl2О3 : 1 SiO2 : 10 Н2O. Для этого в 6,28 г воды растворяют 1,013 г Al2(SO4)3•18H2O и к полученному раствору добавляют при перемешивании 1,317 г NaOH (98% основного вещества), растворенных в 7,21 г воды. К полученному щелочному раствору последовательно добавляют 9,065 г 54% раствора сульфата тетраэтиламмония, полученного по примеру 2, 1,02 г воды и 7,084 г силикагеля КСК (93.76% SiO2, 0.085% Аl2О3, 0.03% Na2O), предварительно размолотого на дисковой мельнице. Полученную реакционную смесь размешивают в течение 10 мин, после чего загружают в 100-мл автоклав с тефлоновым закрывающимся вкладышем. Кристаллизацию проводят при 157oС в течение 110 ч без перемешивания. После кристаллизации, охлаждения автоклава и его открытия, продукт кристаллизации отделяют от маточного раствора фильтрованием, отмывают дистиллированной водой и высушивают при 100oС. Сухой продукт, выход которого составляет 7,47 г, представляет собой цеолит Бета с незначительной примесью цеолита ZSM-12 (3 мас.%). Цеолит Бета имеет мольное отношение SiO2/Al2O3=66,2.
Пример 6
Готовят реакционную смесь, имеющую мольный состав: 0.21 NaOH : 0.115 (NEt4)2SO4 : 1/50 Аl2О3 : 1 SiO2 : 10 H2O. Для этого в 5,92 г воды растворяют 1,434 г Аl2(SO4)3•18Н2O и к полученному раствору добавляют при перемешивании 1,4715 г NaOH (98%), растворенных в 5,81 г воды. К полученному щелочному раствору последовательно добавляют 9,065 г 54% раствора сульфата тетраэтиламмония, 2,53 г воды и 7,083 г размолотого силикагеля КСК и размешивают в течение 40 мин. Кристаллизацию проводят при 157oС в течение 110 ч без перемешивания. Сухой продукт, выход которого составляет 7,74 г, представляет собой чистый цеолит Бета по данным рентгенофазового анализа. Цеолит Бета имеет мольное отношение SiO2/Аl2О3=45,8.
Пример 7
Готовят реакционную смесь, имеющую мольный состав: 0.21 NaOH : 0.115 (NEt4)2SO4 : 1/20 Аl2О3 : 1 SiO2 : 10 Н2O. Для этого в раствор 6,01 г воды, 3,608 г Аl2(SO4)3•18Н2O и 15,527 г 28.86% раствора сульфата тетраэтиламмония добавляют при перемешивании 2,261 г NaOH (98%) с последующим добавлением 7,000 г размолотого силикагеля КСК. Кристаллизацию проводят при 157oС в течение 238 ч без перемешивания. Сухой продукт, выход которого составляет 8,17 г, представляет собой чистый цеолит Бета со следовыми количествами анальцима по данным рентгенофазового анализа. Цеолит Бета имеет мольное отношение SiO2/Аl2О3=19,8.
Примеры 5-7 показывают, что тетраэтиламмоний сульфат эффективен в образовании цеолита Бета при использовании силикагеля как источника кремния в широком диапазоне концентрации алюминия в реакционной смеси.
Пример 8
Готовят реакционную смесь, аналогичную по количественному составу примеру 6, но с использованием тетраэтиламмоний йодида в качестве органического компонента. Для этого вместо 9,065 г 54% раствора сульфата тетраэтиламмония добавляют 6,46 г NEt4I в 4,17 г воды. После кристаллизации без перемешивания при 157oС в течение 100 ч продукт синтеза содержит только 7 мас.% цеолита ZSM-5.
Пример 9
Готовят реакционную смесь, аналогичную по количественному составу примеру 6, но с применением тетраэтиламмоний нитрата в качестве органического компонента. Для этого 0,465 г алюмината натрия NaAlO2•1.5 H2O и 0,7665 г NaOH (98% основного вещества) растворяют в 10,408 г воды и 13,206 г 36.7% водного раствора NEt4NO3. К полученному раствору добавляют 7,02 г размолотого силикагеля КСК, и смесь размешивают в течение 30 мин. Кристаллизацию реакционной смеси проводят в статических условиях при 150oС в течение 208 ч. Продукт кристаллизации по данным рентгенофазового анализа представляет собой аморфный продукт.
Примеры 8 и 9 показывают, что цеолит Бета в присутствии тетраэтиламмонийного катиона в составе йодидных или нитратных солей, т.е. с анионами, обладающими отрицательной гидратацией, в условиях, аналогичных примеру 6, не образуется.
Пример 10
Реакционную смесь, аналогичную по количественному составу смеси в примере 9, но с применением тетраэтиламмоний фторида в качестве органического компонента, готовят с заменой 13,206 г 36,7% водного раствора NEt4NO3 на 12,266 г 31.52% водного раствора NEt4F и 0,4 г воды. Реакционную смесь мольного состава 0.21 NaOH : 0.23 NEt4F : 1/50 А12O3 : 1 SiO2 : 10 Н2О кристаллизуют без перемешивания при 157oС в течение 95 ч. Сухой продукт кристаллизации, полученный в количестве 7,21 г, представляет собой высокоокристаллизованный цеолит Бета.
Данный пример показывает, что фторид анион, как ион с положительной гидратацией наряду с гидроксид- и сульфат-анионами и в отличие от анионов с отрицательной гидратацией (I-, NO3-, Br- и др.), способствует образованию цеолита Бета.
Пример 11
К раствору 2,942 г NaOH (98%) в 10,796 г воды добавляют 2,091 г тонко растертого Аl2(НРO4)3•2.5 Н2O при перемешивании. После растворения двузамещенного фосфата алюминия к полученному раствору последовательно добавляют 11,705 г 34.84% водного раствора (NEt4)3PO4 и 7,001 г размолотого силикагеля КСК. После тщательного перемешивания полученную густую суспензию, имеющую мольный состав 0.21 NaOH : 0.076 (NЕt4)3РO4 : 1/20 Аl2О3 : 1 SiO2 : 10 Н2O, кристаллизуют при 157oС в течение 112 ч без перемешивания. Сухой продукт, выход которого составляет 7,45 г, представляет собой по данным рентгенофазового анализа преимущественно цеолит Бета (85%) с примесью анальцима (11%) и морденита (4%). Продукт имеет мольное отношение SiO2/Аl2O3=18,4.
Пример 12
К раствору 1,740 г NaOH (98%) в 11,204 г воды добавляют 0,844 г тонко растертого Аl2(НРO4)3•2.5 Н2O при перемешивании. После растворения двузамещенного фосфата алюминия к полученному раствору последовательно добавляют 11,698 г 34.84% водного раствора (NЕt4)3РO4 и 6,999 г размолотого силикагеля КСК. После тщательного перемешивания полученную густую суспензию, имеющую мольный состав 0.21 NaOH : 0.076 (NEt4)3PO4 : 1/50 Аl2О3 : 1 SiO2: 10 Н2O кристаллизуют при 157oС в течение 112 ч без перемешивания. Сухой продукт, выход которого составляет 7,21 г, по данным рентгенофазового анализа представляет собой высокоокристаллизованный цеолит Бета. Продукт имеет мольное отношение SiO2/Аl2O3=39,6. Мольное отношение остаточного фосфора в цеолитном продукте составляет Si/P=386.
Данный пример показывает, что анион, входящий в состав используемой соли тетраэтиламмония, не входит в состав конечного продукта кристаллизации, а именно в цеолит Бета.
Пример 13
Реакционную галлийсиликатную смесь, имеющую мольный состав 0.21 NaOH : 0.105 (NEt4)2SO4 : 1/50 Gа2O3 : 1 SiO2 : 10 Н2O, готовят смешением 25,4 г щелочного галлатного раствора, приготовленного растворением 0,934 г безводного сульфата галлия Gа2(SO4)3 (осч 11-3), 1,473 г NaOH (98%) и 14,171 г 28.86% раствора (NEt4)2SO4 в 8,82 г воды, и 6,982 г аэросила Cab-o-Sil M5 (94% SiO2) в течение 30 мин. Полученный однородный гель кристаллизуют при 157oС в течение 114 ч без перемешивания. Отфильтрованный, отмытый и высушенный продукт (7,47 г) представляет собой чистый высокоокристаллизованный цеолит Бета с мольными отношениями SiO2/Gа2O3=47,3 и SiO2/Al2O3>2400.
Примеры 14-16
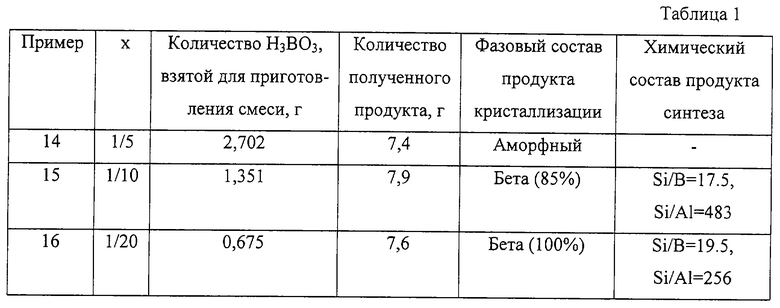
Возможность формирования кристаллического боросиликата со структурой цеолита Бета из щелочных гидрогелей в присутствии тетраэтиламмония этилендиаминтетраацетата ((NEt4)4EDTA) была проверена на ряде реакционных смесей с переменным количеством введенного в них бора и имеющих мольный состав: 0.21 NaOH : 0.0575 (NEt4)4EDTA : x В2O3 : 1 SiO2 : 10 H2O, где значения х указаны в таблице. Реакционные смеси готовят следующим образом. Гидроокись натрия в количестве 0,936 г растворяют в 11,7 г воды, и в полученный раствор добавляют борную кислоту в количестве, удовлетворяющем мольному составу реакционной смеси и указанном в таблице. Борную кислоту растворяют при перемешивании, и в полученный щелочной раствор добавляют 12,144 г 41.85% водного раствора тетраэтиламмония этилендиаминтетраацетата ((NEt4)4EDTA). На последнем этапе приготовления в полученный раствор добавляют 7 г размолотого силикагеля КСК, и смесь тщательно размешивают. Полученную реакционную смесь кристаллизуют при 157oС в течение 15 дней в статических условиях. Продукт гидротермального синтеза фильтруют на воронке Бюхнера, отмывают водой, сушат при 100oС на воздухе и анализируют на содержание цеолитной составляющей и химический состав. Результаты анализа приведены в таблице 1.
Примеры 13-16 иллюстрируют возможность синтеза цеолита Бета в присутствии тетраэтиламмоний сульфата с изоморфнозамещающими элементами, отличными от алюминия.
Пример 17
К раствору 0,763 г NaOH (98%) и 0,464 г NaAlO2•1.5 H2O в 5,039 г воды добавляют 12,192 г 38.8% водного раствора сукцината тетраэтиламмония (NEt4)2[C2H4(COO)2] при перемешивании. Затем к полученному раствору последовательно добавляют 6,45 г воды и 7 г размолотого силикагеля КСК. После тщательного перемешивания полученную суспензию, имеющую мольный состав 0.21 NaOH : 0.115 (NEt4)2[C2H4(COO)2] : 1/50 Аl2О3 : 1 SiO2 : 10 Н2O, кристаллизуют при 157oС в течение 110 ч без перемешивания.
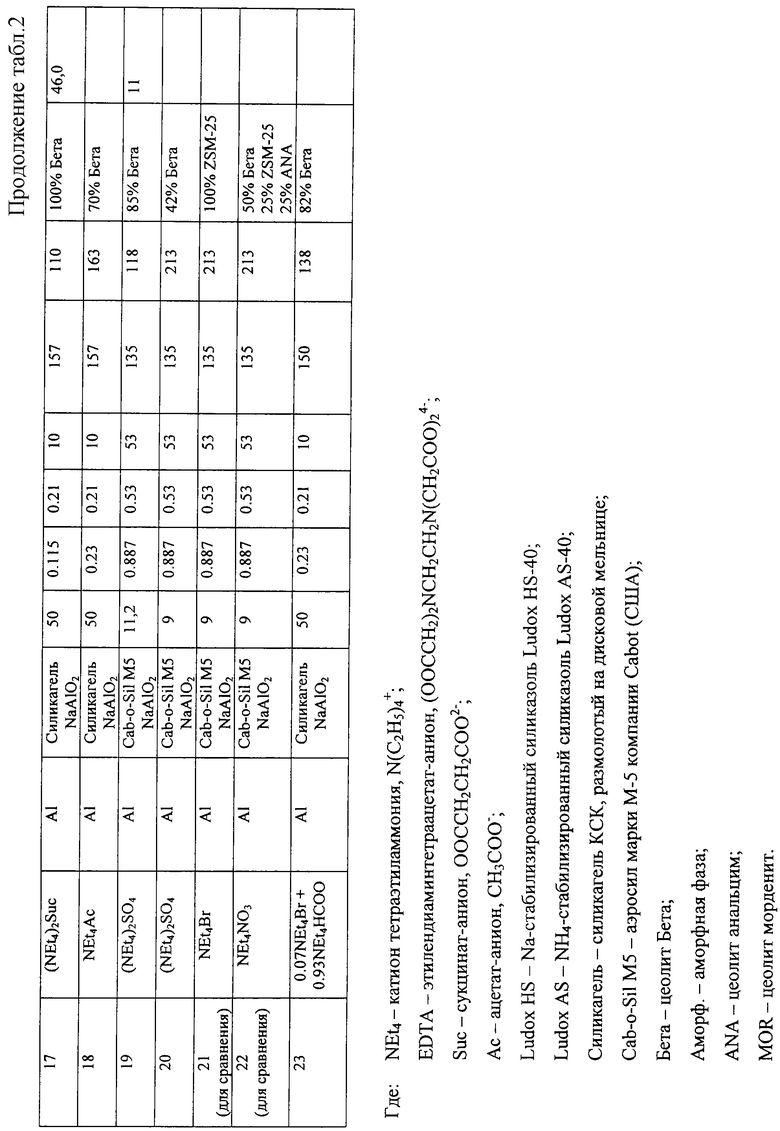
Сухой продукт, выход которого составляет 7,64 г, представляет собой чистый цеолит Бета по данным рентгенофазового анализа. Цеолит Бета имеет мольное отношение SiO2/Al2O3=46,0.
Пример 18
К раствору 0,768 г NaOH (98% основного вещества) и 0,463 г NaAlO2•1.5 H2O в 10,708 г воды добавляют 12,615 г 37.7% водного раствора ацетата тетраэтиламмония NEt4CH3COO при перемешивании. Затем к полученному раствору добавляют 6,999 г размолотого силикагеля КСК. После тщательного перемешивания полученную суспензию, имеющую мольный состав 0.21 NaOH : 0.23 NEt4CH3COO : 1/50 Аl2О3 : 1 SiO2 : 10 H2O, кристаллизуют при 157oС без перемешивания. После 121 ч кристаллизации часть смеси извлекают из автоклава. Содержание цеолитной фазы в сухом твердом остатке после фильтрации и отмывки пробы составляет 29% цеолита Бета. Остальную часть реакционной смеси извлекают из автоклава после 163 ч выдерживания при температуре. Продукт кристаллизации в этой пробе содержит 70% цеолита Бета.
Примеры 11, 12, 14-18 иллюстрируют синтез цеолита Бета в присутствии солей тетраэтиламмония с другими анионами, отличными от сульфат-ионов, обладающих положительной гидратацией.
Пример 18 в сравнении с примером 17 показывает, что тетраэтиламмонийная соль одноосновной уксусной кислоты менее эффективна в образовании цеолита Бета, чем соль этого же катиона с двухосновной янтарной кислотой, хотя последняя взята в половинном количестве, будучи условно димером первой.
Пример 19
В 3,666 г воды и 23,960 г 28.86% раствора (NEt4)2SO4 растворяют 0,314 г NaOH и 0,426 г NaAlО2•1.5 H2О. К полученному раствору добавляют при перемешивании 1,396 г аэросила Cab-o-Sil M5. После тщательного перемешивания однородный текучий густой гель, имеющий мольный состав 0.53 NaOH : 0.887 (NEt4)2SO4 : 1/11.2 Аl2О3 : 1 SiO2 : 53 Н2O, загружают в автоклав с тефлоновым вкладышем, который помещают радиально на краю поворотного диска. Синтез проводят при температуре 135oС с вращением поворотного диска со скоростью 60 об/мин в течение 118 ч. По завершению синтеза твердый продукт отделяют фильтрацией, промывают дистиллированной водой и сушат при 135oС в течение ночи. Выход сухого продукта - 1,11 г. Содержание цеолита Бета в продукте составляет 85% с незначительной примесью анальцима по данным рентгенофазового анализа. По этим же данным мольное отношение SiO2/Аl2O3 цеолита Бета примерно равно 11.
Пример 20
В 1,712 г воды и 23,893 г 28.86% раствора (NEt4)2SO4 растворяют 0,256 г NaOH и 0,531 г NaAlO2•1.5 H2O. К полученному раствору добавляют при перемешивании 3,333 г силиказоля Ludox HS-40. После перемешивания в течение 15 мин полученный опалесцирующий раствор, имеющий мольный состав 0.53 NaOH : 0.887 (NEt4)2SO4 : 1/9 Аl2O3 : 1 SiO2 : 53 Н2О, загружают в автоклав с тефлоновым вкладышем, который помещается радиально на краю поворотного диска. Синтез проводят при температуре 135oС с вращением поворотного диска со скоростью 60 об/мин в течение 213 ч. По завершению синтеза твердый продукт отделяют фильтрацией, промывают дистиллированной водой и сушат при 135oС в течение ночи. Вес сухого продукта - 1,69 г. По данным рентгенофазового анализа содержание цеолита Бета в продукте составляет 42% без дополнительных кристаллических фаз.
Пример 21
Готовят реакционную смесь, аналогичную по количественному составу примеру 20, но с применением тетраэтиламмоний бромида в качестве органического компонента. Для этого вместо 23,893 г 28.86% раствора сульфата тетраэтиламмония добавляют 8,128 г NEt4Br в 17,0 г воды. После кристаллизации с перемешиванием при 135oС в течение 116 ч твердый продукт реакции выделяют и анализируют методом рентгенофазового анализа. Образец представляет собой цеолит ZSM-25 со 100% содержанием.
Пример 22
Готовят реакционную смесь, аналогичную по количественному составу примеру 20, но с применением тетраэтиламмоний нитрата в качестве органического компонента. Для этого вместо 23,893 г 28.86% раствора сульфата тетраэтиламмония добавляют 20,347 г 36.7% раствора NEt4NO3 и 3,844 г воды. После кристаллизации с перемешиванием при 135oС в течение 218 ч твердый продукт реакции выделяют и анализируют методом рентгенофазового анализа. Образец представляет смесь кристаллических цеолитных фаз Бета (50%), ZSM-25 (25%) и анальцима (25%).
Примеры 19-22 показывают, что специфичность сульфатных анионов, как анионов из ряда ионов с положительной гидратацией, в образовании цеолита Бета проявляется в широкой области составов реакционных смесей, в то время как бромид- и нитрат-анионы, как примеры ионов с отрицательной гидратацией, способствуют образованию других типов цеолитных структур.
Пример 23
Раствор тетраэтиламмоний бромида, полученный растворением 38 г NEt4Br в 145 г воды, пропускают через колонку, наполненную 150 мл анионообменной смолы AG 1-X8 (Bio-Rad Laboratories, США) в формиатной форме со скоростью 2 мл/мин. После пропускания основного раствора колонка промывается 150 мл дистиллированной воды. Собранные вместе элюат и промывная вода упариваются в роторном испарителе под вакуумом (остаточное давление 12 мм Hg). После упаривания получается 122,25 г 23.6 мас.% водного раствора формиата тетраэтиламмония, который содержит 2,1 мас.% NEt4Br (степень обмена - 93%; выход при обмене NEt4 + катиона - 98,3%).
Готовят щелочной раствор, содержащий 0,464 г NaAlO2•1.5 H2O, 0,765 г NaOH (98%) и 6,05 г воды. К полученному щелочному раствору добавляют 17,370 г 23.6% раствора формиата тетраэтиламмония, содержащего примесь NEt4Br. К итоговому раствору добавляют при перемешивании 7.002 г размолотого силикагеля КСК и перемешивание продолжают в течение 20 мин. Полученную реакционную смесь, имеющую мольный состав: 0.21 NaOH : 0.23 NEt4 (0.93 HCOO+0.07 Br) : 1/50 Аl2О3 : 1 SiO2 : 10 Н2О, нагревают в 100-мл автоклаве до 150oС и выдерживают при этой температуре 138 ч. Полученный продукт кристаллизации фильтруют, отмывают дистиллированной водой и сушат при 110oС в течение ночи. Получают 7,33 г цеолита Бета, имеющего степень кристалличности 82% по данным рентгенофазового анализа.
Пример 23 показывает, что эффективный синтез цеолита Бета возможен из реакционных смесей, содержащих сумму солей тетраэтиламмонийного катиона, в которых один из анионов (в данном случае - формиат-ион) обладает положительной гидратацией.
Как видно из приведенных примеров и таблиц, предлагаемый способ позволяет значительно упростить синтез цеолита Бета, в том числе и в его различных изоморфнозамещенных вариантах, в широком диапазоне допускаемых химических составов реакционных смесей и выбора реакционных источников для их приготовления без снижения качества получаемого цеолита и без ухудшения эффективности процесса.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТА | 2000 |
|
RU2174952C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ МОТОРНЫХ ТОПЛИВ (ВАРИАНТЫ) И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) | 2003 |
|
RU2235591C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА И СПОСОБ ПОЛУЧЕНИЯ ИЗОПРОПИЛБЕНЗОЛА С ИСПОЛЬЗОВАНИЕМ ЭТОГО КАТАЛИЗАТОРА | 2020 |
|
RU2737897C1 |
| КАТАЛИЗАТОР ДЛЯ АЛКИЛИРОВАНИЯ БЕНЗОЛА ПРОПИЛЕНОМ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 1995 |
|
RU2097129C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬДЕГИДОВ | 2002 |
|
RU2212396C1 |
| СПОСОБ ГИДРОПЕРЕРАБОТКИ НЕФТЯНЫХ ФРАКЦИЙ | 1999 |
|
RU2148611C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ МОНОАЛЬДЕГИДОВ | 2002 |
|
RU2205174C1 |
| СПОСОБ ПЕРЕРАБОТКИ НЕФТЯНЫХ ДИСТИЛЛЯТОВ (ВАРИАНТЫ) | 2001 |
|
RU2181750C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОТОРНЫХ ТОПЛИВ (ВАРИАНТЫ) | 2003 |
|
RU2235755C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6-ТРИМЕТИЛБЕНЗОХИНОНА И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2164510C1 |
Изобретение относится к области синтеза цеолита Бета, который находит широкое применение в качестве катализатора в процессах нефтепереработки, основной и тонкой органической химии, а также в качестве адсорбента. Способ получения цеолита Бета включает гидротермальную кристаллизацию реакционной смеси, содержащей воду, щелочь, источник кремния, источник изоморфнозамещающего кремний элемента и тетраэтиламмонийную соль, анион которой имеет положительную гидратацию, или применяют смесь тетраэтиламмонийных солей, имеющих хотя бы один анион, обладающий положительной гидратацией. Источник изоморфнозамещающего кремний элемента представляет собой соединение алюминия, и/или бора, и/или галлия, и/или железа, и/или ванадия, и/или титана, и/или их любую смесь. Изобретение решает задачу упрощения получения цеолита Бета без снижения качества получаемого цеолита и без ухудшения эффективности проведения процесса синтеза. 2 з.п. ф-лы, 2 табл.
| WO 9426663 А1, 24.11.1994 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТА БЕТА | 1996 |
|
RU2116250C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТА БЕТА | 1998 |
|
RU2151101C1 |
Авторы
Даты
2003-10-27—Публикация
2002-12-18—Подача