Изобретение относится к области материаловедения фотолюминофоров с длительным послесвечением, излучающих свет в течение многих часов после прекращения действия возбуждающего света. Подобные материалы также называют светонакопительными и они предназначены для использования в системах аварийного и автономного освещения, в различных эвакуационных указателях и элементах одежды при пожаротушении, в устройствах и конструкциях дорожного оповещения, рекламы и т.д.
Современные фотолюминофоры (ФЛ) с длительным послесвечением представляют собой алюминатные системы, активированные комбинацией из редкоземельных элементов Ln (Ln - элементы Периодической системы ряда лантана (La)), отличающихся друг от друга величиной сродства к электрону. Один из элементов входит в кристаллическую матрицу люминофора, образуя центр свечения, является активатором, другой, образуя ловушку для электронов или дырок, является соактиватором.
Известен фотолюминофор состава MeAl2O4 : Eu, Ln (пат. US 5424006, 1995 г. ), где Me - Sr, Ca, Ba, Mg. Кроме лантаноидов Ln в качестве соактиваторов могут также использоваться олово (Sn) и висмут (Bi). Этот ФЛ является структурным и формульным аналогом шпинели, излучательными центрами в нем являются центры Eu2+. Центры обладают интенсивным поглощением в фиолетово-синей области спектра и имеют широкую полосу желто-зеленой люминесценции. После прекращения возбуждения ФЛ светом, в течение нескольких часов наблюдается интенсивная фосфоресценция (длительное желто-зеленое послесвечение). Наибольшее значение интенсивности послесвечения достигается при использовании в качестве соактиватора Dy3+. В описании патента подчеркивается, что оптимальные свойства соответствуют только стехиометрическому составу при соотношении Σ(MeO+EuO)/Σ(Аl2O3+Ln2О3), равном 1:1.
Описанный в патенте ФЛ имеет высокую эффективность фосфоресценции, однако указанному составу фотолюминофора свойственны недостатки и прежде всего плохая устойчивость к воздействию влаги. Люминофор быстро теряет яркость в водно-эмульсионных красках либо в водном растворе, выделяя в раствор ионы стронция, образующие нерастворимую гидроокись стронция. При подобных гидролитических реакциях полностью теряются и накопительные свойства фотолюминофора, фосфоресценция исчезает.
Известен фотолюминофор состава Sr2Al10O17:Eu,Dy (пат. US 5665793, 1997 г. ) Изобретатели данного патента полагали, что устранению недостатка в виде гидролитической неустойчивости соединения типа шпинели способствует введение в состав шпинели дополнительного количества оксида Аl2О3 при стехиометрическом соотношении молярных концентраций [Аl2О3]/[SrO]=2,5. Новый люминофор, содержащий Еu+2 и Dy+3, по сравнению с алюминатом стронция SrAl2O4:Eu+2,Dy+3 имеет сдвинутые в коротковолновую область спектры возбуждения и излучения с максимумом излучения, соответствующим длине волны λ = 485-495 нм. Технология изготовления подобного фотолюминофора близка к ранее описанной для состава стронция SrAl2О4:Eu+2,Dy+3. Изменение формульного состава ФЛ позволило несколько повысить его гидролитическую стойкость, однако получить устойчивое химическое соединение и стабильный фотолюминофор не удалось. Кроме того, для состава Sr2Al10O17:Eu+2,Dy+3 характерно значительное уменьшение люмен-эквивалента фосфоресценции, а следовательно, и световой эффективности.
Известен фотолюминофор состава (МеО) (ХО) (Аl2О3) (В2О3):Еu, Ln (пат. US 6117362, ), где ХО-ZnO и MgO. В состав дополнительно введены элементы второй (Zn, Mg) и третьей (В) группы. Подобный ФЛ имеет более высокую эффективность фосфоресценции, чем предыдущий аналог, излучает в желто-зеленой области спектра, однако уступает ему по параметрам гидролитической стойкости. После контакта с водой люминесцентные свойства ФЛ значительно ухудшаются, эксплуатация люминофора в условиях внешнего атмосферного воздействия затруднена.
Причины плохой гидролитической стойкости алюмината стронция связаны не только с химической активностью стронция по отношению к воде, но и со структурными особенностями алюминатов, а именно:
- сильно деформированными тетраэдрами АlО4;
- напряжениями в структуре, возникающими за счет искажения связей в Sr-О октаэдрах;
- наличием крупных полостей в реальной кристаллической структуре (примерный радиус 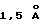 ).
).
Так как размер молекулы воды составляет не более 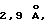 то молекулы воды легко проникают в структуру ФЛ и вступают в реакцию со щелочноземельными ионами, разрушая люминофор. Гидролитическая активность материала напрямую зависит от наличия полостей в кристаллической решетке и заполнения этих полостей стабилизирующими состав примесями.
то молекулы воды легко проникают в структуру ФЛ и вступают в реакцию со щелочноземельными ионами, разрушая люминофор. Гидролитическая активность материала напрямую зависит от наличия полостей в кристаллической решетке и заполнения этих полостей стабилизирующими состав примесями.
Замедление процесса гидратации можно, по нашему мнению, осуществить с помощью введения в решетку одновалентных атомов щелочных элементов. При замещении Sr+2(Ba+2,Ca+2) на Na+(Li+,К+) в решетке алюмината происходит обмен иона на ион. Баланс же валентностей осуществляется за счет второго, формально не изоморфного, иона Na+, располагающегося по соседству в пустотах структуры, так чтобы соблюдалась схема Sr+2←→2 Na+. Чем больше ионов Na+ проникает в решетку алюмината и замещает стронций, чем больше этих ионов располагается в полостях структуры для компенсации заряда, тем меньше остается пустот решетки для проникновения воды и тем слабее протекает процесс гидратации алюмината.
Известно также, что под воздействием примесей в алюминатах происходит перестройка типа кристаллической решетки. Так введение дополнительно натрия в виде Na2O в трехкальциевый алюминат 3CaO•Al2O3 в концентрации до 5 вес.% приводит к последовательной перестройке структуры от кубической до ромбоэдрической, тетрагональной и моноклинной сингоний, т.е. от менее плотной к более плотной решетке [2] . Этот процесс благоприятен также для повышения гидроустойчивости материала.
По нашим данным аналогичный переход к более плотным структурам происходит и в алюминате стронция при введении в его решетку щелочных металлов. Исходные образцы SrAl2O4 кубические, но уже при концентрации Σ[Na][K]/[Sr]= 0,1 ат. % они представляют собой многофазную смесь кубической, гексагональной, тетрагональной и моноклинной сингоний, а при концентрации Σ[Na][K]/[Sr] >1 ат.% доминирует моноклинная фаза. Люминесцентные характеристики материала при этом практически не изменяются, а влагостойкость увеличивается.
Техническая задача, решаемая посредством настоящего изобретения, состоит в создании стабильного эффективного фотолюминофора с длительным послесвечением, обладающего повышенной гидролитической стойкостью, способного работать в различных покрытиях, эксплуатируемых в условиях атмосферного воздействия.
Технический результат, достигаемый при реализации указанного изобретения, состоит в широком использовании стабилизированного фотолюминофора с высокой яркостью и большой длительностью послесвечения в различных изделиях народно-хозяйственного назначения: красках, лаках, пластмассах, облицовочных плитках, подвергающихся интенсивным атмосферным воздействиям (дождь, град, снег и др.).
Указанный технический результат достигается использованием фотолюминофора на основе алюмината стронция, активированного европием и соакгивированного редкоземельными элементами Периодической системы, в состав которого дополнительно введены стабилизирующие примеси щелочных металлов с получением общей формулы
(SrO)1-x-2y-z(Eu0)x(Ln2O3)у(K2O)z(Аl2Oз)1-q(В2O3)q,
где Ln - Dy,Nd;
K - Na, K, Li;
х=0,005-0,1;
у=0,005-0,1;
z=0,002-0,1;
q=0,005-0,1.
Примесь европия входит в кристаллическую структуру материала преимущественно в виде двухзарядных ионов Еu2+, образуя центр свечения, а лантаноиды входят в кристаллическую структуру материала преимущественно в виде трехзарядных ионов Ln3+. Щелочные металлы, входящие в состав, обеспечивают компенсацию зарядов и электронейтральность структуры с заполнением катионных вакансий (пустот). Такая комбинация обеспечивает стабильность люминофора.
Синтез фотолюминофора.
Высокие светотехнические и светонакопительные свойства предлагаемого фотолюминофора реализуются при тщательно проведенном синтезе этого материала. Для проведения этой операции используются специально подготовленные материалы высокой чистоты:
СаСО3 с содержанием основного вещества - 99,5%
SrCOs -" - - 99,5%
Аl(ОН)3 -"- - 99,8%
Еu2O3 -" - - 99,999%
Nd2O3 - 99,999%
Dу2O3 - 99,99%
Na2CO3 - 99,5%
Na2O - 99,5%
К2СОз - 99,5%
К2O - 95%
Li2СО3 - 95%
В соответствии с рецептурой предлагаемого фотолюминофора взвешивают расчетные количества исходных реактивов, тщательно их перемешивают, загружают в тигли (контейнеры) объемом 1500 или 2000 мл. В каждом из таких тиглей дополнительно размещается необходимое количество активного угля, способствующего протеканию реакций
Н2O+С-->2+СO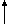 ,
,
СO2+С-->2СО,
в процессе которых внутри тигля (контейнера) устанавливается восстановительная атмосфера, необходимая и способствующая протеканию реакции
Еu2O3+СO-->2EuO+CO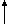 ,
,
Еu2O3+H2-->2EuO+H2O.
Восстановительная атмосфера из СО и Н2, создаваемая внутри каждого тигля, существенно дешевле и удобнее, чем использование специальных печей с подачей в них осушенного Н2-газа либо смеси газов N2 + Н2.
Для облегчения протекания твердофазного синтеза в состав шихты можно добавлять плавни. В качестве плавня обычно используют SrF2. Роль плавня может выполнять также реагент содержащий бор, например борная кислота.
Пример 1. Получение фотолюминофора оптимального состава.
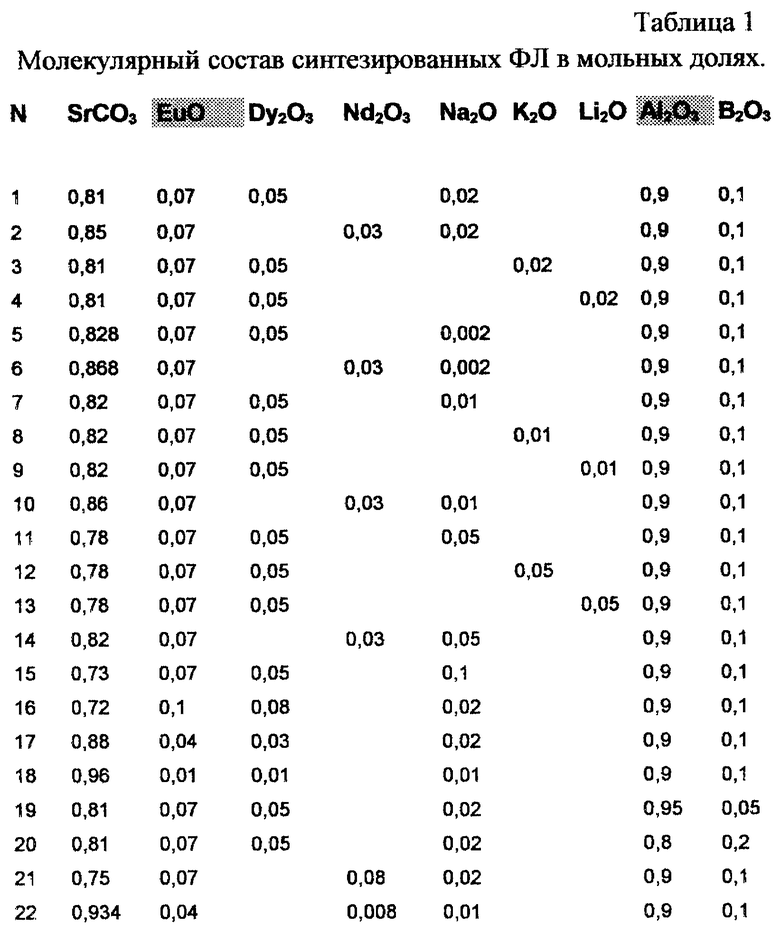
Смешивают 0,81М SrСО3, 0,035М Еu2О3, 0,05М Dy2О3, 0,02М Na2О, 1,8М Аl(ОН)3, 0,2М H3BO3, перетирают их в аттриторе до полной гомогенности. Далее шихту загружают в 2000 мл тигель, утрамбовывают до насыпной плотности 1,2 г/см3, затем в тигель загружают до 10 г активированного угля, закрывают тигель крышкой и загружают в нагретую до 500oС печь. Скорость подъема температуры в печи составляет 10o/мин.
Выдержку шихты в печи проводят в течение 120 минут при Т=1320oС, после чего печь охлаждают до 700oС. Содержимое тиглей закаливают охлаждением в проточной дистиллированной воде. Королек люминофора разбирают под УФ-лампой, далее диспергируют в мельнице, после чего измеряют параметры материала в специальной установке при дозированной внешней засветке. Параметры образцов приведены в таблице 1.
Пример 2. Смешивают 0,85М SrСО3, 0,035М Еu2О3, 0,03М Nd2O3 0,02M Na2О, 1,8М Аl(ОН)3, 0,2М H2BO3. Остальные операции аналогичны приведенным примере 1.
Пример 3. Смешивают 0,81М SrСО3, 0,035М Еu2О3, 0,05М Dу2О3, 0,02М K2O, 1,8М Аl(ОН)3, 0,2М НВО3. Остальные операции, как в примере 1.
Пример 4. Смешивают 0,81 М SrСО3, 0,035М Еu2O3, 0,05М Dу2О3 , 0,02М Li2CО3, 1,8М Аl(ОН)3, 0,2М H3ВO3. Остальные операции, как в примере 1.
Пример 5. Смешивают 0,828М SrСО3, 0,035М Еu2O3, 0,05М Dу2O3, 0,002М Na2O, 1,8М Аl(ОН),3 0,2М H3BО3. Остальные операции, как в примере 1.
Пример 6. Смешивают 0,868М SrСO3, 0,035М Eu2O3, 0,03M Nd2O3, 0,002М Na2O, 1,8М Аl(ОН)3, 0,2М H3BО3. Остальные операции, как в примере 1.
Пример 7. Смешивают 0,82М SrСO3, 0,035М Eu2O3, 0,05M Dу2O3, 0,01 М Na2O, 1,8М Аl(ОН)3, 0,2М H3BO3. Остальные операции, как в примере 1.
Пример 8. Смешивают 0,82М SrСО3, 0,035М Еu2O3, 0,05М Dу2O3, 0,01 М К20, 1,8М Аl(ОН)3, 0,2М Н3ВО3. Остальные операции, как в примере 1.
Пример 9. Смешивают 0,82М SrCO3, 0,035М Еu2O3, 0,05М Dу2O3 ,0,01 М Li2CO3, 1,8М Аl(ОН)3, 0,2М Н3BO3. Остальные операции, как в примере 1.
Пример 10. Смешивают 0,86М SrСО3, 0,035М Еu2O3 0,03М Nd2O3, 0,01 М Na2O, 1,8М Аl(ОН)3, 0,2М H3BO3 . Остальные операции, как в примере 1.
Пример 11. Смешивают 0,73М SrСО3, 0,035М Eu2O3, 0,05M Dy2O3, 0,05М Na2O, 1,8М AI(OH)3, 0,2М H3BO3. Остальные операции, как в примере 1.
Пример 12. Смешивают 0,78М SrCO3, 0,035M Eu2O3, 0,05М Dy2O3, 0,05М К2O, 1,8М Аl(ОН)3, 0,2М Н3ВО3. Температура термообработки 1350oС. Остальные операции, как в примере 1.
Пример 13. Смешивают 0,78М SrСО3, 0,035M Eu2O3, 0,05M Dy2O3, 0,05М Li2CO3, 1,8М AI(OH)3, 0,2M Н3BО3. Температура термообработки 1340oС. Остальные операции, как в примере 1.
Пример 14. Смешивают 0,82М SrСО3, 0,035M Eu2O3, 0,03M Nd2O3, 0,05М Na2O, 1,8М AI(OH)3, 0,2М Н3ВО3. Остальные операции, как в примере 1.
Пример 15. Смешивают 0,73М SrCO3, 0,035M Eu2O3, 0,05М Dy2O3, 0,1М Na2O, 1,8М Аl(ОН)3, 0,2М Н3ВO3. Остальные операции, как в примере 1.
Пример 16. Смешивают 0,72М SrCO3, 0,05M Eu2O3, 0,08M Dy2O3, 0,02М Na2O, 1,8М Аl(ОН)3, 0,2М H3ВО3. Остальные операции, как в примере 1.
Пример 17. Смешивают 0,88М SrСО3, 0,02М Eu2O3, 0,03М Dy2O3, 0,02М Na2O, 1,8М AI(OH)3, 0,2M H3BO3. Остальные операции, как в примере 1.
Пример 18. Смешивают 0,95М SrСО3, 0,005М Eu2O3, 0,01 М Dy2O3, 0,01M Na2O, 1,8M Al(OH)3, 0,2M H3BO3. Остальные операции, как в примере 1.
Пример 19. Смешивают 0,81 M SrCO3, 0,035M Eu2O3, 0,05M Dy2O3, 0,02М Na2O, 1,9M AI(OH)3, 0,1M H3BO3. Остальные операции, как в примере 1.
Пример 20. Cмешивают 0,81M SrCO3 , 0,035M Eu2O3, 0,05M Dy2O3, 0,02 Na2O, 1,6М Al(OH)3, 0,4М Н3ВО3. Остальные операции, как в примере 1.
Пример 21. Смешивают 0,75М SrCO3, 0,035M Eu2O3, 0,08M Nd2O3, 0,02М Na2O, 1,8М Аl(ОН)3, 0,2М H3BO3. Остальные операции, как в примере 1.
Пример 22. Смешивают 0,934М SrСО3, 0,02М Eu2O3, 0,008М Nd2O3, 0,01 М Na2O, 1,8М Al(OH)3, 0,2M H3BO3. Остальные операции, как в примере 1.
Кроме перечисленных примеров проведения синтеза образцов ФЛ по сути предлагаемого изобретения, синтезировался также оптимальный образец по пат. USA 5424006. Этот образец использовался далее для сравнительного анализа характеристик новых образцов.
Химический состав синтезированных образцов отражен в сводной табл. 1.
Все образцы исследовались по параметрам влагостойкости и светотехническим параметрам фосфоресценции в течение 30 минут после прекращения облучения.
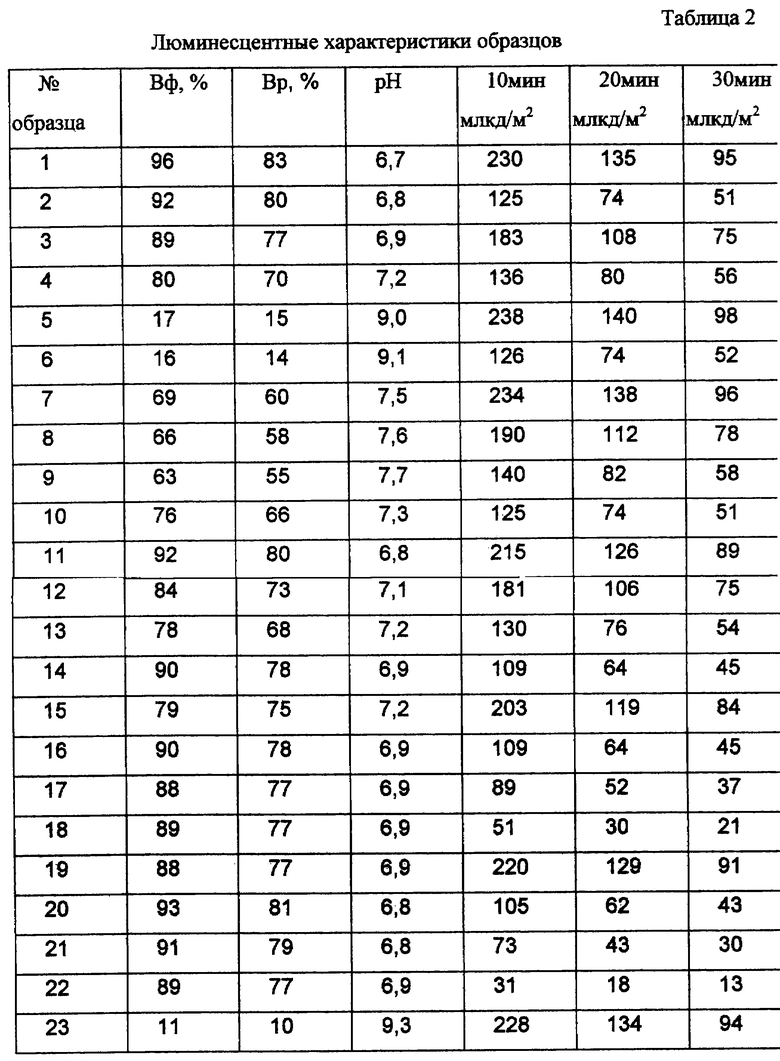
Гидролитическую устойчивость ФЛ контролировали погружением порошка люминофора в воду на 1 час и определением концентрации ионов водорода (рН). Величина рН водной вытяжки в растворе колебалась в пределах 9,1 (образец 6) - 6,7 (образец 1) единиц, тогда как известный материал SrAl2O4:Eu:Dy (образец 23) обычно имеет щелочную реакцию (рН 9,3) и переходит в течение 1 часа в желеобразное состояние.
Влагостойкость образцов Вр определяли косвенно с помощью рентгеновского метода по относительной интегральной интенсивности максимумов брэгговских отражений ((2θ = 35,15o) до и после взаимодействия ФЛ с водой в течение 1 часа [3] . Параметр влагостойкости Вф определяли также и по остаточной величине относительной эффективности (яркости) фосфоресценции через 30 минут после облучения светом D65 при освещенности 250 люкс в течение 30 минут. Параметры влагостойкости и рН образцов люминофоров после часовой выдержки в воде предоставлены в табл.2. Введение в состав ФЛ дополнительно щелочных металлов К в атомной концентрации, приближенно соответствующей концентрации лантаноидов, образующих трехзарядные центры, повышает влагостойкость люминофора. Предлагаемый состав имеет значительно большую влагостойкость чем образец 23, соответствующий лучшему варианту из известных составов. Наибольшей влагостойкостью обладают люминофоры, в структуру которых введен Na. Увеличение концентрации вводимого Na (К) более z=0,02 обычно снижает люминесцентные характеристики материала, вероятно из-за уменьшения доли Eu+2 в подрешетке стронция. Для Li ухудшение люминесцентных характеристик наблюдается при концентрации z>0,01.
Затухание описывается обычным степенным законом Беккереля с показателем n=0,9-1,1. Щелочные металлы вплоть до концентраций 2 мол.% не ухудшают яркостные свойства люминофора.
Кинетические характеристики послесвечения образцов измерялись после облучения ФЛ источником света D65 при освещенности 250 люкс в течение 30 мин. Величины остаточной яркости послесвечения ФЛ в млкд/м2 через 10, 20 и 30 мин также представлены в табл.2. Наивысшими значениями параметров обладает образец, синтезированный в примере 1, который и представляет оптимальный вариант предлагаемого фотолюминофора. Светотехнические параметры этого образца соответствуют лучшему варианту, выполненному по известному патенту (образец 23).
Дополнительное введение в формулу ФЛ примеси бора (В2O3), замещающего алюминий, позволяет частично устранить пагубное влияние нестехиометричности состава и несколько повысить яркость послесвечения. Кроме того, введение в состав люминофора легкоплавкого оксида В2O3, позволяет понизить температуру синтеза и улучшить накопительные характеристики люминофора, особенно при возбуждении ФЛ светом ламп накаливания.
Предлагаемый фотолюминофор при возбуждении в течение 15 минут светом с освещенностью 250 люкс накапливает светосумму, достаточную для наблюдения послесвечения в течение 16 часов и более. Время затухания ФЛ до уровня 1 млк/м2 превышает 12 часов.
Новый материал может найти применение
- для покраски крупных сооружений и конструкций, таких как морские платформы, причальные стенки портовых сооружений, нефтяные вышки и т.д.;
- для специальной одежды водолазов, пожарных, шахтеров и т.п.;
- для крыш зданий и сооружений, предназначенных для ориентировки с воздуха, посадочных площадок, разметки дорог, авиаполос.
| название | год | авторы | номер документа |
|---|---|---|---|
| Фотостимулируемое люминесцентное соединение | 2022 |
|
RU2797662C1 |
| ФОТОЛЮМИНОФОР С ДЛИТЕЛЬНЫМ ПОСЛЕСВЕЧЕНИЕМ | 2001 |
|
RU2192444C2 |
| ФОТОЛЮМИНОФОР СО СВЕРХДЛИТЕЛЬНЫМ ПОСЛЕСВЕЧЕНИЕМ | 2000 |
|
RU2194736C2 |
| ФОТОНАКОПИТЕЛЬНЫЙ ЛЮМИНОФОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2236434C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЮМИНОФОРА С ДЛИТЕЛЬНЫМ ПОСЛЕСВЕЧЕНИЕМ | 2016 |
|
RU2634024C1 |
| ФОТОЛЮМИНОФОРЫ ДЛЯ КОРОТКОВОЛНОВЫХ СВЕТОИЗЛУЧАЮЩИХ ДИОДОВ (СИД) | 2004 |
|
RU2315078C2 |
| КРАСНОИЗЛУЧАЮЩИЙ ФОТОЛЮМИНОФОР ДЛЯ ЭКРАНОВ ПЛАЗМЕННЫХ ПАНЕЛЕЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2236432C2 |
| СИНЕИЗЛУЧАЮЩИЙ ФОТОЛЮМИНОФОР ДЛЯ ЭКРАНОВ ПЛАЗМЕННЫХ ПАНЕЛЕЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2236433C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕКОРАТИВНОГО ПОКРЫТИЯ, СОДЕРЖАЩЕГО ЛЮМИНОФОРЫ (ВАРИАНТЫ) | 2010 |
|
RU2416529C1 |
| БЕСЦВЕТНЫЕ ПРИ ДНЕВНОМ ОСВЕЩЕНИИ ЛЮМИНЕСЦЕНТНЫЕ КРАСКИ ДЛЯ ХУДОЖЕСТВЕННЫХ РАБОТ | 2010 |
|
RU2429263C1 |
Изобретение предназначено для материаловедения и может быть использовано при изготовлении систем аварийного и автономного освещения, эвакуационных указателей, элементов спецодежды, дорожного освещения, рекламы. Фотолюминофор на основе бороалюмината стронция, активированный двухзарядными ионами европия и соактивированный трехзарядными ионами редкоземельных элементов, содержащий по меньшей мере один оксид щелочного металла и имеет общую формулу (SrO)1-x-2y-z (EuO)x (Ln2O3)y (Me2O)z(Al2O3)1-q(B2O3)q, где Ln - Dy или Nd; Me - Na, K, Li; x=0,005-0,1; y=0,005-0,1; z=0,002-0,1; q=0,005-0,1. Оксиды европия(III), диспрозия(III) и щелочного металла смешивают с карбонатом стронция, гидроксидом алюминия и борной кислотой в соответствующих мольных долях. Гомогенизируют. Загружают в тигель, засыпают активированным углем, закрывают крышкой. Прокаливают при 1320oС 120 мин. Охлаждают, диспергируют. Фотолюминофор гидролитически устойчив, при возбуждении в течение 15 мин накапливает светосумму, достаточную для наблюдения послесвечения в течение 15 ч и более. Время затухания фотолюминесценции превышает 12 ч. 2 табл.
Фотолюминофор на основе бороалюмината стронция, активированный двухзарядными ионами европия и соактивированный трехзарядными ионами редкоземельных элементов, содержащий, по меньшей мере, один оксид щелочного металла, отличающийся тем, что он имеет общую формулу
(SrO)1-x-2y-Z(EuO)x(Ln2O3)y(Me2O)Z(Al2O3)1-q(B2O3)q,
где Ln - Dy или Nd;
Me - Na, K, Li;
x = 0,005 - 0,1;
y = 0,005 - 0,1;
z = 0,002 - 0,1;
q = 0,005 - 0,1.
| US 6117362 A, 12.09.2000 | |||
| RU 2001103025 A, 27.07.2001 | |||
| RU 20024570 C1, 15.12.1994 | |||
| US 5424006 A, 13.06.1995 | |||
| US 5611959 A, 18.03.1997 | |||
| US 5665793 A, 09.09.1997 | |||
| US 6284156 A, 04.09.2001 | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Устройство для питания нагрузки | 1978 |
|
SU765925A2 |
| АХМЕТОВ Н.С | |||
| Неорганическая химия | |||
| - М.: Высшая школа, 1975, с.510, 520, 528. | |||
Авторы
Даты
2003-11-27—Публикация
2001-12-14—Подача