За последние годы усилился интерес к получению диметилового эфира (ДМЭ) как промежуточного продукта для получения моторного топлива или в связи с прогнозируемым его использованием непосредственно как экологически чистого топлива.
В промышленности осуществлен синтез диметилового эфира дегидратацией метанола на высококремнистых цеолитах. Вместе с тем, опубликован ряд патентов по каталитическому синтезу диметилового эфира из оксидов углерода и водорода, в отдельных случаях с добавлением водяного пара.
Процесс синтеза ДМЭ включает реакции гидрирования оксидов углерода до метанола, конверсии оксида углерода водяным паром и дегидратации метанола в ДМЭ. Для осуществления такого процесса необходимы катализаторы, обладающие полифункциональными свойствами, которые должны обеспечивать протекание всех перечисленных реакций.
В известных патентах указывается на применение для этих целей оксида алюминия и катализаторов синтеза метанола.
В качестве катализаторов применяют, как правило, медь-цинк-хромовые, медь-цинк-хром-алюминиевые или медь-цинк-хром-алюмосиликатные системы.
Во всех случаях катализаторы получают соосаждением компонентов из азотно-кислых растворов с последующей отмывкой осадков, их сушкой, прокаливанием и таблетированием, раздельным осаждением гидрирующих и дегидратирующих компонентов с последующим их смешением (пат. ФРГ 3118620) или с использованием их раздельно, путем загрузки в реактор чередующимися слоями катализатора, обладающего гидрирующей функцией, и дегидратирующего катализатора (Пат. Италии 929006). При этом в состав катализатора входят карбонаты (основные карбонаты) и/или гидроксиды металлов, которые при последующей прокалке превращаются в оксиды (смешанные оксиды).
Кроме таких недостатков вышеуказанных способов, как значительные затраты в производстве, связанные с расходом чистого конденсата или деминерализованной воды на отмывку осадков, сложности при дальнейшей переработке фильтрата и использовании промывных вод, содержащих примеси цветных металлов, полученные с помощью этих способов катализаторы обладают недостаточной стабильностью в процессе синтеза диметилового эфира, и их приходится регенерировать непосредственно в процессе синтеза через небольшой промежуток времени (40-60 ч), что осложняет процесс, ведет к уменьшению выработки продукции и дополнительным затратам (Пат. США 2097382 и Германии 3118620).
Наиболее близким к предлагаемому катализатору является медь-цинк-хром-алюминиевый катализатор, полученный по патенту Японии 5071297 В4. Катализатор готовят совместным осаждением цинка и хрома и/или алюминия с получением осадка А и осаждением меди и цинка с хромом и/или алюминием с получением осадка Б. Осадки А и Б совместно диспергируют в воде, затем сушат и прокаливают.
Цель предлагаемого изобретения заключается в разработке стабильного катализатора, обеспечивающего высокую производительность в процессе синтеза диметилового эфира (ДМЭ) и метанола в течение длительного времени.
Указанная цель достигается тем, что для получения катализатора используют следующие исходные компоненты:
- компонент А, полученный обработкой гидроксида алюминия в количестве 5-10 мас.% (в пересчете на оксид алюминия) от общей массы конечного прокаленного катализатора раствором хромового ангидрида;
- компонент Б, представляющий собой аммиачный, либо аммиачно-карбонатный, либо аммиачно-формиатный, либо аммиачно-ацетатный раствор меди и цинка;
- компонент В, в качестве которого используют оксид или гидроксид алюминия, предпочтительно в виде порошка или водной суспензии 1:1,
и катализатор получают путем проведения операций смешения вышеуказанных компонентов, отгонки аммиака или аммиака и углекислоты из раствора при температуре 80-90oС, сушки полученного осадка до текучего состояния и его прокаливания при температуре не выше 380oС, причем смешение компонентов А, Б и В проводят последовательно следующим образом: либо вначале смешивают компоненты А и Б, а компонент В добавляют позже, либо вначале смешивают компоненты Б и В, а в дальнейшем добавляют компонент А, и, при этом, в том случае, когда вначале проводят смешение компонентов А и Б, компонент В добавляют к промежуточному продукту после стадии сушки либо после стадии прокаливания; а операцию отгонки проводят либо после смешения всех трех компонентов, либо после смешения двух компонентов, одним из которых является компонент Б.
Полученный описанным способом катализатор синтеза диметилового эфира и метанола представляет собой медь-цинк-хром-алюминийсодержащий катализатор, предпочтительно следующего состава (в мас. %): СuО - (17,5-35,0); ZnO - (17,5-35,0); Сr2O3 - (12,5-25,0); Al2O3 - (5-52,5) (содержание компонентов дано в пересчете на содержание оксидов в прокаленном катализаторе), в том числе не менее 10 мас.% от массы прокаленного катализатора соединения алюминия с хромом и не менее 10 мас. % соединений хрома с медью и цинком (суммарно).
Таким образом, предлагаемый способ получения катализатора обеспечивает повышенное содержание хрома и алюминия в катализаторе, а также наличие в его составе более стабильных, не разрушающихся в процессе синтеза ДМЭ и метанола компонентов -предпочтительно хромитов меди и цинка (Cu•Zn)Cr2O4 и гидроксохромитов алюминия Аl(ОН)СrO4.
Прокаленный катализатор, содержащий все три компонента А, Б и В, может быть дополнительно обработан раствором соли меди, предпочтительно из расчета введения 2-9% CuO на прокаленный катализатор, а затем снова подвергнут сушке и прокаливанию при тех же условиях.
Преимущества промышленного получения катализатора по способу согласно настоящему изобретению заключаются в том, что:
- не требуется расхода реактива-осадителя, например Nа2СО3;
- нет необходимости в отмывке осадков. Соответственно не требуется дополнительного оборудования для переработки фильтрата в товарный побочный продукт и оборудования для очистки и переработки промывных вод.
Улавливание аммиака и углекислоты осуществляют водой, т.е. наиболее просто по сравнению с другими методами очистки; полученные при этом аммиачные или амиачно-карбонатные растворы возвращают в цикл производства.
Получение катализатора согласно настоящему изобретению иллюстрируется далее примерами, не имеющими ораничивающего характера.
Примеры приготовления катализатора.
Пример 1.
Получение компонента А.
Растворяют в 150 мл Н2О 33 г хромового ангидрида. Добавляют в раствор 15 г размолотого гидроксида алюминия (фракция 0-0,06 мм), перемешивают при 50-70oС в течение 4-6 ч.
Получение компонента Б.
1. Растворяют 28 г меди в 250 мл аммиачно-карбонатного раствора, содержащего 200 г/л NН3 и 150 г/л СO2, при температуре 50-70oС.
2. Растворяют 28 г цинка в 200 мл аммиачно-карбонатного раствора, содержащего 200 г/л NН3 и 150 г/л СО2, при температуре 50-70oС.
3. Сливают оба раствора вместе.
Компонент В.
Гидроксид алюминия в виде порошка в количестве 15 г.
Смешение компонентов.
В полученный раствор компонента Б добавляют компонент В и перемешивают. Затем добавляют компонент А, поднимают температуру в растворе до 90oС и отгоняют аммиак (до остаточного содержания 5 г/л) и углекислоту. Образовавшийся осадок фильтруют, сушат при 100-120oС до сыпучего состояния, перемешивают, прокаливают при температуре не выше 380oС (прокаливание продолжают до тех пор, пока вес отобранной пробы, дополнительно прокаленной при 900oС, не будет меньше ее веса после прокалки при 380oС на 5-6%) и таблетируют.
Состав катализатора после прокалки в пересчете на оксиды: СuО - 30,5, ZnO - 30,5, Сr2O3 - 22, Аl2О3 - 17 мас.%.
Во всех последующих примерах операции получения компонентов А и Б, отгонки аммиака или аммиака и углекислоты, сушки полученного осадка и его прокаливания проводят таким же образом, как описано в примере 1.
Пример 2.
Компонент В - гидроксид алюминия в виде порошка в количестве 15 г.
Смешение компонентов.
В отличие от примера 1, после смешения компонентов Б и В осуществляют отгонку аммиака и углекислоты, осадок фильтруют, смешивают с компонентом А, сушат и прокаливают, как описано в примере 1.
Состав катализатора после прокалки в пересчете на оксиды: CuO - 30,5, ZnO - 30,5, Сr2O3 - 22, Аl2O3 - 17 мас.%.
Примеры 3 и 4.
Операции смешения и последующие операции аналогичны примерам 1 и 2 соответственно.
Отличие состоит в том, что компонент В добавляют в количестве 70 г.
Состав катализатора после прокалки в пересчете на оксиды: CuO - 23,25, ZnO - 23,25, Сr2O3 - 16,6, Аl2О3 - 36,9 мас.%.
Пример 5.
Компонент В - оксид алюминия в виде порошка в количестве 46 г.
Смешение компонентов.
Вначале смешивают компоненты А и Б, отгоняют аммиак и углекислоту, полученный осадок фильтруют и сушат, как описано в примере 1, а затем добавляют компонент В и прокаливают, как описано в примере 1.
Состав катализатора после прокалки в пересчете на оксиды: CuO - 23,25, ZnO - 23,25, Сr2O3 - 16,6, Аl2О3 - 36,9 мас.%.
Пример 6.
Компонент В - как в примере 5.
Смешение компонентов.
Вначале смешивают компоненты А и Б, отгоняют аммиак и углекислоту, полученный осадок отфильтровывают, сушат и прокаливают, как описано в примере 1, а затем добавляют компонент В.
Состав катализатора после прокалки в пересчете на оксиды: СuО - 23,25, ZnO - 23,25, Сr2О3 - 16,6, Аl2О3 - 36,9 мас.%.
Пример 7.
Компонент В - как в примере 5.
Смешение компонентов, как в примере 6.
Полученный катализатор дополнительно обрабатывают раствором соли меди из расчета введения 2-9% CuO (на прокаленный катализатор), с последующей сушкой и прокаливанием при температуре не выше 380oС.
Другое воплощение настоящего изобретения, позволяющее реализовать его цель, представляет собой способ получения ДМЭ и метанола из синтез-газа при повышенных температуре и давлении, в котором используют описанные выше катализаторы.
Далее приведены примеры, иллюстрирующие преимущества, которые достигаются при применении катализаторов по настоящему изобретению в способе синтеза ДМЭ и метанола.
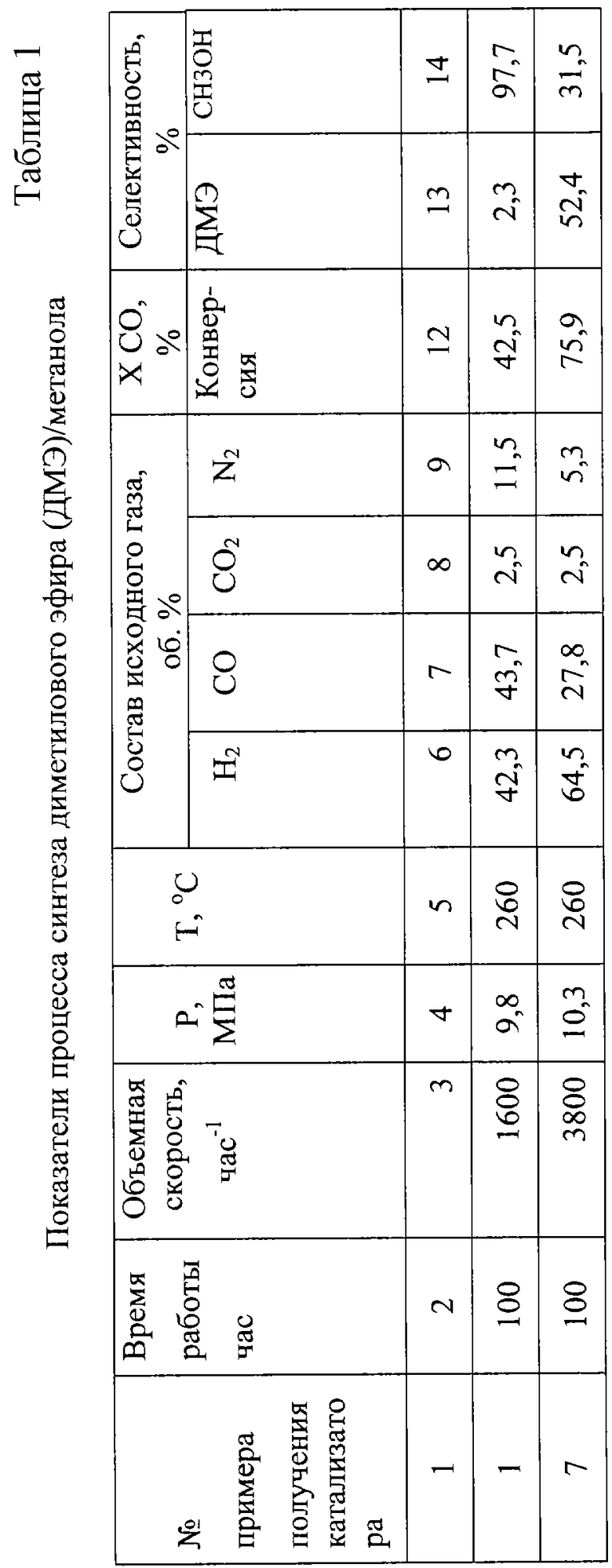
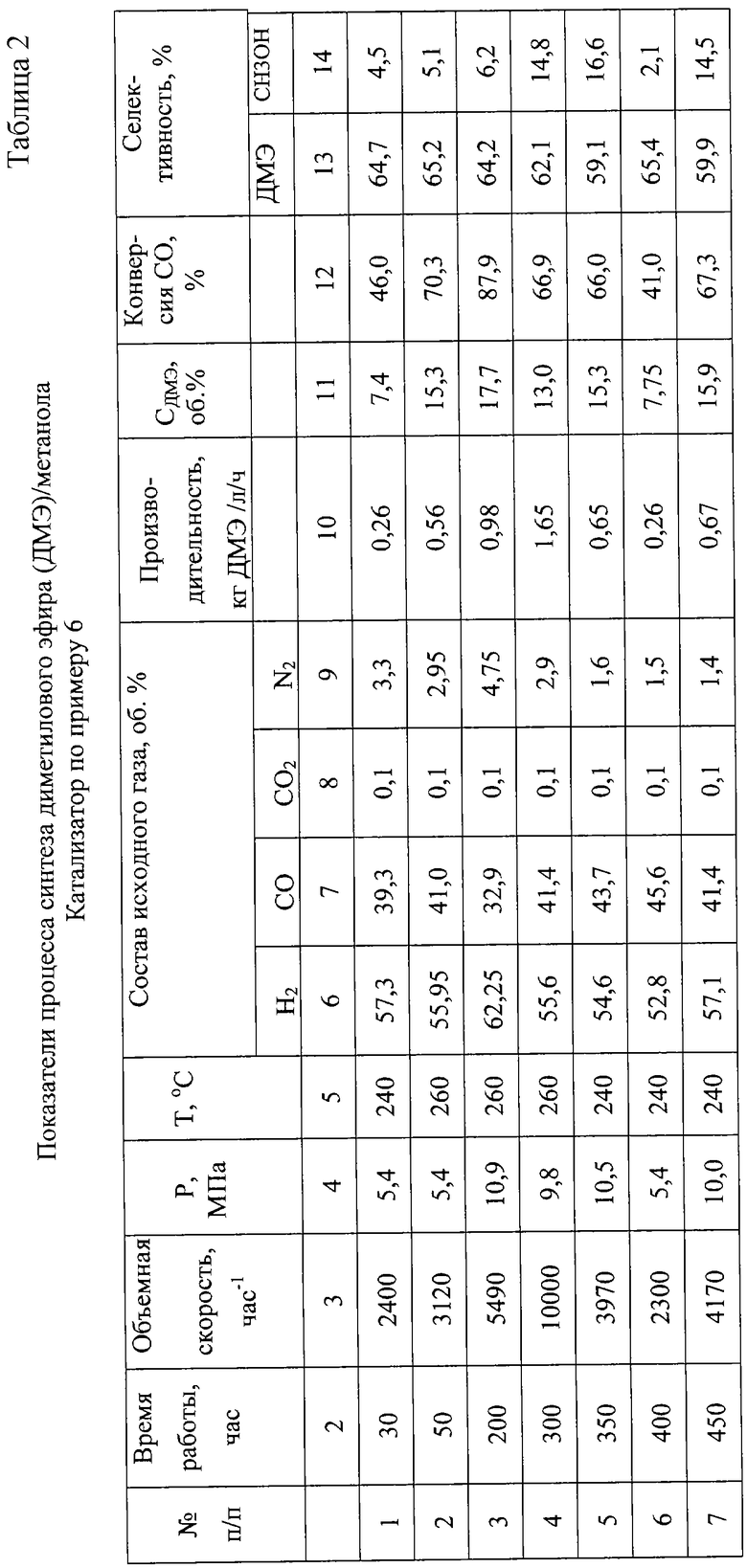
Более подробно, в табл.1 даны условия проведения процесса синтеза смеси ДМЭ и метанола на катализаторах, приготовленных согласно некоторым примерам настоящей заявки, и представлены полученные данные по их активности (конверсия СО) и селективности в названном процессе. В табл.2 приведены результаты для катализатора, приготовленного по примеру 6, полученные в различные моменты времени при его непрерывной работе в течение 450 ч в разных режимах.
Испытания катализаторов (табл.1, 2) проводили в проточных реакторах.
В первой графе табл.1 приведены номера примеров, в которых были получены исследуемые катализаторы. В первой графе табл.2 приведены номера опытов в порядке их проведения.
Во второй графе обеих таблиц приведено суммарное время работы катализатора до снятия показателей процесса синтеза ДМЭ и метанола; в третьей графе - объемная скорость подачи исходного синтез-газа, затем (графы 4, 5 и 6-9) - давление в реакторе, температура и состав исходного синтез-газа соответственно. В графе 10 табл.1 приведена конверсия оксида углерода в процентах, а в графах 11 и 12 - селективность по диметиловому эфиру и метанолу соответственно. В графе 10 табл.2 приведена производительность катализатора по диметиловому эфиру (кг ДМЭ на 1 л катализатора в час). В графе 11 табл.2 дана концентрация диметилового эфира в объемных процентах на выходе из слоя катализатора, в графе 12 - конверсия оксида углерода в процентах, в графах 13 и 14 - селективность по диметиловому эфиру и метанолу.
Как видно из табл.1 и 2, применение заявляемых катализаторов обеспечивает высокую конверсию оксида углерода в проточном реакторе. При этом в зависимости от условий смешения компонентов А, Б, В можно получить на выходе смесь метанола и диметилового эфира с различной селективностью по диметиловому эфиру и метанолу.
Из табл. 2 можно также видеть при сравнении показателей синтеза ДМЭ на приготовленном по примеру 6 катализаторе в различные моменты времени, что после 400 ч работы катализатора его производительность по диметиловому эфиру не изменилась (ср. опыты 1 и 6). Небольшое уменьшение конверсии оксида углерода в опыте 6 связано с увеличением концентрации оксида углерода в исходном газе опыта 6 (45,6 об.% по сравнению с 39,3 об.% в опыте 1). О стабильной работе катализатора свидетельствуют также показатели процесса синтеза ДМЭ для опытов 5 (350 ч работы) и 6 (450 ч работы катализатора).
Следует также отметить, что, как следует из данных табл.2, катализатор обладает не только высокой стабильностью, но и высокой активностью. Так, конверсия оксида углерода в проточном реакторе уже при давлении 5,4 МПа достигает 70,3% (пример 2). При давление 10,9 МПа и объемной скорости 5490 ч-1 конверсия оксида углерода за проход составляет 87,9% при производительности по диметиловому эфиру 0,98 кг ДМЭ/л кат-ра/ч (пример 3).
Таким образом, результаты испытаний показали, что предлагаемый катализатор в течение 450 ч практически не теряет своей активности и селективности по отношению к синтезу ДМЭ (табл.2). В то же время, в процессе известного уровня техники регенерацию катализатора приходится проводить через 40-60 ч, предпочтительно ежесуточно (пат. США 2097382 и пат. Германии 3118620), т.е. через примерно на порядок более короткие периоды времени.
При этом при увеличении объемной скорости до 10000 ч-1 при оптимальной температуре (260oС) и давлении 9,8 МПа достигается чрезвычайно высокая производительность катализатора по ДМЭ - 1,65 кг/л/ч, при степени превращения оксида углерода в проточном реакторе (за проход) 67%. Эта производительность в несколько раз превышает наилучшие показатели запатентованных способов. В частности, для сравнения можно указать, что достигнутая производительность по метанолу по общепринятой в настоящее время в мире технологии при близком давлении 8 МПа составляет 0,4 кг/кг/ч, тогда как на предлагаемом катализаторе в пересчете на производимый метанол она составляет более 2 кг/л/ч (или 2 кг/кг/ч, с учетом того, что плотность катализатора по изобретению близка к 1).
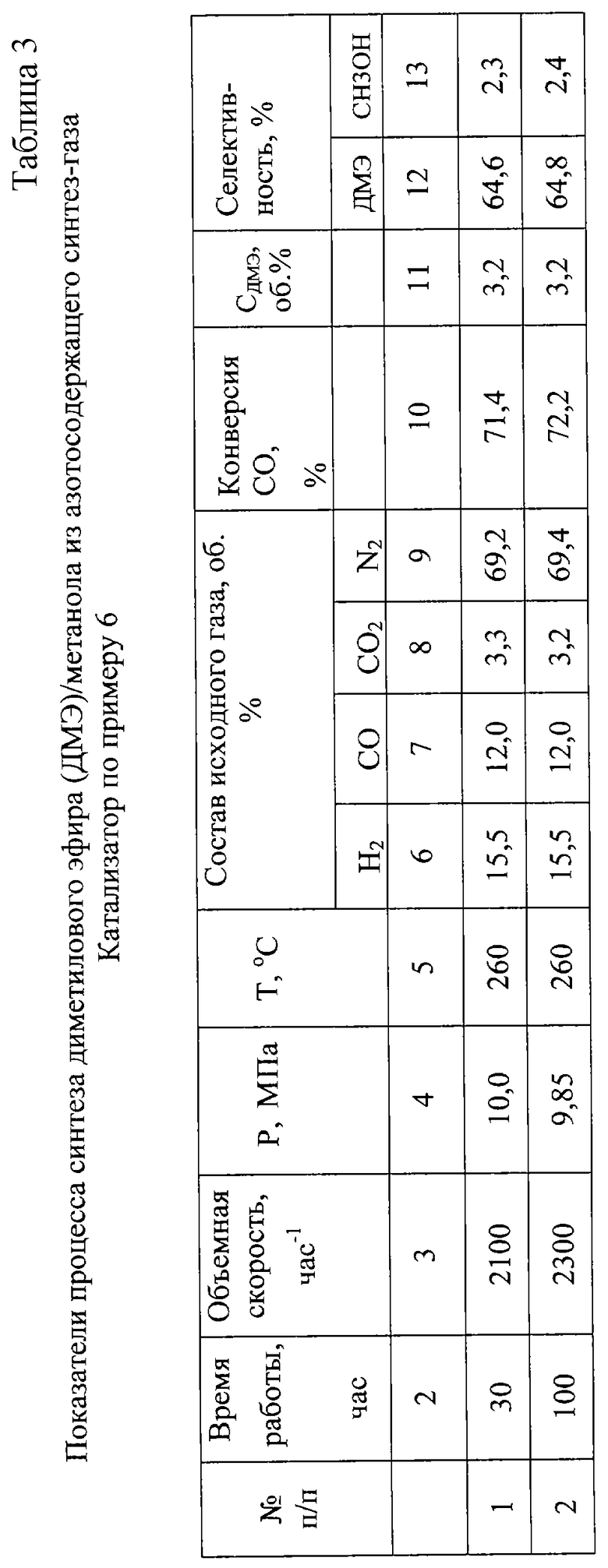
Кроме того, дополнительное преимущество способа синтеза ДМЭ и метанола согласно настоящему изобретению состоит в том, что можно использовать синтез-газ произвольного состава. Предлагаемые катализаторы позволяют перерабатывать синтез-газ, содержащий вплоть до 70% азота, полученный воздушным окислением метана, с высокой конверсией за проход - свыше 70% (практически до равновесия). Соответствующий пример приведен в табл.3 для катализатора по примеру 6 (обозначения те же, что и в табл.1, 2). В отличие от этого, описанные здесь известные процессы проводятся с применением синтез-газа, практически не разбавленного азотом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДОВ БЕНЗИНОВОГО РЯДА ИЗ ПОПУТНОГО НЕФТЯНОГО ГАЗА ЧЕРЕЗ СИНТЕЗ-ГАЗ И ОКСИГЕНАТЫ | 2015 |
|
RU2616981C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕДЬЦИНКХРОМАЛЮМИНИЕВОГО КАТАЛИЗАТОРА | 2016 |
|
RU2642788C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОБОГАЩЕННОГО ВОДОРОДОМ ГАЗОВОГО ПОТОКА | 2004 |
|
RU2386583C2 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕТИЧЕСКОЙ НЕФТИ ИЗ ПРИРОДНОГО ИЛИ ПОПУТНОГО НЕФТЯНОГО ГАЗА (ВАРИАНТЫ) | 2016 |
|
RU2649629C1 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВ ИЗ ДИМЕТИЛОВОГО ЭФИРА В ЕГО ПРИСУТСТВИИ | 2008 |
|
RU2391135C1 |
| Способ регенерации катализатораКОНВЕРСии ОКиСи углЕРОдА илиСиНТЕзА МЕТАНОлА | 1977 |
|
SU806106A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛОВОГО ЭФИРА МЕТОДОМ ОДНОСТАДИЙНОГО СИНТЕЗА И ЕГО ВЫДЕЛЕНИЯ | 2013 |
|
RU2528409C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКОЛОГИЧЕСКИ ЧИСТОГО ВЫСОКООКТАНОВОГО БЕНЗИНА | 2010 |
|
RU2442767C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ КОНВЕРСИИ ОКИСИ УГЛЕРОДА С ВОДЯНЫМ ПАРОМ | 1983 |
|
SU1152127A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОТОРНЫХ ТОПЛИВ ИЗ УГЛЕРОДСОДЕРЖАЩЕГО СЫРЬЯ | 1998 |
|
RU2143417C1 |
Катализатор синтеза диметилового эфира и метанола из синтез-газа на основе медь-цинк-хром-алюминиевой системы, отличающийся тем, что он приготовлен путем смешения компонента А, полученного обработкой гидроксида алюминия в количестве 5-10 мас.% (в пересчете на оксид алюминия) от общей массы раствором хромового ангидрида, компонента Б, представляющего собой аммиачный, либо аммиачно-карбонатный, либо аммиачно-формиатный, либо аммиачно-ацетатный раствор меди и цинка, и компонента В, в качестве которого используют оксид или гидроксид алюминия; отгонки аммиака или аммиака и углекислоты из раствора; сушки полученного осадка и его прокаливания при температуре не выше 380oС, причем операцию смешения компонентов А, Б и В проводят таким образом, что либо вначале смешивают компоненты Б и В, а в дальнейшем добавляют компонент А, либо вначале смешивают компоненты А и Б, а компонент В добавляют позже после стадии сушки или после стадии прокаливания, а операцию отгонки проводят либо после смешения всех трех компонентов, либо после смешения двух компонентов, один из которых компонент Б. Техническим результатом является получение стабильного катализатора, обеспечивающего высокую производительность в течение длительного времени, 2 с. и 2 з.п. ф-лы, 3 табл.
| Дзисько В.А | |||
| Основы методов приготовления катализаторов | |||
| - Новосибирск: Наука, 1983, с.130-139 | |||
| Способ приготовления катализатора для синтеза метанола и конверсии оксида углерода | 1987 |
|
SU1524920A1 |
| Устройство контроля информацион-НОгО КОдА | 1979 |
|
SU845294A1 |
| Устройство для контроля толщины и скорости осаждения тонких пленок | 1973 |
|
SU483609A1 |
Авторы
Даты
2003-12-20—Публикация
2002-01-09—Подача