Изобретение относится к медицине и фармации, а именно к препаратам для стимулирования родовой деятельности.
Одной из актуальных проблем акушерства и гинекологии является разработка препаратов для стимуляции родовой деятельности. В последние годы в акушерско-гинекологической практике для стимуляции родовой деятельности наиболее часто используются интраамниальный, экстраамниальный и интравагинальный пути введения растворов простагландинов (ПГ) [1, 2]. При этом наблюдается быстрое разрушение ПГ, что обуславливает необходимость повторного их введения. Использование катетера и водных растворов ПГ приводит к быстрому всасыванию веществ, что вызывает побочные действия, характерные для ПГ.
Известны [13] импортные препараты с простагландинами E2: Препидил - гель (США) и Цервипрост (Нидерланды). Недостатком препаратов является фиксированная концентрация действующего вещества, недостаточная для достижения необходимого эффекта, например, для прерывания патологической беременности.
Представляет интерес создание готовой формы стерильной гидрофильной мазевой основы, допускающей превращение ее в готовую композицию с действующим веществом в любой момент времени, например непосредственно перед использованием композиции, посредством асептического введения действующего вещества заданной концентрации в герметичную упаковку готовой формы основы.
Наиболее перспективной группой мазевых основ являются гидрофильные основы, т.к. они обладают рядом преимуществ перед гидрофобными и эмульсионными основами. Гидрофильные основы совместимы с большой группой действующих веществ, не препятствуют их абсорбции. Гидрофильные основы способны практически неограниченно смешиваться с водой или растворяться в ней и дают возможность технологически просто получать мази с задаваемыми реологическими свойствами [22].
В данной группе основ особый интерес представляют гели натрийкарбоксиметилцеллюлозы (натрий-КМЦ), полиэтиленоксидов различных марок (ПЭО) и гели редкосшитых акриловых полимеров (РАП).
Гели натрий-КМЦ не имеют запаха и вкуса и характеризуются нейтральной реакцией среды, устойчивы в широких пределах рН (от 3,0 до 12,0). Они хорошо переносятся больными, более полно отдают действующие вещества. Многочисленными исследованиями установлено, что гели натрий-КМЦ безвредны для организма, не оказывают непосредственного раздражающего или сенсибилизирующего действия. Натрий-КМЦ широко используется в фармации и косметике [7, 22].
Среди гелей синтетических высокомолекулярных соединений активно применяются в фармацевтической практике ПЭО различной молекулярной массы и гели РАП. Широкое внедрение указанных носителей в практику объясняется многими положительными качествами.
ПЭО растворимы в воде и этаноле, устойчивы к действию света, температуры, сдвигам рН, не препятствуют тепло- и газообмену кожи, способны растворять многие лекарственные вещества и обеспечивают их высокую биологическую доступность. Они обладают высокой осмотической активностью и бактерицидными свойствами [9, 22].
РАП легко образуют вязкие и прозрачные гели. Их широко применяют в качестве носителей различных лекарственных веществ, так как они обладают рядом преимуществ перед другими мазевыми основами: обеспечивают высокую биологическую доступность, пролонгирующий эффект и удобство применения, нетоксичны, не подвергаются гидролизу и окислению и устойчивы к факторам внешней среды [3, 16, 20].
Гидрофильные мазевые основы входят в состав многих готовых лекарственных форм и косметических композиций с зафиксированными параметрами системы: вязкостью, концентрацией действующего вещества и др. В то же время физико-химические свойства гидрофильных основ, их совместимость с большой группой лекарственных веществ позволяют предусмотреть возможность изготовления (в т.ч. экстемпорально) композиций с действующими веществами на базе готовых стерильных основ. Параметры таких композиций могут быть продиктованы ситуацией. Однако в настоящее время стерильные гидрофильные мазевые основы как таковые в упаковках не производятся.
Создание готовой формы основы позволит смешивать ее с действующим веществом в любой удобный момент времени и в требуемых ситуацией пропорциях.
Известна стерильная форма основы для глазных мазей, представляющая собой однородный сплав [19]. Указанная основа является гидрофобной, недостаточно высвобождает лекарственные вещества, оказывает раздражающее действие, ее упаковка не позволяет сохранять стерильность после первого использования [7] .
Наиболее близким к основе предлагаемого изобретения является 8,6% гель натрий-КМЦ [1] . Для получения геля 0,6 г измельченной натрийкарбоксиметилцеллюлозы растворяют в 7 мл воды во флаконе вместимостью 10 мл. Флакон укупоривают и стерилизуют насыщенным паром 20-25 минут при температуре 120oС. Однако гель с указанной концентрацией обладает слишком высоким значением эффективной вязкости, что затрудняет его смешивание с лекарственным веществом и введение полученного препарата больному, а жесткие условия стерилизации заметно нарушают реологические свойства основы [15, 19]. Кроме того, оптимальное время стерилизации объемов до 100 мл согласно ГФ-XI, в.2. (С. 193) и приказу МЗ РФ от 16.07.97 г. 214 "О контроле качества лекарственных средств, изготовляемых в аптеках" составляет 8 минут, а до 1000 мл - 15 минут.
Прототипом предлагаемого технического решения является препарат с ПГ на базе мазевой основы в виде 8,6%-ного геля натрий-КМЦ [1]. Однако такой препарат обладает слишком высокой вязкостью, что затрудняет его введение и ухудшает результат лечения.
Задачей, поставленной авторами, стало создание препарата с удовлетворительными для интравагинального введения реологическими свойствами, обладающего высокой родостимулирующей активностью без побочных явлений, характерных для ПГ, с возможностью индивидуального дозирования действующего вещества.
И с этой целью создание готовой формы стерильной гидрофильной мазевой основы, отличающейся экспериментально обоснованной концентрацией полимера, обеспечивающей равномерность распределения в нем действующего вещества, эффективность и длительность действия предлагаемой композиции с таковой основой за счет задаваемых основе необходимых реологических свойств, а также отвечающей требованиям ГФ-ХI по условиям тепловой стерилизации и восстанавливающей реологические свойства после охлаждения.
Задача изобретения решена созданием препарата, состоящего из готовой стерильной формы гидрофильной мазевой основы и простагландинов E1 или F2α в качестве действующего вещества.
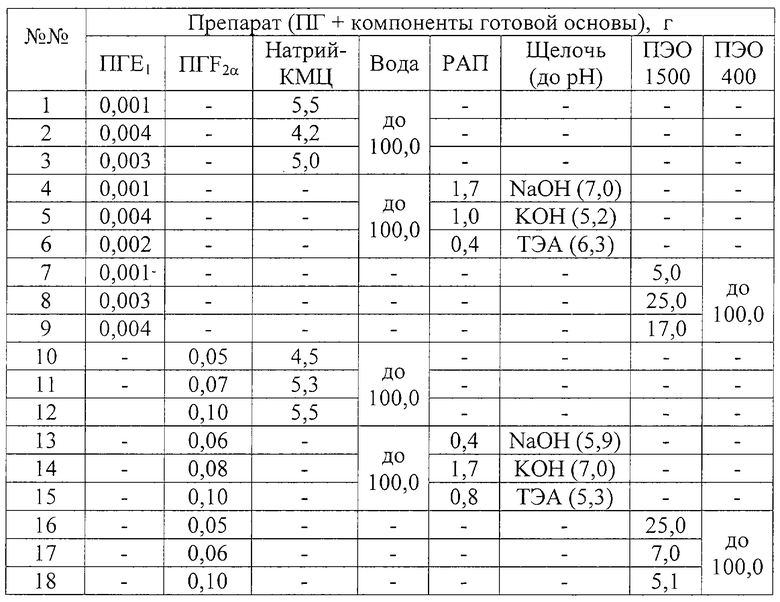
Удовлетворительные реологические параметры препарата обоснованы экспериментально, отвечают реологическому оптимуму экструзионной способности и обеспечиваются предложенным составом готовой формы стерильной гидрофильной мазевой основы. Индивидуально дозируемое количество простагландинов продиктовано эффективной дозой и составляет для ПГЕ1 0,001-0,004 вес.%, для ПГF2α 0,05-0,10 вес.%.
Задача решена созданием готовой формы стерильной гидрофильной мазевой основы, выполненной в виде гелевой структуры с экспериментально обоснованными реологическими свойствами и помещенной в оболочку герметичной емкости.
Герметичная емкость может представлять собой любую, соответствующую целям и выдерживающую тепловую стерилизацию упаковку с возможностью асептического проникновения в нее, в частности укупоренные резиновой пробкой под обкатку стеклянные флакон, бутылку или пластиковый контейнер.
Структура мазевой основы может быть выполнена из гелей натрий-КМЦ, РАП (Ареспол, Марс и др.) или ПЭО или других подходящих природных или синтетических полимеров, имеющих реологические характеристики, находящиеся в пределах реологического оптимума экструзионной способности гидрофильных основ [5].
Реологический оптимум экструзионной способности основ ограничивается областью величин касательного напряжения сдвига от 30 до 420 Па при скоростях сдвига от 1 до 365 с-1 соответственно (фиг.1) и обеспечивается составами, вес.%:
Натрий-КМЦ - 4,5-6,0
Вода очищенная или - До 100,0
РАП - 0,4-1,7
Раствор NaOH или КОН водный, или триэтаноламин - До рН 5,0- 7,0
Вода очищенная или - До 100,0
ПЭO 1500 - 5,0-25,0
ПЭO 400 - До 100,0
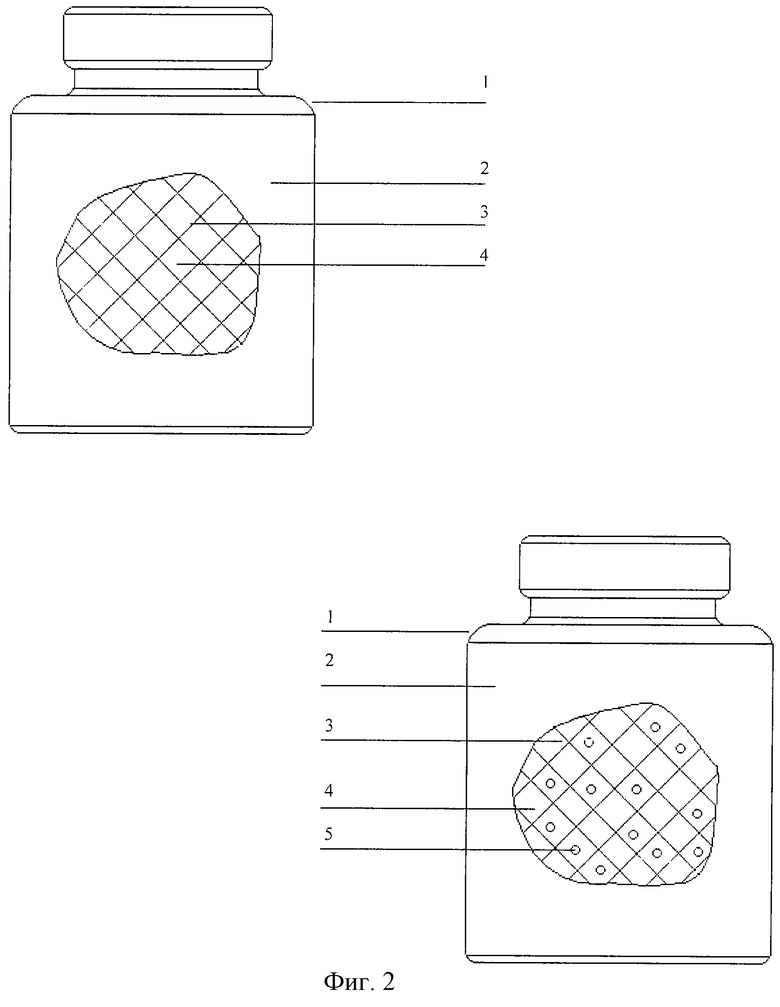
Общий вид готовой формы стерильной мазевой основы и заявляемого препарата приведены на фиг. 2, где показаны: 1 - герметичная емкость, 2 - стерильная гидрофильная мазевая основа, представляющая собой однородный гель, образованный рыхлой структурной сеткой 3 и дисперсионной средой 4. Простагаландины 5 равномерно распределены в стерильной гидрофильной мазевой основе.
Изобретение реализуется следующим орбразом.
Для получения геля натрий-КМЦ к 5,0 частям (точная навеска) натрийкарбоксиметилцеллюлозы добавляют равное количество воды очищенной и тщательно перемешивают. Затем по частям добавляют оставшуюся воду и перемешивают до получения однородной массы. Полученный гель фильтруют, расфасовывают во флаконы вместимостью до 1 литра и укупоривают резиновыми пробками под обкатку. Гель стерилизуют паром под давлением при 120oС в течение 8-15 минут в зависимости от объема.
Гели различных видов РАП получают следующим образом: РАП при перемешивании вносят в рассчитанное количество воды очищенной, затем добавляют щелочной агент, например раствор натрия или калия гидроксида или триэтаноламина, и перемешивают до получения однородного прозрачного геля с рН от 5,0 до 7,0. Полученный гель фильтруют, расфасовывают во флаконы необходимой вместимости (от 5 мл до 1000 мл), укупоривают резиновыми пробками под обкатку и стерилизуют паром под давлением при 120oС в течение 8-15 минут в зависимости от объема.
Гель ПЭО получают следующим образом: полиэтиленоксид 1500 сплавляют с полиэтиленоксидом 400 на водяной бане при температуре 60±5oC. Полученную массу перемешивают при охлаждении до комнатной температуры. Затем сплав фильтруют, расфасовывают во флаконы до 1 литра, укупоривают резиновыми пробками под обкатку и стерилизуют паром под давлением при 120oС в течение 8-15 минут в зависимости от объема.
В результате смешения компонентов гидрофильной мазевой основы начинается гелеобразование, то есть переход системы в твердообразное состояние. При этом за счет сцепления частиц гелеобразователя в объеме жидкости возникает пространственная структурная сетка.
Жидкая дисперсионная среда 4 входит в ячейки рыхлой пространственной сетки 3, уменьшая текучесть основы в целом до заданных составом реологических свойств. Контакты между частицами структуры легко и обратимо нарушаются при введении геля в емкость и стерилизации. После охлаждения внутри герметичной емкости 1 стерильная гидрофильная мазевая основа 2 восстанавливает свою гелевую структуру с сохранением первоначальных свойств. Дисперсионная среда, входящая в ячейки пространственной структуры, способна в случае необходимости принимать действующее вещество и удерживать его в себе. Экспериментально обоснованный состав мазевой основы позволяет при этом сохранять заданные реологические свойства и предлагаемому препарату.
Изучение реологических свойств описанных выше гелей показало, что последние обладают тиксотропными свойствами, а их реограммы укладываются в реологический оптимум экструзии для гидрофильных мазей (фиг.1), что позволяет сделать вывод об их удовлетворительной экструзионной способности, характеризующей, например, легкость забора препарата в шприц и выдавливаемость из него.
Изучение возможности стерилизации гелей показало, что реологические свойства гелей не изменяются.
Все полученные гели характеризуются термической стабильностью при +45oС и -(5-10)oС [17].
Предложенные гидрофильные основы совместимы с большой группой лекарственных веществ и практически неограниченно смешиваются с ними и с водой. Введение требуемого вещества в основу непосредственно перед лечебной процедурой позволяет значительно расширить возможности врача, связанные с необходимостью индивидуального дозирования действующего вещества или получения готовой лекарственной формы из лабильного действующего вещества, или из смеси нескольких действующих веществ.
Для получения какой-либо композиции с готовой формой стерильной гидрофильной мазевой основы действующее вещество в индивидуально дозированном количестве вводится в строго асептических условиях (например, в чистой зоне класса А) в герметичную емкость 1 (например, в виде стерильного раствора шприцем через резиновую пробку флакона или подобным способом). При введении действующего вещества в мазевую основу 2 равномерное его распределение в структурированной массе достигается простым встряхиванием, и таким образом получается готовая лекарственная форма или любая иная композиция на мазевой основе (лекарственная или лечебно-косметическая).
При введении простагландинов 5 в емкость 1 со стерильной гидрофильной мазевой основой 2 и перемешивании путем простого встряхивания молекулы действующего вещества распределяются в дисперсионной среде 4, заключенной в рыхлую сетку 3 структурированной гелевой системы.
Так получены препараты, составы которых приведены в таблице.
В момент введения препарата в организм рыхлая пространственная сетка 3 гелевой основы защищает действующее вещество 5 от одномоментного деструктирующего контакта с тканями организма. Вследствие механических и тепловых воздействий связи между частицами гелевой структуры разрушаются и выделяется действующее вещество. Экспериментально обоснованные реологические свойства системы обуславливают требуемые условия контакта действующего вещества с тканями и системами организма, стимулируя родовую деятельность.
Изучение специфической активности гелей с простагландином ПГF2α в опытах in vitro на модели изолированных матки и кишечника [10] и in vivo на беременных и небеременных крысах показало, что гели обладают высокой родостимулирующей активностью.
Изготовленный в асептических условиях аптеки Ленинградской клинической больницы (ЛОКБ) в виде готовой формы стерильный гель натрий-КМЦ и препарат с ПГ на его основе применялся в отделении патологии беременности ЛОКБ по медицинским показаниям для прерывания беременности во втором триместре как самостоятельно, так и в сочетании с внутривенным введением простагландинов. Отмечена высокая родостимулирующая активность заявляемого препарата в сравнении с прототипом и импортными аналогами (Препидил-гель, Цервипрост). Аллергических проявлений, побочных явлений, обычных для увеличенной дозы простагландинов, и непереносимости не наблюдалось. Использование готовой формы стерильной гидрофильной мазевой основы позволило осуществить препарат с возможностью индивидуального подбора дозы простагландина и исключить побочные явления, характерные для тех же доз ПГ, вводимых в водных растворах.
Литература
1. Абрамченко В. В. , Богдашкин Н.Г. Простагландины и репродуктивная система женщины. - Киев: Здоровья, 1988. - 165 с.
2. Айламазян Э. К., Абрамченко В.В. Простагландины в акушерско-гинекологической практике. - Спб.: Петрополь, 1993. - 214 с.
3. Алексеев К.В., Ли В.Н., Демишев В.Н. и др. Редкосшитые акриловые полимеры в фармации.// Фармация. 1987. 5. С.15-18.
4. Алексеев К.В., Стародубова М.В., Слюсар О.И. Ареспол - новое вспомогательное вещество в технологии мазей. // VII Российский национальный конгресс "Человек и лекарство": Тезисы докладов. - М., 2000. С. 598.
5. Аркуша А.А. Оценка и контроль консистентных свойств мазей при помощи реограмм: Методические рекомендации. - Харьков, 1986. - 12 с.
6. Астраханова М. М. , Стародубова М.В., Алексеева К.В., Елагина И.А. Новые лекарственные средства противовоспалительного действия для наружного применения. // VI конгресс "Человек и лекарство": Тезисы докладов. - М., 1999. С. 383.
7. Грецкий В.М. Основы для медицинских мазей. - М., 1975. С.22-30.
8. Гунько В. Г. , Гунько А.А., Мусиенко Н.М. Изучение осмотической активности некоторых мазевых основ. // Химико-фармацевтический журнал. 1982. 3. С.345-346.
9. Дашевская Б. И., Глузман М.Х, Бодня В.М. Полиэтиленоксиды и их применение в фармации. // Обз. инф.: Химико-фармацевтическая промышленность. 1974. В.2. С.3-27.
10. Исай С.В., Иванкина, Н.Ф., Кафанова Т.В. Простагландины пантов пятнистого оленя. // Химико-фармацевтический журнал. 1994. 7. С.23-26.
11. Кудрякова Э.А., Молдавер Б.Л., Марченко Л.Г., Цветкова Ю.А. Исследование возможности получения гелей нового отечественного редкосшитого акрилового полимера "Ареспол". // Сб. трудов НИИФ. Т.39. Ч.1. С.207-211.
12. Кузин М. И., Костюченок Б.М., Даценко Б.М. Местное медикаментозное лечение ран: Методические рекомендации. - М., 1985. - 18 с.
13. Лекарственные препараты в России: Справочник Видаль. - М.: АстраФармСервис, 1995. - 1168 с.
14. Майорова А.В., Алексеев К.В., Суслина С.Н. Опыт использования редкосшитого акрилового полимера Ареспола в составе новых дерматологических препаратов. // Мат. науч. - практ. конф. "Актуальные вопросы косметологии".- Санкт-Петербург, 2000. С.80.
15. Изготовление стерильных растворов в аптеках: Методические указания. - М.: Минздрав РФ, 1994. - 145 с.
16. Обзорная информация: Медицина и здравоохранение. Фармация и фармакология. - 1982. 6. С. 39-46.
17. ОСТ 18-304-76. Кремы косметические. Правила приемки, отбора проб. Методы испытания. - М.: Министерство пищевой промышленности СССР, 1976. - 47 с.
18. Перцев И. М. , Даценко Б.М., Гунько В.Г. Многокомпонентные мази на гидрофильной основе. // Фармация. 1990. 5. С.73-77.
19. Приказ Министерства здравоохранения РФ от 16.07.97 г. 214 "О контроле качества лекарственных средств, изготовляемых в аптеках". - М.: Минздрав РФ, 1997. - 70 с.
20. Проспект Carbopol. / B.F. Goodrich. - 1998. - 39 с.
21. Суслина С. Н. , Слюсар О.И., Арефьева Н.В. Лекарственные формы для наружного применения с маслом "Витон". // VI Российский национальный конгресс "Человек и лекарство": Тезисы докладов. - М., 1999. С.476.
22. Тенцова А.И., Грецкий В.М. Современные аспекты исследования и производства мазей. - М.: Медицина, 1980. - 153 с.
23. Шалдырван Е.А., Алексеев К.В. Экспериментальное изучение гелей интерферона. // Сб. науч. трудов ВНИИбиотехнологии. T.1. - М.: ВНИИСЭНТИ. С. 66-69.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕЛЬ С СЕРОЙ И СПОСОБ ЛЕЧЕНИЯ ЧЕСОТКИ | 2002 |
|
RU2217127C1 |
| СТИМУЛЯТОР РОСТА ВОЛОС | 2001 |
|
RU2181584C1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ, ОБЛАДАЮЩИЙ ВЕНОТОНИЧЕСКИМ И АНТИКОАГУЛЯНТНЫМ ДЕЙСТВИЕМ (ВАРИАНТЫ) | 2012 |
|
RU2548785C2 |
| СТИМУЛЯТОР РОСТА ВОЛОС | 2001 |
|
RU2182478C1 |
| ГЕЛЬ-ОСНОВА ДЛЯ РАНОЗАЖИВЛЯЮЩИХ И КОСМЕТИЧЕСКИХ СРЕДСТВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2485938C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНОГО ВАГИНОЗА (ВАРИАНТЫ) | 2007 |
|
RU2325148C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЙ КОЖИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2019 |
|
RU2716158C1 |
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО НА ОСНОВЕ ШТАММА Trichoderma harzianum Rifai | 2013 |
|
RU2528065C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ ПРИ КЛИМАКТЕРИЧЕСКИХ РАССТРОЙСТВАХ НА ОСНОВЕ СИГЕТИНА | 2007 |
|
RU2360670C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАЗИ "АПИЛАР-Г", ОБЛАДАЮЩЕЙ ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2001 |
|
RU2196569C1 |
Изобретение относится к медицине и фармации, а именно к набору для стимулирования родовой деятельности. Для экстемпорального получения препарата, стимулирующего родовую деятельность, предложен набор из готовой стерильной формы гидрофильной мазевой основы и простагландинов в качестве действующего вещества. Реологические параметры готового препарата обоснованы экспериментально, отвечают реологическому оптимуму экструзионной способности и обеспечены составом основы. Индивидуально дозируемое количество простагландинов продиктовано эффективной дозой. Мазевая основа может быть выполнена из гелей натрийкарбоксиметилцеллюлозы, редкосшитых акриловых полимеров (Ареспол, Марс и др. ) или полиэтиленоксидов. Герметичная емкость может представлять собой любую, соответствующую целям и выдерживающую тепловую стерилизацию упаковку с возможностью асептического проникновения в нее. Получаемый препарат обладает высокой родостимулирующей активностью без побочных явлений, характерных для простагландинов, с возможностью индивидуального дозирования действующего вещества. 2 з.п.ф-лы, 2 ил., 1 табл.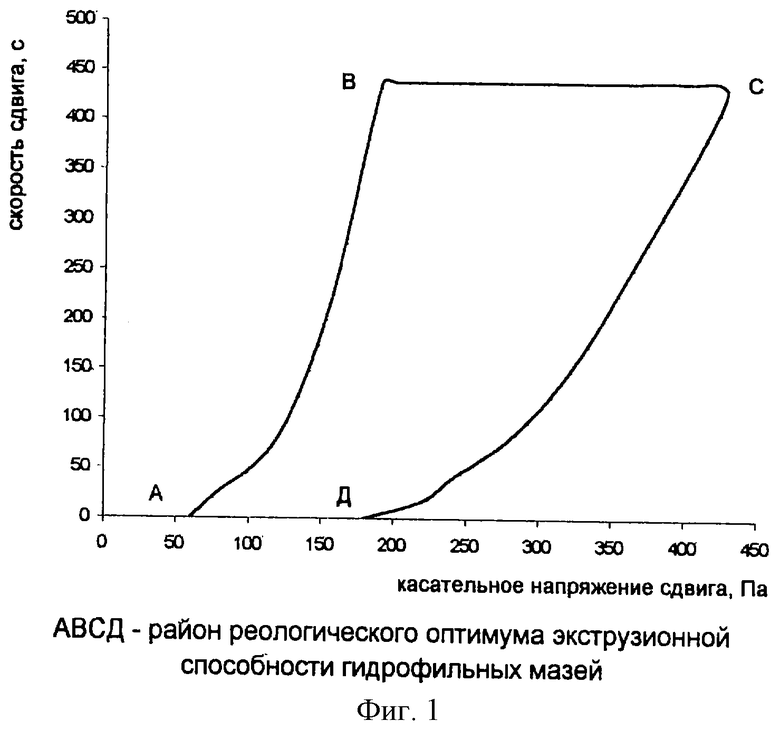
Натрий КМЦ 4,5 - 5,5
Вода очищенная До 100,0
или гель РАП, включающий редкосшитый акриловый полимер, водный раствор NaOН или КОН или триэтаноламин и воду очищенную при следующем соотношении компонентов, мас.%:
РАП 0,4 - 1,7
Водный раствор NaOH или КОН,
или триэтаноламин До рН 5,0 - 7,0
Вода очищенная До 100,0
или сплав полиэтиленоксида 400 и полиэтиленоксида 1500, при следующем соотношении компонентов, мас.%:
ПЭО 1500 5,0 - 25,0
ПЭО 400 До 100,0
при этом указанные количества компонентов обеспечивают основе реологический оптимум экструзионной способности, ограниченный областью величин касательного напряжения сдвига в пределах 30 - 420 Па при скоростях сдвига 1,0 - 365,0 с-1 соответственно, простагландин выбран из группы ПГЕ1 или ПГF2а, а количество простогландина - индивидуально эффективным.
| Технология лекарственных форм | |||
| Под ред | |||
| Т.С | |||
| Кондратьевой | |||
| - М.: Медицина, 1991, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ДВОЙНОЙ ГАЕЧНЫЙ КЛЮЧ | 1920 |
|
SU288A1 |
| Фармацевтические и медико-биологические аспекты лекарств | |||
| Под ред | |||
| проф | |||
| И.М | |||
| Перцева и др | |||
| - Харьков: Изд-во НФАУ, 1999, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Приспособление для уменьшения дымовой тяги паровоза | 1920 |
|
SU270A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ НА ОСНОВЕ ПРОСТОГО ЭФИРА ЦЕЛЛЮЛОЗЫ | 1999 |
|
RU2158279C1 |
| КОСМЕТИЧЕСКИЙ ГЕЛЬ ДЛЯ ЛИЦА | 1994 |
|
RU2102975C1 |
| Абрамченко В.В | |||
| и др | |||
| Простагландины и репродуктивная система женщины | |||
| - Киев: Здоровья, 1988, с | |||
| Устройство для отыскания металлических предметов | 1920 |
|
SU165A1 |
| Лекарственные препараты в России | |||
| Справочник Видаль | |||
| - М.: АстраФармСервис, 1995, с | |||
| Приспособление для извещения станции о месте нахождения поезда | 1924 |
|
SU1168A1 |
| US 4680312 А, 14.07.1987. | |||
Авторы
Даты
2004-02-10—Публикация
2001-10-04—Подача