Изобретение относится к новым производным 10Н-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола, а именно к водорастворимым солям 10-со-арилоксиалкил-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола формулы I
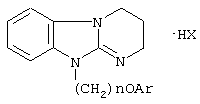
где Аr=С6Н5, C6H4R, где R = алкоксикарбонил- или карбоксигруппа в о-, м- и п-положениях бензольного кольца, n=1-6, Х = Сl или Вr, обладающим местно-анестезирующим действием при инфильтрационной, проводниковой и спинномозговой анестезии.
Одним из наиболее активных и длительно действующих местных анестетиков является препарат маркаин (бупивакаин). Он находит широкое практическое применение для местной инфильтрационной анестезии (0,25%), блокады периферических нервов (0,25-0,5%) (М.Д.Машковский. Лекарственные средства, 15-ое изд., перераб. и дополн., М.: Медицина, 1998, ч. 1, с. 378), спинномозговой, эпидуральной, каудальной, внутрисуставной анестезии, при проведении парацервикальной и ретробульбарной блокад (например, R.P. Alston. Spinal anaesthisis with 0,5% bupivacaine 3 ml: Comparison of plain and hyperbarric solutions administered to seated patients. Brit. J.Anatsth., 1988, vol. 61, №4, p. 385-389; A.R.Wolf, R.D.Valley, D.W.Fear et al. Bupivacaine for caudal analgesia in infants and childrens the optimal effective concentration. Anaesthesiology, 1988, vol. 69, №1, p. 101-105). Следует отметить, что маркаин не только высокоактивный, но и весьма токсичный анестетик (Н.Б.Рациборинская. Местноанестезирующие свойства некоторых производных пиперидина и индола. Автореф. дис. канд. мед. наук. Ростов-на-Дону, 1991; J.Kambam, B.Mets, R.Hickman et al. Comparative systemic toxicity ofintravenously infused bupivacaine (B), cocaine (C) and lidocaine (L) in pigs: [Abstr.] Int. Anaesth. Res. Sос.66th Congr., San-Francisco, Calif., March 13-17, 1992; Anaesth. And Analg., 1992, vol. 74, №25, p. 87), что требует повышенного внимания при его использовании в практической медицине. При правильном подборе доз препарат обеспечивает сильную и длительную анестезию. При повышении их возможны судороги, угнетение сердечной деятельности (вплоть до остановки сердца) (М.Д.Машковский, 1998). Кроме того, маркаин может вызывать генерализованную сыпь, отек Квинке, стридор гортани, бронхоспазм (H.GacI, V.Reichert, R.Kauftnann. Localanaestheticaintoleranz auf Leitungsanaesthesia mit Prilocain und Bupivacain. Allergologie, 1992, Bd. 15, №3, S. 89-91).
В ряду 10-замещенных 10Н-2,3,4,10-тетрагидропиримидо[1,2-а]-бензимидазола не известны соединения, обладающие местно-обезболивающим действием.
Наиболее близкими по структуре среди производных 10Н-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола являются соли 10-диалкиламиноэтил-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола, проявляющие гипогликемические и антиагрегантные свойства (V.A.Anisimova, M.V.Levchenko, T.B.Korochma et al. Nouveaux derives du benzimidazole, leur procede de preparation et les compositions pharmaceutiques qui les contiennent. Fr.Pat.2691462(1995); Bull., 95/23. ЕР 0571253).
Техническим результатом изобретения являются новые соединения в ряду 1 ОН-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола, проявляющие неизвестное для данного класса соединении местно-анестезирующее действие, более эффективное, чем действие известного местно-анестезирующего препарата.
Технический результат достигается соединениями I, синтез которых заключается во взаимодействии N-незамещенного 1Н-1,2,3,4 -тетрагидропиримидо[1,2-а]бензимидазола в нейтральных условиях с 1-ω-арилокси-2-галогеналканами в среде растворителя или без него (метод А), а также замещением атома галогена в 10-ω-галогеналкил-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазолах на арилоксигруппу при действии на них фенолятов щелочных металлов (метод Б).
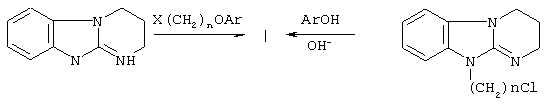
где Аr, R, n и Х принимают значения, указанные выше.
Ниже приведены примеры методик синтеза предлагаемых соединений.
Пример 1. Гидрохлорид 10-β-феноксиэтил)-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола(I, Аr = С6Н5, n=2, Х=Сl; РУ-1151).
Метод А. Смесь 1,73 г (10 ммоль) 1Н-1,2,3,4-тетрагидропиримидо[ 1,2-а]бензимидазола и 2,0 мл (15 ммоль) β-феноксиэтилхлорида в 5 мл диметилформамида кипятят 3,5 часа. На следующий день выпавший осадок отфильтровывают, тщательно промывают ацетоном, получая 3,2 г (94%) гигроскопичного гидрохлорида. Последний кристаллизуют из изопропилового спирта и сушат при 105°С. Т.пл. 206-207°С.
Найдено, %: С 65,5; Н 6,2; С1 10,6; N 12,5.
C18H19N30·HCl.
Вычислено, %: С65,6; Н6,1; Сl 10,8; N 12,7.
ИК-спектр (вазелин, масло), см-1: 1660 (С= N).
Спектр ПМР (300 МГц, СОСl3), δ, м.д.: 2,25 (2Н, м, 3-СH2, 3,75 (2Н, м, 4-СН2), 4,06 (2Н, м, 2-СН2), 4,50 (2Н, т, СН2O), 4,93 (2Н, т, NCH2), 6,78 (2Н, д, 2’- и 6’-Н, J=7,9 Гц), 6,90 (1Н, т, 4’-Н, J=7,3 Гц), 7,19 (1Н, д, 6-Н, J=8,5 Гц), 7,20 (2Н, т, 3’- и 5’-Н), 7,31 (1Н, т, 7-Н), 7,37 (1Н, т, 8-Н), 7,57 (1Н, д, 9-Н,.7 =7,6 Гц), 11,64(1Н, N+Н).
Метод Б. В перемешиваемый раствор 1,73 г (10 ммоль) 1Н-1,2,3,4-тетрагидропиримидо[1,2-а]бензимидазола в 4 мл диметилформамида, полученный при нагревании, вносят 1 мл (15 ммоль) этиленхлоргидрина и смесь кипятят. Реакцию ведут до исчезновения пятна исходного трицикла на ТСХ. Смесь оставляют на ночь при пониженной температуре (5-7°С). Выпавший осадок гидрохлорида 10-(β-гидроксиэтил)-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола отфильтровывают, тщательно промывают ацетоном. Выход 2,16 -2,3 г (85,0-91,0%). Т.пл. 238 -240°С (разл., из 2-пропанола).
Найдено, %: С 56,7; Н6,5; Сl 14,1; N 16,6.
C12H15N3O HCl.
Вычислено, %: С 56,8; Н 6,4; Cl 14,0; N 16,6.
ИК-спектр (вазелин, масло), см-1: 1660 (C=N).
Спектр ПМР (300 МГц, ДМСО-d6), δ м.д.: 2,13 (2Н, кв, 3-CH2, J = 5,8 Гц), 3,48-3,56 (2Н, м, 2-СН2), 3,71 (2Н, т, СН2О, J = 5,1 Гц), 4,11 (2Н, т, 4-СН2, J = 5,9 Гц), 4,22 (2Н, т, NCH2, 7-5,1 Гц), 5,05 (1H, широкий с, ОН), 7,27 -7,34 (2Н, м, аром.Н), 7,47 -7,59 (2Н, м, аром.Н), 9,53 (1H, с, N+Н).
Основание -10-(β-гидроксиэтил)-2,3,4,10-тетрагидропиримидо[1,2-а]-бензимидазол - выделяют обработкой 22%-ного раствором NH4OH соответствующего гидрохлорида, синтез которого описан выше, и экстрагируют хлороформом. Для очистки экстракт пропускают через слой оксида алюминия, элюируя основание хлороформом. Остаток после испарения растворителя из элюата перекристаллизовывают из этанола или ацетонитрила. Т.пл. 155-156°С.
Найдено,%: С 66,5; Н 7,0; N 19,1. C12H15N3O.
Вычислено, %: С 66,4; Н 7,0; N 19,3.
ИК-спектр (вазелин, масло), см-1: 1640 (C=N), 3250 (ОН).
К раствору 2,17 г (10 ммоль) 10-β-гидроксиэтилзамещенного в 10-15 мл сухого хлороформа прибавляют 0,7 мл (15 ммоль) хлористого тионила, а затем кипятят ее 4-5 часов, контролируя процесс хлорирования с помощью ТСХ (Аl2О3, элюент – СНСl3, Rf исходного - 0,1, Rf конечного - 0,55). Хлороформ испаряют, остаток обрабатывают петролейным эфиром или гексаном, отгоняя последние вместе с избытком хлористого тионила. Выход гидрохлорида 10-(β-хлорэтил)-2,3,4,10-тетрагидропиримидо [ 1,2-] бензимидазола количественный.
Т.пл. 221-223°С.
Найдено, %: С 52,8; Н 5,6; С1 25,9; N 15,6.
C12H14ClN3 НСl.
Вычислено, %: C53,0; H5,6; Cl 26,0; N 15,4.
Соль вводят в дальнейшие превращения без дополнительной очистки или переводят с помощью раствора аммиака в основание, которое также используют в реакциях с различно замещенными фенолами. Выход 95-98%. Т.пл. 69-70°С (из ацетонитрила).
Найдено, %: С 61,3; Н6,1; Cl 14,7; N 18,1.
C12H14ClN3.
Вычислено, %: С 61,2; Н 6,0; Cl 14,9; N 17,9.
К раствору 0,2 г (~2 ммоль) фенола и 0,12 г КОН в 7-10 мл метанола добавляют 2 ммоль 10-хлорэтилзамещенного и кипятят смесь до полного протекания реакции (контроль - ТСХ: полное исчезновение пятна исходного хлорпроизводного). По окончании реакции спирт упаривают, остаток очищают на хроматографической колонке с γ-Аl2О3, элюируя хлороформом и собирая первую фракцию с Rf 0,22. Выход 10-(β-феноксиэтил)-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола 74,2%. Т.пл. 98-99°С (из изооктана).
Найдено, %: С 73,6; Н 6,5; N14,5.
C18H19N3O.
Вычислено, %: С73,7; Н 6,5; N 14,3.
Полученное основание может служить основой для получения любых солей с фармацевтически приемлемыми кислотами.
Гидрохлорид, идентичный описанному в методике А, получен при подкислении раствора основания в спирте или ацетоне насыщенным раствором НСl в изопропиловом спирте или эфире.
Пример 2. Гидробромид 10-(β-феноксиэтил)-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола (I, Аr = С6Н5, Х = Вr). Смесь 1,73 г (10 ммоль) 1Н-1,2,3,4-тетрагидропиримидо[1,2-а]бензимидазола и 2,4 г (20 ммоль) β-феноксиэтилбромида (М.В.Рубцов, А.Г.Байчиков. Синтетические химико-фармацевтические препараты, М.: Медицина, 1971, с. 86) в 5 мл диметилформамида или какого-либо другого растворителя кипятят 3-5 часов (контроль за протеканием реакции - ТСХ). Охлаждают, выпавший осадок отфильтровывают, промывают ацетоном, получая 3,2-3,4 г (85,5 - 90,7%) гидробромида. Очищают соль перекристаллизацией из этилового спирта. Т.пл. 150-152°С.
Идентичная соль была получена при подкислении ацетонового или спиртового раствора 10-(β-феноксиэтил)-2,3,4,10-тетрагидропиримидо[1,2-а]-бензимидазола конц. НВг.
Пример 3. Гидробромид 10-[β-(4-метоксикарбонилфенокси)этил]-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола (I, Аr = С6H4СООСН3, Х = Вr). Смесь 0,87 г (5 ммоль) 1Н-1,2,3,4-тетрагидропиримидо[1,2-а]бензимидазола и 1,55 г (6 ммоль) метилового эфира 4-(β-бромэтокси)бензойной кислоты (П.М.Кочергин, Р.М.Палей, Л.В.Баландина и др. Хим.-фарм.ж., 1995, №2, с. 56-57), тщательно растирают и нагревают при 150°С (температура бани) в течение 30 мин. Затем плав охлаждают и обрабатывают ацетоном, кристаллический осадок отфильтровывают, промывают ацетоном. Выход хроматографически чистого гидробромида 1,88 г (87,3%). Т.пл. 222-223°С (из ацетонитрила).
Найдено, %: С 55,5; Н 5,2; Bi-18,8; N 9,9.
C20H21N3O3 HBr.
Вычислено, %: С 55,6; Н 5,1; Br 18,5; N 9,7.
ИК-спектр (вазелин.масло), см-1: 1680 (C=N), 1720 (С=O).
Спектр ПМР (300 МГц, СDСl3), δ, м.д.: 2,28 (2Н, м, 3-СН2), 3,77 (2Н, т, 4-СН2), 3,84 (3Н, с, СН2), 4,09 (2Н, т, 2-СН2, J-6,1 Гц), 4,55 (2Н, т, ОСН2, J = 4,7 Гц), 4,93 (2Н, т, NCH2, J = 4,4 Гц), 6,81 (2Н, д, 2’,6’-Н, J = 8,8 Гц), 7,23 (1Н, д, 6-Н, J = 7,3 Гц), 7,31 -7,41 (2Н, м, 7,8-Н), 7,55 (1Н, д, 9-Н, J = 7,6 Гц), 7,89 (2Н, д, 3’,5’-Н, J = 8,8 Гц), 10,72 (1Н, с, N+Н).
Пример 4. Гидробромид 10-[β-(4-карбоксифенокси)этил]-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола (I, Аr = С6Н4СООН, Х = Br)
получен взаимодействием эквимолярных количеств 1Н-1,2,3,4-тетрагидропиримидо[1,2-а]бензимидазола и 4-(р-бромэтокси)бензойной кислоты (П.М.Кочергин и др., 1995) в диметилформамиде (выход 78%) или омылением метоксикарбонильной группы в 4-метоксикарбонилфеноксиэтилзамещенном пиримидо[1,2-а]бензимидазола (см. пример 3). Омыление проводят следующим образом: 0,86 г (2 ммоль) 4-метоксикарбонилзамещенного, 10 мл ледяной уксусной кислоты и 2 мл конц. НВr кипятят 3 часа. Полученный раствор охлаждают и оставляют на ночь в холодильнике. Выпавший осадок отфильтровывают, промывают ацетоном. Выход 0,71 г (84,9%). Т.пл. 260-261°С (из этанола).
Найдено, %: С 54,6; Н 4,9; Br 18,9; N11,1.
С19Н19N3О3·HBr.
Вычислено, %: 54.6; Н 4,8; Br 19,1; N 10,0.
ИК-спектр (вазелин, масло), см-1: 1673 (C=N), 1693 (С=O), 3285-3605 (ОН).
Спектр ПМР (300 МГц, ДМСО-d6), δ, м.д.: 2,15 (2Н, м, 3-СН2), 3,56 (2Н, т, 4-СН2, J = 5,3 Гц), 4,10 (2Н, т, 2-CH2, J = 5,6 Гц), 4,37 (2Н, т, СН2О, J = 4,7 Гц), 4,58 (2Н, т, NCH2, J = 4,7 Гц), 6,91 (2Н, д, 2,6-Н, J = 8,80 Гц), 7,34 (2Н, м, 7,8-Н), 7.51 (1Н, д, 6-Н, J = 8,8 Гц), 7,66 (1Н, д, 9-Н, J = 8,80 Гц), 7,84 (2Н, д, 3’,5’-Н, J = 8,80 Гц), 9,62 (1Н, широкий м, N+H), 12,40 (1Н, уширен. С, ОН).
Инфильтрационную анестезию исследовали в опытах на коже морских свинок (Bulbring E., Wajda J. Biologicak comparison of local anaesthetica //J. Pharmacol. and exp. therap. -1945. -Vol. 85, №1. -P. 78-84).
Проводниковую анестезию изучали в экспериментах на нервах хвостов крыс (Игнатов Ю.Д., Васильев Ю.Н., Жуков В.Н. и др. Методические рекомендации по экспериментальному изучению местно-анестезирующих средств. - М.: МЗ СССР, 1990. - 49 с.).
Спинномозговую анестезию исследовали в опытах на крысах (Ю.Д.Игнатов и соавт., 1990), катетеризируя субарахноидальное пространство (Хван А.А. Болеутоляющее действие клофелина при введении в желудочки головного мозга и под оболочки спинного мозга //Фармакол. и токсикол. - 1987. - №2. - С. 26 -29; Yaksh T.L., Rudy T.A. Chronic catheterisation of the spinal subarachnoid space //Physiol. Behav. -1976. - Vol. 17. - P. 1031 -1036).
Обезболивающее действие веществ в условиях проводниковой и спинномозговой анестезии оценивали в стандартном алгезиметрическом тесте tail-flick (Grossman M.L., Basbaum A.I., Fields H.L. Afferent and efferent connections of the rat tail flick reflex (a model used to analyze pain control mechanisms) //J. Сотр. Neurol. -1982. -Vol. 206. -P. 9 -16; Hahn E.E. Testing and evaluation of opiate analgesics and antagonists //Meth. Find. Exp. Clin. Pharmacol. -1985. -Vol. 7. -P. 373-381).
Местно-раздражающее и повреждающее действие изучали в опытах на коже крыс (Ю.Д.Игнатов и соавт., 1990).
Острую токсичность исследовали [определяли среднюю летальную (смертельную) дозу -ЛД50] в опытах на мышах при подкожном введении (Прозоровский В.Б. Использование метода наименьших квадратов для пробит-анализа кривых летальности //Фармакол. и токсикол. -1962. -Т. 25, №1.-С. 115-119).
В качестве вещества сравнения был взят маркаин (бупивакаин).
Статистическую обработку данных, учитываемых в градированной форме, проводили по М.Л.Беленькому (Беленький М.Л. Элементы количественной оценки фармакологического эффекта. -Л., 1963. -152 с.), в альтернативной [определение ЛД50, средних эффективных концентраций (ЕС50), границ их доверительного интервала, терапевтического индекса, или широты терапевтического действия (ЛД50/ЕС50)] - по В.Б.Прозоровскому (1962) и Ю.Д.Игнатову с соавт. (1990).
При инфильтрационной анестезии в экспериментах на морских свинках минимальной обезболивающей концентрацией как для РУ-1151, так и маркаина является 0,0156%. Однако следует отметить, что в этой концентрации индекс Бюльбринг и Уэйд для РУ-1151 равен 13,0, тогда как для маркаина - 6,4. С увеличением концентрации растворов до 0,0312 и 0,0625% индексы Бюльбринг и Уэйд для РУ-1151 соответственно составили 26,2 и 36,0, тогда как для маркаина - 10,8 и 32,6 (табл. 1).
Сопоставление EC50 показало (табл. 2), что РУ-1151 в 1,70 раза более активно, чем маркаин. При этом по терапевтическому индексу (широте терапевтического действия) РУ-1151 в 1,34 превосходит маркаин.
В результате исследования проводниковой анестезии в опытах на крысах установлено (табл. 3), что в 0,25 и 0,5% растворах как РУ-1151, так и маркаин через 5 мин после введения их в корень хвоста вызывают полное (100%-ное) обезболивание, тогда как по длительности анестезирующего эффекта РУ-1151 в 1,89 и 2,60 соответственно более значимо, чем маркаин.
В условиях спинномозговой анестезии в экспериментах на крысах показано (табл. 4), что в 0,25 и 0,5% растворах РУ-1151, подобно маркаину, индуцирует полное (100%-ное) обезболивание спустя 5 мин после субарахноидального введения, тогда как по длительности анестезирующего действия РУ-1151 в 3,17 и 2,39 раза соответственно превосходит маркаин.
Соединение РУ-1151 в 0,5, 1 и 2% растворах не оказывает раздражающего и повреждающего действия на кожу крыс.
Таким образом, вещество РУ-1151 при инфильтрационном, проводниковом и спинномозговом методах обезболивания значительно превосходит маркаин как по местно-анестезирующей активности, так и по широте терапевтического действия.
На основе соединения РУ-1151 представляется возможным создание местно-анестезирующего лекарственного средства для инфильтрационной, проводниковой и спинномозговой анестезии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЛИ 9-ω-АРИЛОКСИАЛКИЛ-2,3-ДИГИДРОИМИДАЗО[1,2-А]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2003 |
|
RU2233279C1 |
| ДИГИДРОХЛОРИД 1-(3-ПИПЕРИДИНОПРОПИЛ)-2-(4-ФТОРОФЕНИЛ)ИМИДАЗО[1,2-A]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2006 |
|
RU2314311C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ МЕСТНО-АНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2006 |
|
RU2313341C1 |
| ДИГИДРОХЛОРИД 1-(3-ДИЭТИЛАМИНОПРОПИЛ)-2-(4-ФТОРОФЕНИЛ)ИМИДАЗО[1,2-а]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНО-АНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2006 |
|
RU2311416C1 |
| ДИГИДРОБРОМИД 1-(2-ДИЭТИЛАМИНОЭТИЛ)-2-ФЕНИЛИМИДАЗО [1,2-А]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2000 |
|
RU2160266C1 |
| ДИГИДРОХЛОРИД 2-ТРЕТ-БУТИЛ-1-(3-ЦИКЛОГЕКСИЛАМИНОПРОПИЛ)-ИМИДАЗО [1,2-А]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2000 |
|
RU2160264C1 |
| ДИГИДРОХЛОРИД 1-(2-ДИЭТИЛАМИНОЭТИЛ)-2-ФЕНИЛИМИДАЗО[1,2-А]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2006 |
|
RU2314312C1 |
| ДИГИДРОХЛОРИД 1-(3-ПИРРОЛИДИНОПРОПИЛ)-2-ФЕНИЛИМИДАЗО [1,2-А]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2000 |
|
RU2160265C1 |
| ДИГИДРОХЛОРИД 1-ДИЭТИЛАМИНОПРОПИЛ-2-ФЕНИЛИМИДАЗО[1,2-А]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 1999 |
|
RU2148057C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5,8,9,10-ТЕТРАГИДРОПИРИМИДО[4,5-d]АЗОЦИНОВ, ИМЕЮЩИХ В 4-М ПОЛОЖЕНИИ ТРИФЛАТНУЮ, ВТОРИЧНУЮ И ТРЕТИЧНУЮ АМИНОГРУППЫ | 2011 |
|
RU2478637C2 |

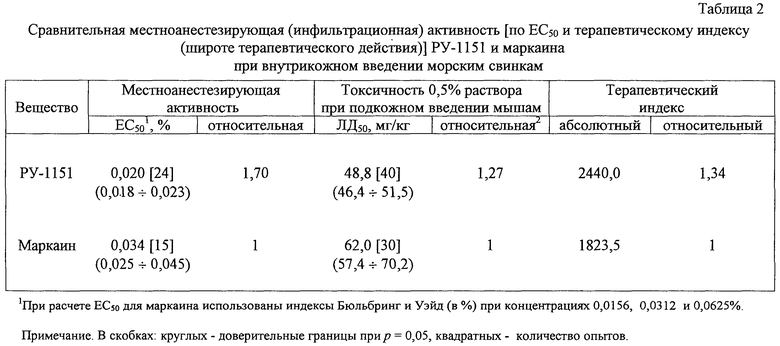
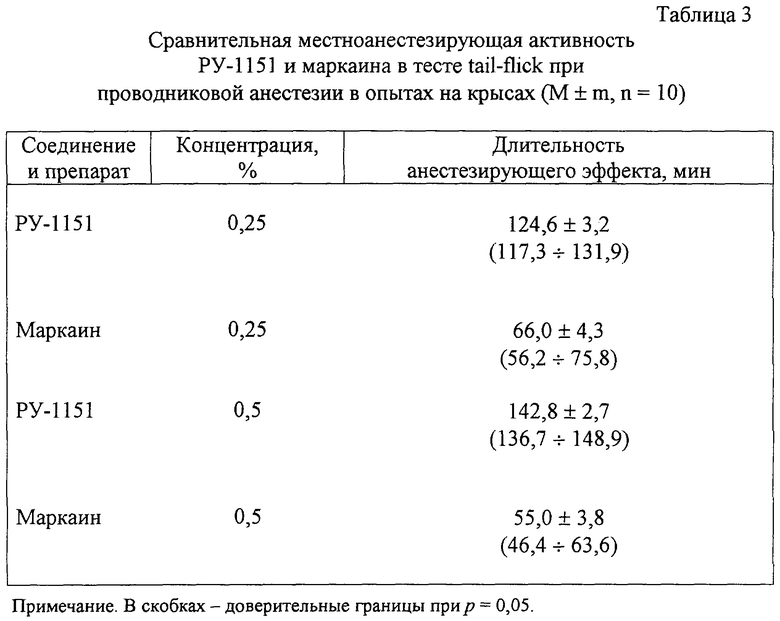

Изобретение относится к новым производным 10Н-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола, а именно к водорастворимым солям 10-ω-арилоксиалкил-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола общей формулы
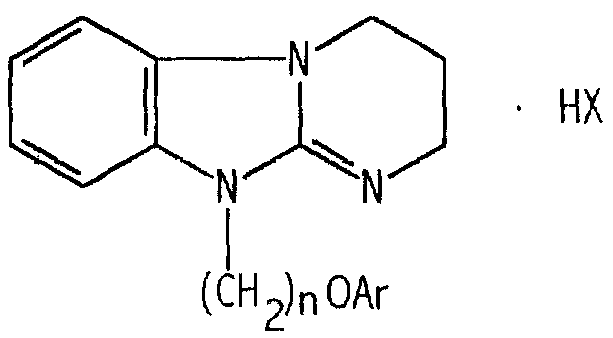
где Ar=С6Н5, С6H4R, где R = алкоксикарбонил- или карбоксигруппа в о-, м- и п-положениях бензольного кольца, n=1-6, X=С1 или Br, обладающим местноанестезирующим действием при инфильтрационной, проводниковой и спинномозговой анестезии. 1 н.з.п. ф-лы, 4 табл.
Соли 10-ω-арилоксиалкил-2,3,4,10-тетрагидропиримидо[1,2-а]бензимидазола общей формулы
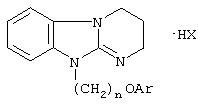
где Аr - С6Н5, С6H4R, где R - алкоксикарбонил- или карбоксигруппа в о-, м- и п-положениях бензольного кольца;
n=1-6;
X - Cl или Br.
| 10-БЕНЗИЛ-2- ГИДРОКСИ -4-ОКСО-4Н- ПИРИМИДО/1,2-А/-БЕНЗИМИДАЗОЛ, ПРОЯВЛЯЮЩИЙ НЕЙРОЛЕПТИЧЕСКУЮ, ПРОТИВОСУДОРОЖНУЮ, ПРОТИВОГИПОКСИЧЕСКУЮ, АНАЛЬГЕТИЧЕСКУЮ И АНТИНОЦИЦЕПТИВНУЮ АКТИВНОСТИ | 1993 |
|
RU2042679C1 |
| Способ получения 9-замещенных 2,3-дигидроимидазо [1,2-а] бензимидазола или их солей | 1981 |
|
SU952848A1 |
| US 3989709 A, 02.11.1976 | |||
| GB 1585965 A, 11.03.1981 | |||
| CHEMCATS | |||
| EXPLORATORY LIBRARY | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
Авторы
Даты
2004-07-27—Публикация
2003-03-25—Подача