Изобретение относится к ветеринарной медицине, а именно к генной инженерии, в частности к способу получения оригинальной нуклеотидной последовательности EgF, которая, будучи клонированной в экспрессирующую векторную систему pQE-SG 13009, позволяет получать неограниченное количество антигена эхинококка E.granulosus, используемого в качестве основного компонента иммуноферментного диагностикума для прижизненного выявления больных людей и животных ларвальным гидатидозом.
Ларвальный гидатидоз является тяжелым паразитарным заболеванием человека и с/х животных, вызываемым личиночной стадией эхинококка и приводящим к гибели заболевших. К сожалению, единственным радикальным методом лечения этого заболевания остается хирургический, зачастую малоэффективный на поздних стадиях развития инвазии.
Поэтому ранняя диагностика ларвальных эхинококкозов у больных может существенно помочь консервативному лечению данной категории пациентов (Клименко В.В. и др., АС №1363564 от 1.09.1987 г.). Однако производство антигена для соответствующей диагностики затруднено ввиду труднодоступности исходного материала для его получения обычными биохимическими методами, а качество последнего далеко не всегда обеспечивает стандартность и его высокую диагностическую эффективность.
Цель изобретения заключается в использовании генно-инженерной методики получения стандартизированного антигена EgF E.grariulosus в неограниченном количестве.
Наиболее близким прототипом является работа Smith D.B., Kevin S. and Johnson R.S. 1988. В качестве вектора авторами была выбрана фагмида λ/ZAP. Клонирование фрагмента кДНК эхинококка в данный вектор проводилось по сайтам EcoRl и Xhol. Субклонирование фрагмента ДНК E-granulosus осуществлялось в вектор pGEX с глутатион-S-трансферазой.
Недостатками прототипа являются недоступность и дороговизна используемых реагентов в условиях России.
Наша работа отличается тем, что клонированный фрагмент ДНК эхинококка размером 450 п.н. является оригинальным и отсутствует в каталоге секвенированных последовательностей E.granulosus в мировом банке генов (Gen Bank).

SEQ ID NO1 Первичная структура фрагмента F кДНК E.granulosus.
Размер фрагмента составляет 453 основания, подчеркнуты области затупленных Eco RI сайтов, мелким шрифтом выделены части сайта, по которому было проведено клонирование в полилинкер плазмиды pUC19. Нумерация начинается с конца EcoRI-линкера.
Ниже приводится аминокислотная структура получаемого рекомбинантного антигена EgF:
SEQ ID NO2

Аминокислотная структура белка Echinococcus granulosus, транслируемого с последовательности клона F. Мелким шрифтом выделены EcoRI линкеры.
Для создания банка ДНК паразита протосколексы эхинококка получали из гидатидозных цист, собранных на мясокомбинатах (хозяин - овцы, крупный рогатый скот), в охотохозяйствах (хозяин лось, кабан) и в 7-м хирургическом отделении Медицинской Академии им. И.М.Сеченова (операционный материал от людей).
Протосколексы подвергали замораживанию в жидком азоте, растирали до порошкообразного состояния и суспендировали в 1 мл раствора, содержащего 4М гуанидинизотиоционата, цитрата натрия и 5% саркозила.
Очистку и переосаждение нуклеиновых кислот проводили стандартным методом (Маниатис, Фрич, Сэмбрук, 1984, стр.109).
Конструирование кДНК библиотеки проводили по стандартным методам с помощью вектора λgt11.
Была получена кДНК библиотека в векторе λgt11. Матрицей для синтеза кДНК послужила роlу(А)РНК, выделенная из протосколексов E.granulosus из печени овцы.
Библиотека скринирована с использованием авидин-биотиновой системы с применением белков сыворотки крови людей с подтвержденным диагнозом “эхинококкоз”. Предварительно белки сыворотки крови очищались от антител к белкам Е coli, которые присутствуют в любой сыворотке крови человека. Очистка сывороток проводилась при помощи аффинной хроматографии на колонках с CH-Sepharose 4В, к которой были пришиты тотальные белки E.coli (Остерман, 1985).
Библиотеки в λgt11 высевались на чашки диаметром 95 мм, полученные клоны переносили на нитроцеллюлозные фильтры, которые окрашивали в реакции dot-ELISA.
В результате было получено несколько рекомбинантных клонов λgt11, которые продуцировали белки, обладавшие антигенными свойствами эхинококка.
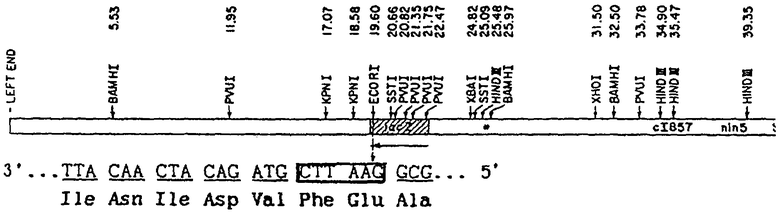
Схема клонирования фрагментов кДНК эхинококка в фаг λgt11.
Lac-Z - область фага, кодирующая β-галактозидазу. Горизонтальной стрелкой обозначено направление транскрипции. Вертикальной стрелкой - место лигирования по сайту Есо RI.
Таким образом, был проклонирован экспрессирующийся фрагмент ДНК эхинококка, представляющий собой кДНК копию информационной РНК, транскрибирующий уникальный ген E.granulosus.
С целью получения препаративных количеств гибридного антигена EgF было осуществлено субклонирование вставки кДНК E.granulosus в экспрессирующую векторную систему pQE-SG 13009.
Способ получения гибридного антигена EgF включает следующие этапы:
1) выделение эукариотической геномной ДНК E.granulosus из
протосколексов паразита;
2) получение препаративных количеств фрагмента ДНК F эхинококка с помощью ПЦР;
3) получение препаративных количеств ДНК векторной плазмиды pQE;
4) конструирование рекомбинантной плазмиды pQE-F E.granulosus;
5) проведение реакции трансформации клеток E.coli рекомбинантной плазмидой и скрининг положительных клонов;
6) экспрессия гибридного белка рекомбинантной плазмидой и его очистка;
7) определение диагностической эффективности полученного рекомбинантного антигена EgF.
Выделение эукариотической геномной ДНК Е. granulosus из протосколексов паразита
К 50 мкг отмытых в физиологическом растворе протосколексов эхинококка добавляют 10 мл лизисного буфера следующего состава: 100 мМ трис-HCl, рН 7,4; 100 мМ NaCl; 50 мМ ЭДТА. Суспендируют на шейкере 2-3 минуты, после чего вносят додецилсульфат Na до конечной концентрации 1% и протеиназу К в количестве 1 мг на 1 мл буферного раствора.
Инкубацию проводят при 37°С в течение 6 часов и при 56°С.
Депротеинизацию нуклеиновых кислот проводят стандартным фенол-хлороформовым методом (см. руководство Маниатиса, 1989 г.), вплоть до исчезновения интерфазы.
Освобожденную от протеинов ДНК осаждают 3 объемами этилового спирта, инкубируют при - 20°С 15 минут и центрифугируют 10 минут при 7000 об/мин. Полученный осадок последовательно отмывают в 70, 80 и 96%-ном этаноле, центрифугируя после каждого этапа по 5 минут при 10000 об/мин.
Осадок ДНК лиофильно высушивают и растворяют в ТЕ-буфере (10 мМ ТРИС-НС1, рН 7,4 и 1 мМ ЭДТА).
Дальнейшую очистку ДНК осуществляют следующим образом: к раствору ДНК добавляют LiCl до конечной концентрации 5М, осторожно перемешивают и инкубируют при 0°С в течение 10 минут.
Затем проводят центрифугирование при 5 тыс. оборотах в течение 30 минут при 4°С. Образовавшийся супернатант переносят в чистые пробирки Эппендорф и помещают на инкубацию в водяную баню на 10 минут при 65°С. Последующее 40-минутное центрифугирование при 17000 об/мин позволяет осадить остатки протеинов и полисахаридов. Супернатант переносят в новую пробирку и осаждают 3 объемами этанола. Полученный осадок тщательно высушивают, растворяют в воде и сохраняют при +4°С.
Получение препаративных количеств ДНК векторной плазмиды рQЕ
Оборудование: центрифуга Bekman-J2-21, микролаборатория Эппендорф (центрифуга, миксер, термостат, автоматические пипетки), водоструйный насос, ФЭК-56М, термостат, РН-метр, прибор для электрофореза, диализные мембраны, хроматоскоп, необходимая стеклянная и пластиковая посуда.
Реактивы: трис-ОН, ЭДТА, глюкоза, лизоцим, среда LB, бромистый этидий, SDS, ацетат калия, фенол, хлороформ, 70 и 96% этанол, рибонуклеаза, агароза, изопропиловый спирт, ампициллин, хлористый литий.
Засевают 5 мл среды LB в пробирке отдельной колонией бактерий, содержащей плазмиду. Инкубируют 30 минут при 37°С и добавляют соответствующий антибиотик (ампициллин 50 мг/мл). Далее ночную культуру инкубируют в том же температурном режиме при интенсивном встряхивании 16 часов. Бактериальные клетки собирают центрифугированием при 4000 об/мин в течение 10 минут. Надосадочную жидкость удаляют. Осадок бактерий ресуспендируют в 2 мл охлажденного раствора: 50 мМ глюкоза, 25 мМ трис-НСl, рН 8,0, 10 мМ ЭДТА, лизоцим 5 мг/мл. Время инкубации при 20°С - 5 минут. Затем в пробирки добавляют 4 мл раствора, содержащего 1% SDS и 0,2N NaOH, и ставят на 10 минут в лед. Периодически проводят перемешивание суспензии. Не вынимая пробирки из ледяной бани, добавляют 3 мл холодного раствора 5М ацетата калия, перемешивают содержимое и инкубируют при 0°С в течение 10 минут.
Центрифугируют в роторе Becman JS-13 при 13000 об/мин в течение 30 минут. Бактериальная ДНК и обломки клеток на дне пробирки образуют плотный осадок, надосадочная жидкость, содержащая плазмидную ДНК, полностью прозрачна. Ее переносят в чистые пробирки и добавляют по 0,6 объема изопропанола, инкубируя при комнатной температуре не менее 20 минут. Плазмидную ДНК осаждают центрифугированием при 13000g при комнатной температуре в течение 30 минут. Полученный осадок подсушивают под вакуумом, несколько раз промывают 70%-ным и 1 раз 96%-ным этанолом, спирт тщательно сливают, а осадок до полного высыхания помещают в термостат при 56°С. Высушенный осадок растворяют в 200 мкл деионизированной воды. Очистку плазмидной ДНК осуществляют 10М раствором хлористого лития, добавляя равный объем в каждую пробирку. Инкубация во льду длится не менее 20 минут, центрифугирование при 1200 об/мин - 10 минут. Супернатант, содержащий плазмидную ДНК, с помощью водоструйного насоса переносят в чистые пробирки и добавляют по 1 мл 96% этанола, инкубируют 15 минут при - 20°С, после чего центрифугируют при 12000 об/мин 5 минут.
Анализирующий электрофорез проводят в 1% агарозном геле.
Проведение реакции амплификации гомологичных фрагментов из генома эхинококка синтезированными олигонуклеотидными праймерами
В специальные пробирки Эппендорф объемом 0,5 мл добавляют последовательно 35 мкл Н2О, 5 мкл 10х полимеразного буфера (трис-HCl, рН 8.8, КСl 0,5 М, MgCl2 15 мМ, желатина 0,01%), 8 мкл смеси всех четырех трифосфатов в концентрации 50 мМ, специфические олигонуклеотидные прямые и обратные праймеры, 0,5 мкл фермента Taq DNA полимеразы, 25 нг геномной ДНК, 20 мкл минерального масла.
Устанавливают следующий цикл амплификации:
94°С - 1-2 минуты, 72°С - 1-5 минут. Количество циклов 25-30.
В последнем цикле время инкубации при 72°С - 15 минут.
Режим амплификации геномной ДНК эхинококка:
Т1-95°С – 5 минут
Т2-50°С - 2 минуты 2 цикла
Т3-72°С - 1 минуту
Т1-95°С - 30 секунд
Т2-50°С - 2 минуты 30 циклов
Т3-72°С - 1 минута
Т1-95°С-30 секунд
Т2-50°С - 2 минуты 1 цикл
Т3-72°С - 5 минут
Весь цикл амплификации длится около 4 часов. После остановки ПЦР амплификатора пробирки извлекаются из штатива и, не нарушая верхнего слоя минерального масла, берутся аликвоты ДНК в количестве 10-15 мкл для последующего проведения электрофореза в 2% агарозном геле.
Конструирование рекомбинантной плазмиды pQE-F E. granulosus
Полученные в ПЦР фрагменты имеют на концах участки узнавания для рестриктаз Bam H1 и Hind III, что делает их удобными для клонирования в векторную молекулу со стандартным полилинкером.
Выделенную и очищенную векторную ДНК рестрицируют ферментом (EcoR-1, Bam H-1) в течение 1,5 часов при 37°С. Лианеризованную ДНК подвергают очистке от протеинов фенолом и хлороформом по стандартной методике, затем двукратно переосаждают этанолом. Полученный осадок подсушивают под вакуумом и растворяют в 50 мкл ТЕ буфера. К векторной ДНК добавляют согласно общепринятой методике (Маниатис, 1986 г.) эквимолярное количество наработанного в ПЦР фрагмента F ДНК эхинококка, 10х лигазный буфер, затем проводят отжиг при 68°С в течение 10 минут, после чего реакционную смесь охлаждают во льду и добавляют 1 мкл 100 мМ раствора АТФ и 10 единиц фермента ДНК-лигазы фага Т-4. Собственно реакция лигирования (сшивания in vitro ДНК векторной молекулы и фрагмента гена эхинококка) длится 16 часов при температуре 8-10°С.
Проведение реакции трансформации клеток Е.соli рекомбинантной плазмидой
Проведение реакции трансформации компетентных клеток Е.соli лигирующей смесью позволяет оценить жизнеспособность рекомбинантной конструкции.
В качестве контроля используют ДНК нативной векторной плазмиды для трансформации тех же компетентных клеток. Эффективность трасформации дикой плазмидой составляет 105 или 106 колоний на 1 мкг векторной ДНК, рекомбинантной - 102 или 103 колоний на 1 мкг конструированной ДНК.
Скрининг положительных клонов
Скрининг рекомбинантных клонов осуществляют по модифицированному методу Ледерберга и Коэна (1986 г.). Отобранные с чашек рекомбинантные клоны повторно проверяют на наличие в них вставки ДНК эхинококка на молекулярном уровне, проводя реакции рестрикции соответствующими ферментами и электрофорез в 0,8% агарозном геле.
Экспрессия гибридного белка рекомбинантной плазмидой и его очистка
Засеивают 80 мл среды LB клетками, содержащими гибридную плазмиду.
Наращивают до плотности D600=0,5, отбирают 1 мл, центрифугируют и разбавляют клетки SDS-PAGE буфером.
Добавляют IPTG до концентрации 0,3 мМ, инкубируют 2 часа при 37°С. Отбирают 0,5 мл осадка клеток и делят на 2 пробирки.
Культуру центрифугируют при 4000 об/мин 10 минут. Удаляют супернатант, осадок замораживают при -20°С.
Из клеточного лизата белки высаливают сульфатом аммония. Фракции собирают в интервале от 35% до 65% насыщения. Далее проводят гель-фильтрацию на сефакриле S-300 на колонке диаметром 2 см и длинной 1 метр. При проведении хроматографии на ДЕАЕ-целлюлозе используют колонку диаметром 2 см и длиной 20 см. Элюция белков-антигенов осуществляется градиентом хлористого натрия в концентрации от 0 до 0,7 М.
Диагностическую эффективность полученного рекомбинантного антигена проверяют в ИФА.
Определение диагностической эффективности полученного рекомбинантного антигена F
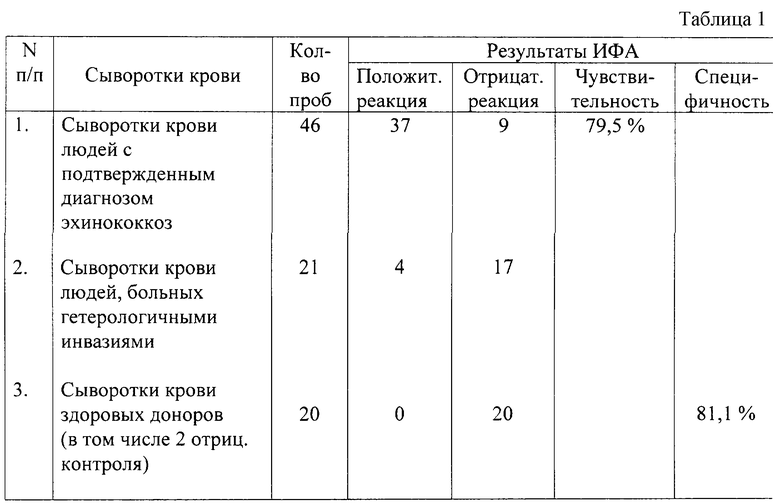
Пример 1. Диагностическую эффективность рекомбинантного антигена F оценили с 87 пробами сывороток крови людей, в том числе зараженных: E.granulosus - 46 проб, другими гельминтозами - 21, клинически здоровых доноров - 20.
Результаты испытаний представлены в таблице 1.
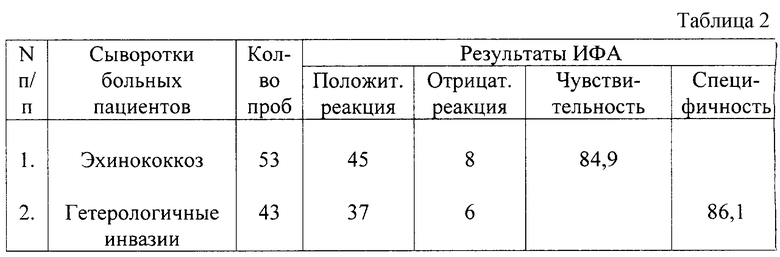
Пример 2. Диагностическую эффективность рекомбинантного антигена F оценили с 96 сыворотками людей, больных как эхинококкозом (53 пробы), так и другими инвазиями (43 пробы).
Результаты испытаний представлены в таблице 2.
Пример 3. Диагностическую эффективность рекомбинантного антигена F сравнили в комиссионном испытании в ИФР "ELISA" с коммерческим антигеном “Эхинококк IgG стрип” ЗАО “Вектор-Бест” г. Новосибирск.
Результаты испытаний представлены в таблице 3.

Анализ данных по оценке диагностической эффективности рекомбинантного антигена "F" в ИФР "ELISA" свидетельствует о его достаточно высокой чувствительности и специфичности. Это дает основание применять антиген "F" в качестве диагностикума при эхинококкозе человека и животных.
Источники информации
1. Девис Р., Ботстайн Д., Рот Дж. Методы генетической инженерии, М.: Мир, 1984.
2. Клименко В.В., Белозеров С.Н., Шеховцов Н.В. Способ получения эхинококкового диагностического антигена для иммуноферментного анализа, АС №1363564, 1987.
3. Клонирование ДНК. Методы: Пер. с англ./Под ред. Д.Гловера. - М.: Мир, 1988. - 538 с.
4. Коробко В.Г., Добрынин В.Н., Болдырев Е.Ф. Быстрый метод сборки ДНК из синтетических олигонуклеотидов. Доклады АН СССР, 1994 г., т.278, №5, - с. 1250-1253.
5. Маниатис Т., Фрич Э., Сэмбрук Дж. Молекулярное клонирование - М.: Мир, 1984.
6. Новое в клонировании ДНК. Методы: Пер. с англ. /Под ред. Д.Гловера. - М.: 1989, - 368 с.
7. Остерман Л.А. Методы исследования белков и нуклеиновых кислот. Электрофорез и центрифугирование. М.: Наука, 1981.
8. Плазмиды. Методы: Пер. с англ./Под ред. К.Харди, М.: Мир, 1989. - 267 с.
9. Birnboim H.C., Doly J. A rapid alkaline extraction method for screening recombinant plasmid DNA//Nucl.Acids Res. – 1979 -Vol.7, N6, p. 1513-1522.
10. Smith D.B. and Johnson R.S. Single-step purification of polypeptides expressed in Escherichia coli as fusions with glutathione-S-transferase//Gene, 1988, 67, 31-40.
Способ относится к ветеринарной медицине, в частности генной инженерии. Способ позволяет получать рекомбинантный антиген F E. granulosus в неограниченном количестве при его высокой чувствительности и специфичности. 3 табл.
Способ получения рекомбинантного антигена F Echinococcus granulosus, предусматривающий выделение эукариотической геномной ДНК из протосколексов паразита, получение препаративных количеств фрагмента ДНК F эхинококка с помощью ПЦР, получение препаративных количеств ДНК векторной плазмиды pQE, конструирование рекомбинантной плазмиды pQE-F Е. granulosus, трансформацию клеток рекомбинантной плазмидой, скрининг положительных клонов, экспрессию гибридного белка рекомбинантной плазмидой и его очистку, определение диагностической эффективности полученного рекомбинантного антигена EgF, отличающийся тем, что размер клонированного фрагмента ДНК эхинококка составляет 450 н.п. и представлен в SEQ ID NO1, аминокислотная структура получаемого рекомбинантного антигена EgF представлена в SEQ ID NO2.
| US 5541078 A, 30.07.1996 | |||
| Способ получения эхинококкового диагностического антигена для иммуноферментного анализа | 1985 |
|
SU1363564A1 |
Авторы
Даты
2004-08-20—Публикация
2002-07-25—Подача