Изобретение относится к области медицины, в частности к парафармацевтической промышленности, производящей препараты лечебного и профилактического назначения, и может быть использовано в качестве вспомогательного средства для усиления функций иммунной системы.
Известна биологически активная добавка (БАД) "Полифит-М" (Пилат Т.Л. (ред.). Федеральный реестр биологически активных добавок к пище. М.: Когелет, 2000, с.215), в составе которой содержатся ферментированные масла облепихи, солодки, ореха грецкого, шиповника, зверобоя, подорожника ланцетного, тысячелистника, крапивы двудомной, фиалки трехцветной, чабреца, мелиссы, василистника, дурнушника, череды трехраздельной, хвоща полевого, мать-и-мачехи, вероники и которая применяется в качестве общеукрепляющего средства, положительно влияющего на иммунную систему.
Известна биологически активная добавка (БАД) "Малиновый аромат" (Пилат Т.Л. (ред.). Федеральный реестр биологически активных добавок к пище. М.: Когелет, 2000, с.215), в составе которой содержатся трава эхинацеи, цветы липы, трава зверобоя, корни и корневища девясила, корни солодки, экстракт шиповника. Выпускается в виде пакетиков с порошком и применяется в качестве общеукрепляющего средства, положительно влияющего на иммунную систему.
Недостатком известных препаратов является наблюдающаяся у отдельных пациентов индивидуальная непереносимость к некоторым компонентам препарата.
Задачей изобретения является разработка нового доступного лекарственного препарата - биологически активной добавки, выпускаемой в таблетированной форме, удобной для применения и обладающей сбалансированным комплексом витаминов и микроэлементов.
Изобретение направлено на расширение ассортимента альтернативных лекарственных средств для поддержания функции иммунной системы и компенсации индивидуальной непереносимости к некоторым компонентам.
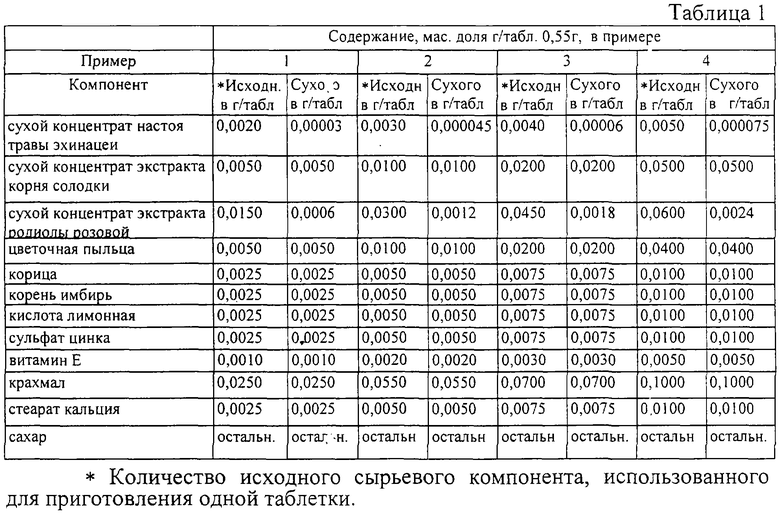
Это достигается тем, что предложен препарат, обладающий иммунокорректирующим действием, включающий сухой концентрат настоя травы эхинацеи, сухой концентрат экстракта корня солодки, сухой концентрат экстракта родиолы розовой, цветочную пыльцу, корицу, корень имбиря, кислоту лимонную, сульфат цинка, витамин Е, крахмал, стеарат кальция и сахар при следующем соотношении компонентов в граммах на таблетку массой 0,55 г:
Сухой концентрат настоя травы эхинацеи 0,00003-0,000075
Сухой концентрат экстракта корня солодки 0,0050-0,0500
Сухой концентрат экстракта родиолы розовой 0,0006-0,0024
Цветочная пыльца 0,0050-0,0400
Корица 0,0025-0,0100
Корень имбиря 0,0025-0,0100
Кислота лимонная 0,0025-0,0100
Сульфат цинка 0,0025-0,0100
Витамин Е 0,0010-0,0050
Крахмал 0,0250-0,100
Стеарат кальция 0,0025-0,0100
Сахар Остальное
Препарат назван - Биологически активная добавка "Иммунные плюс".
БАД "Иммунные плюс" оказывает иммунокорректирующее действие, повышает неспецифическую резистентность организма, увеличивает фагоцитарную активность и функциональную активность гуморального и клеточного звена иммунитета, тормозит патологические иммунные реакции, предупреждает токсико-аллергические реакции, усиливает энергетику клетки, регулирует обмен веществ.
БАД "Иммунные плюс" показана к применению при вторичной иммунологической недостаточности, для профилактики и вспомогательной терапии бактериальных (в том числе туберкулеза), вирусных и грибковых инфекций, воспалительных процессов различной локализации, гнойных заболеваний кожи, ослабленных состояний, соматических заболеваний, в условиях неблагоприятной экологической обстановки, повышенной физической и психоэмоциональной нагрузок.
Биологически активную добавку "Иммунные плюс" в форме таблеток получают следующим образом.
0,56 кг предварительно измельченной травы эхинацеи заливают в эмалированной емкости на 10-15 л водой комнатной температуры в количестве 7 л и выдерживают на кипящей водяной бане 25 минут при частом помешивании, затем охлаждают при комнатной температуре 15 минут. Настой процеживают, отжимая растительное сырье. При необходимости доливают до требуемого количества очищенную воду. Фильтруют через 4 слоя марли.
Выход настоя 5,6 кг.
Сахар в количестве 83,0 кг взвешивают в мешке на весах, визуально проверяют на наличие механических примесей, затем при отсутствии примесей измельчают на мельнице. Для этого сахар из мешка загружают порциями в загрузочный бункер. Измельченный сахар через нижний штуцер мельницы собирают в полиэтиленовый мешок, концы которого предварительно закрепляют на штуцере. Мешок помещают в приемник.
Выход измельченного сахара 82,1 кг.
Пыльцу цветочную в количестве 1,9 кг взвешивают в мешке на весах, визуально просматривают на наличие механических примесей, затем при отсутствии примесей измельчают на мельнице. Для этого цветочную пыльцу из мешка загружают порциями в загрузочный бункер. Измельченную цветочную пыльцу через нижний штуцер мельницы собирают в полиэтиленовый мешок, концы которого предварительно закрепляют на штуцере. Мешок помещают в приемник.
Выход измельченной пыльцы 1,85 кг.
Корень имбиря просматривают на наличие посторонних примесей и механических загрязнений, взвешивают на весах в количестве 1,0 кг и измельчают на мельнице.
Выход готового продукта 0,93 кг.
0,93 кг лимонной кислоты взвешивают на весах, добавляют 1,6 кг настоя травы эхинацеи, перемешивают до растворения кислоты, при необходимости подогревают, затем добавляют 3,7 кг фармокопейного сухого экстракта солодкового корня и перемешивают до получения однородной смеси. Фильтруют через 4 слоя марли.
Выход готового продукта 6,2 кг.
Измельченный сахар, пыльцу цветочную, крахмал, корицу, корень имбиря, витамин Е, сульфат цинка просеивают через сито с диаметром отверстий 1 мм, кальций стеарат просеивают через сито с диаметром отверстий 0,5 мм. Воду, фармокопейный экстракт (4% сухого) родиолы розовой фильтруют через 4 слоя марли.
В эмалированной емкости доводят до кипения 3,4 кг настоя. Отдельно готовят взвесь крахмaла в настое, для этого берут крахмал в количестве 0,3 кг и 0,6 кг настоя. Перемешивают смесь и добавляют в кипящий раствор при постоянном помешивании, клейстер доводят до кипения.
Выход крахмального клейстера 4,25 кг.
В смеситель при открытой крышке загружают 72,1 кг измельченного сахара, 9,9 кг крахмала и перемешивают 5 минут. Отдельно смешивают 4 кг измельченного сахара и 0,37 кг витамина Е, перемешивают и добавляют в смеситель. Также отдельно смешивают 6 кг сахара, 0,93 кг сульфата цинка, тщательно перемешивают и загружают в смеситель. Включают мешалку смесителя и смесь перемешивают в течение 10 минут. Затем добавляют 1,85 кг цветочной пыльцы, 0,93 кг порошка корицы и 0,93 кг корня имбиря, перемешивают 10 минут. Увлажняют экстрактом родиолы розовой в количестве 5,6 кг и смесью раствора лимонной кислоты, добавляют фармокопейный сухой экстракт солодкового корня в количестве 6,2 кг. Смесь перемешивают в течение 5 минут. Добавляют крахмальный клейстер в настое в количестве 4,25 кг. Перемешивают 10 минут.
Выход готового продукта 113,06 кг.
Увлажненную таблеточную массу в количестве 113,06 кг раскладывают на бумагу в лотки слоем толщиной 1,5-2 см. Лотки устанавливают в сушильном шкафу.
Включают систему подачи горячего воздуха в распределительное устройство сушильного шкафа. Устанавливают температуру сушки 40-45°С, при повышении которой подача горячего воздуха автоматически отключается. Процесс сушки проводят в течение 10 часов до постоянного веса при периодическом перемешивании (не менее 3-х раз). Контроль за окончанием сушки ведут в лаборатории путем взвешивания проб продукта из лотков до постоянного веса. Влажность продукта не более 2%. Сухую таблеточную массу направляют на сухое гранулирование.
Выход сухой таблеточной массы 101 кг.
Высушенную смесь в количестве 101 кг загружают порциями в установку для получения гранулята из сухих таблетсмесей. Включают шнековое устройство, при помощи которого смесь продавливают через сетку с отверстиями диаметром 1,5-2,0 мм. Сухой гранулят собирают в приемник. Из приемника сухой гранулят загружают при открытой крышке в смеситель. В сухую гранулированную таблеточную смесь в смесителе добавляют просеянный стеарат кальция в количестве 1,02 кг. Включают мешалку и перемешивают в течение 5 минут. Готовый гранулят передают на таблетирование.
Выход готового гранулята 101,0 кг.
Из смесителя сухой гранулят направляют на таблетирование в загрузочный бункер таблетировочной машины. Включают двигатель. Предварительно устанавливают обороты двигателя в соответствии с насыпным весом, зону прессования и высоту таблетки. При запуске машины включается пылесос.
Диаметр таблетки 12,0±0,3 мм
Высота таблетки 4,0±0,3 мм
Средний вес таблетки 0,55±0,03 г
Во время таблетирования следят за работой машины и за качеством таблеток. Каждые 30 минут проверяют распадаемость, прочность и средний вес таблеток. Таблетки, не отвечающие требованиям, отбраковывают и отправляют нa повторную переработку. По окончании процесса машину выключают в обратном порядке. Таблетки собирают в приемник и направляют на обеспыливание.
Выход продукта 100,45 кг.
Готовые таблетки просеивают на вибросите через отверстие диаметром 8 мм, взвешивают на весах по 8 кг и загружают в чистые сухие полиэтиленовые ведра. Образцы готовых таблеток передают в контрольно-аналитическую лабораторию на анализ. При соответствии таблеток нормам технической документации готовые таблетки передают на стадию фасовки.
Выход готовых таблеток 99,9 кг.
Последовательность операций одинакова, независимо от количества приготавливаемого состава.
БАД "Иммунные плюс" содержит известные, разрешенные для применения в медицинской практике лекарственные средства, которые в указанной комбинации (см. таблицу 1, примеры 1-4) могут быть использованы в качестве вспомогательного средства для усиления функций иммунной системы.
В качестве вспомогательных компонентов, обеспечивающих надежность сохранения формы прессованных таблеток в сухом виде и короткое время распадаемости их во влажной среде, использован крахмал, отруби, сахар, а для улучшения текучести гранулята - стеарат кальция и тальк.
Выпускается в виде таблеток, что удобно для применения, имеет длительный срок хранения (2 года).
В ходе клинических испытаний БАД "Иммунные плюс" назначали пациентам с вторичной иммунологической недостаточностью (ВИН) при различных формах хронической патологии (ИБС, нейроциркуляторной дистонии, гипертонической болезни).
При первичном исследовании количественные показатели Т-лимфоцитов CD3, Т-хелперов CD4, естественных киллеров CD16, цитотоксических лимфоцитов CD8 (особенно содержание Т-хелперных лимфоцитов) или находились на нижней границе нормы при нормальном содержании В-лимфоцитов. У всех пациентов отмечалось снижение функциональной активности лимфоцитов на стандартные митогены. Показатели фагоцитоза микро- и макрофагоцитов находились на нижней границе нормы.
У пациентов с кардиальной патологией была выявлена вторичная иммунологическая недостаточность с преимущественными нарушениями Т-клеточного звена иммунитета.
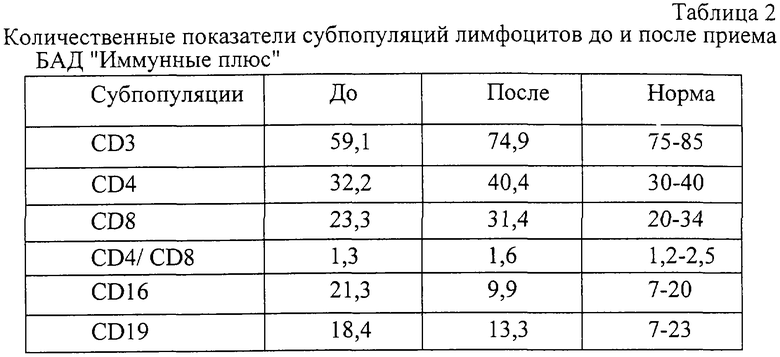
Через 30 дней приема БАД "Иммунные плюс" оценка идентичных показателей иммунного статуса показало достоверное увеличение количества Т-хелперных лимфоцитов и увеличение их функциональной активности в реакции на стандартные митогены. Отмечены также положительные сдвиги в содержании и функциональной активности клеток-фагоцитов (подтвержденные методом хемолюминисценции) (см. таблицу 2).
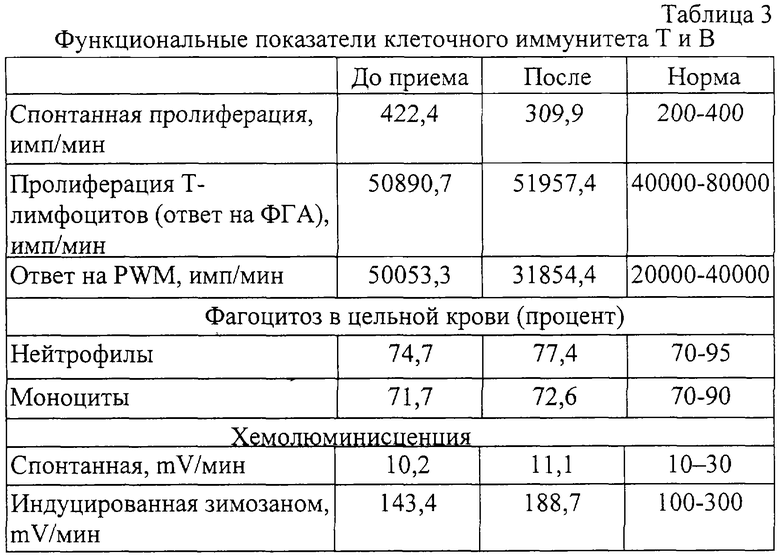
Было отмечено достоверное увеличение количественных и функциональных показателей Т-клеточного звена иммунитета и коррекцию синдрома дисфункции фагоцитоза с улучшением клинического состояния больных и положительной динамикой сопутствующей очаговой инфекции (хронические фарингиты, хронические тозиллиты), имевшихся у 40% пациентов (см. таблицу 3).
БАД "Иммунные плюс" назначали больным с лекарственно-устойчивыми формами туберкулеза на фоне лечение резервными противотуберкулезными препаратами в соответствие с категориями ДОТS+.
Проведенные исследования показали, что использование БАД "Иммунные плюс" в комплексном лечении больных туберкулезом способствовало более быстрому купированию симптомов интоксикации. Так, уже к концу второй недели лечения у больных, принимавших препарат, исчезли слабость, головокружение, потливость. Повысился аппетит, нормализовалась температура. В контрольной группе аналогичный результат был достигнут только в 3-4 недели лечения.
Субъективные признаки улучшения состояния у больных были подтверждены лабораторными показателями: через 10 дней комплексного лечения у больных, принимавших препарат, отмечалась нормализация СОЭ, снизилось количество лейкоцитов. Положительным моментом лечения БАД можно считать уменьшение эозинофилии (количество эозинофилов снизилось с 8 до 2%), что благоприятно отразилось на течении специфического процесса.
Положительные сдвиги через 2 месяца лечения были выявлены у больных опытных групп и в отношении бактериовыделения. Его прекращение к концу срока наблюдения произошло у 36% больных. Причем у остальных больных бактериовыделение из обильного стало скудным, что также отражало благоприятную тенденцию в лечении. Это подтверждали и иммунологические показатели. Изучение уровня противотуберкулезных антител в реакции ИФА показало, что прием изучаемых БАД способствовал снижению специфической сенсибилизации организма и переходу экссудативных процессов в пролиферативные. У больных контрольной группы конверсия мазка была замедленной: лишь у 48% больных бактериовыделение значительно уменьшилось и только у 32% прекратилось (см. таблицу 4).
БАД "Иммунные плюс" назначали пациенткам после гинекологических операций для профилактики осложнений воспалительного характера.
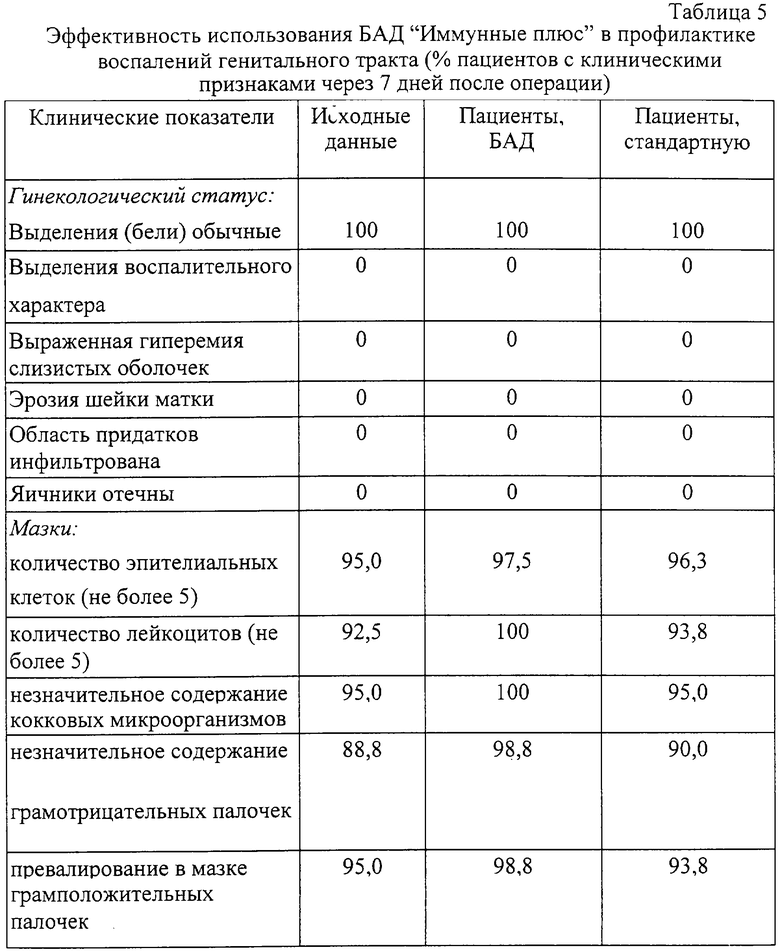
Предварительные исследования выявили у всех обследованных женщин благоприятный гинекологический статус: бели обычного характера, гиперемия вульвы и влагалища не выражена, эрозивных процессов не отмечено. Данные культуральной диагностики подтвердили отсутствие у них возбудителей заболеваний, передающихся половым путем, а также Trichomonas, GN, Candida. Осмотр пациенток после проведенного курса лечения подтвердил сохранение благоприятного гинекологического фона, отсутствие признаков воспалительного процесса, патологических кровотечений. Исследование мазков подтвердило благоприятное состояние генитального тракта. Количество эритроцитов и лейкоцитов в поле зрения мазка не превышало 5. В мазках превалировали грамположительные палочки (см. таблицу 5).
Таким образом, БАД "Иммунные плюс" может быть рекомендована в качестве средства, повышающего функцию иммунной системы.

Изобретение относится к фармацевтической промышленности и используется в качестве вспомогательного средства для усиления функций иммунной системы. Препарат, обладающий иммунокорректирующим действием, содержит сухой концентрат настоя травы эхинацеи, сухой концентрат экстракта корня солодки, сухой концентрат экстракта родиолы розовой, цветочную пыльцу, корицу, корень имбиря, кислоту лимонную, сульфат цинка, витамин Е, крахмал, стеарат кальция и сахар, взятые в определенном соотношении. Препарат выполнен в виде таблетки массой 0,55 г. Препарат способствует эффективному усилению функций иммунной системы. 5 табл.
Препарат, обладающий иммунокорректирующим действием, характеризующийся тем, что содержит сухой концентрат настоя травы эхинацеи, сухой концентрат экстракта корня солодки, сухой концентрат экстракта родиолы розовой, цветочную пыльцу, корицу, корень имбиря, кислоту лимонную, сульфат цинка, витамин Е, крахмал, стеарат кальция и сахар при следующем соотношении компонентов, г на таблетку массой 0,55 г:
Сухой концентрат настоя травы эхинацеи 0,00003-0,000075
Сухой концентрат экстракта корня солодки 0,0050-0,0500
Сухой концентрат экстракта родиолы розовой 0,0006-0,0024
Цветочная пыльца 0,0050-0,0400
Корица 0,0025-0,0100
Корень имбиря 0,0025-0,0100
Кислота лимонная 0,0025-0,0100
Сульфат цинка 0,0025-0,0100
Витамин Е 0,0010-0,0050
Крахмал 0,0250-0,100
Стеарат кальция 0,0025-0,0100
Сахар Остальное
| Пилат Т.Л | |||
| Федеральный реестр биологически активных добавок к пище | |||
| - М.: Когелет, 2000, с | |||
| Кузнечный горн | 1921 |
|
SU215A1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ ДЛЯ ПРОФИЛАКТИКИ ОСЛАБЛЕНИЯ ИММУННОЙ СИСТЕМЫ | 2001 |
|
RU2182011C1 |
| СРЕДСТВО "РЯНЧУН", ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩИМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2208450C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2147223C1 |
| СПОСОБ ПОЛУЧЕНИЯ АППЛИКАЦИОННОГО СРЕДСТВА | 2001 |
|
RU2179456C1 |
| РЕАБИЛИТАЦИОННОЕ СРЕДСТВО НА ОСНОВЕ РАСТИТЕЛЬНОГО СЫРЬЯ | 1999 |
|
RU2164146C2 |
Авторы
Даты
2004-12-10—Публикация
2002-09-26—Подача