Изобретение относится к области иммунологии, медицины, конкретно, к созданию противотуберкулезных вакцин нового поколения. Оно может быть использовано в фармацевтической промышленности и молекулярной фармакологии и представляет собой композицию для доставки и представления иммуногенов микобактерий иммунной системе организма.
В последние несколько лет в мире наметился серьезный рост заболеваемости туберкулезом (1). Около 1,5 миллиарда человек являются инфицированными микобактериями туберкулеза (2). Заболевание вызывается Mycobacterium tuberculosis, облигатным внутриклеточным паразитом, персистирующим в макрофагах человека, причем, вследствие незавершенного фагоцитоза, именно эти клетки участвуют в диссеминации процесса (3).
Контроль над этой инфекцией основан на вакцинации с помощью вакцины БЦЖ - живого, аттенюированного, непатогенного вакцинного штамма Mycobacterium bovis. БЦЖ была введена в календарь вакцинации, предусмотренный программой EPI в 1974 г. Около 100 млн. детей ежегодно получают эту вакцину.
Несмотря на осуществляемые иммунопрофилактические мероприятия, уровень заболеваемости населения остается достаточно высоким. Не все, привитые вакциной БЦЖ, приобретают устойчивый к возбудителю туберкулеза иммунитет. В настоящее время туберкулезом ежегодно заболевают не менее 9 млн. человек и 3-4 млн. ежегодно умирают (4).
Одной из особенностей возбудителя туберкулеза является бактерионосительство, когда микобактерии живут в клетках организма. Это свидетельствует о недостаточной стимуляции Т-клеточного иммунного ответа после иммунопрофилактики вакциной БЦЖ (активация цитотоксических лимфоцитов, способных элиминировать зараженные клетки организма). Поэтому проблема повышения иммуногенности вакцины БЦЖ имеет важное эпидемиологическое и эпизоотологическое значение.
Достижения в области генетики, молекулярной биологии и биотехнологии определили современную стратегию разработки вакцин. На сегодняшний день одним из перспективных направлений является разработка генно-инженерных вакцин при помощи наработки антигенов инфекционных агентов микробиологическим синтезом. К тому же известно, что важнейшим событием в процессе формирования иммунного ответа является определение пути, по которому пойдет развитие Т-хелперов (5). При этом совместное введение вакцины с таким цитокином, как интерферон-гамма, при вакцинации приводит к ускорению дифференцировки Т- и В-лимфоцитов, а совместное введение ФНО-альфа стимулирует их пролиферацию (6). Эти данные обусловили появление множества запатентованных вакцинных конструкций на основе рекомбинантных микобактерий с повышенными иммуностимулирующими свойствами.
Известна микобактериальная вакцина (7), содержащая рекомбинантные бактерии Mycobacterium bovis BCG, несущие плазмиду, в состав которой входит ген, кодирующий цитокин - интерлейкин-2. Данный цитокиновый ген экспрессируется под контролем промотора гена стресс-белка. Цитокин секретируется в активной форме. Такая вакцинная конструкция при введении хозяину (человеку или другому млекопитающему) обеспечивает более сильный иммуный ответ (продукция антител, Т-клеточный ответ), чем BCG дикого типа.
По несколько иному пути пошла другая группа американских разработчиков (Bloom B.R. et al., 8, 9). Они используют геном микобактерий (например, ДНК М. bovis BCG) для интеграции в него генетического материала других видов микобактерий (например, M.leprae antigens), а также иных инфекционных агентов (антигены сальмонелл, вирусные антигены). Сконструированные таким образом микобактериальные частицы могут содержать также гены цитокинов (например, интерферонов - α, β, γ; факторов некроза опухолей -α и -β; интерлейкинов 1-7). При введении млекопитающим такого рода конструкции у последних наблюдается выраженый иммунный ответ.
Описанные рекомбинантные микобактериальные вакцины созданы на основе аттенуированных или инактивированных возбудителей. Однако присутствие части белков инфекционного агента в вакцине не желательно (4, 10). Так, например, известно, что среди вирусных белков есть и В-клеточные эпитопы, стимулирующие продукцию усиливающих инфекционность антител, и Т-клеточные эпитопы, стимулирующие супрессирующие клетки, и области, перекрестно реагирующие с нормальными белками клеток, и иммуносупрессивные районы. Поэтому для создания эффективных и безопасных вакцин нового поколения перспективно разрабатывать синтетические пептидные вакцины, которые будут содержать несколько "важных" Т- и В-клеточных эпитопов инфекционного агента.
Американская фирма Merck and Co., Inc. получила патент в России (11) на полинуклеотидную противотуберкулезную вакцину, представляющую собой генно-инженерную конструкцию, содержащую ген, кодирующий микобактериальный белок 85А, В или С, связанный с цистроном, содержащим ген, кодирующий один из цитокинов (например, ГМ-КСФ, интерферон или интерлейкин-12). Вакцина, содержащая эффективное количество такого химерного полипептида, связанного с фармацевтически приемлемым носителем, обеспечивает индукцию иммунного ответа у позвоночных против микобактериального белка 85А, а также способна ослабить заболевание, вызванное микобактериями. Недостатком описанной конструкции является ограниченный набор микобактериальных антигенных эпитопов.
К недостаткам описанной генно-инженерной вакцины следует отнести сравнительно небольшие молекулярные массы синтезируемых полипептидов-иммуногенов, от тысячи до нескольких десятков тысяч дальтон. Поэтому при вакцинации используют различные адъюванты, что не всегда желательно и вызывает побочные эффекты. Наиболее сильным из адъювантов является адъювант Фрейнда, который для людей использовать запрещено. К тому же введение "незащищенных" рекомбинантных ДНК в организм приводит к их быстрой инактивации под действием нуклеаз крови и, как следствие, низкой эффективности доставки к клеткам-мишеням.
Во многом эти проблемы могут быть решены при использовании молекулярного вектора для доставки генов в клетки-мишени (12), который представлят собой частицы, в центре которых находится нуклеотидный материал (например, рекомбинантная плазмидная ДНК, содержащая доставляемые гены), а на поверхности - антитела к клеткам-мишеням. Антитела входят в состав конъюгата: спермидин-полиглюкин, который несет несколько функций. Во-первых, защищает доставляемые гены от действия нуклеаз; во-вторых, удерживает конъюгат на отрицательно заряженной ДНК за счет положительного заряда спермидина, который является еще и стимулятором проникновения молекул ДНК в эукариотические клетки.
Для вакцинации людей перспективным представляется создание такой конструкции противотуберкулезной вакцины, которая бы сочетала в себе и антигенные свойства, и стимулятор иммунного ответа, и в то же время имела молекулярную массу, сравнимую с молекулярными весами микобактерий, т.е. являлась бы полным антигеном.
Известна молекулярная конструкция (вакцина) вирусоподобного вида как средство доставки иммуногенов (13, прототип), содержащая в центре полинуклеотидный комплекс в виде двуспиральной РНК, как стимулятор иммунной резистентности организма, покрытый слоем конъюгата: спермидин-полиглюкин-субстрат и/или аналог субстрата фермента, а на поверхности частиц - гибридные белки, содержащие эпитопы инфекционного агента и фермент. Такого рода вирусоподобные частицы вызывали повышение и пролонгацию иммунного ответа, выступая в качестве своеобразного депо антигенов инфекционного агента (например, ВИЧ).
Описанная конструкция касается только вирусоподобных частиц (вакцин). Искусственные бактериальные частицы в литературе пока не описаны.
Технической задачей изобретения является создание генно-инженерной противотуберкулезной вакцинной композиции на основе широкого спектра антигенов микобактерий вакцинного штамма БЦЖ, способной эффективно стимулировать Т- и В-клеточные факторы иммунного ответа у млекопитающих при иммунизации этими препаратами.
Поставленная задача решается путем создания молекулярной конструкции, которая представляет собой искусственные микобактериальные частицы, в центре которых находится полинуклеотидный комплекс (двуспиральная РНК), а на поверхности - полный репертуар белков-антигенов вакцинного штамма БЦЖ в составе конъюгата: спермидин - полиглюкин.
Сущность изобретения заключается в том, что искусственные микобактериальные частицы для иммунизации против туберкулеза представляют собой частицы размером 25-30 нм в диаметре (это сравнительно большие размеры, что позволяет их использовать для иммунизации без адъювантов как полноценные антигены), содержащие в центре полинуклеотидный комплекс (двуспиральную РНК - стимулятор неспецифической резистентности организма; например, дсРНК киллерных дрожжей Sacharomyces serevisiae), а на поверхности - белки-антигены вакцинного штамма БЦЖ (полный репертуар) в составе конъюгата: спермидин - полиглюкин. Связь между полинуклеотидным комплексом и конъюгатом осуществляется посредством ионного взаимодействия между отрицательным зарядом полинуклеотидного комплекса и положительным зарядом спермидина.
Поставленная цель (эффективная стимуляция Т- и В-клеточных факторов иммунного ответа при иммунизации искусственными микобактериальными частицами) достигается также созданием противотуберкулезных вакцинных композиций, включающих кроме описанных выше искусственных микобактерий дополнительно эффективное количество цитокинов - интерферона - γ и ФНО-α.
Известно, что ведущую роль в стимуляции иммунного ответа играет интерферон - γ, и индивиды с нарушенной системой интерферона более подвержены воздействию инфекционных агентов (14). Исходя из этих данных и была сконструирована модель микобактериальных частиц с индуктором интерферона - двуспиральной РНК, а также созданы композиции, включающие цитокины. Последнее объясняется тем, что максимальный синтез интерферона - γ на введение дсРНК происходит через 4-6 ч после инъекции (10), тогда как его действие необходимо с момента попадания патогена в организм. В состав вакцинных композиций цитокины введены из расчета по 10 мкг интерферона - γ (105 ME) и по 10 мкг ФНО-α. (105 Е) на 30 мкг белков-антигенов микобактерий вакцинного штамма БЦЖ.
Именно эта совокупность признаков обеспечивает более высокий титр антител и более выраженный иммунный ответ при иммунизации созданными композициями по сравнению с иммунизацией просто вакцинным щтаммом БЦЖ.
Состав противотуберкулезных вакцинных композиций представлен ниже.
1. Искусственные микобактериальные частицы (МБЧ), обладающие иммуногенными свойствами против возбудителя туберкулеза, содержащие в центре полинуклеотидный комплекс в виде дсРНК (20 мкг), а на поверхности - полный репертуар белков-иммуногенов вакцинного штамма БЦЖ (30 мкг) в составе конъюгата [полиглюкин-спермидин].
2. МБЧ + интерферон - γ 10 мкг (105 ME) на 30 мкг белков-антигенов БЦЖ.
3. МБЧ + интерферон - γ 10 мкг (105 ME) + ФНО-α. 10 мкг (105 Е) на 30 мкг белков-антигенов БЦЖ.
Изобретение иллюстрируется следующими примерами графических изображений.
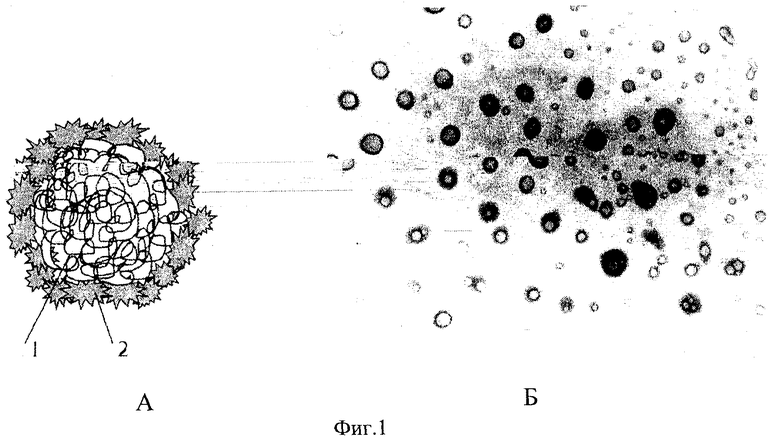
Фиг.1 - искусственные микобактериальные частицы:
А - схема искусственной микобактериальной частицы, где: 1 - нуклеотидный материал двуспиральной РНК; 2 - конъюгат: спермидин-полиглюкин-микобактериальные белки-антигены вакцинного штамма БЦЖ.
Б - электронная фотография частиц (увеличение × 88000).
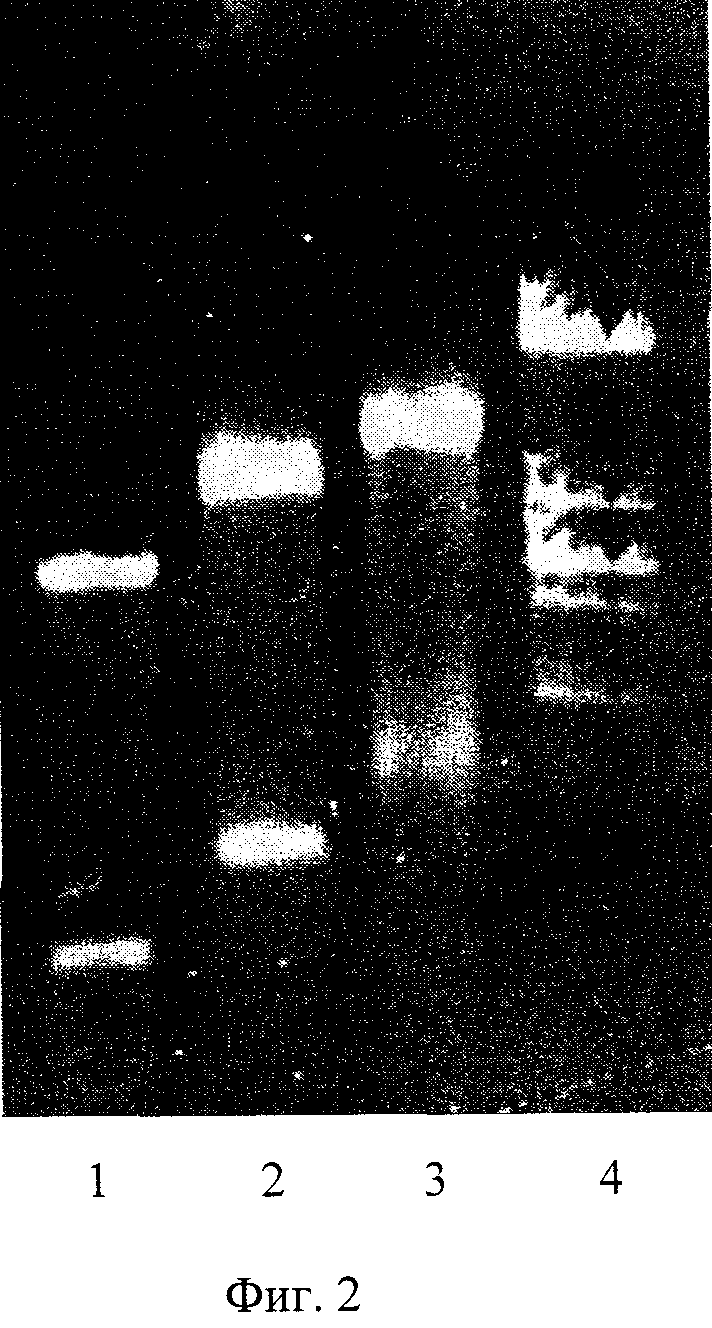
Фиг.2 - электрофореграмма препаратов компонентов искусственных микобактериальных частиц в 1%-ном геле агарозы, где дорожки:
1 - исходная двуспиральная РНК (дсРНК);
2 - дсРНК в оболочке из конъюгата "спермидин-полиглюкин";
3 - дсРНК в оболочке из конъюгата "спермидин-полиглюкин-антигенные белки" вакцинного штамма БЦЖ;
4 - маркеры мол.массы (гидролизат ДНК фага λ рестриктазой EcoRI).
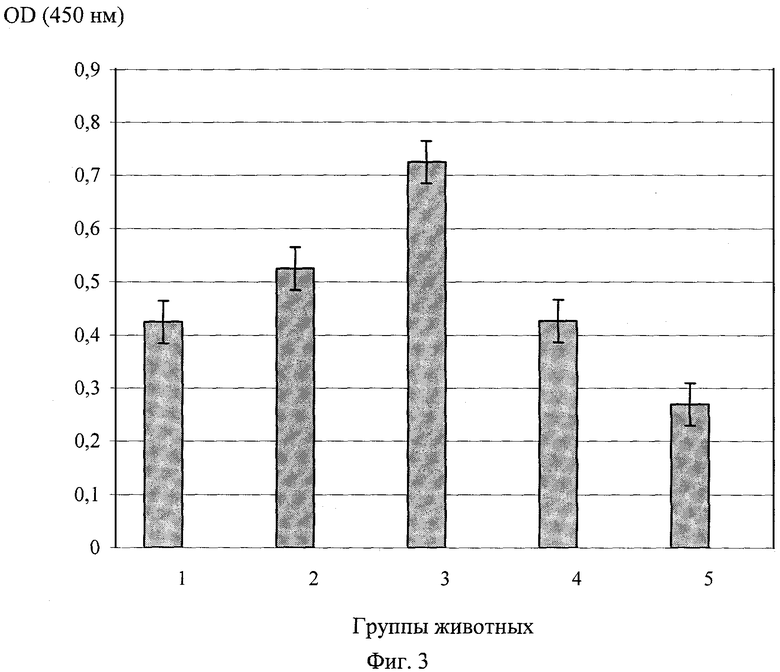
Фиг.3 - диаграмма уровеня суммарного пула антител у животных после иммунизации разными образцами препаратов вакцинных композиций (р<0,05).
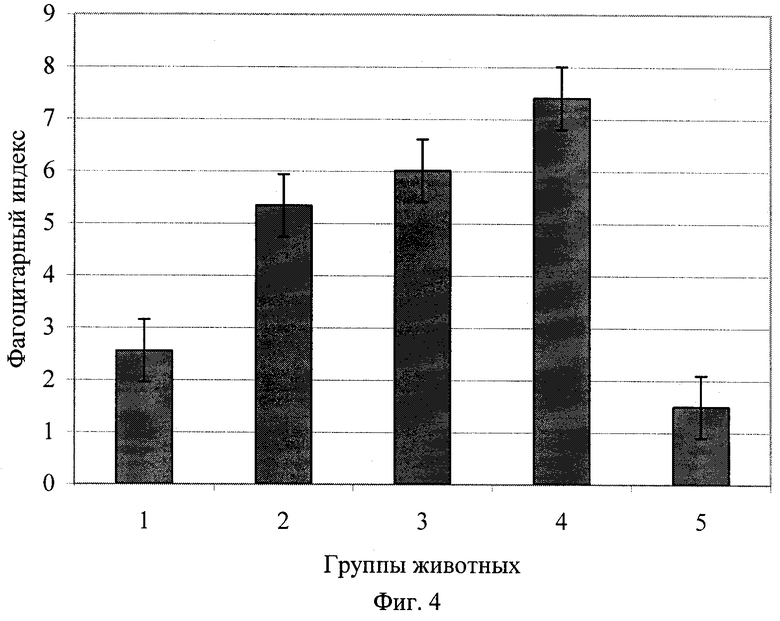
Фиг.4 - диаграмма уровня фагоцитарной активности мононуклеарных клеток после вакцинации животных разными образцами препаратов вакцинных композиций (р<0,05).
Для лучшего понимания сущности изобретения ниже приводятся примеры его конкретного выполнения.
Пример 1. Получение белков-антигенов (полного репертуара) вакцинного штамма БЦЖ.
Белки-антигены получают из вакцинного штамма БЦЖ. Клетки микобактеорий (20 мг) суспендируют в 5 мл буфера (10 мМ калий-фосфат, рН 7,5, 150 мМ NaCl) и разрушают ультразвуком (УЗДН-2Т, 22 кГц), 5 экспозиций по 20 сек. Для удаления липополисахаридов к полученной суспензии добавляют 250 мкл хлороформа, интенсивно перемешивают 5 мин и центрифугируют (20 мин, 10000 об/мин). Отбирают пипеткой водную фазу и для осаждения ДНК добавляют 1,3 мл раствора 5 М NaCl и 0,3 мл 10%-ного раствора полиэтиленимина. Смесь перемешивают, инкубируют 20 мин в ледяной бане и центрифугируют (20 мин, 10000 об/мин). Полученный осадок растворяют в 200 мкл ТЕ буфера, далее раствор диализуют против карбонатного буфера (25 мМ, рН 9,0), содержащего 150 мМ NaCl.
Пример 2. Синтез конъюгата.
Для синтеза конъюгата 3 мг реополиглюкина растворяют в 0,5 мл 10 мМ раствора периодата натрия и инкубируют 2 ч при комнатной температуре. Активированный полисахарид отделяют от периодата натрия гель-фильтрацией на колонке с сефадексом G-50 (V=2 мл) и добавляют 6 мл раствора, содержащего 1 мг спермидина и 5 мг антигенов БЦЖ. После инкубации в течение ночи при 6°С непрореагировавшие компоненты удаляют гель-фильтрацией на колонке с сефадексом G-50 (V=20 мл).
Пример 3. Сборка искусственных микобактериальных частиц. В качестве "центрального ядра" (полинуклеотидного комплекса) композиции используют двуспиральную РНК дрожжей штамма Saccharomyces cerevisiae M437 Y116 (L-форма - 3000000 Д, М-форма - 1200000 Д). Выбор обусловлен тем, что она является основным компонентом лекарственного препарата "Ридостин", который разрешен к применению в медицинской практике в качестве стимулятора неспецифической резистентности. Этот препарат стимулирует иммунореактивность, оказывает противоопухолевое и радиопротективное действие, хорошо метаболизируется и не накапливается в организме (15). Для сборки искусственных микобактериальных частиц к 3 мг двуспиральной РНК, растворенной в 1 мл физиологического раствора, добавляют полученный конъюгат, смесь инкубируют 2 ч при 4°С и образовавшийся комплекс отделяют гель-фильтрацией на колонке с сефарозой CL-6B (V=25 мл). Полученный препарат стерилизуют ультрафильтрацией.
Пример 4. Получение противотуберкулезной вакцинной композиции.
В раствор с полученными искусственными микобактериальными частицами добавляют препараты цитокинов: γ-интерферона (γ-ИФН) или совместно γ-интерферона и фактора некроза опухолей (α-ФНО) из расчета на 30 мкг белков-антигенов по 10 мкг γ-ИФН (105 ME) или по 10 мкг γ-ИФН (105 ME) + 10 мкг α-ФНО (105 Е). В работе используют препараты γ-интерферона (γ-ИФН) и фактора некроза опухолей-α (α-ФНО) производства ГНЦ ВБ “Вектор”.
Пример 5. Характеристика искусственных микобактериальных частиц.
Вид полученных искусственных микобактериальных частиц схематично представлен на фиг.1А. При электронной микроскопии такие конструкции имеют шарообразный вид с диаметром около 10-25 нм (фиг.1Б.). На электрофореграмме в агарозном геле (фиг.2.) видно, что двуспиральная РНК (L- и М-формы), покрытая конъюгатом [полиглюкин-спермидин], имеет меньшую подвижность. Это можно объяснить увеличением молекулярной массы и тем, что положительно заряженный спермидин частично нейтрализует в комплексе отрицательный заряд РНК. Искусственные микобактериальные частицы (дсРНК, покрытые конъюгатом [спермидин-полиглюкин-белки БЦЖ]) имеют еще меньшую подвижность в геле агарозы, на уровне фрагментов ДНК с молекулярной массой около 10-12 МД (фиг.2).
Для проверки полноты упаковки нуклеотидного материала в собранной конструкции проводят ее обработку РНКазой (0,05 мг/мл). Методом гель-электрофореза было установлено, что если для исходной двуспиральной РНК полная деградация наблюдается уже через 30 мин инкубации, то в собранной конструкции нуклеотидный материал сохраняется интактным не менее суток. Частицы в препарате вакцины сохраняют свою компактную структуру при хранении в условиях бытового холодильника не менее 6 мес.
Пример 6. Иммунизация лабораторных животных
Для иммунизации сконструированными вакцинными препаратами были использованы мыши линии BALB/c, весом 18-20 г. Животные содержались в эксперименте с соблюдением норм и требований биоэтического комитета ГНЦ ВБ “Вектор”. Пяти группам животных (по 8 особей в каждой группе) вводили внутримышечно трехкратно с интервалом через две недели следующие препараты в объеме 0,1 мл:
1. БЦЖ (30 мкг) - для контроля и сравнения.
2. Микобактериальные частицы (МБЧ): дсРНК (20 мкг) - белки БЦЖ (30 мкг).
3. МБЧ + γ-интерферон 10 мкг (105 ME).
4. МБЧ + γ-интерферон 10 мкг (105 МЕ) + α-ФНО 10 мкг (105 Е).
5. Физиологический раствор (контрольные животные).
Пример 7. Оценка иммунного ответа
Уровень суммарного пула антител в сыворотках крови животных, после иммунизации разными препаратами определяют методом иммуноферментного анализа. В лунки планшет сорбируют микобактериальные клетки вакцинного штамма БЦЖ, затем вносят образцы исследуемых сывороток. Связавшиеся с антигеном специфические антитела выявляют конъюгатом антивидовых антител с пероксидазой. Из данных, представленных на фиг.3, видно, что уровень суммарного пула антител при иммунизации микобактериальными частицами выше, чем при использовании вакцинного штамма БЦЖ. Введение в состав вакцинной композиции цитокина γ-ИФН способствует повышению уровня антител, а введение α-ФНО ингибирует их синтез (фиг.3).
В иммунопрофилактике туберкулеза основным компонентом иммунологической перестройки является активация клеточных факторов специфической защиты, прежде всего Т-лимфоцитов и макрофагов, а также их регуляторов, цитокинов [4].
Фагоцитарную активность мононуклеарных клеток иммунизированных животных изучают на 35-й день после начала иммунизации. Результаты эксперимента по влиянию на фагоцитарную активность испытанных препаратов представлены на фиг.4. Из диаграммы видно, что фагоцитарная активность мононуклеарных клеток у группы животных, иммунизированных микобактериальными частицами, выше, чем у группы животных, иммунизированных вакциной БЦЖ. Введение в состав вакцины препаратов γ-ИФН, а также γ-ИФН в сочетании с α-ФНО приводит к значимому повышению фагоцитарной активности. Вероятно, это обусловлено их специфическими функциями [6, 14, 16].
Эффективность клеточного иммунитета является интегральным показателем и включает с себя определение фагоцитарного числа, завершенности фагоцитоза и уровня бластной трансформации лимфоцитов [5, 17]. Реакцию бластной трансформации лимфоцитов (РБТЛф) проводили с использованием цельной гепаринизированной крови от иммунизированных животных [18]. При этом установлено иммуностимулирующее действие испытанных препаратов: БЦЖ - 8%, молекулярная конструкция - 9%, конструкция в сочетании с γ-ИФН - 10%, в сочетании с γ-ИФН и α-ФНО - 11%. Наличие более 7% бласттрансформированных клеток в исследуемых образцах свидетельствует о иммуностимулирующем эффекте испытанных препаратов. В проведенных экспериментах наибольшей иммуностимулирующей активностью обладала конструкция в сочетании с γ-ИФН и α-ФНО (11%). Известно, что чем выше пролиферативная активность лимфоцитов периферической крови у иммунизированных животных, тем ниже уровень туберкулезных изменений и выше продолжительность жизни после заражения [14].
Введение γ-ИФН и его индуктора при иммунизации стимулирует как В-клеточный (фиг.3), так и Т-клеточный иммунный ответ (фиг.4). При этом γ-ИФН ускоряет дифференцировку Т- и В-лимфоцитов, а сочетанное введение α-ФНО стимулирует их пролиферацию [6]. При этом введение γ-ИФН и α-ФНО способствует пролиферации мононуклеарных клеток в бласттрансформированные клетки, что свидетельствует об усилении Т-клеточного иммунного ответа. В свою очередь дсРНК, воздействуя на макрофаги и NK-клетки (неспецифические клетки-киллеры), индуцирует синтез интерферонов [10].
Таким образом, использование предлагаемой конструкции микобактериальных частиц позволяет:
- экспонировать на поверхности молекулярной конструкции полный репертуар белков вакцинного штамма БЦЖ;
- использовать двуспиральную РНК в молекулярной конструкции ("центральное ядро" частиц) в качестве неспецифического стимулятора иммунного ответа;
- используемый для получения конъюгата полиглюкин также является стимулятором иммунного ответа;
- сравнительно большие размеры частиц молекулярной конструкции (около 25 нм) позволяют ее использовать для иммунизации без адъювантов как полноценные антигены.
Введение в состав противотуберкулезной вакцинной композиции цитокинов (γ-интерферона и α-ФНО) приводит к более выраженному ответу клеточного звена иммунной системы организма млекопитающего.
Источники информации
1. Raviglione, M.C. et al., "Global epidemiology of tuberculosis", JAMA, 1995, v.273, p.220-226.
2. Schitt-Gerowitt H. "On the development of mycobacterial infections". I.A review concerting the common situation", Zentrabl.Bacteriol, 1995, v.1, p.5-13.
3. Sibill Y., Reynolds H. "Macrophages and polymorphonuclear neutrophils in lung defense and injury", Am.Rev.Respir. Dis., 1990, v.141, p.47-50.
4. Визель А.А., Гурылева М.Э. "Туберкулез", М., ГЭОТАР Медицина, 1999.
5. Хаитов P.M., Пинегин Б.В. "Современные представления о защите организма от инфекции", Иммунология, 2000, №1, с.61-64.
6. Ярилин А.А. "Система цитокинов и принципы ее функционирования в норме и при патологии", Иммунология, 1997, №5, с.7-14.
7. Патент США №5776465, кл. А 61 К 39/04, опубл. 07.07.1998 г.
8. Патент США №5504005, кл. С 12 N 15/64, опубл. 02.04.1996 г.
9. Патент США №6270774, кл. А 61 К 35/00, опубл. 07.08.2001 г.
10. Ершов Ф.И. "Система интерферона в норме и при патологии", М., Мир, 1996.
11. Патент РФ №2186109, кл. С 12 N 15/11, опубл. 27.07.2002 г.
12. Патент РФ №2190018, кл. С 12 N 15/87, опубл. 27.09.2002 г.
13. Заявка на патент РФ №2000109010/13 от 10.04.2000 г., кл. А 61 К 39/00, опубл. 20.05.2002 г.
14. Lalvani A., Brookes R., Wilkinson R.J. et al. "Human cytolytic and interferon γ-secreting CD8+ Т lymphocytes specific for Mycobacterium tuberculosis", Proc. Natl. Acad. Sci. USA, 1998, Vol.95, p.270-272.
15. Патент РФ №2083221, кл. А 61 К 38/20, опубл. 10.07.1997 г.
16. Чекнев С.Б. "Эффекторы естественной цитотоксичности в нецитотоксических регуляторных взаимодействиях". Иммунология, 1999, №6, с.25-36.
17. Никитин В.М. Справочник методов иммунологии, Кишинев, “Штиинца”, 1982, с.113-116.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО НА ОСНОВЕ НАНОЧАСТИЦ, НЕСУЩИХ РЕКОМБИНАНТНЫЙ ФАКТОР НЕКРОЗА ОПУХОЛИ АЛЬФА ЧЕЛОВЕКА | 2008 |
|
RU2386447C1 |
| ВАКЦИНА ПРОТИВ ВИРУСНЫХ ИНФЕКЦИЙ | 2000 |
|
RU2217162C2 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ПРОТИВ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА | 2006 |
|
RU2317107C2 |
| РЕКОМБИНАНТНЫЕ ШТАММЫ ВИРУСА ГРИППА, ЭКСПРЕССИРУЮЩИЕ МИКОБАКТЕРИАЛЬНЫЙ ПРОТЕКТИВНЫЙ АНТИГЕН ESAT-6, И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2005 |
|
RU2318872C2 |
| ПОЛИАНТИГЕННАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ И ВСПОМОГАТЕЛЬНОГО ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2019 |
|
RU2724896C1 |
| ВАКЦИНА РЕКОМБИНАНТНАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ И АДЪЮВАНТ ДЛЯ НЕЕ | 2017 |
|
RU2665817C1 |
| Противоопухолевое средство на основе биодеградируемых наночастиц, несущих рекомбинантный фактор некроза опухоли альфа человека | 2018 |
|
RU2691938C1 |
| Конъюгат белка рецепторсвязывающего домена (RBD) поверхностного гликопротеина S вируса SARS-CoV-2 с полимером полиглюкин-спермидин (PGS) и вакцинный комплекс против коронавирусной инфекции COVID-19 на основе указанного конъюгата и плазмидной ДНК pVAX-RBD | 2022 |
|
RU2781294C1 |
| ПОЛИНУКЛЕОТИДНАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ ВАКЦИНА | 1995 |
|
RU2186109C2 |
| КОМПОЗИЦИЯ ДЛЯ СТИМУЛИРОВАНИЯ СОЗРЕВАНИЯ ДЕНДРИТНЫХ КЛЕТОК, СОДЕРЖАЩАЯ ГИБРИДНЫЙ БЕЛОК Rv2299c/ESAT-6 | 2017 |
|
RU2733886C2 |
Изобретение относится к области иммунологии, медицины, конкретно, к созданию противотуберкулезных вакцин нового поколения. Оно может быть использовано в фармацевтической промышленности и молекулярной фармакологии и представляет собой композицию для доставки и представления иммуногенов микобактерий иммунной системе организма. Искусственные микобактериальные частицы, содержащие в центре полинуклеотидный комплекс (двуспиральную РНК - стимулятор неспецифической резистентности организма, дс РНК киллерных дрожжей Saccharomyces cerevisiae), а на поверхности - белки-антигены вакцинного штамма БЦЖ (полный репертуар) в составе конъюгата: спермидин-полиглюкин. Введение в состав противотуберкулезной вакцинной композиции кроме искусственных микобактериальных частиц эффективного количества препаратов цитокинов (γ-интерферона и ФНО-α) приводит к более выраженному ответу клеточного звена иммунной системы организма млекопитающего по сравнению с вакциной на основе штамма БЦЖ. Преимущество изобретения заключается в повышении специфической активности. 2 н. и 4 з.п. ф-лы, 4 ил.
| ПОЛИНУКЛЕОТИДНАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ ВАКЦИНА | 1995 |
|
RU2186109C2 |
| ВАКЦИНА ПРОТИВ ТУБЕРКУЛЕЗА | 1999 |
|
RU2153354C1 |
| RU 2000121671 A, 27.08.2002 | |||
| МОЛЕКУЛЯРНЫЙ ВЕКТОР ДЛЯ ДОСТАВКИ ГЕНОВ В КЛЕТКИ-МИШЕНИ | 2000 |
|
RU2190018C2 |
Авторы
Даты
2004-12-20—Публикация
2003-01-10—Подача