Уровень техники изобретения
Область техники, к которой относится изобретение
Изобретение относится к веществам и способам получения (1S,2S,3S)-2-[2-(1-этоксикарбонил-3-фенилпропиламино)пропионил]-1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты (формулы 1)
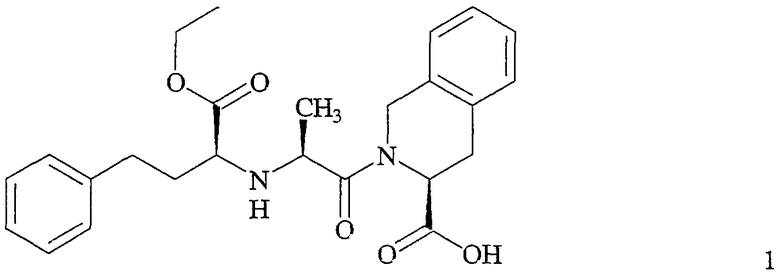
которая широко известна как хинаприл.
Обсуждение
Гидрохлорид хинаприла является активным фармацевтическим ингредиентом (препаратов) ACCUPRIL® и ACCURETIC®, который продается Pfizer Inc. для лечения гипертензии и застойной сердечной недостаточности. Хинаприл и его основной метаболит - хинаприлат (хинаприлдикислота) являются известными ингибиторами ангиотензинпревращающего фермента (АСЕ). АСЕ представляет собой пептидилдипептидазу, которая катализирует превращение ангиотензина I в сосудосуживающий фактор - ангиотензин II. См., например, патент США № 4344949, выданный Hoefle и др. (патент '949), и патент США № 4761479, выданный Goel и др. (патент '479). См. также Klutchko et al. "Synthesis of Novel Angiotensin Converting Enzyme Inhibitor Quinapril and Related Compounds. A Divergence of Structure-Activity Relationships for Non-Sulfhydryl and Sulfhydryl Types," J. Med. Chem. Vol. 29, p. 1553 (1986).
Способы получения хинаприла и его хлористоводородной соли включают процессы, основанные на патенте '949 и патенте США № 4686295, выданном Youssefyeh и др. (патент '295). Указанные способы включают взаимодействие бензилового эфира (3S)-1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты (бензилового эфира THIQ) (формулы 2)
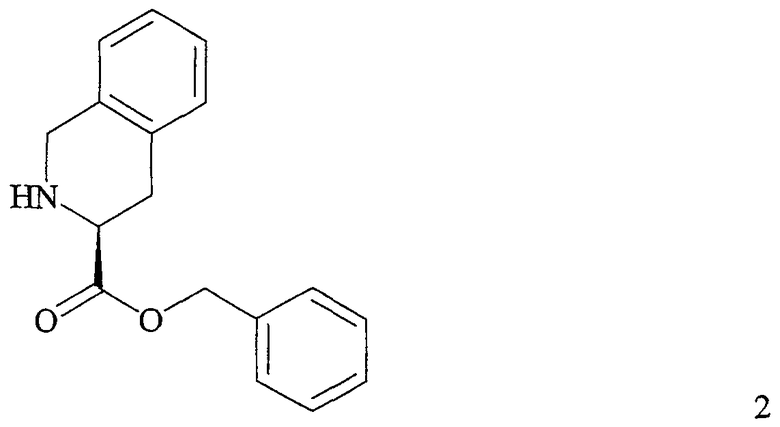
с этиловым эфиром (1S,2S)-2-(1-карбоксиэтиламино)-4-фенилмасляной кислоты (формулы 3)
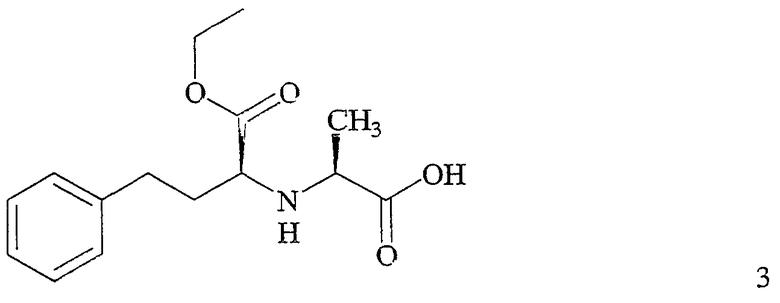
или с этиловым эфиром (2S,4S)-2-(4-метил-2,5-диоксооксазолидин-3-ил)-4-фенилмасляной кислоты (формулы 4)
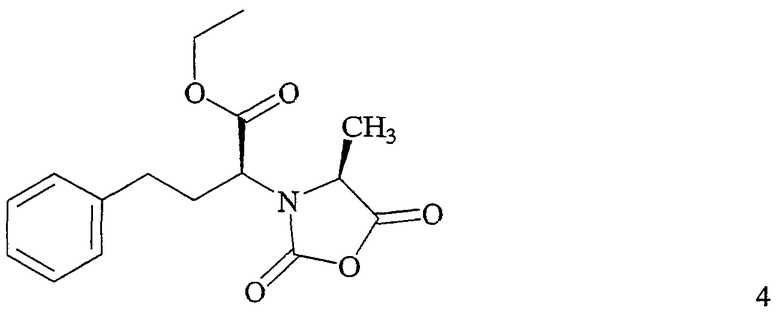
с получением бензилового эфира (1S,2S,3S)-2-[2-(1-этоксикарбонил-3-фенилпропиламино)пропионил]-1,2,3,4-терагидроизохинолин-3-карбоновой кислоты (формулы 5)
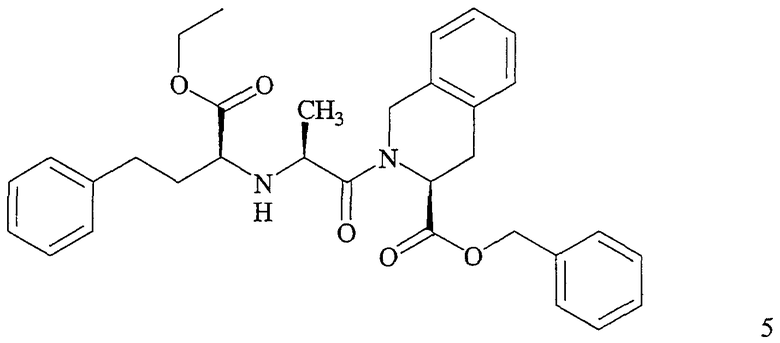
Обе реакции проводят в апротонном растворителе, таком как метиленхлорид. Реакция с N-замещенной аминокислотой (формула 3) включает использование агента сочетания (например, дициклогексилкарбодиимида) и катализатора (например, N-гидроксибензотриазола), тогда как в реакции с N-карбоксиангидридом (формула 4) используют каталитические количества кислоты.
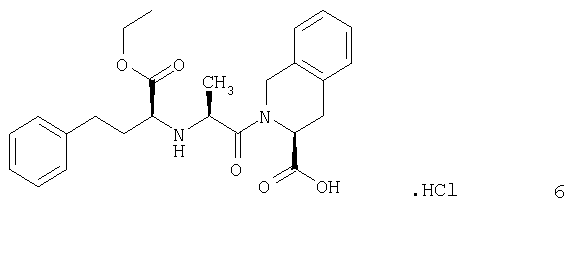
После катализируемого Pd/C гидрогенолиза обработкой смесью HCl и растворителя удаляют бензильную защитную группу, получая после обработки хлористоводородную соль хинаприла (формулы 6)
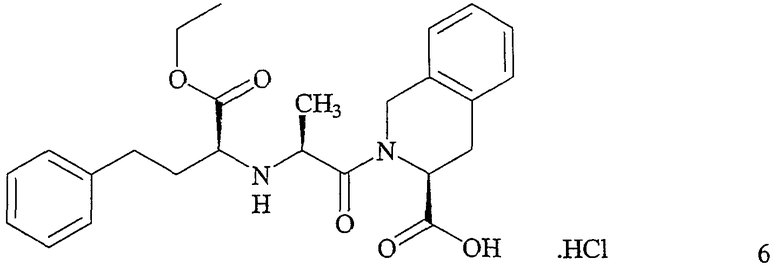
Пути синтеза, основанного на патентах '949 и '295, используют легко доступные исходные вещества (формула 2 - формула 4), но при этом теряется от 20 до 40% выхода в расчете на лимитирующие реагенты. Потери выхода приписывают внутримолекулярной циклизации (аминолизу) хинаприла (формула 1) или его бензилового эфира (формула 5) до дикетопиперазина. См. G. Guo et al. "Physical Characteristics and Chemical Degradation of Amorphous Quinapril Hydrochloride", J. Pharm. Sci. Vol. 89, p. 128 (2000). Образование дикетопиперазина ускоряется при температуре выше примерно 45°C и происходит прежде всего во время перегонки для удаления растворителя процесса гидрогенолиза.
Данное изобретение направлено на преодоление или уменьшение влияния одной или более описанных выше проблем.
Сущность изобретения
Данное изобретение предоставляет вещества и способы получения хинаприла (формула 1), хинаприла.HCl (формула 6) и их фармацевтически приемлемых солей, включая аморфные и кристаллические формы солей. По сравнению с существующими способами предлагаемый способ дает хинаприл и его соли со значительно более высоким выходом (более высоким примерно на 25%), что приводит к заметной экономии. Дополнительно способ устраняет необходимость в гидрогенолизе, исключая при этом трудности, связанные с обращением с водородом, и заметно увеличивая производительность процесса. Фактически данное изобретение дает приблизительно трехкратное повышение производительности при использовании существующего оборудования.
Таким образом, один из аспектов данного изобретения предлагает способ получения соединения формулы 1,
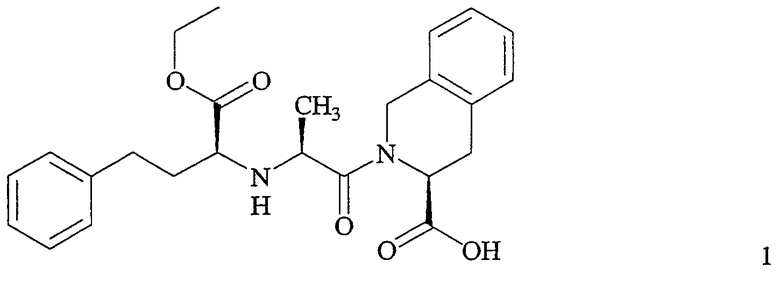
или фармацевтически приемлемой соли соединения формулы 1.
Способ включает взаимодействие соединения формулы 4
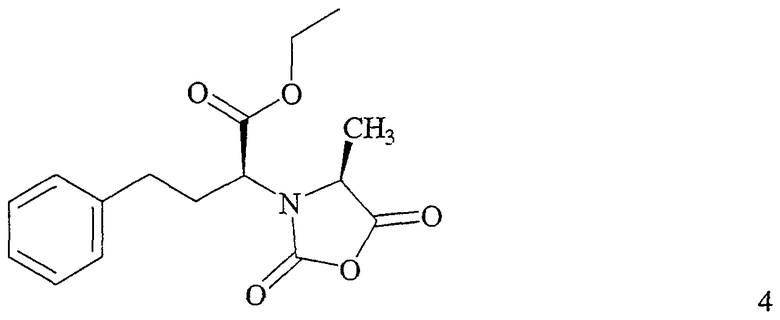
с соединением формулы 7
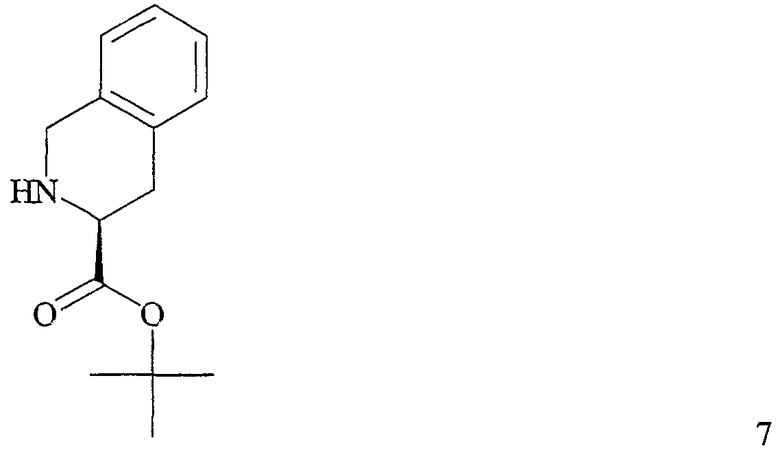
с получением соединения формулы 8
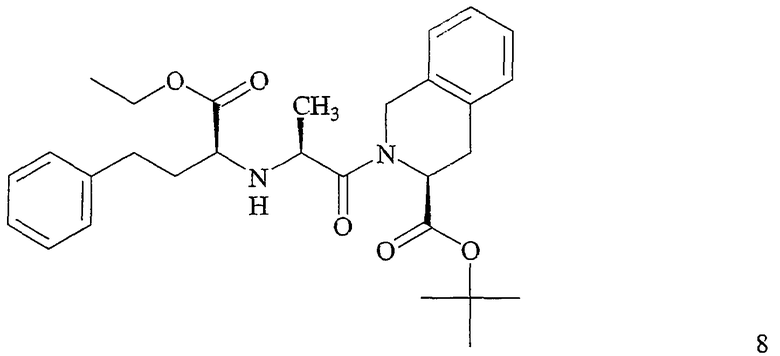
которое затем контактирует с кислотой с получением соединения формулы 1 или его фармацевтически приемлемой соли.
В другом аспекте данного изобретения предложен способ получения соединения формулы 6
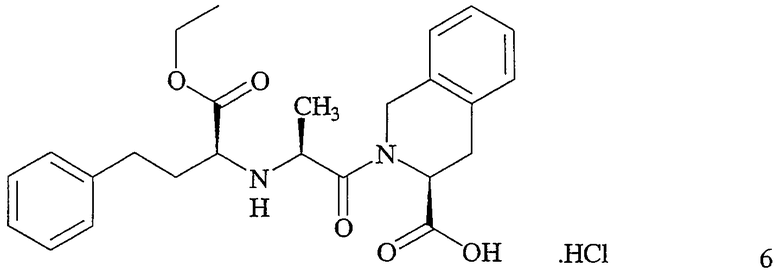
включающий взаимодействие соединения формулы 4 с соединением формулы 7 с получением соединения формулы 8 (как описано выше). Способ также включает контактирование соединения формулы 8 с HCl с получением соединения формулы 6.
Дополнительный аспект данного изобретения включает способ получения аморфной формы соединения формулы 6. Способ включает взаимодействие соединения формулы 4 с соединением формулы 7 с получением соединения формулы 8 (как описано выше). Способ также включает контактирование соединения формулы 8 с HCl и ацетоном с получением соединения формулы 9
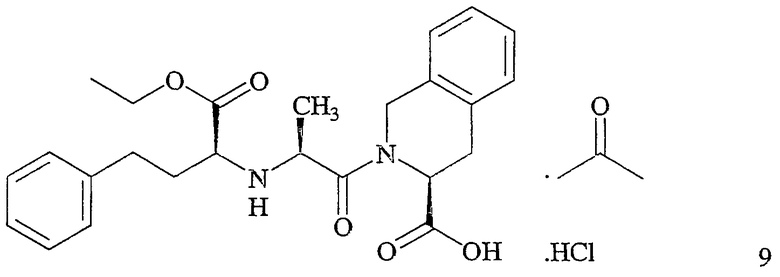
и последующую перекристаллизацию соединения формулы 9 из полярного апротонного растворителя с получением аморфной формы соединения формулы 6 после сушки.
Подробное описание
В описании использована следующая таблица списка сокращений:
Схема I иллюстрирует способ получения аморфной хлористоводородной соли хинаприла (формула 6). Указанный способ, который может быть легко модифицирован для получения свободного основания (формула 1) или другой соли и полиморфных форм, включает взаимодействие этилового эфира (2S,4S)-2-(4-метил-2,5-диоксооксазолидин-3-ил)-4-фенилмасляной кислоты (формула 4) с трет-бутиловым эфиром (3S)-1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты (формула 7) в присутствии каталитических количеств кислоты (например, НОАс, трифторуксусной кислоты или кислоты с аналогичным значением рКа) с получением трет-бутилового эфира хинаприла - трет-бутилового эфира (1S,2S,3S)-2-[2-(1-этоксикарбонил-3-фенилпропиламино)пропионил]-1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты (формула 8).
Реакцию проводят в одном или более апротонных или протонных растворителях при температуре ниже примерно 60°C и, более типично, при температуре ниже или равной примерно 45°C. Хотя более низкие температуры реакции помогают минимизировать образование нежелательных побочных продуктов, реакцию обычно проводят при температуре примерно 15°C или выше, чтобы гарантировать по существу полную конверсию в приемлемый промежуток времени (то есть менее 3 ч). Таким образом, температура реакции обычно находится в интервале от примерно 15°C до примерно 45°C включительно и, более типично, в интервале от примерно 30°C до примерно 35°C включительно. Применимые апротонные растворители включают, но не ограничиваются ими, ароматические растворители, такие как толуол, галогеналкилы, такие как MeCl2, хлороформ и подобные; циклические или ациклические простые эфиры, такие как ТГФ, диэтиловый эфир и диметоксиэтан; и кетоны, такие как ацетон, 2-бутанон и подобные. Применимые протонные растворители включают, но не ограничиваются ими, спирты, такие как MeOH, EtOH и подобные; сложные алкиловые эфиры, такие как этилацетат; и воду.
Трет-бутиловый эфир THIQ (формула 7) может быть получен из CHEMICREA в виде соли с пара-толуолсульфокислотой (соли PTSA с трет-бутиловым эфиром THIQ) и выделен путем экстракции водой и органическим растворителем (например, толуолом) в щелочных условиях (например, от рН 8 до рН 9) с последующей перегонкой органической фазы. Если не указано иначе, любая ссылка в описании на интервал температур, интервал рН и т.д. включает указанные конечные точки.
После реакции сочетания N-карбоксиангидрида (формула 4) и трет-бутилового эфира THIQ (формула 7) защитную трет-бутильную группу удаляют взаимодействием трет-бутилового эфира хинаприла (формула 8) с водной или безводной хлористоводородной кислотой. Реакцию проводят в одном или более апротонных или протонных растворителях (например, НОАс, MeCl2, толуол и т.д.) обычно при КТ и получают в твердой фазе гидрохлорид хинаприла. Количество органического растворителя, добавляемого к реакционной смеси, достаточно велико, чтобы предотвратить осаждение компонентов реакционной смеси, но достаточно мало, чтобы избежать необходимости последующего удаления перегонкой, минимизируя этим образование дикетопиперазина. Хотя трет-бутильная группа может быть удалена использованием другой кислоты, взаимодействие трет-бутилового эфира THIQ c HCl позволяет провести удаление защитной группы и образование хлористоводородной соли в одну стадию.
После образования твердофазной хлористоводородной соли хинаприла реакционную смесь помещают в вакуум примерно при КТ для выделения HCl. К раствору добавляют ацетон и охлаждают раствор до температуры примерно 0°C для осаждения хинаприла.HCl в виде сольвата с ацетоном (формула 9). Полученное кристаллическое твердое вещество отделяют от смеси фильтрованием (например, фильтрованием на центрифуге) и затем перекристаллизовывают из полярного апротонного растворителя, такого как ацетонитрил. Перекристаллизованный сольват затем сушат, получая аморфное твердое вещество. Способ дает аморфный хинаприл.HCl с хорошим выходом (то есть 90%-ный выход в расчете на соль PTSA c трет-бутиловым эфиром THIQ).
Кроме хинаприла (формула 1), другие предложенные соединения способны образовать фармацевтически приемлемые соли (включая дисоли). Указанные соли включают, но не ограничиваются ими, аддитивные соли с кислотами и соли с основаниями. Фармацевтически приемлемые аддитивные соли с кислотами могут включать нетоксичные соли, полученные из неорганических кислот, таких как соляная, азотная, фосфорная, серная, бромистоводородная, йодистоводородная, фтористоводородная, фосфористая и подобные, так же как и нетоксичные соли, полученные из органических кислот, таких как алифатические моно- и дикарбоновые кислоты, фенилзамещенные алкановые кислоты, гидроксиалкановые кислоты, алкандиовые кислоты, ароматические кислоты, алифатические и ароматические сульфокислоты и т.д. Указанные соли, таким образом, включают сульфаты, пиросульфаты, бисульфаты, сульфиты, бисульфиты, нитраты, фосфаты, моногидрофосфаты, дигидрофосфаты, метафосфаты, пирофосфаты, хлориды, бромиды, йодиды, ацетаты, трифторацетаты, пропионаты, каприлаты, изобутираты, оксалаты, малонаты, сукцинаты, субераты, себацинаты, фумараты, малеаты, манделаты, бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, фталаты, бензолсульфонаты, толуолсульфонаты, фенилацетаты, цитраты, лактаты, соли яблочной кислоты, тартраты, метансульфонаты и подобные.
Фармацевтически приемлемыми солями с основаниями могут быть нетоксичные соли, полученные из оснований, включая катионы металлов, такие как катионы щелочных или щелочноземельных металлов, так же как амины. Примеры подходящих катионов металлов включают, но не ограничиваются ими, катионы натрия (Na+), катионы калия (К+), катионы магния (Mg2+), катионы кальция (Са2+) и подобные. Примеры подходящих аминов включают, но не ограничиваются ими, N,N'-дибензилэтилендиамин, хлорпрокаин, холин, диэтаноламин, дициклогексиламин, этилендиамин, N-метилглюкамин и прокаин. Для обсуждения применимых аддитивных солей с кислотами и солей с основаниями см. S.M.Berge et al. "Pharmaceutical Salts", J. of Pharm. Sci., Vol. 66, p. 1-19 (1977); см. также Stahl and Wermuth, Handbook of Pharmaceutical Salts: Properties, Selection and Use (2002).
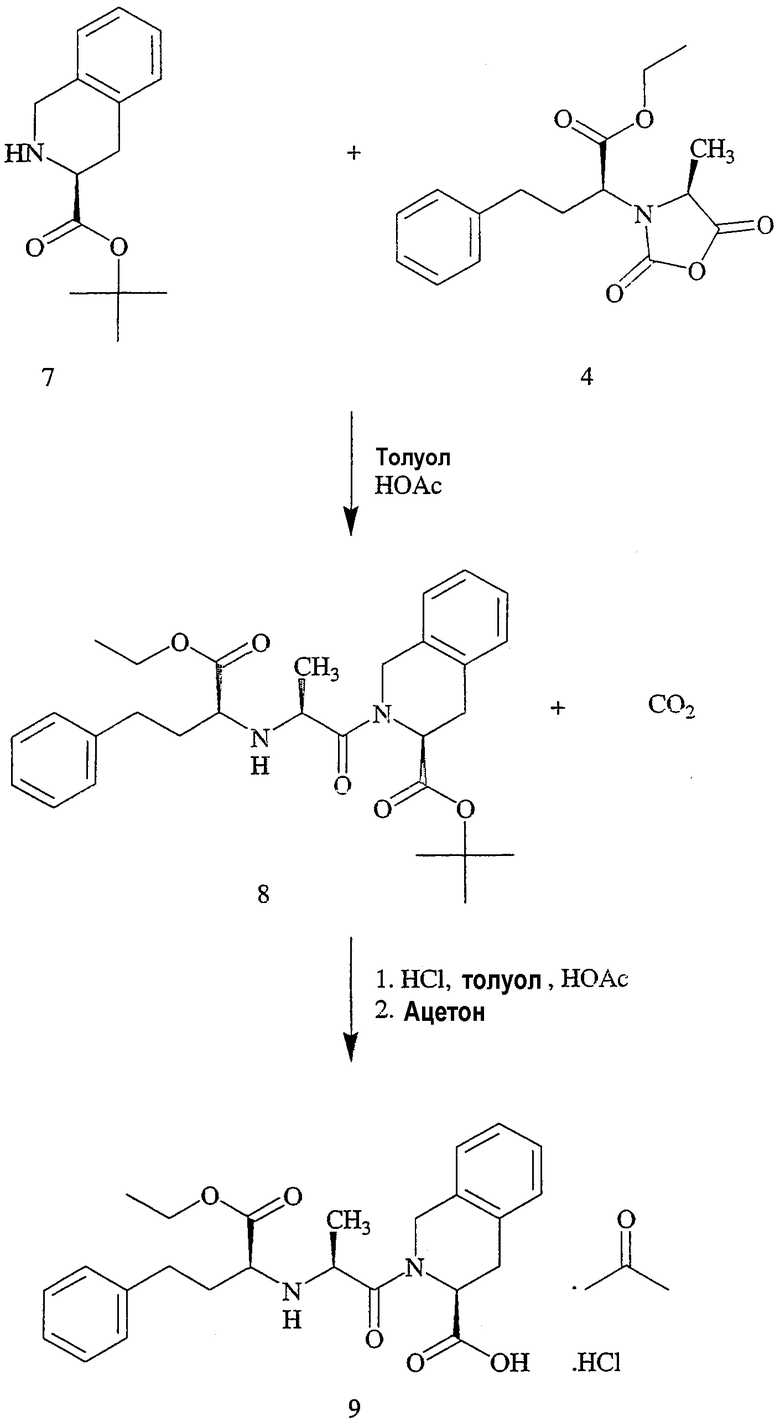
Схема I
Обычно можно получить фармацевтически приемлемую аддитивную соль с кислотой (или соль с основанием) контактированием свободного основания (или свободной кислоты) соединения с достаточным количеством желаемой кислоты (или основания) с образованием нетоксичной соли. Затем можно выделить соль фильтрованием, если она осаждается из раствора, или упариванием для выделения соли. Можно также регенерировать свободное основание (или свободную кислоту) контактированием основания с аддитивной солью с кислотой (или кислоты с солью с основанием). Хотя некоторые физические свойства свободного основания (или свободной кислоты) и его соответствующей аддитивной соли с кислотой (или соли с основанием) могут различаться (например, растворимость, кристаллическая структура, гигроскопичность и т.д.), свободные основания и аддитивные соли с кислотами соединения (или его свободная кислота и соль с основанием) в остальном эквивалентны целям данного изобретения.
Как указано выше и в примерах ниже, гидрохлорид хинаприла выделяют в виде сольвата с ацетоном (формула 9). Некоторые другие соединения данного изобретения могут существовать в виде нерастворимой формы или в форме сольвата, включая гидратированные формы. Фармацевтически приемлемые сольваты включают гидраты и сольваты, в которых растворитель для кристаллизации может быть изотопно замещенным, например D2O, d6-ацетон, d6-ДМСО и т.д. Обычно для целей данного описания сольватированные формы, включая гидратированные формы, эквивалентны несольватированным формам. Таким образом, если не указано специально, все ссылки на свободные основания, свободные кислоты или несольватированные формы соединения также включают соответствующие аддитивные соли с кислотами, соли с основаниями или сольватированные формы соединения.
Предложенные соединения также включают все фармацевтически приемлемые вариации изотопов, в которых по меньшей мере один атом заменен на атом, имеющий тот же атомный номер, но атомная масса которого отличается от атомной массы, обычно встречающейся в природе. Примерами изотопов, подходящих для включения в предложенные соединения, являются, но не ограничиваются ими, изотопы водорода, такие как 2Н и 3Н; изотопы углерода, такие как 13С и 14С; изотопы азота, такие как 15N; изотопы кислорода, такие как 17О и 18О; изотопы фосфора, такие как 31Р и 32Р; изотопы серы, такие как 35S; изотопы фтора, такие как 18F; и изотопы хлора, такие как 36Cl. Использование разновидностей изотопов (например, дейтерия, 2Н) может давать определенные терапевтические преимущества в результате большей метаболической стабильности, например, увеличивая in vivo период полувыведения или уменьшая потребности в дозах. Кроме того, некоторые изотопные разновидности предложенных соединений могут вводить радиоактивный изотоп (например, тритий, 3Н), который может быть использован при изучении лекарственного средства и/или распределения в субстратных тканях.
ПРИМЕРЫ
Следующие примеры приведены для иллюстрации, но не ограничения, и для представления специфических вариантов осуществления данного изобретения.
ПРИМЕР 1. Трет-бутиловый эфир THIQ
Гидроксид натрия (5,9 кг, 50%-ный водный раствор по массе), толуол (56 л) и воду (28 л) добавляли в стальной, покрытый изнутри стеклом (остеклованный) перегонный куб, содержащий соль PTSA c трет-бутиловым эфиром THIQ (30 кг) и воду (28 л). Полученную смесь перемешивали при КТ в течение примерно 10 мин для растворения твердых веществ. Смесь оставляли для разделения водного и органического слоев. К водному слою для поддержания значения рН примерно от 8 до 9, включительно, добавляли аликвоты HCl (37%-ный водный раствор по массе) или NaOH (50%-ный водный раствор по массе). После последнего добавления HCl или NaOH смесь перемешивали еще 30 мин и водный и органический слои оставляли отстаиваться в течение 15 мин. Нижний водный слой отделяли, а оставшийся органический слой перегоняли в вакууме примерно при 5 мм ртутного столба до объема органической смеси примерно 14 л. Полученный раствор трет-бутилового эфира THIQ охлаждали ниже КТ и помещали в остеклованный переходный сосуд. Внутренность перегонного куба споласкивали толуолом (2 л) для удаления остатков трет-бутилового эфира THIQ и помещали в переходный сосуд.
ПРИМЕР 2. Трет-бутиловый эфир хинаприла
Трет-бутиловый эфир из примера 1 при перемешивании добавляли за период свыше примерно пяти минут в остеклованный перегонный куб, содержащий этиловый эфир (2S,4S)-2-(4-метил-2,5-диоксооксазолидин-3-ил)-4-фенилмасляной кислоты (23,5 кг), толуол (12 л) и НОАс (0,09 кг). Внутренность переходного сосуда споласкивали толуолом (7 л) для удаления остатков трет-бутилового эфира THIQ и помещали в перегонный куб. Содержимое перегонного куба перемешивали в течение по меньшей мере 30 мин при температуре примерно от 30 до 35°C для обеспечения практически полного превращения (≥99,9%) трет-бутилового эфира THIQ в трет-бутиловый эфир хинаприла. Затем реакционную смесь охлаждали до температуры примерно от 15 до 25°C. Во время превращения трет-бутилового эфира THIQ в трет-бутиловый эфир хинаприла выделялся CO2, который отводили в атмосферу.
ПРИМЕР 3. Раствор хинаприла.HCl
Уксусную кислоту (10,5 кг) добавляли к реакционной смеси примера 2 с трет-бутиловым эфиром хинаприла, которая была охлаждена до температуры примерно от -5 до 5°C. После добавления НОАс к реакционной смеси при перемешивании добавляли безводный хлористый водород (8,1 кг) со скоростью, которая поддерживала давление в головной части перегонного куба менее 5 фунтов/кв. дюйм. Во время добавления HCl реакционную смесь охлаждали, чтобы поддерживать температуру ниже или равной примерно 20°C. Изобутилен, который образовывался во время реакции удаления защитной группы, отводили в скруббер с каустической содой всякий раз, когда давление в головной части перегонного куба достигало примерно 10 фунтов/кв. дюйм. После завершения добавления HCl реакционную смесь перемешивали при температуре примерно от 20 до 25°C до тех пор, пока практически весь (≥99,5%) трет-бутиловый эфир хинаприла не превратился в хинаприл.HCl.
ПРИМЕР 4. Сольват хинаприла.HCl с ацетоном
После добавления ацетона (75 л) к раствору хинаприла.HCl из примера 3 головную часть перегонного куба откачивали для удаления избытка HCl. Затем реакционную смесь охлаждали до температуры примерно от 10 до 20°C для стимулирования кристаллизации сольвата хинаприла.HCl с ацетоном. После начала кристаллизации содержимое перегонного куба перемешивали при температуре примерно от 15 до 25°C в течение по меньшей мере 8 ч, а затем при температуре примерно от -5 до 5°C в течение по меньшей мере 2 ч. Содержимое перегонного куба переносили в центрифугу для выделения кристаллического сольвата хинаприла.HCl с ацетоном. Для выделения остатков хинаприла.HCl перегонный куб загружали ацетоном (20 л) и охлаждали до температуры примерно от 0 до 10°C. Полученную ацетоновую промывную жидкость переносили в центрифугу для промывания кристаллов. Спектр ядерного магнитного резонанса 13С (ДМСО-d6): δ 13,65, 14,48, 29,82, 30,43, 30,51 (ацетон), 31,06, 43,36, 44,35, 51,77, 52,44, 52,96, 53,73, 57,14, 61,83, 126,08, 126,54, 127,95, 128,23, 128,29, 131,91, 132,24, 132,36, 140,09, 168,20, 171,11, 171,24, 208,16 (ацетон) м.д.
ПРИМЕР 5. Хинаприл.HCl (аморфный)
Ацетонитрил, предварительно нагретый до температуры примерно от 75 до 82°C, добавляли в остеклованный сосуд, содержащий сольват хинаприла.HCl с ацетоном из примера 4. Количество добавленного ацетонитрила примерно в 3,5 раза превышало массу сольвата хинаприла.HCl с ацетоном и было достаточным для полного растворения твердого вещества. Содержимое сосуда перемешивали и нагревали до температуры примерно от 75 до 82°С в течение менее чем 10 мин и полученный раствор через фильтр переносили в остеклованный перегонный куб. Содержимое перегонного куба перемешивали при температуре примерно от 0 до 5°C в течение по меньшей мере 8 ч, чтобы закристаллизовать сольват хинаприла.HCl с ацетонитрилом. Содержимое перегонного куба переносили в центрифугу, где сольват хинаприла.HCl с ацетонитрилом собирали в 1-3 микронной полиэтиленовой камере центрифуги. Для выделения остатка сольвата хинаприла.HCl с ацетонитрилом перегонный куб загружали ацетонитрилом (10 кг) и охлаждали до температуры примерно 5°C или ниже. Полученную ацетонитрильную промывную жидкость переносили в центрифугу для промывки твердых веществ, которые затем сушили в вакууме примерно при 5 мм ртутного столба и при температуре примерно от 50 до 55°C до тех пор, пока уровни ацетонитрила и ацетона в твердом веществе не достигли менее чем 0,041 и 0,25 мас.% соответственно. Во время процесса сушки кристаллический сольват хинаприла.HCl с ацетонитрилом превращался в аморфный хинаприл.HCl. Общий выход в расчете на количество соли PTSA с трет-бутиловым эфиром THIQ составлял примерно 90%. Спектр ядерного магнитного резонанса 13С (ДМСО-d6): δ 13,79, 14,59, 29,92, 30,37, 30,53, 43,47, 44,41, 51,84, 52,52, 53,02, 53,81, 57,18, 61,93, 126,21, 126,67, 127,08, 128,20, 128,37, 131,50, 132,06, 132,47, 140,23, 168,41, 171,31, 171,43 м.д.
Следует понимать, что приведенное выше описание является иллюстративным, а не ограничивающим. Специалистам в данной области техники после прочтения вышекузанного описания могут быть очевидны многие варианты осуществления. Поэтому область данного изобретения следует определять не со ссылкой на вышеуказанное описание, но со ссылкой на приложенную формулу изобретения вместе с полным объемом эквивалентов, соответствующих указанной формуле изобретения. Раскрытие всех статей, ссылок, включая патенты, патентные описания и публикации, введены в качестве ссылок во всей их полноте и для всех целей.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЛЬФА-2-ДЕЛЬТА ЛИГАНД ДЛЯ ЛЕЧЕНИЯ СИМПТОМОВ НИЖНИХ МОЧЕВЫВОДЯЩИХ ПУТЕЙ | 2003 |
|
RU2331438C2 |
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ И КОМПОЗИЦИИ | 2019 |
|
RU2813780C2 |
| СПОСОБЫ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ В ПОЛУЧЕНИИ C5aR АНТАГОНИСТОВ | 2015 |
|
RU2712233C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕНЕЛИГЛИПТИНА | 2013 |
|
RU2654069C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АЗОТИСТОГО ИПРИТА | 2016 |
|
RU2715233C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ ПРОСТОГО АМИНОЦИКЛОГЕКСИЛОВОГО ЭФИРА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2478617C2 |
| ПРОИЗВОДНЫЕ β АМИНО α ГИДРОКСИКАРБОНОВЫХ КИСЛОТ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ ИЛИ ЭФИРОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2120447C1 |
| СОЕДИНЕНИЯ ПРОСТОГО АМИНОЦИКЛОГЕКСИЛОВОГО ЭФИРА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2003 |
|
RU2330017C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, ВКЛЮЧАЯ ТРАНС-7-ОКСО-6-(СУЛЬФОКСИ)-1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАН-2-КАРБОКСАМИД И ЕГО СОЛИ | 2012 |
|
RU2769076C2 |
| ИНГИБИРОВАНИЕ ЦИКЛИЧЕСКОГО AMP-ЧУВСТВИТЕЛЬНОГО ЭЛЕМЕНТ-СВЯЗЫВАЮЩЕГО БЕЛКА (CREB) | 2020 |
|
RU2831142C2 |
Изобретение относится к способу получения хинаприла, его фармацевтически приемлемых солей, включая гидрохлорид хинаприла. Способ включает взаимодействие этилового эфира (2S,4S)-2-(4-метил-2,5-диоксооксазолидин-3-ил)-4-фенилмасляной кислоты с трет-бутиловым эфиром (3S)-1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты с получением трет-бутилового эфира хинаприла, который затем взаимодействует с кислотой с получением хинаприла или аддитивной соли хинаприла с кислотой. Технический результат: способ приводит к более высокому выходу хинаприла, что приводит к заметной экономии, а также отсутствие гидрогенеза, исключая при этом трудности, связанные с обращением с водородом. 5 з.п. ф-лы, 1 табл.
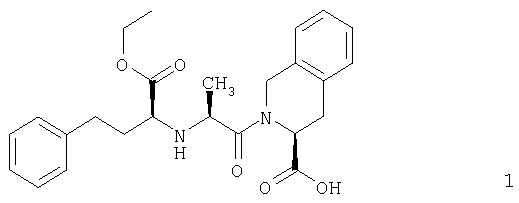
или его фармацевтически приемлемой соли, который включает:
взаимодействие соединения формулы 4
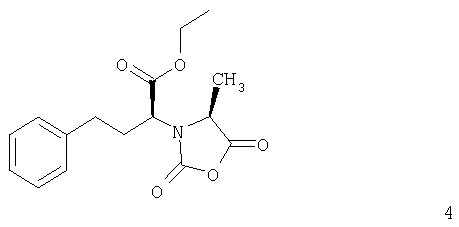
с соединением формулы 7
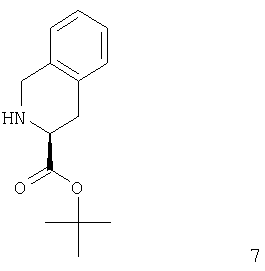
с получением соединения формулы 8
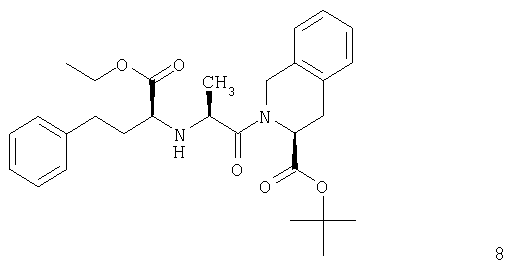
и контактирование соединения формулы 8 с кислотой с получением соединения формулы 1 или его фармацевтически приемлемой соли.
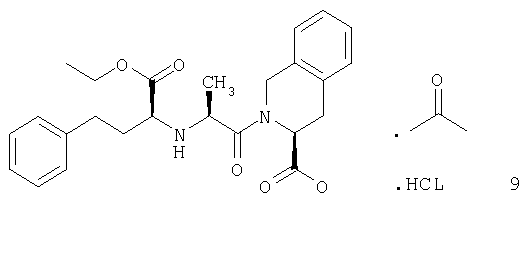
с последующей перекристаллизацией соединения формулы 9 из полярного апротонного растворителя с получением сольвата и сушку сольвата с получением аморфной формы соединения формулы 6.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Устройство для механической дойки | 1934 |
|
SU49605A1 |
| Способ получения амидных производных хинолина или их солей присоединения кислоты | 1987 |
|
SU1470183A3 |
| Способ получения производных 6,7диметокси-1,2,3,4-тетрагидро-1-изохинолин-ацетамида или их солей | 1977 |
|
SU691087A3 |
| Способ получения фенилэтиламинов или их солей | 1978 |
|
SU700061A3 |
Авторы
Даты
2007-04-27—Публикация
2004-03-19—Подача