Изобретение относится к микробиологии, касается способа оценки антагонистической активности бактерий и может быть использовано для оценки антагонистической активности молочнокислых бактерий или бактерий кишечной группы к патогенным микобактериям.
Известны различные способы оценки антагонистической активности микробов с использованием плотных однослойных, двух- и трехслойных питательных сред. На однослойные различные по составу питательные среды культуры засевают в лунки перпендикулярными штрихами или перекрывающимися каплями или на одной половине с последующим подсевом индикаторных микробов штрихами на другой половине [1]. Двух- и трехслойные питательные среды были использованы для изучения, бактериоциногенности [2], антагонистической активности лактобацилл к грибам [3], эшерихиям [4], протеям, стафилококкам, псевдомонадам [5], для оценки действия бифидобактерий на рост гарднерелл, энтеробактерий, стафилококков, энтерококков и псевдомонад [6], а также способности Bacillus spp.и Hafhia spp. подавлять рост микрококков, стафилококков и эшерихий [7]. Антагонистическую активность оценивают сравнением зоны задержки роста вокруг колоний антагониста или от участка нижнего слоя агара, содержащего культуру антагониста, засеянную штрихообразно [5], по «коэффициенту ингибирования» (отношение величины зоны задержки роста индикаторной культуры к диаметру колоний антагониста) [7]. Для оценки антагонистической активности Lactobacillus spp. определяют минимальное количество эшерихий (КОЕ/мл), способных вырасти на верхнем слое среды, если в нижнем слое в течение 24 часов росли лактобациллы, внесенные в концентрации 91 g КОЕ/мл [8] или контролируют концентрации лактобацилл в нижнем слое агара с помощью серийных разведений культур при одной и той же засевной дозе для индикаторных микробов [9].
Цель изобретения - способ оценки антагонистической активности молочнокислых бактерий или бактерий кишечной группы к патогенным микобактериям.
Поставленная цель достигается способом двухслойной среды, второй слой которой представляет собой солевой агар, содержащий солевой состав среды Sauton, водный раствор желтка куриного яйца (1:1), гумивит и агар при следующем соотношении компонентов, г:
а антагонистическую активность оценивают по количеству КОЕ (колониеобразующих единиц), ингибирующих рост 1-5×103 КОЕ индикаторного штамма на 1 мл суспензии.
Гумивит - щелочной гидролизат низинных сортов торфа (выпускается ООО Агропром), представляет собой высокодисперсный золь натриевых солей комплекса гумусных кислот - гуминовых, гуматомелановых и фульвокислот [10]. Раствор солей гуминовых кислот состоит из длинных фрагментарных цепочек с различными функциональными группами, важнейшими из которых являются карбоксильные (СООН) и фенольные (ОН), способные образовывать хелатные комплексы с микроэлементами, что обеспечивает их высокую обменную емкость и транспорт в клетку микроорганизмов [11, 12]. Гумивит - жидкость от темно-коричневого до черного цвета со специфическим сладковатым запахом.
Способ осуществляется следующим образом.
Нижний слой среды готовят из мясопептонного агара (МПА). В стерильные чашки Петри заливают расплавленный агар по 10 мл. На поверхность нижнего слоя засевают штаммы молочнокислых бактерий или бактерий кишечной группы. Чашки Петри с засеянными штаммами помещают в термостат и выдерживают при температуре 37°С в течение 72 часов. Затем на поверхность нижнего слоя наливают 10 мл расплавленного солевого агара (температура 65-70°С) и оставляют при комнатной температуре на 18-20 часов, после чего на поверхность верхнего слоя засевают культуру индикаторного штамма микобактерий. Антагонистическую активность оценивают по количеству КОЕ антагониста, ингибирующих рост 1-5×103 КОЕ индикаторного штамма в 1 мл суспензии. Контролем служат чашки с двухслойной средой, в нижний слой которой молочнокислые бактерии или бактерии кишечной группы не засевают.
Для приготовления солевого агара в химически чистую стерильную колбу емкостью 2,0 л наливают 300,0 мл дистиллированной воды, прогревают на водяной бане до 75-85°С. В воде растворяют последовательно 2,0 г лимонной кислоты, 4,0 г L-аспарагина, 0,5 г сернокислого магния, 0,5 г двузамещенного фосфорнокислого калия, 0,05 г лимоннокислого аммиачного железа, 40,0 г глицерина, 90,0 мл гумивита и 30,0 г агара. Каждый компонент добавляют после полного растворения предыдущего. После внесения всех компонентов общий объем доводят до 750,0 мл стерильной дистиллированной водой.
Устанавливают рН 7,1-7,2 добавлением 1н. NaOH или 1н. HCl. Раствор автоклавируют в течение 30 минут при 1 атм. Свежие куриные яйца хорошо промывают в проточной воде, протирают 96° этиловым спиртом, разбивают в стерильных условиях и отделяют белок от желтка. В стерильной колбе смешивают желток и дистиллированную воду в соотношении 1:1 и 250,0 мл полученного раствора добавляют в расплавленную агаровую среду и перемешивают.
Сущность способа поясняется примерами.
Пример 1. Определение антагонистической активности молочнокислых бактерий к патогенным микобактериям.
Использовали штаммы Lactobacillus plantarum 8P-A3 (Лактобактерин «ИмБио», Россия), M.tuberculosis (штамм H37Ra), M.bovis (штамм Vallee), M.avium (штамм ГИСК), M.smegmatis (штамм 7) и штамм M.tuberculosis, выделенный от больного туберкулезом легких. Лактобациллы культивировали на МПА, микобактерии - на среде Левенштейна-Йенсена. Антагонистическую активность лактобацилл к патогенным микобактериям определяли методом двухслойной среды. Нижний слой готовили из МПА. В стерильные чашки Петри наливали расплавленный МПА по 10 мл. На поверхность расплавленного остывшего МПА вносили 50 мкл суспензии лактобацилл, содержавшей 1-5×103-1-5×108 КОЕ лактобацилл в 1 мл суспензии. Чашки Петри с засеянными лактобациллами помещали в термостат и выдерживали при температуре 37°С в течение 72 часов. Затем на поверхность нижнего слоя наливали 10 мл расплавленного солевого агара (температура 65-70°С), содержавшего солевой состав среды Sauton, водный раствор желтка куриного яйца (1:1), гумивит и агар при следующем соотношении компонентов: L-аспарагин - 4,0 г; двузамещенный фосфорнокислый калий - 0,5 г; сернокислый магний - 0,5 г; лимонная кислота - 2,0 г; лимоннокислое аммиачное железо - 0,05 г; глицерин - 40,0 г; агар - 30,0 г; гумивит - 95,0 мл; водный раствор желтка куриного яйца (1:1) - 250,0 мл; дистиллированная вода - до 1000,0 мл. Приготовленный таким образом двухслойный агар оставляли при комнатной температуре на 18-20 часов. Далее на поверхность верхнего слоя засевали 50 мкл суспензии культуры индикаторного штамма, содержавшей 1-5×103 KOE в 1 мл суспензии. Засеянные чашки Петри помещали в термостат и выдерживали при температуре 37°С в течение 7 суток, после чего их заклеивали скотчем. Контролем служили чашки с двухслойной средой, в нижний слой которой лактобациллы не засевали. Результаты представлены в таблице 1.
Антагонистическая активность лактобацилл к патогенным микобактериям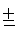
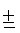 - слабый рост (1-4 КОЕ); ± - средний рост (5-9 КОЕ); + - сильный рост (10-50 КОЕ)
- слабый рост (1-4 КОЕ); ± - средний рост (5-9 КОЕ); + - сильный рост (10-50 КОЕ)
Как видно из таблицы 1, минимальную антагонистическую активность лактобациллы проявляли в отношении М. smegmatis. Росту М. bovis и M.avium лактобациллы препятствовали в концентрации 1-5×106 КОЕ в 1 мл суспензии. Для подавления роста M.tuberculosis концентрация лактобацилл составила 1-5×107 KOE в 1 мл суспензии.
Пример 2. Определение антагонистической активности бактерий кишечной группы к патогенным микобактериям.
Использовали штаммы Escherichia coli, Enterobacter faecalis (Окарин «ИмБио», Россия), M.tuberculosis (штамм Н37Ra), M.bovis (штамм Vallee), M.avium (штамм ГИСК), M.smegmatis (штамм 7) и штамм M.tuberculosis, выделенный от больного туберкулезом легких. Бактерии кишечной группы культивировали на МПА, микобактерии - на среде Левенштейна-Йенсена. Антагонистическую активность бактерий кишечной группы к патогенным микобактериям определяли методом двухслойной среды. Двухслойную среду готовили и оценку антагонистической активности проводили, как в примере 1. Контролем служили чашки с двухслойной средой, в нижний слой которой бактерии кишечной группы не засевали. Результаты представлены в таблице 2.
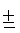 - слабый рост (1-4 КОЕ); ± - средний рост (5-9 КОЕ); + - сильный рост (10-50 КОЕ)
- слабый рост (1-4 КОЕ); ± - средний рост (5-9 КОЕ); + - сильный рост (10-50 КОЕ)
Как видно из таблицы 2, минимальную антагонистическую активность бактерии кишечной группы проявляли в отношении М. smegmatis. Росту М. bovis, M.avium и M.tuberculosis (клинический штамм) бактерии кишечной группы препятствовали в концентрации 1-5×105 КОЕ в 1 мл суспензии. Для подавления роста M.tuberculosis (штамм Vallee) концентрация бактерий кишечной группы составила 1-5×106 KOE в 1 мл суспензии.
Проведенные исследования подтверждают, что предложенный способ позволяет оценивать антагонистическую активность молочнокислых бактерий или бактерий кишечной группы к патогенным микобактериям с использованием двухслойной среды. Из доступных источников информации не известны способы изучения взаимодействия молочнокислых бактерий или бактерий кишечной группы с микобактериями. Особенности биологии микобактерий затрудняют их одновременное выращивание с другими микроорганизмами. Неспособность микобактерий синтезировать разнообразные химические вещества и витаминоподобные факторы роста самостоятельно, что снижает обмен веществ клеток микроорганизмов, следствием чего является очень медленный рост, обусловливает их потребность в полноценных, богатых белком, углеродом, минеральными веществами и стимуляторами роста питательных средах, которая реализуется использованием питательных яичных, картофельных, кровяных сред. Известные плотные среды для культивирования микобактерий не могут быть использованы в составе многослойных сред, создающих условия для оценки взаимодействия микробов с различными типами метаболизма, поскольку технология их приготовления предусматривает их свертывание. Таким образом, совокупность отличительных признаков соответствует критериям «новизна» и «изобретательский уровень».
Источники информации
1. Mardth P.A., Soltesz L.V. In vitro interactions between lactobacilli and other microorganisms occurring in the vaginal flora. Scand. J, Infect. Dis. Suppl. l983, (1.40) 3: 47-51.
2. Кудлай Д.Г., Уртаева З.А., Смеянов В.В. и др. Изучение антагонистической активности бифидобактерий in vitro и in vivo с использованием гнотобиотической техники. Журн. микробиол. 1999, 5: 72-75.
3. Magnusson J., Schnurer J. Lactobacillus coryniformis subsp. Coryniformis strain S13 produces a broad-spectrum proteinaceous antifungal compound. Appl. Environ. Microbiol. 2001, 1 (67): 1-5.
4. McGroarty J.A., Reid G. Detection of a lactobacillus substance that inhibits Escherichia coli. Cand. J. Microbiol. 1988, (134): 974-978.
5. Osset J., Bartolome R.M., Garsia E.A., Assessement of the capacity of Lactobacillus to inhibit the growth of uropathogens and block their adhesion to vaginal epithelial cells. J. Infect. Dis. 2001, 183 (3): 485-491.
6. Коршунов В.М., Уртаева З.А., Смеянов В.В. и др. Изучение антагонистической активности бифидобактерий in vitro и in vivo с использованием гнотобиологической технологии. Журн. микробиол. 1999, 5: 72-75.
7. Альтшуллер М.Л., Блинкова Л.П., Батуро А.П. Обнаружение штаммов-антагонистов у представителей родов Bacillus и Hafhia. Журн. микробиол. 1993, 6: 22-23.
8. Reid G., Cook R.I., Bruce A.W. Examination of strains of Lactobacillus for properties that may influence bacterial interference in the urinary tract. J. Urol. 1987, 138 (2): 330-335.
9. Ермоленко Е.И., Исаков В.А., Ждан-Пушкина С.Х., Тец В.В. Количественная оценка антагонистической активности лактобацилл. ЖМИЭ, 2004, 5: 94-98.
10. Гришин Г.И., Слинина К.Н. Дар природы - гумивит // Практик. - 2004. - №3-4. - С.80-82.
11. Левинский Б.В. Все о гуматах. - Иркутск: ИП Макаров С.Е., 1999, - 198 с.
12. Сорокина Н.Ф. Физиология активности продуктов окисления торфа // Новые процессы и продукты переработки торфа. - Минск: Наука, 1982. - С.109-115.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТИ ПРОБИОТИКОВ НА ОСНОВЕ ЛИОФИЛИЗИРОВАННОЙ БИОМАССЫ АЭРОБНЫХ БАКТЕРИЙ ПО ОТНОШЕНИЮ К ПАТОГЕННЫМ МИКОБАКТЕРИЯМ | 2007 |
|
RU2351655C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТИ БИФИДОБАКТЕРИЙ ПО ОТНОШЕНИЮ К МИКОБАКТЕРИЯМ И РОДОКОККАМ | 2007 |
|
RU2345140C1 |
| СПОСОБ ОЦЕНКИ АНТАГОНИСТИЧЕСКИХ СВОЙСТВ БАКТЕРИЙ КИШЕЧНОЙ ГРУППЫ К ПАТОГЕННЫМ МИКОБАКТЕРИЯМ | 2006 |
|
RU2333248C1 |
| СПОСОБ ОЦЕНКИ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТИ ПРОБИОТИКОВ НА ОСНОВЕ ЛИОФИЛИЗИРОВАННОЙ БИОМАССЫ АНАЭРОБНЫХ БАКТЕРИЙ ПО ОТНОШЕНИЮ К ПАТОГЕННЫМ МИКОБАКТЕРИЯМ | 2007 |
|
RU2350648C1 |
| СПОСОБ ВЫЯВЛЕНИЯ АНТАГОНИСТИЧЕСКИХ СВОЙСТВ ПО ОТНОШЕНИЮ К ПАТОГЕННЫМ МИКОБАКТЕРИЯМ У МОЛОЧНОКИСЛЫХ БАКТЕРИЙ И БАКТЕРИЙ ГРУППЫ КИШЕЧНОЙ ПАЛОЧКИ | 2006 |
|
RU2320724C1 |
| ПЛОТНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ | 2006 |
|
RU2320716C2 |
| ПЛОТНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ ПАТОГЕННЫХ МИКОБАКТЕРИЙ И НОКАРДИОФОРМНЫХ АКТИНОМИЦЕТОВ | 2008 |
|
RU2375446C1 |
| ШТАММ Lactobacillus fermentum Z, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРОИЗВОДСТВА ПРОБИОТИЧЕСКИХ МОЛОЧНОКИСЛЫХ ПРОДУКТОВ | 2008 |
|
RU2412239C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ИЗ БИОЛОГИЧЕСКОГО МАТЕРИАЛА И КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ | 2006 |
|
RU2315812C1 |
| Способ определения чувствительности кампилобактерий к пробиотикам и аутопробиотикам | 2022 |
|
RU2816763C1 |
Изобретение относится к биотехнологии и может быть использовано для оценки антагонистической активности молочнокислых бактерий и бактерий кишечной группы к патогенным микобактериям. Способ предусматривает засев молочнокислых бактерий или бактерий кишечной группы на нижний слой питательной среды, представляющий собой мясопептонный агар, нанесение верхнего слоя питательной среды, содержащей калий фосфорнокислый двузамещенный, сернокислый магний, L-аспарагин, глицерин, лимонную кислоту, лимоннокислое аммиачное железо, гумивит, агар, водный раствор желтка куриного яйца и дистиллированную воду на нижний слой, засев верхнего слоя питательной среды культурой индикаторного штамма микобактерий и определение антагонистической активности, которую оценивают по количеству колониеобразующих единиц (КОЕ), ингибирующих рост 1-5×103 КОЕ индикаторного штамма микобактерий в 1 мл суспензии. Изобретение позволяет определять антагонистическую активность молочнокислых бактерий и бактерий кишечной группы к патогенным микобактериям. 2 табл.
Способ оценки антагонистической активности молочнокислых бактерий и бактерий кишечной группы к патогенным микобактериям, предусматривающий засев молочнокислых бактерий или бактерий кишечной группы на нижний слой питательной среды, представляющий собой мясопептонный агар, нанесение верхнего слоя питательной среды, содержащей калий фосфорнокислый двузамещенный, сернокислый магний, L-аспарагин, глицерин, лимонную кислоту, лимоннокислое аммиачное железо, гумивит, агар, водный раствор желтка куриного яйца и дистиллированную воду на нижний слой при следующем содержании компонентов, г:
засев верхнего слоя питательной среды культурой индикаторного штамма микобактерий и определение антагонистической активности, которую оценивают по количеству колониеобразующих единиц (КОЕ), ингибирующих рост 1-5×103 КОЕ индикаторного штамма микобактерий в 1 мл суспензии.
| ЕРМОЛЕНКО Е.И., ИСАКОВ В.А | |||
| и др., Количественная оценка антагонистической активности лактобацилл | |||
| Журнал микробиологии и эпидемиологии | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| КОРШУНОВ В.М | |||
| и др | |||
| Изучение антагонистической активности бифидобактерий in vitro и vivo с использованием гнотобиологической технологии, Микробиология, 1999, с.72-75 | |||
| RIED G., COOK R.I., BRUCE | |||
Авторы
Даты
2008-02-20—Публикация
2006-06-27—Подача