Настоящее изобретение относится к способу концентрирования изомеров гликопиррония R,R- или S,S-конфигурации и их тиенильных аналогов с R,S- или S,R-конфигурацией.
Вещества, блокирующие мускариновые рецепторы, используют во всем мире в большом объеме в случае многочисленных заболеваний (Goodman and Gilman's. "The Pharmacological Basis of Therapeutics", 9 издание, McGraw Hill, 1996; Mutschler "Arzneimittelwirkungen", 8 издание, Wissenschaftliche Verlagsgesellschaft Stuttgart, 2001), как, например, для лечения хронических обструктивных заболеваний дыхательных путей, нарушений опорожнения мочевого пузыря, почечных и вызываемых желчным камнем колик, а также раздражений гладкой мускулатуры желудочно-кишечного тракта (в частности, в случае синдрома раздраженной толстой кишки).
Эти действия опосредуются пятью разными подтипами мускаринового рецептора. Отдельные стереоизомеры лиганда могут обладать различным сродством в отношении этих пяти подтипов рецептора и тем самым предпочтительно вызывают разные - желательные - действия по сравнению с другими - нежелательными - действиями. Селективные вещества нужно предпочитать неселективным биологически активным веществам из-за их более незначительных побочных действий, что в некоторых случаях может достигаться за счет использования отдельных чистых стереоизомеров.
Изомер гликопиррония с R,R-конфигурацией обладает особенно благоприятными фармакологическими свойствами (международная заявка WO-9821183). Его получение описано в международной заявке WO-9821183. Гликопирронийбромид, соответственно производимые от него соединения, содержат два стереогенных центра, откуда следует существование соответственно четырех стереоизомеров.
Объектом настоящего изобретения является способ получения гликопиррониевых солей 3R,2'R-конфигурации или родственных гликопирронийбромиду соединений с соответствующим пространственным расположением (например, в случае тиенила, по правилу Cahn, Ingold, Prelog, = 3R,2'S-расположение), отличающийся тем, что из энантиомерно чистой смеси диастереомеров из 3R,2'R- и 3R,2'S- или из 3R,2'R- и 3S,2'R-изомера (соответственно в случае тиенильных аналогов, из энантиомерно чистой смеси диастереомеров из 3R,2'S- и 3R,2'R- или из 3R,2'S- и 3S,2'S-изомера) за счет использования пригодного растворителя во время кватернизации и/или путем перекристаллизации четвертичных солей выделяют желательный стереоизомер.
Способ пригоден, в принципе, равным образом для получения антиподов (3S,2'S в случае фенильного соединения или 3S,2'R в случае тиенильного аналога), если используют антиподы (3S,2'S + 3S,2'R или 3S,2'S + 3R,2'S в случае фенильного соединения или 3S,2'R + 3S,2'S или 3S,2'R + 3R,2'R в случае тиенильного аналога).
Объектом настоящего изобретения соответственно этому является способ
а) выделения 3R,2'R-стереоизомера гликопирронийбромида или -иодида (формула (II), A = Br или I)
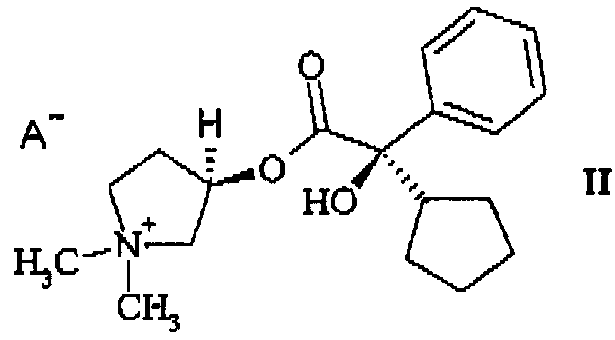
из смеси диастереомеров, состоящей из 3R,2'R- и 3R,2'S-изомера (формула (III))
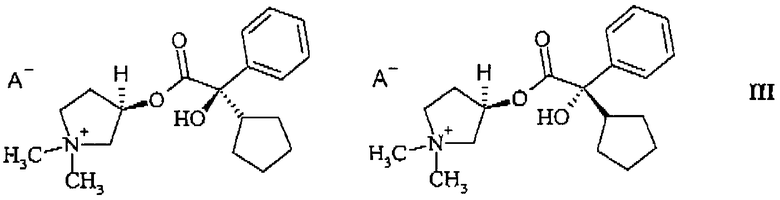
или из смеси диастереомеров, состоящей из 3R,2'R- и 3S,2'R-изомера (формула (IIIb))
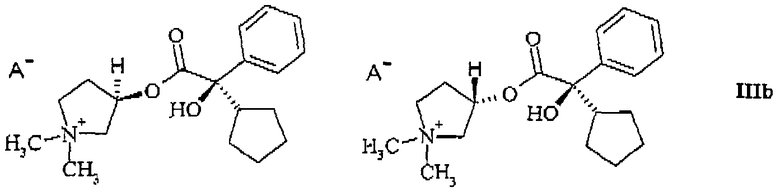
или
b) выделения 3S,2'S-изомера (формула (IV), A = Br или I)
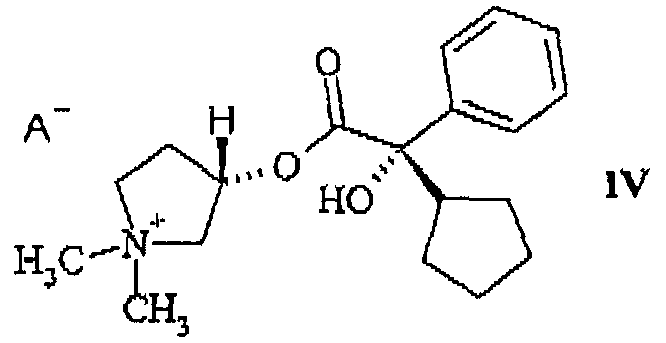
из смеси диастереомеров, состоящей из 3S,2'R- и 3S,2'S-изомера (формула (V))
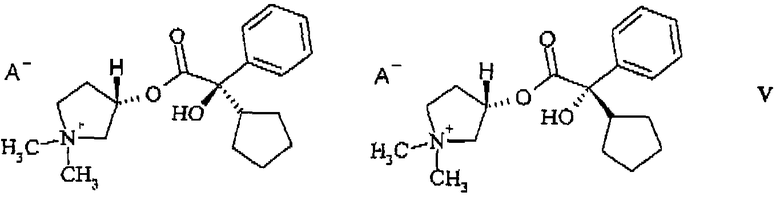
или из смеси диастереомеров, состоящей из 3R,2'S- и 3S,2'S-изомера (формула (Vb))
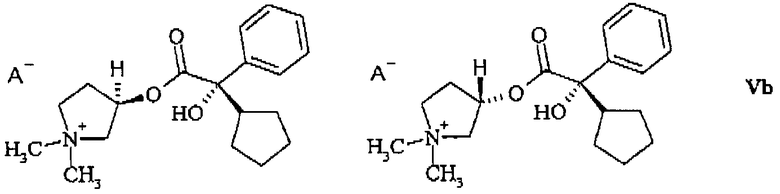
или
с) выделения 3R,2'S-изомера тиенильного аналога гликопиррония (формула (VI), A = Br или I)
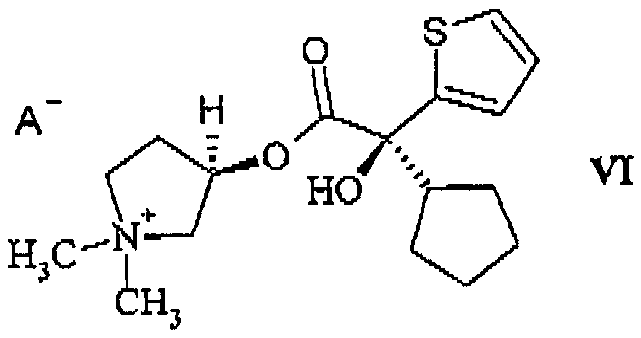
из смеси диастереомеров, состоящей из 3R,2'S- и 3R,2'R-изомера (формула (VII))
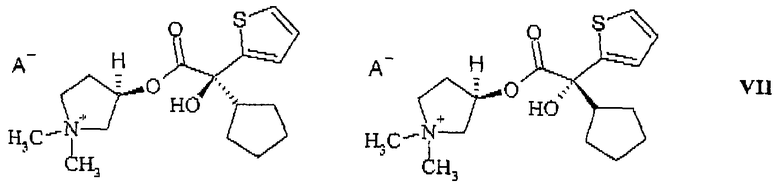
или из смеси диастереомеров, состоящей из 3R,2'S- и 3S,2'S-изомера (формула (VIIb))
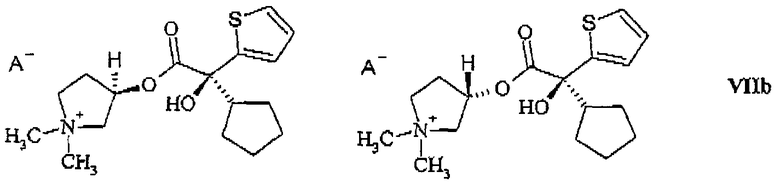
или
d) выделения 3S,2'R-изомера (формула (VIII), A = Br или I)
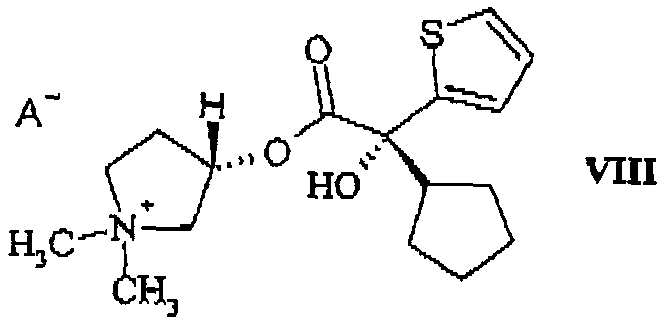
из смеси диастереомеров, состоящей из 3S,2'S- и 3S,2'R-изомера (формула (IX))
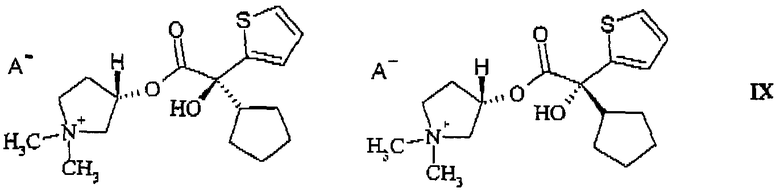
или из смеси диастереомеров, состоящей из 3S,2'R- и 3R,2'R-изомера (формула (IXb))
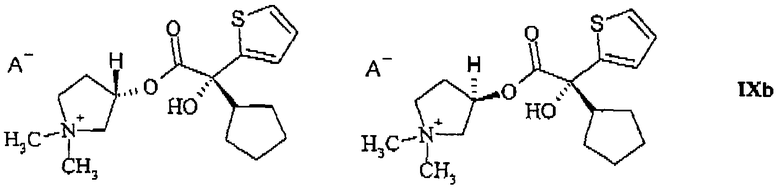
отличающийся тем, что
при кватернизации до получения вышеуказанных смесей диастереомеров используют пригодный растворитель для того, чтобы выделяемый, в каждом случае, стереоизомер получать концентрированным в виде осадка,
и/или
вышеописанные смеси диастереоизомеров четвертичных соединений перекристаллизовывают из пригодного растворителя или смеси растворителей и при этом получают концентрированным каждый желательный изомер.
В случае одного из вариантов осуществления изобретения в способе используют растворители или смеси растворителей с содержанием воды, что приводит к тому, что только желательный диастереомер выделяется в кристаллическом виде в то время, как другой диастереомер остается в растворе или выделяется в виде масла.
Если кватернизацию смесей диастереомеров исходных третичных оснований до указанных смесей диастереомеров аммониевых солей осуществляют в пригодном растворителе с достаточным содержанием воды, то получают желательные стереоизомеры концентрированными в виде осадка в то время, как другой диастереомер остается в растворе.
При осуществлении предлагаемого согласно изобретению способа для кватернизации можно использовать растворитель, в котором растворяется третичное основание, а также образующиеся четвертичные соли, и добавка другого растворителя вызывает кристаллизацию желательного изомера.
Согласно другому признаку предлагаемого согласно изобретению способа для кватернизации используют растворитель, в котором плохо растворяются оба диастереомера образующихся четвертичных солей, и добавка другого растворителя приводит к тому, что нежелательный изомер растворяется или выделяется в виде масла.
В качестве пригодных растворителей для кватернизации можно назвать, например, разветвленные и неразветвленные спирты с низкой молекулярной массой, как метанол, этанол, изопропанол, пропан-1-ол, трет-бутанол, изобутанол, н-бутанол, а также ацетон, бутанон, ацетонитрил и тому подобные, смотря по обстоятельствам, индивидуально или в виде смесей с другими растворителями.
На практике, в случае предлагаемого согласно изобретению способа, в качестве растворителя для кватернизации предпочтительно используют ацетон предпочтительно с содержанием воды примерно 0,5-2% (при концентрации основания в растворителе примерно 5-20%), еще более предпочтительно с содержанием воды примерно 1%.
Согласно следующему признаку способа согласно изобретению для перекристаллизации используют растворитель, в котором смесь диастереомеров хорошо растворяется, и добавляют второй, вызывающий кристаллизацию растворитель для проведения кристаллизации.
Предпочтительно для растворения используют метанол и/или этанол и кристаллизацию вызывают с помощью этилацетата и/или метил-трет-бутилового эфира.
Согласно следующему признаку предлагаемого в изобретении способа для перекристаллизации смесь диастереомеров растворяют в нагретом растворителе и кристаллизация осуществляется путем охлаждения.
Предпочтительно в случае предлагаемого согласно изобретению способа для перекристаллизации смесь диастереомеров растворяют в пропан-2-оле или этаноле при температуре кипения и кристаллизация осуществляется путем охлаждения до комнатной температуры или ниже.
Предпочтительно в случае предлагаемого согласно изобретению способа для перекристаллизации смесь изомеров растворяют при температуре кипения в пропан-2-оле, содержание воды в котором составляет примерно 0,2-3% (при концентрации четвертичной аммониевой соли в растворителе примерно 5-30%), еще более предпочтительно примерно 0,5%, и кристаллизация осуществляется путем охлаждения.
В качестве пригодных растворителей для перекристаллизации можно назвать, например, разветвленные или неразветвленные спирты с низкой молекулярной массой, как метанол, этанол, изопропанол, пропан-1-ол, трет-бутанол, изобутанол, н-бутанол, а также ацетон, бутанон, ацетонитрил и тому подобные, используемые соответственно индивидуально или в виде смесей с другими растворителями.
Согласно изобретению предлагаемый способ предпочтительно используют для концентрирования 3R,2'R-изомера гликопирронийбромида.
Как при кватернизации исходных третичных оснований до указанных смесей диастереомеров аммониевых солей, так и при перекристаллизации четвертичных солей путем дополнительной промывки осадков желательного стереоизомера с его поверхности удаляют прилипающий нежелательный изомер. Эту дополнительную промывку можно также еще осуществлять после выделения сырого продукта, при этом сырой продукт настаивают в растворителе, в котором он только частично растворяется (предпочтительно ацетон с содержанием воды 1%), и затем очищенный от нежелательного диастереомера осадок отсасывают на нутч-фильтре.
Предлагаемый в изобретении способ можно с успехом использовать также в комбинации с другими способами для повышения чистоты стереоизомеров. Если, например, используемые для кватернизации основания или четвертичные аммониевые соли уже являются диастереомерно концентрированными, то это концентрирование можно оптимизировать с помощью предлагаемого в изобретении способа.
С другой стороны, предлагаемый способ, в отношении предварительной очистки, может уже приводить к высокому избытку стереоизомера, который при применении последующего способа является предпочтительным для дальнейшего повышения чистоты стереоизомера.
Заявляемый способ пригоден для концентрирования изомера из образующейся при использовании энантиомерно чистого аминоспирта 3R-конфигурации и рацемической кислоты (или соответствующего сложного эфира или активированного производного кислоты) смеси 3R,2'R-/3R,2'S-диастереомеров третичного гликопирролята или при использовании аминоспирта 3S-конфигурации, образующейся смеси из 3S,2'R- и 3S,2'S-изомеров за счет использования пригодного растворителя во время кватернизации и/или путем перекристаллизации четвертичных аммониевых солей, в котором асимметрические центры аминоспиртового компонента и кислотного компонента имеют ту же самую абсолютную конфигурацию (следовательно, 3R,2'R и 3S,2'S; формула (Ia)). За счет повторения процедуры кристаллизации можно дальше повышать чистоту стереоизомеров.
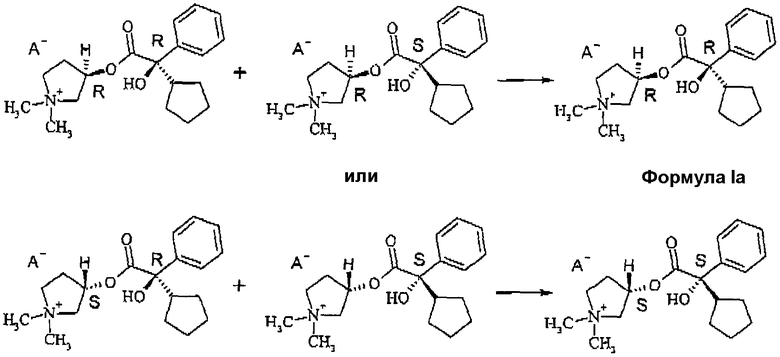
В случае 2-тиенильного аналога из смеси диастереомеров, состоящей из 3R,2'S- и 3R,2'R-изомера, соответственно из смеси диастереомеров, состоящей из 3S,2'R-/3S,2'S-изомера, на основании более высокого приоритета тиенильного остатка, получают стереоизомеры, которые имеют противоположное обозначение конфигурации (следовательно, 3R,2'S и 3S,2'R; формула (Ib)), однако, обладают тем же самым пространственным расположением, как в случае фенильного соединения.
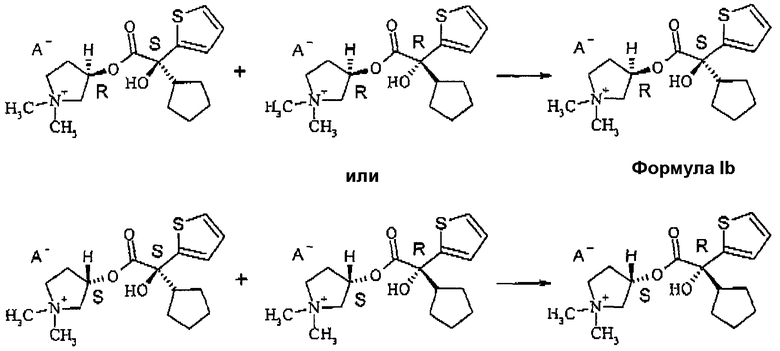
Альтернативно этому также можно исходить из энантиомерно чистого кислотного компонента (или соответствующего сложного эфира или активированного производного кислоты) и рацемического аминоспирта и из полученной в результате основной смеси диастереомеров путем использования пригодного растворителя во время кватернизации и/или путем перекристаллизации четвертичных солей можно выделять желательный стереоизомер.
В случае кислотного компонента с 2R-конфигурацией при этом из образующейся смеси диастереомеров, состоящей из 3R,2'R-/3S,2'R-изомера, третичного гликопирролята, соответственно в случае использования кислотного компонента с 2S-конфигурацией из образующейся смеси диастереомеров, состоящей из 3R,2'S- и 3S,2'S-изомера, за счет использования пригодного растворителя во время кватернизации и/или путем перекристаллизации четвертичных аммониевых солей получают изомер, в котором асимметрические центры аминоспиртового компонента и кислотного компонента имеют ту же самую абсолютную конфигурацию (следовательно, 3R,2'R или соответственно 3S,2'S; формула (Ic)).
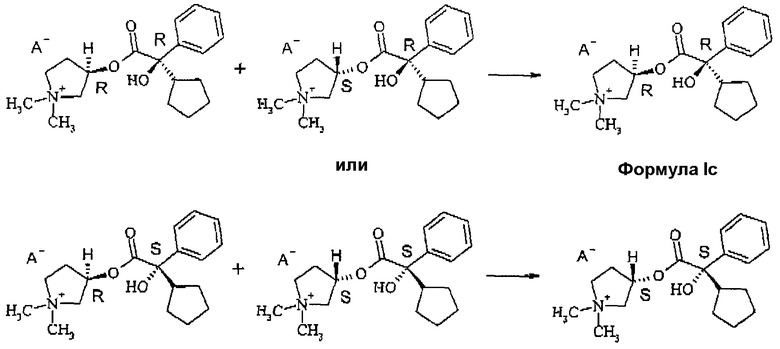
В случае 2-тиенильного аналога из смеси диастереомеров, состоящей из 3R,2'S- и 3S,2'S-изомера или из смеси диастереомеров, состоящей из 3R,2'R-/3S,2'R-изомера, на основании более высокого приоритета тиенильного остатка получают стереоизомеры, которые имеют противоположную конфигурацию (следовательно, 3R,2'S и 3S,2'R; формула (Id)), однако, обладают тем же самым пространственным расположением, как в случае фенильного соединения.
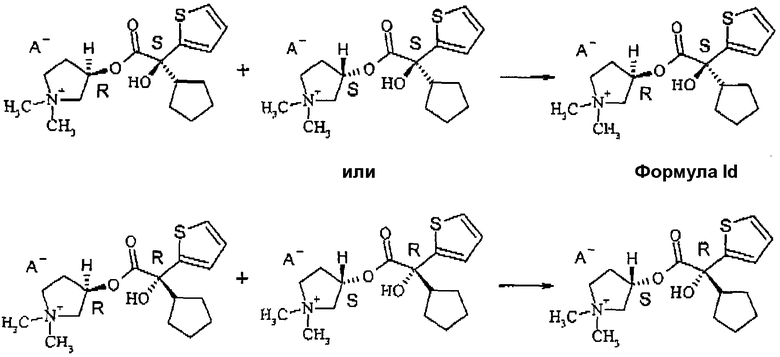
Если в случае гликопирронийбромида, напротив, перекристаллизовывают смесь всех четырех изомеров четвертичной аммониевой соли, то получают в виде твердого вещества смесь из 3R,2'S- и 3S,2'R-изомера, то есть в случае этого способа происходит потеря изомера с самыми предпочтительными фармакологическими свойствами.
Для выделения указанных стереоизомеров из смесей диастереомеров четвертичных аммониевых солей возможно использование различных способов кристаллизации.
В качестве растворителей для перекристаллизации, в общем, пригодны все растворители и смеси растворителей, в которых смесь диастереомеров, в случае необходимости, при нагревании растворяется, и за счет пригодных мер может быть вызвана кристаллизация, причем желательный изомер выделяется концентрированным в виде твердого вещества.
В качестве пригодных мер для инициирования кристаллизации из раствора смеси диастереомеров следует указать: охлаждение раствора; добавление других растворителей, в которых желательный изомер обладает меньшей растворимостью, чем в первоначальном растворителе; концентрирование объема растворителя; удаление одного компонента из смеси растворителей, в котором желательный изомер обладает более высокой растворимостью, чем в остающейся смеси растворителей.
Как установлено, нежелательный изомер обладает сильно гигроскопическим поведением, в то время как это нельзя наблюдать в случае желательного изомера. Согласно одному из вариантов осуществления заявляемого способа, в случае которого используют растворитель с достаточным содержанием воды или добавляют воду к безводному растворителю, эта характерная особенность приводит к тому, что выкристаллизовывается исключительно желательный диастереомер, в то время как другой диастереомер остается в растворе или образует отделяемое масло.
Предпочтительным является использование летучих растворителей, которые можно легко удалять из полученного твердого вещества.
Особенно предпочтительны растворители, из которых выкристаллизовывается в виде твердого вещества исключительно желательный стереоизомер.
Заявляемый способ при небольших технических расходах позволяет получать желательный стереоизомер очень высокой чистоты.
Расход исходных веществ из-за разделения изомеров на последней стадии реакции является относительно высоким по сравнению с другими возможными способами, при которых разделение изомеров осуществляют на более ранней стадии синтеза. Этот предполагаемый недостаток, однако, сверхкомпенсируется за счет простого осуществления заявляемого способа.
В особенности факт, что в случае этого способа желательный изомер по сравнению с нежелательным диастереомером проявляет резко повышенную тенденцию к кристаллизации, составляет особое преимущество этого способа и заслуживает особого внимания.
Энантиомерно чистый аминоспиртовой компонент можно получать способами, которые описаны в литературе (расщепление рацемата и асимметрический синтез: J. Med. Chem., 34, 1314-1328 (1991)). То же самое имеет значение также для кислотного компонента (расщепление рацемата: Bioorg. Med. Chem., 7, 2555-2567 (1999); асимметрический синтез: Bioorg. Med. Chem. Lett., 9, 2037-2038 (1999)). Следовательно, представлена осуществимость способа.
Принимая во внимание техническую применимость, предлагаемый согласно изобретению способ обладает отчетливыми преимуществами по сравнению с другими возможными способами получения указанного стереоизомера из соответствующей смеси диастереомеров. Так, в случае предлагаемого согласно изобретению способа нет необходимости ни в каких дополнительных, отчасти очень дорогостоящих и возможно вообще не доступных в гораздо больших количествах, хиральных вспомогательных веществах. Достаточно использования единственного энантиомерно чистого вещества, которое и без того является структурным элементом продукта. Вместе с тем получение чистого изомера является едва более дорогостоящим, чем получение смеси из всех четырех изомеров, или имеющейся в настоящее время в продаже смеси изомеров из 3R,2'S- и 3S,2'R-гликопирронийбромида. В указанном последним случае терапевтически самый рациональный изомер даже не содержится в продукте.
Кроме того, в предлагаемом согласно изобретению способе избегают дополнительных рабочих стадий, которые необходимы при расщеплениях рацематов, как кристаллизации с хиральными основаниями или кислотами, многократные перекристаллизации образующихся солей, высвобождения из указанных солей и, в случае кислотного компонента, предшествующее омыление сложного эфира и новое образование сложного метилового эфира.
Нижеследующие примеры служат для пояснения изобретения и не представляют собой никакого ограничения его объема.
Пример 1
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификация
В сухую реакционную аппаратуру вводят 0,17 моль (3R)-1-метилпирролидин-3-ола и 0,17 моль сложного рацемического метилового эфира 2-циклопентил-2-гидрокси-2-фенилуксусной кислоты в 800 мл абсолютного н-гептана. Затем 400 мл гептана отгоняют для удаления всех следов влаги и удаляют с помощью водоотделителя. После охлаждения добавляют 0,9 г NaOMe (10 мол.%) и снова кипятят. Отгоняющееся количество растворителя в течение 5-6 часов непрерывно заменяют с помощью капельной воронки. После обработки водой реакционной смеси и экстракции простым эфиром органическую фазу сушат над Na2SO4/K2CO3 в соотношении 2:1. Путем удаления осушителя и растворителя получают свободное основание с выходом 82%.
Кватернизация
Свободное основание кватернизуют путем добавки 3 экв. метилбромида, растворенного в метил-трет-бутиловом эфире, и выделяющийся в кристаллическом состоянии продукт с выходом 93% отсасываются на нутче. Образовавшаяся смесь диастереомеров из (3R,2'S)- и (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида находится в соотношении примерно один к одному.
Разделение диастереомеров путем перекристаллизации
Сырой продукт растворяют в 250 мл метанола, разбавляют с помощью 300 мл этилацетата и смешивают с 450 мл диэтилового эфира. Спустя два дня образовавшиеся кристаллы отсасывают на нутче и два раза перекристаллизовывают. Получают (3R,2'R)-изомер с 50%-ным выходом.
Аналитические данные
Внешний вид: бесцветные кристаллы.
1Н-ЯМР (D2O) (300 МГц): δ = 7,55-7,52 (м, 2Н, фенил); 7,37-7,24 (м, 3Н, фенил); 5,42-5,34 (м, 1Н); 4,67 (с, Н2О); 3,65 (дд, 1Н); 3,61-3,43 (м, 2Н); 3,40 (дд, 1Н); 3,13-2,98 (м, 1Н, циклопентилметин); 3,04 (с, 3Н, NCH3, (3R,2'R)); 2,75 (с, 3Н, NCH3, (3R,2'R)); 2,71-2,55 (м, 1Н); 2,30-2,17 (м, 1Н (3R,2'R)); 1,65-1,43 (м, 7Н, циклопентил); 1,19-1,05 (м, 1Н).
При этом диастереомерные соединения различаются по существу сдвигами следующих сигналов: 3,08 (с, NCH3); 2,91 (с, NCH3); 2,11-1,92 (м).
Из сравнения интегралов сигналов при 2,75 (с, 3Н, NCH3, (3R,2'R)) и 2,91 (c, NCH3 (диастереомеры)) для R,R-гликопирронийбромида получается диастереомерный избыток выше 98% (избыток диастереомера). Энантиомерная чистота достигается за счет использования энантиомерно чистого 3R-N-метилпирролидинола.
13С-ЯМР (D2O) (50 МГц): δ = 177,1 (с, 1'-СОО); 143,2 (с, фенил); 131,4 (д, фенил); 131,0 (д, фенил); 128,8 (д, фенил); 83,2 (с); 76,6 (д); 72,9 (т); 67,6 (т); 56,3 (кв, NCH3); 55,6 (кв, NCH3); 47,5 (д, циклопентилметин); 32,4 (т); 29,2/28,8/28,7/28,4 (т, циклопентилметилен).
Суммарная формула/масса катиона (С19Н28NO3)+(Br)-/318,44.
Масс-спектр (ионизация электронным распылением с образованием положительных ионов (ESI+)): 318,2 = М+.
Элементный анализ
Рассчитано, %: С 57,29; Н 7,09; N 3,52.
Найдено, %: С 57,41; Н 7,00; N 3,54.
Определение абсолютной конфигурации осуществляют с помощью рентгеноструктурного анализа.
Пример 2
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию и кватернизацию осуществляют, как описывается в примере 1.
Разделение диастереомеров осуществляют путем перекристаллизации смеси диастереомеров из изопропанола. Для этого сырой продукт растворяют в 8-кратном массовом количестве изопропанола при температуре кипения. Выдерживают в течение ночи при комнатной температуре и образовавшиеся кристаллы отсасывают на нутче. Эту процедуру повторяют еще раз. Таким образом полученный (3R,2'R)-гликопирронийбромид имеет такие же аналитические данные, как указанные в примере 1.
Пример 3
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийиодида
(формула (Ia), A- = I-)
Переэтерификацию, кватернизацию (с помощью метилиодида) и разделение диастереомеров осуществляют, как описывается в примере 1.
Таким образом полученный (3R,2'R)-гликопирронийиодид имеет такие же данные ЯМР-спектроскопии, как указанные в примере 1.
Пример 4
Получение (3R,2'S)-3-[(2'-циклопентил-2'-гидрокси-2'-(2"-тиенил)ацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ib), A- = Br-)
Переэтерификацию (с помощью (3R)-1-метилпирролидин-3-ола и сложного рацемического метилового эфира 2-циклопентил-2-гидрокси-2-(2'-тиенил)уксусной кислоты), кватернизацию и разделение диастереомеров осуществляют, как описывается в примере 1.
1Н-ЯМР (300 МГц; D2O): δ = 7,33 (д, 1Н, тиенил); 7,13 (д, 1Н, тиенил); 6,96 (дд, 1Н, тиенил); 5,50-5,42 (м, 1Н); 4,67 (с, Н2О); 3,78-3,62 (м, 2Н); 3,58-3,47 (м, 2Н); 3,08 (с, 3Н, N-CH3, (3R,2'S)); 3,01-2,83 (м, 4Н, N-CH3, (3R,2'S) и циклопентилметин); 2,76-2,62 (м, 1Н); 2,37-2,22 (м, 1Н (3R,2'S)); 1,65-1,20 (м, 8Н, циклопентилметилен).
При этом диастереомерные соединения (3R,2'R и 3S,2'S) различаются по существу сдвигами следующих сигналов: 3,11 (с, NCH3); 3,04 (с, NCH3); 2,15-2,03 (м).
Диастереомерный избыток определяют с помощью капиллярно-электрофоретического метода, который составляет выше 98% (избыток диастереомера). Энантиомерная чистота достигается за счет использования энантиомерно чистого 3R-N-метилпирролидинола.
13С-ЯМР (50 МГц, D2O): δ = 176,2 (с, 1'-СОО); 147,7 (с, тиенил); 130,1 (д, тиенил); 128,8 (д, тиенил); 128,4 (д, тиенил); 82,2 (с); 76,9 (д); 72,9 (т); 67,7 (т); 56,4 (кв, NCH3); 55,8 (кв, NCH3); 49,4 (д, циклопентилметин); 32,5 (т); 29,2/29,0/28,7/28,4 (т, циклопентилметилен).
Суммарная формула/масса катиона: (С17Н26NO3S)+(Br)-/324,47.
Масс-спектр (ESI+): 324,4 = М+.
Определение абсолютной конфигурации осуществляют с помощью рентгеноструктурного анализа.
Пример 5
Получение (3S,2'S)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию (с помощью (3S)-1-метилпирролидин-3-ола и сложного рацемического метилового эфира 2-циклопентил-2-гидрокси-2-фенилуксусной кислоты), кватернизацию и разделение диастереомеров осуществляют, как описывается в примере 1.
Данные ЯМР-спектроскопии соответствуют значениям, указанным в примере 1 для энантиомерного соединения.
Пример 6
Получение (3S,2'R)-3-[(2'-циклопентил-2'-гидрокси-2'-(2"-тиенил)ацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ib), A- = Br-)
Переэтерификацию (с помощью (3S)-1-метилпирролидин-3-ола и сложного рацемического метилового эфира 2-циклопентил-2-гидрокси-2-(2'-тиенил)уксусной кислоты), кватернизацию и разделение диастереомеров осуществляют, как описывается в примере 1.
Данные ЯМР-спектроскопии соответствуют значениям, указанным в примере 4 для энантиомерного соединения.
Пример 7
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию (с помощью рацемического 1-метилпирролидин-3-ола и сложного метилового эфира (2R)-2-циклопентил-2-гидрокси-2-фенилуксусной кислоты) и кватернизацию осуществляют, как описывается в примере 1.
Разделение диастереомеров осуществляют, как описывается в примере 2, путем перекристаллизации смеси диастереомеров из изопропанола.
Данные ЯМР-спектроскопии соответствуют значениям, указанным в примере 1.
Пример 8
Получение (3R,2'S)-3-[(2'-циклопентил-2'-гидрокси-2'-(2"-тиенил)ацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ib), A- = Br-)
Переэтерификацию (с помощью рацемического 1-метилпирролидин-3-ола и сложного метилового эфира (2S)-2-циклопентил-2-гидрокси-2-(2'-тиенил)уксусной кислоты) и кватернизацию осуществляют, как описывается в примере 1.
Разделение диастереомеров осуществляют, как описывается в примере 1, путем перекристаллизации смеси диастереомеров из смеси, состоящей из метанола, этилацетата и диэтилового эфира.
Данные ЯМР-спектроскопии соответствуют значениям, указанным в примере 4.
Пример 9
Получение (3S,2'S)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию (с помощью рацемического 1-метилпирролидин-3-ола и сложного метилового эфира (2S)-2-циклопентил-2-гидрокси-2-фенилуксусной кислоты) и кватернизацию осуществляют, как описывается в примере 1.
Разделение диастереомеров осуществляют, как описывается в примере 2, путем перекристаллизации смеси диастереомеров из изопропанола.
Данные ЯМР-спектроскопии соответствуют значениям, указанным в примере 1 для энантиомерного соединения.
Пример 10
Получение (3S,2'R)-3-[(2'-циклопентил-2'-гидрокси-2'-(2"-тиенил)ацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ib), A- = Br-)
Переэтерификацию (с помощью рацемического 1-метилпирролидин-3-ола и сложного метилового эфира (2R)-2-циклопентил-2-гидрокси-2-(2'-тиенил)уксусной кислоты) и кватернизацию осуществляют, как описывается в примере 1.
Разделение диастереомеров осуществляют, как описывается в примере 1, путем перекристаллизации смеси диастереомеров из смеси, состоящей из метанола, этилацетата и диэтилового эфира.
Данные ЯМР-спектроскопии соответствуют значениям, указанным в примере 4 для энантиомерного соединения.
Пример 11
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию и кватернизацию осуществляют, как описывается в примере 1, с тем различием, что метилирование проводят в изопропаноле. Отсасывание на нутче образовавшегося осадка приводит к соотношению диастереомеров, составляющему 98% 3R,2'R-изомера и 2% 3R,2'S-изомера.
Дальнейшее разделение диастереомеров осуществляют, как описывается в примере 2. Так как для перекристаллизации используют уже диастереомерно концентрированный сырой продукт, достигают более высокой чистоты стереоизомеров при одинаковом числе стадий кристаллизации, соответственно для такого же концентрирования необходимо меньшее число перекристаллизаций.
Таким образом, полученный (3R,2'R)-гликопирронийбромид имеет такие же аналитические данные, как указанные в примере 1.
Пример 12
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию и кватернизацию осуществляют, как описывается в примере 1, с тем различием, что метилирование проводят в ацетоне. Отсасывание на нутче образовавшегося осадка приводит к соотношению диастереомеров, составляющему 90% 3R,2'R-изомера и 10% 3R,2'S-изомера.
Дальнейшее разделение диастереомеров осуществляют, как описывается в примере 11.
Таким образом, полученный (3R,2'R)-гликопирронийбромид имеет такие же аналитические данные, как указанные в примере 1.
Пример 13
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
Переэтерификацию осуществляют, как описывается в примере 1.
Кватернизация
Свободное основание, растворенное в ацетоне, содержание воды в котором составляет 1%, кватернизуют путем добавления 1,3 экв. метилбромида и выделившийся в кристаллическом состоянии продукт с выходом примерно 74% (в расчете на желательный диастереомер) отсасывают на нутче. Соотношение диастереомеров составляет 95:5 или выше.
Дальнейшее разделение диастереомеров осуществляют, как описывается в примере 2. Так как для перекристаллизации используют уже диастереомерно концентрированный сырой продукт, достигают более высокой чистоты стереоизомеров при одинаковом числе стадий кристаллизации, соответственно для такого же концентрирования необходимо меньшее число перекристаллизаций.
Таким образом, полученный (3R,2'R)-гликопирронийбромид имеет такие же аналитические данные, как указанные в примере 1.
В случае в остальном такого же образа действий, однако при использовании ацетона с содержанием воды от 0,5 до 2%, в котором растворяется столько основания, что оно, по отношению к смеси растворителей, находится в концентрации от 5 до 20 мас.%, при кватернизации в отношении концентрирования диастереомеров получают сравнимые результаты.
Пример 14
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
Переэтерификацию осуществляют, как описывается в примере 1, кватернизацию проводят, как описывается в примере 13.
Разделение диастереомеров осуществляют путем перекристаллизации смеси диастереомеров из изопропанола, содержание воды в котором составляет 0,5%. После только однократного повторения перекристаллизации доля нежелательного диастереомера составляет меньше чем 0,5%.
Таким образом полученный (3R,2'R)-гликопирронийбромид имеет такие же аналитические данные, как указанные в примере 1.
В случае в остальном такого же образа действий, однако при использовании изопропанола с содержанием воды от 0,2 до 3%, которого добавляют столько, что сырой продукт, по отношению к смеси растворителей, находится в концентрации от 5 до 30 мас.%, после двукратной перекристаллизации в отношении концентрирования диастереомеров получают сравнимые результаты.
Пример 15
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
Переэтерификацию осуществляют подобным образом, как описывается в примере 1.
Кватернизация
6 кг гликопирролята в качестве основания растворяют в 55 л ацетона, содержание воды в котором составляет примерно 1%, и смесь охлаждают до температуры -5°С (±5°С). Медленно вводят 1,3 эквивалента газообразного бромметана, так чтобы он мог конденсироваться в охлажденном растворе. Затем нагревают в течение 3 часов до комнатной температуры и выдерживают при перемешивании следующие 3 часа. Выпавший осадок отфильтровывают и для удаления метилбромида из продукта дополнительно промывают с помощью 10 л ацетона.
Путем высушивания получают сырой продукт в виде кристаллического осадка белого цвета с выходом примерно 70% (в расчете на желательный диастереомер), в котором содержатся менее 5% нежелательного диастереомера.
Перекристаллизация
К осадку добавляют 20 л изопропанола, содержание воды в котором составляет 0,5%, и эту смесь кипятят с обратным холодильником. Когда твердое вещество полностью растворяется, раствор фильтруют для очистки от находящихся во взвешенном состоянии веществ. Для кристаллизации раствор охлаждают в течение 3 часов до комнатной температуры. Спустя следующие 3 часа выпавший в осадок продукт можно отсасывать на нутче, причем дополнительно промывают с помощью 5 л изопропанола.
Однократного повторения процесса перекристаллизации достаточно для получения (3R,2'R)-гликопирронийбромида качества, которое превосходит требования, предъявляемые к биологически активному веществу для получения лекарственных средств, то есть в нем содержатся в сумме менее 0,5% других трех стереоизомеров и менее 1% всех примесей.
Пример 16
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию и кватернизацию осуществляют, как описывается в примере 1.
Выделяют образовавшуюся смесь диастереомеров из (3R,2'S)- и (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида в соотношении примерно один к одному.
3 г этой смеси диастереомеров суспендируют в 21 мл ацетона, содержание воды в котором составляет 1%, и перемешивают в течение 6 часов при комнатной температуре. Путем отсасывания на нутче твердого вещества получают 1,047 г, где желательный диастереомер содержится в количестве 93% (избыток диастереомера).
Пример 17
Получение (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида
(формула (Ia), A- = Br-)
Переэтерификацию и кватернизацию осуществляют, как описывается в примере 1.
Выделяют образовавшуюся смесь диастереомеров из (3R,2'S)- и (3R,2'R)-[(2-циклопентил-2-гидрокси-2-фенилацетил)окси]-1,1-диметилпирролидинийбромида в соотношении примерно один к одному.
8 г этой смеси диастереомеров растворяют в 40 мл кипящего изопропанола, содержание воды в котором составляет 0,5%, и затем раствор в течение 3 часов охлаждают до комнатной температуры. После перемешивания в течение следующих 3 часов при комнатной температуре выпавший в осадок продукт отсасывают на нутче. Получают 2,227 г твердого вещества, в котором желательный диастереомер содержится в количестве 96% (избыток диастереомера).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭНАНТИОМЕРНО ЧИСТЫЕ ОСНОВНЫЕ ЭФИРЫ АРИЛ-ЦИКЛОАЛКИЛГИДРОКСИКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В ЛЕКАРСТВЕННЫХ СРЕДСТВАХ | 1997 |
|
RU2238936C2 |
| ПРОИЗВОДНЫЕ ХИНУКЛИДИНАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, КОМБИНИРОВАННЫЙ ПРОДУКТ И СПОСОБ ИНГИБИРОВАНИЯ МУСКАРИНОВЫХ РЕЦЕПТОРОВ | 2003 |
|
RU2314306C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ ПИРРОЛИДИНИЯ | 2010 |
|
RU2554878C2 |
| НОВЫЕ СЛОЖНЫЕ ЭФИРЫ КВАТЕРНИЗОВАННОГО ХИНУКЛИДИНА | 2005 |
|
RU2382041C2 |
| СОЕДИНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ ПРОТЕАЗЫ ВИЧ | 1994 |
|
RU2139280C1 |
| Иммуномодулирующие азалиды на основе мочевины | 2021 |
|
RU2811591C1 |
| ТРАНСИЗОМЕРНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПОЛУЧЕНИЕ | 2018 |
|
RU2759443C2 |
| ПРОИЗВОДНЫЕ ХИНУКЛИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2001 |
|
RU2282629C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ОПТИЧЕСКИ ЧИСТЫХ (S)-(+) И/ИЛИ (R)-(-)-ИЗОМЕРОВ 10, 11-ДИГИДРО-10-ГИДРОКСИ-5H-ДИБЕНЗ[b,f]АЗЕПИН-5-КАРБОКСАМИДА, ИХ СООТВЕТСТВУЮЩИХ 10-АЦЕТОКСИПРОИЗВОДНЫХ И НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2002 |
|
RU2318813C2 |
| ИНГИБИТОР ДИПЕПТИДИЛПЕПТИДАЗЫ-4 ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА 2-ГО ТИПА, СОЕДИНЕНИЯ (ВАРИАНТЫ) | 2018 |
|
RU2712097C1 |
Настоящее изобретение может быть использовано в медицине или фармацевтике и относится к способу получения стереоизомера гликопирронийбромида или -иодида формулы

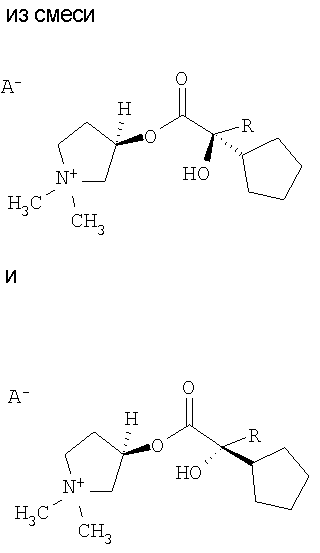
где А-=Br или I, R означает фенил или тиенил. Технический результат - получение с высоким выходом биологически активного диастереоизомера гликопирронийбромида или -иодида. 1 н. и 7 з.п. ф-лы.
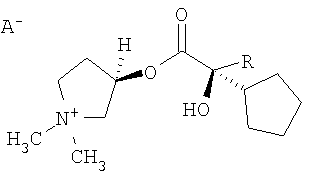
где А=Br или I; R означает фенил или тиенил,
отличающийся тем, что используют смесь диастереомеров, которая содержит энантиомерно чистую долю спирта и рацемическую долю кислоты или рацемическую долю спирта и энантиомерно чистую долю кислоты, и состоящую из 3R,2'R и 3R,2'S изомеров формул

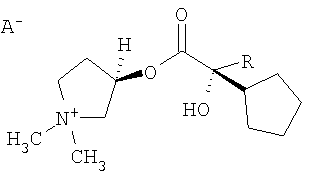
где А=Br или I; R означает фенил или тиенил,
и указанную смесь четвертичных диастереомеров получают посредством кватернизации соответствующих смесей третичных основных диастереомеров, и при кватернизации каждый изолируемый, особенно хорошо кристаллизируемый стереоизомер после реакции получают концентрированным в виде осадка, причем используют растворитель или смесь растворителей, которые предпочтительно, по меньшей мере, содержат один растворитель, выбранный из группы, состоящей из разветвленных или неразветвленных спиртов с низкой молекулярной массой, таких как метанол, этанол, изопропанол, пропан-1-ол, трет-бутанол, изобутанол, н-бутанол, а также ацетона, бутанона, ацетонитрила, и указанную смесь четвертичных диастереомеров (возможно в уже концентрированной форме) перекристаллизовывают и получают каждый выделяемый, особенно хорошо кристаллизуемый стереоизомер сильно концентрированный в виде осадка, причем в качестве растворителя используют метанол и/или этанол, и кристаллизацию проводят при помощи этилацетатата и/или трет-бутилметилового эфира.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Способ получения производных пирролидина или их солей с неорганической кислотой | 1984 |
|
SU1416056A3 |
| US 2956062 (ROBINS CO INC) 11.10.1960 | |||
| I | |||
| DEMIAN ET ALL, J | |||
| LIQ | |||
| CHROMATOGR., 1990, VOL.13, №46, 779-787 | |||
| ZHI WANG ET ALL, J | |||
| HIGH RESOL | |||
| CHROMATOGR., 1996, VOL.19, №12, 697-699. | |||
Авторы
Даты
2008-10-27—Публикация
2003-12-18—Подача