Изобретение относится к области биотехнологии, в частности к способам получения вакцинных препаратов с помощью методов генетической инженерии и иммунологии, и может быть использовано в медицине и смежных отраслях для повышения экспрессии белков, в частности белка Gp140 как фрагмента белка Env вируса иммунодефицита человека 1 типа (ВИЧ-1) субтипа А или его фрагментов и синтетических аналогов в эукариотических клетках.
Одной из глобальных проблем, стоящих перед биотехнологией, является повышение выхода веществ, продуцируемых клетками прокариот и эукариот. Для решения указанных задач, как правило, клетки подвергают воздействию различных внешних факторов: повышению температуры выше 42°С, уменьшению количества питательных веществ, например фосфатов или азота, до уровня, лежащего ниже того, который требуется для выживания микроорганизмов, токсическое воздействие - например использование красителей, кислот или эксудатов растений, метаболическое разрушение клеток в результате изменения уровня содержания ионов, воздействующих на способность микроорганизмов к осморегуляции, или введение витаминов или кофакторов, которые способны вызвать прекращение метаболизма (RU 2179980, 2002).
Однако, т.к. воздействие вышеперечисленных факторов на выход конкретных продуцентов характеризуется высокой видоспецифичностью, то для каждого конкретного случая необходимо проведение большого объема исследований.
Наиболее сложно вопросы стимулирования экспрессии решаются в случае получения вакцин против вируса иммунодефицита человека (ВИЧ), для изготовления которых необходимо научиться добиваться экспрессии вирусных белков в клетках эукариот без введения вируса, что позволило бы выработать в организме необходимый иммунный ответ. Проблема связана с особенностями последовательностей генов вируса иммунодефицита человека, в частности с использованием в вирусных генах кодонов, не характерных для интенсивно экспрессирующихся генов млекопитающих, в частности человека, а также большая вариабельность вирусной популяции, выраженная в генетической дивергенции.
Одним из подходов к решению этой проблемы является использование геномов ретро-вирусов, аденовирусов, папилломавирусов и паповавирусов в качестве стимуляторов для экспрессии протективных антигенов патогенных вирусов в клетках млекопитающих.
Наиболее детально исследования проводились с использованием вируса осповакцины (ВОВ). В частности, были сконструированы рекомбинантные ВОВ, экс-прессирующие отдельно индивидуальные белки ВИЧ-1: gp160, gp120. Tat и обратную транскриптазу (Moss В., and Flexner С. // Ann. Rev. Immunol, 1987, v.5, p.305; Moss В. // Seminars in Virology, 1992, v.3, p.277; Falkner F.G., et al. // Virology, 1988, v.164, p.450; Flexner C., et al. // Virology, 1988, v.166, p.339; Takahashi H., et al. // Proc. Natl. Acad. Sci. USA, 1988, v.85, p.3105; Walker B.D, et al. // Science, 1988, v.240, p.64; Willey R.L., et al. // J.Virol, 1988, v.62, p.139). Полученные рекомбинантные BOB были использованы для иммунизации лабораторных животных и выявления белков ВИЧ-1, способных вызывать индукцию нейтрализующих вирус антител. Однако с помощью рекомбинантных ВОВ не удалось индуцировать полноценный протективный иммунный ответ против ВИЧ-инфекции. По-видимому, это обусловлено низкой иммуногенностью индивидуальных вирусных белков (RU 2194075, 2002).
Для решения проблемы получения иммунного ответа на белки ВИЧ был создан белок TBI, который включает в свой состав несколько клеточных эпитопов ВИЧ-1. Однако при его использовании не удается получить весь спектр целевых продуктов. Кроме того, степень экспрессии получаемых белков недостаточно высока (RU 2237089, 2005).
Известна рекомбинантная плазмидная ДНК pUE 41, содержащая BamHI - Hin-dIII фрагмент плазмидной ДНК pUR292, Bg1II-HindIII фрагмент плазмидной ДНК рВН292, уникальный сайт рестрикции HindIII, а также следующие гены и генетические маркеры:
- ген bla, обеспечивающий синтез β-лактамазы,
- ген lacZ, обеспечивающий синтез α частицы β-галактозидазы,
- фрагмент гена env ВИЧ-1, обеспечивающий синтез полипептида, обладающего антигенным свойством белков оболочки вируса иммунодефицита человека первого типа. Данная плазмидная ДНК обеспечивает синтез в клетках E.coli гибридного полипептида, способного связывать антитела к белкам оболочки ВИЧ-1 gp120 и gp41. При этом образуется слитый белок, N-концевая часть которого содержит β-галактозидазу, а С-конец - искомый фрагмент гена env (SU 1766070).
Известна также рекомбинантная плазмидная ДНК pESG, которая используется для экспрессии фрагмента гена env Т-лимфотропного вируса человека первого типа (HTLV-1) в клетках E.coli. Как и в предыдущем случае, в бактериальных клетках образуется слитый белок, N-конец которого содержит β-галактозидазу, а С-конец - часть гена env HTLV-1. Структура плазмиды сходна с описанной в предыдущем случае (RU 2081172, 2000).
Однако экспрессия гена env ВИЧ-1 или других ретровирусов, а также его фрагментов, например белков gp120 или gp140, в клетках высших эукариот с помощью таких конструкций обеспечиваться не может.
Наиболее близким по технической сущности и достигаемому эффекту к заявляемому изобретению является стимулирование экспрессии гена env в виде белка Gp120, введением в клетку высших эукариот экспрессионной плазмидной ДНК pBMC-gp120(A)m-1, содержащей модифицированный ген gp120 вируса иммунодефицита человека типа 1 субтипа А (пат. РФ №2229518, 2002). Недостатком указанного стимулятора являлся: невысокий выход целевого продукта, низкая иммунологическая представленность некоторых аминокислот синтезируемого белка Gp120, в популяции ВИЧ-инфицированных индивидуумов на территории России и потеря важных иммунологических эпитопов, представленных в области белка Gp41.
Технической задачей, решаемой авторами, являлось создание стимулятора синтеза белка Gp140, позволяющего повысить его выход и иммуногенность.
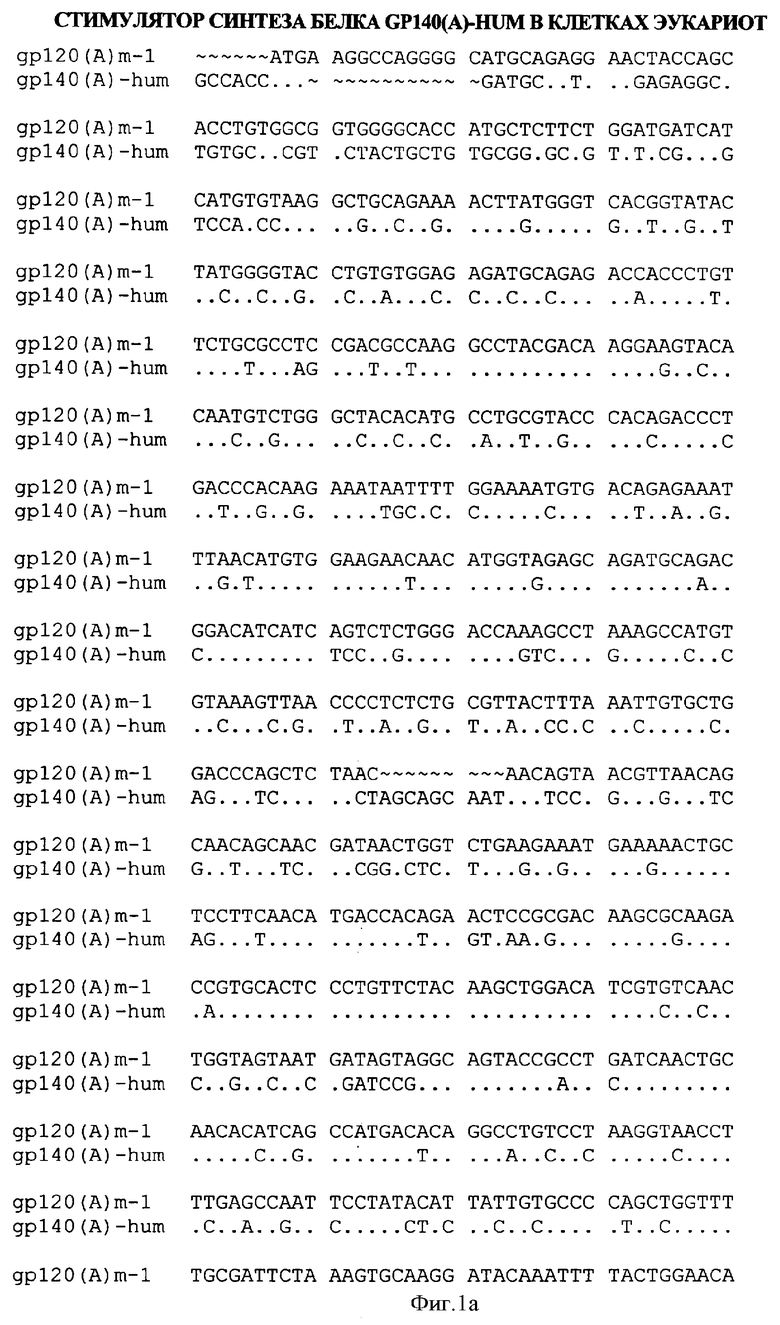
Технический результат был получен при использовании в качестве стимулятора экспрессионной плазмидной ДНК, содержащей модифицированный ген gp120 вируса иммунодефицита человека типа 1 субтипа А, названный gp120(A)m-1, последовательность которого представлена на фиг.1а-1в.
В основу изобретения были положены представления о том, что в генах вируса имеются так называемые ингибирующие участки (INS), в которых много аденина и тимина и редко встречаются гуанин и цитозин. Содержание в составе мРНК таких участков приводит к преждевременному распаду мРНК в клеточном ядре. Для транспорта вирусных мРНК из ядра в цитоплазму вирус использует свой вирусный белок - Rev. Пока Rev не синтезировался и не проник в ядро, вирусные мРНК будут находиться в ядре и там подвергаться деградации. Появившийся в ядре Rev связывается со специфической последовательностью RRE (Rev Responsible Element) в мРНК вируса, переносит мРНК в цитоплазму, где затем синтезируются вирусные белки, в том числе Env. В результате проведенных авторами исследований было установлено, что при устранении из гена gp120 ингибирующих участков удается в 10-15 раз повысить выход белка gp120.
Согласно настоящему изобретению новый стимулятор был получен по следующей методике.
Был осуществлен анализ кодонов в составе фрагмента гена env, кодирующего белок Gp140 ВИЧ-1 субтипа А. Все кодоны с высоким содержанием аденина и тимина были заменены на синонимичные кодоны со сниженным содержанием аденина и тимина и, соответственно, более высоким содержанием гуанина и цитозина, при этом в состав гена предпочтительно включали кодоны, характерные для интенсивно экспрессирующихся генов человека. Кроме того, в последовательность гена включили последовательность Козака, инициирующий и два терминирующих трансляцию кодоны. Также были выявлены кодоны, соответствующие редко встречаемым аминокислотам в иммунологически важных областях белка Gp120, и заменены на кодоны аминокислот, часто встречающихся в популяции ВИЧ-1 на территории России и стран СНГ. Кроме того, к последовательности белка Gp120 были добавлены две иммунологически важные области белка Gp41 и заменена последовательность природного сигнального пептида на последовательность, кодирующую сигнальный пептид тканевого активатора плазминогена человека. В результате с помощью автоматизированного химического синтеза был получен искусственный ген gp140(A)-hum, кодирующий синтетический белок Gp140(A)-hum, который был вставлен в вектор рВМС с получением экспрессионной плазмиды pBMC-gp140(A)-hum.
Сущность изобретения поясняется чертежами, на которых представлены:
На фиг.1а-1в - последовательность нуклеотидов гена gp140(A)-hum в сравнении с последовательностью нуклеотидов гена gp120(A)m-1 (прототип);
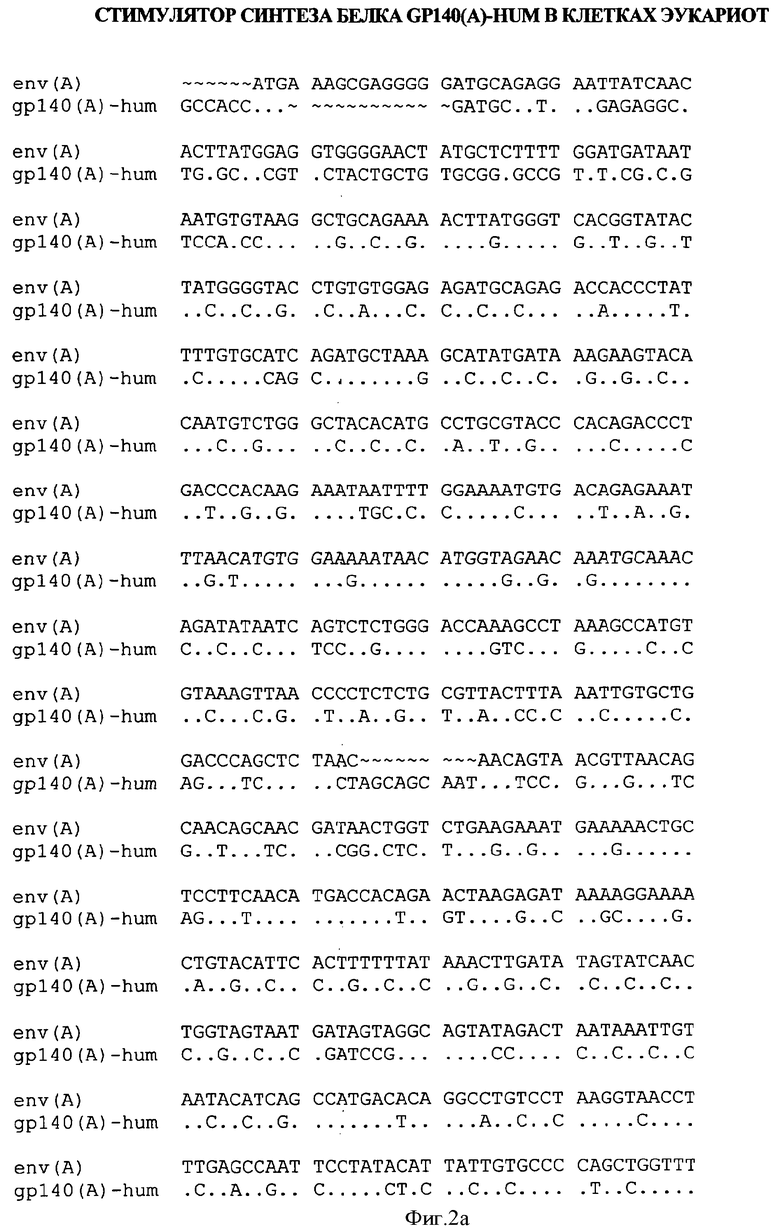
На фиг.2а-2г - последовательность нуклеотидов гена gp140(A)-hum в сравнении с последовательностью нуклеотидов природного гена env(A);
На фиг.3а-3б - последовательность аминокислот белка Gp140(A)-syn в сравнении с последовательностью аминокислот белка Env(A) (прототип).
Нуклеотиды и аминокислоты, одинаковые для представленных генов, отмечены в сравниваемой последовательности точкой (.), отсутствующие в последовательностях - тильдой (˜), различающиеся - приведены соответствующей буквой. Ген gp140(A)-hum длиной 1830 нуклеотидов отличается от прототипа Gp120(A)m-1 по 809 нуклеотидам и по 1325 нуклеотидам отличается от природного гена env (A). Белок Gp140(A)-hum длиной 608 аминокислот отличается от прототипа Env(A) по 309 аминокислотам.
Промышленная применимость заявляемого стимулятора синтеза белка и синтетического белка иллюстрируется следующими примерами.
Пример 1. Получение плазмидной ДНК, обеспечивающий экспрессию синтетического белка Gp140(A)-hum с использованием искусственного гена gp140(A)-hum
Искусственный ген gp140(A)-hum, последовательность которого представлена на фиг.1, получали при помощи химического синтеза перекрывающихся фрагментов с последующим отжигом и лигированием. Собранный ген вставляли известным способом в плазмидный вектор рВМС с получением экспрессионной плазмиды pBMC-gp140(A)-hum. Полученной плазмидой pBMC-gp140(A)-hum трансформировали клетки Escherichia coli для ее последующей наработки.
Пример 2. Изучение синтеза синтетического белка Gp140(A)-hum в эукариотических клетках
Культуру клеток человека линии 293 трансформировали ДНК рекомбинантной плазмиды pBMC-gp140(A)-hum. В качестве контроля параллельную культуру клеток 293 трансформировали равным количеством ДНК плазмиды pBMC-gp120(A)m-1. Трансформированные культуры клеток инкубировали в питательной среде в течение 48 часов при температуре +37°С и содержании СО2 в воздухе, равном 5%, лизировали и анализировали белки клеточных лизатов с помощью электрофореза в ПААГ с последующим иммуноблоттингом с сывороткой пациента, инфицированного ВИЧ-1 субтипа А. Интенсивность окраски полос, соответствующих белкам Gp120 и Gp140, анализировали с помощью компьютизированной видеосистемы. Установлено, что в культуре клеток, трансформированных плазмидной ДНК pBMC-gp140(A)-hum, уровень синтетического белка Gp140(A)-hum не менее чем 6-8 раз выше, чем синтез белка Gp120(A) в клетках, трансформированных контрольной плазмидой рВМС-gp120(A)m-1.
Пример 3. Использование плазмидной ДНК pBMC-gp140(A)-hum для иммунизации
Лабораторным мышам линии BALB/c вводили внутримышечно трехкратно по 10 микрограмм плазмидной ДНК pBMC-gp140(A)-hum, контрольной группе мышей вводили аналогичную дозу pBMC-gp120(A)m-1. Через 6 недель в сыворотках крови животных определяли титры антител к природному вирусному белку Gp120 известным способом. Результаты приведены в таблице 1.
Полученные результаты показали, что использование в качестве стимулятора синтеза белка Gp140(A)hum в клетках эукариот искусственного гена gp140(A)-hum позволяет примерно в 6-8 раза повысить выход целевого продукта.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭКСПРЕССИОННАЯ ПЛАЗМИДНАЯ ДНК pBMC-nef(A)-hum | 2006 |
|
RU2335540C1 |
| ЭКСПРЕССИОННАЯ ПЛАЗМИДНАЯ ДНК р-ВМС-gag(A)-hum ДЛЯ ЭКСПРЕССИИ БЕЛКА р55 ВИЧ-1 В КЛЕТКАХ ЭУКАРИОТ | 2006 |
|
RU2345138C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBMC-RT(А)-hum ДЛЯ ЭКСПРЕССИИ БЕЛКА ОБРАТНОЙ ТРАНСКРИПТАЗЫ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2006 |
|
RU2355764C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РВМС-QP120(A)M-1 ДЛЯ ИММУНИЗАЦИИ ПРОТИВ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2003 |
|
RU2227161C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PBMC-GAG(A)MOD ДЛЯ ЭКСПРЕССИИ БЕЛКА GAG ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА В ЭУКАРИОТИЧЕСКИХ КЛЕТКАХ | 2003 |
|
RU2241752C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РВМС-RT(A)M-1, ИСПОЛЬЗУЕМАЯ ДЛЯ ЭКСПРЕССИИ ОБРАТНОЙ ТРАНСКРИПТАЗЫ (RT) ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА В КЛЕТКАХ ВЫСШИХ ЭУКАРИОТ | 2003 |
|
RU2238977C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РВМС-NEF(A)M-1, ЭКСПРЕССИРУЮЩАЯ БЕЛОК NEF ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ТИПА 1 В ЭУКАРИОТИЧЕСКИХ КЛЕТКАХ | 2003 |
|
RU2229518C1 |
| ПРОФИЛАКТИЧЕСКАЯ ВАКЦИНА ПРОТИВ ВИЧ, ОСНОВАННАЯ НА ВИЧ-СПЕЦИФИЧЕСКИХ АНТИТЕЛАХ | 2008 |
|
RU2505604C2 |
| Кассетная генетическая конструкция, экспрессирующая две биологически активные siPHK, эффективно атакующие мишени в мРНК генов vpu и env ВИЧ-1 субтипа А у больных в России, и одну siPHK, направленную на мРНК гена CCR5 | 2016 |
|
RU2630644C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДОСТАВКИ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА | 1994 |
|
RU2174845C2 |






Изобретение относится к области биотехнологии, в частности к способам получения вакцинных препаратов с помощью методов генетической инженерии и иммунологии. Предлагается экспрессионная плазмида ДНК pBMC-gp140(A)-hum, содержащая искусственный ген gp140(A)-hum, для экспрессии белка Gp140(A)-hum в клетках эукариот, что позволяет в 6-8 раз повысить выход синтетического белка Gp140(A)-hum no сравнению с прототипом. Изобретение может быть использовано в медицине и смежных отраслях для повышения экспрессии белков, в частности кодируемого геном gp140 белка Gp140 или его фрагментов в эукариотических клетках. 3 ил., 1 табл.
Экспрессионная плазмида ДНК pBMC-gp140(A)-hum для экспрессии белка Gp140(A)-hum в клетках эукариот, отличающаяся тем, что она содержит искусственный ген gp140(A)-hum, имеющий последовательность нуклеотидов, представленную на фиг.1.
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PESG, СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОЙ ПЛАЗМИДНОЙ ДНК PESG И ШТАММ БАКТЕРИЙ ESCHERICHIA COLI, СОДЕРЖАЩИЙ РЕКОМБИНАНТНУЮ ПЛАЗМИДНУЮ ДНК PESG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ГИБРИДНОГО БЕЛКА, СОСТОЯЩЕГО ИЗ 485 А.К., ОБЛАДАЮЩЕГО АНТИГЕННЫМИ СВОЙСТВАМИ ПОВЕРХНОСТНОГО ГЛИКОПРОТЕИНА ВИРУСА Т-КЛЕТОЧНОГО ЛЕЙКОЗА ЧЕЛОВЕКА ПЕРВОГО ТИПА | 1994 |
|
RU2081172C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РВМС-NEF(A)M-1, ЭКСПРЕССИРУЮЩАЯ БЕЛОК NEF ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ТИПА 1 В ЭУКАРИОТИЧЕСКИХ КЛЕТКАХ | 2003 |
|
RU2229518C1 |
Авторы
Даты
2009-02-10—Публикация
2006-12-25—Подача