FОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к области биохимии микробов. В одном аспекте изобретение касается воздействия на биохимические пути, включая азотный катаболизм в организмах, способных к ферментации углеводов с получением этилового спирта. В выбранных реализациях изобретение касается культур и способов производства вина и других продуктов ферментации.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Аргинин является одной из преобладающих аминокислот, присутствующих в виноградном сусле (Henschke and Jiranek, 1993). Считают, что аргинин транспортируется в дрожжевую клетку обычной пермеазой аминокислот, кодируемой геном GAP1 (Jauniaux and Grenson, 1990) или пермеазой аргинина, кодируемой геном CAN1 (Hoffmann, 1985). Согласно имеющимся сообщениям в Saccharomyces cerevisiae аргинин расщепляется на мочевину и орнитин с помощью аргиназы, продукта гена CAR1 (Middelhoven, 1964; Sumrada and Cooper, 1982).
Ген DUR1,2 кодирует бифункциональный фермент, карбоксилазу мочевины-аллофанатгидролазу (Dur1,2; амидолиазу мочевины), который может расщеплять мочевину на аммиак и СО2. Мочевино-карбоксилазная функция кодируется отдельно в ферменте из зеленых водорослей, который катализирует реакцию: АТФ+мочевина+СО2=АДФ+фосфат+мочевина-1-карбоксилат (ЕС 6.3, 4.6; систематическое название: мочевина: СО2-лигаза (АДФ-образующая); другие названия: уреаза(АТФ-гидролизующая); карбоксилаза мочевины (гидролизующая); АТФ-амидолиаза мочевины; CAS регистрационный номер: 9058-98-4; Roon et al, 1970; Roon and Levenberg, 1972; Sumrada and Cooper, 1982). Аллофанатгидролазная функция также кодируется отдельно в ферменте из зеленых водорослей, который катализирует реакцию: мочевина-1-карбоксилат+Н2O=2СO2+2NH3 (EC 3.5.1.54; систематическое название: мочевина-1-карбоксилат амидогидролаза; другое название: аллофанатлиаза; CAS регистрационный номер: 79121-96-3; Maitz et al., 1982; Roon, et al., 1972; Sumrada and Cooper, 1982).
В S. cerevisiae ген DUR1,2 подвергается азотной катаболитной репрессии (АКР от англ. NCR - nitrogen catabolite repression) предпочтительными источниками азота, присутствующими в виноградном сусле (Genbauffe and Cooper, 1991). Мочевина, которая не расщепляется, может секретироваться дрожжевыми клетками в бродящее виноградное сусло. Секретируемая мочевина может взаимодействовать в сусле с этанолом с образованием этилкарбамата, который, как было показано, вызывает различные доброкачественные и злокачественные опухоли у множества экспериментальных животных (Mirvisch, 1968) и поэтому может рассматриваться в качестве потенциального фактора риска для здоровья людей.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте изобретения обнаружено, что концентрацией мочевины в бродящем виноградном сусле, вине или дистиллированном напитке можно управлять путем модуляции азотной катаболитной репрессии гена DUR1,2 в S. cerevisiae, кодирующего мочевино-карбоксилазную и аллофанатгидролазную активности. В одном аспекте изобретения соответственно предложены дрожжевые штаммы, трансформированные для уменьшения азотной катаболитной репрессии гена, кодирующего мочевино-деградирующую ферментативную активность, экспрессирующуюся дрожжевым штаммом при условиях ферментации. Дрожжевой штамм, например, может быть трансформирован рекомбинантной нуклеиновой кислотой, содержащей последовательность, кодирующую мочевино-деградирующую ферментативную активность, или промотором, подходящим для опосредования экспрессии мочевино-деградирующей ферментативной активности при условиях ферментации. В некоторых реализациях изобретения используют нативные или модифицированные последовательности, гомологичные промоторной и кодирующей последовательностям гена DUR1,2 из S. cerevisiae. Дрожжевые штаммы и нуклеиновые кислоты по настоящему изобретению могут быть использованы, например, для получения ферментированных алкогольных напитков, таких как вина и другие продукты ферментации.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 представляет графическое изображение расположенного в 3'-5' направлении участка гена DUR1,2, оканчивающегося в начале кодирующей последовательности DUR.1,2. Информация, представленная на Фиг.1, получена из опубликованной полной последовательности хромосомы II Saccharomyces cerevisiae (Genbank LOCUS NC_001134, ACCESSION NC_001134, REGION: complement (635670..643177), VERSION NC_001134.2, G1:14270686; Feldmann, H., Aigle, M., Aljinovic, G., Andre, В., Baclet, M.C., Barthe, C., Baur, A, Becam, A.M., Biteau, N., Boles, E. et al. "Complete DNA sequence of yeast chromosome II" EMBO J.13 (24), 5795-5809 (1994); Goffeau, A, Barrell, B.G., Bussey, H., Davis, R.W., Dujon, В., Feldmann, H., Galibert, F., Hoheisel, J.D., Jacq, C., Johnston, M., Louis, E.J., Mewes, H.W., Murakami, Y., Philippsen, P., Tettelin, H. and Oliver, S.G. "Life with 6000 genes" Science 274 (5287), 546 (1996)).
Фиг.2 представляет часть последовательности расположенного в 3'-5' направлении участка гена DUR.1,2, оканчивающегося в стартовом кодоне ATG гена DUR.1,2. Рамкой выделены два предполагаемых АКР-элемента: GATAA(G)-боксы (один в положении от -54 до -58, а другой в положении от -320 до -324), а также предполагаемые ТАТАА-боксы.
Фиг.3 демонстрирует активацию транскрипции и трансляции DUR1,2 в дрожжах, контролируемую экспрессионной кассетой, содержащей DUR1,2. (А) Экспрессию DUR1,2 в трансформированных клетках GVY400, содержащих (дорожка 2) или не содержащих (дорожка 1) кДНК DUR1,2, сравнивали с помощью Нозерн-анализа тотальной РНК с использованием α32Р-dАТР-меченого зонда для DUR1,2. HHFI, кодирующий гистон 4, использовали в качестве стандарта нагрузки РНК. (В) Экспрессию амидолиазы мочевины в трансформированных клетках GVY400, содержащих (дорожка 3) или не содержащих (дорожка 2) кДНК DUR1,2, визуализировали с помощью вестерн-блота биотинилированных белков, присутствующих в тотальном белке, экстрагированном из трансформантов. Определение проводили с помощью хемилюминисценции на рентгеновской пленке, используя стрептавидин, конъюгированный с пероксидазой из хрена. Высокомолекулярные биотинилированные стандарты (5 мкг на дорожку) включали в качестве маркеров молекулярной массы (дорожка 1).
Фиг.4 представляет схематическое изображение стратегии клонирования гена DUR1,2 в плазмиде pHVX2 с получением PJC1 согласно способу DI/TRISEC (Dietmaler and Fabry, 1995). Геномную ДНК из S. cerevisiae TCY 1 получали согласно стандартным способам (Ausubel et al., 1995). Кодирующую последовательность гена DUR1,2 амплифицировали с помощью ПЦР, используя ДНК-полимеразу ExTaq (Takara). Использовали праймеры:
5TAAAAAAATGACAGTTAGTTCCGATACA3' для 5'-конца и 5TCGAAAAAGGTATTTCATGCCAATGTTATGAC3' для 3'-конца гена. Так называемый стартовый кодон и комплементарная последовательность для стоп-кодона представлены полужирным шрифтом. Продукт амплификации обрабатывали ДНК-полимеразой Т4 для удаления нескольких нуклеотидов на 3'-фланкирующем конце. При необходимости 3'-5'-экзонуклеазную активность фермента подавляли путем добавления адекватных нуклеотидов. Плазмиду pHVX2 (Volschenk et al., 1997) разрезали рестрикционными ферментами EcoRI и BgRlII и затем обрабатывали фрагментом Кленова ДНК-полимеразы I из Е.coli. Рестрикционные сайты были частично заполнены в присутствии dATP и dGTP, для того чтобы иметь последовательности, совместимые с клонированием вставки.
Фиг.5 представляет схему клонирования флеомицин-резистентной генной кассеты в pJCl (меченная pHVX2 или pRUR.1,2), содержащей ген DUR1,2. Для конструирования pJC2 использовали стандартные рекомбинантные методы (меченная pHVX2phleo или pDUR1,2phleo) (Ausubel et al., 1995).
Фиг.6 представляет схематическое изображение плазмиды pJC2/DUR1,2phleo (меченная pDUR1,2phleo на иллюстрации), которая является мультикопийной, эписомной челночной плазмидой S. cerevisiae - E.coli, полученной из вектора pJC2phleo, где ген DUR1,2 встроен между регуляторными последовательностями гена дрожжевой фосфоглицераткиназы (PGK1) (промоторной и терминаторной последовательностями). Маркер LEU2 облегчает селекцию трансформированных дрожжевых клеток, которые являются ауксотрофными по лейцину. Эта плазмида содержит также ген Тn5Вlе, управляемый конститутивным дрожжевым промотором TEF1, и дрожжевой терминатор CYC1. Дрожжевые клетки, несущие эту кассету, становятся устойчивыми к флеомицину. Применение этого положительного селективного маркера может быть особенно полезным для работы с трансформированными промышленными дрожжевыми штаммами, которые не несут ауксотрофных маркеров.
Фиг.7 представляет графическое изображение способности трансформированных дрожжей по настоящему изобретению уменьшать концентрацию мочевины в культуральной среде. Гаплоидный лабораторный дрожжевой штамм, разрезанный в DUR1,2 хромосомном локусе, был трансформирован плазмидой pJC2/DUR1,2phleo или плазмидой pJC2phleo без гена DUR1,2. Применение этого мутантного штамма позволяет охарактеризовать исследуемый штамм в отсутствие фона, обусловленного мочевино-амидолиазной эндогенной активностью. Трансформированные клетки выращивали в минимальной среде, содержащей 0,1% глутамина, отбирали и использовали для инокуляции свежей среды. Через 1 ч добавляли мочевину 33 мг/л. Каждые 2 ч отбирали аликвоты культуры, клетки разрушали в среде со стеклянными бусинами и клеточный дебрис удаляли центрифугированием. После того как супернатант был собран, ферменты инактивировали нагреванием и определяли количество мочевины, присутствующей в образце. Этот способ облегчает одновременное измерение внутриклеточной и внеклеточной мочевины, позволяя делать различие между мочевиной, поглощаемой клетками, и мочевиной, метаболизируемой клетками. Для контроля стадии роста каждой культуры регулярно измеряли также поглощение при 600 нм. Стандартное отклонение n=6. Данные, представленные закрашенными кружками, представляют собой концентрацию мочевины в среде, инокулированной лабораторным штаммом, трансформированным pJC2phleo. Данные, представленные закрашенными квадратиками, представляют собой концентрацию мочевины в среде, инокулированной лабораторным штаммом, трансформированным pJC2/DUR1,2phleo. Данные, представленные незакрашенными кружками, представляют собой поглощение при 600 нм для штамма pJC2phleo. Данные, представленные незакрашенными квадратиками, представляют собой поглощение при 600 нм для штамма pJC2/DUR1,2phleo. Левая ось Y означает концентрацию мочевины в мг/л. Правая ось Y означает поглощение при 600 нм. Ось Х означает часы после инокуляции.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В различных аспектах настоящее изобретение касается модификации генов и применения рекомбинантных генов. В этом контексте термин "ген" используют в соответствии с его обычным определением для обозначения группы связанных друг с другом последовательностей нуклеиновой кислоты. Модификация гена в контексте настоящего изобретения может включать модификацию любой из различных последовательностей, сцепленных в гене. Термин "сцепленный" означает, что отдельные последовательности взаимодействуют либо прямо, либо опосредованно для осуществления их предполагаемой функции, например опосредования или модуляции генной экспрессии. В качестве примера, взаимодействие сцепленных последовательностей может быть опосредовано белками, которые, в свою очередь, взаимодействуют с этими последовательностями.
Экспрессия гена обычно приводит к образованию полипептида, который кодируется частью гена. Обычно этот процесс включает в себя по меньшей мере два этапа: транскрипцию кодирующей последовательности с образованием РНК, которая сама по себе может обладать биологической активностью или которая может обеспечивать трансляцию части мРНК в полипептид. Хотя процессы транскрипции и трансляции не полностью поняты, считают, что транскрипция последовательности ДНК в мРНК контролируется несколькими участками ДНК. Каждый участок представляет собой последовательность оснований (т.е. последовательность нуклеотидных остатков, включающих аденозин (А), тимидин (Т), цитидин (С) и гуанидин (G)), которые располагаются в желательной последовательности.
Участки, которые обычно представлены в гене, включают в себя промоторную последовательность с участком, который обеспечивает связывание РНК-полимеразы и других транскрипционных факторов с промоторным сегментом ДНК. В норме РНК-полимераза движется вдоль промежуточного участка промотора до начала транскрипции в инициирующей транскрипцию последовательности, которая направляет РНК-полимеразу, для того чтобы начать синтез мРНК. Полагают, что РНК-полимераза начинает синтез мРНК на определенном расстоянии, например приблизительно от 20 до 30 оснований, выше последовательности, инициирующей транскрипцию. Вышеупомянутые последовательности обозначаются вместе как промоторный участок гена, который может включать другие элементы, которые модифицируют экспрессию гена. Такие сложные промоторы могут содержать одну или более последовательностей, которые вовлечены в индукцию или репрессию гена.
В контексте настоящего изобретения "промотор" обозначает нуклеотидную последовательность, которая способна опосредовать или модулировать транскрипцию интересующей нуклеотидной последовательности в желательной пространственной или временной системе и в желательной степени, когда транскрипционный регуляторный участок сцеплен с интересующей последовательностью. Транскрипционный регуляторный участок и интересующая последовательность являются "сцепленными", если эти последовательности функционально связаны, что позволяет опосредовать или модулировать транскрипцию интересующей последовательности транскрипционным регуляторным участком. В некоторых реализациях, будучи сцепленным, транскрипционный регуляторный участок может располагаться на той же цепи, что и интересующая последовательность. В некоторых реализациях транскрипционный регуляторный участок может располагаться на 5'-конце интересующей последовательности. В таких реализациях транскрипционный регуляторный участок может представлять собой непосредственно 5'-конец интересующей последовательности, или между этими участками могут существовать промежуточные последовательности. В некоторых реализациях транскрипционные регуляторные последовательности могут располагаться на 3'-конце интересующей последовательности. Сцепленность транскрипционного регуляторного участка и интересующей последовательности может требовать соответствующих молекул (таких как белки-активаторы транскрипции) для связывания с транскрипционным регуляторным участком, поэтому изобретение охватывает реализации, в которых предложены такие молекулы, либо in vitro, либо in vivo.
Последовательность ДНК, которая транскрибируется РНК-полимеразой в матричную РНК, обычно начинается с последовательности, которая не транслируется в белок и обозначается как 5'-нетранслируемый конец цепи мРНК, который может присоединяться к рибосоме. Эта нетранслируемая последовательность (CAP) может присоединяться после транскрипции гена. мРНК движется через рибосому до встречи со "стартовым кодоном". Стартовый кодон обычно представляет собой последовательность из трех оснований AUG; редко к инициации трансляции может приводить кодон GUG.
Следующую последовательность оснований в гене обычно называют кодирующей последовательностью или структурной последовательностью. Стартовый кодон предписывает рибосоме начать соединение последовательности аминокислот друг с другом пептидными связями с образованием полипептида, начиная с метионина, который образует аминотерминальный конец полипептида (метиониновый остаток затем может быть удален из полипептида другими ферментами). Основания, которые следуют за стартовым кодоном AUG, разделяются на группы из 3 оснований, каждая из которых представляет собой кодон. "Рамка считывания", которая устанавливает, каким образом основания распределяются в группы по 3 основания, определяется стартовым кодоном. Каждый кодон кодирует присоединение специфической аминокислоты к образующемуся полипептиду. Три кодона (UAA, UAG и UGA) обычно представляют собой "стоп"-кодоны; когда стоп-кодон достигает трансляционного механизма рибосомы, образовавшийся полипептид отделяется от рибосомы и последний предшествующий аминокислотный остаток становится карбокситерминальным концом полипептида.
Участок мРНК, который в моноцистронном гене расположен на 3'-конце от стоп-кодона, обозначают как 3'-нетранслируемый участок. Этот участок может вовлекаться в процессинг, стабильность и/или транспорт мРНК после ее транскрипции. Этот участок может включать также сигнал полиаденилирования, который распознается в клетке ферментом, добавляющим значительное количество остатков аденозина к молекуле мРНК для образования поли-А-хвоста.
Различные гены и последовательности нуклеиновой кислоты по настоящему изобретению могут представлять собой рекомбинантные последовательности. Термин "рекомбинантный" означает, что что-то рекомбинировало, так что в отношении конструкции нуклеиновой кислоты этот термин означает молекулу, которая состоит из последовательностей нуклеиновой кислоты, которые соединили вместе в некоторой точке или получили с помощью молекулярно-биологических методов. Термин "рекомбинантный", если он касается белка или полипептида, означает молекулу белка или полипептида, которую экспрессируют, используя рекомбинантную конструкцию нуклеиновой кислоты, созданную с помощью молекулярно-биологических методов. Термин "рекомбинантный", если он касается генетической комбинации, означает гамету, или потомство, или клетку, или геном с новыми комбинациями аллелей, которые не встречаются в природных родительских геномах. Рекомбинантные конструкции нуклеиновой кислоты могут включать нуклеотидную последовательность, которую лигируют или на которую воздействуют, для того чтобы ее можно было лигировать с последовательностью нуклеиновой кислоты, с которой она не лигирует в природе или с которой она лигирует в природе, но в другом положении. Поэтому ссылка на конструкцию нуклеиновой кислоты как на "рекомбинантную" указывает на то, что человек воздействует на молекулу нуклеиновой кислоты, используя методы генной инженерии.
Рекомбинантные конструкции нуклеиновой кислоты могут вводиться в хозяйскую клетку, например, путем трансформации. Такие рекомбинантные конструкции нуклеиновой кислоты могут включать последовательности, полученные из тех же видов хозяйских клеток или из других видов хозяйских клеток, которые были выделены и повторно введены в клетки хозяев.
Рекомбинантные последовательности нуклеиновой кислоты могут быть интегрированы в хозяйский клеточный геном либо в результате первичной трансформации хозяйских клеток, либо в результате последующей рекомбинации и/или этапов репарации. В качестве альтернативы, рекомбинантные последовательности могут сохраняться в виде внехромосомных элементов. Такие последовательности могут репродуцироваться, например, с помощью организма, такого как трансформированный дрожжевой штамм в качестве исходного штамма для процедур, связанных с улучшением штамма, осуществленных путем мутации, массового скрещивания или слияния протопластов. Полученные штаммы, которые сохраняют рекомбинантную последовательность по настоящему изобретению, считаются "рекомбинантными" в контексте использующегося здесь термина.
В различных аспектах изобретения, молекулы нуклеиновой кислоты могут быть химически синтезированы с помощью методов, которые раскрыты, например, у Itakura с соавт. в патенте US 4598049; Caruthers с соавт. в патенте US 4458066; и Itakura в патентах US 4401796 и 4373071. Такие синтетические нуклеиновые кислоты являются по своей природе "рекомбинантными" в соответствии с использующимся здесь термином (являясь продуктом последовательных этапов комбинирования составных частей молекулы).
Трансформация представляет собой процесс, благодаря которому генетический материал, который переносится клеткой, изменяется путем включения одной или более экзогенных нуклеиновых кислот в клетку. Например, дрожжи могут быть трансформированы с помощью множества протоколов (Gietz et al., 1995). Такая трансформация может происходить в результате включения экзогенной нуклеиновой кислоты в генетический материал клетки или благодаря изменению в эндогенном генетическом материале клетки, которое является результатом экспозиции клетки с экзогенной нуклеиновой кислотой. Трансформанты или трансформированные клетки являются клетками или потомками клеток, которые были генетически изменены вследствие поглощения экзогенной нуклеиновой кислоты. Поскольку эти термины используются здесь, они применяются и к потомкам трансформированных клеток, где желательное генетическое изменение было сохранено на протяжении последующих клеточных генераций, независимо от других мутаций или изменений, которые также могут присутствовать в клетках последующих генераций.
В альтернативных аспектах изобретение касается дрожжевых штаммов, применяющихся в ферментации для производства множества продуктов, таких как вино, пиво, тесто, этанол или уксус. В альтернативных реализациях изобретения могут применяться, например, дрожжевые штаммы S. cerevisiae, дрожжевые штаммы S. bayanus или дрожжевые штаммы Schizosaccharomyces. Трансформированные хозяйские клетки для применения в виноделии могут включать, например, штаммы S. cerevisiae или Schizosaccharomyces, такие как Bourgovin (RC 212 Saccharomyces cerevisiae), ICV D-47 Saccharamyces cerevisiae, 71B-1122 Saccharomyces cerevisiae, K.1V-1116 Saccharomyces cerevisiae, EC-1118 Saccharomyces bayanus, Vin13, Vin7, N96 и WE352. Существует множество коммерческих источников дрожжевых штаммов, таких как Lallemand Inc. из Монреаля (Квебек, Канада).
В некоторых реализациях аспектов изобретения можно использовать эндогенные или гетерологичные ферменты, обладающие мочевино-деградирующей активностью, например мочевино-карбоксилазной и аллофанатгидролазной активностью DUR.1,2. Эти ферменты, например, могут быть гомологичны DUR.1,2 или участкам DUR1,2, обладающим соответствующей активностью.
Степень гомологии между последовательностями (такими как нативный белок DUR1,2 или нативные последовательности нуклеиновой кислоты DUR1,2 и последовательность альтернативного белка или нуклеиновой кислоты для применения в изобретении) может быть выражена как процент идентичности в случае оптимального выравнивания последовательностей, которое подразумевает наличие точных пар между последовательностями. Оптимальное выравнивание последовательностей для сравнения идентичности может быть выполнено с использованием множества алгоритмов, таких как алгоритм поиска локальных гомологий Смита и Ватермана (Smith and Waterman, 1981, Adv. Appl. Math 2: 482), алгоритм выравнивания по гомологии Нидлемана и Вунша (Needleman and Wunsch, 1970, J.Mol. Biol. 48: 443), способ поиска сходства по Пирсону и Липману (Pearson and Lipman, 1988, Proc. Natl. Acad. Sci. USA 85: 2444), и компьютеризированные реализации этих алгоритмов (такие как GAP, BESTFIT, FAST и TFASTA в программном пакете Wisconsin Genetics Software Package, Genetics Computer Group, Мэдисон, Висконсин, США). Выравнивание последовательностей может осуществляться также с использованием алгоритма BLAST, описанного у Altschul с соавт. (J.Mol. Biol., 1990, 215: 403-10), использующего опубликованные параметры по умолчанию. Программное обеспечение для осуществления BLAST-анализа может быть получено из Национального Центра Биотехнологической Информации (National Center for Biotechnology Information, адрес в Интернете http://www.ncbi.nlm.nih.gov/). BLAST-алгоритм включает в себя первичную идентификацию пар последовательностей с высокой степенью сходства (HSP от англ. high scoring sequence pairs) путем идентификации коротких слов (группы символов) длиной W в запрашиваемой последовательности, которые либо образуют пары, либо удовлетворяют некоторому положительно оцениваемому пороговому показателю (score) Т при выравнивании со словом той же длины в последовательности из базы данных. Т обозначает пороговую оценку сходства родственных слов. Первоначальное "попадание" в соседнее слово является источником для инициации поисков с целью найти более длинные HSP. Поиски совпадения слов расширяются в обоих направлениях вдоль каждой последовательности, поэтому кумулятивная оценка выравнивания может увеличиваться. Расширение поиска слов в каждом направлении прекращается, когда встречаются следующие параметры: кумулятивная оценка выравнивания резко уменьшается благодаря параметру Х от ее максимально достигнутого значения; кумулятивная оценка стремится к нулю или ниже благодаря накоплению одного или более отрицатально-оцениваемых выравниваний остатков; или достижению конца одной из двух последовательностей. Параметры BLAST-алгоритма W, Т и Х определяют чувствительность и скорость выравнивания. BLAST-программы могут использовать длину слова по умолчанию (W), равную 11, выравнивание (В), равное 50, оценочной матрицы BLOSUM62 (Henikoff and Henikoff, 1992, Proc. Natl. Acad. Sci. USA 89: 10915-10919), ожидание (Е) равное 10 (которое может меняться в альтернативных реализациях до 1, или 0,1, или 0,01, или 0,001, или 0,0001; хотя значения Е, гораздо большие 0,1, могут не идентифицировать функционально сходные последовательности, полезно проверять удачные попытки с более низкой значимостью, значения Е, от 0,1 до 10, для коротких участков сходства), М=5, N=4, для нуклеиновых кислот сравнение обеих цепей. Для сравнения белков может быть использована по умолчанию программа BLASTP следующим образом: G=11 (штраф за открытие пропуска); Е=1 (штраф за расширение пропуска); Е=10 (величина ожидания, в этом параметре предполагают, что 10 "попаданий" с показателями, равными или лучшими, чем определенный показатель выравнивания S, появляются случайно в базе данных того же размера, что и искомая последовательность; величина Е может увеличиваться или уменьшаться для изменения строгости поиска); и W=3 (размер слова, по умолчанию составляет 11 для BLASTN, 3 для других blast-программ). Матрица BLOSUM определяет оценку вероятности для каждого положения при выравнивании, которое основано на частоте, с которой, как известно, замена встречается среди консенсусных блоков в пределах родственных белков. Матрицу замен BLOSUM62 (штраф за пропуск = 11; штраф за пропуск остатка = 1; соотношение лямбда = 0,85) используют по умолчанию в BLAST 2.0. Множество других матриц может быть использовано в качестве альтернативных вариантов к BLOSUM62, включая: РАМ30 (9,1,0.87); РАМ70 (10,1,0.87) BLOSUM80 (10,1,0.87); BLOSUM62 (11,1,0.82) и BLOSUM45 (14,2,0.87). Одно измерение статистического сходства между двумя последовательностями с использованием BLAST-алгоритма представляет собой наименьшую сумму вероятностей (P(N)), которая указывает на вероятность, с которой совпадение двух нуклеотидных или аминокислотных последовательностей будет происходить случайно. В альтернативных реализациях изобретения нуклеотидные или аминокислотные последовательности считаются, по существу, идентичными, если наименьшая сумма вероятностей по сравнению с тест-последовательностями составляет примерно менее 1, предпочтительно менее 0,1, более предпочтительно, менее 0,01 и наиболее предпочтительно менее 0,001.
Последовательности нуклеиновой кислоты по настоящему изобретению в некоторых реализациях могут быть, по существу, идентичными, например, белку DUR1,2 или последовательностям нуклеиновой кислоты DUR1,2. Значительная идентичность таких последовательностей может быть отражена в проценте идентичности при оптимальном выравнивании, который, например, может быть больше 50%, от 80% до 100%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95%, что в случае ген-определяющих субстратов может относиться к идентичности части ген-определяющего субстрата участку последовательности-мишени, где степень идентичности может облегчать гомологичное спаривание и рекомбинацию и/или репарацию. Альтернативным указанием на то, что две последовательности нуклеиновой кислоты являются, по существу, идентичными, является то, что эти две последовательности гибридизуются друг с другом в умеренно жестких или предпочтительно жестких условиях. Гибридизацию с фильтр-связанными последовательностями в умеренно жестких условиях можно осуществлять, например, в 0,5 М NaHPO4, 7%-ном додецилсульфате натрия (ДСН), 1 мМ ЭДТА при 65°С, и промывку в 0,2×SSC/0,l% ДСН при 42°С (см. Ausubel, et al. (eds), 1989, Current Protocols in Molecular Biology, Vol.1, Green Publishing Associates, Inc., and John Wiley & Sons, Inc., New York, p.2.10.3). Альтернативно, гибридизацию с фильтр-связанными последовательностями в жестких условиях можно осуществлять, например, в 0,5 М NaHPO4, 7% ДСН, 1 мМ ЭДТА при 65°С, и промывку в 0,1×SSC/0,1% ДСН при 68°С (см. Ausubel, et al. (eds), 1989, выше). Условия гибридизации могут быть модифицированы в соответствии с известными способами в зависимости от интересующей последовательности (см. Tijssen, 1993, Laboratory Techniques in Biochemistry and Molecular Biology - Hybridization - with Nucleic Acid Probes, Часть I, Глава 2 "Обзор принципов гибридизации и стратегии анализов с использованием нуклеотидных зондов", Elsevier, New York). Обычно выбирают такие жесткие условия, которые примерно на 5°С ниже, чем точка плавления специфической последовательности при определенной ионной силе и рН. Промывки для жесткой гибридизации могут длиться, например, в течение по меньшей мере 15 мин, 30 мин, 45 мин, 60 мин, 75 мин, 90 мин, 105 мин или 120 мин.
Хорошо известно в данной области, что в структуру полипептида, такого как DUR1,2, можно внести некоторые модификации и изменения без существенного изменения биологической функции этого пептида, для того чтобы получить биологически эквивалентный полипептид. В одном аспекте изобретения, белки, мочевино-карбоксилазная и/или аллофанатгидролазная активность могут включать белки, которые отличаются от нативной последовательности DUR1,2 консервативными заменами аминокислот. Использующийся здесь термин "консервативные замены аминокислот" касается замены одной аминокислоты на другую в заданном положении в белке, где замена может осуществляться без существенной потери соответствующей функции. При осуществлении таких изменений, замены похожих аминокислотных остатков могут быть произведены на основе относительного сходства боковых цепей заместителей, например их размера, заряда, гидрофобности, гидрофильности и тому подобного, и влияние таких замен на функцию белка может быть проанализировано с помощью стандартного исследования.
В некоторых реализациях могут быть выполнены консервативные замены аминокислот, где аминокислотный остаток замещен на другой аминокислотный остаток, имеющий похожую величину гидрофильности (например, в пределах значения плюс или минус 2,0), где нижеследующее может быть аминокислотой, имеющей показатель гидропатичности около -1,6, например, Туг (-1,3) или Pro (-1,6) соотносятся с аминокислотными остатками (как подробно описано в патенте US 4554101, включенном здесь посредством ссылки): Arg (+3,0); Lys (+3,0); Asp (+3,0); Glu (+3,0); Ser (+0,3); Asn (+0,2); Gin (+0,2); Gly (0); Pro (-0,5); Thr (-0,4); Ala (-0,5); His (-0,5); Cys (-1,0); Met (-1,3); Val (-1,5); Leu (-1,8); Ilе (-1,8); Тyr (-2,3); Phe (-2.5) и Тrр (-3,4).
В альтернативных реализациях могут быть выполнены консервативные замены аминокислот, где аминокислотный остаток замещен на другой аминокислотный остаток, имеющий похожую величину гидрофильности (например, в пределах значения плюс или минус 2,0). В таких реализациях каждому аминокислотному остатку может быть приписан показатель гидропатичности на основе его гидрофобности и заряда следующим образом: Ilе (+4,5); Val (+4,2); Leu (+3,8); Phe (+2,8); Cys (+2,5); Met (+1,9); Ala (+1,8); Gly (-0,4); Thr (-0,7); Ser (-0,8); Тrр (-0,9); Тyr (-1,3); Pro (-1,6); His (-3,2); Glu (-3,5); Gin (-3,5); Asp (-3,5); Asn (-3,5); Lys (-3,9) и Arg (-4,5).
В альтернативных реализациях могут быть выполнены консервативные замены аминокислот, где аминокислотный остаток замещен на другой аминокислотный остаток того же класса, где аминокислоты подразделяются на классы неполярных, кислых, основных и нейтральных аминокислот, как следует ниже: неполярные: Аlа, Val, Leu, Ile, Phe, Trp, Pro, Met; кислые: Asp, Glu; основные: Lys, Arg, His; нейтральные: Gly, Ser, Thr, Cys, Asn, Gin, Tyr.
В альтернативных реализациях консервативные замены аминокислот включают замены, основанные на представлениях о гидрофильности или гидрофобности, размере, или объеме, или заряде. Как правило, аминокислоты могут быть охарактеризованы как гидрофобные или гидрофильные главным образом в зависимости от свойств аминокислотной боковой цепи. Гидрофобная аминокислота имеет гидрофобность больше нуля, а гидрофильная аминокислота имеет гидрофильность менее нуля, исходя из нормированной шкалы гидрофобности Айзенберга с соавт. (Eisenberg et al., J.Mol. Bid. 179:125-142, 184). Генетически кодируемые гидрофобные аминокислоты включают Gly, Ala, Phe, Val, Leu, Ile, Pro, Met и Trp, и генетически кодируемые гидрофильные аминокислоты включают Thr, His, Glu, Gin, Asp, Arg, Ser и Lys. Негенетически кодируемые гидрофобные аминокислоты включают m-бутиламин, тогда как негенетически кодируемые гидрофильные аминокислоты включают цитруллин и гомоцистеин.
Гидрофобные или гидрофильные аминокислоты могут быть дополнительно разделены на основе свойств их боковых цепей. Например, ароматическая аминокислота представляет собой гидрофобную аминокислоту с боковой цепью, содержащей по меньшей мере одно ароматическое или гетероароматическое кольцо, которое может содержать один или более заместителей, таких как -ОН, -SH, -CN, -F, -Cl, -Br, -I, -NO2, -NO, -NH2, -NHR, -NRR, -C(O)R, -C(O)OH, -C(O)OR, -C(O)NH2, -C(O)NHR, -C(O)NRR и т.д., где R независимо представляет собой (С1-С6)-алкил, замещенный (С1-С6)-алкил, (С1-С6)-алкенил, замещенный (С1-С6)-алкенил, (C1-С6)-алкинил, замещенный (С1-С6)-алкинил, (С5-С20)-арил, замещенный (С5-С20)-арил, (С6-С26)-алкарил, замещенный (С6-С26)-алкарил, 5-20-членный гетероарил, замещенный 5-20-членный гетероарил, 6-26-членный алкгетероарил или замещенный 6-26-членный алкгетероарил. Генетически кодируемые ароматические аминокислоты включают Phe, Тyr и Trp.
Неполярная аминокислота представляет собой гидрофобную аминокислоту с боковой цепью, которая является незаряженной при физиологическом рН и имеет связи, в которых пара электронов, обобществленная двумя атомами, как правило, в равной степени удерживается каждым из двух атомов (т.е. боковая цепь является неполярной). Генетически кодируемые неполярные аминокислоты включают Gly, Leu, Val, Ile, Ala и Met. Неполярные аминокислоты могут быть дополнительно разделены с включением алифатических аминокислот, которые представляют собой гидрофобные аминокислоты, имеющие алифатическую углеводородную боковую цепь. Генетически кодируемые алифатические аминокислоты включают Ala, Leu, Val и Ilе.
Полярная аминокислота представляет собой гидрофильную аминокислоту с боковой цепью, которая является незаряженной при физиологическом рН, но имеет одну связь, в которой пара электронов, обобществленная двумя атомами, находится ближе к одному из атомов. Генетически кодируемые полярные аминокислоты включают Ser, Thr, Asn и Gin.
Кислая аминокислота представляет собой гидрофильную аминокислоту со значением рКа для боковой цепи менее 7. Кислые аминокислоты обычно имеют отрицательно заряженные боковые цепи при физиологическом рН благодаря потере иона водорода. Генетически кодируемые кислые аминокислоты включают Asp и Glu. Основная аминокислота представляет собой гидрофильную аминокислоту со значением рКа для боковой цепи больше 7. Основные аминокислоты обычно имеют положительно заряженные боковые цепи при физиологическом рН благодаря ассоциации с ионом гидроксония. Генетически кодируемые основные аминокислоты включают Arg, Lys и His.
Специалистам в данной области следует принять во внимание, что вышеупомянутые классификации не являются абсолютными и что аминокислоты могут быть отнесены к более чем одной категории. Кроме того, аминокислоты могут быть классифицированы на основе известного поведения и/или характерных химических, физических или биологических свойств, на основе специфических анализов или на сравнении с предварительно идентифицированными аминокислотами.
В различных аспектах изобретения мочевино-деградирующая активность хозяина может регулироваться таким образом, что она будет находиться на желательном уровне при условиях ферментации, таких как условия винной ферментации. Термин "условия ферментации" или "ферментирующие условия" означает условия, при которых организм, например, S. cerevisiae, производит энергию путем ферментации, т.е. условия культивирования, при которых происходит ферментация. В широком смысле, ферментация представляет собой совокупность анаэробных реакций, которые могут обеспечивать энергию для роста микроорганизмов при отсутствии кислорода. Энергия в процессе ферментации обеспечивается за счет фосфорилирования на уровне субстрата. В процессе ферментации органическое соединение (источник энергии) служит в качестве донора электронов, а другое органическое соединение является акцептором электронов. Для ферментации могут использоваться различные органические субстраты, например углеводы, аминокислоты, пурины и пиримидины. В одном аспекте изобретение касается таких организмов, как дрожжи, которые способны ферментировать углеводы с получением этилового спирта.
В винной ферментации условия культивирования муста (виноградного сусла) включают фруктовый сок, использующийся в качестве исходного сырья. Например, основными составляющими виноградного сока являются глюкоза (обычно примерно от 75 до 150 г/л), фруктоза (обычно примерно от 75 до 150 г/л), винная кислота (обычно примерно от 2 до 10 г/л), яблочная кислота (обычно примерно от 1 до 8 г/л) и свободные аминокислоты (обычно примерно от 0,2 до 2,5 г/л). Однако фактически любой фруктовый или сладкий растительный сок может быть преобразован в алкогольный напиток способом, в котором основной реакцией является превращение углевода в этиловый спирт.
Обычно винные дрожжи растут и ферментируют в диапазоне рН примерно от 4 до 4,5 и требуют минимальной активности воды около 0,85 (или относительной влажности около 88%). Ферментация может происходить спонтанно или может запускаться с помощью инокуляции мустом, который был предварительно ферментирован, и в этом случае сок может быть инокулирован популяциями дрожжей с концентрацией примерно от 106 до 107 КОЕ/мл сока. Муст может быть аэрирован для усиления дрожжевой популяции. После того как начнется ферментация, анаэробные условия, как правило, сохраняются благодаря быстрой продукции углекислого газа. Температура ферментации обычно находится в диапазоне от 10°С до 30°С, и длительность ферментационного процесса может составлять, например, от нескольких дней до нескольких недель.
В одном аспекте настоящего изобретения предложены дрожжевые штаммы, способные уменьшать концентрацию этилкарбамата в ферментированных алкогольных напитках. Например, изобретение может быть использовано для производства вин, имеющих концентрацию этилкарбамата менее 40 ppb (частей на миллиард), 35 ppb, 30 ppb, 25 ppb, 20 ppb, 15 ppb, 10 ppb или 5 ppb (или любое значение от 50 ppb до 1 ppb). В альтернативных реализациях изобретение может быть использовано для получения крепленых вин или дистиллированных спиртов, имеющих концентрацию этилкарбамата примерно менее 500 ppb, 400 ppb, 300 ppb, 200 ppb, 150 ppb, 100 ppb, 90 ppb, 80 ppb, 70 ppb, 60 ppb, 50 ppb, 40 ppb, 30 ppb, 20 ppb или 10 ppb (или любое целое значение от 500 ppb до 10 ppb).
В альтернативных реализациях изобретения предложены дрожжевые штаммы, которые способны поддерживать пониженную концентрацию мочевины в виноградном сусле. Например, концентрации мочевины могут поддерживаться примерно ниже 15 мг/л, 10 мг/л, 5 мг/л, 4 мг/л, 3 мг/л, 2 мг/л или 1 мг/л.
В одном аспекте изобретения предложены способы отбора природных мутантов ферментирующего организма, имеющих желательный уровень мочевино-деградирующей активности в условиях ферментации. Например, могут быть отобраны дрожжевые штаммы, у которых отсутствует АКР гена DUR1,2. В качестве примеров протоколов мутации и селекции дрожжей см. патент US 6140108 Mortimer с соавт., опубликованный 31 октября 2000 года. В таких способах дрожжевой штамм можно обработать мутагеном, таким как этилметансульфонат, азотистая кислота или гидроксиламин, который дает мутанты с заменами пар оснований. Мутанты с измененной мочевино-деградирующей активностью могут быть выделены, например, путем культивирования в подходящей среде.
В альтернативных реализациях может быть использован сайт-направленный мутагенез для изменения уровня мочевино-деградирующей активности в хозяине. Например, сайт-направленный мутагенез может быть использован для удаления АКР-опосредующих элементов из промотора DUR1,2. Например, GАТАА(G)-боксы в нативной промоторной последовательности DUR1,2, как показано на фиг.2, могут быть делегированы или модифицированы заменой. В одной реализации, например, один или оба GATAA-бокса могут быть модифицированы путем замены Т на G с получением последовательности ТАТАА. Методы сайт-направленного мутагенеза раскрыты, например, у Rothstein (1991); Simon и Moore (1987); Winzeler с соавт. (1999) и Negritto с соавт. (1997). В альтернативных реализациях гены, кодирующие Gln3p и Gatlp, которые опосредуют АКР в S. cerevisiae, могут быть также мутированы для модуляции АКР.
Относительная мочевино-деградирующая ферментативная активность дрожжевого штамма по настоящему изобретению может быть определена относительно нетрансформированного родительского штамма. Например, трансформированные дрожжевые штаммы по настоящему изобретению могут быть отобраны таким образом, чтобы иметь при условиях ферментации большую, чем родительский штамм, мочевино-деградирующую активность, или активность, которая несколько больше значения активности родительского штамма при тех же условиях ферментации, например, по меньшей мере 150%, 200%, 250%, 300%, 400% или 500% от активности родительского штамма. Аналогично, активность ферментов, экспрессируемых или кодируемых рекомбинантными нуклеиновыми кислотами по настоящему изобретению, может быть определена относительно нерекомбинантных последовательностей, из которых они получены, с использованием похожих кратных значений активности.
В одном аспекте изобретения может быть предложен вектор, содержащий рекомбинантную молекулу нуклеиновой кислоты, имеющую кодирующую последовательность DUR1,2 или ее гомологи, под контролем гетерологичной промоторной последовательности, которая опосредует регулируемую экспрессию полипептида DUR1,2. Для обеспечения таких векторов открытая рамка считывания (ОРС) DUR1, 2 из S. cerevisiae может быть встроена в плазмиду, содержащую экспрессионную кассету, которая будет управлять экспрессией рекомбинантного гена DUR.1, 2. Рекомбинантная молекула может быть введена в отобранный дрожжевой штамм для получения трансформированного штамма, имеющего измененную мочевино-деградирующую активность. В альтернативных реализациях экспрессия нативной гомологичной кодирующей последовательности DUR1,2 в хозяине, таком как S. cerevisiae, может осуществляться также путем замены нативного промотора другим промотором. Дополнительные регуляторные элементы могут быть использованы также для конструирования рекомбинантных экспрессионных кассет, в которых используют эндогенную кодирующую последовательность. Рекомбинантные гены или экспрессионные кассеты могут быть встроены в хромосомную ДНК хозяина, например, S. cerevisiae.
Промоторы для применения в альтернативных аспектах изобретения могут быть выбраны из подходящих нативных промоторов S. cerevisiae, например промоторов PGK.1 или CAR1. Такие промоторы могут быть использованы с дополнительными регуляторными элементами, например терминаторами PGK1 и CAR1. Могут использоваться многие нативные или рекомбинантные промоторы, где промоторы выбраны или сконструированы для опосредования экспрессии мочевино-деградирующих активностей, таких как активности DUR1,2, при выбранных условиях, например условиях виноделия.
В одном аспекте изобретения предложен способ ферментации углеводов, например способ ферментации вина с использованием хозяина, например дрожжевого штамма, трансформированного рекомбинантной нуклеиновой кислотой, которая модулирует мочевино-деградирующую активность хозяина. Например, АКР гена DUR1,2 можно регулировать таким образом, чтобы увеличить деградацию мочевины до аммиака и углекислого газа в дрожжевом штамме, применяющемся в виноделии. В соответствии с этим аспектом изобретения ферментация виноградного сусла дрожжевым штаммом может осуществляться таким образом, что приводит к образованию ограниченного количества этилкарбамата.
В одной реализации, используя стандартные рекомбинантные методы (Ausubel et al., 1995), клонировали флеомицин-резистентную генную кассету в дрожжевой челночный вектор с получением плазмиды, обозначенной pJC2phleo. Открытая рамка считывания (ОРС) гена DUR1,2 была амплифицирована с помощью ПЦР и клонирована в плазмиду pJC2phleo с получением вектора, обозначенного pJC2/DUR1,2phleo. Вектор pJC2/DUR1,2phleo является мультикопийной, эписомной челночной плазмидой S. cerevisiae-E.соli, в которой кодирующая последовательность DUR1,2 встроена между регуляторными последовательностями гена дрожжевой фосфоглицераткиназы (PGKI), так что промоторная и терминаторная последовательности PGK1 связаны с кодирующей последовательностью DUR1,2. Маркер LEU2 позволяет осуществить селекцию трансформированных дрожжевых клеток, которые ауксотрофны по лейцину. Плазмида pJC2/DUR1,2phleo содержит также ген Тn5Вlе, управляемый конститутивным дрожжевым промотором TEF1, и терминатор CYC1. Анализ трансформантов in vivo показал, что способность клеток S. cerevisiae, трансформированных плазмидой pJC/DUR1, 2phleo, расщеплять мочевину значительно увеличивалась по сравнению с клетками, трансформированными pJC2phleo, как было определено по концентрации мочевины в культуральной среде.
Хотя здесь раскрыты различные реализации изобретения, в рамках изобретения могут быть выполнены различные модификации в соответствии с общими представлениями специалистов в данной области. Такие модификации включают замену известных эквивалентов для любого аспекта изобретения с тем, чтобы достичь того же результата, по существу, тем же путем. В числовые диапазоны включены числа, определяющие этот диапазон. В описании слово "содержащий" используют как неограниченный термин, эквивалентный, по существу, фразе "включающий, но не ограниченный", и слово "содержит" имеет соответствующее значение. Цитирование ссылок здесь не следует истолковывать как допущение, что такие ссылки составляют предшествующий уровень техники настоящего изобретения. Все публикации, включая, но не ограничиваясь патентами и патентными заявками, процитированные в этом описании, включены здесь посредством ссылки, как если бы каждая отдельная публикация была специально и отдельно указана здесь путем включения ссылки и полностью изложена. Изобретение включает все реализации и варианты, в общих чертах описанные выше, со ссылкой на примеры и чертежи.
ПРИМЕРЫ
Материалы и методы:
Штаммы и среда
Геномную ДНК выделяли из штамма Saccharomyces cerevisiae TCY1 (МАТ-α, ura3, lys2), Для анализа экспрессионной кассеты in vitro использовали штамм Saccharomyces cerevisiae CNY400 (МАТ-α/МАТ-α, ura 3-52/ura3-52, leu2-Δ-l/leu-2-Δ-1TRP1/trp1-Δ-63). Использовали Линейную кассету ura3-PGK1p-DUR1,2-PGL1t-ura3, интегрировали в локус URA3 промышленных винных дрожжей UC Davis 522. Дрожжи культивировали на среде YPD, а трансформированные дрожжи культивировали в аэробных условиях при 30°С либо на твердой синтетической полной среде (0,17% yeast nitrogen base без сульфата аммония и аминокислот [Difco, Spares, NV] 2% глюкоза, 0,5% сульфат аммония и необходимые аминокислоты, кроме лейцина) или минимальной жидкой среде (0,17% nitrogen base без сульфата аммония и аминокислот и 2% глюкозы; аминокислоты добавляли при необходимости для компенсации аускотрофии, мочевину (0,1%), сульфат аммония (0,1%) или глютамин (0,1%) добавляли при необходимости в качестве источников азота). Для отбора трансформантов промышленных дрожжей на пластины агара добавляли флеомицин (100 мкг/мл).
Виноградный сок Рислинг (22 брикс, рН 2,85, аммоний 79 мг/л. FAN 112 мг/л) получали от Hawthorne Mountain Vineyards, Okanagan Valley, ВС, Канада. Сок обрабатывали 0,02 мл пектиназы (РЕС51, Scott Labs, Petaluma, Калифорния) в течение 3 ч при 40°С. Добавляли желатин до достижения конечной концентрации 0,2 г/л и инкубировали при 7°С в течение 12 ч до осаждения частиц. Сок затем подвергали стерильной фильтрации с использованием 0,22 мкм фильтра (Millipore, Billerica, Массачусетс) и замораживали при -20°С. SO2 в сок не добавляли. Перед инокуляцией в соке растворяли 2,5 г/л аргинина и доводили рН до 3,2 с помощью КОН. Сок подвергали стерильной фильтрации. (0,22 мкм фильтр, Millipore) Виноградный сок Шардонне (23,75 брикс, рН 3,41, аммоний 91,6 мг/л, FAN 309,6 мг/л) получали от Hawthorne Mountain Vineyards, Okanagan Valley. Сок подвергали стерильной фильтрации с помощью 0,22 мкм фильтра (Millipore) и добавляли 1,5 мг/л биотина к виноградному соку Шардонне, инокулированному модифицированными дрожжами.
Штамм Eschricchia coli FФ80dlacZΔM15Δ(lacZYA-argF) U19 recA 1 endA1 hsdR17 (rk-, mk+) phoA supE44λ- thi-1 gyrA96 relA1 выращивали в аэробных условиях на среде LB при 37°С. Трансформанты Eschrerichia coli выращивали на той же среде с добавлением 50 мкг/мл ампициллина и использовали для селекции плазмид. Использовали стандартные процедуры выделения плазмид и геномной ДНК и трансформации Е. coli (Ausubel et al., 1995) и S. cerevisiae (Gietz and Schiestl 1995).
Клонирование открытой рамки считывания DUR1,2 и конструирование экспрессионной кассеты
DUR1,2 амплифицировали с геномной ДНК S. cerevisiae TCY1 с использованием термостабильной ДНК полимеразы Ex-Taq (Takara Biochemicals, Otsu, Япония) Праймеры 5'-TTAAAAAAATGACAGTTAGTTCCGATACA-3' (стартовый кодон обозначен жирным) и 5'-TCGAAAAAGGTATTTCATGCCAATGTTATGAC-3' (антисмысловой стоп кодон обозначен жирным) были сконструированы таким образом, чтобы клонировать конечный продукт амплификации непосредственно в плазмиду pHVX2 между промотором PGK1 и сигнальной последовательностью терминатора (Volschenk et al., 1997) способом DI-TRSEC (Dietmaier и Fabry 1995). Это привело к деструкции сайтов клонирования плазмиды EcoRI и BglII.
Последовательность DUR1,2 гена конечной плазмиды устанавливали с помощью секвенирования (Mobix, McMaster University, Канада) и последовательность выведенного белка сравнили с двумя опубликованными последовательностями амидолиазы мочевины (Feldmann et al., 1994, Genbauffe and Cooper. 1991). Плазмиду PJC2 (фиг.6) конструировали, клонировав кассету устойчивости к флеомицину из pUT (Cayla, Toulouse, Франция) в сайты клонирования ВаmHI и SmaI PJC1 (Coulon 2001).
Нозерн блоттинг
Тотальную РНК выделили из выдерживавшихся в течение ночи культур S. cerevisiae CVY400, трансформированных pJC2 (CVY400:pJC2) или pHVX2 (CVY400: pHVX2), которые выращивали на минимальной среде, содержащей сульфат аммония в качестве источника азота, отделяли электрофорезом в 1% геле агароза-формальдегид (Ausubel et al. 1995), переносили и фиксировали на нейловновой мембране (Amersham Biosciences, Piscataway, Нью Джерси). Для двунитевых ПЦР проб использовали праймеры 5'-TTAGACTGCGTCTCCATCTTTG-3' и 5'-TGCTGGCTTTACTGAAGAAGAG-3' для DUR1,2 и 5'-GGCCGGATCCATGTCCATGTCCGGTAGAGGTA-3' и 5'-GGCCGAATTCTTAACCACCGAAACCGTATAAGG-3' для HHF1. Прегибридизацию, гибридизацию проб, отмывку и выявление выполняли с помощью системы прямого мечения и выявления нуклеиновых кислот CDP-Star AlkPhos (Amersham).
Вестерн блоттинг и биохимический анализ рекомбинантного белка амидолиазы мочевины, продуцируемого плазмидой
Штаммы Saccharomyces cerevisiae GVY400:pJC2 или CVY400:pHVX2 культивировали до достижения плотности А600 нм приблизительно 1,5 в минимальной среде, содержащей в качестве источников азота либо мочевину, либо аммониевые соли. Клетки промывали дважды в одном объеме 0,9% NaCl, ресуспендировали в 20 мМ фосфатном буфере с рН8, содержащем полную смесь ингибиторов протеаз (Roche Molecular Biochemicals, Basel, Швейцария) и разрушали с помощью 0,4-мм стеклянных гранул (BDH, Poole, Великобритания). Экстракты центрифугировали в течение 20 мин при 4°С. Концентрацию белка оценивали способом с применением бихинхониновой кислоты (Pierce Laboratories, Rockford, Израиль). Экстракты разделяли на 8% SDS-PAGE геле (полиакриламидный гель с додецилсульфатом натрия) и переносили на плоивинилфторидную мембрану (Bio-Rad, Hercules, Калифорния). Хемолюминесцентное выявление природных биотинилированных белков осуществляли, используя стрептавидин, коньюгированный с пероксидазой хрена (ВМ набор для хемолюминисцентного блоттинга биотин/стрептавидин, Roche Molecular Biochemicals, Basel). Второй SDS-РАGЕ гель окрашивали Кумасси-голубым, для подтверждения того, что загрузка белка была одинаковой.
Анализ активности амидолиазы мочевины проводили на тех же экстрактах, измеряя количество NH4+, выделившегося из мочевины. Аммоний реагирует со щелочным гипохлоритом и фенолом в присутствии катализатора - щелочного нитропруссида с образованием индофенола. Реакции гидролиза мочевины с высвобождением аммония и диоксида углерода инициировали добавлением 20 мкл неочищенного экстракта к 480 мкл реакционной смеси (29 мМ фосфатный буфер с рН 8, 5 мМ MgSO4, 80 мМ КСl, 4 мМ АТФ, 8 мМ КНСО3, мочевина от 0 до 10 мМ, предварительное нагревание при 30°С в течение 5 мин). Реакции гидролиза позволяли протекать в течение 20 мин, после чего ее останавливали, добавляя 1 мл раствора фенол-нитропруссида и 1 мл раствора щелочного гипохлорита (оба реактива от Sigma Diagnostics, St Louis, МО). Образцы инкубировали при 30°С в течение 30 мин, чтобы вызвать катализ образования индофенола из высвободившегося аммония нитропруссидом и щелочным гипохлоритом. Концентрация высвободившегося нитрофенола прямо пропорциональна поглощению индофенола при 570 нм. Коэффициент поглощения индофенола измеряли при используемых авторами условиях анализа, и специфические активности ферментов приведены как высвободившийся аммоний (нмоль)/мин/мг тотального белка. Результаты были скорректированы относительно фона вследствие использования неочищенного экстракта и добавления субстрата.
Конструирование и интергация линейной ura3-PGK1p-DUR1,2-PGL1t-ura3 кассеты в URA3 локус S.cerevisiae 522
Конструирование ura3-PGK1p-DUR1,2-PGL1t-ura3 кассеты осуществляли согласно Volschenk et al. (2004). Экспрессионную кассету амплифицировали с помощью праймеров
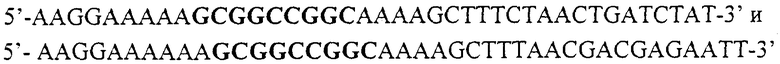 (сайты NotI обозначены жирным) и лигировали в pHVJH1 (Volchenk et al. 2004) с получением плазмиды pJC3. Переваривание pJC3 с помощью SrfI привело к вырезанию фрагмента ura3-PGK1p-DUR1,2-PGL1t-ura3 размером 9191 пар нуклеотидов, фланкированного последовательностями URA3 944 и 959 пар нуклеотидов. Интеграция ura3-PGK1p-DUR1,2-PGL1t-ura3 кассеты в URA3 локус промышленных винных дрожжей UC Davis 522 была выполнена путем ко-трансформации линейной фланкированной URA3 PGK1p-DUR1,2-PGL1t интеграционной кассеты и плазмиды pUT332ΔURA3, содеожащей ген T5ble для селекции устойчивости к флеомицину (Catingol et al. 1990, Wenzl et al., 1992). Плазмиду pUT332ΔURA3 сконструировали путем переваривания pUT332 рестриктазой BglII, удалением последовательностей URA3 и повторным лигированием плазмиды. Трансформанты Saccharomyces cerevisiae 522 высевали на агар YEC, содержащий 100 мкг/мл флеомицина, для того, чтобы минимизировать количество колоний, которые необходимо подвергать скринингу с помощью ПЦР. Инкубацию производили при 30°С в течение 72 ч. ПЦР колоний производили на устойчивых к флеомицину колониях с использованием следующих праймеров: 5'-AGCACAGCAATTAATACTTGATAAGAAGAGTATTGAG-3' и 5'-CACAAATTACATTTGCCTGTGATAAACCTAATCAAG-3', получив таким образом фрагмент размером 1059 пар нуклеотидов, соответствующих 5'-концу интегрированного фрагмента. Праймеры имели специфичность внутри и вне кассеты для того, чтобы определить, что интеграция произошла.
(сайты NotI обозначены жирным) и лигировали в pHVJH1 (Volchenk et al. 2004) с получением плазмиды pJC3. Переваривание pJC3 с помощью SrfI привело к вырезанию фрагмента ura3-PGK1p-DUR1,2-PGL1t-ura3 размером 9191 пар нуклеотидов, фланкированного последовательностями URA3 944 и 959 пар нуклеотидов. Интеграция ura3-PGK1p-DUR1,2-PGL1t-ura3 кассеты в URA3 локус промышленных винных дрожжей UC Davis 522 была выполнена путем ко-трансформации линейной фланкированной URA3 PGK1p-DUR1,2-PGL1t интеграционной кассеты и плазмиды pUT332ΔURA3, содеожащей ген T5ble для селекции устойчивости к флеомицину (Catingol et al. 1990, Wenzl et al., 1992). Плазмиду pUT332ΔURA3 сконструировали путем переваривания pUT332 рестриктазой BglII, удалением последовательностей URA3 и повторным лигированием плазмиды. Трансформанты Saccharomyces cerevisiae 522 высевали на агар YEC, содержащий 100 мкг/мл флеомицина, для того, чтобы минимизировать количество колоний, которые необходимо подвергать скринингу с помощью ПЦР. Инкубацию производили при 30°С в течение 72 ч. ПЦР колоний производили на устойчивых к флеомицину колониях с использованием следующих праймеров: 5'-AGCACAGCAATTAATACTTGATAAGAAGAGTATTGAG-3' и 5'-CACAAATTACATTTGCCTGTGATAAACCTAATCAAG-3', получив таким образом фрагмент размером 1059 пар нуклеотидов, соответствующих 5'-концу интегрированного фрагмента. Праймеры имели специфичность внутри и вне кассеты для того, чтобы определить, что интеграция произошла.
Саузерн блоттинг вьполняли с использованием геномной ДНК, переваренной рестриктазой BglII для подтверждения интеграции ura3-PGK1p-DUR1,2-PGL1t-ura3 линейной кассеты в локус URA3. Использовали пробу URA3 927 пар нуклеотидов и DUR1,2 736 пар нуклеотидов. Пробу DUR1,2 генерировали с помощью ПЦР с использованием плазмиды pDUR1,2 и праймеров DUR1,2probe5 (5'-TTAGACTGCGTCTCCATCTTTG-3') и DUR1,2F (5'-TGCTGGCTTTACTGAAGAAGAG-3').
Потеря устойчивости к флеомицину у трансформантов
Изолировали геномную ДНК из 522EC- штамма 522, в который интегрировали линейную кассету ura3-PGK1p-DUR1,2-PGL1t-ura3, и хозяйского штамма 522, переваривали ее EcoRI и разделяли электрофорезом на 0,7% агарозном геле. После электрофореза проводили блоттинг ДНК на положительно заряженные мембраны Nylon и фиксировали. Саузерн блоттинг выполняли с использованием пробы Tn5Ble, полученной с помощью ПЦР с использованием pUT332ΔURA3 в качестве матрицы (использовалась для ко-трансформации) и праймеров PhleoF (5'-AATGACCGACCAAGCGACG-3' и PleoR (5'-ATCCTGGGTGGTGAGCAG-3'). Второй Саузерн-блоттинг выполнили с использованием пробы bla, полученной с помощью ПЦР с использованием pUT332ΔURA3 в качестве матрицы и праймеров AmpRF (5'-TTGCGGCATTTTGCCTTCCT-3') и AmpRF (5'-GTTGCCGGGAAGCTAGAGTA-3').
Количественное определение этилкарбамата в вине с помощью микровыделения твердой фазы (SPME-solid phase micro emission) и газовой хроматографии - спектрометрии
Для стимулирования продукции этилкарбамата вино Шардонне нагревали до 70°С в течение 48 ч. Пробы вина 10 мл переносили пипеткой в 20 мл виал для проб. Туда помещали маленький груз для магнитной мешалки, добавляли 3 г NaCl и закрывали виал политетрафторэтиленовой/силиконовой крышкой. Виал помещали на мешалку и уравновешивали при перемешивании в течение 15 мин. Волокно для SPME (65 мкм карбовакс/дивинилбензен кондиционировали при 250°С в течение 39 мин перед использованием. После уравновешивания пробы волокно помещали в верхнее пространство виала. Спустя 30 мин волокно удаляли из виала для проб и помещали в устройство для инъекций на 15 мин. Перед каждым пробегом пробы осуществляли пустой пробег. Количественное определение выполняли с помощью внешнего стандартного способа.
Стандартный стоковый раствор этилкарбамата (Sigma-Aldrich, Milwaukee, Висконсин) с концентрацией 0,1 мг/мл приготовили в дистиллированной воде, содержащей 12 об.% этанола и 1 мМ винной кислоты при рН 3,1. Стандарты для калибровки получали с концентрациями этилкарбамата 5, 10, 20, 40 и 90 мкг/л. Стандартные растворы хранили в холодильнике при 4°С.
Количественное определение этилкарбамата в вине проводили с помощью Agilent 6890 GC, интерфейсом для которого был селективный детектор массы 5973N. Использовали открытую трубчатую колонну со сплавленным оксидом кремния. DBWAX, толщина 0,25 мкм. (J&W Scientific, Folsom, Калифорния). Газ-носитель представлял собой гелий сверхвысокой чистоты с постоянным потоком 36 см/с. Температура инжектора и подающей линии была установлена на 250°С. Температура печи была установлена первоначально на 70°С на 2 мин, потом ее поднимали до 180°С и поддерживали 3 минуты. Затем изменение температуры запрограммировали таким образом, чтобы она возрастала на 20°С в минуту до 220°С, и на этом уровне температуру поддерживали в течение 15 мин. Общее время пробега составляло 35,75 мин. Инжекцию проводили непрерывно в течение 5 мин (5 мл/мин). Детектор массы работал в режиме селективного мониторинга ионов с ионизацией от удара электрона. Температура в детекторе составляла 150°С, а температура в источнике детектора 230°С. Задержка растворителя составляла 8 мин. Мониторинг конкретных ионов 44, 62, 74 и 89 осуществляли со временем пребывания 100 миллисекунд. Для количественного определения использовали массу 62 в спектре массы аутентичного стандарта этилкарбамида.
Результаты
Конститутивная, функциональная экспрессия DUR1,2
Saccharomyces cerevisiae CVY 400 (диплоидный) трансформировали плазмидой pJC2, содержащей ген DUR1,2 S. cerevisiae под контролем сигнальных последовательностей промотора и терминатора DUR1,2 S. cerevisiae. Таким образом, трансформированные дрожжевые клетки содержали три копии гена DUR1,2 - две копии нативного гена в хромосоме под контролем нативного промотора DUR1,2, который подвергается азотной катаболитной репрессии (АКР), и плазмидную копию DUR1,2, конститутивно экспрессирующуюся под контролем промоторных и терминаторных сигнальных последовательностей PGK1 в JC2.
Анализ с помощью Нозерн блоттинга подтвердил чувствительность к АКР экспрессии хромосомных копий DUR1,2, при этом рекомбинантный транскрипт присутствовал в CVY:400:pJC2 в большом количестве, вне зависимости от АКР. Анализ с помощью Вестерн блоттинга показал наличие биотинилированного белка, похожего по размеру на природную амидолизу мочевины в биотинилированном состоянии (202 кДа) только в клетках, экспрессирующих рекомбинантный транскрипт (GVY400:pJC2), но этот белок отсутствовал в контрольных клетках (GVY400:pHVX2), что подверждало присутствие рекомбинантного белка и отсутствие эндогенной амидолиазы мочевины в клетках, выращиваемых в условиях АКР.
Измерение амидолиазы мочевины на экстрактах целых клеток, которые выращивали в условиях АКР, подтвердило данные экспрессии. Как и ожидалось, эндогенная активность амидолиазы мочевины была снижена до фонового уровня у клеток, которые выращивали в условиях АКР, в то время как активность рекомбинантного фермента была выше в 10 раз, причем вычисленное значение Vmax составляло 53,2 ммоль высвободившегося аммония в минуту на миллиграмм белка. Константа аффинности, вычисленная для рекомбинантного фермента (Km на 0,41 мМ мочевины) согласовалась с константой, определенной для эндогенного фермента (Km на 0,39 мМ мочевины) и с ранее опубликованной константой для амидолиазы мочевины (Km на 0,39 мМ мочевины) (Whitney and Cooper 1973), что указывало на то. что мочевино-деградирующая активность рекомбинантной амидолиазы мочевины неотличима от ее природной активности. Представленные данные свидетельствуют о том, что находящийся в рекомбинантной плазмиде ген DUR1,2 под контролем сигнальных последовательностей промотора и терминатора PGK1 (pJC2) является полностью функциональным в клетках S.cerevisiae, выращиваемых в лабораторной среде, препятствующей экспрессии нативного гена DUR1,2. Поскольку плазмиды в S. cerevisiae являются нестабильными, авторы настоящего изобретения интегрировали линейную кассету ura3-PGK1p-DUR1,2-PGL1t-ura3 в URA3 локус штамма промышленных винных дрожжей 522. Полная кассета для интеграции, включая гомологичные ura3-фланкирующие области и экспрессионную кассету DUR1,2, была получена из донорских штаммов S. cerevisiae. Сравнение последовательности рекомбинантного белка Dur1,2 с опубликованными ранее последовательностями (Fieldman et al., 1994, Genbauff and Cooper 1991) показало, что 1835 аминокислот белка Dur1,2 не совпадают с одной из опубликованных последовательностей. Эти различия вполне могут быть следствием генетического полиморфизма. Однако нельзя исключать возможности того, что данные аномалии появились вследствие ошибок при ПЦР амплификации фрагментов ДНК, а также того, что эти различия могут быть следствием ошибок в опубликованных последовательностях. Однако эти изменения не затрагивают функционирование PGK1p-DUR1,2-PGL1t экспрессионной кассеты, поскольку она была полностью функциональна и мочевина активно разлагалась штаммом 522EC-.
В штамме S. cerevisiae 522EC- снижено образование мочевины и этилкарбамата
Образование и разложение мочевины in vivo в виноградном сусле Рислинг с добавлением 2,5 г/л аргинина штаммом 522 дикого типа и 522EC- происходило следующим образом.
Штамм дикого типа 522 образовал 115,09 (±5,91) мг/л мочевины в течение 3 дней, после чего произошло разложение мочевины до уровня содержания 42,21 (±3,33) мг/л. В то же время, генетически модифицированный штамм 522EC- образовал 27,91 (±5,82) мг/л мочевины за три дня, после чего произошло разложение мочевины до уровня содержания 4,08 (±1,79) мг/л вина. Таким образом, конечное количество образовавшейся мочевины было в случае рекомбинантного штамма 522EC- на 90,3% по сравнению с штаммом 522 дикого типа.
Количество этилкарбамата, образованного штаммами 522 дикого типа и 522EC- в виноградном сусле Шардонне, приведено в таблице. Штамм дикого типа образовал 87,85 мкг/л (87,85 ppb) этилкарбамата, в то время как штамм 522EC- образовал 9.61 мкг/л (9,61 ppb) этилкарбамата, то есть меньше на 89,1%.
Следует также отметить что цвет, запах и вкусовые качества вина Шардонне, полученного с помощью клеток штамма UC Davis 522EC-, не отличались от таковых вина, полученного с помощью клеток штамма UC Davis 522.
Источники информации
Ausubel F.М., Brent R., Kingston R.E., Moore D.D., Seidman J.G., Smith J.A., and Struhl K., editors. 1999. Short Protocols in Molecular Biology, 4"Ed. John Wiley and Sons, N.Y.
Ausubel F.M., Brent R., Kingston R.E., Moore D.D., Seidman J.G., Smith J.A., Struhl К. eds. Current Protocols in Molecular Biology. 1987-2000. John Wiley and Sons, Inc.
Dietmaier W. and Pabry S. (1995). Protocol:!/tri nucleotide Sticky End Cloning. Boerhinger Mannheim PCR Application Manual.
Genbauffe F.S., and Cooper T.G. 1991. The urea amidolyase (DUR1,2) gene of Saccharomyces cerevisiae. DNA Seq. 2 (1): 19-32.
Gietz R.D., Schiest R.H., Willems A.R., Woods R.A.: Studies on the transformation of intact yeast cells by the LiAc/SS-DNA/PEG procedure. Yeast 11: 355-360 (1995).
Henschke P.A., and Jiranek V. 1993. Yeasts: metabolism of nitrogen compounds. InG. H. Fleet, editor. Wine Microbiology and Biotechnology. 77-164, Switzerland: Harwood Academic Publishers.
Hoffrnann W. 1985 Molecular characterization of the CAN1 locus in Saccharomyces cerevisiae: a transmembrane protein without N-terminal hydrophobic signal sequence. J. Biol. Chem. 260 (21): 11831-11837.
Jauniaux J.С., and Grenson M. 1990. GAP1, the general amino acid permease gene of Saccharomyces cerevisiae: nucleotide sequence, protein similarity with the other bakers yeast amino acid permeases, and nitrogen catabolite repression. Eur.J. Biochem. 190 (1): 39-44.
Maitz G.S., Haas, E.M. and Castric, P.A. Purification and properties of the allophanate hydrolase from Chlamydomonas reinhardii. Biochim. Biophys. Acta 714 (1982) 486-491.
Middelhoven W.J. 1964. The pathway of arginine breakdown in Saccharomyces cerevisiae. Biochem. Biophys. Acta. 156: 650-652.
Mirvish S.S. 1968. The carcinogenic action and metabolism of urethan and n-hydroxyurethan Adv. Cancer Res. 11: 1-42.
Negritto M.T., Wu X., Kuo T., Chu S., Bailis A.M.: Influence of DNA sequence identity on efficiency of targeted gene replacement. Mol Cell Biol 17: 278-286 (1997).
Roon R.J. and Levenberg B. ATP-Urea amidolyase (ADP) (Candida utilis). Methods Enzymol. 17A (1970) 317-324.
Roon R.J. and Levenberg B. Ureaamidolyase. I. Properties of the enzyme from Candida utilis. J.Biol. Chem. 247 (1972) 4107-4113.
Rothstein R.: Targeting, disruption, replacement, and allele rescue: integrative DNA transformation in yeast. Methods Enzymol. 194: 281-301 (1991).
Simon J.R., Moore P.D. Homologous recombination between single-stranded DNA and chromosomal genes in Saccharomyces cerevisiae. Mol Cell Biochem 7, pp.2329-2334. 1987.
Sumrada R.A., and Cooper T.G. 1982. Urea carboxylase and allophanate hydrolase are components of a multifunctional protein in yeast. J. Biol. Chem. 257 (15): 9119-9127.
Volschenk H., М.Viljoen, M.Grober, J.Bauer, F.F. Subden, R.E. Denayrolles, M. Lonvaud, A. Young, R.A. & H.J.J. van Vuuren. 1997. Engineering a pathway for malate degradation in Saccharomyces cerevisiae. Nature Biotechnol. 15: 253-257.
Winzeler E.A., Shoemaker D.D., Astromoff A., Liang H., Anderson K., Andre B., Bangham R., Benito R., Boeke J.D., Bussey H., Chu A.M., Connelly C., Davis K., Dietrich F., Dow S.W., E.l. Bakkoury, M. Foury, F. Friend, S.H. Gentalen, E. Giaever, G. Hegemann, J.H. Jones, T. Laub, M. Liao, H. Davis, RW: Functional characterization of the S. cerevisiae genome by gene deletion and parallel analysis. Science 285: 901-906 (1999).
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pPBS-St9, КОДИРУЮЩАЯ ПОЛИПЕПТИД СОМАТОТРОПИНА, И ШТАММ ДРОЖЖЕЙ SACCHAROMYCES CEREVISIAE ДЛЯ ПРОДУКЦИИ РЕКОМБИНАНТНОГО СОМАТОТРОПИНА | 2011 |
|
RU2465315C1 |
| КОМПОЗИЦИИ И СПОСОБЫ СНИЖЕНИЯ УРОВНЯ HS В ФЕРМЕНТИРОВАННЫХ НАПИТКАХ | 2008 |
|
RU2476590C2 |
| ФУНКЦИОНАЛЬНОЕ УЛУЧШЕНИЕ МИКРООРГАНИЗМОВ ДЛЯ МИНИМИЗАЦИИ ПРОДУКЦИИ АКРИЛАМИДА | 2011 |
|
RU2603061C2 |
| ГЕНЫ АГГЛЮТИНАЦИИ, ДРОЖЖИ | 1994 |
|
RU2159807C2 |
| Рекомбинантный фрагмент ДНК, кодирующий альфа-фетопротеин (АФП) человека, содержащий "медленные" кодоны, кодирующие лейцин, экспрессионная плазмида, содержащая указанный фрагмент, клетка Saccharomyces cerevisiae, трансформированная указанной плазмидой, и способ получения рекомбинантного АФП человека | 2015 |
|
RU2617943C2 |
| СПОСОБ ПОЛУЧЕНИЯ КСИЛИТА | 1993 |
|
RU2142999C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВ В ТРАНСФОРМИРОВАННЫХ ДРОЖЖЕВЫХ КЛЕТКАХ | 1999 |
|
RU2238323C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТОИНА | 2015 |
|
RU2686614C2 |
| КЛЕТКИ-ХОЗЯЕВА И СПОСОБЫ ИСПОЛЬЗОВАНИЯ | 2014 |
|
RU2663587C2 |
| УРЕОГИДРОЛАЗЫ В КАЧЕСТВЕ ДОМИНАНТНЫХ СЕЛЕКТИВНЫХ МАРКЕРОВ У ДРОЖЖЕЙ | 2015 |
|
RU2702766C2 |
Изобретение относится к биотехнологии, а именно к применению трансформированной клетки Saccharomyces cerevisiae, принадлежащей к штамму, применяющемуся в виноделии, способной к увеличенной по сравнению с нетрансформированной клеткой указанного штамма деградации мочевины в условиях ферментации виноградного сусла. Клетка трансформирована рекомбинантной нуклеиновой кислотой, содержащей последовательность, включающую открытую рамку считывания, гомологичную открытой рамке считывания DUR1,2 и кодирующую белок, имеющий мочевино-деградирующую ферментативную активность, и промотор, подходящий для опосредования экспрессии белка, имеющего мочевино-деградирующую ферментативную активность, в условиях ферментации виноградного сусла. Изобретение позволяет получить вино, не отличающееся по своим органолептическим свойствам от вина, полученного с помощью нетрансформированной клетки. 7 н. и 6 з.п. ф-лы, 7 ил., 1 табл.
1. Способ ферментации виноградного сусла для получения вина, получаемого ферментацией с применением дрожжей, включающий выдерживание при условиях ферментации виноградного сусла трансформированной клетки Saccharomyces cerevisiae, принадлежащий к штамму, применяющемуся в виноделии, при котором указанная клетка трансформирована рекомбинантной нуклеиновой кислотой, содержащей последовательность, включающую открытую рамку считывания, гомологичную открытой рамке считывания DUR1,2 и кодирующую белок, имеющий мочевино-деградирующую ферментативную активность, и промотор, подходящий для опосредования экспрессии белка, имеющего мочевино-деградирующую ферментативную активность, в условиях ферментации виноградного сусла.
2. Способ по.1, при котором вино имеет концентрацию этилкарбамата менее 30 ррb.
3. Клетка Saccharomyces cerevisiae, принадлежащая к штамму, применяющемуся в виноделии, способная к увеличенной, по сравнению с нетрансформированной клеткой указанного штамма, деградации мочевины в условиях ферментации виноградного сусла, трансформированая рекомбинантной нуклеиновой кислотой, содержащей последовательность, включающую открытую рамку считывания, гомологичную открытой рамке считывания DUR1,2 и кодирующую белок, имеющий мочевино-деградирующую ферментативную активность, и промотор, подходящий для опосредования экспрессии белка, имеющего мочевино-деградирующую ферментативную активность, в условиях ферментации виноградного сусла.
4. Трансформированная клетка по п.3, характеризующаяся тем, что ее применяют для получения вина.
5. Трансформированная клетка по п.4, характеризующаяся тем, что вино имеет концентрацию этилкарбамата менее 30 ppb.
6. Применение трансформированной клетки по п.3 для получения вина, получаемого ферментацией с применением дрожжей.
7. Применение по п.6, где вино имеет концентрацию этилкарбамата менее 30 ppb.
8. Способ получения вина, получаемого ферментацией с применением дрожжей, включающий выдерживание трансформированной клетки по п.3 в условиях ферментации виноградного сусла.
9. Способ по п.8, при котором вино имеет концентрацию этилкарбамата менее 30 ppb.
10. Вино, содержащее трансформированную клетку по п.3.
11. Вино по п.10, имеющее концентрацию этилкарбамата менее 30 ppb.
12. Способ получения рекомбинантной клетки Saccharomyces cerevisiae, принадлежащей к штамму, применяющемуся в виноделии, для получения вина с пониженным содержанием этилкарбамата по сравнению с вином, получаемым ферментацией с применением нетрансформированной клетки указанного штамма, включающий трансформацию клетки Saccharomyces cerevisiae, принадлежащей к штамму, применяющемуся в виноделии, при котором клетку трансформируют рекомбинантной нуклеиновой кислотой, содержащей последовательность, включающую открытую рамку считывания, гомологичную открытой рамке считывания DUR 1,2 и кодирующую белок, имеющий мочевино-деградирующую ферментативную активность, и промотор, подходящий для опосредования экспрессии белка, имеющего мочевино-деградирующую ферментативную активность, в условиях ферментации виноградного сусла.
13. Применение выделенной последовательности нуклеиновой кислоты для трансформации клетки Saccharomyces cerevisiae, принадлежащей к штамму, применяющемуся в виноделии, для получения клетки Saccharomyces cerevisiae, позволяющей получить вино с пониженным содержанием этилкарбамата по сравнению с вином, получаемым ферментацией с применением с нетрансформированной клетки указанного штамма, где выделенная последовательность нуклеиновой кислоты содержит кодирующую последовательность, которая на 80% идентична нативной кодирующей последовательности DUR1,2, при оптимальном выравнивании, и кодирует белок, имеющий мочевино-деградирующую ферментативную активность, причем кодирующая последовательность связана с промоторной последовательностью, которая не опосредует азотную катаболитную репрессию этой кодирующей последовательности в хозяйской клетке Saccharomyces cerevisiae в условиях ферментации виноградного сусла.
| JP 05244959 A, 24.09.1993 | |||
| KATSUHIKO KITAMOTO, Mutant isolation of non-urea producing sake yeast by positive selection, Journal of fermentation and bioengineering, vol.75, №5, 359-363, 1993 | |||
| Способ сбраживания углеводов до этанола | 1990 |
|
SU1794085A3 |
Авторы
Даты
2009-08-10—Публикация
2002-11-06—Подача