Изобретение относится к аналитической химии, а именно к способам определения йода, и может быть использовано для его количественного анализа в различных объектах, например в водах (питьевых, поверхностных, артезианских, расфасованных минеральных и др.), в пищевых продуктах, продовольственном сырье.
Известны разнообразные методы определения йода и йодид-ионов.
Министерством здравоохранения РФ от 1.03.2002 г. рекомендован титриметрический метод анализа водных объектов для определения в них содержания йода в диапазоне концентраций 0,01-1 мг/дм3 [Методические указания. Определение йода в воде. / Министерство здравоохранения РФ, 1 марта 2002 г.]. Метод основан на окислении йодидов до йодатов в кислой среде бромной водой с восстановлением последних до свободного йода. Образовавшийся йод титруют раствором тиосульфата натрия в присутствии крахмала как индикатор. Нижний предел измерения йода в анализируемой пробе 10 мкг.
Этот метод имеет определенные недостатки. Для концентрирования проб рекомендуется упаривание проб и прокаливание сухих остатков, что удлиняет анализ. Для извлечения йода из прокаленного осадка требуется экстракция его этиловым спиртом, которую проводят в 2 приема. Полученный экстракт выпаривают на водяной бане, просушивают в сушильном шкафу и прокаливают. После растворения остатка ведут окисление йодидов, применяя бромную воду, т.е. эти операции являются длительными и связаны с использованием токсичного вещества - бромной воды. Определению мешают другие галогены.
Разработана методика определения валентных форм йода в воде в виде йодид-ионов на ртутно-пленочных электродах методом катодной инверсионной вольтамперометрии [Носкова Г.Н., Толмачева Т.П., Заичко А.В., Мерта А.Н. Определение валентных форм йода в воде методом катодной инверсионной вольтамперометрии. Тезисы докладов VII конференции «Аналитика Сибири и Дальнего Востока», 2004 г.]. Валовое содержание йода определяют на фоне 0,4М муравьиной кислоты (Еэ=-0,10 В, tэ=10-60 с). Для восстановления йодат-ионов и йодорганических соединений до йодид-ионов и устранения мешающего влияния растворенных органических веществ, адсорбирующихся на поверхности электрода, пробу подвергают УФ-облучению в течение 600 с.
При определении йодид-ионов данным методом необходимо предварительное удаление растворенного кислорода, для чего используют инертный газ.
Недостатки этого метода - сложность оборудования, необходимого для УФ-облучения анализируемых проб, для деаэрации проб инертным газом, для выполнения метода инверсионной вольтамперометрии. Известны экстракционно-фотометрические методы определения йодид-ионов в виде окрашенных ионных пар, которые образуются с основными красителями, например, метиловым фиолетовым (экстракция бензолом или толуолом) или ферроином (экстракция нитробензолом) [З.Марченко. Фотометрическое определение элементов (перевод с польского). М.: Мир, 1971, 502 с.].
Недостаток этих методов - работа с токсичными экстрагентами типа бензол, нитробензол, толуол.
Известен фотометрический метод определения йодид-ионов, основанный на цветной реакции с крахмалом; предварительно йодид-ионы окисляют до йода, применяя в качестве окислителей нитраты или железо (III) [З.Марченко. Фотометрическое определение элементов (перевод с польского). М.: Мир, 1971, 502 с.2].
Чувствительность этого метода невелика, но возрастает в несколько раз, если окислять йодиды сначала до йодатов в кислой среде бромной водой, после чего провести восстановление последних до свободного йода с помощью йодида калия
I-+3Br2+3H2O=IO3 -+6H++6Br-
KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O
Избыток брома удаляют кипячением или связывают фенолом с образованием трибромфенола. Молярный коэффициент поглощения йодкрахмального комплекса равен 1,08·105 при λ=590 нм.
Описанный метод имеет определенные недостатки. Они связаны с использованием сильно токсичных веществ - бромной воды и фенола. Удаление избытка брома кипячением требует достаточно много времени.
Задачей изобретения является упрощение фотометрического способа определения йодид-ионов: сокращение числа операций и времени определения, а также отказ от использования токсичных веществ.
Поставленная задача решается тем, что способ турбидиметрического определения йодит-ионов заключается в фотометрировании суспензии йодида серебра, выделенной из анализируемого раствора, осаждение ведут в аммиачной среде (pH=9-11) в присутствии хлорид-ионов и измеряют оптическую плотность при длине волны 380 нм.
Сущность способа определения йодид-ионов заключается в переведении этих ионов в малорастворимые соединения AgI (ПPAgI=1,1·10-6). Наличие в природной воде хлорид-ионов, в концентрациях гораздо больших, чем йодид-ионов, мешает определению последних, т.к. хлорид-ионы также образуют осадок AgCl
(ПPAgCl=1,8·10-10), поэтому осаждение Agl проводили в присутствии 25%-ного раствора аммиака, тем самым, препятствуя одновременному выпадению осадка AgCl. Хлорид серебра в отличие от йодида серебра растворим в гидроксиде аммония с образованием комплексной соли [Ag(NH3)2]Cl(Kн[Ag(NH3)2]=9,3·10-8), поэтому предусмотрено добавление в анализируемый раствор 25%-ного раствора NH4OH (pH=9-11) для растворения AgCl и спирта в качестве стабилизатора.
Измеряют оптическую плотность полученной суспензии йодида серебра на фотоколориметре или спектрофотометре.
Для определения длины волны максимального поглощения была приготовлена суспензия йодида серебра, измерена оптическая плотность данной суспензии при разных длинах волн. По полученным данным построен график зависимости оптической плотности от длины волны. Найдено, что максимум поглощения суспензии наблюдается при 380 нм, поэтому все дальнейшие измерения проводились при этой длине волны.
Используя калибровочную кривую, построенную с применением стандартного раствора йодида калия, рассчитывают содержание йодид-ионов в анализируемой пробе.
Построение калибровочного графика йодида калия
В мерные колбы на 50 мл помещают 1,5; 2,0; 3,0; 5,0 стандартного раствора KI, с концентрацией 5·10-5 моль/л, 15 мл этилового спирта (в качестве стабилизатора суспензии), 5 мл 25%-ного раствора аммиака (pH=9-11) и 5 мл раствора нитрата серебра, с концентрацией 5·10-3 моль/л.
Образовавшуюся суспензию выдерживают 5-10 мин (для получения устойчивой системы; большее количество времени может вызвать осаждения взвешенных частиц на дно колбы).
Далее объем раствора доводят до метки водой. Оптическую плотность суспензии AgI измеряют на фотоколориметре или спектрофотометре в кювете толщиной 1 см при длине волны 380 нм (максимум светопоглощения суспензии AgI). По полученным данным строят график зависимости A=f(V).
ПРИМЕР 1. Определение содержания йодид-ионов в минеральной воде
Пробу воды объемом 400 мл помещают в фарфоровую чашку и выпаривают до уменьшения объема примерно в 10 раз. Объем пробы после выпаривания обязательно измеряют, чтобы учесть степень концентрации воды в конечном расчете.
5 мл полученного концентрата помещают в колбу на 50 мл, добавляют 15 мл этилового спирта, 5 мл 25%-ного раствора аммиака (pH=9-11) и 5 мл раствора нитрата серебра, с концентрацией 5·10-3 моль/л. Суспензию выдерживают 5-10 мин и доводят объем до метки водой.
Оптическую плотность полученной суспензии AgI измеряют на фотоколориметре или спектрофотометре в кювете толщиной 1 см при длине волны 380 нм.
По калибровочному графику, полученному с использованием стандартных растворов KI, находят содержание йодид-ионов в концентрате, затем, учитывая степень концентрирования, определяют содержание йодид-ионов в анализируемой пробе
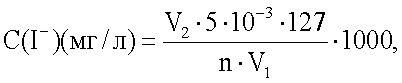
где V1 - исходный объем пробы воды, (мл);
V2 - объем раствора, найденный по калибровочному графику, (мл);
127 - молярная масса йодид-ионов, (г/моль);
n - степень концентрирования пробы;
5·10-3 - концентрация стандартного раствора KI, (моль/л).
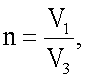
где V1 - исходный объем пробы воды, (мл);
V3 - объем пробы после концентрирования, (мл).
Для сравнения результатов было определено содержание йодид-ионов в исследуемой воде методом потенциометрии с использованием йод-селективного электрода.
Результаты сравнительных определений приведены в таблице 1.
Исходя из полученных данных, можно сделать вывод, что предлагаемый способ определения йодид-ионов является быстрым, высокоточным методом, исключает использование токсичных реагентов. Он позволяет определять содержание йодид-ионов в присутствии хлорид-ионов в питьевых и природных водах, а также в продуктах питания.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения йода | 2022 |
|
RU2788747C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЙОДА В МОЧЕ | 2003 |
|
RU2265847C2 |
| Способ определения сальсолина гидрохлорида | 1981 |
|
SU957075A1 |
| Способ определения анальгина | 1990 |
|
SU1744603A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ УЛЬТРАМИКРОКОЛИЧЕСТВ ЙОДА | 1999 |
|
RU2164214C1 |
| СПОСОБ ПРОБОПОДГОТОВКИ БИОЛОГИЧЕСКИХ ОБРАЗЦОВ ДЛЯ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЙОДА | 2023 |
|
RU2808066C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МЫШЬЯКА В ПРИСУТСТВИИ СУРЬМЫ В ПРИРОДНЫХ И СТОЧНЫХ ВОДАХ | 2007 |
|
RU2347219C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЙОДА ИЗ МИНЕРАЛЬНЫХ ИСТОЧНИКОВ | 2012 |
|
RU2481266C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЙОДА | 2010 |
|
RU2431824C1 |
| Способ определения иодидов | 1990 |
|
SU1767396A1 |
Изобретение относится к аналитической химии и позволяет определять содержание йодид-ионов в различных объектах, например в водах (питьевых, поверхностных, артезианских, расфасованных минеральных и др.), в пищевых продуктах, продовольственном сырье и т.д. Способ основан на переведении йодид-ионов в малорастворимые соединения AgI (ПPAgI=1,1·10-6). При этом осаждение AgI проводят в присутствии 25%-ного раствора аммиака (pH=9-11), исключающее выпадение осадка AgCl, который переходит в комплексный ион [Ag(NH3)2]+, для стабилизации суспензии предусмотрено добавление спирта в качестве стабилизатора. Затем измеряют оптическую плотность полученной суспензии йодида серебра на спектрофотометре. Измерения проводят при длине волны 380 нм, которая соответствует максимуму поглощения данной суспензии. По калибровочному графику, полученному с использованием стандартных растворов KI, находят содержание йодид-ионов в концентрате, затем, учитывая степень концентрирования, определяют содержание йодид-ионов в анализируемых пробах. Технический результат заключается в упрощении фотометрического способа определения йодид-ионов, сокращении числа операций и времени определения, а также отказ от использования токсичных веществ. 1 табл.
Способ определения йодид-ионов, включающий фотометрирование суспензии йодида серебра, выделенной из анализируемого раствора, отличающийся тем, что в присутствии хлорид-ионов осаждение ведут в аммиачной среде (pH 9-11) и измеряют оптическую плотность при длине волны 380 нм.
| Марченко З | |||
| Фотометрическое определение элементов - перевод с польского И.В.Матвеевой | |||
| - М.: Мир, 1971 г | |||
| Способ экстракционно-фотометрического определения серебра | 1990 |
|
SU1728741A1 |
| Способ определения железа | 1989 |
|
SU1732224A1 |
| Способ определения йода | 1986 |
|
SU1379726A1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ФТАЛОЦИАНИНОВОГО ЗЕЛЕНОГО | 2001 |
|
RU2197723C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЙОДА В МОЧЕ | 2003 |
|
RU2265847C2 |
Авторы
Даты
2009-12-27—Публикация
2008-02-26—Подача