Область техники
Настоящее изобретение относится к способу получения соединения индолина, пригодного в качестве лекарственного средства, а также получению его промежуточных соединений. В особенности настоящее изобретение относится к способу получения соединения индолина (общее название: силодозин), представленного следующей структурной формулой:
[Соед.1]
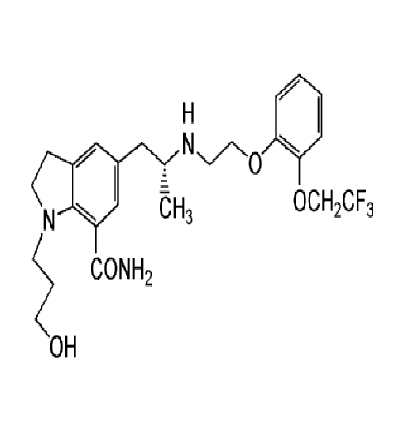
которое полезно в качестве терапевтического агента при расстройстве мочеиспускания, связанного с доброкачественной гиперплазией простаты, а также к получению промежуточных соединений для использования в его производстве.
Уровень техники
Силодозин обладает селективным ингибирующим влиянием против сокращения гладкой мускулатуры уретры и снижает внутреннее давление уретры без большого влияния на кровяное давление. Более того, силодозин селективно влияет на α1A подтип адренорецептора и чрезвычайно полезен в качестве терапевтического агента при расстройстве мочеиспускания, связанного с доброкачественной гиперплазией простаты и тому подобного (см. патентные ссылки 1 и 2).
В качестве эффективного и рационального способа получения силодозина предлагали или сообщали о том, что оптически активное соединение амина, представляемое следующей общей формулой:
[Соед. 2]
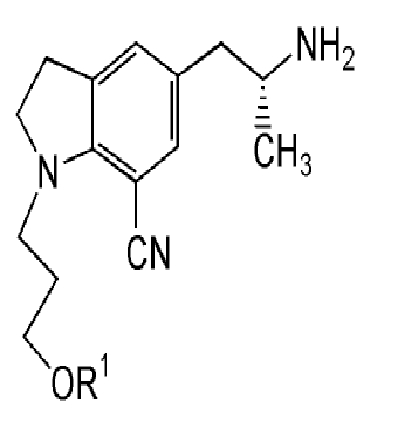
в которой R1 представляет собой атом водорода или защитную группу для гидроксила, вводили в реакцию с соединением феноксиэтана, представленного следующей общей формулой:
[Соед.3]
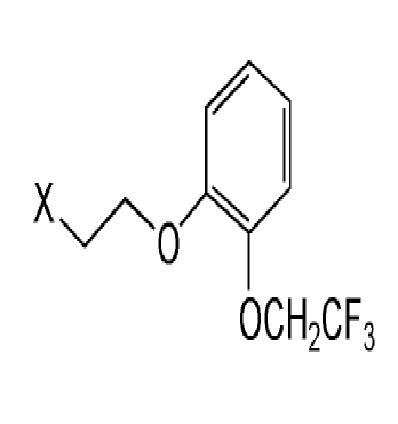
в которой X представляет собой уходящую группу, и необязательно снимали защиту, и цианогруппу превращали в карбамоильную группу (см. патентные ссылки 3 и 4).
Однако в вышеупомянутых способах получения иногда из-за реакции одной молекулы оптически активного соединения амина и двух молекул соединения феноксиэтана в качестве побочного продукта образовывалось диалкильное соединение (C), представленное следующей общей формулой:
[Соед.4]
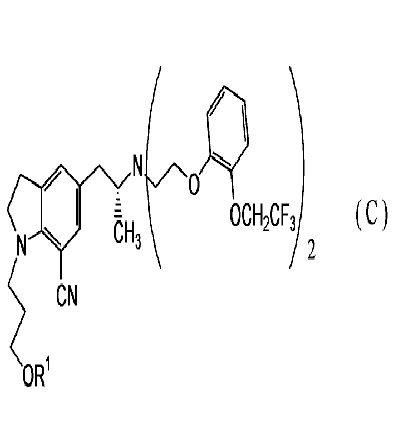
в которой R1 представляет собой атом водорода или защитную группу для гидроксила. Поскольку представляется сложным удалить побочный продукт методом очистки, используемым в обычном промышленном производстве, таким как перекристаллизация и тому подобное, то для удаления побочного продукта требуется использовать такой метод очистки, как колоночная хроматография или тому подобное. Таким образом, усложняясь, процесс очистки перестает удовлетворять способу промышленного производства. Таким образом, требуется разработка способа очистки, более подходящего для промышленного производства.
Патентная ссылка 1: Японская патентная публикация H6-220015;
Патентная ссылка 2: Японская патентная публикация 2000-247998;
Патентная ссылка 3: Японская патентная публикация 2001-199956;
Патентная ссылка 4: Японская патентная публикация 2002-265444.
Раскрытие изобретения
Задачи, которые должно решить изобретение
Цель настоящего изобретения заключается в обеспечении способа промышленного получения силодозина.
Способы решения задачи
Для достижения вышеупомянутой цели изобретатели настоятельно изучили и обнаружили, что путем превращения 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоата, представленного следующей структурной формулой:
[Соед.5]
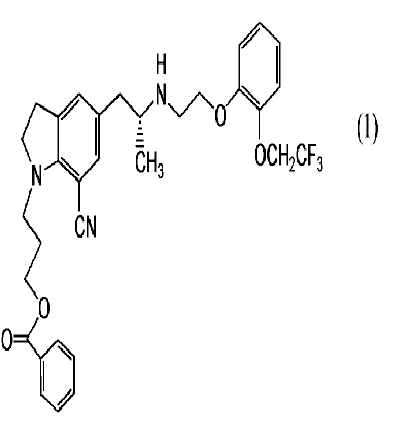
в оксалат и его выделения при помощи перекристаллизации может быть удален побочный продукт (C-a), представленный формулой
[Соед.6]
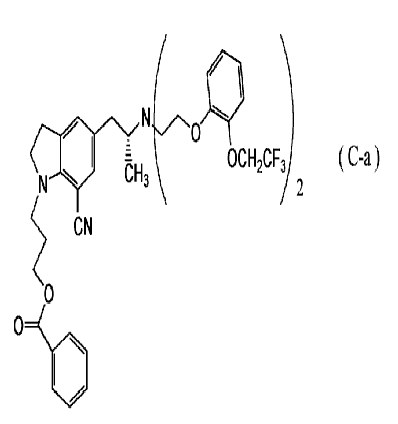
что формирует таким образом основу настоящего изобретения.
То есть, настоящее изобретение относится к способу получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбоксамида, представленного структурной формулой (3):
[Соед.9]
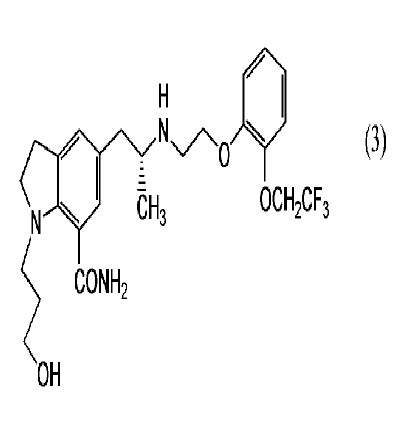
который включает смешивание 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоата, представленного следующей формулой (1):
[Соед.7]

с щавелевой кислотой с получением 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалата, последующий гидролиз оксалата с получением 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]-этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрила, представленного структурной формулой (2):
[Соед.8]
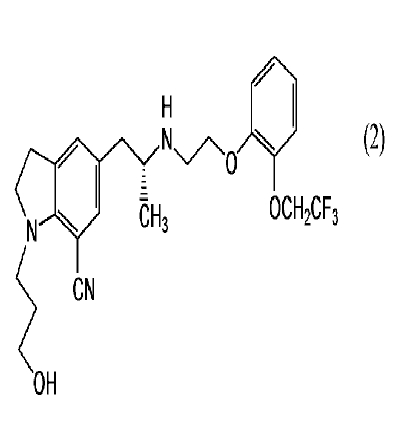
и дальнейший гидролиз соединения, представленного общей формулой (2), а также получение промежуточных соединений, используемых в способе получения.
Эффект от изобретения
3-{7-Циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)-фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалат, получаемый в качестве промежуточного соединения согласно способу получения настоящего изобретения, хорошо кристаллизуется, легко отделим от побочного продукта (C-a) и прост в обращении. Таким образом, данный оксалат становится отличнейшим промежуточным продуктом в способе промышленного производства.
Наилучший вариант воплощения изобретения
Способ получения согласно настоящему изобретению включает 4 стадии, как объясняется ниже.
(Стадия 1)
Получение 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоата
3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат, используемый в способе получения согласно настоящему изобретению, может быть получен способом, аналогичным тому, который описан в Патентной ссылке 3, по реакции 3-{7-циано-5-[(2R)-2-аминопропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоата, представленного структурной формулой(A):
[Соед.10]
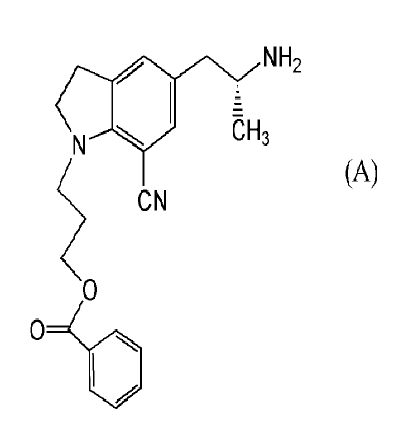
или его соли с соединением феноксиэтана, представленным общей формулой (B):
[Соед.11]
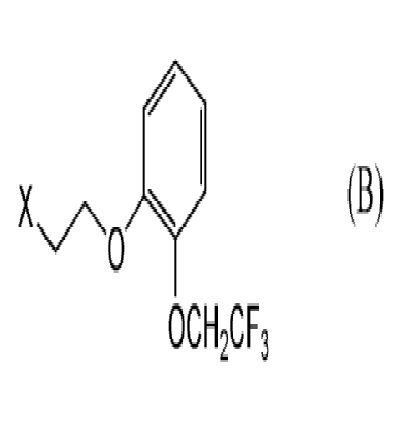
в которой X представляет собой уходящую группу,
в органическом растворителе и предпочтительно в присутствии основания.
В качестве уходящей группы Х в общей формуле (B) могут быть приведены примеры атомов хлора, брома и йода, низшей алкилсульфонилоксигруппы, такой как метансульфонилоксигруппа и ей подобные, арилсульфонилоксигруппы, такой как бензолсульфонилоксигруппа или толуолсульфонилоксигруппа и им подобные. Среди них низшая алкилсульфонилоксигруппа является предпочтительной.
В качестве органического растворителя, используемого как растворитель для реакции, может быть использован любой органический растворитель, если только он не ингибирует реакцию. В качестве примера можно привести низший спирт, такой как метанол, этанол, пропанол, изопропиловый спирт, трет-бутанол и им подобные; апротонный полярный растворитель, такой как диметилформамид, диметилсульфоксид, ацетонитрил и им подобные, или смеси растворителей, выбираемых из них же. Среди них низший спирт является предпочтительным, в особенности трет-бутанол является наиболее предпочтительным.
В качестве основания может быть приведен пример неорганического основания, такого как гидроксид щелочного металла, такой как гидроксид натрия, гидроксид калия и им подобные, и карбонат щелочного металла, такой как карбонат натрия, карбонат калия, карбонат цезия и им подобные, а также органическое основание, такое как амин низшего алкила, такой как триэтиламин, диизопропиламин и им подобные. Среди них неорганическое основание, особенно карбонат щелочного металла, является предпочтительным, и карбонат натрия является особенно предпочтительным.
Реакцию обычно проводят при температуре от комнатной до точки кипения органического растворителя, используемого в реакции в течение времени от 30 минут до 48 часов.
После реакции 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2- трифторэтокси)фенокси]этил}амино)пропил-2,3-дигидро-1H-индол-1-ил}
пропилбензоат может быть получен с использованием обычного метода. Вышеупомянутый побочный продукт (C-a) обычно входит в состав продукта в количестве приблизительно от 5 до 20%, хотя его количество отличается в зависимости от условий реакции. Количество содержащегося побочного продукта может быть вычислено по отношению площади, измеренной методом высокоэффективной жидкостной хроматографии в следующих условиях.
Условия измерения
Колонка: Inertsil ODS-2
Длина волны: 254 нм
Подвижная фаза: метанол:0,01 моль/л фосфатный буфер (pH 7,6) = 7:3
(Стадия 2)
Получение 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино]пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалата.
Кристаллический 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2- трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалат может быть выделен путем растворения почти эквимолярных количеств 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоата и щавелевой кислоты в подходящем растворителе и, необязательно, при нагревании раствора до образования 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалата и его кристаллизации. В качестве растворителя могут быть приведены примеры низшего спирта, такого как метанол, этанол, пропанол, изопропиловый спирт и им подобные, или вышеупомянутого спирта, содержащего воду, смесь растворителей, выбираемых из них же, и тому подобное. Среди них низший спирт является предпочтительным, особенно предпочтительным является этанол, изопропиловый спирт и смешанный растворитель, состоящий из воды и изопропилового спирта.
Хотя это может зависеть от растворителя, предпочтительное количество щавелевой кислоты, которое следует использовать, представляет собой обычно от 0,7 до 1,5 эквивалентов по отношению к 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоату.
Кристаллический оксалат может быть выкристаллизован, если оставить стоять вышеупомянутый раствор оксалата. В то же время могут быть использованы необязательные затравочные кристаллы оксалата или охлаждение. Более того, оксалат также может быть выкристаллизован при концентрировании раствора оксалата или при добавлении к раствору оксалата плохого растворителя.
Путем вышеупомянутого способа количество содержащегося побочного продукта (C-a) может быть понижено до 1% или меньше при помощи 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалата. Таким образом, полученный оксалат может быть непосредственно использован в следующей реакции.
(Стадия 3)
Получение 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрила
1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрил может быть получен путем гидролиза 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалата в подходящем растворителе.
Реакция гидролиза может быть проведена с использованием щелочи, такой как гидроксид щелочного металла, такого как гидроксид натрия, гидроксид калия или им подобные; карбоната щелочного металла, такого как карбонат натрия, карбонат калия, карбонат цезия и им подобные, или используя кислоту, такую как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота или им подобные. Среди них щелочь является предпочтительной, особенно предпочтительным является гидроксид щелочного металла.
В качестве растворителя, используемого для гидролиза, можно привести примеры воды, низшего спирта, такого как метанол, этанол, пропанол, изопропиловый спирт и им подобные; водорастворимые органические растворители, такие как ацетон, тетрагидрофуран, диоксан и им подобные, а также смеси растворителей, выбираемых из них же. Среди них смешанный растворитель из воды и низшего спирта является предпочтительным.
Реакция гидролиза обычно может быть проведена при температуре от 0°С до точки кипения используемого растворителя в течение времени от 30 минут до 48 часов, и тогда 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрил может быть получен с использованием обычного метода. Полученное соединение может быть использовано для следующей реакции непосредственно или необязательно после дополнительной очистки.
(Стадия 4)
Получение 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбоксамида
1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбоксамид может быть получен при гидролизе 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрила в подходящем растворителе.
Реакция гидролиза может быть проведена, используя щелочь, такую как гидроксид щелочного металла, такой как гидроксид натрия, гидроксид калия или им подобные; карбонат щелочного металла, такой как карбонат натрия, карбонат калия, карбонат цезия или им подобные, или используя кислоту, такую как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота или им подобные. Среди них щелочь является предпочтительной, особенно предпочтительным является гидроксид щелочного металла. В дополнение, предпочтительным является, чтобы реакцию гидролиза проводили в присутствии окисляющего агента, такого как пероксид водорода или ему подобного.
В качестве растворителя, используемого для гидролиза, можно привести примеры воды, низшего спирта, такого как метанол, этанол, пропанол, изопропиловый спирт и им подобные; водорастворимые органические растворители, такие как ацетон, тетрагидрофуран, диоксан, диметилсульфоксид и им подобные, а также смеси растворителей, выбираемых из тех же самых и им подобных. Среди них смешанный растворитель из воды и диметилсульфоксида является предпочтительным.
Реакция гидролиза может быть проведена при температуре от 0°С до 100°С в течение времени от 30 минут до 48 часов, и тогда 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбоксамид может быть получен с использованием обычного метода.
ПРИМЕРЫ
Настоящее изобретение далее иллюстрируется более детально при помощи следующих примеров, однако изобретение этим не ограничивается.
Пример 1
3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил)-2,3-дигидро-1H-индол-1-ил)пропилбензоат
К смеси этилацетата (50 мл) и водного раствора (50 мл) карбоната калия (13,5 г) понемногу добавляли 3-[5-((2R)-2-аминопропил)-7-циано-2,3-дигидро-1H-индол-1-ил]пропилбензоат(2R,3R)монотартрат (5,0 г) и смесь перемешивали при комнатной температуре 2 часа. Слой этилацетата отделяли и водный слой экстрагировали раствором этилацетата (50 мл). Объединенный слой этилацетата промывали водным раствором карбоната калия и сушили над безводным сульфатом натрия. Фильтрат концентрировали при пониженном давлении. Полученное масло растворяли в безводном трет-бутаноле (25 мл) и к раствору добавляли 2-[2-(2,2,2-трифторэтокси)фенокси]этилметансульфонат (3,67 г) и карбонат натрия (1,08 г). Смесь кипятили с обратным холодильником в течение 24 часов. После этого реакционной смеси давали остыть и затем добавляли водный раствор бикарбоната натрия (50 мл). Смесь дважды экстрагировали этилацетатом (50 мл). Объединенный слой этилацетата промывали водным раствором бикарбоната натрия, водой и солевым раствором и сушили над безводным сульфатом натрия. Фильтрат концентрировали при пониженном давлении, получая 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат (6,40 г). На данном этапе содержание побочного продукта (C-a) в полученном продукте составляло 13,6%. Продукт был использован для следующей реакции. Структура полученного 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоата была подтверждена ЯМР-анализом при использовании небольшого количества очищенного продукта.
1H-ЯМР (CDCl3) δppm: 1,06 (3H, д, J=6,4 Гц), 2,15 (2H, м), 2,44 (1H, дд, J=6,9, 13,8 Гц), 2,61 (1H, дд, J=6,3, 13,8 Гц), 2,85-3,10 (5H, м), 3,57 (2H, т, J=8,6 Гц), 3,74 (2H, т, J=7,2 Гц), 4,05-4,15 (2H, м), 4,32 (2H, кв., J=8,4 Гц), 4,47 (2H, т, J=6,4 Гц), 6,89-7,06 (6H, м), 7,44 (2H, т, J=7,8 Гц), 7,55 (1H, т, J=7,5 Гц), 8,06 (2H, д, J=8,4 Гц).
Пример 2
3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалат
Изопропиловый спирт (50 мл) и дигидрат щавелевой кислоты (1,20 г) добавляли к 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоату (6,40 г), который был получен в примере 1, и смесь растворяли при нагревании. После введения затравки целевого соединения смесь оставляли на ночь. Осажденные кристаллы отделяли фильтрованием и промывали небольшим количеством охлажденного изопропилового спирта и сушили под вакуумом до получения 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалата (5,43 г). На данном этапе содержание побочного продукта (C-a) в получаемом продукте составляло 0,9%.
1H-ЯМР (DMSO-d6) δppm: 1,13 (3H, д, J=6,2 Гц), 2,08 (2H, м), 2,45-2,57 (1H, м), 2,88-3,05 (3H, м), 3,35-3,50 (3H, м), 3,60 (1H, т, J=8,6 Гц), 3,70 (2H, т, J=7,1 Гц), 4,29 (2H, шир.с), 4,39 (2H, т, J=6,1 Гц), 4,71 (2H, кв., J=8,9 Гц), 6,95-7,16 (6H, м), 7,51 (2H, т, J=7,7 Гц), 7,65 (1H, т, J=7,4 Гц), 7,99 (2H, д, J=7,4 Гц).
Пример 3
1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрил
3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-1-ил}пропилбензоат монооксалат (10,0 г) растворяли в метаноле (40 мл), затем понемногу добавляли водный раствор гидроксида калия, приготовленный из гидроксида калия (2,93 г) и воды (10 мл), и смесь перемешивали при комнатной температуре в течение ночи. К реакционной смеси добавляли воду (150 мл) и последовательно экстрагировали этилацетатом (150 мл и 50 мл). Объединенный слой этилацетата промывали насыщенным водным раствором бикарбоната натрия и солевым раствором и сушили над безводным сульфатом натрия. Фильтрат концентрировали при пониженном давлении, получая 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрил (7,86 г).
1H-ЯМР (CDCl3) δppm: 1,05 (3H, д, J=6,1 Гц), 1,85-1,95 (2H, м), 2,43 (1H, дд, J=13,5, 6,8 Гц), 2,60 (1H, дд, J=13,7, 6,3 Гц), 2,80-3,10 (5H, м), 3,57 (2H, т, J=8,8 Гц), 3,67 (2H, т, J=7,2 Гц), 3,80 (2H, т, J=6,0 Гц), 4,05-4,15 (2H, м), 4,32 (2H, кв., J=8,4 Гц), 6,85-7,05 (5H, м).
Пример 4
1-(3-Гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбоксамид
1-(3-Гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбонитрил (6,00 г) растворяли в диметилсульфоксиде (75 мл) и к этому раствору добавляли 5 моль/л водный раствор гидроксида натрия (4,50 мл). К реакционной смеси понемногу добавляли 30% пероксид водорода (2,63 мл) при температуре не выше 25°C. Реакционную смесь перемешивали при температуре от 20 до 25°C в течение 5 часов. К реакционной смеси осторожно добавляли водный раствор сульфита натрия, приготовленный из сульфита натрия (2,1 г), растворенного в воде (150 мл). Реакционную смесь дважды экстрагировали этилацетатом (50 мл). Объединенный слой этилацетата дважды экстрагировали 2 моль/л соляной кислоты. Экстрагированный водный раствор соляной кислоты нейтрализовали бикарбонатом натрия и дважды экстрагировали этилацетатом (50 мл). Объединенный слой этилацетата промывали насыщенным водным раствором бикарбоната натрия и солевым раствором и сушили над безводным сульфатом натрия. Фильтрат концентрировали при пониженном давлении и остаток растворяли в этилацетате. Раствор охлаждали до получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1H-индол-7-карбоксамида (4,49 г).
1H-ЯМР (CDCl3) δppm: 1,08 (3H, д, J=6,2 Гц), 1,75-1,85 (2H, м), 2,53 (1H, дд, J=13,6, 6,7 Гц), 2,68 (1H, дд, J=13,6, 6,6 Гц), 2,90-3,10 (5H, м), 3,19 (2H, т, J=6,7 Гц), 3,41 (2H, т, J=8,5 Гц), 3,75 (2H, т, J=5,6 Гц), 4,05-4,15 (2H, м), 4,30 (2H, кв., J=8,4), 5,79 (1H, шир.с), 6,65 (1H, шир.с), 6,85-7,05 (5H, м), 7,16 (1H, с).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ИНДОЛА И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ ИХ | 1999 |
|
RU2212404C2 |
| АРИЛ-ЗАМЕЩЕННЫЕ КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ БЛОКАТОРОВ КАЛЬЦИЕВЫХ ИЛИ НАТРИЕВЫХ КАНАЛОВ | 2010 |
|
RU2575168C2 |
| N-(2-ЦИАНОГЕТЕРОЦИКЛИЛ)ПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ЯНУС-КИНАЗЫ | 2014 |
|
RU2669922C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛОПИРИДИНОНА В КАЧЕСТВЕ TTX-S БЛОКАТОРОВ | 2013 |
|
RU2646754C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛОПИРИДИНА В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2013 |
|
RU2652117C2 |
| НОВОЕ СОЕДИНЕНИЕ БИФЕНИЛА ИЛИ ЕГО СОЛЬ | 2018 |
|
RU2765152C2 |
| ЦИКЛОАЛКИЛНИТРИЛПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ЯНУС-КИНАЗЫ | 2014 |
|
RU2655380C2 |
| ПРОИЗВОДНЫЕ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБЫ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ И ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2001 |
|
RU2265011C2 |
| НОВОЕ СОЕДИНЕНИЕ БИФЕНИЛА ИЛИ ЕГО СОЛЬ | 2016 |
|
RU2726622C2 |
| 6,7-ДИГИДРО-5H-ПИРИДО[2,3-C]ПИРИДАЗИНОВЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ БЕЛКОВ BCLXL И ПРОАПОПТОТИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2832191C2 |
Изобретение относится к улучшенному способу получения силодозина формулы
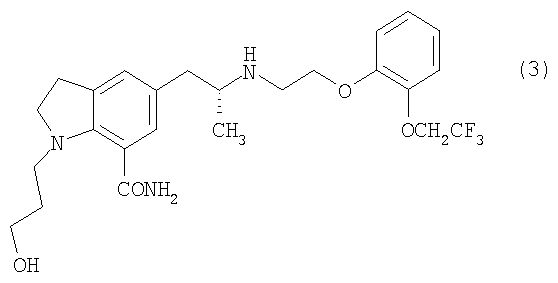
используемого при расстройстве мочеиспускания. Способ заключается в смешении нового соединения 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино]пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата с щавелевой кислотой, с получением соответствующего оксалата, с последующим его гидролизом, приводящим к образованию нового соединения 1-(3-гидроксипропил)-5-[(2R-)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино]пропил]-2,3-дигидро-1H-индол-7-карбонитрила, и его гидролизом с получением целевого соединения. Описаны способы получения новых промежуточных соединений. 8 н. и 4 з.п. ф-лы.
1. Способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбоксамида, представленного структурной формулой (3):
[Соединение 3]
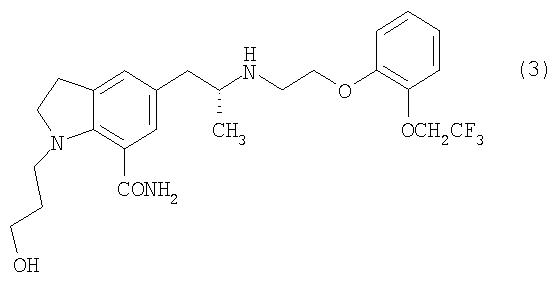
включающий смешивание 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата, представленного структурной формулой (1):
[Соединение 1]
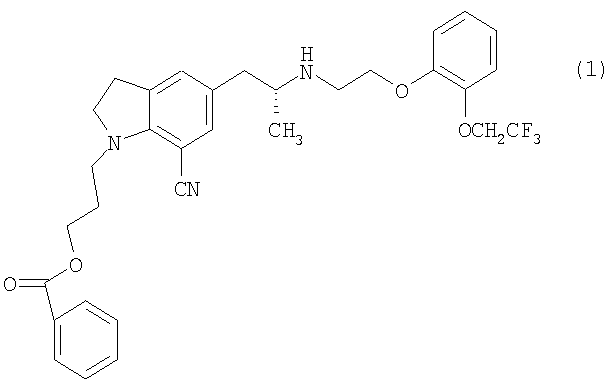
с щавелевой кислотой с образованием 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата монооксалата с последующим гидролизом оксалата с образованием 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила, представленного структурной формулой (2):
[Соединение 2]
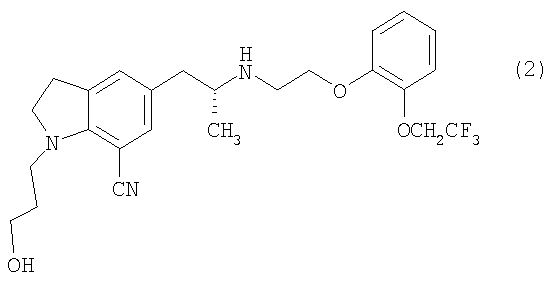
и гидролиз соединения, представленного структурной формулой (2).
2. Способ получения по п.1, включающий выделение 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата монооксалата.
3. Способ получения по п.1 или 2, включающий гидролиз 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата монооксалата с гидроксидом щелочного металла.
4. Способ получения по п.1, в котором 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрил гидролизуют в присутствии окисляющего агента.
5. Способ получения по п.4, в котором окисляющим агентом является пероксид водорода.
6. Способ получения 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата, представленного структурной формулой (1):
[Соединение 6]

включающий взаимодействие 3-{7-циано-5-[(2R)-2-аминопропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата, представленного структурной формулой (А):
[Соединение 4]
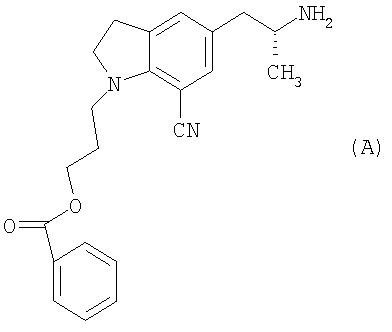
с соединением феноксиэтана, представленным общей формулой (В):
[Соединение 5]
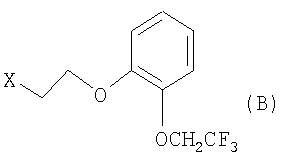
где X представляет собой уходящую группу.
7. Способ получения 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата монооксалата, включающий смешивание 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата и щавелевой кислоты.
8. Способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила, представленного структурной формулой (2):
[Соединение 7]

включающий гидролиз 3-{7-циано-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоата монооксалата.
9. Способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбоксамида, представленного структурной формулой (3):
[Соединение 8]

включающий гидролиз 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила.
10. 3-{7-Циано-
5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил)пропилбензоат.
11. 3-{7-Циано-
5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-1-ил}пропилбензоат монооксалат.
12. 1-(3-Гидроксипропил)-
5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрил.
| EP 6600675 08.06.1994 | |||
| JP 2002265444 A, 18.09.2002 | |||
| ИНДОЛИНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2104268C1 |
| ПРОИЗВОДНЫЕ ИНДОЛИН-2-ОНА И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2128170C1 |
Авторы
Даты
2010-01-20—Публикация
2005-10-24—Подача