Изобретение относится к области биохимии и медицины. Более конкретно изобретение относится к способам и фармацевтическим агентам для лечения аденомы кишечника (также называемой полипозом) и/или аденокарциномы.
Тонкий кишечник представляет собой наиболее длинный компонент пищеварительного тракта и главное место переваривания и всасывания. Кроме того, получая химус из желудка, начальный сегмент тонкого кишечника, двенадцатиперстная кишка, получает желчь из желчного пузыря и пищеварительные ферменты из поджелудочной железы. Ферменты поджелудочной железы продуцируются в неактивной форме и становятся активными только в просвете двенадцатиперстной кишки. Тонкий кишечник подразделяется на три части, двенадцатиперстную кишку, тощую кишку и подвздошную кишку.
Поверхность просвета полностью покрыта рядом пальце- или листообразных выростов, называемых ворсинками, 0,5-1,5 мм длины. Основа ворсинки представляет собой вырост собственной пластинки слизистой оболочки и ее поверхность покрыта простым колончатым эпителием. Отверстия на люминальной поверхности у оснований ворсинок представляют собой простые трубчатые структуры, называемые кишечными железами или либеркюновыми криптами. Крипты простираются вниз внутрь мышечной оболочки слизистой. Выстилающий их простой колончатый эпителий является непосредственным продолжением эпителия, покрывающего ворсинки.
Преобладающим клеточным типом эпителия является энтероцит или всасывающая клетка. Каждый энтероцит обладает на своей люминальной поверхности приблизительно 3000 микроворсинками, которые выглядят в световом микроскопе как опушенная полосатая граница на поверхности ворсинок. Ворсинки и микроворсинки совместно со складками в субмукозном слое, называемыми круговыми складками, увеличивают поверхность всасывания в тонком кишечнике приблизительно в 600 раз.
Эпителий тонкого кишечника состоит из следующих клеточных типов: энтероцитов, бокаловидных клеток, клеток Панета, энтероэндокринных клеток, микроскладчатых клеток и недифференцированных клеток. Некоторые их этих клеток будут обсуждаться более подробно.
Энтероциты (также называемые всасывающими клетками) представляют собой вытянутые колончатые клетки с микроворсинками и базальным ядром, специализирующиеся на транспорте веществ. Они связаны друг с другом и с другими клеточными типами с помощью комплексов для контакта. Аминокислоты и моносахариды всасываются с помощью активного транспорта, моноглицериды и жирные кислоты проходят через мембраны микроворсинок пассивно. Поглощенные вещества поступают либо в фенестрированные капилляры в собственной пластинке слизистой оболочки как раз под эпителием, либо в лимфатические млечные протоки (большинство липидов и липопротеиновые частицы). Продолжительность жизни энтероцитов составляет приблизительно 5-6 дней.
Бокаловидные клетки представляют собой клетки, секретирующие слизь, и являются вторыми наиболее распространенными эпителиальными клетками. Они обнаруживаются в виде распределенных среди других клеточных типов. Их слизь представляет собой очень большой гликопротеин, который аккумулируется на апикальном конце клетки. Тонкое основание клетки содержит ядро и органеллы. Распространенность бокаловидных клеток растет от двенадцатиперстной кишки к концу подвздошной кишки. Продолжительность их жизни также составляет приблизительно 5-6 дней.
Недифференцированные клетки представляют собой стволовые клетки и выявляются только у основания крипт и дают начало всем другим клеточным типам. Клетка, предназначенная для превращения в бокаловидную клетку или энтероцит, после выхода из пула стволовых клеток проходит приблизительно 2 дополнительных деления и мигрирует из крипты в ворсинку. Она будет потеряна на вершине ворсинки.
Толстый кишечник состоит из ободочной, слепой кишок, аппендикса, прямой кишки и прохода. Главными функциями ободочной кишки являются реабсорбция электролитов и воды и выведение непереваренной пищи и шлаков. Слизистая выглядит гладкой на макроскопическом уровне, так как не имеет ворсинок. Присутствует множество прямых трубчатых желез. Они простираются по всему пути до мышечного слоя слизистой. Железы и поверхность выстланы простым колончатым эпителием, чьи клеточные типы являются такими же, что и описанные для тонкого кишечника. Однако клетки Панета обычно отсутствуют у взрослого человека и энтероэндокринные клетки редки. Колончатые всасывающие клетки и бокаловидные клетки распространены. Бокаловидные клетки преобладают больше в криптах, чем на поверхности, и их количество растет дистально в направлении прямой кишки. Слизь содействует прохождению растущего твердого содержимого ободочной кишки и окутывает бактерии и частички вещества. Всасывающие клетки обладают короткими, нерегулярными микроворсинками и, хотя они секретируют гликокаликс, не обнаружено, что они содержат пищеварительные ферменты. Всасывающие клетки активно транспортируют электролиты, вода также поглощается, так как она пассивно следует за электролитами. Как и в тонком кишечнике, в основании крипт найдены недифференцированные клетки.
Несмотря на обширные знания в отношении множества форм рака (варьирующихся по внешнему виду от солидных опухолей и относящимся к ним метастазам в отдельных частях организма до лейкозных клеток крови, которые циркулируют в организме, и варьирующихся от полностью доброкачественных до агрессивных злокачественных), эффективное лечение рака затруднено и в целом ограничивается тремя типами терапии: лечением с помощью облучения, химиотерапии и хирургии.
Возможностей более специфического лечения, направленного против лежащей в основе причины конкретного рака или группы раковых заболеваний, в настоящее время фактически не существует. Разнообразные попытки направлены на обеспечение такими конкретными лекарствами путем попыток открытия лекарств с тем, чтобы попытаться идентифицировать потенциальные лекарства для специфической терапии рака.
Развитие рака часто начинается с изменений в клетке, которые ведут к ее неограниченному развитию и делению, так что эта первая клетка превращается в постоянно делящуюся популяцию клеток. Эти изменения часто представляют собой аккумуляцию мутаций или других изменений в ключевых генах, которые возникают хронологически, за счет чего популяция мутантных клеток теряет свой исходный, часто специализированный тип и все больше и больше приобретает раковую природу. Нормальные процессы регуляции роста клеток в измененных клетках нарушаются. Транскрипция генов, которые обычно только слегка экспрессируются в указанном типе клеток, в раковых клетках больше не контролируется.
Активация транскрипции генов с помощью транскрипционных факторов, которые в другом случае не должны экспрессироваться в конкретном типе клеток, может, например, вести к такому типичному неограниченному росту и неопластической природе рака.
Примеры представляют собой мутации в генах-супрессорах, которые обычно работают, давая белки, которые подавляют транскрипционные пути, которые больше не используются в специализированной клетке. Мутантные гены-супрессоры больше не помогают держать рост клетки в постоянном контроле. Лекарства, направленные против или вмешивающиеся в конкретные межбелковые взаимодействия или взаимодействия белок-ДНК в транскрипционных путях, контролирующих рост или развитие клетки, могут рассматриваться как типичные потенциальные лекарства для применения в конкретной раковой терапии, особенно, когда такие пути искажены и ведут к неограниченному росту клеток.
Типичный пример неправильного транскрипционного пути, ведущий к развитию рака, может быть найден с помощью гена аденоматозного полипоза coli (APC). Мутации в этом гене находятся среди наиболее общих событий, вызывающих заболевание у человека, приблизительно у 50% популяции в течение нормальной жизни будут развиваться колоректальные полипозы, возникающие в результате мутаций APC. У индивидуумов с врожденными мутациями развиваются тысячи колоректальных опухолей. Белок APC взаимодействует, по меньшей мере, с шестью другими белками; β-катенином, γ-катенином, тубулином, ЕВ1, hDLG и ZW3/GSKβ киназой, которые могут быть совместно с APC вовлечены в связанный с APC контроль роста. Клетки карциномы ободочной кишки с мутантным APC содержат большие количества мономерного цитоплазматического β-катенина. Повторное введение APC дикого типа снижает избыточное количество β-катенина.
Особенно в течение последнего десятилетия молекулярно-генетический анализ колоректального рака выявил, что ген-супрессор опухоли аденоматозного полипоза coli (APC), первоначально идентифицированный как ген, ответственный за семейный аденоматозный полипоз (FAP), играет лимитирующую скорость роль в формировании колоректального рака: он мутирует в большинстве спорадических колоректальных опухолей, и инактивация обоих аллелей APC возникает на ранних стадиях развития опухоли у мыши и человека.
Более того, хотя колоректальные опухоли являются признаком FAP, зародышевые мутации APC часто ведут к широкому спектру повреждений экто-, мезо- и эндодермального происхождения. Действительно, больные FAP находятся в состоянии высокого риска развития десмоидов (фибром), опухолей двенадцатиперстной кишки и желудка, врожденных гипертрофии эпителия сетчатки (CHRPEs), эпидермальных кист, остеом, опухолей ЦНС и других. Более поздние наблюдения ясно указывают на то, что ген АРС играет решающую роль в поддержании гомеостаза тканей во многих различных частях организма.
Сигнализация Notch контролирует пространственную структуру и решения о судьбе клетки во всем животном мире (Artavanis-Tsakonas et al., 1999). Гены Notch кодируют большие одноцепочечные трансмембранные рецепторы. Взаимодействие рецепторов Notch с лигандами ведет к протеолитическому расщеплению рецептора. Образованный в результате свободный внутриклеточный домен Notch (NICD) транслоцируется в ядро, где он связывается с транскрипционным фактором RBP-Jk (CSL или CBF1), активируя в результате этого транскрипцию генов-мишеней (Baron 2003, Mumm & Kopan 2000). Лучше всего охарактеризованные гены-мишени Notch представляют собой гены волосистости/усилители расщепления(HES) транскрипционных репрессоров. Белки HES в свою очередь подавляют экспрессию нижележащих генов (Heitzler et al., 1996, Oellers et al., 1994).
Несмотря на то, что компоненты пути Notch экспрессируются в кишечнике мыши (Schroder & Gossler 2002), в настоящее время нет генетических доказательств вовлечения этих компонентов в контроль судьбы эпителиальных клеток. Животные, дефицитные по HES-1, известные как представляющие ген-мишень Notch в других тканях, характеризуются относительным увеличением секретирующих слизь и энтероэндокринных клеток при расходе всасывающих клеток (Jensen et al., 2000). Предполагаемая нижележащая в положении «даунстрим» мишень репрессии HES-1 в кишечнике, Match-1 (Jensen et al., 2000) (Zeng et al., 2000), необходима для коммитирования в сторону секреторной линии дифференцировки, что обнаружено с помощью нокаута гена (Yang et al., 2001). Эти результаты интерпретируются как указание на то, что сигнализация Notch изменяет судьбу дифференцирующихся клеток крипт, покидающих переходный компартмент амплификации, и направляет их дифференцировку в сторону фенотипа энтероцитов. По этой схеме сигнализация Notch активирует гены транскрипционных факторов, такие как HES1, которые в свою очередь подавляют такие гены как Mathi, уводя дифференцирующиеся клетки с пути секреторной линии дифференцировки.
Непрямое подтверждение контроля судьбы клеток кишечника с помощью Notch дает применение ингибиторов гамма-секретазы, как исходно было разработано для болезни Альцгеймера. Notch представляет собой один из нескольких известных субстратов γ-секретазы. Протеолитический процессинг Notch γ-секретазой представляет собой существенную стадию последующей активации пути. Как следствие, одним из эффектов ингибиторов γ-секретазы является отмена активации пути Notch (De Strooper et al., 1999, Kopan & Goate 2000). Токсикологические исследования на грызунах с данными ингибиторами показали увеличение размера и количества секретирующих слизь бокаловидных клеток (Searfoss et al., 2003; Wong et al., 2004; Milano et al., 2004). Благодаря такого рода исследованиям дальнейшее клиническое развитие многочисленных, многообещающих ингибиторов γ-секретазы для лечения болезни Альцгеймера было прекращено, поскольку были серьезные основания ожидать индукцию ими аномалий кишечника.
В изобретении раскрывается удивительный факт, что ингибиторы активации пути Notch (например, ингибиторы γ-секретазы) чрезвычайно полезны для лечения аденомы и/или аденокарциномы кишечника. Лечение аденомы и/или аденокарциномы кишечника ингибитором активации пути Notch приводит к ингибированию пролиферации трансформированных/злокачественных клеток и приводит к их дифференцировке в постмитотические (т.е. более (визуально) не делящиеся) клетки, такие как бокаловидные клетки. Данные дифференцированные клетки имеют относительно короткую продолжительность жизни (5-6 дней), и организм удаляет их после их гибели, и аденома и/или аденокарцинома кишечника уменьшается(ются), по меньшей мере, частично в своем размере/объеме.
В первом осуществлении в изобретении предлагается способ модификации судьбы клетки аденомы и/или аденокарциномы, включающий воздействие на активацию пути Notch. Более конкретно, в изобретении предлагается (in vitro и/или in vivo) способ индукции образования постмитотической клетки из клетки аденомы и/или аденокарциномы, по меньшей мере, частично ингибирующий активацию пути Notch в указанной клетке аденомы и/или аденокарциномы. Примером постмитотической клетки является бокаловидная клетка.
В дополнительном осуществлении в изобретении предлагается способ для, по меньшей мере, частичного уменьшения аденомы и/или аденокарциномы кишечника, имеющейся у животного, включающий, по меньшей мере, частичное ингибирование активации пути Notch у указанного животного.
Активация пути Notch обычно включает следующие события. Notch представляет собой трансмембранный поверхностный рецептор, который может быть активирован посредством множественных протеолитических расщеплений, одно из которых представляет собой расщепление комплексом белков с протеазной активностью, называемым γ-секретазой. Гамма (γ)-секретаза представляет собой протеазу, которая осуществляет свою расщепляющую активность в мембране. Гамма (γ)-секретаза представляет собой многокомпонентный фермент и состоит из, по меньшей мере, четырех различных белков, а именно презенилинов (презенилин 1 или 2), никастрина, PEN-2 и АРН-1. Презенилин представляет собой каталитический центр γ-секретазы. При связывании лиганда рецептор Notch подвергается конформационному изменению, которое позволяет эктодомену отделяться благодаря действию протеазы ADAM, которая является металлопротеазой. Это сопровождается немедленным действием γ-секретазного комплекса, что приводит к высвобождению внутриклеточного домена Notch (NICD). NICD транслоцируется в ядро, где он взаимодействует с CSL (С-промотор-связывающий фактор/белок, связывающий последовательность сигнала рекомбинации Jk/Suppressor-of-Hairless/Lag1). Связывание NICD превращает CSL из транскрипционного репрессора в активатор, что ведет к экспрессии генов-мишеней Notch.
Заявители настоящего изобретения исследовали экспрессию различных компонентов и генов-мишеней пути Notch в аденомах, которые спонтанно возникают у мышей с мутацией АРС min, испытанной животной модели семейного аденоматозного полипоза и рака кишечника. Изобретатели выявили экспрессию многих компонентов пути Notch в аденомах, включая Notch2 и Delta-like-1. Более того, изобретатели обнаружили, что в аденомах экспрессируется ген-мишень Notch Hesi, что указывает на то, что в аденомах имеется активная сигнализация Notch. На следующей стадии изобретатели выявили действие ингибиторов активации пути Notch на аденомы.
С помощью применения ингибитора активации пути Notch в отношении злокачественной/трансформированной клетки, вовлеченной в аденому и/или аденокарциному кишечника, изменяли судьбу указанной клетки в направлении постмитотической судьбы, например, в направлении типа бокаловидной клетки. Такая клетка имеет относительно короткую продолжительность жизни (5-6 дней) и должна погибнуть вскоре после применения ингибитора, что приводит к снижению количества клеток аденомы и/или аденокарциномы кишечника, т.е. к снижению объема, по меньшей мере, одной аденомы и/или аденокарциномы.
С помощью применения ингибитора активации пути Notch пролиферативная способность аденомы и/или аденокарциномы кишечника, по меньшей мере, частично снижается. Предпочтительно, снижение является таким, что оно является видимым при сканировании или при диагностической операции. Еще более предпочтительно, чтобы снижение аденомы и/или аденокарциномы кишечника было полным, т.е. не оставалось (видимых) злокачественных/трансформированных клеток.
Животное здесь определяется как отличное от человека животное или человек.
Ингибирование (по меньшей мере, частичное, но предпочтительно полное) активации пути Notch достигается разными путями, которые (не ограничиваясь этим) описаны здесь ниже. Предпочтительно ингибирование производится местно, т.е. в клетке аденомы и/или аденокарциномы, без вмешательства в путь сигнализации Notch в отличных от аденомы и/или аденокарциномы клетках.
Более того, активация пути Notch определяется как включающий путь активации молекул, подобных Notch, и/или различных аллельных вариантов молекул Notch (-подобных).
Аденома кишечника обычно определяется как доброкачественная опухоль, такая как полип. Аденокарцинома обычно определяется как злокачественная опухоль и также обозначается как колоректальный рак. Применяемый здесь термин «аденома и/или аденокарцинома кишечника» также включает метастаз, возникший из указанной аденокарциномы. Предпочтительно, указанный метастаз возникает из аденокарциномы кишечника. Такой метастаз может локализоваться в любом месте организма субъекта (подвергающегося (подлежащего) лечению), например метастаз аденокарциномы кишечника, локализованный в легком, или мозге, или почке, или печени указанного субъекта.
Более того, способ изобретения подходит для лечения аденомы и/или аденокарциномы кишечника и/или происходящих от нее метастазов независимо от их размера. Одним из недостатков применяемой в настоящее время терапии опухолей является то, что указанная терапия часто заставляет надеяться на присутствие вновь образованных кровеносных сосудов (ангиогенеза) для доставки вещества, применяемого в указанной терапии, к указанной опухоли или ее метастазам. Настоящее изобретение рассчитывает на ингибирование пролиферации трансформированных/злокачественных клеток и их дифференцировку в постмитотические клетки. Следовательно, маленькая опухоль или маленький метастаз (еще без каких-либо вновь образованных кровеносных сосудов) можно лечить намного ранее по сравнению с некоторыми видами традиционной терапии.
В предпочтительном осуществлении в изобретении предлагается способ, по меньшей мере, частичного снижения аденомы и/или аденокарциномы кишечника, присутствующей у животного, включающий, по меньшей мере, частичное ингибирование активации пути Notch у указанного животного, где активация указанного пути Notch, по меньшей мере, частично ингибируется с помощью обеспечения указанного животного ингибитором γ-секретазы. Такой ингибитор γ-секретазы представляет собой, например, пептидную по природе или непептидную, или полупептидную молекулу и предпочтительно является небольшой молекулой. Ингибиторы гамма-секретазы были первоначально определены для болезни Альцгеймера. Ключевой стадией в патогенезе болезни Альцгеймера является протеолиз АРР, ведущий к образованию β-амилоидного пептида, главного белкового компонента характерных для болезни бляшек в мозге. АРР (в самом деле подобный Notch) сначала расщепляется во внеклеточном домене (в этом случае с помощью β-секретазы) и оставшаяся часть АРР расщепляется в мембране под действием γ-секретазы с получением Аβ пептида. Ингибирование продукции Аβ пептида путем блокирования активности γ-секретазы является в настоящее время одним из наиболее обещающих терапевтических стратегий для снижения прогрессии болезни Альцгеймера. Несколько компаний тем временем имеют разработанные ингибиторы γ-секретазы, такие как DAPT (N-[N-(3,5-дифторфенилацетил)L-аланил]-3-фенилглицина трет-бутиловый эфир). Кроме того, соединения других химических классов AS (арилсульфонамид), DBZ (дибензазепин (DBZ), BZ (бензодиазепин), LY-411575 и многие другие были протестированы на их ингибирующую активность в отношении γ-секретазы. Обзор в отношении ингибиторов γ-секретазы сделан, например, в Harrison et al., 2004, в котором ингибиторы γ-секретазы подразделены на сульфонамиды/сульфоны и бензодиазепины/бензолактамы. Несколько ингибиторов γ-секретазы уже проходили фазу I и II клинических испытаний. Специалисту в данной области техники ясно, что способ, по меньшей мере, снижения аденомы и/или аденокарциномы кишечника, присутствующей у животного, включающий, по меньшей мере, частичное ингибирование активации пути Notch у указанного животного, где активация указанного пути Notch, по меньшей мере, частично ингибируется с помощью обеспечения указанного животного ингибитором γ-секретазы, может быть осуществлен с помощью обеспечения, по меньшей мере, одним или, по меньшей мере, двумя или более ингибиторами γ-секретазы, т.е. путем обеспечения сочетанием различных ингибиторов γ-секретазы. Ясно, что γ-секретазы обычно способны действовать (по меньшей мере) двумя путями: АРР и Notch путями. Химические компании тем временем имеют разработанные γ-секретазы, которые специфичны для одного или другого пути, например γ-секретазы, которые специфичны для пути АРР, и не вмешиваются в путь Notch. Ясно, что γ-секретазы, которые не вмешиваются в путь Notch, не пригодны для способа изобретения. Следовательно, предпочтительно γ-секретаза, способная вмешиваться в путь Notch, а также в путь АРР, или γ-секретазы, способные специфически вмешиваться в путь Notch, являются предпочтительными. Такие ингибиторы, например, могут быть найдены в Harrison et al., 2004, что включено здесь в качестве ссылки.
В предпочтительном осуществлении в изобретении предлагается способ, по меньшей мере, частичного снижения аденомы и/или аденокарциномы кишечника, присутствующей у животного, включающий, по меньшей мере, частичное ингибирование активации пути Notch у указанного животного, где активация указанного пути Notch, по меньшей мере, частично ингибируется с помощью обеспечения указанного животного ингибитором γ-секретазы, где указанный ингибитор γ-секретазы представляет собой DAPT или дибензазепин (DBZ), или бензодиазепин (BZ).
DAPT, DBZ или BZ, все эффективны в отношении индукции образования постмитотической клетки из клетки аденомы и/или аденокарциномы, и эти соединения, таким образом, имеют сходный эффект в способе в соответствии с изобретением. Для DBZ, однако, IC50 составляет 1,7 нМ, для BZ IC50 составляет 2,2 нМ, в то время как для DAPT IC50 составляет 10 нМ, и, следовательно, для получения сходных результатов могут быть использованы более низкие количества DBZ или BZ по сравнению с DAPT.
Как уже подчеркивалось выше, γ-секретаза представляет собой комплекс белков. Другой путь, по меньшей мере, частичного ингибирования активации пути Notch осуществляется с помощью, по меньшей мере, частичного ингибирования образования указанного комплекса белков, так как только комплекс рассматривается как активное состояние. Это осуществляется, например, с помощью обеспечения одним из компонентов в качестве доминантно-негативной молекулы или путем обеспечения частью/молекулой указанного комплекса, причем часть/молекула имеет мутацию, предотвращающую дальнейшее образование комплекса или ведущую к нестабильному (неактивному) комплексу белков. Еще одним путем, по меньшей мере, частичного ингибирования активации пути Notch является специфическое ингибирование каталитической части указанного комплекса, т.е. специфическое ингибирование пресенилинов.
В другом предпочтительном осуществлении в изобретении предлагается способ, по меньшей мере, частичного снижения аденомы и/или аденокарциномы кишечника, присутствующей у животного, включающий, по меньшей мере, частичное ингибирование активации пути Notch у указанного животного, где активация указанного пути Notch, по меньшей мере, частично ингибируется с помощью, по меньшей мере, частичного снижения опосредуемой лигандом активации Notch. Как подчеркивалось выше, активация пути Notch начинается со связывания лиганда после этого события рецептор Notch подвергается конформационному изменению, которое позволяет эктодомену отделяться благодаря действию протеазы ADAM. Специалисту в данной области техники ясно, что связывание лиганда с Notch может быть, по меньшей мере, частично, но предпочтительно полностью, ингибировано с помощью множества стратегий. Предпочтительно указанная опосредуемая лигандом активация Notch, по меньшей мере, частично, снижается с помощью обеспечения указанного животного доминантно-негативным лигандом Notch. Примерами природных лигандов Notch являются белки Delta, Jagged и Serrate. Доминантно-негативные лиганды, т.е. лиганды, способные связываться с Notch по существу без дальнейшей активации пути Notch (блокирующие активацию пути Notch), могут быть производными указанных природных лигандов, например, полученными в виде маленьких связывающих молекул на основе связывающей части указанного природного лиганда. В том случае, когда такие доминантно-негативные лиганды вводятся в контакт с Notch, связывание указанного доминантно-негативного лиганда с Notch имеет место без дальнейшей активации пути Notch. Предпочтительно, чтобы указанный доминантно-негативный лиганд прилипал/связывался с Notch в течение более длительных периодов времени и связывание природного лиганда частично и предпочтительно полностью блокировалось/ингибировалось и, как следствие, активация пути Notch (по меньшей мере, частично) ингибировалась. Примерами доминантно-негативного лиганда являются, например, мутанты Delta и Serrate, включающие внутриклеточные делеции (Sun and Artavanis-Tsakonas, 1996).
В другом предпочтительном осуществлении указанная опосредуемая лигандом активация Notch, по меньшей мере, снижается введением указанному животному доминантно-негативного Notch. В принципе для этой цели может быть использован любой тип молекулы Notch, т.е. Notch1, 2, 3 или 4 или его функциональный фрагмент и/или функциональное производное. Функциональным фрагментом является любой фрагмент (N-концевой фрагмент, С-концевой фрагмент или промежуточный фрагмент или любое их сочетание), полученный из любой из этих молекул (или эквивалентных им), способный связываться с лигандом Notch. Такой функциональный фрагмент может быть, например, представлен связанным с мембраной или немембранным компонентом. Благодаря связыванию доминантно-негативного Notch с доступными лигандами, указанный лиганд не может связаться с природно/исходно/функционально доступным Notch, вследствие чего активация пути Notch, по меньшей мере, частично ингибируется. Функциональное производное представляет собой, например, мутантную молекулу Notch (точечная мутация, вставки), так что еще возможно связывание лиганда, но такая мутация препятствует проведению сигнала связывания лиганда. Функциональное производное может также брать начало от других видов. В еще одном предпочтительном осуществлении указанная опосредуемая лигандом активация Notch, по меньшей мере, снижается введением указанному животному антитела, способного, по меньшей мере, частично блокировать взаимодействие между лигандом Notch и Notch. Такое антитело представляет собой, например, антитело против лигандсвязывающей части Notch или против части лиганда, которая взаимодействует с Notch. Получение антител является обычным в данной области техники и поэтому дополнительные подробности, касающиеся данного вопроса, не предлагаются. Независимо от типа применяемого ингибирования опосредуемой лигандом активации Notch, результатом является одно и то же: образование (по меньшей мере, части) NICD ингибируется, что в конечном итоге приводит к образованию постмитотических клеток (например, бокаловидных клеток) из трансформированных/злокачественных клеток.
Как уже указывалось, ингибирование (по меньшей мере, частичное, но, предпочтительно, полное) активации пути Notch осуществляется разными путями. В еще одном предпочтительном осуществлении изобретения предлагается способ, по меньшей мере, частичного уменьшения имеющейся у животного аденомы и/или аденокарциномы, включающий, по меньшей мере, частичное ингибирование активации пути Notch у указанного животного, где указанная активация пути Notch, по меньшей мере, частично ингибируется введением указанному животному протеазного ингибитора ADAM. После связывания лиганда Notch с Notch рецептор Notch претерпевает конформационное изменение, которое позволяет удаление эктодомена под действием протеазы ADAM. ADAM обозначает дисинтегрин и металлопротеазу. Благодаря введению вещества, способного ингибировать протеазу, которая осуществляет удаление эктодомена, происходит, по меньшей мере, частичное, но, предпочтительно, полное ингибирование активации пути Notch, т.е. не происходит образование NICD. В случае аденомы и/или аденокарциномы кишечника это приводит к превращению пролиферирующих клеток аденомы и/или аденокарциномы в постмитотические, например бокаловидные клетки. И вновь предпочтительно местное ингибирование активации пути Notch во избежание, насколько возможно, любых возможных нежелательных побочных эффектов.
Для специалиста в данной области техники ясно, что можно также сочетать разные пути, по меньшей мере, частичного ингибирования активации Notch для, например, повышения эффективности.
Аденомы кишечника возникают из-за мутационной активации пути Wnt, чаще всего из-за утраты супрессорного гена АРС опухоли кишечника (Kinzler and Vogelstein, 1996). Заявители недавно раскрыли программу генов-мишеней Wnt в клетках колоректального рака и тем самым выявили поразительную симметрию между клетками аденомы и пролиферирующими предшественниками крипт (van de Wetering et al 2002). Для изучения того, распространяется ли эта симметрия на путь Notch, заявители исследовали экспрессию различных компонентов Notch и генов-мишеней в аденомах, которые спонтанно возникают у мышей с мутацией min APC. В целом экспрессия рецепторов и лигандов в аденомах близко следовала экспрессии в криптах, как сообщалось ранее (Schroder and Gossler, 2002). В качестве примеров, на фиг.1 представлена экспрессия Notch2 и Delta-like-1 в аденомах мышей с мутацией APC min. Важнее то, что экспрессия HES1, указывающая на активную сигнализацию Notch, имела место не только в криптах, но и постоянно наблюдалась в аденомах всех размеров в кишечнике мышей APCmin (фиг.1). Данное наблюдение означает, что, как и в криптах, в пролиферирующих аденомных клетках активны пути и Notch, и Wnt. Раскрытые здесь примеры неожиданно показывают, что для сохранения способности оставаться недифференцированными стволовым клеткам/клеткам-предшественникам эпителия кишечника необходима сигнализация как Wnt, так и Notch. Здесь раскрыто, что то же самое верно для трансформированных/злокачественных клеток, в которых каскад Wnt конститутивно активен: активность Notch необходима для сохранения трансформированного/малигнизированного состояния клетки.
В предпочтительном осуществлении изобретения предлагается способ, по меньшей мере, частичного уменьшения имеющейся у животного аденомы и/или аденокарциномы, включающий, по меньшей мере, частичное ингибирование активации пути Notch у указанного животного, дополнительно включающий, по меньшей мере, частичное ингибирование активации пути Wnt у указанного животного.
Путем доставки ингибитора активации пути Wnt к клетке, страдающей от аденомы и/или аденокарциномы кишечника, злокачественная/нетрансформированная клетка дифференцируется и вскоре после ее образования гибнет, что ведет к уменьшению размера/объема аденомы и/или аденокарциномы кишечника. Благодаря сочетанному действию ингибитора активации пути Notch и ингибитора активации пути Wnt клетки аденомы и/или аденокарциномы кишечника дифференцируются, что приводит к, по меньшей мере, частичному снижению злокачественности кишечника. Специалисту в данной области техники ясно, что аденому и/или аденокарциному кишечника можно также лечить изолированным действием ингибитора пути Wnt.
В другом осуществлении изобретения предлагается применение ингибитора пути Notch для получения лекарства для лечения аденомы и/или аденокарциномы кишечника. Как уже отмечалось выше для способов по изобретению, для, по меньшей мере, частичного уменьшения образования NICD и тем самым для, по меньшей мере, частичного предотвращения активации пути Notch можно использовать множество ингибиторов. Примерами предпочтительных ингибиторов Notch являются: ингибиторы γ-секретазы, такие как DAPT или дибензазепин (DBZ), или бензодиазепин (BZ), ингибитор, способный снижать опосредуемую лигандом активацию Notch (например, посредством доминантно-негативного лиганда Notch или посредством доминантно-негативного Notch, или посредством антитела, способного, по меньшей мере, частично блокировать взаимодействие между лигандом Notch и Notch), или ингибитор протеаз ADAM. Более того, такой ингибитор может быть дополнен ингибитором пути Wnt или объединен с уже существующей терапией, такой как химиотерапия, хирургическая операция или облучение.
В предпочтительном осуществлении изобретения предлагается применение ингибитора пути Notch для получения лекарства для лечения аденомы и/или аденокарциномы кишечника, где указанная аденома и/или аденокарцинома кишечника имеется у больного с наследуемым синдромом семейного аденоматозного полипоза (FAP). FAP вызывается наследуемой мутацией в гене аденоматозного полипоза кишечника (АРС). Полипоз по существу означает «много полипов». Полипы представляют собой небольшие выросты ткани на стенке кишечника. Наиболее обычным и единственным полипом, который становится аденокарциномой, является аденоматозный полип. При FAP вдоль ободочной кишки развиваются сотни-тысячи полипов. Эти полипы обычно начинают образовываться в возрасте приблизительно 16 лет. Если их не удалить, то данные полипы почти всегда развиваются в рак. Индивидуумы с диагностированной мутацией АРС имеют риск не только колоректального рака, но и могут также иметь повышенный по сравнению со всей популяцией риск других типов рака. Ослабленный FAP (AFAP) представляет собой менее тяжелый вариант FAP, при котором у человека развивается меньше полипов. AFAP обычно развивается не так рано, как FAP, но он несет столь же высокий риск рака. После установления диагноза FAP больного в конечном итоге обычно подвергают профилактической (суб)тотальной колэктомии. Такой колэктомии в настоящее время можно частично избежать, если больного, страдающего FAP, подвергнуть способу или применению по изобретению. Применяемые здесь мыши APCmin в принципе являются эквивалентами FAP человека.
В еще одном осуществлении изобретения предлагается фармацевтическая композиция, включающая, по меньшей мере, два ингибитора активации пути Notch или включающая, по меньшей мере, один ингибитор активации пути Notch и, по меньшей мере, один ингибитор пути Wnt.
Фармацевтические композиции по изобретению могут предлагаться в форме порошка, раствора или суспензии в (не)водной жидкости или в виде эмульсии. Указанный фармацевтический препарат может дополнительно включать фармацевтически приемлемые носители и/или разбавители. Фармацевтические композиции можно вводить перорально, парентерально, внутримышечно, внутривенно, парентально, внутрибрюшинно или колоректально (например, с помощью суппозитория). Пероральная и колоректальная доставка является предпочтительной, поскольку подлежащие лечению области легко доступны при данных путях доставки. Более того, доставка является предпочтительно местной во избежание нежелательных побочных эффектов.
Что касается доз, то следует отметить, что специалист способен на основании примера уже известной фармакокинетики определить эффективную дозу, например, DAPT и/или DBZ и/или BZ. Более того, эффективные дозы могут быть определены специалистом также с помощью одного или ряда хорошо известных экспериментов по определению дозы.
Помимо применения фармацевтического препарата в любом из описанных способов, фармацевтический препарат по изобретению является также очень полезным в качестве дополнения (разности) к другим видам лечения. Например, если принято решение удалить аденому или аденокарциному хирургическим путем, фармацевтический препарат по изобретению вводят до и/или во время и/или после операции для индукции образования постмитотической клетки из аденомы и/или аденокарциномы или, по меньшей мере, дополнительного уменьшения аденомы и/или аденокарциномы или для лечения оставшихся (возможно, невидимых) резидуальных клеток аденомы и/или аденокарциномы. Это, например, производят путем промывания брюшной полости жидким фармацевтическим препаратом по изобретению или путем прямой инъекции фармацевтического препарата по изобретению в подозрительные области.
Изобретение будет объяснено подробнее в следующем описании, которое не ограничивает изобретение.
Экспериментальная часть
Эксперимент 1
Материалы и методы
Антитела для иммуногистохимии
Использовали следующие антитела. Мышиные против Ki67 (1:100; Novocastra), мышиные против β-катенина (1:50, Transduction Labs).
Получение образца ткани, иммуногистохимия и гибридизация in situ.
Кишечный тракт вырезали целиком и осторожно промывали холодным ЗФР для удаления всех содержащихся фекалий с последующей промывкой формалином. Тонкий кишечник сворачивали в компактный круг и фиксировали в формалине при комнатной температуре в течение 16 час. Получали срезы тканей (2-6 мкм). После удаления парафина и гидратации срезы предварительно обрабатывали блокирующим пероксидазу буфером (120 мМ Na2HPO4, 43 мМ лимонная кислота, 30 мМ NaN3, 0,2% H2O2; рН 5,8) в течение 15 минут при комнатной температуре. Восстановление антигена производили кипячением образцов в Na-цитратном буфере (10 мМ, рН 6,0). Через 20 минут сосуду для кипячения давали медленно остыть до комнатной температуры. Инкубацию антител производили в БСА в ЗФР в течение ночи при 4°С и при комнатной температуре в течение 1 часа в случае лизозима, Ki67. Во всех случаях в качестве вторичного реагента использовали набор Envision+ (DAKO). Время инкубации составляло 30 мин. Окрашивание производили с помощью DAB. Срезы затем подкрашивали гематоксилином и монтировали. Зонды, использованные для гибридизации in situ, соответствовали описанным (Schroder et al 2002).
Сходную гибридизацию in situ проводили с хорошо охарактеризованными заключенными в парафин патологическими образцами человека, но, разумеется, с последовательностями РНК человека в качестве зондов.
Окраска альциановым синим
После депарафинизации и гидратации ткани инкубировали в течение 5 мин в альциановом синем (1% в 0,5% уксусной кислоте). Затем промывали водой, инкубировали 1 мин в нейтральном красном. Быстро дегидратировали, промывали ксилолом и фиксировали с помощью Pertex.
Фармакологическое ингибирование сигнализации Notch у мышей APCmin
8-Недельных мышей APCmin обрабатывали двумя различными, доставляемыми перорально ингибиторами γ-секретазы (DAPT: 100 мг/кг в кукурузном масле) в течение 2,5, 6,5 или 15 дней, после чего их кишечник извлекали и гистологически обследовали.
Результаты
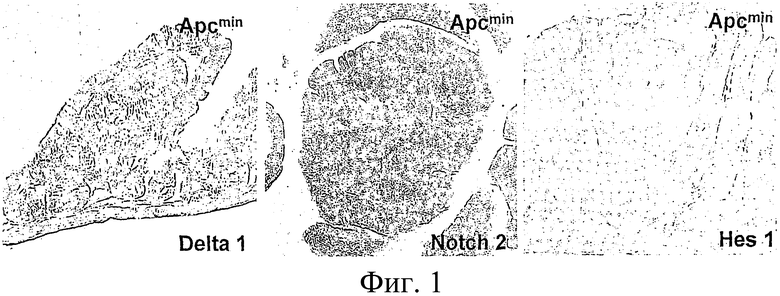
Аденомы кишечника возникают в результате мутационной активации пути Wnt, чаще всего из-за утраты гена супрессора опухоли кишечника АРС (см. обзоры Kinzler и Vogelstein, 1996; Beinz и Clevers, 2000). Заявители недавно сообщили о примечательной симметрии между колоректальными раковыми клетками и предшественниками пролиферативных крипт в плане экспрессии программы генов-мишеней Wnt (van de Wetering et al 2002). Для выяснения того, распространяется ли симметрия между криптами и неоплазией кишечника на путь Notch, заявители исследовали экспрессию различных компонентов пути Notch и генов-мишеней в аденомах, которые спонтанно возникают у мышей с мутацией min в АРС. В целом экспрессия рецепторов и лигандов в аденомах хорошо соответствовала экспрессии в криптах, как сообщалось ранее (Schroder и Gossler, 2002) (табл.1). В качестве примера на фиг.1 показана экспрессия Notch2 и Delta-like-1 в аденомах. Более важно то, что экспрессия Hes 1, указывающей на активную сигнализацию Notch, происходила не только в криптах (Schroder и Gossler, 2002), но и постоянно наблюдалась в аденомах любого размера в кишечнике мышей APCmin (фиг.1, правая часть). Данное наблюдение позволяет предполагать, что, как и в криптах, пути Notch и Wnt активны одновременно в пролиферирующих аденомных клетках.
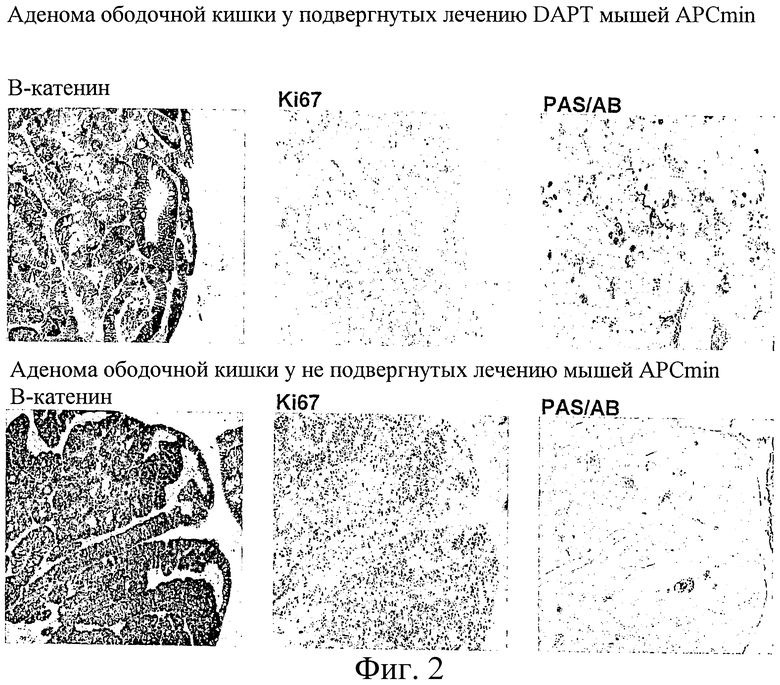
После этого заявители задались вопросом о том, необходима ли активность пути Notch для поддержания недифференцированного, пролиферативного фенотипа аденомных клеток. Заявители решили произвести ингибирование пути Notch фармакологически, используя ингибитор γ-секретазы DAPT. После этого заявители начали лечение 15-недельных мышей APCmin, которые в этом возрасте имеют 30-60 макроскопически определимых аденом или полипов в тонком кишечнике и 1-3 аденомы в ободочной кишке. Мышей лечили на протяжении периода до 15 дней, после чего их кишечник обследовали гистологически. На основании пилотного эксперимента и опубликованных режимов лечения мышам APCmin вводили перорально один раз в день дозу DAPT 100 мг/кг в маисовом масле. Стабильных эффектов через 2,5 или 6,5 дней лечения не наблюдалось. Однако большие изменения в аденомах происходили на 15 день лечения соединениями. Как показано на фиг.2 и 3, количество пролиферирующих, Ki67-позитивных клеток резко снижалось. На фиг.2 аденомы ободочной кишки визуализировали окраской бета-катенина (левые части). Примечательно, что пролиферация в соседних, нормальных криптах не менялась. В аденомах появлялись большие очаги окрашиваемых альциановым синим бокаловидных клеток. Ядерная окраска β-катенина в остановленных и дифференцированных клетках показала, что они возникли из Ape-негативной аденомы. На фиг.3 показаны примеры аденом в тонком кишечнике. Ткань аденомы вновь окрашивается темно-коричневым в левых частях. Клеточная пролиферация, обнаруживаемая окрашиванием с помощью Ki67 (правые части), прекращалась после лечения соединением DAPT.
Получена масса данных, свидетельствующих о том, что каскад Wnt является главной движущей силой для пролиферативного потенциала переходных амплифицирующихся клеток-предшественников крипт, а также аденом и аденокарцином кишечника мыши и человека. Эти данные показывают, что активная сигнализация Notch играет столь же важную роль в поддержании недифференцированного состояния предшественников крипт и мутантных по Аре неопластических клеток. В то время как каскад Wnt активируется мутациями при включении процесса трансформации, путь Notch, вероятнее всего, остается без мутаций во время прогрессии опухоли. Тем не менее, можно предполагать наличие сильного давления отбора в запущенных опухолях на наличие активирующих путь Notch мутаций. О таких активирующих мутациях при колоректальном раке не сообщалось.
Каскад Wnt, активированный при колоректальном раке, обычно рассматривают как достаточно неблагодарный объект для создания лекарств, поскольку сегмент каскада ниже супрессорного белка Аре опухолей управляется исключительно межбелковыми взаимодействиями. Как прямо показано здесь, путь Notch представляет собой альтернативную стратегию для направленного лекарственного воздействия при лечении неоплазии кишечника, такой как семейный аденоматозный полипоз или случайный колоректальный рак. Для лечения болезни Альцгеймера были созданы разнообразные ингибиторы γ-секретазы разной химической природы. Было отмечено увеличение количества бокаловидных клеток кишечника в исследованиях токсичности у животных в качестве главного нежелательного побочного действия этих соединений. Тем не менее заявители утверждают, что данное связанное с Notch действие придает данным ингибиторам γ-секретазы привлекательность с точки зрения терапии колоректального рака.
Эксперимент II
Материалы и методы
Антитела для иммуногистохимии
Использовали следующие антитела. Мышиные против Ki67 (1:100; Novocastra), мышиные против β-катенина (1:50, Transduction Labs), кроличьи против Mathi (1:50, любезно предоставленные Dr Jane Johnson).
Получение образца ткани, иммуногистохимия и гибридизация in situ
Кишечный тракт вырезали целиком и осторожно промывали холодным ЗФР для удаления всех содержащихся фекалий с последующей промывкой формалином. Тонкий кишечник сворачивали в компактный круг и фиксировали в формалине при комнатной температуре в течение 16 час. Получали срезы тканей (2-6 мкм). После удаления парафина и гидратации срезы предварительно обрабатывали блокирующим пероксидазу буфером (120 мМ Na2HPO4, 43 мМ лимонная кислота, 30 мМ NaN3, 0,2% H2O2; рН 5,8) в течение 15 минут при комнатной температуре. Восстановление антигена производили кипячением образцов в Na-цитратном буфере (10 мМ, рН 6,0). Через 20 минут сосуду для кипячения давали медленно остыть до комнатной температуры. Инкубацию антител производили в БСА в ЗФР в течение ночи при 4°С для антител против Math1 и при комнатной температуре в течение 1 часа для антител против Ki67 и β-катенина. Во всех случаях в качестве вторичного реагента использовали набор Envision+ (DAKO). Окрашивание производили с помощью DAB. Срезы подкрашивали гематоксилином и монтировали.
Ингибитор гамма-секретазы DBZ
Три грамма DBZ (Milano et al 2004) синтезировали по заказу в Syncom, Groningen, Нидерланды, с чистотой >99,9%. DBZ тщательно суспендировали в 0,5% (мас./об.) гидроксипропилметилцеллюлозе (Methocel E4M) и 0,1% (мас./об.) твин 80 в воде.
Обработка животных ингибитором гамма-секретазы DBZ
Мышам С57В16 вводили в/бр ингибитор гамма-секрет азы DBZ ежедневно в количестве 0, 3, 10 и 30 мкм/кг в течение 5 дней.
Заявители лечили 8-недельных мышей Apcmin, каждые две мыши получали инъекции DBZ 0, 3, 10 или 30 мкм/кг. DBZ вводили через каждые 48 часов внутрибрюшинно в течение 10 дней, после чего кишечник обследовали гистологически с помощью серийных срезов.
Результаты
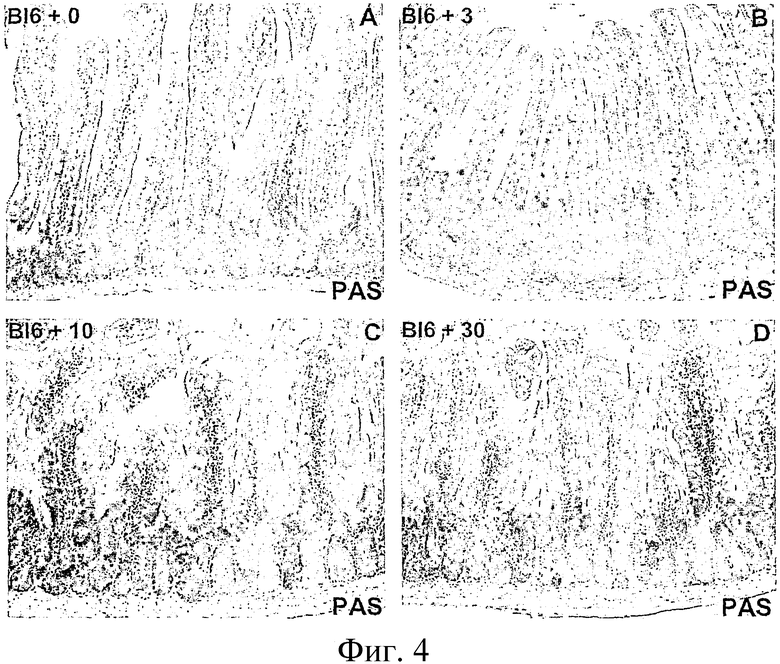
В качестве альтернативного средства блокирования сигнализации Notch in vivo заявители синтезировали ингибитор γ-секретазы DBZ 18 с чистотой до 99,9%. DBZ блокировал расщепление Notch в тесте на основе клеток с IC50<2 нМ (не показано). В эксперименте по подбору дозы соединение вводили ежедневно в/бр в количестве 0, 3, 10 и 30 мкм/кг мышам С57В16 в течение 5 дней. При более высоких дозах (10 и 30 мкм/кг) превращение бокаловидных клеток завершалось после 5 дней в/бр введения, как показано с помощью окрашивания PAS (фиг.4С и D, соотв.). Более того, клеточная пролиферация полностью останавливалась, и гистологические маркеры (Ki67 и Mathi) показали, что изменения ткани не отличались от наблюдаемых при делеции CSL (результаты не показаны). При дозе 3 мкм/кг количество бокаловидных клеток слегка увеличивалось, как показано с помощью окрашивания PAS (фиг.4В). В совокупности генетические и фармакологические данные показывают, что сигнализация Notch существенна в компартменте крипт и необходима для поддержания недифференцированного состояния предшественников крипт.
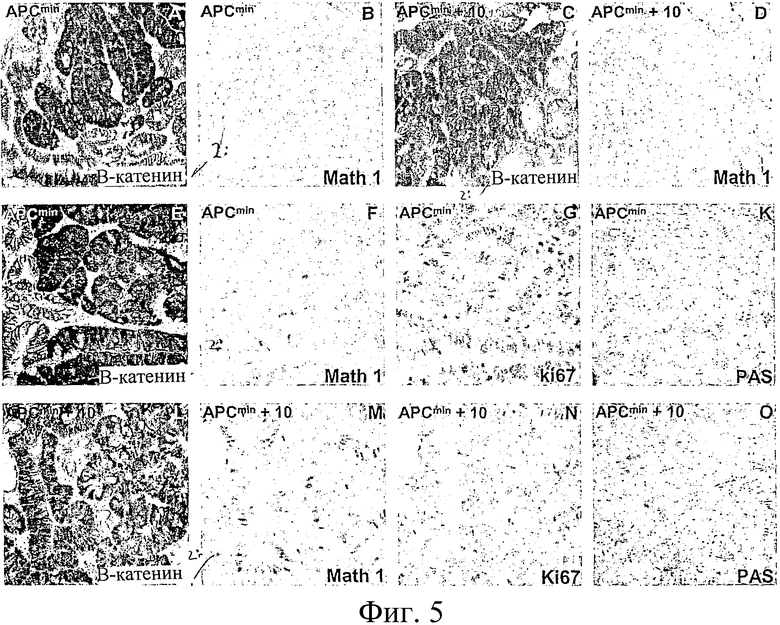
Для выяснения вопроса о том, необходима ли активность пути Notch для поддержания недифференцированного, пролиферативного фенотипа аденомных клеток, заявители выбрали фармакологическое ингибирование пути Notch. В эксперименте I это было осуществлено посредством применения ингибитора γ-секретазы DAPT. В эксперименте II заявители решили ингибировать путь Notch фармакологически с помощью ингибитора γ-секретазы DBZ (Wong et al 2004). Заявители начали лечение 8-недельных мышей Apcmin, которые в этом возрасте имеют 30-60 макроскопически определимых аденом (полипов) в тонком кишечнике и 0-3 аденомы в ободочной кишке. Каждые две мыши получали 0, 3, 10 или 30 мкм/кг DBZ в течение 10 дней, после чего кишечник обследовали гистологически с помощью серийных срезов. Окраска на β-катенин выявляла аденомы, которые часто были погружены в скопление гиперпластических, хотя и нетрансформированных нормальных крипт (фиг.5А, С). DBZ в дозе 10 или 30 мкм/кг быстро индуцировал бокаловидные клетки Math1+/PAS+/Ki67 - в аденомах (фиг.5D, М-O), тогда как действие дозы 3 мкм/кг было минимальным, как и действие на нормальные крипты (не показано). В индивидуальных аденомах наблюдались разные скорости превращения, даже у одного и того же животного. Для количественной оценки скорости превращения анализировали 100 аденом от мыши, получавшей 10 мкм/мг DBZ, для определения процента ядер Math+. В 8% аденом >50% всех эпителиальных клеток превращалось в клетки Math+. В 20% аденом происходило 10-50% превращение; в 28% выявлено превращение 1-10%, тогда как в 46% превращение в бокаловидные клетки не происходило. Превращение в бокаловидные клетки никогда не наблюдалось у мышей Apcmin без лечения: в каждой из 100 анализированных аденом наблюдалось <1% бокаловидных клеток Math1. Эти наблюдения показывают, что клетки аденомы можно заставить дифференцироваться при ингибировании пути Notch.
Эксперимент III
Материалы и методы
Антитела для иммуногистохимии
Использовали следующие антитела. Мышиные против Ki67 (1:100; Novocastra), мышиные против β-катенина (1:50, Transduction Labs).
Получение образца ткани и иммуногистохимия
Кишечный тракт вырезали целиком и осторожно промывали холодным ЗФР для удаления всех содержащихся фекалий с последующей промывкой формалином. Тонкий кишечник сворачивали в компактный круг и фиксировали в формалине при комнатной температуре в течение 16 час. Получали срезы тканей (2-6 мкм). После удаления парафина и гидратации срезы предварительно обрабатывали блокирующим пероксидазу буфером (120 мМ Na2HPO4, 43 мМ лимонная кислота, 30 мМ NaN3, 0,2% H2O2; рН 5,8) в течение 15 минут при комнатной температуре. Восстановление антигена производили кипячением образцов в Na-цитратном буфере (10 мМ, рН 6,0). Через 20 минут сосуду для кипячения давали медленно остыть до комнатной температуры. Инкубацию антител производили в БСА в ЗФР в течение ночи при комнатной температуре в течение 1 часа для антител против Ki67 и β-катенина. Во всех случаях в качестве вторичного реагента использовали набор Envision+ (DAKO). Окрашивание производили с помощью DAB. Срезы подкрашивали гематоксилином и монтировали.
Ингибитор гамма-секретазы DBZ и BZ
Три грамма DBZ и BZ (Milano et al 2004) синтезировали по заказу Syncom, Groningen, Нидерланды с чистотой >99,9%. DBZ тщательно суспендировали в 0,5% (мас./об.) гидроксипропилметилцеллюлозе (Methocel E4M) и 0,1% (мас./об.) твин 80 в воде, a BZ тщательно суспендировали в смеси 6% (об./об.)/94% (об./об.) Labrafil М 1944 CS.
Лечение животных ингибитором гамма-секретазы DBZ и BZ
Мышам С57 В16 вводили в/бр ингибитор гамма-секретазы BZ ежедневно в дозе 0, 3, 10 и 30 мкм/кг в течение 5 дней.
Для перорального исследования лекарства (DBZ и BZ) вводили 8-недельным мышам Apcmin (10, 20 или 30 мкм/кг), после чего кишечник обследовали гистологически с помощью серийных срезов.
Результаты
В качестве альтернативного способа блокирования сигнализации Notch in vivo заявители также синтезировали ингибитор γ-секретазы BZ с чистотой >99,9%. И BZ, и DBZ ингибировали расщепление Notch в основанном на клетках тесте с IC50 2,2 и 1,7 нМ, соотв. (данные не показаны). В эксперименте по подбору дозы соединение BZ вводили ежедневно в/бр в количестве 0, 3, 10 и 30 мкм/кг мышам С57 В16 в течение 5 дней. При более высоких дозах (10 и 30 мкм/кг) превращение бокаловидных клеток завершалось после 5 дней в/бр введения, как показано с помощью окрашивания PAS. Изменения ткани не отличались от наблюдаемых при делеции CSL (результаты не показаны) и после лечения DBZ (см. эксперимент II). Эти данные еще раз подтвердили, что сигнализация Notch существенна в компартменте крипт и необходима для поддержания недифференцированного состояния предшественников крипт.
Для выяснения вопроса о том, необходима ли активность пути Notch для поддержания недифференцированного, пролиферативного фенотипа аденомных клеток, заявители выбрали фармакологическое ингибирование пути Notch. В эксперименте I это было осуществлено посредством применения ингибитора γ-секретазы DAPT. В эксперименте II заявители решили ингибировать путь Notch фармакологически с помощью ингибитора γ-секретазы DBZ с помощью в/бр введения. В эксперименте III заявители решили ингибировать путь Notch фармакологически с помощью применения различных концентраций ингибитора γ-секретазы DBZ и BZ при пероральном введении. Смысл применения различных концентраций заключается в том, что высокая концентрация данных соединений может влиять не только на опухоль кишечника, но и на нормальную ткань.
Заявители начали пероральное лечение 8-недельных мышей Apcmin, которые в этом возрасте имеют 30-60 макроскопически определимых аденом (полипов) в тонком кишечнике и 0-3 аденомы в ободочной кишке. Каждые три мыши получали перорально 10, 15 или 30 мкм/кг BZ или DBZ в течение максимум 12 дней, после чего кишечник обследовали гистологически с помощью серийных срезов. Окраска на (В-катенин выявляла аденомы, которые часто были погружены в скопление гиперпластических, хотя и нетрансформированных нормальных крипт. На 12 день перорального лечения соединениями DBZ и BZ происходили изменения в аденомах. При концентрации 15 мкм/кг число пролиферирующих, Ki67-позитивных клеток в аденомах резко снижалось, тогда как основная часть нормальной ткани кишечника не имела видимых изменений.
Таким образом, после перорального лечения мышей Apcmin соединениями BZ и DBZ клеточная пролиферация в аденомах по результатам окрашивания Ki67/β-катенина прекращалась, тогда как нормальная ткань не имела видимых изменении.
крипт
Описание фигур
Фиг.1
Представление примеров компонентов пути Notch (Delta-like I (левая часть), Notch2 (средняя часть) и гена-мишени активированного пути Notch (Hes1 (правая часть)) в аденомах мышей APCmin, как показано гибридизацией in situ.
Фиг.2
Анализ аденом ободочной кишки мышей APCmin, подвергнутых (верхние части) или не подвергнутых (нижняя часть) лечению DAPT, как указано в тексте. Темная окраска в левых верхних/нижних частях выявляет области в эпителии с высоким уровнем бета-катенина, представляющие ткань аденомы. Средние верхние/нижние части показывают окрашивание на маркер клеточного цикла/пролиферации Ki67. Примечательно, что лечение DAPT ведет к сильному снижению пролиферативной активности в аденоме. На правых верхних/нижних частях показано увеличение бокаловидных клеток после лечения DAPT, о чем свидетельствуют темно-окрашенные клетки после окрашивания альциановым синим.
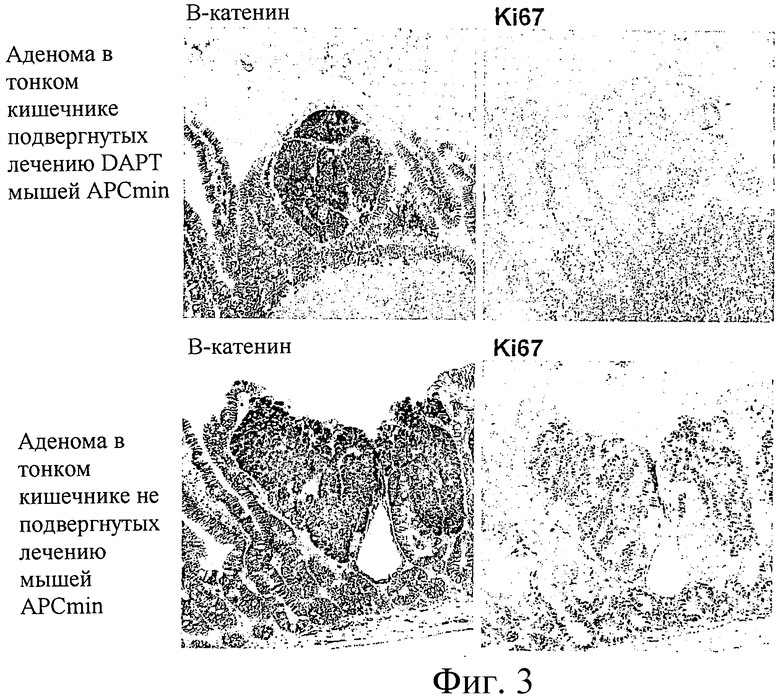
Фиг.3
Анализ аденом тонкого кишечника мышей APCmin, подвергнутых (верхние части) или не подвергнутых (нижняя часть) лечению DAPT, как указано в тексте. Темная окраска в левых верхних/нижних частях выявляет области в эпителии с высоким уровнем бета-катенина, представляющие ткань аденомы. Правые верхние/нижние части показывают окрашивание на маркер клеточного цикла/пролиферации Ki67. Примечательно, что лечение DAPT ведет к сильному снижению пролиферативной активности в аденоме.
Фиг.4
Превращение пролиферирующих клеток крипт в постмитотические бокаловидные клетки под действием ингибитора гамма-секретазы DBZ.
Мышам С57 В16 вводили в/бр ингибитор гамма-секретазы DBZ ежедневно в дозе 0, 3, 10 и 30 мкм/кг в течение 5 дней. При дозе 3 мкм/кг количество бокаловидных клеток слегка увеличивалось, как показано окрашиванием РАЗ (В), тогда как при дозах 10 и 30 мкм/кг превращение пролиферирующих клеток крипт в постмитотические бокаловидные клетки было полным (С и D соотв.).
Фиг.5
Превращение пролиферирующих клеток в опухоли APCmin в постмитотические бокаловидные клетки под действием ингибитора гамма-секретазы DBZ.
Мышей APCmin лечили 0 мкм/кг DBZ (А, В, Е, F, G, K) или 10 мкм/кг DBZ (С, D, L, M, N, О) в течение 10 дней, после чего кишечник обследовали гистологически с помощью серийных срезов. Окрашивание на β-катенин выявляло аденомы (фиг.A, C, E, L). Лечение DBZ индуцировало экспрессию Math1 (D против В, при большем увеличении М против F) и Раs (О против К) и снижало экспрессию Ki67 (N против G).
Фиг.6
Анализ кишечника и аденом кишечника мышей APCmin, подвергнутых или не подвергнутых лечению BZ, как указано в тексте.
Мышам С57 В16 вводили в/бр ингибитор гамма-секретазы BZ ежедневно в дозе 0, 3, 10 и 30 мкм/кг в течение 5 дней. При дозе 3 мкм/кг количество бокаловидных клеток слегка увеличивалось, как показано окрашиванием PAS (не показано), тогда как при дозах 10 и 30 мкм/кг превращение пролиферирующих клеток крипт в постмитотические бокаловидные клетки было полным (А).
Анализ аденом мышей APCmin, подвергнутых (верхние части) или не подвергнутых (нижняя часть) пероральному введению BZ или DBZ, как указано в тексте. Темная окраска в частях фиг. (В, С) выявляет области в эпителии с высоким уровнем бета-катенина, представляющие ткань аденомы. Части (D, E) показывают окрашивание на маркер клеточного цикла/пролиферации Ki67. Примечательно, что лечение DBZ (не показано) или BZ (часть Е против D) ведет к сильному снижению пролиферативной активности в аденоме, тогда как окружающие клетки не имеют видимых изменений.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ ПИЩЕВОДА БАРРЕТТА | 2006 |
|
RU2432163C2 |
| КУЛЬТУРАЛЬНАЯ СРЕДА СТВОЛОВЫХ КЛЕТОК | 2012 |
|
RU2714256C2 |
| УЛУЧШЕННЫЙ СПОСОБ ДИФФЕРЕНЦИРОВКИ | 2017 |
|
RU2772435C2 |
| КУЛЬТУРАЛЬНАЯ СРЕДА ДЛЯ ЭПИТЕЛИАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК И ОРГАНОИДОВ, СОДЕРЖАЩИХ УКАЗАННЫЕ СТВОЛОВЫЕ КЛЕТКИ | 2010 |
|
RU2555545C2 |
| ОРГАНОИД ПЕЧЕНИ, ВАРИАНТЫ ЕГО ПРИМЕНЕНИЯ И СПОСОБ КУЛЬТИВИРОВАНИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2579995C2 |
| ИНГИБИТОРЫ ПУТИ ПЕРЕДАЧИ СИГНАЛА NOTCH И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ РАКА | 2012 |
|
RU2631611C2 |
| ДВОЙНЫЕ ТРУБЧАТЫЕ СТРУКТУРЫ | 2017 |
|
RU2756404C1 |
| СПОСОБЫ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ С ИСПОЛЬЗОВАНИЕМ ИНГИБИТОРОВ ПУТИ ПЕРЕДАЧИ СИГНАЛА NOTCH | 2008 |
|
RU2584579C2 |
| СПОСОБ СТИМУЛЯЦИИ РЕГЕНЕРАЦИИ ТКАНЕЙ | 2007 |
|
RU2480213C2 |
| АНТИТЕЛА ПРОТИВ NOTCH2 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2580029C2 |

Изобретение относится к области медицины, а именно к онокологии, и касается лечения аденомы и/или аденокарциномы кишечника путем ингибирования пути Notch. Для этого вводят ингибитор γ-секретазы или фармацевтическую композицию на его основе в эффективном количестве. Это обеспечивает эффективное лечение за счет дифференциации аденомных и/или аденокарциномных клеток в бокаловидные. 3 н. и 17 з.п. ф-лы, 1 табл., 6 ил.
1. Способ индукции дифференциации аденомной и/или аденокарциномной клетки в бокаловидную клетку, включающий ингибирование пути Notch.
2. Способ по п.1, где указанная активация пути Notch, по меньшей мере, частично ингибируется посредством, по меньшей мере, частичного снижения опосредуемой лигандом активации Notch.
3. Способ по п.1, где указанная активация пути Notch, по меньшей мере, частично ингибируется применением ингибитора γ-секретазы.
4. Способ по п.3, где указанный ингибитор γ-секретазы представляет собой DAPT, или дибензазепин (DBZ), или бензодиазепин (DB).
5. Способ по п.2, где указанная опосредуемая лигандом активация Notch, по меньшей мере, частично снижается применением доминантно-негативного лиганда Notch.
6. Способ по п.2, где указанная опосредуемая лигандом активация Notch, по меньшей мере, частично снижается применением доминантно-негативного Notch.
7. Способ по п.2, где указанная опосредуемая лигандом активация Notch, по меньшей мере, частично снижается применением антитела, способного, по меньшей мере, частично блокировать взаимодействие между лигандом Notch и Notch.
8. Способ по п.1, где указанная активация пути Notch, по меньшей мере, частично ингибируется применением протеазного ингибитора ADAM.
9. Способ по п.1, дополнительно включающий, по меньшей мере, частичное ингибирование активации пути Wnt.
10. Применение ингибитора пути Notch для получения лекарственного средства для индукции дифференциации аденомной и/или аденокарциномной клетки в бокаловидную клетку при лечении аденомы и/или аденокарциномы кишечника.
11. Применение по п.10, где указанный ингибитор пути Notch представляет собой ингибитор γ-секретазы.
12. Применение по п.11, где указанный ингибитор γ-секретазы представляет собой DAPT, или дибензазепин (DBZ), или бензодиазепин (DB).
13. Применение по п.10, где указанный ингибитор пути Notch представляет собой ингибитор, способный снижать опосредуемую лигандом активацию Notch.
14. Применение по п.13, где указанный ингибитор представляет собой доминантно-негативный лиганд Notch.
15. Применение по п.13, где указанный ингибитор представляет собой доминантно-негативный Notch.
16. Применение по п.10, где указанный ингибитор представляет собой антитело, способное, по меньшей мере, частично блокировать взаимодействие между лигандом Notch и Notch.
17. Применение по п.10, где указанный ингибитор представляет собой протеазный ингибитор ADAM.
18. Применение по любому из пп.10-17, дополнительно включающий ингибитор пути Wnt.
19. Применение по любому из пп.10-17, где аденома и/или аденокарцинома кишечника имеется у больных с наследуемым синдромом семейного аденоматозного полипоза (FAP).
20. Фармацевтическая композиция, включающая, по меньшей мере, два ингибитора активации пути Notch или включающая, по меньшей мере, один ингибитор активации пути Notch и, по меньшей мере, один ингибитор пути Wnt.
| СПОСОБ ЛЕЧЕНИЯ РАКА ЖЕЛУДКА | 1996 |
|
RU2134549C1 |
| WO 2004073630, 02.09.2004 | |||
| AU 2002339157 A1, 26.05.2003 | |||
| US 6762185 B1, 13.07.2004 | |||
| MAASER K | |||
| et al | |||
| "Specific ligands of the peripheral benzodiazepine receptor induce apoptosis and cell cycle arrest in human colorectal cancer cells" | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| MILANO J et al | |||
| "Modulation of Notch | |||
Авторы
Даты
2010-06-27—Публикация
2005-11-10—Подача