Изобретение относится к химии природных соединений, конкретно - к синтезу экдистероидов - гормонов линьки насекомых.
Экдистероиды - относительно новый класс природных соединений, полигидроксилированных стеринов, выполняющих функцию гормонов линьки, метаморфоза и диапаузы насекомых и ракообразных. Открытые в середине 1950-х годов в организме насекомых, они спустя 10 лет были выделены из растений. Фитоэкдистероиды рассматриваются как аллелохимические токсины и антифиданты для насекомых, неадаптированных к определенным экдистероидам. Наряду с одним основным экдистероидом (2-2.5%) растения, как правило, содержат набор минорных экдистероидов модифицированной структуры, синтезируемых в ответ на приобретаемую адаптацию насекомых - фитофагов к поступающим с пищей фитоэкдистероидам.
2-Дегидро-3-эпи-20-гидроксиэкдизон (1) является минорным экдистероидом, ранее выделенным в количестве 15 мг из семян растения Froelichia floridana [Sarker S.D., Sik V., Rees H.H., Dinan L. Phytochemistry, 1998, 49, 2311-2314].
В настоящее время известен шестистадийный синтез [Charoensuk S., Yingyongnarongkul В., Suksamrarn A., Tetrahedron, 2000, 56, 9313-9317] экдистероида (1) из 20-гидроксиэкдизона (2), одного из наиболее доступных экдистероидов (схема 1).
Схема 1
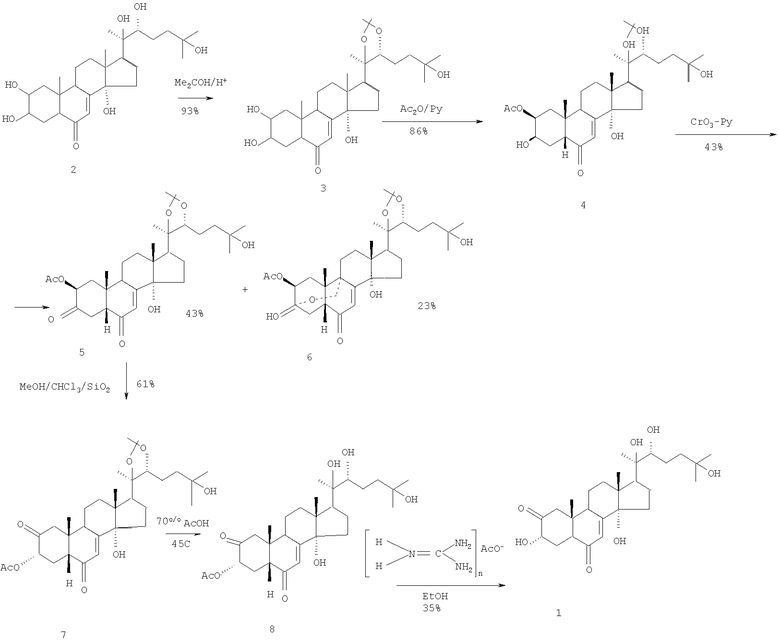
20-Гидроксиэкдизон 2 был превращен в 20,22-ацетонид 3, затем - в 2-ацетат 4. При его окислении пиридинийхлорхроматом образуется смесь 3-кетона 5 и соединения 6. Выделенный с помощью колоночной хроматографии кетон 5 изомеризуется в растворе MeOH - СНCl3 в присутствии SiO2, превращаясь в 3-эпи-ацетат-2-кетон 7. Его кислотный гидролиз (деблокирование 20,22-гидроксигрупп) дает соединение 8, а последующий гидролиз ацетата 8 в этаноле в присутствии ацетата гуанидина приводит к целевому соединению 1. Выход экдистероида 1 в данном 6-стадийном синтезе составил 7% в расчете на исходный 20-гидроксиэкдизон 2. Полученный таким образом экдистероид 1 представлял собой аморфный продукт, для него не были определены температура плавления и удельный угол оптического вращения.
Задачей предлагаемого изобретения является разработка эффективного, одностадийного метода синтеза экдистероида 1, химически более чистого.
Это достигается тем, что экдистероид 1 образуется из 20-гидроксиэкдизона 2 в одну стадию при озонировании его в растворе пиридина при температуре 0-25°C в течение 10-20 минут. За это время достигается 50% конверсия исходного соединения, а выход соединения 1 составлял 83% в расчете на прореагировавший 20- гидроксиэкдизон 2, или 42% на взятый в реакцию (Схема 2). Выделенный и хроматографически очищенный экдистероид 1 был кристаллическим (Т.пл.136-138°C), [α]D 20+13.05° (с 2.18, CHCl3). Спектры ИК, ЯМР 1Н и 13С полученного экдистероида 1 аналогичны спектрам соединения, полученного в 6 стадий и приведенным в работе [Charoensuk S., Yingyongnarongkul В., Suksamrarn A., Tetrahedron, 2000, 56, 9313-9317].
Схема 2
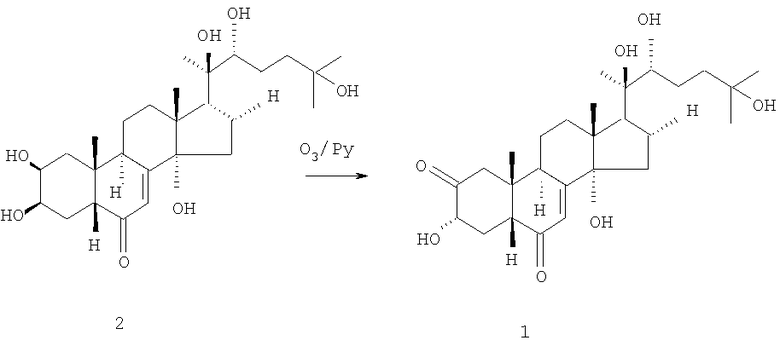
Структура, полученного нами экдистероида 2-дегидро-3-эпи-20-гидроксиэкдизона 1 была подтверждена комбинацией спектров 1D и 2D ЯМР 1Н и 13С.
Преимущества разработанного способа перед известным заключаются в следующем:
1. Способ осуществляется в одну стадию вместо шести.
2. Выход целевого соединения в 6 раз выше, причем выделенный непрореагировавший исходный 20-гидроксиэкдизон может вновь использоваться для синтеза.
3. Полученный экдистероид кристаллический, отличается высокой чистотой (данные тонкослойной хроматографии, ЯМР 1Н и 13С спектров).
Сущность метода демонстрируется следующими примерами.
Пример 1.
Через раствор 20-гидроксиэкдизона 2 (0.3 г, 0.63 мМ) в 3 мл пиридина при комнатной температуре и перемешивании пропускали озонокислородную смесь со скоростью 70 мл/мин в течение 20 мин (10 ммоль О3, производительность озонатора 30 ммоль/час). Реакционную смесь продули аргоном, упарили. Сухой остаток растворили в метаноле и хроматографировали на колонке (10 г SiO2, элюент смесь (20:1) хлороформ-метанол). Выделили 0.13 г (43%) соединения 1 (Rf 0.59) и 0.15 г (50%) исходного соединения 2 (Rf 0.48, Sorbfil, CHCl3-MeOH, 3:1).
Для 1: т.пл. 136-138°C, [α]D 20+13.05° (с 2.18, CHCl3). ИК (KBr, ν/см-1): 3410, 2960, 1710, 1650. 1Н ЯМР (400 МГц, CDCl3), δ: 0.87 (с, 3H, 18-Me), 1.07 (с, 3H, 19-Me), 1.18 (с, 3H, 21-Me), 1.18 (с, 3H, 26-Me), 1.18 (с, 3H, 27-Me), 1.29 и 1.66 (м, 2H, 23-H), 1.41 и 1.78 (м, 2H, 24-H), 1.58-1.96 (м, 4H, 15-H, 16-H), 1.73 и 1.97 (м, 2H, 11-H), 1.81 и 2.18 (м, 2H, 4-H), 1.84 и 2.09 (м, 2H, 12-H), 2.37 (м, H, 17-H), 2.38 и 2.57 (оба д, 2H, 1-H, J 13.8 Гц), 2.66 (д. д, 1H, 5-H, J 14.6, 4.5 Гц), 2.79 (м, 1H, 9-H), 3.31 (м, 1H, 22-H), 4.34 (д. д, 1H, 3-H, J 11.9, 7.3 Гц), 5.83 (с, 1H, 7-H). 13C ЯМР (75.47 МГц, CDCl3, сигналы углеродных атомов редактированы в стандартных режимах DEPT-135, HHCOSY, HSQC, НМВС), δ: 18.14 (C-18), 21.06 (C-21), 21.18 (C-11), 21.45 (C-16), 21.60 (C-19), 27.46 (C-23), 29.16 (C-27), 29.77 (C-26), 31.86 (C-15), 32.41 (C-12), 36.36 (C-4), 36.94 (C-9), 42.48 (C-24), 44.06 (C-10), 48.84 (C-1), 50.64 (C-13), 50.70 (C-17), 56.38 (C-5), 71.47 (C-25), 75.23 (C-3), 78.08 (C-22), 78.63 (C-20), 85.09 (C-14), 122.07 (C-7), 167.05 (C-8), 203.27 (C-6), 210.98 (C-2).
Пример 2.
Через раствор 0.3 г (0.63 мМ) 20-гидроксиэкдизона 2 в 3 мл сухого пиридина при 0°C и перемешивании пропускали озонокислородную смесь со скоростью 70 мл/мин в течение 20 мин и далее обрабатывали, как описано в примере 1, получив 0.03 г (10%) соединения 1, идентичного полученному в примере 1 и 0.24 г (80%) непрореагировавшего 20-гидроксиэкдизона 2.
Пример 3.
Через раствор 0.3 г (0.63 мМ) 20-гидроксиэкдизона 2 в 3 мл сухого пиридина при комнатной температуре и перемешивании пропускали озонокислородную смесь со скоростью 70 мл/мин в течение 10 минут и далее обрабатывали, как описано в примере 1, получив 0.06 (20%) соединения 1, идентичного полученному в примере 1 и 0.25 г (83%) 20-гидроксиэкдизона 2.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 7,8-ДИГИДРОАНАЛОГОВ ЭКДИСТЕРОИДОВ | 2010 |
|
RU2434877C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДЕЗОКСИ-ΔЭКДИСТЕРОИДОВ | 2020 |
|
RU2760001C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА (6-ГИДРОКСИ-2,5,7,8-ТЕТРАМЕТИЛХРОМАН-2-ИЛ)АЦЕТАЛЬДЕГИДА С 20-ГИДРОКСИЭКДИЗОНОМ И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИОКСИДАНТНОГО СРЕДСТВА, ИНГИБИРУЮЩЕГО ПРОЦЕСС ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ | 2010 |
|
RU2490267C2 |
| СПОСОБ ПОЛУЧЕНИЯ ШИДАСТЕРОНА | 2001 |
|
RU2183641C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛПЕРЕГРУППИРОВАННОГО ЭКДИСТЕРОИДА - 2,3:20,22-ДИАЦЕТОНИДА 9α,13α-ЭПОКСИ-14β-МЕТИЛ-13-ДЕМЕТИЛ-14-ДЕЗОКСИ-7,8-ДИГИДРО-20-ГИДРОКСИЭКДИЗОНА | 2010 |
|
RU2443709C1 |
| СПОСОБ ПОЛУЧЕНИЯ (8R)-8,13-ЦИКЛО-13,14-СЕКО-5β-ПРЕГН-2-ЕН-6,14,20-ТРИОНА | 2017 |
|
RU2677344C2 |
| Использование анилов фенхона в качестве УФ-абсорберов фотополимеризующихся композиций для 3D-печати | 2023 |
|
RU2813528C1 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2830163C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-МОНОАЦЕТОНИДА 20-ГИДРОКСИЭКДИЗОНА | 2007 |
|
RU2351604C1 |
| ХИРАЛЬНЫЕ МИРТАНИЛСУЛЬФОНАМИДЫ | 2019 |
|
RU2725878C1 |
Изобретение относится к химии природных соединений, конкретно - к улучшенному синтезу экдистероидов - гормонов линьки насекомых. Описан одностадийный способ получения 2-дегидро-3-эпи-20-гидроксиэкдизона 1 при озонировании 20-гидроксиэкдизона (2) в растворе пиридина при температуре 0-25°С в течение 10-20 мин. Полученный таким образом экдистероид 1 был выделен в кристаллическом виде с выходом 83% в расчете на прореагировавший 20-гидроксиэкдизон (2), для него были определены и дополнены температура плавления и удельный угол вращения, структура полученного продукта подтверждена комбинацией спектров 1D и 2D ЯМР 1Н и 13С. Способ позволяет при одностадийном процессе получать высокий выход экдистероида.
Способ получения 2-дегидро-3-эпи-20-гидроксиэкдизона формулы 1,
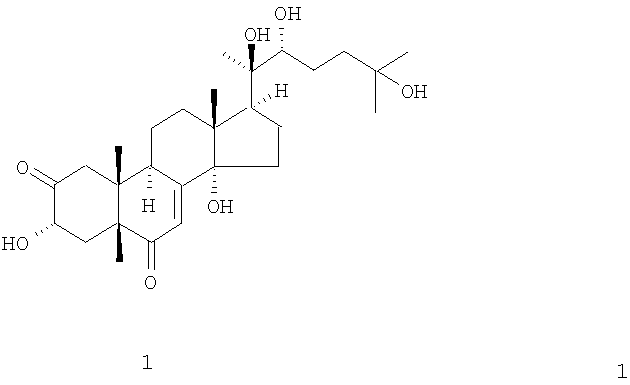
минорного экдистероида семян растения Froelichia floridana, отличающийся тем, что 20-гидроксиэкдизон озонируют в растворе пиридина при температуре 0-25°С в течение 10-20 мин с последующим упариванием растворителя и очисткой целевого продукта с помощью колоночной хроматографии на силикагеле.
| SIRITON CHAROENSUK, et al // Tetrahedron, v 56, 2000, p.9313-9317 SARKER S.D | |||
| et al // Phytochemistry, 1998, v.49, p.2311-2314. |
Авторы
Даты
2010-08-20—Публикация
2008-08-06—Подача